
МЕДЬ И СЕРЕБРО Суханова К. Г. МГП-10

Медь

Серебро

История открытия и область применения СЕРЕБРО: МЕДЬ: Медь — один из первых металлов, широко освоенных человеком из-за сравнительной доступности для получения из руды и малой температуры плавления. В древности применялась в основном в виде сплава с оловом — бронзы для изготовления оружия и т. п. Латинское название меди Cuprum произошло от названия острова Кипр, где уже в III тысячелетии до н. э. существовали медные рудники и производилась выплавка меди. За 2500 лет до н. э. в Древнем Египте носили украшения и чеканили монеты из серебра, считая, что оно дороже золота. В X в. было показано, что между серебром и медью существом аналогия, и медь рассматривалась как серебро, окрашенное в красный цвет. В XVI в. Парацельс получил хлорид серебра из элементов а Бойль определил его состав. Шееле изучал действие света на хлорид серебра, а открытие фотографии привлекло внимание и кдругим галогенидам серебра. В 1663 г. Глазер предложил нитрат серебра в качестве прижигающего средства. С конца XIX в. комплексные цианиды серебра используются в гальванопластике.

Халькофильные элементы В соответствии с классификацией норвежского геохимика В. М. Гольдшмидта, к ним относятся химические элементы сульфидных руд, то есть элементы побочных группы периодической системы химических элементов. В их число входит 19 элементов: S, Cu, Zn, Ga, Ge, As, Se, Ag, Cd, In, Sb, Te, Au, Hg, Tl, Pb, Bi, Po. Металлические халькофильные элементы обладают специфическим сродством к сере, селену и теллуру. На долю всех халькофильных элементов приходится всего 0, 046 % массы земной коры, но из-за способности накапливаться в определённых условиях они образуют рудные месторождения, среди которых доминируют гидротермальные жильные. В осадочных породах сульфиды ряда элементов (меди, свинца, цинка и частично серебра) образуют стратиформные (пластовые) рудные залежи.
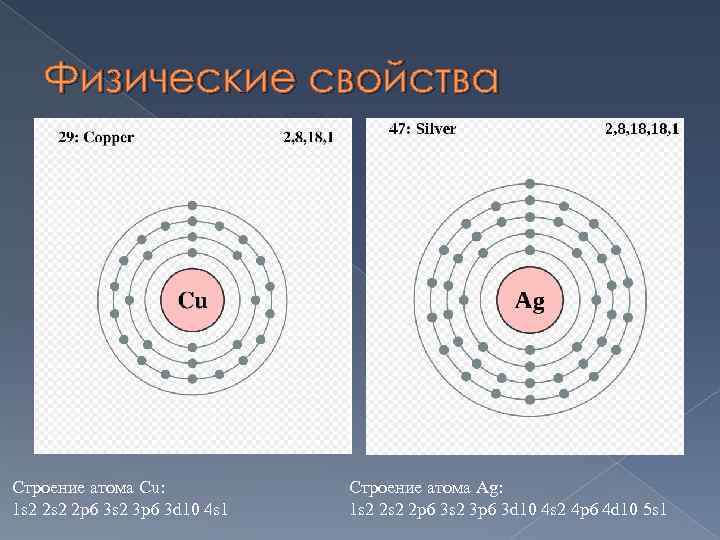
Физические свойства Строение атома Cu: 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 1 Строение атома Ag: 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 6 4 d 10 5 s 1

Физические свойства меди Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой, которая придаёт ей характерный интенсивный желтовато-красный оттенок. Тонкие плёнки меди на просвет имеют зеленовато-голубой цвет. Наряду с осмием и золотом, медь - один из трех металлов, имеющих явную цветовую окраску, отличную от серой или серебристой у прочих металлов. Этот цветовой оттенок объясняется наличием электронных переходов между заполненной третьей и полупустой четвертой атомными орбиталями: разница между ними соответствует длине волны оранжевого света. Тот же механизм отвечает за характерный цвет золота.

Медь обладает высокой тепло- и электропроводностью (занимает второе место по электропроводности после серебра). Удельная электропроводность при 20 °C 55, 5 -58 МСм/м. Медь имеет относительно большой температурный коэффициент сопротивления: 0, 4 %/°С. Имеет два стабильных изотопа — 63 Cu и 65 Cu, и несколько радиоактивных изотопов. Самый долгоживущий из них, 64 Cu, имеет период полураспада 12, 7 ч и два варианта распада с различными продуктами. Существует ряд сплавов меди: латуни — с цинком, бронзы — с оловом и другими элементами, мельхиор — с никелем, баббиты — со свинцом и другие.

Физические свойства серебра Металлическое серебро в компактном полированном виде представляет собой белый блестящий металл, обладающий большой отражательной способностью по отношению к инфракрасным и видимым лучами и более слабой — к ультрафиолетовым лучам. Серебро в виде тонких листочков (они кажутся синими или фиолетовыми в проходящем свете) обладает электрическими и оптическими свойствами, отличными от свойств металлического серебра в слитках. Физико-химические свойства серебра значительной степени зависят от его чистоты. В числе физико-механических свойств следует отметить пластичность, относительную мягкость (твердость 2, 5— 3), ковкость и тягучесть, малую прочность. Серебро образует сплавы типа твердых растворов с золотом с палладием. в

По большинству физических свойств серебро приближается к меди и золоту. В подгруппе меди серебро обладает наиболее низкими температурами плавления и кипения и максимальным значением коэффициента расширения, максимальной тепло- и электропроводностью. Серебро проявляет большее сходство с палладием (за которым он следует в периодической системе), чем с рубидием (с которым он находится рядом в I группе периодической системы и в том же пятом периоде). Расположение серебра в побочной подгруппе I группы периодической системы определяется электронной структурой атома которая аналогична электронной структуре атома рубидия. Большое различие в химических свойствах серебра и рубидия определяется разной степенью заполненности электронами 4 й-орбитали. Атом серебра отличается от атома палладия наличием одного электрона на 5 й-орбитали. При легировании устраняются основные недостатки серебра, такие, как мягкость, низкая механическая прочность и высокая реакционная способность по отношению к сере и сульфидам. Некоторые газы, например водород, кислород, окись и двуокись углерода, растворяются в серебре, причем растворимость их пропорциональна квадратному корню от давления.
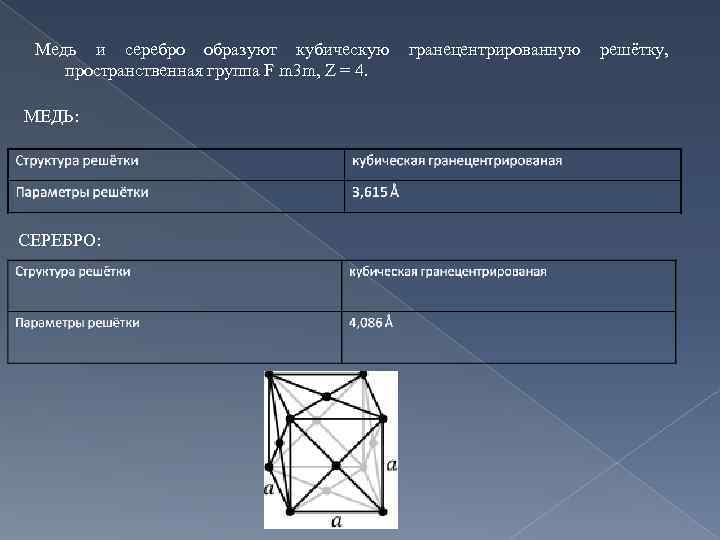
Медь и серебро образуют кубическую гранецентрированную решётку, пространственная группа F m 3 m, Z = 4. МЕДЬ: СЕРЕБРО:

Химические свойства меди Возможные степени окисления: В соединениях медь проявляет две степени окисления: +1 и +2. Первая из них устойчива только в нерастворимых соединениях (Cu 2 O, Cu. Cl, Cu. I и т. п. ) или комплексах (например [Cu(NH 3)2]-. Её соединения бесцветны. Более устойчива степень окисления +2, которая даёт соли синего и сине-зелёного цвета. В необычных условиях можно получить соединения со степенью окисления +3 и даже +5. Последняя встречается в солях купраборанового аниона Cu(B 11 H 11)23 , полученных в 1994 году.

Простое вещество Не изменяется на воздухе в отсутствие влаги и диоксида углерода. Является слабым восстановителем, не реагирует с водой, разбавленной соляной кислотой. На влажном воздухе медь окисляется, образуя основный карбонат меди(II) Соединения меди(I) Степени окисления +1 соответствует оксид Cu 2 O красно-оранжевого цвета. Многие соединения меди +1 имеют белую окраску либо бесцветны. Это объясняется тем, что в ионе Сu+ все пять Зd-орбиталей заполнены парами электронов. Соединения меди(II) Степень окисления II — наиболее стабильная степень окисления меди. Ей соответсвует чёрный оксид Cu. O и голубой гидроксид Cu(OH)2, который при стоянии легко отщепляет воду и при этом чернеет: Гидроксид меди (II) носит преимущественно основный характер и только в концентрированной щелочи частично растворяется с образованием синего гидроксокомплекса. Соединения меди(III) и меди(IV) Степени окисления III и IV являются малоустойчивыми степенями окисления и представлены только соединениями с кислородом, фтором или в виде комплексов.

Геохимические барьеры меди: сорбционный нейтральный восстановительный, термодинамический Хорошо мигрирует в кислых водах окислительной и восстановительно-глеевой обстановок в форме комплексных соединений.

Химические свойства серебра Серебро, будучи благородным металлом, отличается относительно низкой реакционной способностью, оно не растворяется в соляной и разбавленной серной кислотах. Однако в окислительной среде (в азотной, горячей концентрированной серной кислоте, а также в соляной кислоте в присутствии свободного кислорода) серебро растворяется. Серебро также легко растворяется в ртути, образуя амальгаму (жидкий сплав ртути и серебра). Серебро не окисляется кислородом даже при высоких температурах, однако в виде тонких плёнок может быть окислено кислородной плазмой или озоном при облучении ультрафиолетом. Во влажном воздухе в присутствии даже малейших следов двухвалентной серы (сероводород, тиосульфаты, резина) образуется налёт малорастворимого сульфида серебра, обуславливающего потемнение серебряных изделий

При нагревании с серой серебро даёт сульфид. Наиболее устойчивой степенью окисления серебра в соединениях является +1. В присутствии аммиака соединения серебра (I) дают легко растворимый в воде комплекс [Ag(NH 3)2]+. Серебро образует комплексы так же с цианидами, тиосульфатами. Комплексообразование используют для растворения малорастворимых соединений серебра, для извлечения серебра из руд. Более высокие степени окисления (+2, +3) серебро проявляет только в соединении с кислородом (Ag. O, Ag 2 O 3) и фтором (Ag. F 2, Ag. F 3), такие соединения гораздо менее устойчивы, чем соединения серебра (I). Соли серебра (I), за редким исключением (нитрат, перхлорат, фторид), нерастворимы в воде, что часто используется для определения ионов галогенов (хлора, брома, йода) в водном растворе. Коллоидное серебро является энергичным восстановителем по отношению к Fe 2 Cl 6, Hg. Cl 2, KMn 04, разбавленной HN 03, обладает хорошей адсорбционной способностью (по отношению к кислороду, водороду, метану, этану и др. ), является катализатором и сильным бактерицидом и служит для лечения некоторых трудно излечиваемых кожных болезней.
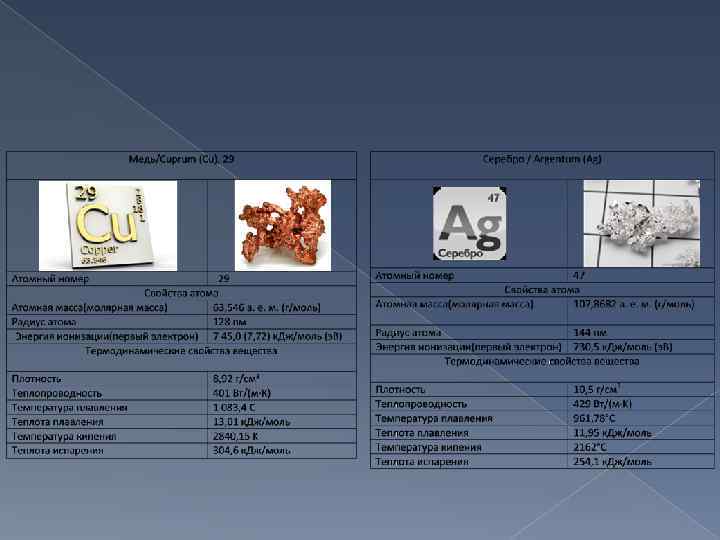

Распространенность Меди Среднее содержание Меди в земной коре 53 г/т, в нижней части земной коры, сложенной основными породами, ее больше, чем в верхней, где преобладают граниты и другие кислые изверженные породы. Медь энергично мигрирует как в горячих водах глубин, так и в холодных растворах биосферы; сероводород осаждает из природных вод различные сульфиды Меди, имеющие большое промышленное значение. Среди многочисленных минералов Меди преобладают сульфиды, фосфаты, сульфаты, хлориды, известны также самородная Медь, карбонаты и оксиды.

Распространенность Серебра Среднее содержание серебра в земной коре — 0, 073 г/т. Максимальные его концентрации устанавливаются в глинистых сланцах, где достигают 900 мг/т. Серебро характеризуется относительно низким энергетическим показателем ионов, что обуславливает незначительное проявление изоморфизма этого элемента и сравнительно трудное его вхождение в решётку других минералов. Наблюдается лишь постоянный изоморфизм ионов серебра и свинца. Ионы серебра входят в решётку самородного золота, количество которого иногда достигает в электруме почти 50 % по весу. В небольшом количестве ион серебра входит в решётку сульфидов и сульфосолей меди, а также в состав теллуридов, развитых в некоторых полиметаллических и особенно, в золото-сульфидных и золотокварцевых месторождениях. Серебро встречается также в метеоритах и содержится в морской воде.
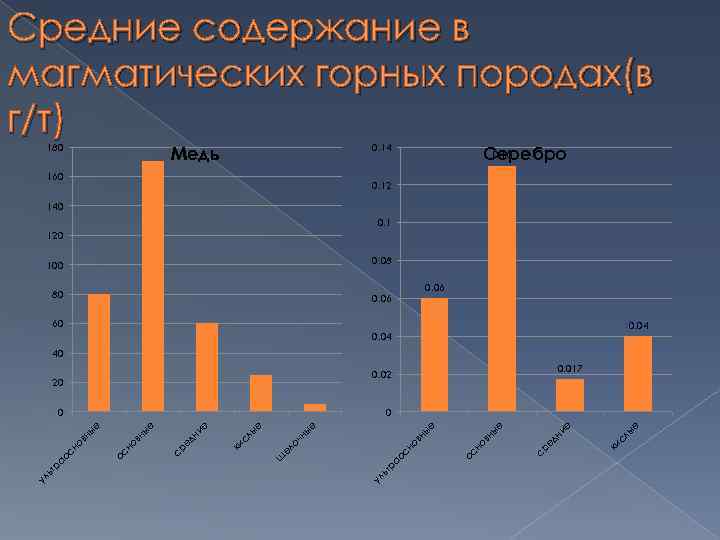
Средние содержание в магматических горных породах(в г/т) 180 0. 14 Медь 160 0. 13 Серебро 0. 12 140 0. 1 120 100 0. 08 80 0. 06 60 0. 04 40 сл ые ки ср ед ни е е ов ос н ны ов сн ао ьт р ул ны е е ны щ ел оч ки е ед ни ср ос н ов ны е ны ов сн ао ьт р сл ые 0 ул 0. 017 0. 02 20
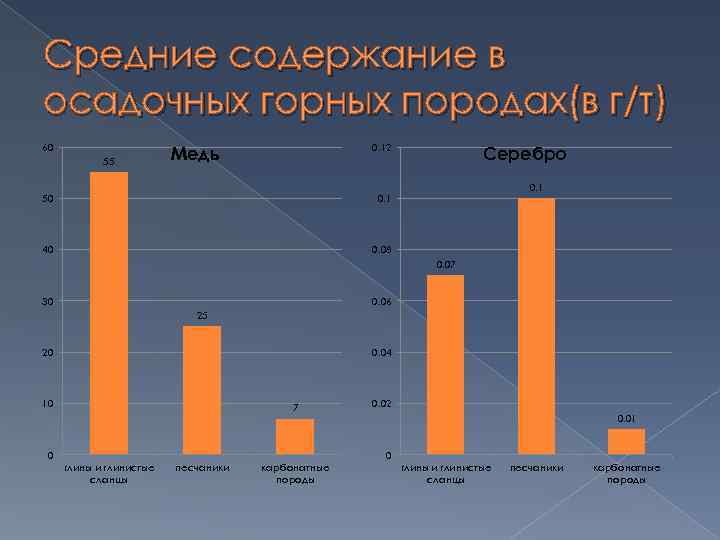
Средние содержание в осадочных горных породах(в г/т) 60 55 0. 12 Медь 50 0. 1 40 Серебро 0. 08 0. 07 30 0. 06 25 20 0. 04 10 7 0 0. 02 0. 01 0 глины и глинистые сланцы песчаники карбонатные породы

Основные минералы меди Известно 198 минералов меди, из них преобладают сульфиды (47 %), фосфаты (35 ), сульфаты (18 ) и галоиды (18 %). Промышленное значение имеют: самородная медь Cu (92 %), халькопирит (4, 5% ), борнит (63, 3%); халькозин (79, 8%), кубанит (22– 24%), ковеллин (66, 5%), куприт (88, 8%), малахит (57, 4%), азурит ( 55, 3 %). Для промышленности важны только 17 из них. Сульфиды: ковеллин Cu. S, халькозин Cu 2 -x. S, халькопирит Cu. Fe. S 2, , борнит Cu 5 Fe. S 4 Окислы: тенорит CUO , куприт Cu 2 O Карбонаты: малахит Cu 2[CO 3](OH)2 , азурит Cu 3[CO 3]2(OH)2 Сульфаты: халькантит Cu. SO 4∙ 5 H 2 O , брошантит

Чистая медь - тягучий, вязкий металл красного, в изломе розового цвета, в очень тонких слоях на просвет медь выглядит зеленовато-голубой. Эти же цвета, характерны и для многих соединений меди, как в твердом состоянии, так и в растворах. Понижение окраски при повышении валентности видно из следующих двухпримеров: Cu. Cl - белый Cu 2 O – красный Cu. Cl 2+H 2 O - голубой Cu. O - черный Карбонаты характеризуются синим и зеленым цветом при условии содержания воды, чем намечается интересный практический признак для поисков.

Основные минералы серебра Серебро в виде самородков встречается в природе реже, чем самородная медь, и часто это бывают сплавы с золотом, медью, сурьмой, ртутью и платиной. Образование самородного серебра связано с действием воды или водорода на сульфид серебра (на аргентит). Металлическое серебро представляет собой кубические кристаллы серебристо-белого цвета, часто покрыты черным налетом. В качестве пpимеси сеpебpо встpечается почти во всех медных и сеpебpяных pудах. Из этих pуд и получают около 80% всего добываемого сеpебpа.

Наиболее важными минералами серебра являются следующие: Аргентит, (Ag 2 S), серые кубические кристаллы, устойчивые при температуре ниже +179°С. Аргентит — основной источник серебра. В природе он сопутствует самородному серебру, кераргиту (Ag. Cl), церусситу (Рb. С 03), арсенидам и антимонидам серебра; его залежи часто находятся рядом с сульфидами свинца, цинка и меди. Кантпит, (Ag 2 S), серые ромбические кристаллы, неустойчивые при температуре выше +179°С. Обе модификации природного сульфида серебра содержат 87, 1% Ag, Галенит (Pb. S), добываемый в Румынии, Франции, содержит серебро. Прустит (Ag 3 [As. S 3]), содержит 65, 4% серебра. Пираргерит (Ag 3 [Sb. S 3]), содержит 68, 4% серебра. Стефанит (8(Ag, Cu)2 S-Sb 2 S 3), содержит 62, 1— 74, 9% Ag Кераргирит (Ag. Cl), содержит 75, 3% серебра.

При окислении аргентита (акантита) Ag 2 S образуется сульфат серебра Ag 2 SO 4, который будучи частично растворим, вымывается водой. Когда на пути вод, содержащих сульфат серебра, встречается сульфат железа(II), выделяется свободное серебро, а если встречаются хлориды (т. е. ионы Сl-), то образуется кераргирит: Ag 2 SO 4 + 2 Fe. SO 4 - 2 Ag + Fe 2(SO 4 )3 Ag 2 SO 4 + 2 Na. Cl = 2 Ag. Cl + Na 2 SO 4 Если воды, содержащие сульфид серебра, встречают сульфиды других элементов, то образуются скопления двойных сульфидов подобно встречающимся смесям серебро - мышьяк, серебро - сурьма, серебро - медь, серебро - свинец, серебро - германий.

Поведение меди в геологических процессах Из приведенной характеристики ионов вытекают общие тип миграции меди: слабая миграция ионов w=1 и очень сильная - ионов w=2 с рядом довольно легко растворимых солей галоидов и аниона(SО 4); равным образом осаждаемость благодаря активной поляризации ионами: (CО 3), (Si. O 4), (PO 4), (As. O 4). 1) легкое отщепление меди из магм с переходом в пневматолиты еще при дифференцации основных пород и даже может быть при ликвации ультраосновных; 2) при гидротермальном процессе главное осаждение меди в геофазы процессов G-H, т. е. около 400 -300˚; 3) в гипергенной обстановке фиксация меди преимущественно анионами (SО 4), ( Si. O 4), при общей большой миграционной способности меди (особенно в виде легкорастворимого сульфата). С. С. Смирнов характеризует миграцию так: "миграция меди тем более облегчается, чем выше в рудах отношение серы к меди, чем менее активна обстановка, чем менее влажен климат и чем более проницаема рудная масса".

Поведение серебра в геологических процессах В эндогенных условиях серебро имеет ювенильный и мантийный источник и связан щелочно-базальтоидным магматизмом. В этом случае повышенные концентрации серебра встречаются в суьфидных медноникелевых месторождения. Собственно серебряные и серебрянополиметаллические месторождения гидротермального генезиса связаны с магмами среднего и кислого состава, в том числе с вулканическими комплексами. В вулканических областях рудоносные растворы, отлагающие серебро, могли иметь различное происхождение: магматическое, метеорное и океаническое. В гидротермальных растворах серебро находится в виде подвижных тиосульфатных и хлоридных комплексов. В экзогенных условиях, в зоне окисления сульфидных месторождений, серебро переходит в раствор в виде сульфата или тиосульфата и переотлагается в самородной форме или в форме галоидов. Вэлювиальных, делювиальных и аллювиальных россыпях серебро накапливается в незначительных количествах.

Геохимическая миграция меди В гидротермах Cu мигрирует в форме различных комплексов Cu+ 0 и Cu 2+ и концентрируется на геохимических барьерах в виде халькопирита и других сульфидов (меднопорфировые, медноколчеданные и др. месторождения). В поверхностных водах обычно содержится n*10 -6 г/л Cu, что соответствует коэффициенту водной миграции 0, n. Большая часть Cu мигрирует с глинистыми частицами, которые энергично ее адсорбируют. Наиболее энергично мигрирует в сернокислых водах зоны окисления сульфидных руд, где образуется легко растворимый Cu. SO 4. Содержание Cu в таких водах достигает n г/л, на участках месторождений возникают купоросные ручьи и озера. Однако такая миграция непродолжительна: при нейтрализации кислых вод на барьере Д 1 осаждаются вторичные минералы Cu, она адсорбируется глинами, гидрооксидами марганца, гумусом, кремнеземом. Так образуется повышенное содержание меди в почвах и континентальных отложениях ландшафтов на участках месторождений. Медь здесь активно вовлекается в биологический круговорот, появляются растения, обогащенные медью, крупные размеры приобретают моллюски и другие животные с голубой кровью. Многие растения и животные плохо переносят высокие концентрации меди и болеют. Значительно слабее миграция Cu в ландшафтах влажного климата со слабокислыми водами. Медь здесь частично выщелачивается из почв. Известны болезни животных а растений, вызванные недостатком меди. Особенно бедны Cu пески и торфяники, где эффективны медные удобрения и подкормка животных. Медь энергично мигрирует и в пластовых водах, откуда она осаждается на восстановительном сероводородном барьере. Эти процессы особенно характерны для красноцветной формации, к которым приурочены месторождения и рудопроявления типа "медистых песчаников".

Формы нахождения и поведение в водной и воздушной средах, участие в биологическом круговороте Медь - важный элемент жизни, она участвует во многих физиологических процессах. Среднее содержание Меди в живом веществе 2· 10 -4%, известны организмы - концентраторы Меди. В таежных и других ландшафтах влажного климата Медь сравнительно легко выщелачивается из кислых почв, здесь местами наблюдается дефицит Меди и связанные с ним болезни растений и животных (особенно на песках и торфяниках). В степях и пустынях (с характерными для них слабощелочными растворами) Медь малоподвижна; на участках месторождений Медь наблюдается ее избыток в почвах и растениях, отчего болеют домашние животные. В речной воде очень мало Меди, 1· 10 -7%. Приносимая в океан со стоком Медь сравнительно быстро переходит в морские илы. Поэтому глины и сланцы несколько обогащены Медью (5, 7· 103%), а морская вода резко недосыщена Медью (3· 10 -7%). В морях прошлых геологических эпох местами происходило значительное накопление Меди в илах, приведшее к образованию месторождений (например, Мансфельд в Германии). Медь энергично мигрирует и в подземных водах биосферы, с этими процессами связано накопление руд Меди в песчаниках.

Формы нахождения и поведение в водной и воздушной средах, участие в биологическом круговороте Геохимия серебра в биосфере изучена плохо, его кларк в живом веществе 1, 2*10 -6 %. Серебро - энергичный водный мигрант, в подземных водах гипергенеза 2, 9 *10 -7 г/л, в морской воде - 3*10 -8% (талассофильность значительная -4, 3*10 -3, больше, чем у меди и цинка). Ионы сеpебpа подавляют развитие бактерий и уже в очень низкой концентрации (около 10 г-ион/л) сеpилизуют питьевую воду. В медицине для дезинфекции слизистых оболочек применяются стабилизированные специальными добавками коллоидные pаствоpы сеpебpа (пpотаpгол, коллаpгол и дp. ). Известны концентрации серебра в углях, глинах и других осадочных породах

Основные типы месторождений меди 1) В ультраосновных породах и наритах вместе с пирротином и, следовательно, в ассоциации с никелем, кобальтом, частично с палладием. Обычно халькопирит является последним сульфидом в этом ряду кристаллизации и, следовательно, приурочен преимущественно или к эндоконтактовым или даже к экзаконтактовым зонам. 2) Выделение меди в пустотах мелафиров и вообще в основных эффузивах вместе с циолитами в начале геофазы H. 3) Выделение пирита вместе с халькопиритом из дериватов гранодиоритовой магмы и связанных с ними альбитофиров. Колчиданные линзы с цинком и золотом (например Урал). 4) Медно-жильный комплекс в связи с кислыми гранитами, с выделением меди в геофазах G-H, между комплексами Au-W-B и B-Zn-F. К этому типу относятся и взрывные месторождения меди в порфировых рудах и во вторичных кварцитах. В этом случае интересна связь с молебденом и бором. Окварцевание с выносом всех катионов, очевидно, перегретыми гидролизирующими водами и эманациями. Генетический тип представляет огромный интерес, но самый ход процесса остается не ясным. Большое промышленное значение, несмотря на низкое содержание (1 -2%)Cu. 5) Контактный тип кислых и гранодиоритовых магм обычно во вторую фазу коктактового процесса накопления гранато-пироксенного скарна; медь обычно накапливется в геофазы G-H с молебденитом, пиритом, шеелитом, иногда гематитом среди магнетита более ранней кристаллизации. Этот тип в небольших количествах всегда присутствует в контактных магнетитах. Очень типичен для Срдней Азии (Тянь-Шань). 6) Очень многочисленна и своеобразна осадочные скопления меди в песчаниках, сланцах, песках, битуминозных осадках. Весьма возможен билогический процесс образования (Мансфильд в Тюрингии, пермские песчаники в Приуралье). Геохимически изучен плохо.

Основные типы месторождений серебра Как и другим благородным металлам, серебру свойственны два типа проявлений: • собственно серебряные месторождения, где оно составляет более 50 % стоимости всех полезных компонентов; • комплексные серебросодержащие месторождения (в которых серебро входит в состав руд цветных, легирующих и благородных металлов в качестве попутного компонента). Собственно серебряные месторождения играют достаточно существенную роль в мировой добыче серебра, однако следует отметить, что основные разведанные запасы серебра (75 %) приходятся на долю комплексных месторождений.