0ea9c386350bf4dacd71db9fa8d19f6e.ppt
- Количество слайдов: 53

MBM 223 KRİSTALOGRAFİ 1. Hafta KRİSTAL YAPILARI VE KRİSTAL SİSTEMLER
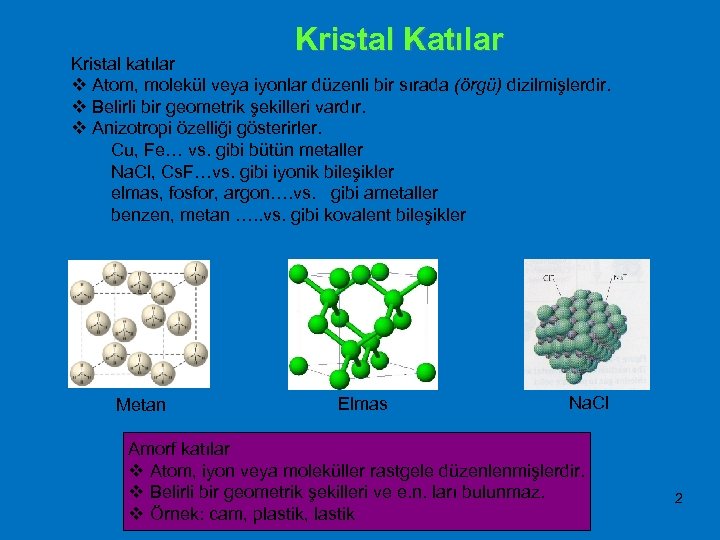
Kristal Katılar Kristal katılar v Atom, molekül veya iyonlar düzenli bir sırada (örgü) dizilmişlerdir. v Belirli bir geometrik şekilleri vardır. v Anizotropi özelliği gösterirler. Cu, Fe… vs. gibi bütün metaller Na. Cl, Cs. F…vs. gibi iyonik bileşikler elmas, fosfor, argon…. vs. gibi ametaller benzen, metan …. . vs. gibi kovalent bileşikler Metan Elmas Na. Cl Amorf katılar v Atom, iyon veya moleküller rastgele düzenlenmişlerdir. v Belirli bir geometrik şekilleri ve e. n. ları bulunmaz. v Örnek: cam, plastik, lastik 2

Başlangıçtaki düşünceler • Kristaller katıdır, ancak katıların kristalin olması gerekmez. • Kristaller simetriye ve uzun mesafeli düzene sahiptirler. (Kepler) • Küreler ve küçük şekiller düzgün şekiller oluşturacak şekilde biraraya gelebilirler. (Hooke, Hauy) ?
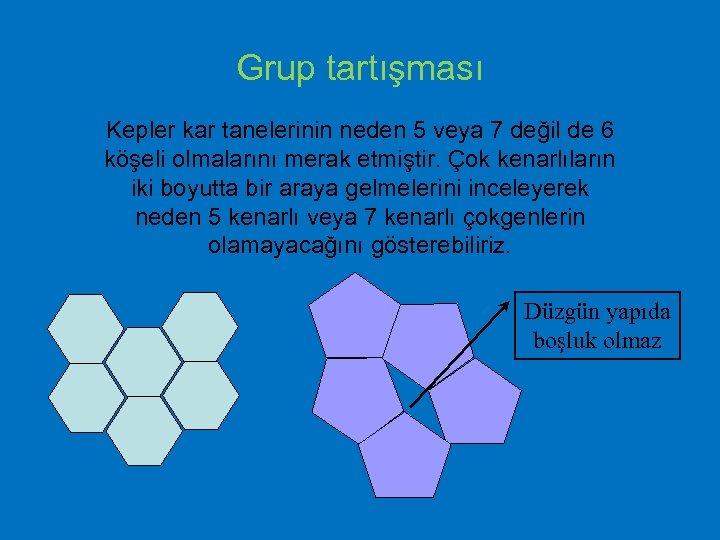
Grup tartışması Kepler kar tanelerinin neden 5 veya 7 değil de 6 köşeli olmalarını merak etmiştir. Çok kenarlıların iki boyutta bir araya gelmelerini inceleyerek neden 5 kenarlı veya 7 kenarlı çokgenlerin olamayacağını gösterebiliriz. Düzgün yapıda boşluk olmaz
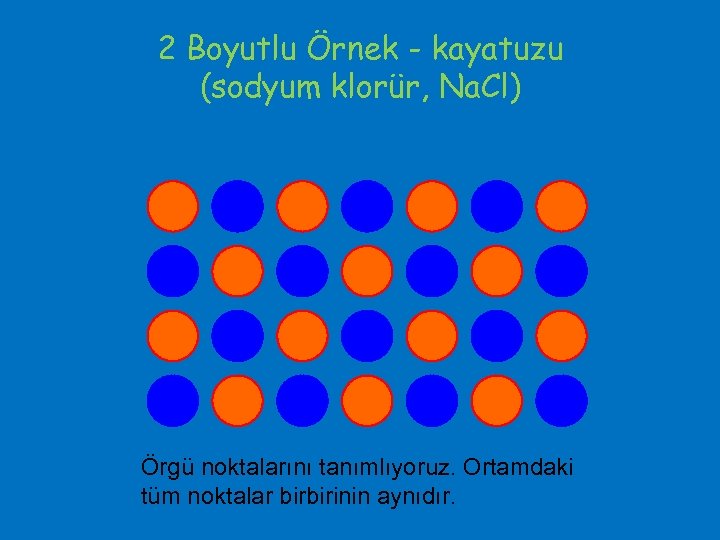
2 Boyutlu Örnek - kayatuzu (sodyum klorür, Na. Cl) Örgü noktalarını tanımlıyoruz. Ortamdaki tüm noktalar birbirinin aynıdır.
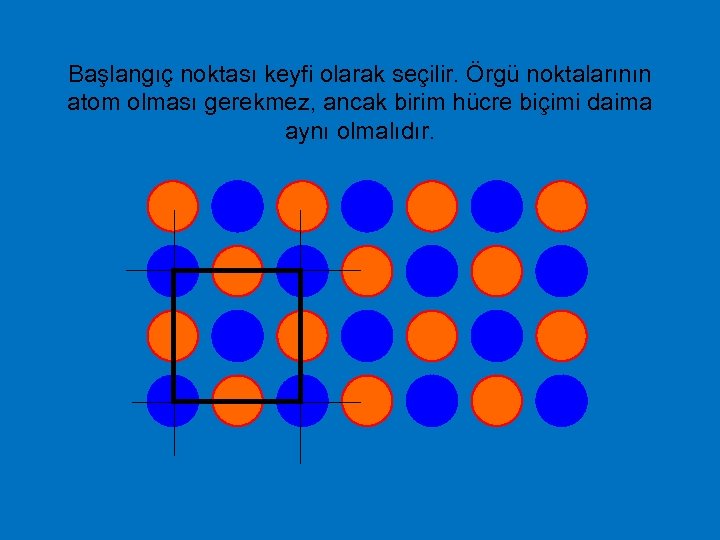
Başlangıç noktası keyfi olarak seçilir. Örgü noktalarının atom olması gerekmez, ancak birim hücre biçimi daima aynı olmalıdır.

Bu da bir Birim Hücredir Na veya Cl’dan başlamak bir şeyi değiştirmez
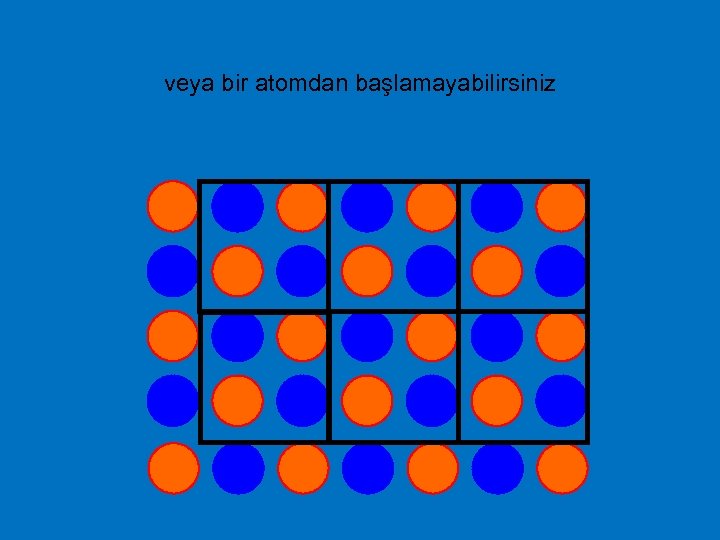
veya bir atomdan başlamayabilirsiniz
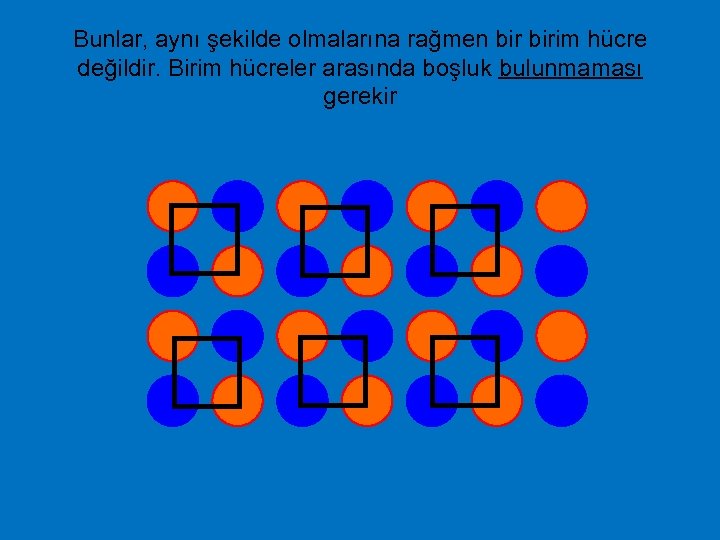
Bunlar, aynı şekilde olmalarına rağmen birim hücre değildir. Birim hücreler arasında boşluk bulunmaması gerekir

2 boyutta bu birim hücredir, fakat 3 boyutta değildir.

Özet Ø Birim hücreler birbirleri ile temas halinde olmalıdırlar, aralarında boşluk bulunamaz Ø Bütün birim hücreler aynı olmalıdır Ø Birim hücreler yapının tüm simetrisine sahip olmalıdır

Tanımlar 1. Birim Hücre “Bir kristal yapısında, 3 boyutta tekrarlanan ve yapının tüm simetrisini gösteren en küçük birime Birim Hücre denir” Birim Hücre • 3 kenarlı - a, b, c • 3 açılı - , , bir kutudur

7 Birim Hücre Şekli • • Kübik Tetragonal Orthorhombik Monoklinik Triklinik Hegzagonal Rhombohedral a=b=c a=b c a b c a=b c a=b=c = = =90°, 90° = =90°, =120° = = 90°
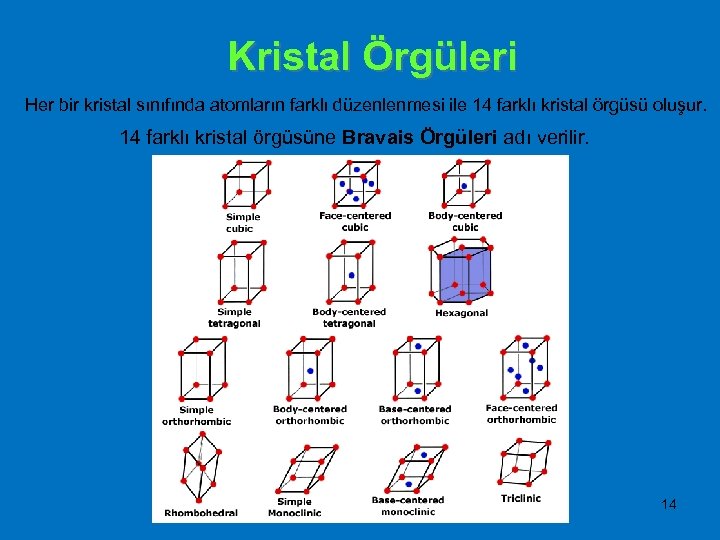
Kristal Örgüleri Her bir kristal sınıfında atomların farklı düzenlenmesi ile 14 farklı kristal örgüsü oluşur. 14 farklı kristal örgüsüne Bravais Örgüleri adı verilir. 14
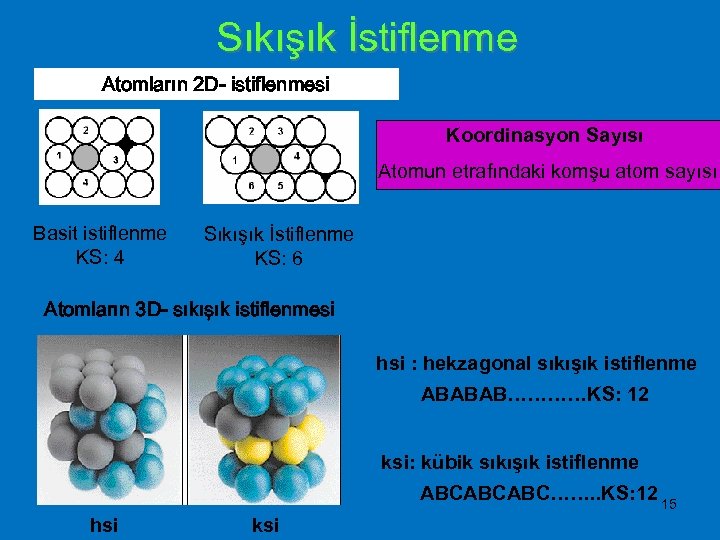
Sıkışık İstiflenme Atomların 2 D- istiflenmesi Koordinasyon Sayısı Atomun etrafındaki komşu atom sayısı Basit istiflenme KS: 4 Sıkışık İstiflenme KS: 6 Atomların 3 D- sıkışık istiflenmesi hsi : hekzagonal sıkışık istiflenme ABABAB…………KS: 12 ksi: kübik sıkışık istiflenme ABCABCABC……. . KS: 12 15 hsi ksi
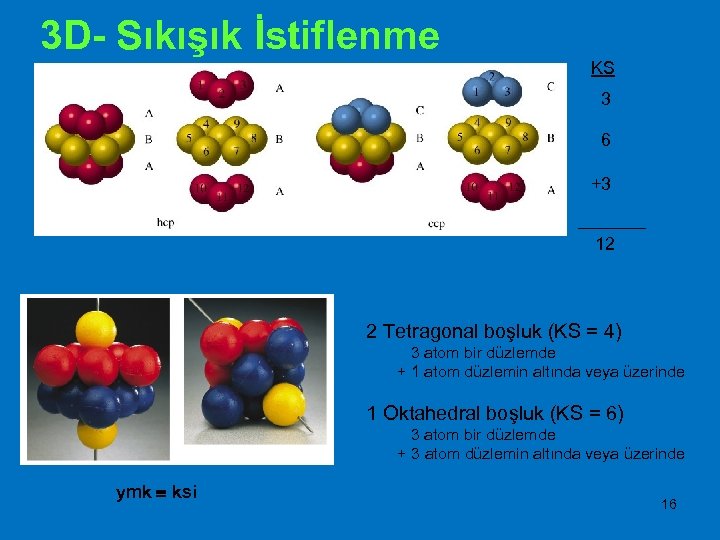
3 D- Sıkışık İstiflenme KS 3 6 +3 12 2 Tetragonal boşluk (KS = 4) 3 atom bir düzlemde + 1 atom düzlemin altında veya üzerinde 1 Oktahedral boşluk (KS = 6) 3 atom bir düzlemde + 3 atom düzlemin altında veya üzerinde ymk ksi 16
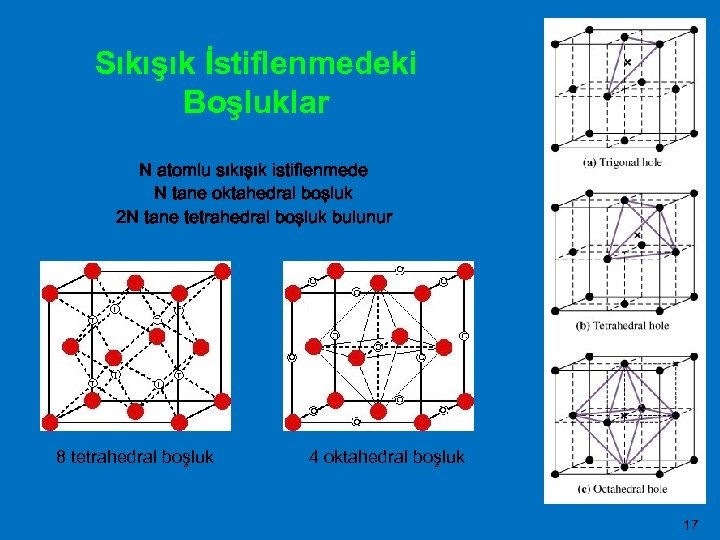
Sıkışık İstiflenmedeki Boşluklar N atomlu sıkışık istiflenmede N tane oktahedral boşluk 2 N tane tetrahedral boşluk bulunur 8 tetrahedral boşluk 4 oktahedral boşluk 17
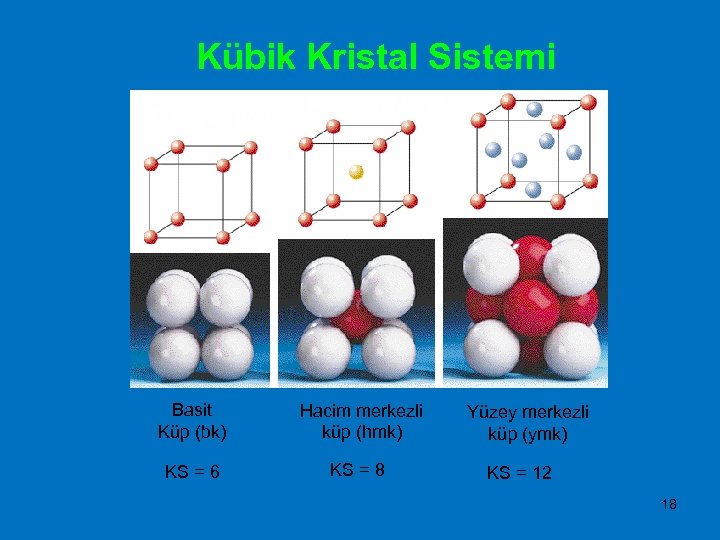
Kübik Kristal Sistemi Polonyum (Po) Fe, V, Cr, Mo, W Basit Küp (bk) Hacim merkezli küp (hmk) KS = 6 KS = 8 Yüzey merkezli küp (ymk) KS = 12 18

Amaç • Basit kristal yapısının çizilmesi • Bir çok önemli kristal yapısının close-packing ile tanımlanabilir olmasının önemi • Benzer yapıların karşılaştırılması ve farklarının anlaşılması
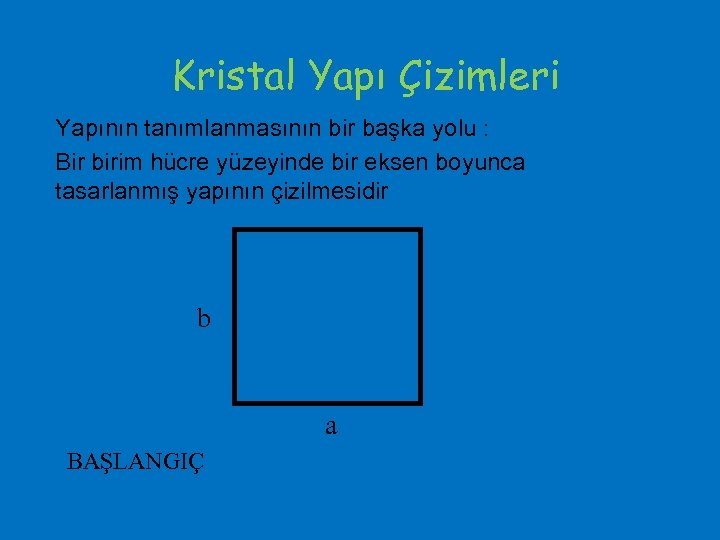
Kristal Yapı Çizimleri Yapının tanımlanmasının bir başka yolu : Bir birim hücre yüzeyinde bir eksen boyunca tasarlanmış yapının çizilmesidir b a BAŞLANGIÇ
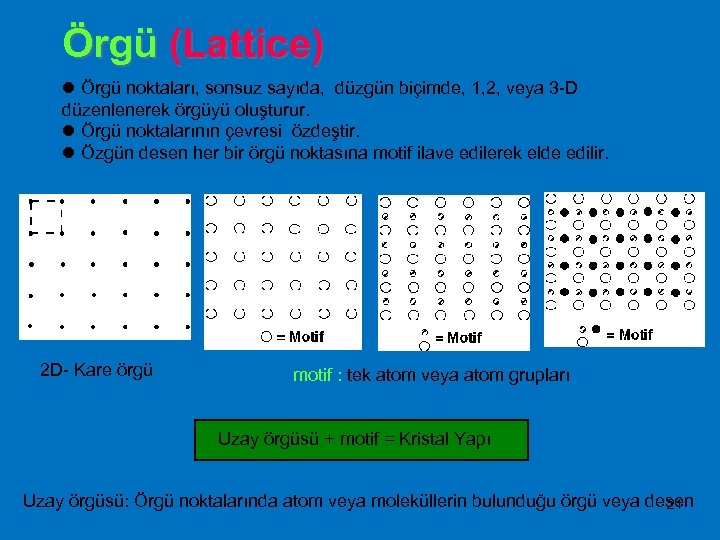
Örgü (Lattice) l Örgü noktaları, sonsuz sayıda, düzgün biçimde, 1, 2, veya 3 -D düzenlenerek örgüyü oluşturur. l Örgü noktalarının çevresi özdeştir. l Özgün desen her bir örgü noktasına motif ilave edilerek elde edilir. 2 D- Kare örgü motif : tek atom veya atom grupları Uzay örgüsü + motif = Kristal Yapı Uzay örgüsü: Örgü noktalarında atom veya moleküllerin bulunduğu örgü veya desen 21

Metalik Kristaller • Çoğu metaller (ksi), (hsi) ve (hmk) hacim merkezli kübik kristal yapılarına bulunur. hmk(KS: 8) Be, Mg, Zn, Cd, Ti, Zr, …. hsi (KS: 12) Zn, Cd, Tl…. ksi (KS: 12) Cu, Ag, Au, Al, Ni, Pd, Pt • Bir metal için, basınç ve sıcaklık değiştirilirse birden çok kristal yapıda elde edilebilir. Co ABCABC 500 °C > Co ABABAB 500 °C < • Yumuşak ve dövülebilir metaller, genellikle (ymk) yapısındadır. (bakır) ymk yapılarda daha çok düzlem mevcuttur. • Sert ve kırılgan metaller genellikle (hsi) yapısındadır (çinko) • Çoğu metal bükülebilir, çünkü metalik bağ yöne bağımlı değildir. • Atomlar birbiri üzerinde kayabilir ve yeniden kristal şekli alabilir. 22
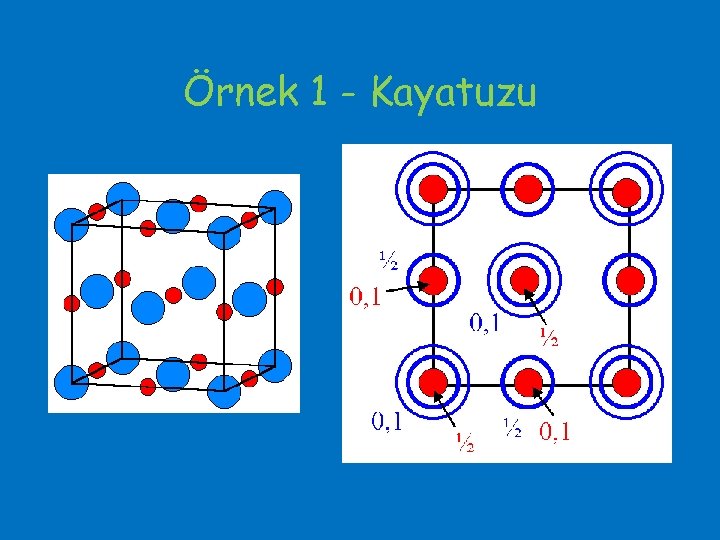
Örnek 1 - Kayatuzu
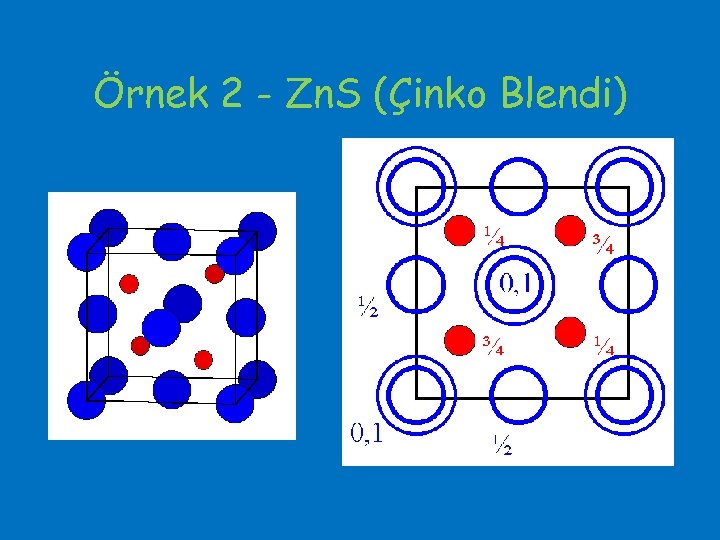
Örnek 2 - Zn. S (Çinko Blendi)
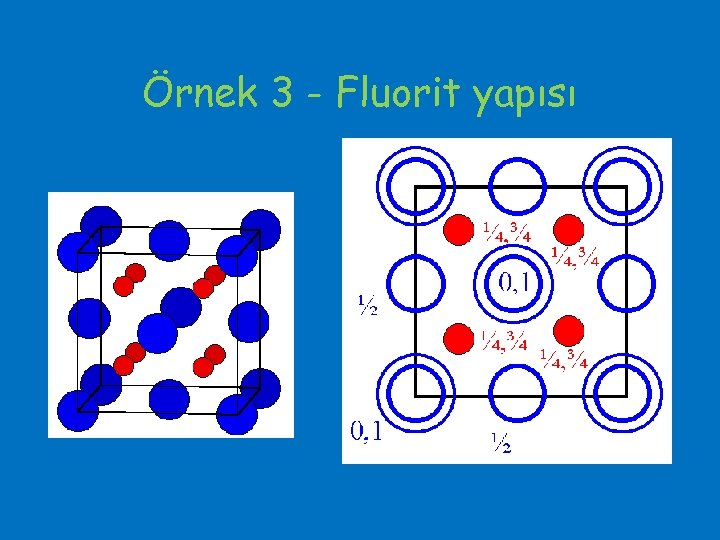
Örnek 3 - Fluorit yapısı
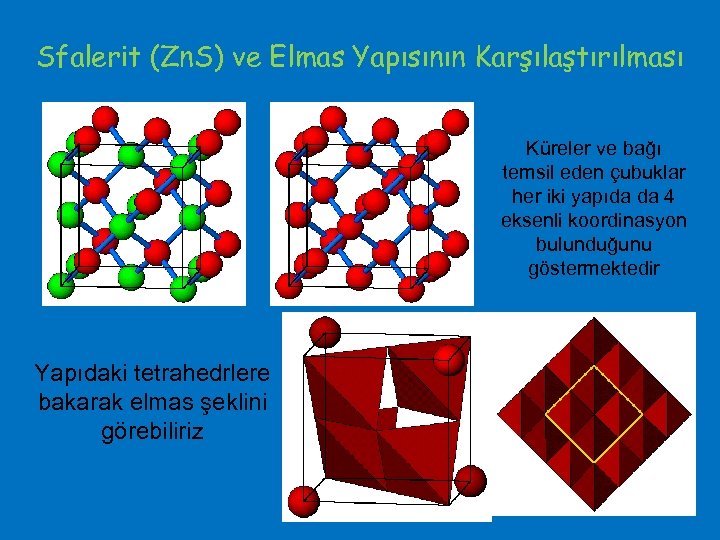
Sfalerit (Zn. S) ve Elmas Yapısının Karşılaştırılması Küreler ve bağı temsil eden çubuklar her iki yapıda da 4 eksenli koordinasyon bulunduğunu göstermektedir Yapıdaki tetrahedrlere bakarak elmas şeklini görebiliriz
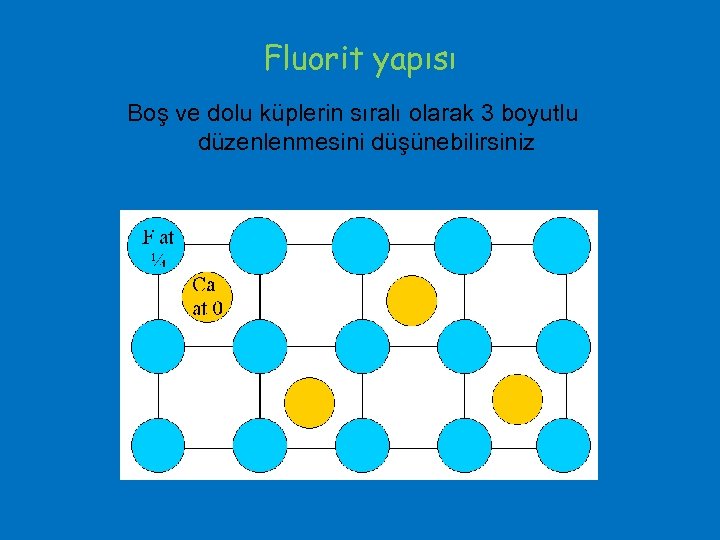
Fluorit yapısı Boş ve dolu küplerin sıralı olarak 3 boyutlu düzenlenmesini düşünebilirsiniz
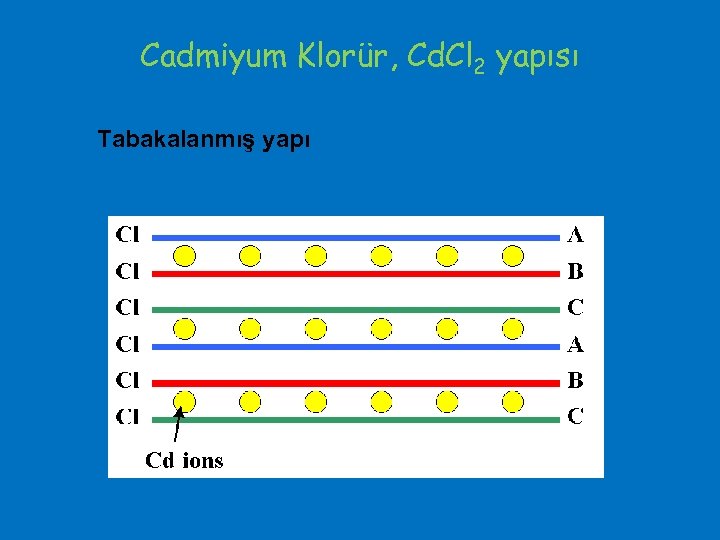
Cadmiyum Klorür, Cd. Cl 2 yapısı Tabakalanmış yapı
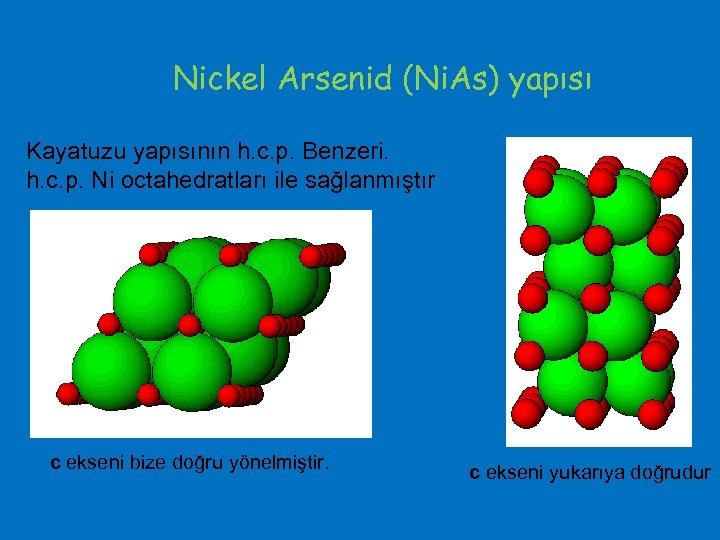
Nickel Arsenid (Ni. As) yapısı Kayatuzu yapısının h. c. p. Benzeri. h. c. p. Ni octahedratları ile sağlanmıştır c ekseni bize doğru yönelmiştir. c ekseni yukarıya doğrudur
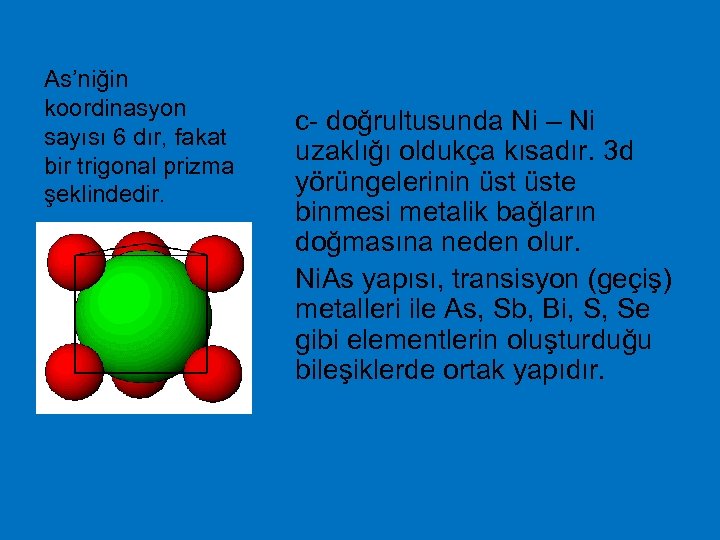
As’niğin koordinasyon sayısı 6 dır, fakat bir trigonal prizma şeklindedir. c- doğrultusunda Ni – Ni uzaklığı oldukça kısadır. 3 d yörüngelerinin üste binmesi metalik bağların doğmasına neden olur. Ni. As yapısı, transisyon (geçiş) metalleri ile As, Sb, Bi, S, Se gibi elementlerin oluşturduğu bileşiklerde ortak yapıdır.

AX yapısının özeti Zn. S wurtzit sfalerit koordinasyon sayısı = 4 Na. Cl, Ni. As koordinasyon sayısı = 6 Cs. Cl koordinasyon sayısı = 8 Genel kural, daha büyük (ağır) katyonların daha büyük koordinasyon sayısına sahip olduğu şeklindedir. Bu AX 2 yapısında da gözlenebilir

AX 2 yapısının özeti Si. O 2, Be. F 2 silisyum yapısı Ti. O 2, Mg. F 2 rutil yapısı KS = 4 : 2 KS = 6 : 3 Cd. Cl 2, Cd. I 2 tabaka yapısı KS = 6 : 3 Pb. O 2, Ca. F 2 fluorit yapısı KS = 8 : 4

Amaç • Kesirli koordinatlar yardımı ile atom pozisyonlarının belirlenmesi • Bir küp içindeki octahedral ve tetrahedral konumlar arasındaki uzaklıkların hesaplanması • Bir küp içindeki intersitisyel konumların büyüklüklerinin hesaplanması
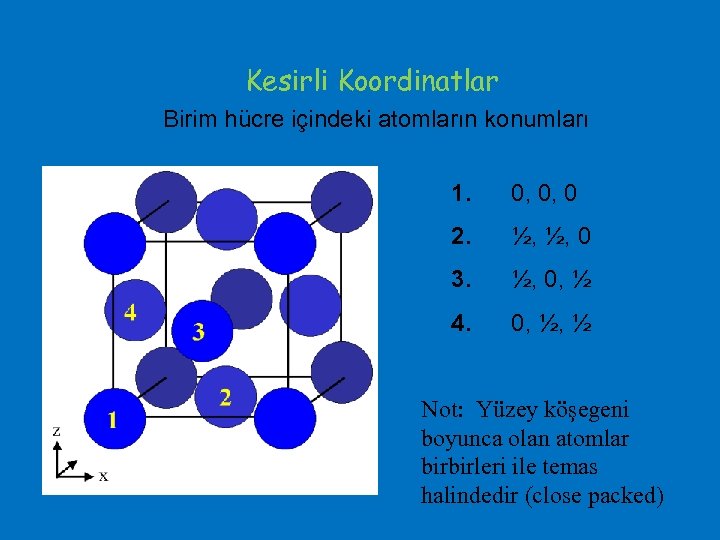
Kesirli Koordinatlar Birim hücre içindeki atomların konumları 1. 0, 0, 0 2. ½, ½, 0 3. ½, 0, ½ 4. 0, ½, ½ Not: Yüzey köşegeni boyunca olan atomlar birbirleri ile temas halindedir (close packed)
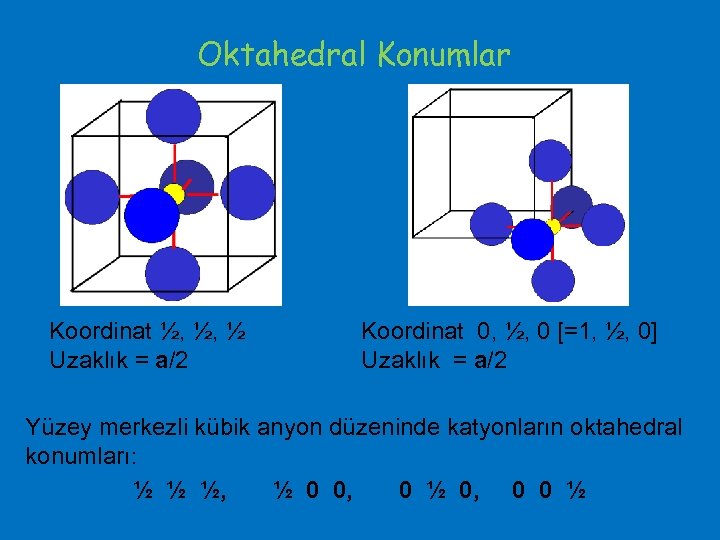
Oktahedral Konumlar Koordinat ½, ½, ½ Uzaklık = a/2 Koordinat 0, ½, 0 [=1, ½, 0] Uzaklık = a/2 Yüzey merkezli kübik anyon düzeninde katyonların oktahedral konumları: ½ ½ ½, ½ 0 0, 0 ½ 0, 0 0 ½
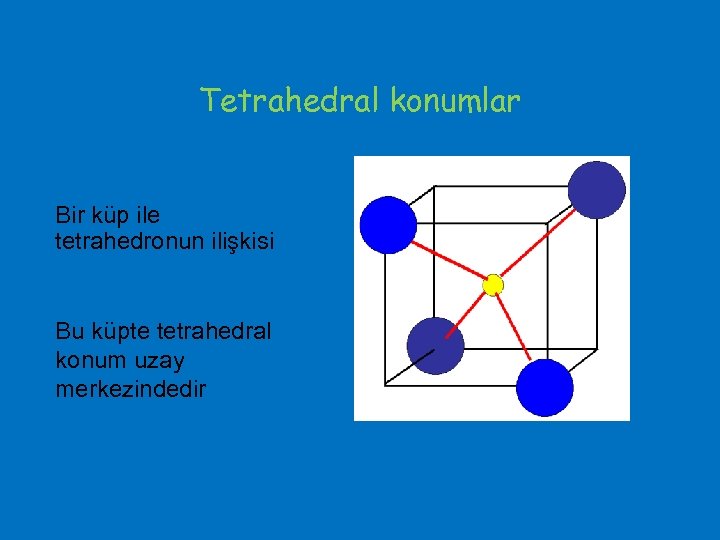
Tetrahedral konumlar Bir küp ile tetrahedronun ilişkisi Bu küpte tetrahedral konum uzay merkezindedir
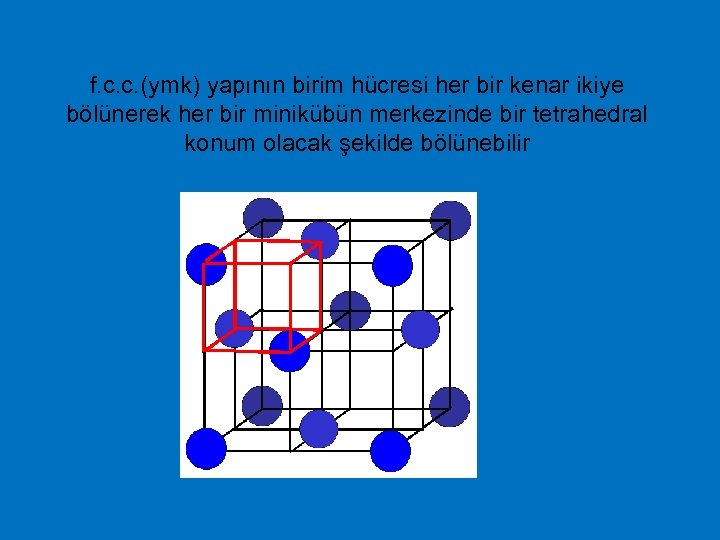
f. c. c. (ymk) yapının birim hücresi her bir kenar ikiye bölünerek her bir minikübün merkezinde bir tetrahedral konum olacak şekilde bölünebilir
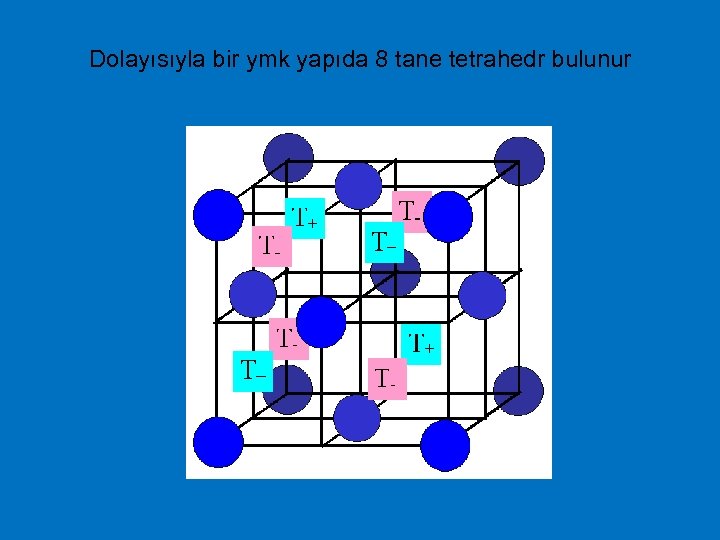
Dolayısıyla bir ymk yapıda 8 tane tetrahedr bulunur
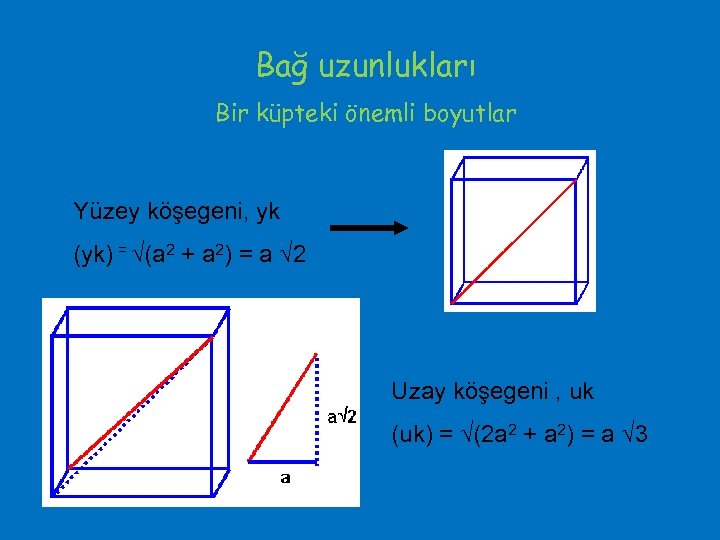
Bağ uzunlukları Bir küpteki önemli boyutlar Yüzey köşegeni, yk (yk) = (a 2 + a 2) = a 2 Uzay köşegeni , uk (uk) = (2 a 2 + a 2) = a 3
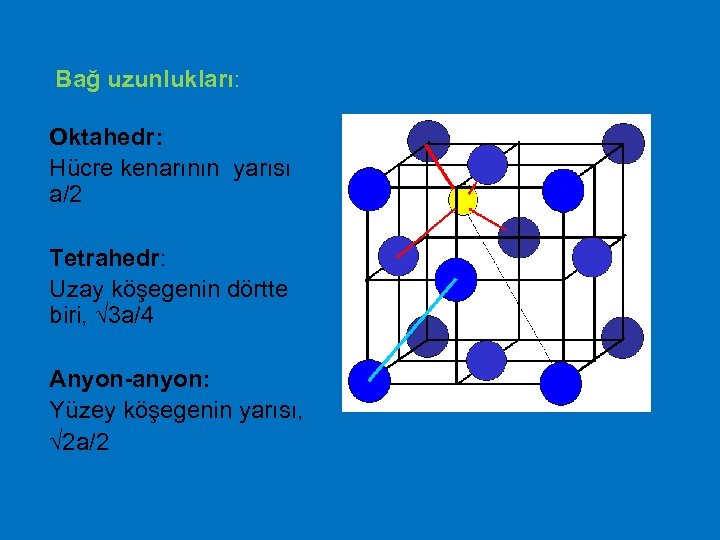
Bağ uzunlukları: Oktahedr: Hücre kenarının yarısı a/2 Tetrahedr: Uzay köşegenin dörtte biri, 3 a/4 Anyon-anyon: Yüzey köşegenin yarısı, 2 a/2
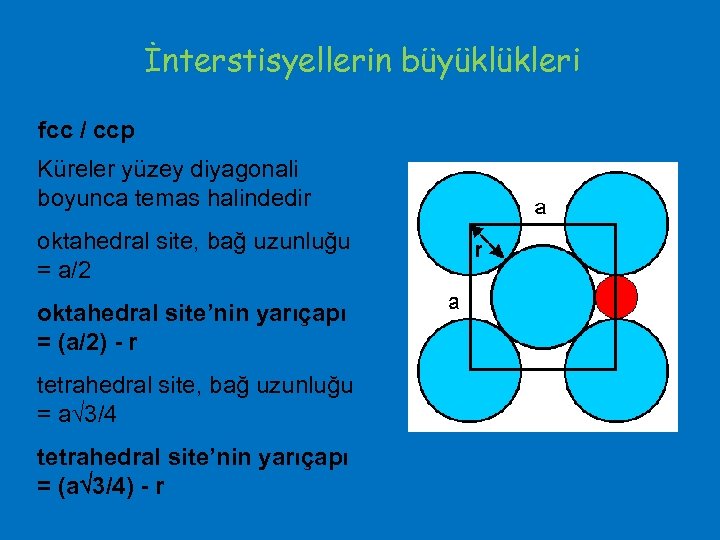
İnterstisyellerin büyüklükleri fcc / ccp Küreler yüzey diyagonali boyunca temas halindedir oktahedral site, bağ uzunluğu = a/2 oktahedral site’nin yarıçapı = (a/2) - r tetrahedral site, bağ uzunluğu = a 3/4 tetrahedral site’nin yarıçapı = (a 3/4) - r
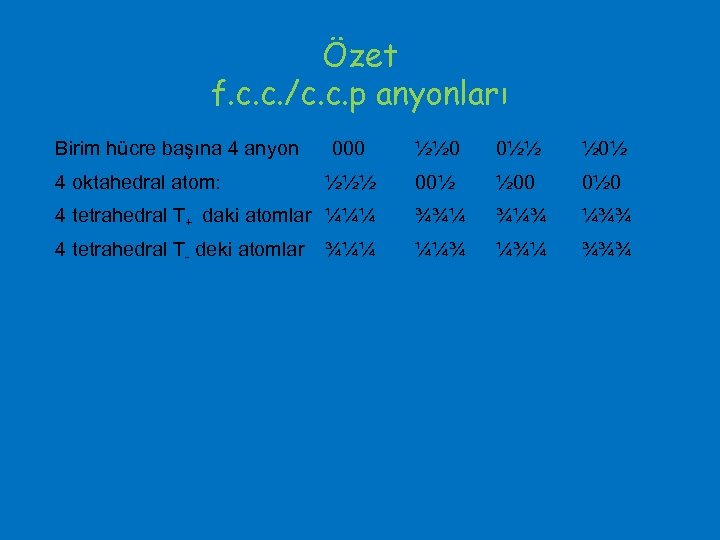
Özet f. c. c. /c. c. p anyonları Birim hücre başına 4 anyon 000 ½½ 0 0½½ ½ 0½ 4 oktahedral atom: 00½ ½ 00 0½ 0 4 tetrahedral T+ daki atomlar ¼¼¼ ¾¾¼ ¾¼¾ ¼¾¾ 4 tetrahedral T- deki atomlar ¼¼¾ ¼¾¼ ¾¾¾ ½½½ ¾¼¼

Özet Ø Kübün basit geometrisi ve Pisagor teoremi kullanılarak bir fcc (ymk) yapıda oktahedral bağ uzunluklarını (a/2) ve tetrahedral bağ uzunluklarını ( 3 a/4) hesaplayabiliriz. Ø Sonuç olarak oktahedral interstisyelin [(a/2) – r] ve tetrahedral interstisyelin [(a 3/4) – r] yarıçapları hesaplanabilir. Burada r, iyon paketlenme yarıçapıdır.

Amaç • Paketleme kesrinin gösterilmesi • Paketleme kesirlerinin iki farklı paketleme rejimi için tanımlanması • Bir primitif hücre için ilk n çizgilerinin hkl değerlerinin bulunması
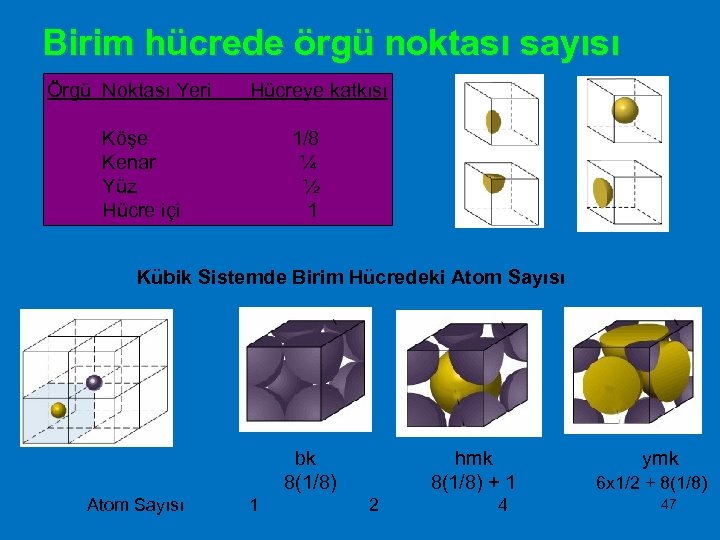
Birim hücrede örgü noktası sayısı Örgü Noktası Yeri Hücreye katkısı Köşe 1/8 Kenar ¼ Yüz ½ Hücre içi 1 Kübik Sistemde Birim Hücredeki Atom Sayısı bk hmk ymk 8(1/8) + 1 6 x 1/2 + 8(1/8) Atom Sayısı 1 2 4 47
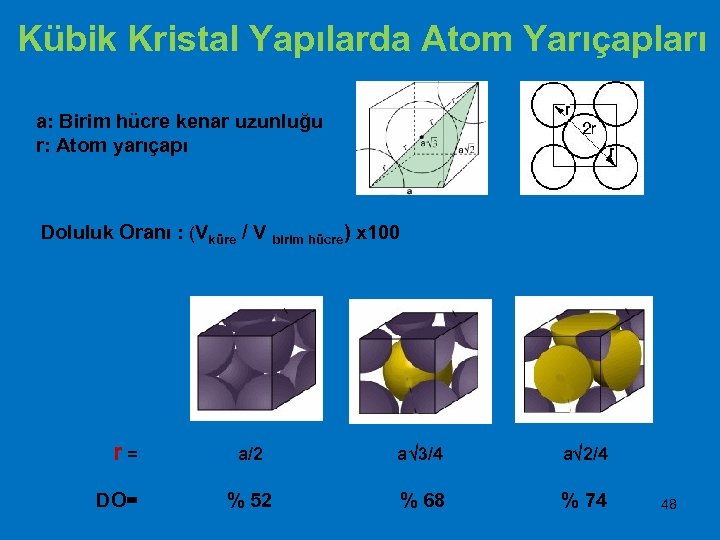
Kübik Kristal Yapılarda Atom Yarıçapları a: Birim hücre kenar uzunluğu r: Atom yarıçapı Doluluk Oranı : (Vküre / V birim hücre) x 100 r= DO= a/2 a 3/4 a 2/4 % 52 % 68 % 74 48

Örnek: Basit kübik birim hücre için paketleme kesrini hesaplayınız.
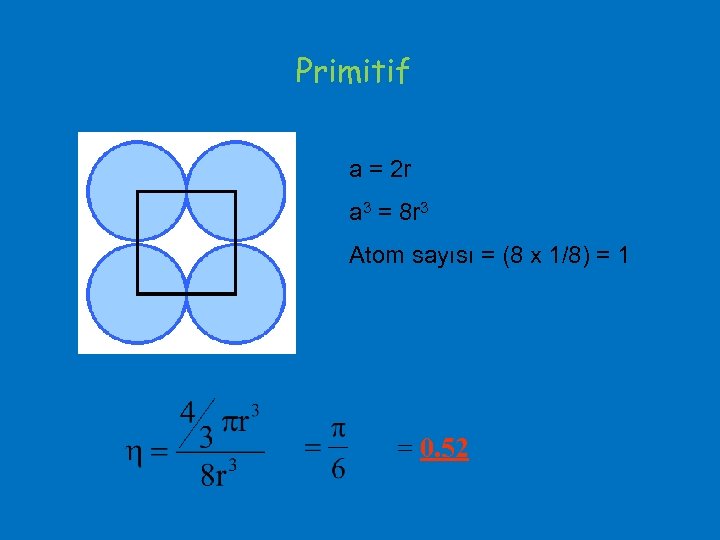
Primitif a = 2 r a 3 = 8 r 3 Atom sayısı = (8 x 1/8) = 1 = 0. 52

Paketleme Kesirleri - ccp Kübik kapalı paket (cubic close packing) = fcc
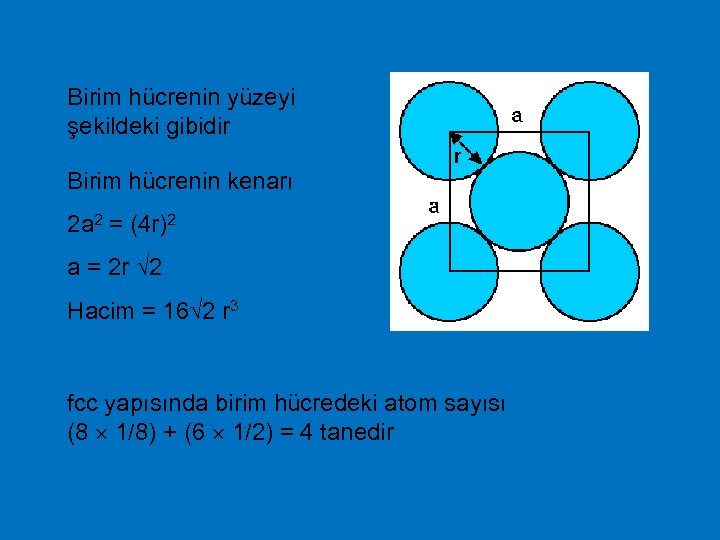
Birim hücrenin yüzeyi şekildeki gibidir Birim hücrenin kenarı 2 a 2 = (4 r)2 a = 2 r 2 Hacim = 16 2 r 3 fcc yapısında birim hücredeki atom sayısı (8 1/8) + (6 1/2) = 4 tanedir

Paketleme Kesri Bir yapıda atomların işgal ettiği hacmin toplam hacme oranına paketleme kesri denir ve ile gösterilir. Kübik kapalı paket için Küreler paketleme kesri 0, 74 olacak şekilde birbirleri ile mümkün olabildiğince sıkı paket haline gelmişlerdir.

Problem Al ( 26. 98 akb) ymk yapıya sahiptir ve atom yarıçapı 143. 2 pm dir. a) Birim hücre boyutunu b) Al metalinin yoğunluğunu hesaplayınız. a) r = a 2/4 a = 4(143. 2)/(2)1/2 = 405. 0 pm b) Birim hücre kütlesi = 4 Al atom kütlesi (26. 98)(g/mol)(1 mol/6. 022 x 1023 atom)(4 atom/birim hücre) = 1. 792 x 10 -22 g Birim hücre hacmi a 3 = (405 x 10 -10 cm)3 = 66. 43 x 10 -24 cm 3 Yoğunluk d = m / V ( birim hücre başına g/cm 3) Birim hücre yoğunluğu = 1. 792 x 10 -22 g / 66. 43 x 10 -24 cm 3 = 2. 698 g/cm 3 54

Problem : ymk kristal örgüsünde doluluk oranı nedir? Küre hacmi : 4/3 r 3 ymk örgüde toplam küre hacmi V = 4(4/3 r 3) Birim hücre hacmi = a 3 ymk örgüde r = a 2/4 Doluluk Oranı : (Vtoplam küre / a 3) x 100 DO = 4(4/3 r 3) a 3 4(4/3 )(a 2/4)3 x 100 = % 74 X 100 = a 3 55
0ea9c386350bf4dacd71db9fa8d19f6e.ppt