Лекция 7. Диаграмма железо-цементит.pptx
- Количество слайдов: 22
 Материаловедение Железоуглеродистые сплавы Характеристика компонентов (структура, свойства) в системе железо – углерод. Структурные составляющие системы железо-углерод. Диаграммы состояния железо – углерод. Основной и упрощенный варианты. Характеристические точки диаграммы состояния железо-цементит. Основные линии и области диаграммы плавкости. Анализ диаграммы по фрагментам и характеристика структуры сплавов в зависимости от температуры и концентрации углерода. Построение кривых охлаждения сплавов по диаграмме состояния.
Материаловедение Железоуглеродистые сплавы Характеристика компонентов (структура, свойства) в системе железо – углерод. Структурные составляющие системы железо-углерод. Диаграммы состояния железо – углерод. Основной и упрощенный варианты. Характеристические точки диаграммы состояния железо-цементит. Основные линии и области диаграммы плавкости. Анализ диаграммы по фрагментам и характеристика структуры сплавов в зависимости от температуры и концентрации углерода. Построение кривых охлаждения сплавов по диаграмме состояния.
 • В промышленности чистое железо практически не используется, а наиболее широко применяются его сплавы. Основными из них являются системы железа с углеродом называемые сталями и чугунами. • Сталь – сплав железа и углерода с содержанием углерода до 2. 14% • Чугун – сплав железа и углерода с содержанием углерода свыше 2. 14%
• В промышленности чистое железо практически не используется, а наиболее широко применяются его сплавы. Основными из них являются системы железа с углеродом называемые сталями и чугунами. • Сталь – сплав железа и углерода с содержанием углерода до 2. 14% • Чугун – сплав железа и углерода с содержанием углерода свыше 2. 14%
 Гомоядерное металлическое соединение - железо • Химический знак Fe; атомный номер 26; радиус 0, 127 нм; масса 55, 85; металл. • Общее его содержание в земной коре составляет 5, 1 %. Нахождение в природе. Руды: железняки: магнитный или магнетит - Fe 3 O 4, красный или гематит - Fe 2 O 3, бурый или гетит и лимонит - Fe 2 O 3, шпатовый или сидерит Fe. СO 3. Железный или серный колчедан (пирит) - Fe. S 2. • Некоторые физико-химические свойства: Тпл = 1539 5 °С, плотность = 7, 68 - 7, 85 г/см 3. твердость (НВ) 80, в 25 кгс/мм 2; 0, 2 = 12 кгс/мм 2; = 50 %; = 80 %. Техническое железо (99, 8 - 99, 9 % Fе): магнитная проницаемость max = (6, 28 12, 5)· 10 -3 Г/м и коэрцитивная сила НС = 39, 8 79, 6 А/м; чистый металл (99, 99 % Fе): max = 35, 2· 10 -3 Г/м и НC 1, 99 А/м. Коэффициент линейного расширения = 11, 7 10 -6 °C-1, теплопроводность = 83, 6 Вт/(м·К). = 10 104 Ом·м.
Гомоядерное металлическое соединение - железо • Химический знак Fe; атомный номер 26; радиус 0, 127 нм; масса 55, 85; металл. • Общее его содержание в земной коре составляет 5, 1 %. Нахождение в природе. Руды: железняки: магнитный или магнетит - Fe 3 O 4, красный или гематит - Fe 2 O 3, бурый или гетит и лимонит - Fe 2 O 3, шпатовый или сидерит Fe. СO 3. Железный или серный колчедан (пирит) - Fe. S 2. • Некоторые физико-химические свойства: Тпл = 1539 5 °С, плотность = 7, 68 - 7, 85 г/см 3. твердость (НВ) 80, в 25 кгс/мм 2; 0, 2 = 12 кгс/мм 2; = 50 %; = 80 %. Техническое железо (99, 8 - 99, 9 % Fе): магнитная проницаемость max = (6, 28 12, 5)· 10 -3 Г/м и коэрцитивная сила НС = 39, 8 79, 6 А/м; чистый металл (99, 99 % Fе): max = 35, 2· 10 -3 Г/м и НC 1, 99 А/м. Коэффициент линейного расширения = 11, 7 10 -6 °C-1, теплопроводность = 83, 6 Вт/(м·К). = 10 104 Ом·м.
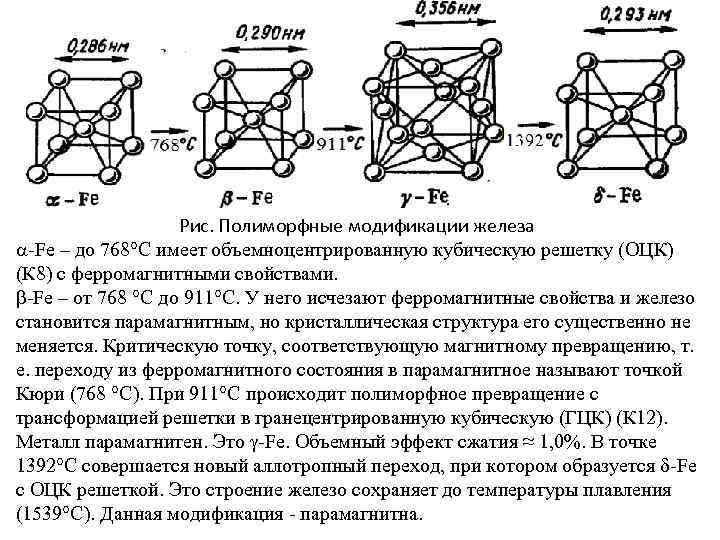 Рис. Полиморфные модификации железа -Fe – до 768 С имеет объемноцентрированную кубическую решетку (ОЦК) (К 8) с ферромагнитными свойствами. -Fe – от 768 С до 911 С. У него исчезают ферромагнитные свойства и железо становится парамагнитным, но кристаллическая структура его существенно не меняется. Критическую точку, соответствующую магнитному превращению, т. е. переходу из ферромагнитного состояния в парамагнитное называют точкой Кюри (768 С). При 911 С происходит полиморфное превращение с трансформацией решетки в гранецентрированную кубическую (ГЦК) (К 12). Металл парамагнитен. Это -Fe. Объемный эффект сжатия ≈ 1, 0%. В точке 1392 С совершается новый аллотропный переход, при котором образуется -Fe с ОЦК решеткой. Это строение железо сохраняет до температуры плавления (1539 С). Данная модификация - парамагнитна.
Рис. Полиморфные модификации железа -Fe – до 768 С имеет объемноцентрированную кубическую решетку (ОЦК) (К 8) с ферромагнитными свойствами. -Fe – от 768 С до 911 С. У него исчезают ферромагнитные свойства и железо становится парамагнитным, но кристаллическая структура его существенно не меняется. Критическую точку, соответствующую магнитному превращению, т. е. переходу из ферромагнитного состояния в парамагнитное называют точкой Кюри (768 С). При 911 С происходит полиморфное превращение с трансформацией решетки в гранецентрированную кубическую (ГЦК) (К 12). Металл парамагнитен. Это -Fe. Объемный эффект сжатия ≈ 1, 0%. В точке 1392 С совершается новый аллотропный переход, при котором образуется -Fe с ОЦК решеткой. Это строение железо сохраняет до температуры плавления (1539 С). Данная модификация - парамагнитна.
 Углерод: алмаз • Углерод – химический знак С, атомный номер 6, радиус 0, 077 нм или 0, 77 Å; масса 12, 011; неметалл. Массовая доля углерода в земной коре составляет 0, 1 %. Он встречается в природе в свободном состоянии в двух аллотропных видоизменениях - алмаза и графита. • Алмаз – прозрачное кристаллическое вещество с атомной кубической решеткой. В ней каждое ядро атома углерода окружено четырьмя близлежащими, образуя тетраэдр с равноценными прочными ковалентными -связями. Межъядерное расстояние d. С-С равно 0, 143 нм. Это обуславливает у алмаза исключительную твердость, очень высокую лучепреломляемость и отсутствие способности проводить тепло и электрический ток в обычных условиях (Е = 5, 7 э. В). Об его жесткой структуре свидетельствует также очень небольшая величина энтропии - всего 2, 4 Дж/(град моль). Плотность алмаза = 3, 5 г/см 3 Структура алмаза
Углерод: алмаз • Углерод – химический знак С, атомный номер 6, радиус 0, 077 нм или 0, 77 Å; масса 12, 011; неметалл. Массовая доля углерода в земной коре составляет 0, 1 %. Он встречается в природе в свободном состоянии в двух аллотропных видоизменениях - алмаза и графита. • Алмаз – прозрачное кристаллическое вещество с атомной кубической решеткой. В ней каждое ядро атома углерода окружено четырьмя близлежащими, образуя тетраэдр с равноценными прочными ковалентными -связями. Межъядерное расстояние d. С-С равно 0, 143 нм. Это обуславливает у алмаза исключительную твердость, очень высокую лучепреломляемость и отсутствие способности проводить тепло и электрический ток в обычных условиях (Е = 5, 7 э. В). Об его жесткой структуре свидетельствует также очень небольшая величина энтропии - всего 2, 4 Дж/(град моль). Плотность алмаза = 3, 5 г/см 3 Структура алмаза
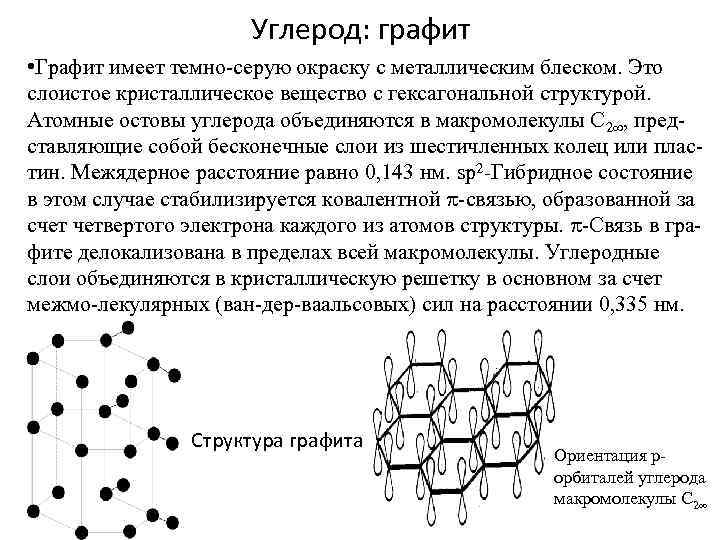 Углерод: графит • Графит имеет темно-серую окраску с металлическим блеском. Это слоистое кристаллическое вещество с гексагональной структурой. Атомные остовы углерода объединяются в макромолекулы С 2 , представляющие собой бесконечные слои из шестичленных колец или пластин. Межядерное расстояние равно 0, 143 нм. sp 2 -Гибридное состояние в этом случае стабилизируется ковалентной -связью, образованной за счет четвертого электрона каждого из атомов структуры. -Связь в графите делокализована в пределах всей макромолекулы. Углеродные слои объединяются в кристаллическую решетку в основном за счет межмо-лекулярных (ван-дер-ваальсовых) сил на расстоянии 0, 335 нм. Структура графита Ориентация рорбиталей углерода макромолекулы С 2
Углерод: графит • Графит имеет темно-серую окраску с металлическим блеском. Это слоистое кристаллическое вещество с гексагональной структурой. Атомные остовы углерода объединяются в макромолекулы С 2 , представляющие собой бесконечные слои из шестичленных колец или пластин. Межядерное расстояние равно 0, 143 нм. sp 2 -Гибридное состояние в этом случае стабилизируется ковалентной -связью, образованной за счет четвертого электрона каждого из атомов структуры. -Связь в графите делокализована в пределах всей макромолекулы. Углеродные слои объединяются в кристаллическую решетку в основном за счет межмо-лекулярных (ван-дер-ваальсовых) сил на расстоянии 0, 335 нм. Структура графита Ориентация рорбиталей углерода макромолекулы С 2
 Углерод: графит • Прочность химических связей в плоскости макромолекулы (716 к. Дж/моль) значительно больше, чем между слоями (всего 17 к. Дж/моль), поэтому графит мягок, обладает низкой прочностью и легко расщепляется на тонкие чешуйки, которые сами по себе очень прочные. Между отдельными пластинками в решетке имеются свободные электроны, сообщающие графиту электро- и теплопроводность, но ниже, чем у металлов. Плотность графита (2, 1 - 2, 5 г/см 3) меньше, чем у алмаза; энтропия - больше и составляет 5, 74 Дж/град моль. • Графит является очень хрупким материалом. Его прочность при сжатии выше, чем при изгибе и растяжении. Для графита характерно увеличение прочности и модуля упругости при нагреве. • Графит не плавится при атмосферном давлении, а при 3700 °С сублимирует (испаряется), минуя стадию плавления, с затратой значительной тепловой энергии на этот процесс (жидкое состояние углерода может быть достигнуто лишь при 4000 °С и давлении выше 10 МПа). Качества природного графита невысоки, он содержит много примесей, порист. Поэтому его применяют лишь как антифрикционный материал и в электротехнике.
Углерод: графит • Прочность химических связей в плоскости макромолекулы (716 к. Дж/моль) значительно больше, чем между слоями (всего 17 к. Дж/моль), поэтому графит мягок, обладает низкой прочностью и легко расщепляется на тонкие чешуйки, которые сами по себе очень прочные. Между отдельными пластинками в решетке имеются свободные электроны, сообщающие графиту электро- и теплопроводность, но ниже, чем у металлов. Плотность графита (2, 1 - 2, 5 г/см 3) меньше, чем у алмаза; энтропия - больше и составляет 5, 74 Дж/град моль. • Графит является очень хрупким материалом. Его прочность при сжатии выше, чем при изгибе и растяжении. Для графита характерно увеличение прочности и модуля упругости при нагреве. • Графит не плавится при атмосферном давлении, а при 3700 °С сублимирует (испаряется), минуя стадию плавления, с затратой значительной тепловой энергии на этот процесс (жидкое состояние углерода может быть достигнуто лишь при 4000 °С и давлении выше 10 МПа). Качества природного графита невысоки, он содержит много примесей, порист. Поэтому его применяют лишь как антифрикционный материал и в электротехнике.
 Структурные составляющие системы железо-углерод: феррит, аустенит Однофазные. • Твердые растворы Объемноцентрированная кубическая (ОЦК) решетка -железа имеет пустые места (поры) в середине каждого ребра, их двенадцать. Диаметр его составляет 0, 62 Å. Если сравнить данное значение с таковым для углерода (0, 77 Å), то можно увидеть, что оно практически недоступно для внедряющегося в железо углерода. Поэтому растворимость данного неметалла в -железе очень низка. При 727 С она составляет практически около 0, 02 %. От 1392 до 1499 С максимальная предельная растворимость углерода равна 0, 1 %. При охлаждении раствора до комнатной температуры данное значение снижается до 0, 006 %. Гранецентрированная кубическая (ГЦК) решетка -железа в отличие от ОЦК располагает всего одной порой, но с большим диаметром – 1, 02 Å. Это позволяет разместиться внедряемому атому углерода в ней, слегка исказив ее, вызвав небольшое увеличение параметров. При 1147 С предельная растворимость углерода в -железе составляет 2, 14 %, а при 727 С всего лишь 0, 8 % (перлит).
Структурные составляющие системы железо-углерод: феррит, аустенит Однофазные. • Твердые растворы Объемноцентрированная кубическая (ОЦК) решетка -железа имеет пустые места (поры) в середине каждого ребра, их двенадцать. Диаметр его составляет 0, 62 Å. Если сравнить данное значение с таковым для углерода (0, 77 Å), то можно увидеть, что оно практически недоступно для внедряющегося в железо углерода. Поэтому растворимость данного неметалла в -железе очень низка. При 727 С она составляет практически около 0, 02 %. От 1392 до 1499 С максимальная предельная растворимость углерода равна 0, 1 %. При охлаждении раствора до комнатной температуры данное значение снижается до 0, 006 %. Гранецентрированная кубическая (ГЦК) решетка -железа в отличие от ОЦК располагает всего одной порой, но с большим диаметром – 1, 02 Å. Это позволяет разместиться внедряемому атому углерода в ней, слегка исказив ее, вызвав небольшое увеличение параметров. При 1147 С предельная растворимость углерода в -железе составляет 2, 14 %, а при 727 С всего лишь 0, 8 % (перлит).
 Структурные составляющие системы железо-углерод: феррит, аустенит Однофазные. Твердые растворы внедрения углерода в -железе (ОЦК-решетка) называют ферритом ( ), а в -железе (ГЦК-решетка) аустенитом ( ). Различают низкотемпературный -феррит с растворимостью углерода до 0, 02 % и высокотемпературный -феррит с предельной растворимостью углерода 0, 1%. Углерод в решетке феррита располагается в центре объема куба. Под микроскопом феррит выявляется в виде однородных полиэдрических зерен. Твердость и механические свойства феррита близки к таковым технически чистого железа ( в=250 МПа, 0, 2=120 МПа, =50 %, =80 %, НВ=800 -900 МПа). Они зависят от количества элементов, присутствующих в нем (многие химические элементы образуют с ферритом твердые растворы замещения). Аустенит – парамагнитен, высокопластичен (НВ=1700 -2200 МПа), имеет низкие механические характеристики, такие как пределы текучести и прочности. Микроструктура аустенита - полиэдрические зерна. Углерод в решетке -железа располагается в центре элементарной ячейки При температуре 1147 °С растворимость углерода максимальна – 2, 14%, с понижением температуры она убывает до 0, 8%
Структурные составляющие системы железо-углерод: феррит, аустенит Однофазные. Твердые растворы внедрения углерода в -железе (ОЦК-решетка) называют ферритом ( ), а в -железе (ГЦК-решетка) аустенитом ( ). Различают низкотемпературный -феррит с растворимостью углерода до 0, 02 % и высокотемпературный -феррит с предельной растворимостью углерода 0, 1%. Углерод в решетке феррита располагается в центре объема куба. Под микроскопом феррит выявляется в виде однородных полиэдрических зерен. Твердость и механические свойства феррита близки к таковым технически чистого железа ( в=250 МПа, 0, 2=120 МПа, =50 %, =80 %, НВ=800 -900 МПа). Они зависят от количества элементов, присутствующих в нем (многие химические элементы образуют с ферритом твердые растворы замещения). Аустенит – парамагнитен, высокопластичен (НВ=1700 -2200 МПа), имеет низкие механические характеристики, такие как пределы текучести и прочности. Микроструктура аустенита - полиэдрические зерна. Углерод в решетке -железа располагается в центре элементарной ячейки При температуре 1147 °С растворимость углерода максимальна – 2, 14%, с понижением температуры она убывает до 0, 8%
 Структурные составляющие системы железо-углерод: цементит Химические соединения 5Å с 51 = 4, А = 6, 726 Å • Железо и углерод, взаимодействуя друг с другом, образуют ряд металлических карбидов: Fе 3 С, Fе 2 С, Fе. С и др. Наиболее распространенным является карбид железа среднего состава Fе 3 С. Стехиометрическое соотношение элементов в нем равно 3 : 1. Концентрация углерода составляет 6, 67% масс. Очень твердый (НВ более 8000 МПа) и хрупкий. Поэтому он и назван цементитом. Температура плавления принимается равной примерно 1260 С. До 210 С цементит ферромагнитен. Кристаллическая решетка: орторомбическая структура с плотной упаковкой атомов (в элементарной ячейке расположено 12 атомов железа и 4 углерода). Характер связи между атомами железа чисто металлический, а между железом и углеродом ионно-металлический с преобладанием металличности и они оба ведут себя как металлы. Такое строение приводит к тому, что он проявляет металлические признаки: блеск, высокая b = 5, 077 Å Fe C Кристаллическая структура цементита • электропроводность, уменьшающаяся с повышением температуры, легкость образования твердых растворов с металлами, значительной жаропрочностью
Структурные составляющие системы железо-углерод: цементит Химические соединения 5Å с 51 = 4, А = 6, 726 Å • Железо и углерод, взаимодействуя друг с другом, образуют ряд металлических карбидов: Fе 3 С, Fе 2 С, Fе. С и др. Наиболее распространенным является карбид железа среднего состава Fе 3 С. Стехиометрическое соотношение элементов в нем равно 3 : 1. Концентрация углерода составляет 6, 67% масс. Очень твердый (НВ более 8000 МПа) и хрупкий. Поэтому он и назван цементитом. Температура плавления принимается равной примерно 1260 С. До 210 С цементит ферромагнитен. Кристаллическая решетка: орторомбическая структура с плотной упаковкой атомов (в элементарной ячейке расположено 12 атомов железа и 4 углерода). Характер связи между атомами железа чисто металлический, а между железом и углеродом ионно-металлический с преобладанием металличности и они оба ведут себя как металлы. Такое строение приводит к тому, что он проявляет металлические признаки: блеск, высокая b = 5, 077 Å Fe C Кристаллическая структура цементита • электропроводность, уменьшающаяся с повышением температуры, легкость образования твердых растворов с металлами, значительной жаропрочностью
 Структурные составляющие системы железо-углерод: перлит, ледебурит Двухфазные механические смеси. Перлит - + Fe 3 C. Продукт эвтектоидного распада аустенита при 727 С. Концентрация углерода 0, 8 % масс. Структура чередующиеся пластинки феррита и цементита (рис. а). Расстояние между пластинками составляет 5 10 -7 -7 10 -7 м. Имеет перламутровый цвет. Σв=900 МПа, δ= 16%, НВ=2000 МПа Ледебурит - + Fe 3 C. Температура образования равна 1147 С при эвтектическом превращении. Концентрация углерода 4, 3 %. Структура – чередующиеся пластинки аустенита и цементита (рис. б). При температурах ниже 727 С аустенит в этой смеси изотермически трансформируется в перлит. Ледебурит такого состава называется низкотемпературным. НВ=6000 МПа a Структура: а) перлита; б) ледебурита б
Структурные составляющие системы железо-углерод: перлит, ледебурит Двухфазные механические смеси. Перлит - + Fe 3 C. Продукт эвтектоидного распада аустенита при 727 С. Концентрация углерода 0, 8 % масс. Структура чередующиеся пластинки феррита и цементита (рис. а). Расстояние между пластинками составляет 5 10 -7 -7 10 -7 м. Имеет перламутровый цвет. Σв=900 МПа, δ= 16%, НВ=2000 МПа Ледебурит - + Fe 3 C. Температура образования равна 1147 С при эвтектическом превращении. Концентрация углерода 4, 3 %. Структура – чередующиеся пластинки аустенита и цементита (рис. б). При температурах ниже 727 С аустенит в этой смеси изотермически трансформируется в перлит. Ледебурит такого состава называется низкотемпературным. НВ=6000 МПа a Структура: а) перлита; б) ледебурита б

![Таблица 1. Точки диаграммы Fе - Fе 3 С Обозначение точек Температура, °С [C], Таблица 1. Точки диаграммы Fе - Fе 3 С Обозначение точек Температура, °С [C],](https://present5.com/presentation/1/51156178_137133357.pdf-img/51156178_137133357.pdf-13.jpg) Таблица 1. Точки диаграммы Fе - Fе 3 С Обозначение точек Температура, °С [C], % масс A 1539 0, 00 D 1260 H Пояснение Обозначение точек Темпе -ратура, °С [C], % масс Пояснение температура плавления железа F 1147 6, 67 наибольшая концентрация углерода в эвтектическом цементите 6, 67 температура плавления цементита G 911 0, 00 полиморфное превращение 1499 0, 10 предельное содержание углерода в -феррите P 727 0, 02 предельное содержание угле -рода в феррите J 1499 0, 16 максимальное количество углерода в аустените ( ) S 727 0, 80 максимальное количество углерода в перлите B 1499 0, 50 концентрация углерода в жидкой фазе, находящейся в равновесии с -ферритом и аустенитом K 727 6, 67 наибольшая концентрация углерода в эвтектоидном цементите N 1392 0, 00 полиморфное превращение Q 25 0, 006 минимальное содержание углерода в феррите E 1147 2, 14 предельное содержание углерода в аустените C 1147 4, 31 максимальное количество углерода в ледебурите
Таблица 1. Точки диаграммы Fе - Fе 3 С Обозначение точек Температура, °С [C], % масс A 1539 0, 00 D 1260 H Пояснение Обозначение точек Темпе -ратура, °С [C], % масс Пояснение температура плавления железа F 1147 6, 67 наибольшая концентрация углерода в эвтектическом цементите 6, 67 температура плавления цементита G 911 0, 00 полиморфное превращение 1499 0, 10 предельное содержание углерода в -феррите P 727 0, 02 предельное содержание угле -рода в феррите J 1499 0, 16 максимальное количество углерода в аустените ( ) S 727 0, 80 максимальное количество углерода в перлите B 1499 0, 50 концентрация углерода в жидкой фазе, находящейся в равновесии с -ферритом и аустенитом K 727 6, 67 наибольшая концентрация углерода в эвтектоидном цементите N 1392 0, 00 полиморфное превращение Q 25 0, 006 минимальное содержание углерода в феррите E 1147 2, 14 предельное содержание углерода в аустените C 1147 4, 31 максимальное количество углерода в ледебурите
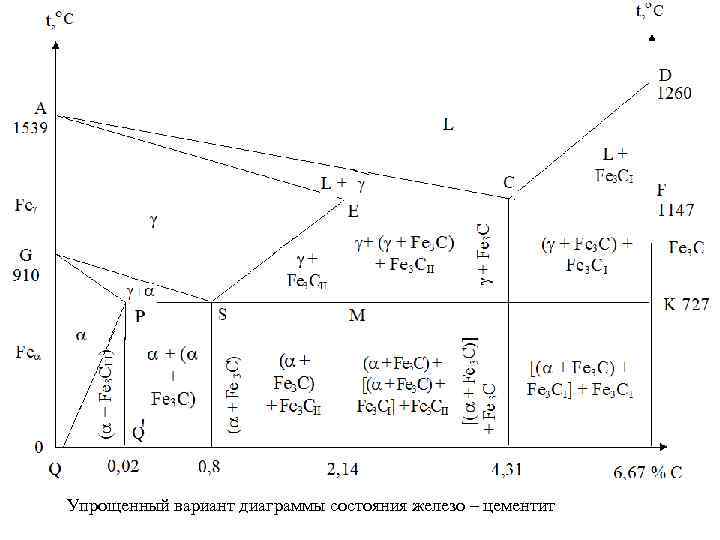 Упрощенный вариант диаграммы состояния железо – цементит
Упрощенный вариант диаграммы состояния железо – цементит
 Описание диаграммы • • • Кривая АСD - линия ликвидус, которая на участке АС соответствует температурам начала выпадения кристаллов аустенита ( ) из жидкого сплава (L), в области СD представляет геометрическое место точек, отвечающих температурам начала кристаллизации первичного цементита (Fe 3 СI) из жидкой фазы (L). Линия АЕСF - солидус, криволинейный кусочек АЕ которой определяет окончание затвердевания аустенита. Прямолинейный же участок ECF является геометрическим местом точек, соответствующих также концу кристаллизации аустенита (ЕС) и первичного цементита - Fe 3 CI (CF), и одновременно отвечает температурам изотермического превращения жидкого сплава состава пункта С в двухфазный эвтектоид - ледебурит – Lc Е + Fe 3 C. Данная реакция наблюдается только у сплавов с содержанием углерода более 2, 14 % масс. Кривые ограничения максимальной растворимости углерода в фазовых составляющих железоуглеродистых сплавов DC, ES и PQ расположены на диаграмме в интервалах трех уровней температур: 1 – от 1260 до 1147 С (DC), 2 – 1147 – 727 С (ES) и 3 – от 727 до 25 С (в некоторых источниках до 600 °С – PQ). Эти линии имеют одну общую особенность: по форме они обращены выпуклой стороной к оси температур чистого железа и определяют максимальную растворимость углерода в той фазе, которая расположена на диаграмме левее данной кривой. Это значит, что отвечающие им области DC, ES и PQ характеризуют предельную концентрацию неметалла: 1 в жидком сплаве L от 6, 67 % в точке D и 4, 31 % - пункт С; 2 в аустените от 2, 14 % точка Е до 0, 8 % для точки S; 3 в феррите - 0, 02 - 0, 006 % в пунктах Р и Q. При понижении температуры системы меньше точек растворимости углерода из фазы, находящейся слева от соответствующей им кривой, выделяется избыток неметалла, образуя цементит определенного уровня: 1 треугольник DCF – первичный (Fe 3 CI); 2 ESM – вторичный (Fe 3 CII) и 3 PQQ’ – третичный (Fe C ).
Описание диаграммы • • • Кривая АСD - линия ликвидус, которая на участке АС соответствует температурам начала выпадения кристаллов аустенита ( ) из жидкого сплава (L), в области СD представляет геометрическое место точек, отвечающих температурам начала кристаллизации первичного цементита (Fe 3 СI) из жидкой фазы (L). Линия АЕСF - солидус, криволинейный кусочек АЕ которой определяет окончание затвердевания аустенита. Прямолинейный же участок ECF является геометрическим местом точек, соответствующих также концу кристаллизации аустенита (ЕС) и первичного цементита - Fe 3 CI (CF), и одновременно отвечает температурам изотермического превращения жидкого сплава состава пункта С в двухфазный эвтектоид - ледебурит – Lc Е + Fe 3 C. Данная реакция наблюдается только у сплавов с содержанием углерода более 2, 14 % масс. Кривые ограничения максимальной растворимости углерода в фазовых составляющих железоуглеродистых сплавов DC, ES и PQ расположены на диаграмме в интервалах трех уровней температур: 1 – от 1260 до 1147 С (DC), 2 – 1147 – 727 С (ES) и 3 – от 727 до 25 С (в некоторых источниках до 600 °С – PQ). Эти линии имеют одну общую особенность: по форме они обращены выпуклой стороной к оси температур чистого железа и определяют максимальную растворимость углерода в той фазе, которая расположена на диаграмме левее данной кривой. Это значит, что отвечающие им области DC, ES и PQ характеризуют предельную концентрацию неметалла: 1 в жидком сплаве L от 6, 67 % в точке D и 4, 31 % - пункт С; 2 в аустените от 2, 14 % точка Е до 0, 8 % для точки S; 3 в феррите - 0, 02 - 0, 006 % в пунктах Р и Q. При понижении температуры системы меньше точек растворимости углерода из фазы, находящейся слева от соответствующей им кривой, выделяется избыток неметалла, образуя цементит определенного уровня: 1 треугольник DCF – первичный (Fe 3 CI); 2 ESM – вторичный (Fe 3 CII) и 3 PQQ’ – третичный (Fe C ).
 • • Описание диаграммы Отрезки ЕС и SP ограничивают соответственно изотермическое превращение жидкого сплава в ледебурит и аустенита в перлит Диаграмму состояния Fе - Fе 3 С по оси абсцисс – концентрация углерода – делят на следующие участки: 0 - 0, 02 % (точка Р); 0, 02 - 0, 80 % (область PS); 0, 80 % (точка S); 0, 80 - 2, 14 % (интервал SM); 2, 14 % (пункт Е); 2, 14 - 4, 31 % (диапазон EC); 4, 31 % (точка С) и 4, 31 - 6, 67 % (отрезок CF). Сплавы соответственно такому делению называют: 1 технически чистое железо; 2 доэвтектоидные; 3 эвтектоидная; 4 заэвтектоидные стали; 6 доэвтектические; 7 эвтектический и 8 заэвтектические чугуны. Железоуглеродистые сплавы с содержанием углерода до 2, 14 %, называют сталями. Они после затвердевания не содержат хрупкой структурной составляющей ледебурита и при высоком нагреве имеют только аустенитную структуру, обладающую высокой пластичностью. Поэтому они легко деформируются при нормальных и повышенных температурах, т. e. являются ковкими сплавами. Сталь – основной металлический конструкционный материал, широко применяемый для инженерных сооружений, изготовления оборудования, машин, приборов и инструментов. Ее обширное использование обусловлено удачным сочетанием ценного комплекса механических, физико-химических и технологических свойств. Кроме того, она сравнительно недорогая и может производиться в любом количестве.
• • Описание диаграммы Отрезки ЕС и SP ограничивают соответственно изотермическое превращение жидкого сплава в ледебурит и аустенита в перлит Диаграмму состояния Fе - Fе 3 С по оси абсцисс – концентрация углерода – делят на следующие участки: 0 - 0, 02 % (точка Р); 0, 02 - 0, 80 % (область PS); 0, 80 % (точка S); 0, 80 - 2, 14 % (интервал SM); 2, 14 % (пункт Е); 2, 14 - 4, 31 % (диапазон EC); 4, 31 % (точка С) и 4, 31 - 6, 67 % (отрезок CF). Сплавы соответственно такому делению называют: 1 технически чистое железо; 2 доэвтектоидные; 3 эвтектоидная; 4 заэвтектоидные стали; 6 доэвтектические; 7 эвтектический и 8 заэвтектические чугуны. Железоуглеродистые сплавы с содержанием углерода до 2, 14 %, называют сталями. Они после затвердевания не содержат хрупкой структурной составляющей ледебурита и при высоком нагреве имеют только аустенитную структуру, обладающую высокой пластичностью. Поэтому они легко деформируются при нормальных и повышенных температурах, т. e. являются ковкими сплавами. Сталь – основной металлический конструкционный материал, широко применяемый для инженерных сооружений, изготовления оборудования, машин, приборов и инструментов. Ее обширное использование обусловлено удачным сочетанием ценного комплекса механических, физико-химических и технологических свойств. Кроме того, она сравнительно недорогая и может производиться в любом количестве.
 • • • Описание диаграммы Механические свойства углеродистой стали зависят от содержания в ней углерода. С увеличением количества углерода повышается концентрация цементита и уменьшается скопление феррита. Это вызывает усиление прочности и твердости и снижение пластичности сплава. Кроме углерода в сталях обязательно присутствуют различные примеси. Примесями называют химические элементы, перешедшие в состав сталей в процессе их производства как технологические добавки или как сопутствующие составляющие шихтовых материалов. Примеси бывают постоянными, скрытыми, случайными и специальными.
• • • Описание диаграммы Механические свойства углеродистой стали зависят от содержания в ней углерода. С увеличением количества углерода повышается концентрация цементита и уменьшается скопление феррита. Это вызывает усиление прочности и твердости и снижение пластичности сплава. Кроме углерода в сталях обязательно присутствуют различные примеси. Примесями называют химические элементы, перешедшие в состав сталей в процессе их производства как технологические добавки или как сопутствующие составляющие шихтовых материалов. Примеси бывают постоянными, скрытыми, случайными и специальными.
 • • Описание диаграммы К постоянным примесям относятся марганец, кремний, фосфор и сера. Марганец способствует уменьшению содержания сульфида железа в сплаве. Сера вредная примесь - попадает в сталь главным образом с исходным сырьем. Она повышает хрупкость материала (красноломкости). Красноломкость наступает при горячей деформации стали вследствие расплавления сульфида железа в -железе (988 С), расположенного по границам зерен. От этого сплав предохраняет марганец, который связывает серу в соответствующий тугоплавкий сульфид (Тпл = 1620 С). Содержание серы допускается не более 0, 06 %. Фосфор также является нежелательной добавкой, так как снижает пластичность сплава. Хрупкость стали, вызванная фосфором, тем выше, чем больше в ней содержится углерода. Поэтому его количество в сплавах не должно превышать 0, 05 %. Скрытые примеси составляют присутствующие в сталях газы. Это азот, кислород и водород. Свое название они получили из-за сложности определения их количества в сплавах. Они очень сильно снижают ее пластичность. Содержание их допускается лишь до 10 -2 - 10 -4 %. Кислород вызывает красно- и хладноломкость и снижает прочность. Азот в виде нитридов железа, вызывающих деформационное старение. В холоднодеформированном сплаве атомы азота накапливаются на дислокациях и блокируют их. Сталь теряет свою пластичность. Положительное влияние азота – связывание его в прочные нитриды легирующих металлов, таких как Al. N, VN, Nb. N и т. д.
• • Описание диаграммы К постоянным примесям относятся марганец, кремний, фосфор и сера. Марганец способствует уменьшению содержания сульфида железа в сплаве. Сера вредная примесь - попадает в сталь главным образом с исходным сырьем. Она повышает хрупкость материала (красноломкости). Красноломкость наступает при горячей деформации стали вследствие расплавления сульфида железа в -железе (988 С), расположенного по границам зерен. От этого сплав предохраняет марганец, который связывает серу в соответствующий тугоплавкий сульфид (Тпл = 1620 С). Содержание серы допускается не более 0, 06 %. Фосфор также является нежелательной добавкой, так как снижает пластичность сплава. Хрупкость стали, вызванная фосфором, тем выше, чем больше в ней содержится углерода. Поэтому его количество в сплавах не должно превышать 0, 05 %. Скрытые примеси составляют присутствующие в сталях газы. Это азот, кислород и водород. Свое название они получили из-за сложности определения их количества в сплавах. Они очень сильно снижают ее пластичность. Содержание их допускается лишь до 10 -2 - 10 -4 %. Кислород вызывает красно- и хладноломкость и снижает прочность. Азот в виде нитридов железа, вызывающих деформационное старение. В холоднодеформированном сплаве атомы азота накапливаются на дислокациях и блокируют их. Сталь теряет свою пластичность. Положительное влияние азота – связывание его в прочные нитриды легирующих металлов, таких как Al. N, VN, Nb. N и т. д.
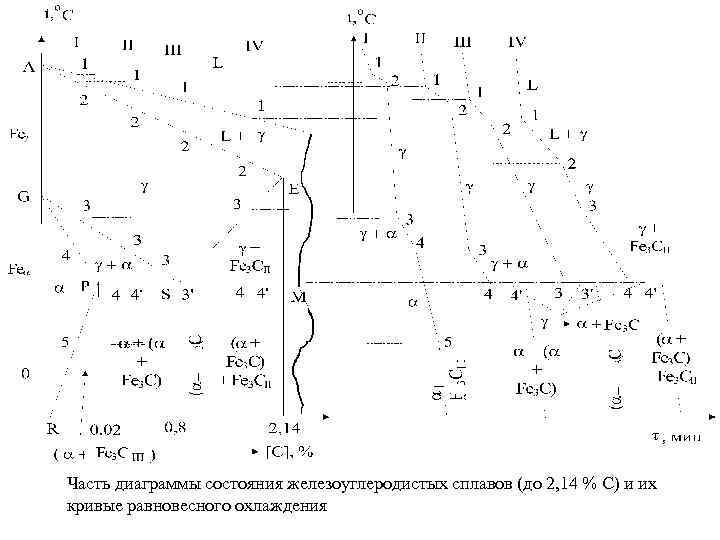 Часть диаграммы состояния железоуглеродистых сплавов (до 2, 14 % С) и их кривые равновесного охлаждения
Часть диаграммы состояния железоуглеродистых сплавов (до 2, 14 % С) и их кривые равновесного охлаждения
 Структура сталей с различной концентрацией углерода: а – 0, 05; б – 0, 25; в – 0, 40; г – 0, 70; д – 0, 80; е – 1, 20 %
Структура сталей с различной концентрацией углерода: а – 0, 05; б – 0, 25; в – 0, 40; г – 0, 70; д – 0, 80; е – 1, 20 %
 Фрагмент диаграммы состояния железо-цементит (2, 14 - 6, 67 % С) с соответствующими кривыми охлаждения
Фрагмент диаграммы состояния железо-цементит (2, 14 - 6, 67 % С) с соответствующими кривыми охлаждения
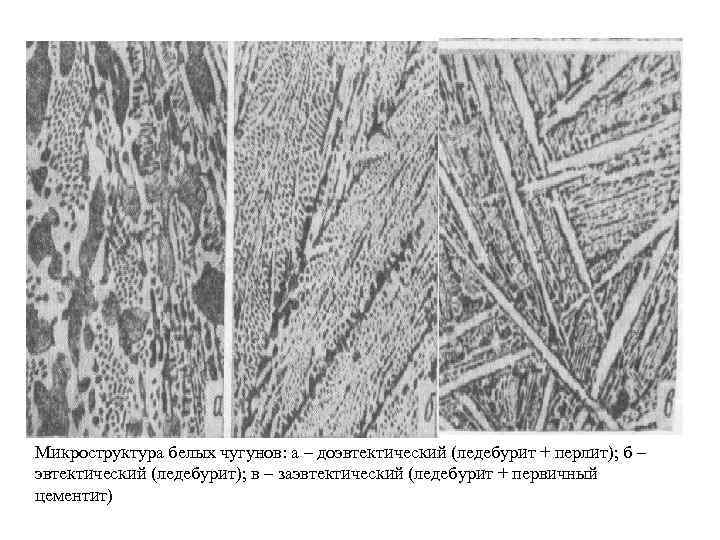 Микроструктура белых чугунов: а – доэвтектический (ледебурит + перлит); б – эвтектический (ледебурит); в – заэвтектический (ледебурит + первичный цементит)
Микроструктура белых чугунов: а – доэвтектический (ледебурит + перлит); б – эвтектический (ледебурит); в – заэвтектический (ледебурит + первичный цементит)


