Семинар2-2012.ppt
- Количество слайдов: 28
 Материаловедение Семинар 2. Методики решения задач на растворы “Только из союза двоих, работающих вместе и при помощи друга, рождаются великие вещи. ” Антуан Де Сент-Экзюпери
Материаловедение Семинар 2. Методики решения задач на растворы “Только из союза двоих, работающих вместе и при помощи друга, рождаются великие вещи. ” Антуан Де Сент-Экзюпери
 Приготовление растворов § Очень часто в практике салонов красоты приходится встречаться со случаями приготовления растворов с определенной массовой долей растворенного вещества, смешением двух растворов разной концентрации или разбавлением коцентрированоого раствора водой. 2 16. 02. 2018
Приготовление растворов § Очень часто в практике салонов красоты приходится встречаться со случаями приготовления растворов с определенной массовой долей растворенного вещества, смешением двух растворов разной концентрации или разбавлением коцентрированоого раствора водой. 2 16. 02. 2018
 Смешение растворов Существует несколько способов смешения растворов: § с помощью расчетной формулы, § “Правила смешения”, § “Правила креста”, § графического метода, § алгебраического метода. 3 16. 02. 2018
Смешение растворов Существует несколько способов смешения растворов: § с помощью расчетной формулы, § “Правила смешения”, § “Правила креста”, § графического метода, § алгебраического метода. 3 16. 02. 2018
 Основные компоненты растворов а) массовая доля растворенного вещества в растворе; § б) масса растворенного вещества в растворе; § в) масса раствора. 4 16. 02. 2018
Основные компоненты растворов а) массовая доля растворенного вещества в растворе; § б) масса растворенного вещества в растворе; § в) масса раствора. 4 16. 02. 2018
 Массовая доля растворенного вещества в растворе (ω) - это отношение массы этого вещества к массе раствора: § ω - массовая доля растворенного вещества в растворе; § m(в-ва) - масса растворенного вещества в растворе; 5 § m(р-ра) - масса раствора 16. 02. 2018
Массовая доля растворенного вещества в растворе (ω) - это отношение массы этого вещества к массе раствора: § ω - массовая доля растворенного вещества в растворе; § m(в-ва) - масса растворенного вещества в растворе; 5 § m(р-ра) - масса раствора 16. 02. 2018
 Массовая доля из формулы (1) можно получить следующие формулы 6 16. 02. 2018
Массовая доля из формулы (1) можно получить следующие формулы 6 16. 02. 2018
 Обозначения § ω1 - массовая доля растворенного вещества в первом растворе; § ω2 - массовая доля растворенного вещества во втором растворе; § ω - массовая доля растворенного вещества в новом растворе, полученном при смешивании первого и второго растворов; 7 16. 02. 2018
Обозначения § ω1 - массовая доля растворенного вещества в первом растворе; § ω2 - массовая доля растворенного вещества во втором растворе; § ω - массовая доля растворенного вещества в новом растворе, полученном при смешивании первого и второго растворов; 7 16. 02. 2018
 Обозначения § m 1(в-ва), m 2(в-ва), m(в-ва) массы растворенных веществ в соответствующих растворах; § m 1(р-ра), m 2(р-ра), m(р-ра) массы соответствующих растворов 8 16. 02. 2018
Обозначения § m 1(в-ва), m 2(в-ва), m(в-ва) массы растворенных веществ в соответствующих растворах; § m 1(р-ра), m 2(р-ра), m(р-ра) массы соответствующих растворов 8 16. 02. 2018
 С помощью расчётной формулы Формула для вычисления массовой доли вещества в смеси: 1. Масса полученного при смешивании раствора равна: § m(р-ра) = m 1(р-ра) + m 2(р-ра). 2. Определим массы растворенных веществ в первом и втором растворах: § m 1(в-ва)= ω1 • m 1(р-ра), § m 2(в-ва)= ω2 • m 2(р-ра). 9 16. 02. 2018
С помощью расчётной формулы Формула для вычисления массовой доли вещества в смеси: 1. Масса полученного при смешивании раствора равна: § m(р-ра) = m 1(р-ра) + m 2(р-ра). 2. Определим массы растворенных веществ в первом и втором растворах: § m 1(в-ва)= ω1 • m 1(р-ра), § m 2(в-ва)= ω2 • m 2(р-ра). 9 16. 02. 2018
 С помощью расчётной формулы 3. масса растворенного вещества вычисляется как сумма масс веществ в исходных растворах: § m(в-ва) = m 1(в-ва) + m 2(в-ва) = ω1 • m 1(р -ра) + ω2 • m 2(р-ра). 4. массовая доля растворенного вещества в полученном растворе равна: ω= m(в-ва) / m(р-ра) 10 16. 02. 2018
С помощью расчётной формулы 3. масса растворенного вещества вычисляется как сумма масс веществ в исходных растворах: § m(в-ва) = m 1(в-ва) + m 2(в-ва) = ω1 • m 1(р -ра) + ω2 • m 2(р-ра). 4. массовая доля растворенного вещества в полученном растворе равна: ω= m(в-ва) / m(р-ра) 10 16. 02. 2018
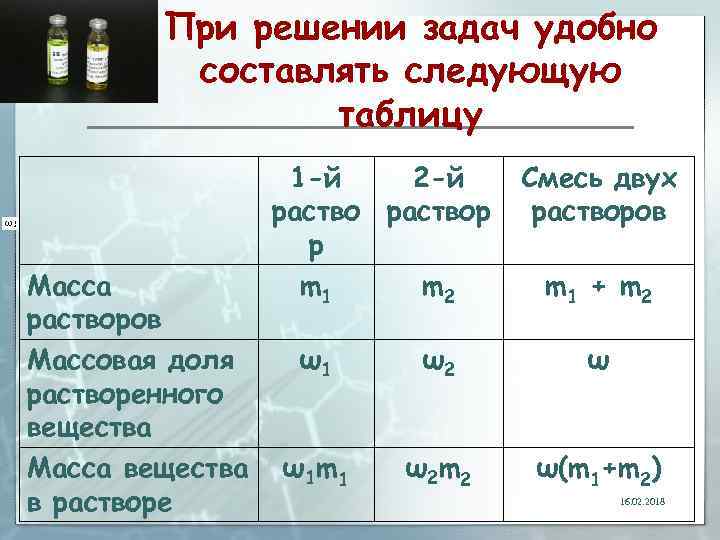 При решении задач удобно составлять следующую таблицу Масса растворов Массовая доля растворенного вещества Масса вещества 11 в растворе 1 -й 2 -й раствор р m 1 m 2 Смесь двух растворов m 1 + m 2 ω1 ω2 ω ω1 m 1 ω2 m 2 ω(m 1+m 2) 16. 02. 2018
При решении задач удобно составлять следующую таблицу Масса растворов Массовая доля растворенного вещества Масса вещества 11 в растворе 1 -й 2 -й раствор р m 1 m 2 Смесь двух растворов m 1 + m 2 ω1 ω2 ω ω1 m 1 ω2 m 2 ω(m 1+m 2) 16. 02. 2018
 “Правило смешения” отношение массы первого раствора к массе второго равно отношению разности массовых долей смеси и второго раствора к разности массовых долей первого раствора и смеси Формула удобна тем, что на практике, как правило, массы веществ не отвешиваются, а берутся в определенном отношении 12 16. 02. 2018
“Правило смешения” отношение массы первого раствора к массе второго равно отношению разности массовых долей смеси и второго раствора к разности массовых долей первого раствора и смеси Формула удобна тем, что на практике, как правило, массы веществ не отвешиваются, а берутся в определенном отношении 12 16. 02. 2018
 “Правило креста” “Правилом креста” называют диагональную схему правила смешения для случаев с двумя растворами: Получаемые массовые части показывают в каком отношении надо слить исходные растворы 13 16. 02. 2018
“Правило креста” “Правилом креста” называют диагональную схему правила смешения для случаев с двумя растворами: Получаемые массовые части показывают в каком отношении надо слить исходные растворы 13 16. 02. 2018
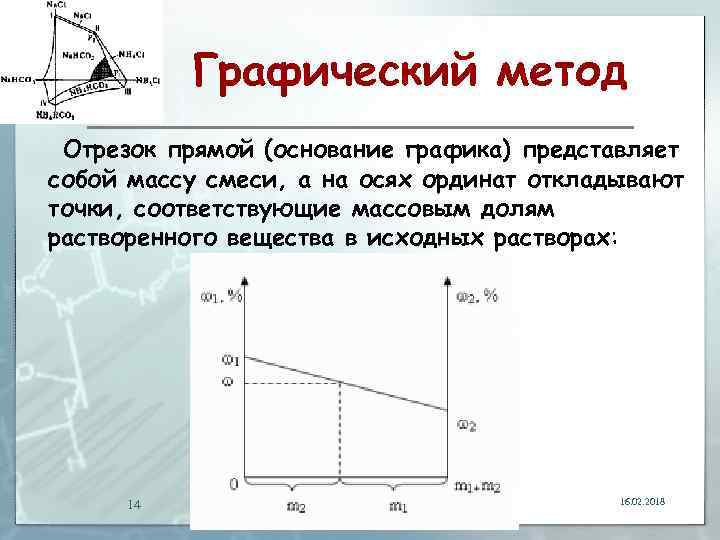 Графический метод Отрезок прямой (основание графика) представляет собой массу смеси, а на осях ординат откладывают точки, соответствующие массовым долям растворенного вещества в исходных растворах: 14 16. 02. 2018
Графический метод Отрезок прямой (основание графика) представляет собой массу смеси, а на осях ординат откладывают точки, соответствующие массовым долям растворенного вещества в исходных растворах: 14 16. 02. 2018
 Графический метод Соединив прямой точки на осях ординат, получают прямую, которая отображает функциональную зависимость массовой доли растворенного вещества в смеси от массы смешанных растворов в обратной пропорциональной зависимости : 15 16. 02. 2018
Графический метод Соединив прямой точки на осях ординат, получают прямую, которая отображает функциональную зависимость массовой доли растворенного вещества в смеси от массы смешанных растворов в обратной пропорциональной зависимости : 15 16. 02. 2018
 Алгебраический метод § смешивание растворов решают с помощью составления уравнения или системы уравнений 16 16. 02. 2018
Алгебраический метод § смешивание растворов решают с помощью составления уравнения или системы уравнений 16 16. 02. 2018
 Примеры решения задач: § В 100 г 20%-ного раствора соли добавили 300 г её 10%-ного раствора. § Определите процентную концентрацию раствора 17 16. 02. 2018
Примеры решения задач: § В 100 г 20%-ного раствора соли добавили 300 г её 10%-ного раствора. § Определите процентную концентрацию раствора 17 16. 02. 2018
 Решение с помощью расчетной формулы: 18 16. 02. 2018
Решение с помощью расчетной формулы: 18 16. 02. 2018
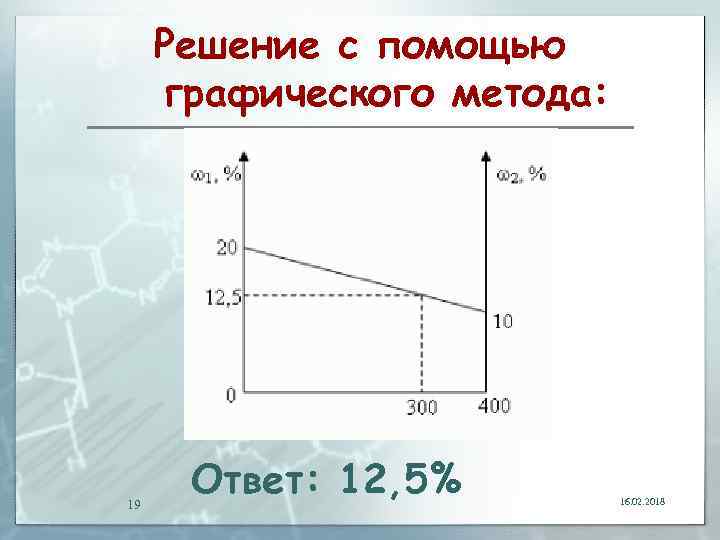 Решение с помощью графического метода: 19 Ответ: 12, 5% 16. 02. 2018
Решение с помощью графического метода: 19 Ответ: 12, 5% 16. 02. 2018
 Решение путем последовательных вычислений: 1. Сколько растворенного вещества содержится: а) в 100 г 20%-ного раствора; [100 • 0, 2 = 20(г)] б) в 300 г 10%-ного раствора? [300 • 0, 1 = 30(г)] 2. Сколько вещества содержится в образовавшемся растворе? 20 г + 30 г = 50 г 3. Чему равна масса образовавшегося раствора? 100 г + 300 г = 400 г 4. Какова процентная концентрация полученного раствора? (50/400)100 = 12, 5(%) Ответ: 12, 5% 20 16. 02. 2018
Решение путем последовательных вычислений: 1. Сколько растворенного вещества содержится: а) в 100 г 20%-ного раствора; [100 • 0, 2 = 20(г)] б) в 300 г 10%-ного раствора? [300 • 0, 1 = 30(г)] 2. Сколько вещества содержится в образовавшемся растворе? 20 г + 30 г = 50 г 3. Чему равна масса образовавшегося раствора? 100 г + 300 г = 400 г 4. Какова процентная концентрация полученного раствора? (50/400)100 = 12, 5(%) Ответ: 12, 5% 20 16. 02. 2018
 Решение с помощью алгебраического метода: Пусть х - процентная концентрация полученного раствора. В первом растворе содержится 0, 2 • 100(г) соли, а во втором 0, 1 • 300(г), а в полученном х • (100 + 300)(г) соли. Составим уравнение: 0, 2 • 100 + 0, 1 • 300 = х • (100 + 300); х = 0, 125 (12, 5%) Ответ: 12, 5% 21 16. 02. 2018
Решение с помощью алгебраического метода: Пусть х - процентная концентрация полученного раствора. В первом растворе содержится 0, 2 • 100(г) соли, а во втором 0, 1 • 300(г), а в полученном х • (100 + 300)(г) соли. Составим уравнение: 0, 2 • 100 + 0, 1 • 300 = х • (100 + 300); х = 0, 125 (12, 5%) Ответ: 12, 5% 21 16. 02. 2018
 1. Решите следующую задачу: Определите концентрацию раствора, полученного при слиянии 150 г 30%-го и 250 г 10%-го растворов перекиси: § Методом пропорций § Алгебраическим способом § Правилом креста Дано: m 1 = 150 г, m 2 = 250 г, ω1 = 30%, ω2 = 10%. Найти: ω3 22 16. 02. 2018
1. Решите следующую задачу: Определите концентрацию раствора, полученного при слиянии 150 г 30%-го и 250 г 10%-го растворов перекиси: § Методом пропорций § Алгебраическим способом § Правилом креста Дано: m 1 = 150 г, m 2 = 250 г, ω1 = 30%, ω2 = 10%. Найти: ω3 22 16. 02. 2018
 2. Решите следующую задачу правилом креста: Определите, сколько нужно взять 10% -го раствора соли и 30%-го раствора этой же соли для приготовления 500 г 20%-го раствора: Дано: ω1 = 10%, ω2 = 30%, ω3 = 20%, m 3 = 500 г. Найти: m 1, m 2 23 16. 02. 2018
2. Решите следующую задачу правилом креста: Определите, сколько нужно взять 10% -го раствора соли и 30%-го раствора этой же соли для приготовления 500 г 20%-го раствора: Дано: ω1 = 10%, ω2 = 30%, ω3 = 20%, m 3 = 500 г. Найти: m 1, m 2 23 16. 02. 2018
 3. Решите следующую задачу правилом креста: Определите, сколько нужно взять растворов соли 60%-й и 10%-й концентраций для приготовления 300 г раствора 25%-й концентрации : Дано: ω1 = 60%, ω2 = 10%, ω3 = 25%, m 3 = 300 г. Найти: m 1, m 2 24 16. 02. 2018
3. Решите следующую задачу правилом креста: Определите, сколько нужно взять растворов соли 60%-й и 10%-й концентраций для приготовления 300 г раствора 25%-й концентрации : Дано: ω1 = 60%, ω2 = 10%, ω3 = 25%, m 3 = 300 г. Найти: m 1, m 2 24 16. 02. 2018
 4. Решите следующую задачу алгебраическим способом и правилом креста: Определите массу раствора Nа 2 СО 3 10%-й концентрации и массу сухого кристаллогидрата Na 2 CO 3 • 10 H 2 O, которые нужно взять для приготовления 540 г раствора 15%-й концентрации: Дано: ω1 = 10%, ω3 = 15%, m 3 = 540 г. Найти: m 1, m 2 25 16. 02. 2018
4. Решите следующую задачу алгебраическим способом и правилом креста: Определите массу раствора Nа 2 СО 3 10%-й концентрации и массу сухого кристаллогидрата Na 2 CO 3 • 10 H 2 O, которые нужно взять для приготовления 540 г раствора 15%-й концентрации: Дано: ω1 = 10%, ω3 = 15%, m 3 = 540 г. Найти: m 1, m 2 25 16. 02. 2018
 5. Решите следующую задачу правилом креста: Сколько воды нужно добавить к 250 г раствора перекиси водорода для понижения концентрации с 45% до 10%? : Дано: ω1 = 45%, ω3 = 10%, m 1 = 250 г. Найти: m 2 26 16. 02. 2018
5. Решите следующую задачу правилом креста: Сколько воды нужно добавить к 250 г раствора перекиси водорода для понижения концентрации с 45% до 10%? : Дано: ω1 = 45%, ω3 = 10%, m 1 = 250 г. Найти: m 2 26 16. 02. 2018
 6. Решите следующую задачу правилом креста: Сколько сухой соли нужно добавить к 250 г раствора 10%-й концентрации для ее увеличения до 45%? Дано: ω1 = 10%, ω3 = 45%, m 1 = 250 г. Найти: m сухой соли 27 16. 02. 2018
6. Решите следующую задачу правилом креста: Сколько сухой соли нужно добавить к 250 г раствора 10%-й концентрации для ее увеличения до 45%? Дано: ω1 = 10%, ω3 = 45%, m 1 = 250 г. Найти: m сухой соли 27 16. 02. 2018
 Контрольная работа Сколько воды нужно добавить к раствору перекиси водорода для понижения концентрации (у каждого свой вариант)? : § Дано: § ω1 = § ω3 = § m 1 = Найти: m 2
Контрольная работа Сколько воды нужно добавить к раствору перекиси водорода для понижения концентрации (у каждого свой вариант)? : § Дано: § ω1 = § ω3 = § m 1 = Найти: m 2


