Материаловедение Лекция 1.ppt
- Количество слайдов: 37
 Материаловедение: неорганические материалы Лекция № 1 Ларионова Татьяна Васильевна к. т. н. , доцент кафедры Технология и исследование материалов, СПб. ГПУ
Материаловедение: неорганические материалы Лекция № 1 Ларионова Татьяна Васильевна к. т. н. , доцент кафедры Технология и исследование материалов, СПб. ГПУ
 ПЛАН ЛЕКЦИИ • Предмет материаловедение • Классификация материалов • Виды химической связи в материалах • Энергия межатомного взаимодействия • Кристаллическое строение • Дефекты кристаллического строения материалов • Колебания атомов в кристаллической решетке
ПЛАН ЛЕКЦИИ • Предмет материаловедение • Классификация материалов • Виды химической связи в материалах • Энергия межатомного взаимодействия • Кристаллическое строение • Дефекты кристаллического строения материалов • Колебания атомов в кристаллической решетке
 Обычно курс Материаловедение включает две части: металловедение и термическая обработка металлов и неметаллические материалы (полимеры, пластмассы, стекло и керамика). Таким образом, деление материалов на металлические и неметаллические составляет основу их классификации. Однако! Резкую границу между металлами и неметаллами в периодической системе Менделеева провести невозможно.
Обычно курс Материаловедение включает две части: металловедение и термическая обработка металлов и неметаллические материалы (полимеры, пластмассы, стекло и керамика). Таким образом, деление материалов на металлические и неметаллические составляет основу их классификации. Однако! Резкую границу между металлами и неметаллами в периодической системе Менделеева провести невозможно.
 Классификация материалов а) по проявляемым металлическим свойствам можно разделить на две большие группы - металлические материалы и неметаллы. К первой группе относятся металлы периодической системы и сплавы на их основе (например, Fe, Ni, Cu, Cr, Pb, Al, Au, W, Mo и др. ) и синтетические композиты на металлической основе. б) по внутреннему строению на кристаллические, аморфные и молекулярные или полимерные. В кристаллических материалах атомы или молекулы располагаются в пространстве в строго определенном порядке на дальнее расстояние. К ним относятся все металлы и их сплавы, а также кристаллические полимеры ( полиэтилен, полипропилен, полиамиды и др. ). Переход из жидкого состояния происходит при строго определенной температуре. в) по отраслевому признаку (назначению)-материалы машиностроительные, приборостроительные, электро- и радиотехнические, строительные; материалы авиационной, космической, медицинской, оптикоэлектронной техники , атомной энергетики и др.
Классификация материалов а) по проявляемым металлическим свойствам можно разделить на две большие группы - металлические материалы и неметаллы. К первой группе относятся металлы периодической системы и сплавы на их основе (например, Fe, Ni, Cu, Cr, Pb, Al, Au, W, Mo и др. ) и синтетические композиты на металлической основе. б) по внутреннему строению на кристаллические, аморфные и молекулярные или полимерные. В кристаллических материалах атомы или молекулы располагаются в пространстве в строго определенном порядке на дальнее расстояние. К ним относятся все металлы и их сплавы, а также кристаллические полимеры ( полиэтилен, полипропилен, полиамиды и др. ). Переход из жидкого состояния происходит при строго определенной температуре. в) по отраслевому признаку (назначению)-материалы машиностроительные, приборостроительные, электро- и радиотехнические, строительные; материалы авиационной, космической, медицинской, оптикоэлектронной техники , атомной энергетики и др.
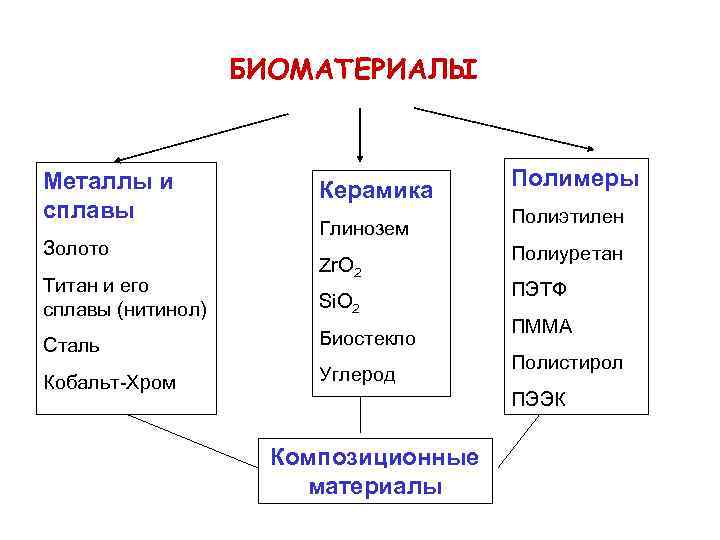 БИОМАТЕРИАЛЫ Металлы и сплавы Золото Титан и его сплавы (нитинол) Керамика Глинозем Zr. O 2 Si. O 2 Сталь Биостекло Кобальт-Хром Углерод Полимеры Полиэтилен Полиуретан ПЭТФ ПММА Полистирол ПЭЭК Композиционные материалы
БИОМАТЕРИАЛЫ Металлы и сплавы Золото Титан и его сплавы (нитинол) Керамика Глинозем Zr. O 2 Si. O 2 Сталь Биостекло Кобальт-Хром Углерод Полимеры Полиэтилен Полиуретан ПЭТФ ПММА Полистирол ПЭЭК Композиционные материалы
 Предмет материаловедение Материаловедением называется наука, устанавливающая связь между составом, структурой и свойствами материалов и изучающая закономерности их изменения при тепловых, химических, механических, электромагнитных и радиоактивных воздействиях. Правильный выбор материала для определенной детали изделия играет решающую роль в обеспечении надежной работы механизма или конструкции в целом в заданных условиях эксплуатации. Плохих материалов не бывает, а причиной ненадежной работы изделия, приводящей к преждевременному выходу из строя, снижению гарантийного срока службы является неправильный выбор материала применительно к конкретным условиям эксплуатации.
Предмет материаловедение Материаловедением называется наука, устанавливающая связь между составом, структурой и свойствами материалов и изучающая закономерности их изменения при тепловых, химических, механических, электромагнитных и радиоактивных воздействиях. Правильный выбор материала для определенной детали изделия играет решающую роль в обеспечении надежной работы механизма или конструкции в целом в заданных условиях эксплуатации. Плохих материалов не бывает, а причиной ненадежной работы изделия, приводящей к преждевременному выходу из строя, снижению гарантийного срока службы является неправильный выбор материала применительно к конкретным условиям эксплуатации.
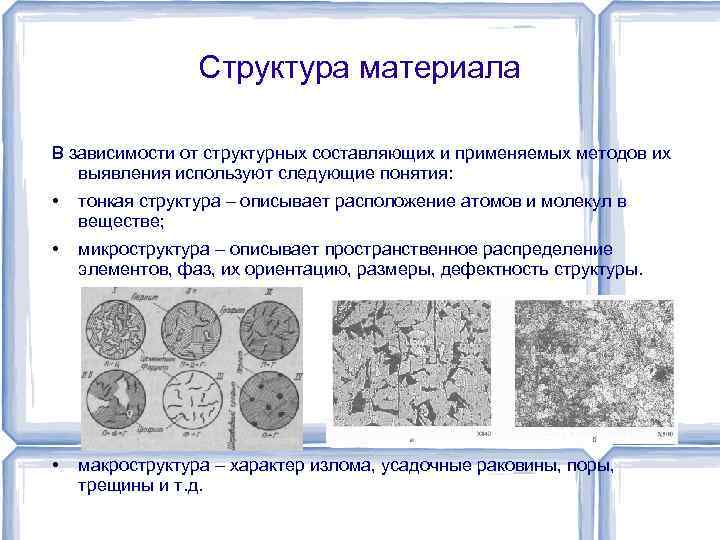 Структура материала В зависимости от структурных составляющих и применяемых методов их выявления используют следующие понятия: • тонкая структура – описывает расположение атомов и молекул в веществе; • микроструктура – описывает пространственное распределение элементов, фаз, их ориентацию, размеры, дефектность структуры. • макроструктура – характер излома, усадочные раковины, поры, трещины и т. д.
Структура материала В зависимости от структурных составляющих и применяемых методов их выявления используют следующие понятия: • тонкая структура – описывает расположение атомов и молекул в веществе; • микроструктура – описывает пространственное распределение элементов, фаз, их ориентацию, размеры, дефектность структуры. • макроструктура – характер излома, усадочные раковины, поры, трещины и т. д.
 Основные виды химических связей Ионная (гетерополярная) Процесс образования соединения из атомов с таким типом связи состоит из 2 -х этапов: (1) образование из нейтральных атомов положительных и отрицательных ионов; (2) притяжение разноименных ионов. Межатомное расстояние определяется уравновешиванием сил электростатического притяжения между катионами и анионами и отталкиванием их электронных оболочек. Ковалентная – за счет образования электронных пар Осуществляется парами электронов одновременно принадлежащим двум соседним атомам, причем каждый атом стремится иметь число соседей, определяемых количеством неспаренных электронов, отдавая для связи один из них. Этот вид связи в идеальном случае образуется между одинаковыми атомами и характеризуется наличием общих пар электронов. Металлическая - атомы отдают валентные электроны в общий “электронный газ” Металлическая связь – основной тип связи, реализующийся в металлах и сплавах. Характеризуется наличием в веществе свободных коллективизированных электронов (их количество соответствует валентности металла) – так называемого электронного «газа» . Отрицательно заряженный электронный газ удерживает положительно заряженные ионы металла на определенных расстояниях друг от друга. Полному сближению препятствуют силы отталкивания, действующие между электронными оболочками. Cвязь ненаправленная и ненасыщенная Молекулярная связь (Ван-дер-ваальсова). Взаимодействие электрически нейтральных молекул или атомов.
Основные виды химических связей Ионная (гетерополярная) Процесс образования соединения из атомов с таким типом связи состоит из 2 -х этапов: (1) образование из нейтральных атомов положительных и отрицательных ионов; (2) притяжение разноименных ионов. Межатомное расстояние определяется уравновешиванием сил электростатического притяжения между катионами и анионами и отталкиванием их электронных оболочек. Ковалентная – за счет образования электронных пар Осуществляется парами электронов одновременно принадлежащим двум соседним атомам, причем каждый атом стремится иметь число соседей, определяемых количеством неспаренных электронов, отдавая для связи один из них. Этот вид связи в идеальном случае образуется между одинаковыми атомами и характеризуется наличием общих пар электронов. Металлическая - атомы отдают валентные электроны в общий “электронный газ” Металлическая связь – основной тип связи, реализующийся в металлах и сплавах. Характеризуется наличием в веществе свободных коллективизированных электронов (их количество соответствует валентности металла) – так называемого электронного «газа» . Отрицательно заряженный электронный газ удерживает положительно заряженные ионы металла на определенных расстояниях друг от друга. Полному сближению препятствуют силы отталкивания, действующие между электронными оболочками. Cвязь ненаправленная и ненасыщенная Молекулярная связь (Ван-дер-ваальсова). Взаимодействие электрически нейтральных молекул или атомов.
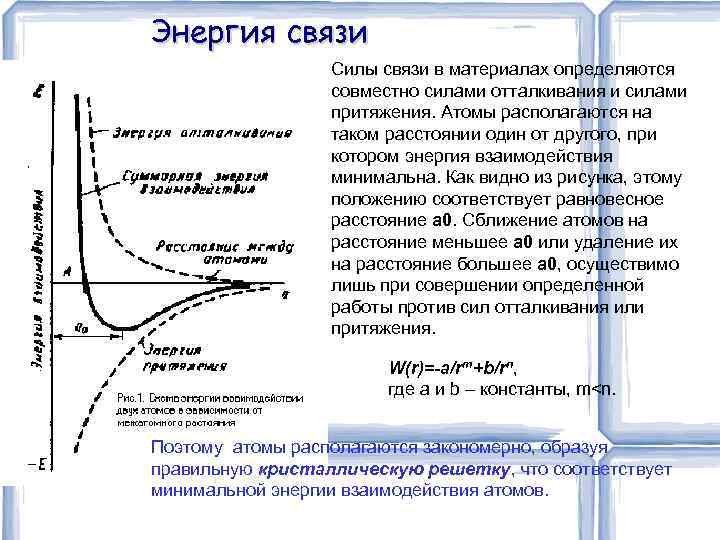 Энергия связи Силы связи в материалах определяются совместно силами отталкивания и силами притяжения. Атомы располагаются на таком расстоянии один от другого, при котором энергия взаимодействия минимальна. Как видно из рисунка, этому положению соответствует равновесное расстояние а 0. Сближение атомов на расстояние меньшее а 0 или удаление их на расстояние большее а 0, осуществимо лишь при совершении определенной работы против сил отталкивания или притяжения. W(r)=-a/rm+b/rn, где а и b – константы, m
Энергия связи Силы связи в материалах определяются совместно силами отталкивания и силами притяжения. Атомы располагаются на таком расстоянии один от другого, при котором энергия взаимодействия минимальна. Как видно из рисунка, этому положению соответствует равновесное расстояние а 0. Сближение атомов на расстояние меньшее а 0 или удаление их на расстояние большее а 0, осуществимо лишь при совершении определенной работы против сил отталкивания или притяжения. W(r)=-a/rm+b/rn, где а и b – константы, m
 Кристаллическое строение В кристалле частицы сближены до “соприкосновения” и располагаются различно, но закономерно по разным направлениям. Для упрощения пространственное изображение заменяют схемами. Для описания кристаллического строения было введено понятие кристаллической решетки – математической системы точек в пространстве. Каждая точка представляет атом или молекулу (в общем случае мотивную единицу). Кристаллическая решетка описывается элементарной ячейкой. Фактически это минимальный воображаемый объём кристалла, параллельные переносы – трансляции - которого в трёх измерениях позволяют построить трёхмерную кристаллическую решётку в целом.
Кристаллическое строение В кристалле частицы сближены до “соприкосновения” и располагаются различно, но закономерно по разным направлениям. Для упрощения пространственное изображение заменяют схемами. Для описания кристаллического строения было введено понятие кристаллической решетки – математической системы точек в пространстве. Каждая точка представляет атом или молекулу (в общем случае мотивную единицу). Кристаллическая решетка описывается элементарной ячейкой. Фактически это минимальный воображаемый объём кристалла, параллельные переносы – трансляции - которого в трёх измерениях позволяют построить трёхмерную кристаллическую решётку в целом.
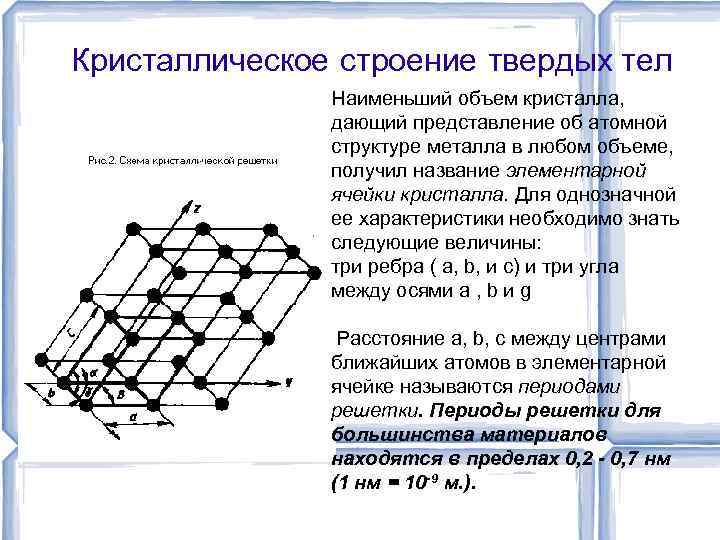 Кристаллическое строение твердых тел Наименьший объем кристалла, дающий представление об атомной структуре металла в любом объеме, получил название элементарной ячейки кристалла. Для однозначной ее характеристики необходимо знать следующие величины: три ребра ( a, b, и c) и три угла между осями a , b и g Расстояние a, b, c между центрами ближайших атомов в элементарной ячейке называются периодами решетки. Периоды решетки для большинства материалов находятся в пределах 0, 2 - 0, 7 нм (1 нм = 10 -9 м. ).
Кристаллическое строение твердых тел Наименьший объем кристалла, дающий представление об атомной структуре металла в любом объеме, получил название элементарной ячейки кристалла. Для однозначной ее характеристики необходимо знать следующие величины: три ребра ( a, b, и c) и три угла между осями a , b и g Расстояние a, b, c между центрами ближайших атомов в элементарной ячейке называются периодами решетки. Периоды решетки для большинства материалов находятся в пределах 0, 2 - 0, 7 нм (1 нм = 10 -9 м. ).
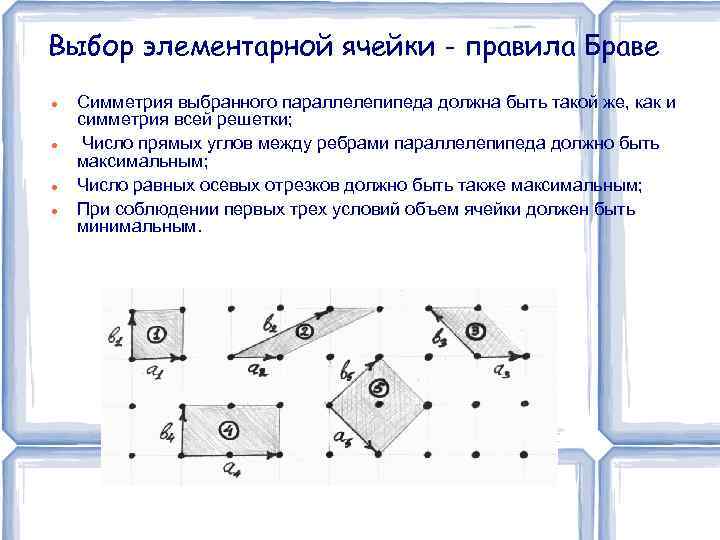 Выбор элементарной ячейки - правила Браве Симметрия выбранного параллелепипеда должна быть такой же, как и симметрия всей решетки; Число прямых углов между ребрами параллелепипеда должно быть максимальным; Число равных осевых отрезков должно быть также максимальным; При соблюдении первых трех условий объем ячейки должен быть минимальным.
Выбор элементарной ячейки - правила Браве Симметрия выбранного параллелепипеда должна быть такой же, как и симметрия всей решетки; Число прямых углов между ребрами параллелепипеда должно быть максимальным; Число равных осевых отрезков должно быть также максимальным; При соблюдении первых трех условий объем ячейки должен быть минимальным.
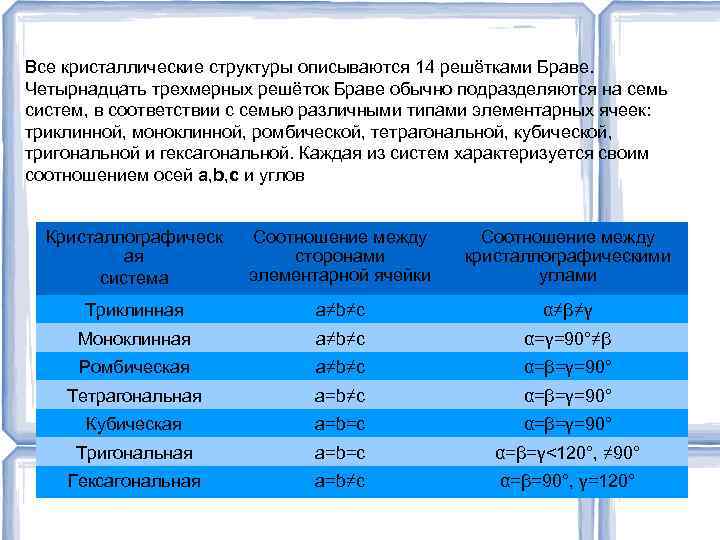 Все кристаллические структуры описываются 14 решётками Браве. Четырнадцать трехмерных решёток Браве обычно подразделяются на семь систем, в соответствии с семью различными типами элементарных ячеек: триклинной, моноклинной, ромбической, тетрагональной, кубической, тригональной и гексагональной. Каждая из систем характеризуется своим соотношением осей a, b, c и углов Кристаллографическ ая система Соотношение между сторонами элементарной ячейки Соотношение между кристаллографическими углами Триклинная а≠b≠с α≠β≠γ Моноклинная а≠b≠с α=γ=90°≠β Ромбическая а≠b≠с α=β=γ=90° Тетрагональная а=b≠с α=β=γ=90° Кубическая а=b=с α=β=γ=90° Тригональная а=b=с α=β=γ<120°, ≠ 90° Гексагональная а=b≠с α=β=90°, γ=120°
Все кристаллические структуры описываются 14 решётками Браве. Четырнадцать трехмерных решёток Браве обычно подразделяются на семь систем, в соответствии с семью различными типами элементарных ячеек: триклинной, моноклинной, ромбической, тетрагональной, кубической, тригональной и гексагональной. Каждая из систем характеризуется своим соотношением осей a, b, c и углов Кристаллографическ ая система Соотношение между сторонами элементарной ячейки Соотношение между кристаллографическими углами Триклинная а≠b≠с α≠β≠γ Моноклинная а≠b≠с α=γ=90°≠β Ромбическая а≠b≠с α=β=γ=90° Тетрагональная а=b≠с α=β=γ=90° Кубическая а=b=с α=β=γ=90° Тригональная а=b=с α=β=γ<120°, ≠ 90° Гексагональная а=b≠с α=β=90°, γ=120°
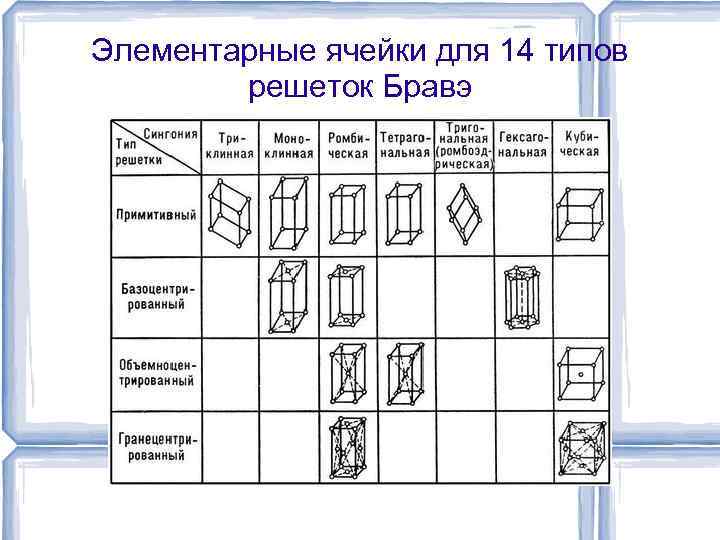 Элементарные ячейки для 14 типов решеток Бравэ
Элементарные ячейки для 14 типов решеток Бравэ
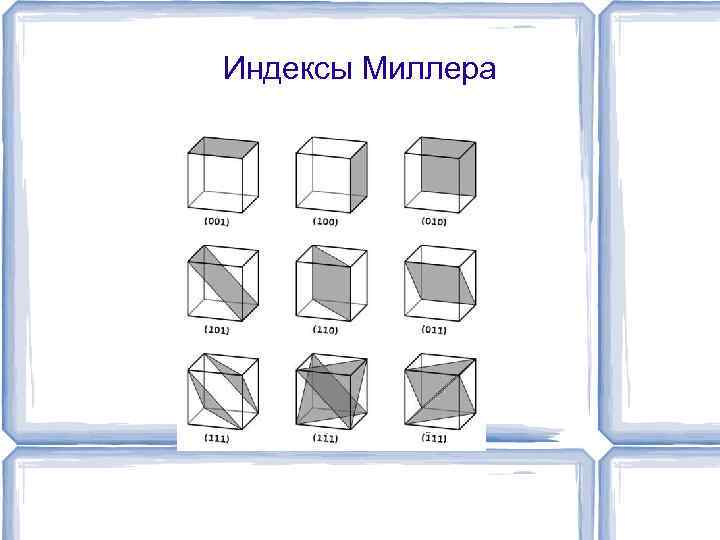
 Индексы Миллера — кристаллографические индексы, характеризующие расположение атомных плоскостей в кристалле. Индексы Миллера связаны с отрезками, отсекаемыми выбранной плоскостью на трёх осях кристаллографической системы координат (не обязательно декартовой). Индексы Миллера выглядят как три взаимно простых целых числа, записанные в круглых скобках: (111), (101), (110)…
Индексы Миллера — кристаллографические индексы, характеризующие расположение атомных плоскостей в кристалле. Индексы Миллера связаны с отрезками, отсекаемыми выбранной плоскостью на трёх осях кристаллографической системы координат (не обязательно декартовой). Индексы Миллера выглядят как три взаимно простых целых числа, записанные в круглых скобках: (111), (101), (110)…
 Индексы Миллера
Индексы Миллера
 Ионные кристаллы ются путем плотной упаковки ионов, заряженных разноименно. К числу ионных кристаллов относится большинство неорганических соединений, например соли. Каждый ион натрия окружен шестью ионами хлора, и, наоборот, каждый ион хлора окружен шестью ионами натрия. В кристалле нет молекул Nа. Сl. Аналогично образуется ионная химическая связь и в других случаях, чаще всего между металлами и галогенами — фтором и хлором.
Ионные кристаллы ются путем плотной упаковки ионов, заряженных разноименно. К числу ионных кристаллов относится большинство неорганических соединений, например соли. Каждый ион натрия окружен шестью ионами хлора, и, наоборот, каждый ион хлора окружен шестью ионами натрия. В кристалле нет молекул Nа. Сl. Аналогично образуется ионная химическая связь и в других случаях, чаще всего между металлами и галогенами — фтором и хлором.
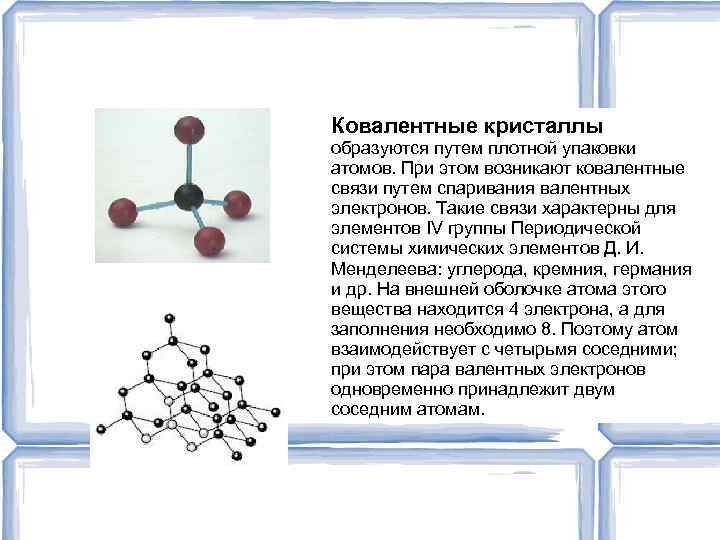 Ковалентные кристаллы образуются путем плотной упаковки атомов. При этом возникают ковалентные связи путем спаривания валентных электронов. Такие связи характерны для элементов IV группы Периодической системы химических элементов Д. И. Менделеева: углерода, кремния, германия и др. На внешней оболочке атома этого вещества находится 4 электрона, а для заполнения необходимо 8. Поэтому атом взаимодействует с четырьмя соседними; при этом пара валентных электронов одновременно принадлежит двум соседним атомам.
Ковалентные кристаллы образуются путем плотной упаковки атомов. При этом возникают ковалентные связи путем спаривания валентных электронов. Такие связи характерны для элементов IV группы Периодической системы химических элементов Д. И. Менделеева: углерода, кремния, германия и др. На внешней оболочке атома этого вещества находится 4 электрона, а для заполнения необходимо 8. Поэтому атом взаимодействует с четырьмя соседними; при этом пара валентных электронов одновременно принадлежит двум соседним атомам.
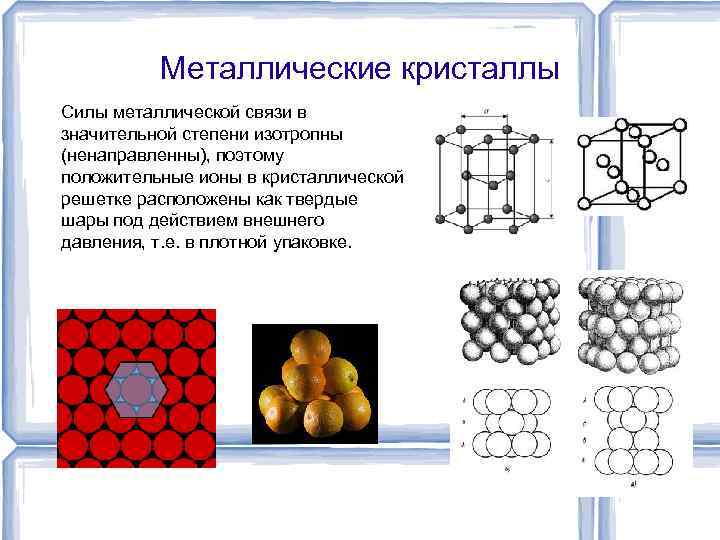 Металлические кристаллы Силы металлической связи в значительной степени изотропны (ненаправленны), поэтому положительные ионы в кристаллической решетке расположены как твердые шары под действием внешнего давления, т. е. в плотной упаковке.
Металлические кристаллы Силы металлической связи в значительной степени изотропны (ненаправленны), поэтому положительные ионы в кристаллической решетке расположены как твердые шары под действием внешнего давления, т. е. в плотной упаковке.
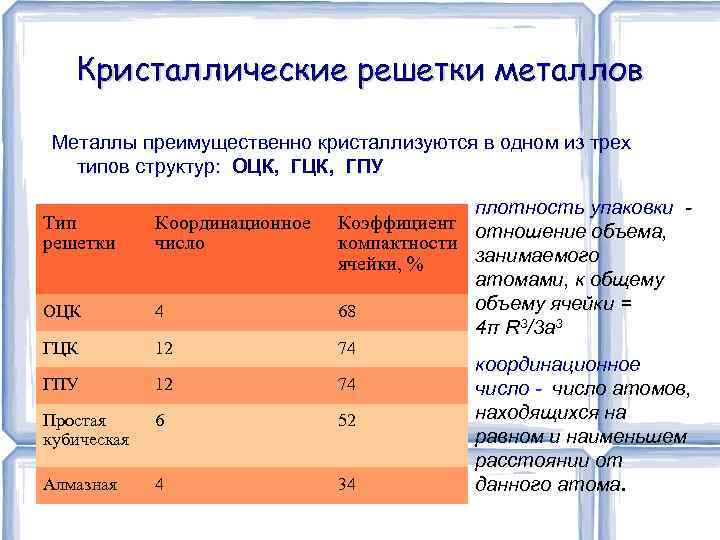 Кристаллические решетки металлов Металлы преимущественно кристаллизуются в одном из трех типов структур: ОЦК, ГПУ плотность упаковки Коэффициент отношение объема, компактности занимаемого ячейки, % атомами, к общему объему ячейки = 68 4π R 3/3 a 3 Тип решетки Координационное число ОЦК 4 ГЦК 12 ГПУ 12 74 Простая кубическая 6 52 Алмазная 4 34 74 координационное число - число атомов, находящихся на равном и наименьшем расстоянии от данного атома.
Кристаллические решетки металлов Металлы преимущественно кристаллизуются в одном из трех типов структур: ОЦК, ГПУ плотность упаковки Коэффициент отношение объема, компактности занимаемого ячейки, % атомами, к общему объему ячейки = 68 4π R 3/3 a 3 Тип решетки Координационное число ОЦК 4 ГЦК 12 ГПУ 12 74 Простая кубическая 6 52 Алмазная 4 34 74 координационное число - число атомов, находящихся на равном и наименьшем расстоянии от данного атома.
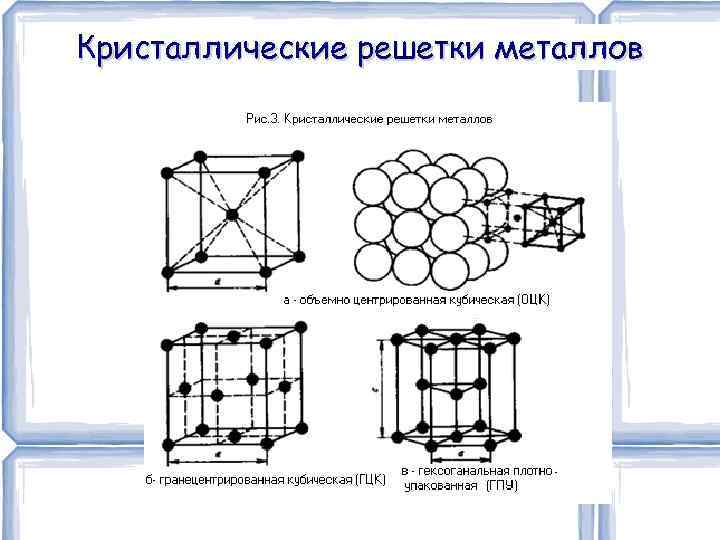 Кристаллические решетки металлов
Кристаллические решетки металлов
 Металлическое состояние вещества Металлическое состояние– это конденсированное состояние вещества, состоящего из положительных ионов и коллективизированных электронов в виде электронного газа. Именно эти коллективизированные электроны и определяют основные свойства металлического состояния вообще (ковкость, блеск, тепло и электропроводность и т. д. ). Таким образом, металлическое состояние вещества определяется действующими видами и природой связей между структурными частицами в твердом теле. Металлы в твердом (кристаллическом или аморфном) и отчасти в жидком состоянии обладают рядом характерных свойств: высокими теплопроводностью и электрической проводимостью; положительным температурным коэффициентом электрического сопротивления; с повышением температуры электрическое сопротивление чистых металлов возрастает; термоэлектронной эмиссией, т. е. способность испускать электроны при нагреве; повышенной способностью к пластической деформации. И др.
Металлическое состояние вещества Металлическое состояние– это конденсированное состояние вещества, состоящего из положительных ионов и коллективизированных электронов в виде электронного газа. Именно эти коллективизированные электроны и определяют основные свойства металлического состояния вообще (ковкость, блеск, тепло и электропроводность и т. д. ). Таким образом, металлическое состояние вещества определяется действующими видами и природой связей между структурными частицами в твердом теле. Металлы в твердом (кристаллическом или аморфном) и отчасти в жидком состоянии обладают рядом характерных свойств: высокими теплопроводностью и электрической проводимостью; положительным температурным коэффициентом электрического сопротивления; с повышением температуры электрическое сопротивление чистых металлов возрастает; термоэлектронной эмиссией, т. е. способность испускать электроны при нагреве; повышенной способностью к пластической деформации. И др.
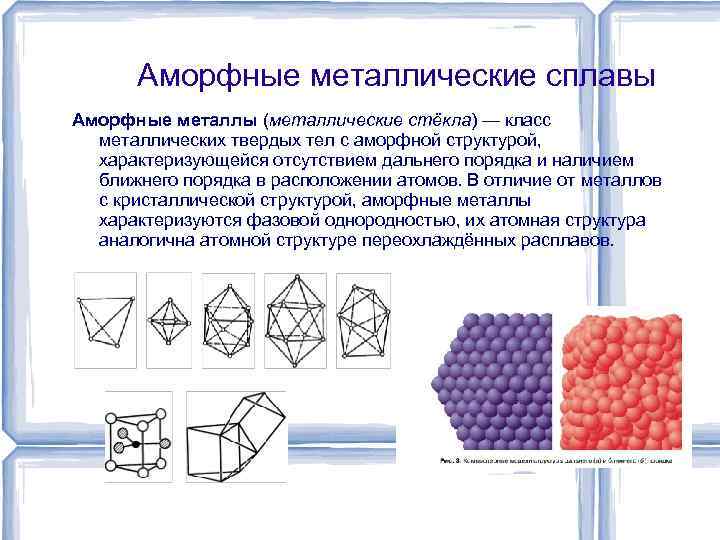 Аморфные металлические сплавы Аморфные металлы (металлические стёкла) — класс металлических твердых тел с аморфной структурой, характеризующейся отсутствием дальнего порядка и наличием ближнего порядка в расположении атомов. В отличие от металлов с кристаллической структурой, аморфные металлы характеризуются фазовой однородностью, их атомная структура аналогична атомной структуре переохлаждённых расплавов.
Аморфные металлические сплавы Аморфные металлы (металлические стёкла) — класс металлических твердых тел с аморфной структурой, характеризующейся отсутствием дальнего порядка и наличием ближнего порядка в расположении атомов. В отличие от металлов с кристаллической структурой, аморфные металлы характеризуются фазовой однородностью, их атомная структура аналогична атомной структуре переохлаждённых расплавов.
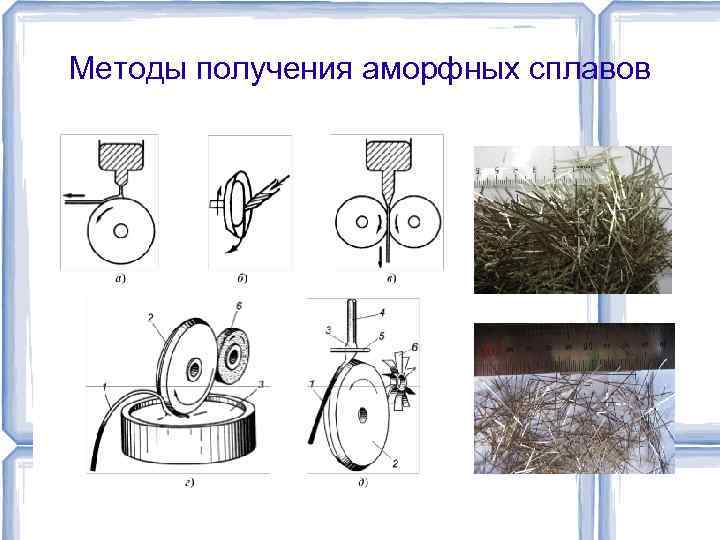 Методы получения аморфных сплавов
Методы получения аморфных сплавов
 Аморфные сплавы Недостатки Достоинства Высокая прочность и твердость Аморфный сплав Fe 69 Cr 6 Mo 6 B 28 Высокопрочн ые стали Высокая коррозионная 4500 МПа 1800 -2000 МПа стойкость Высокая магнитная проницаемость (80%) Малая толщина (< 50 мкм), обусловленная способом получения Низкая термическая стабильность как при повышенных так и при климатических температурах Нестабильность получения и высокая стоимость
Аморфные сплавы Недостатки Достоинства Высокая прочность и твердость Аморфный сплав Fe 69 Cr 6 Mo 6 B 28 Высокопрочн ые стали Высокая коррозионная 4500 МПа 1800 -2000 МПа стойкость Высокая магнитная проницаемость (80%) Малая толщина (< 50 мкм), обусловленная способом получения Низкая термическая стабильность как при повышенных так и при климатических температурах Нестабильность получения и высокая стоимость
 Колебания атомов в кристаллической решетке. 1. Тепловые Происходят при Т>0 К Энергия частиц в зависимости от температуры описывается статистическим распределением Максвелла, средняя энергия равна 3/2 к. Т, наиболее вероятная - к. Т При любой температуре, отличной от 0 К, существуют атомы (ионы) энергия которых превышает любую заданную. Следствия: (i) испарение любого вещества при любой температуре; (ii) диффузия; (iii) образование точечных дефектов.
Колебания атомов в кристаллической решетке. 1. Тепловые Происходят при Т>0 К Энергия частиц в зависимости от температуры описывается статистическим распределением Максвелла, средняя энергия равна 3/2 к. Т, наиболее вероятная - к. Т При любой температуре, отличной от 0 К, существуют атомы (ионы) энергия которых превышает любую заданную. Следствия: (i) испарение любого вещества при любой температуре; (ii) диффузия; (iii) образование точечных дефектов.
 Колебания атомов в кристаллической решетке. 2. Нулевые Происходят даже при Т=0 К Имеют квантово-механическую природу: x· p>h, следовательно, ни одна частица не может находиться в полном покое и при х 0 р будет стремиться к бесконечности. Е=( р)2/2 М следовательно увеличение импульса энергетически не выгодно. В твердом теле максимальное значение амплитуды нулевых колебании должно быть меньше чем расстояние между частицами (ионами) в решетке.
Колебания атомов в кристаллической решетке. 2. Нулевые Происходят даже при Т=0 К Имеют квантово-механическую природу: x· p>h, следовательно, ни одна частица не может находиться в полном покое и при х 0 р будет стремиться к бесконечности. Е=( р)2/2 М следовательно увеличение импульса энергетически не выгодно. В твердом теле максимальное значение амплитуды нулевых колебании должно быть меньше чем расстояние между частицами (ионами) в решетке.
 Дефекты кристаллического строения • Точечные • Линейные • Поверхностные (двумерные)
Дефекты кристаллического строения • Точечные • Линейные • Поверхностные (двумерные)
 Точечные дефекты 1) Вакансии – основной вид точечных дефектов 2) Дислоцированный атом (атом в междоузлии) 3) Атомы примесей: (i) замещения; (ii) внедрения. Важной особенностью точечных дефектов является то, что их образование является РАВНОВЕСНЫМ процессом.
Точечные дефекты 1) Вакансии – основной вид точечных дефектов 2) Дислоцированный атом (атом в междоузлии) 3) Атомы примесей: (i) замещения; (ii) внедрения. Важной особенностью точечных дефектов является то, что их образование является РАВНОВЕСНЫМ процессом.
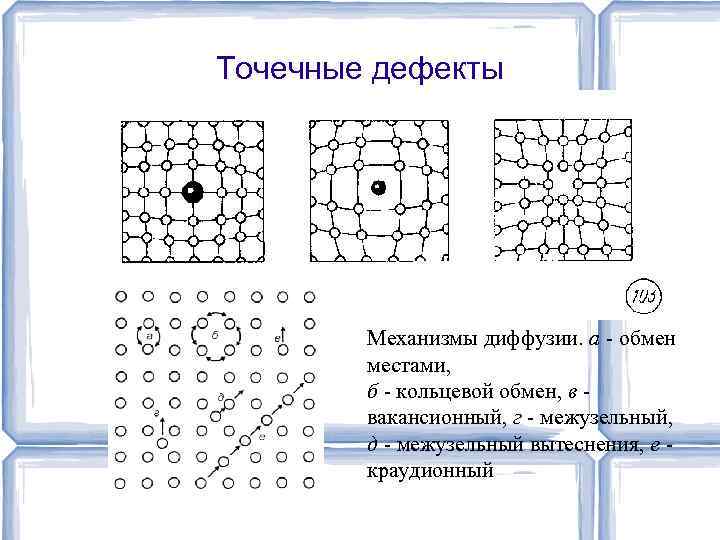 Точечные дефекты Механизмы диффузии. а ‑ обмен местами, б ‑ кольцевой обмен, в ‑ вакансионный, г ‑ межузельный, д ‑ межузельный вытеснения, е ‑ краудионный
Точечные дефекты Механизмы диффузии. а ‑ обмен местами, б ‑ кольцевой обмен, в ‑ вакансионный, г ‑ межузельный, д ‑ межузельный вытеснения, е ‑ краудионный
 Точечные дефекты При образовании точечных дефектов возрастает внутренняя энергия кристалла U, и увеличивается энтропия. При определенной, характерной для данной температуры, концентрации собственных точечных дефектов рост энтропийного члена TS перекрывает увеличение внутренней энергии системы U, и свободная энергия оказывается пониженной. Многие оценочные расчеты равновесной концентрации вакансий можно вести по упрощенной формуле: Cv = exp(-E 0/k. T). Т, К Равновесная концентрация вакансий Cv 300 10 -19 700 10 -8 1100 10 -5 1350 10 -4
Точечные дефекты При образовании точечных дефектов возрастает внутренняя энергия кристалла U, и увеличивается энтропия. При определенной, характерной для данной температуры, концентрации собственных точечных дефектов рост энтропийного члена TS перекрывает увеличение внутренней энергии системы U, и свободная энергия оказывается пониженной. Многие оценочные расчеты равновесной концентрации вакансий можно вести по упрощенной формуле: Cv = exp(-E 0/k. T). Т, К Равновесная концентрация вакансий Cv 300 10 -19 700 10 -8 1100 10 -5 1350 10 -4
 Линейные дефекты Линейные несовершенства имеют малые размеры в двух измерениях и имеют большую протяженность в третьем измерении. Этими несовершенствами могут быть ряд вакансий или ряд межузельных атомов. Особыми и важнейшими видами линейных несовершенств являются дислокации – краевые и винтовые. Краевые дислокации представляют собой локализованное искажение кристаллической решетки, вызываемое наличием в ней "лишние" атомной полуплоскости или экстраплоскости. Винтовая дислокация как и краевая, образована неполным сдвигом кристалла по плоскости Q. В отличие от краевой дислокации винтовая дислокация параллельна вектору сдвига. Дислокационные линии не обрываются внутри кристалла, они выходят на его поверхность, заканчиваются на других дислокациях или образуют замкнутые дислокационные петли.
Линейные дефекты Линейные несовершенства имеют малые размеры в двух измерениях и имеют большую протяженность в третьем измерении. Этими несовершенствами могут быть ряд вакансий или ряд межузельных атомов. Особыми и важнейшими видами линейных несовершенств являются дислокации – краевые и винтовые. Краевые дислокации представляют собой локализованное искажение кристаллической решетки, вызываемое наличием в ней "лишние" атомной полуплоскости или экстраплоскости. Винтовая дислокация как и краевая, образована неполным сдвигом кристалла по плоскости Q. В отличие от краевой дислокации винтовая дислокация параллельна вектору сдвига. Дислокационные линии не обрываются внутри кристалла, они выходят на его поверхность, заканчиваются на других дислокациях или образуют замкнутые дислокационные петли.
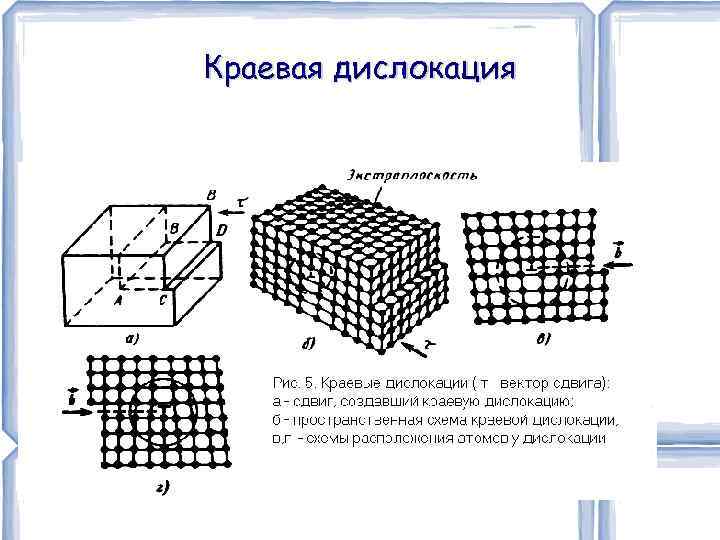 Краевая дислокация
Краевая дислокация
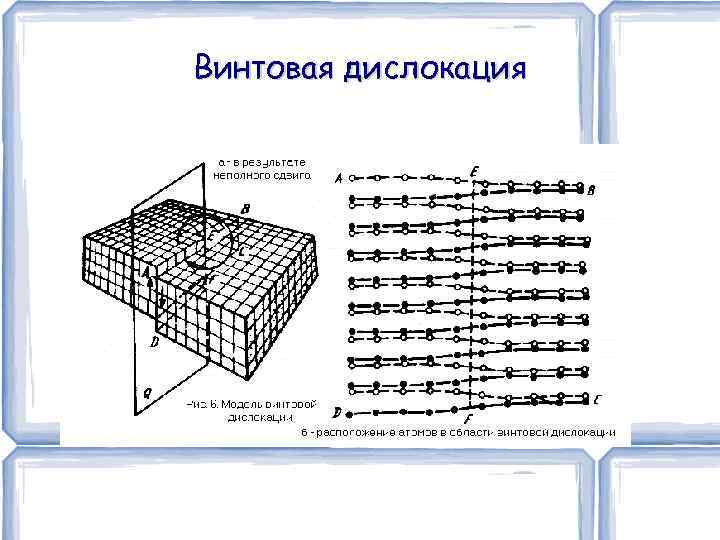 Винтовая дислокация
Винтовая дислокация
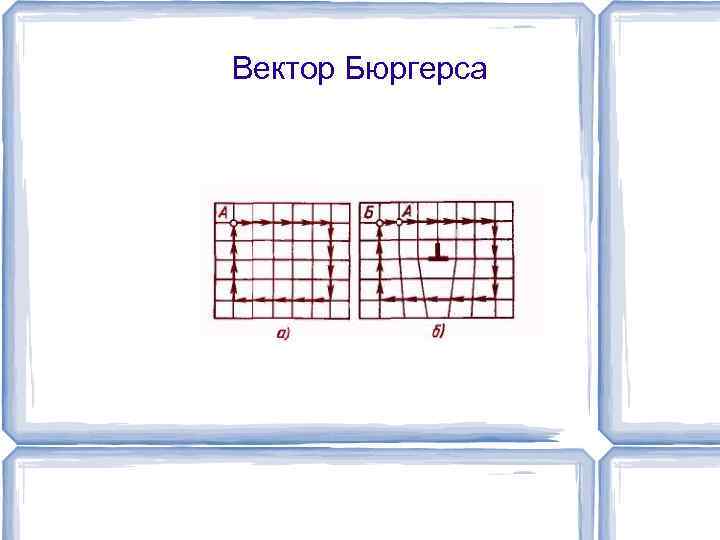 Вектор Бюргерса
Вектор Бюргерса
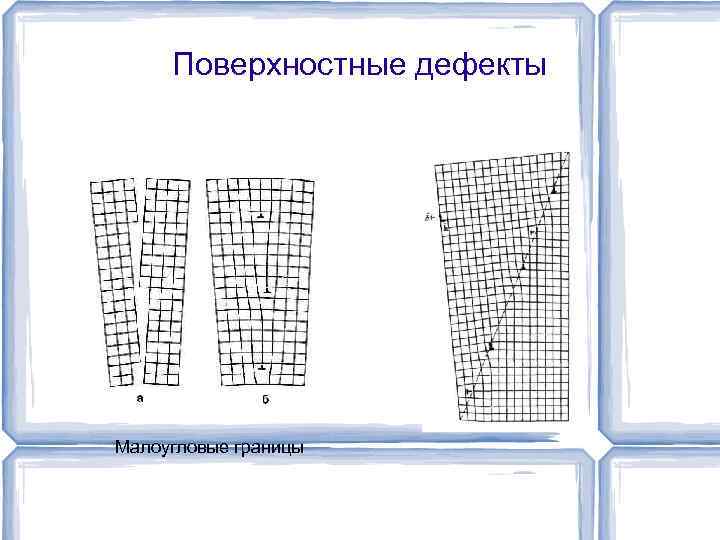 Поверхностные дефекты Малоугловые границы
Поверхностные дефекты Малоугловые границы
 ВЫВОДЫ 1. В равновесном состоянии все практически материалы при понижении температуры имеют кристаллическое строение, атомная структура кристалла определяется видом химической связи (металлическое, ковалентной, ионной или молекулярной) 2. Атомы или ионы в кристаллической решетке находятся в постоянном движении. При температуре отличной от температуры абсолютного нуля всегда есть атомы, имеющие энергию, превышающую любую заданную, что обуславливает протекание различных физико-химических процессов в материале 3. При увеличении температуры увеличивается степень беспорядка в кристаллической решетке (амплитуда теплового движения, равновесное количество дефектов), уменьшается время «оседлой» жизни атома на своем месте в кристаллической решетке. Это ведет к потере устойчивости кристаллической решетки (плавлению).
ВЫВОДЫ 1. В равновесном состоянии все практически материалы при понижении температуры имеют кристаллическое строение, атомная структура кристалла определяется видом химической связи (металлическое, ковалентной, ионной или молекулярной) 2. Атомы или ионы в кристаллической решетке находятся в постоянном движении. При температуре отличной от температуры абсолютного нуля всегда есть атомы, имеющие энергию, превышающую любую заданную, что обуславливает протекание различных физико-химических процессов в материале 3. При увеличении температуры увеличивается степень беспорядка в кристаллической решетке (амплитуда теплового движения, равновесное количество дефектов), уменьшается время «оседлой» жизни атома на своем месте в кристаллической решетке. Это ведет к потере устойчивости кристаллической решетки (плавлению).


