Материаловедение-Лекция4.ppt
- Количество слайдов: 20
 Материаловедение Лекция 4
Материаловедение Лекция 4
 Содержание лекции • Диаграмма состояния. Общие понятия • Определение состава фаз по диаграмме состояния • Диаграмма состояния сплавов с ограниченной растворимостью компонент • Диаграммы состояния сплавов, образующих химические соединения, с полиморфным и эвтектоидными превращениями 2 2
Содержание лекции • Диаграмма состояния. Общие понятия • Определение состава фаз по диаграмме состояния • Диаграмма состояния сплавов с ограниченной растворимостью компонент • Диаграммы состояния сплавов, образующих химические соединения, с полиморфным и эвтектоидными превращениями 2 2
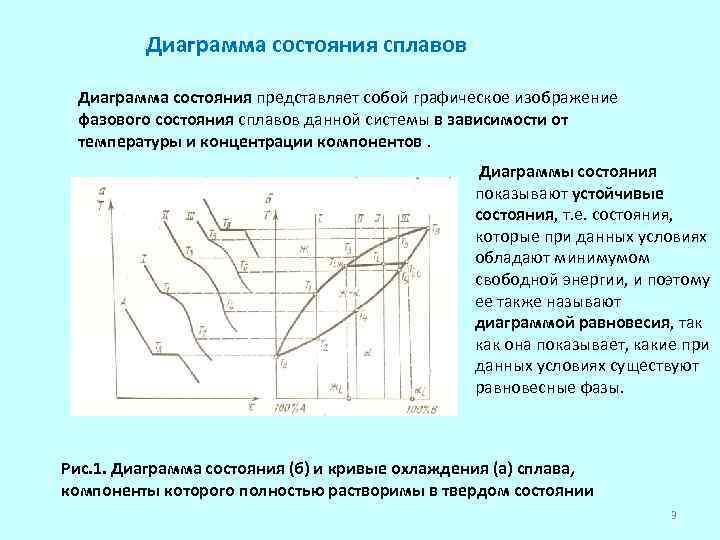 Диаграмма состояния сплавов Диаграмма состояния представляет собой графическое изображение фазового состояния сплавов данной системы в зависимости от температуры и концентрации компонентов. Диаграммы состояния показывают устойчивые состояния, т. е. состояния, которые при данных условиях обладают минимумом свободной энергии, и поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы. Рис. 1. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого полностью растворимы в твердом состоянии 3
Диаграмма состояния сплавов Диаграмма состояния представляет собой графическое изображение фазового состояния сплавов данной системы в зависимости от температуры и концентрации компонентов. Диаграммы состояния показывают устойчивые состояния, т. е. состояния, которые при данных условиях обладают минимумом свободной энергии, и поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы. Рис. 1. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого полностью растворимы в твердом состоянии 3
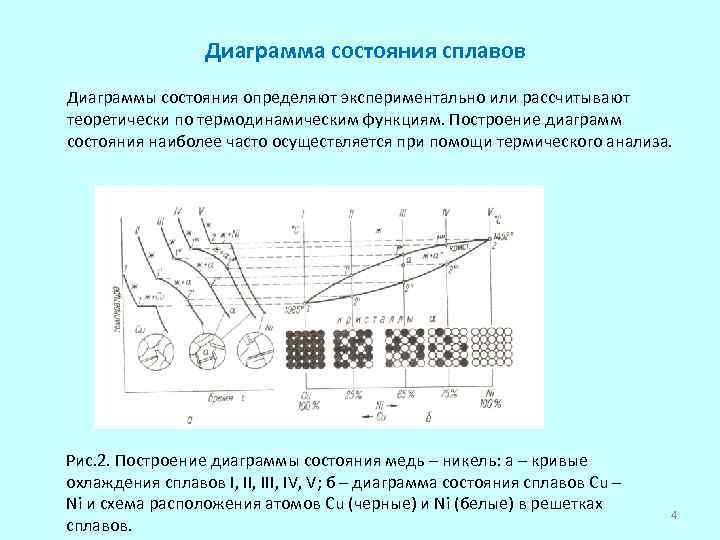 Диаграмма состояния сплавов Диаграммы состояния определяют экспериментально или рассчитывают теоретически по термодинамическим функциям. Построение диаграмм состояния наиболее часто осуществляется при помощи термического анализа. Рис. 2. Построение диаграммы состояния медь – никель: а – кривые охлаждения сплавов I, III, IV, V; б – диаграмма состояния сплавов Cu – Ni и схема расположения атомов Cu (черные) и Ni (белые) в решетках сплавов. 4
Диаграмма состояния сплавов Диаграммы состояния определяют экспериментально или рассчитывают теоретически по термодинамическим функциям. Построение диаграмм состояния наиболее часто осуществляется при помощи термического анализа. Рис. 2. Построение диаграммы состояния медь – никель: а – кривые охлаждения сплавов I, III, IV, V; б – диаграмма состояния сплавов Cu – Ni и схема расположения атомов Cu (черные) и Ni (белые) в решетках сплавов. 4
 Диаграмма состояния сплавов Для экспериментального построения диаграммы состояний сплавов, образованных компонентами А и В, необходимо изготовить серию сплавов, содержащих различные количества компонентов А и В. Для каждого такого сплава экспериментально строят кривые охлаждения и определяют по ним критические точки, т. е. температуры фазовых превращений. Некоторые критические точки имеют названия, например, точки, отвечающие началу кристаллизации, называют точками ликвидус, а концу кристаллизации – точками солидус. 5
Диаграмма состояния сплавов Для экспериментального построения диаграммы состояний сплавов, образованных компонентами А и В, необходимо изготовить серию сплавов, содержащих различные количества компонентов А и В. Для каждого такого сплава экспериментально строят кривые охлаждения и определяют по ним критические точки, т. е. температуры фазовых превращений. Некоторые критические точки имеют названия, например, точки, отвечающие началу кристаллизации, называют точками ликвидус, а концу кристаллизации – точками солидус. 5
 По кривым охлаждения строят диаграмму состава в координатах: по оси абсцисс – концентрация компонентов, по оси ординат – температура. Шкала концентраций показывает содержание компонента В. Левая крайняя точка на оси концентраций соответствует 100% содержанию компонента А. Процентное содержание второго компонента откладывается по этой оси слева направо. Правая крайняя точка соответствует 100 % содержанию второго компонента В. Рис. 1. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого полностью растворимы в твердом состоянии 6
По кривым охлаждения строят диаграмму состава в координатах: по оси абсцисс – концентрация компонентов, по оси ординат – температура. Шкала концентраций показывает содержание компонента В. Левая крайняя точка на оси концентраций соответствует 100% содержанию компонента А. Процентное содержание второго компонента откладывается по этой оси слева направо. Правая крайняя точка соответствует 100 % содержанию второго компонента В. Рис. 1. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого полностью растворимы в твердом состоянии 6
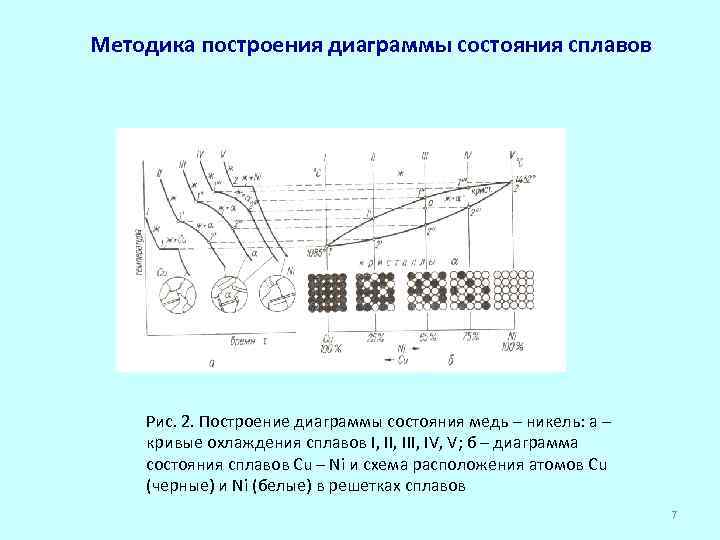 Методика построения диаграммы состояния сплавов Рис. 2. Построение диаграммы состояния медь – никель: а – кривые охлаждения сплавов I, III, IV, V; б – диаграмма состояния сплавов Cu – Ni и схема расположения атомов Cu (черные) и Ni (белые) в решетках сплавов 7
Методика построения диаграммы состояния сплавов Рис. 2. Построение диаграммы состояния медь – никель: а – кривые охлаждения сплавов I, III, IV, V; б – диаграмма состояния сплавов Cu – Ni и схема расположения атомов Cu (черные) и Ni (белые) в решетках сплавов 7
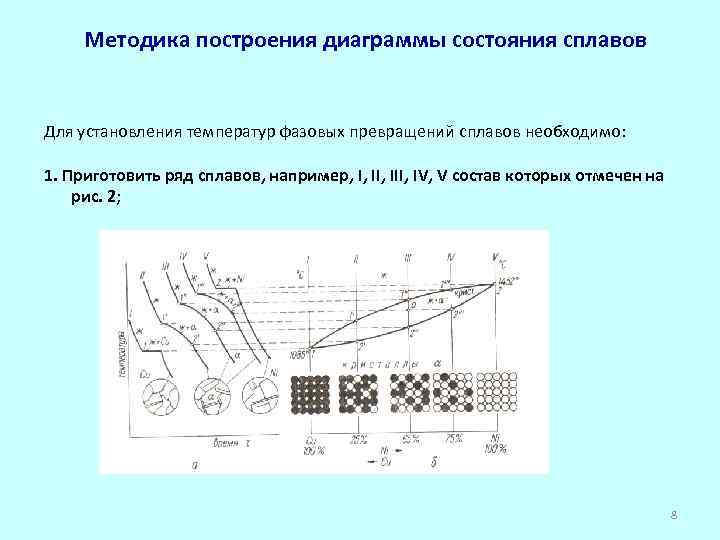 Методика построения диаграммы состояния сплавов Для установления температур фазовых превращений сплавов необходимо: 1. Приготовить ряд сплавов, например, I, III, IV, V состав которых отмечен на рис. 2; 8
Методика построения диаграммы состояния сплавов Для установления температур фазовых превращений сплавов необходимо: 1. Приготовить ряд сплавов, например, I, III, IV, V состав которых отмечен на рис. 2; 8
 3. Построить кривые охлаждения каждого сплава Изучение фазового состояния сплавов I, III, IV, V при температурах выше 1, 1 , 1 , 2 показывает, что в этих условиях все сплавы находятся в жидком состоянии. При температурах 1 – медь, 2 – никель, и в интервале температур 1 -2 … 1 -2 , сплавы находятся в двухфазном состоянии – имеет место жидкая фаза «ж» и кристаллы, которые для сплавов условно обозначены . При температурах ниже 1, 2 , …. 2 , 2 сплавы находятся в однофазном кристаллическом состоянии. Очевидно температуры точек 1, 2 , …. 2 , 2 – являются температурами конца кристаллизации сплавов данной системы. 9
3. Построить кривые охлаждения каждого сплава Изучение фазового состояния сплавов I, III, IV, V при температурах выше 1, 1 , 1 , 2 показывает, что в этих условиях все сплавы находятся в жидком состоянии. При температурах 1 – медь, 2 – никель, и в интервале температур 1 -2 … 1 -2 , сплавы находятся в двухфазном состоянии – имеет место жидкая фаза «ж» и кристаллы, которые для сплавов условно обозначены . При температурах ниже 1, 2 , …. 2 , 2 сплавы находятся в однофазном кристаллическом состоянии. Очевидно температуры точек 1, 2 , …. 2 , 2 – являются температурами конца кристаллизации сплавов данной системы. 9
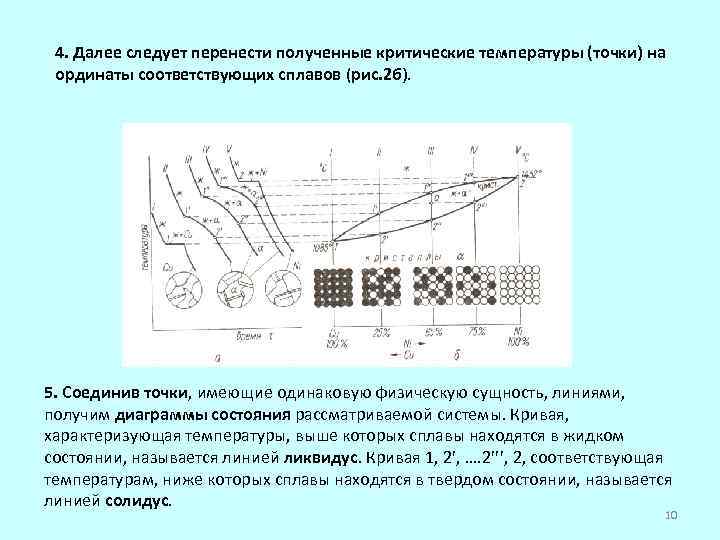 4. Далее следует перенести полученные критические температуры (точки) на ординаты соответствующих сплавов (рис. 2 б). 5. Соединив точки, имеющие одинаковую физическую сущность, линиями, получим диаграммы состояния рассматриваемой системы. Кривая, характеризующая температуры, выше которых сплавы находятся в жидком состоянии, называется линией ликвидус. Кривая 1, 2 , …. 2 , 2, соответствующая температурам, ниже которых сплавы находятся в твердом состоянии, называется линией солидус. 10
4. Далее следует перенести полученные критические температуры (точки) на ординаты соответствующих сплавов (рис. 2 б). 5. Соединив точки, имеющие одинаковую физическую сущность, линиями, получим диаграммы состояния рассматриваемой системы. Кривая, характеризующая температуры, выше которых сплавы находятся в жидком состоянии, называется линией ликвидус. Кривая 1, 2 , …. 2 , 2, соответствующая температурам, ниже которых сплавы находятся в твердом состоянии, называется линией солидус. 10
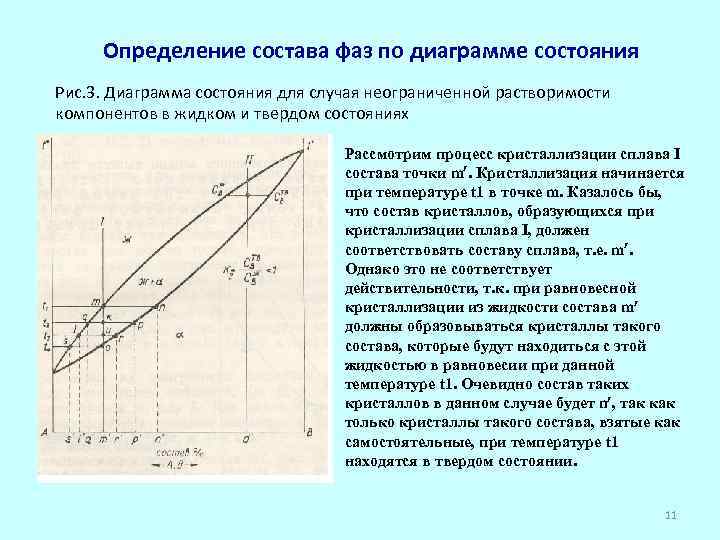 Определение состава фаз по диаграмме состояния Рис. 3. Диаграмма состояния для случая неограниченной растворимости компонентов в жидком и твердом состояниях Рассмотрим процесс кристаллизации сплава I состава точки m. Кристаллизация начинается при температуре t 1 в точке m. Казалось бы, что состав кристаллов, образующихся при кристаллизации сплава I, должен соответствовать составу сплава, т. е. m. Однако это не соответствует действительности, т. к. при равновесной кристаллизации из жидкости состава m должны образовываться кристаллы такого состава, которые будут находиться с этой жидкостью в равновесии при данной температуре t 1. Очевидно состав таких кристаллов в данном случае будет n , так как только кристаллы такого состава, взятые как самостоятельные, при температуре t 1 находятся в твердом состоянии. 11
Определение состава фаз по диаграмме состояния Рис. 3. Диаграмма состояния для случая неограниченной растворимости компонентов в жидком и твердом состояниях Рассмотрим процесс кристаллизации сплава I состава точки m. Кристаллизация начинается при температуре t 1 в точке m. Казалось бы, что состав кристаллов, образующихся при кристаллизации сплава I, должен соответствовать составу сплава, т. е. m. Однако это не соответствует действительности, т. к. при равновесной кристаллизации из жидкости состава m должны образовываться кристаллы такого состава, которые будут находиться с этой жидкостью в равновесии при данной температуре t 1. Очевидно состав таких кристаллов в данном случае будет n , так как только кристаллы такого состава, взятые как самостоятельные, при температуре t 1 находятся в твердом состоянии. 11
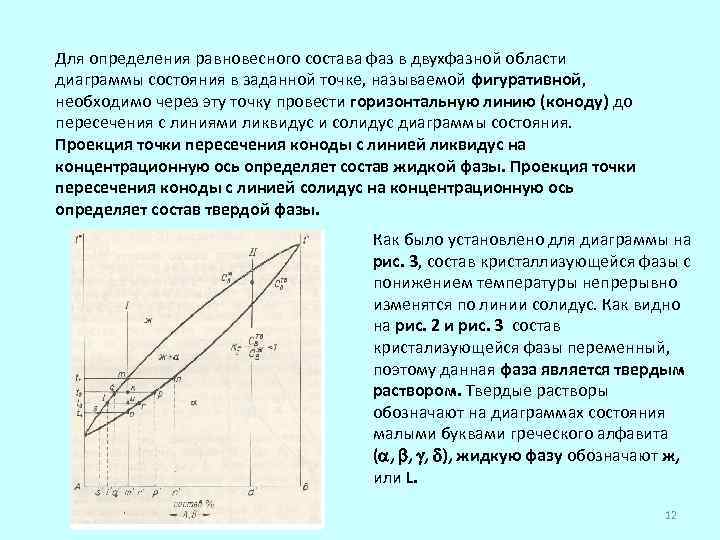 Для определения равновесного состава фаз в двухфазной области диаграммы состояния в заданной точке, называемой фигуративной, необходимо через эту точку провести горизонтальную линию (коноду) до пересечения с линиями ликвидус и солидус диаграммы состояния. Проекция точки пересечения коноды с линией ликвидус на концентрационную ось определяет состав жидкой фазы. Проекция точки пересечения коноды с линией солидус на концентрационную ось определяет состав твердой фазы. Как было установлено для диаграммы на рис. 3, состав кристаллизующейся фазы с понижением температуры непрерывно изменятся по линии солидус. Как видно на рис. 2 и рис. 3 состав кристализующейся фазы переменный, поэтому данная фаза является твердым раствором. Твердые растворы обозначают на диаграммах состояния малыми буквами греческого алфавита ( , , , ), жидкую фазу обозначают ж, или L. 12
Для определения равновесного состава фаз в двухфазной области диаграммы состояния в заданной точке, называемой фигуративной, необходимо через эту точку провести горизонтальную линию (коноду) до пересечения с линиями ликвидус и солидус диаграммы состояния. Проекция точки пересечения коноды с линией ликвидус на концентрационную ось определяет состав жидкой фазы. Проекция точки пересечения коноды с линией солидус на концентрационную ось определяет состав твердой фазы. Как было установлено для диаграммы на рис. 3, состав кристаллизующейся фазы с понижением температуры непрерывно изменятся по линии солидус. Как видно на рис. 2 и рис. 3 состав кристализующейся фазы переменный, поэтому данная фаза является твердым раствором. Твердые растворы обозначают на диаграммах состояния малыми буквами греческого алфавита ( , , , ), жидкую фазу обозначают ж, или L. 12
 Определение количества фаз Пусть требуется определить количество жидкой фазы ж и твердой фазы при температуре точки k сплава I на рис. 3. Если принять общее количество сплава за 1, а количество твердой фазы ( -кристаллов) через х, то количество жидкой фазы будет (1 -х). В сплаве I имеется Аm % компонента В, который при температуре точки k распределяется между жидкой и твердой фазами. Составим уравнение относительно компонента В, количество которого во взятом сплаве I определяется отрезком Аm. Его количество в твердой фазе х. Ар а в жидкой фазе (1 -х)Аq. Очевидно, что х. Ар + (1 -х)Аq = Аm ; х(Ар Аq ) = Аm Аq ; но Ар Аq = р q; Аm Аq = q m = kq, тогда х = = kq/qp, (1) 1 -x = ж= kq/qp. (2) Рис. 3. Диаграмма состояния для случая неограниченной растворимости компонентов в жидком и твердом состояниях 13
Определение количества фаз Пусть требуется определить количество жидкой фазы ж и твердой фазы при температуре точки k сплава I на рис. 3. Если принять общее количество сплава за 1, а количество твердой фазы ( -кристаллов) через х, то количество жидкой фазы будет (1 -х). В сплаве I имеется Аm % компонента В, который при температуре точки k распределяется между жидкой и твердой фазами. Составим уравнение относительно компонента В, количество которого во взятом сплаве I определяется отрезком Аm. Его количество в твердой фазе х. Ар а в жидкой фазе (1 -х)Аq. Очевидно, что х. Ар + (1 -х)Аq = Аm ; х(Ар Аq ) = Аm Аq ; но Ар Аq = р q; Аm Аq = q m = kq, тогда х = = kq/qp, (1) 1 -x = ж= kq/qp. (2) Рис. 3. Диаграмма состояния для случая неограниченной растворимости компонентов в жидком и твердом состояниях 13
 Правило для определения количества фаз в двухфазовых областях Для определения весового или объемного количества фазы в заданной точке нужно: провести через эту точку коноду и разделить длину отрезка противолежащего составу данной фазы на общую длину отрезка (коноды). Соотношение фаз при кристаллизации в системе устанавливают с помощью правила отрезков: массовые (объемные) соотношения твердой и жидкой фазы фаз в сплаве пропорциональны отношению отрезков, примыкающих к линиям ликвидус и солидус. Количественное соотношение фаз в сплаве I по правлу отрезков определяют по соотношению отрезков Tiж. Ti и Ti Tic. Так, содержание твердой фазы в сплаве I = (Tiж. Ti)/(Tiж Tic) 100, содержание жидкой фазы – Жi = (Ti Tic) / (Tiж Tic) 100. Рис. 1. 14
Правило для определения количества фаз в двухфазовых областях Для определения весового или объемного количества фазы в заданной точке нужно: провести через эту точку коноду и разделить длину отрезка противолежащего составу данной фазы на общую длину отрезка (коноды). Соотношение фаз при кристаллизации в системе устанавливают с помощью правила отрезков: массовые (объемные) соотношения твердой и жидкой фазы фаз в сплаве пропорциональны отношению отрезков, примыкающих к линиям ликвидус и солидус. Количественное соотношение фаз в сплаве I по правлу отрезков определяют по соотношению отрезков Tiж. Ti и Ti Tic. Так, содержание твердой фазы в сплаве I = (Tiж. Ti)/(Tiж Tic) 100, содержание жидкой фазы – Жi = (Ti Tic) / (Tiж Tic) 100. Рис. 1. 14
 Диаграмма состояния сплавов с ограниченной растворимостью компонентов В твердом состоянии металлы обычно ограниченно растворимы один в другом. Существуют три типа таких сплавов: • сплавы с ограниченной растворимостью компонентов и эвтектическим превращением; • сплавы компонентов, практически не растворимых в твердом состоянии, с эвтектическим превращением; • сплавы с ограниченной растворимостью компонентов и перитектическим превращением. Эвтектикой ( «легкоплавящийся» ) называют высокодисперсную механическую смесь нескольких твердых фаз, одновременно кристаллизующихся при постоянной температуре из расплава. Эвтектическим превращением называют процесс одновременной кристаллизации из расплава нескольких твердых фаз при постоянной температуре. 15
Диаграмма состояния сплавов с ограниченной растворимостью компонентов В твердом состоянии металлы обычно ограниченно растворимы один в другом. Существуют три типа таких сплавов: • сплавы с ограниченной растворимостью компонентов и эвтектическим превращением; • сплавы компонентов, практически не растворимых в твердом состоянии, с эвтектическим превращением; • сплавы с ограниченной растворимостью компонентов и перитектическим превращением. Эвтектикой ( «легкоплавящийся» ) называют высокодисперсную механическую смесь нескольких твердых фаз, одновременно кристаллизующихся при постоянной температуре из расплава. Эвтектическим превращением называют процесс одновременной кристаллизации из расплава нескольких твердых фаз при постоянной температуре. 15
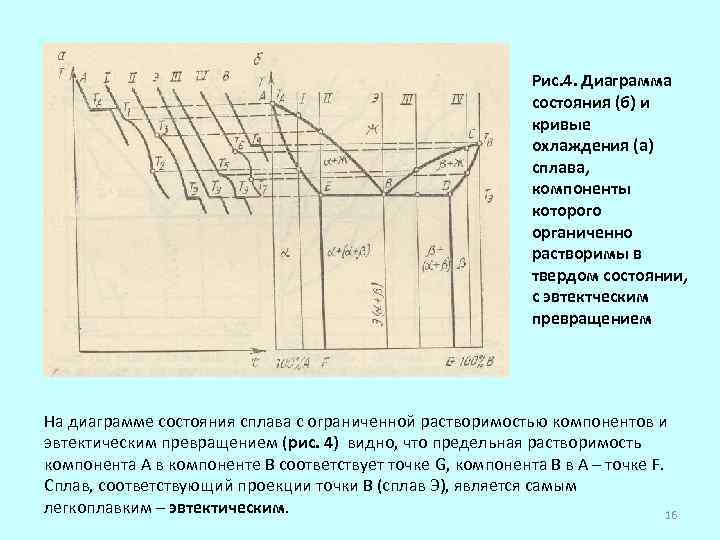 Рис. 4. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого органиченно растворимы в твердом состоянии, с эвтектческим превращением На диаграмме состояния сплава с ограниченной растворимостью компонентов и эвтектическим превращением (рис. 4) видно, что предельная растворимость компонента А в компоненте В соответствует точке G, компонента В в А – точке F. Сплав, соответствующий проекции точки В (сплав Э), является самым легкоплавким – эвтектическим. 16
Рис. 4. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого органиченно растворимы в твердом состоянии, с эвтектческим превращением На диаграмме состояния сплава с ограниченной растворимостью компонентов и эвтектическим превращением (рис. 4) видно, что предельная растворимость компонента А в компоненте В соответствует точке G, компонента В в А – точке F. Сплав, соответствующий проекции точки В (сплав Э), является самым легкоплавким – эвтектическим. 16
 Сплавы, относящиеся к област левее точки В до точки Е, называют доэвтектические, правее точки В до точки D – заэвтектическими. При температурах выше линии АВС (ликвидус) система находится в жидком состоянии; при температурах, соответствующих точкам на линии AEBDC (солидус) – в твердом. Кристаллизация сплава I протекает с понижением температуры, так как система в данном случае является моновариантной. После окончания процесса кристаллизации (температура Т 2) сплав состоит из кристаллов -твердый раствор. При охлаждении доэвтектического сплава II в диапазоне температур Tз – Тэ кристаллизуется -твердый раствор. После достижения системой температуры эвтектического превращения Тэ одновременно начинают кристаллизоваться - и -фазы. В данном случае вариантность системы С=0 (С = 2+1 -3) и эвтектическое превращение протекает при постоянной температуре. На кривой охлаждения такого сплава появляется горизонтальный участок. После выпадения эвтектики система не подвергается никаким превращениям. Состав сплава после охлаждения - + эвтектика ( + ). При охлаждении эвтектического сплава (Э) до температуры Тэ на кривой охлаждения появляется горизонтальный участок, связанный с выделением теплоты кристаллизации. Закристаллизовавшаяся эвтектика состоит из механической смеси кристаллов + . Согласно теории кристаллизации эвтектик, процесс начинается с зарождения кристаллов одной из фаз. Выпадение кристаллов, например из - раствора, вызывает смещение равновесного содержания компонентов в пользу компонента В. Избыток последнего вызывает кристаллизацию -раствора, что, в свою очередь обусловливает появление избыточного содержания компонента А в системе. Таким образом, в каждом до- и заэтектическом сплаве имеется некоторое содержание эвтектики, определяемое правилом отрезков. Примером сплава с подобным типом диаграммы состояния является сплав Pb-Sn. 17
Сплавы, относящиеся к област левее точки В до точки Е, называют доэвтектические, правее точки В до точки D – заэвтектическими. При температурах выше линии АВС (ликвидус) система находится в жидком состоянии; при температурах, соответствующих точкам на линии AEBDC (солидус) – в твердом. Кристаллизация сплава I протекает с понижением температуры, так как система в данном случае является моновариантной. После окончания процесса кристаллизации (температура Т 2) сплав состоит из кристаллов -твердый раствор. При охлаждении доэвтектического сплава II в диапазоне температур Tз – Тэ кристаллизуется -твердый раствор. После достижения системой температуры эвтектического превращения Тэ одновременно начинают кристаллизоваться - и -фазы. В данном случае вариантность системы С=0 (С = 2+1 -3) и эвтектическое превращение протекает при постоянной температуре. На кривой охлаждения такого сплава появляется горизонтальный участок. После выпадения эвтектики система не подвергается никаким превращениям. Состав сплава после охлаждения - + эвтектика ( + ). При охлаждении эвтектического сплава (Э) до температуры Тэ на кривой охлаждения появляется горизонтальный участок, связанный с выделением теплоты кристаллизации. Закристаллизовавшаяся эвтектика состоит из механической смеси кристаллов + . Согласно теории кристаллизации эвтектик, процесс начинается с зарождения кристаллов одной из фаз. Выпадение кристаллов, например из - раствора, вызывает смещение равновесного содержания компонентов в пользу компонента В. Избыток последнего вызывает кристаллизацию -раствора, что, в свою очередь обусловливает появление избыточного содержания компонента А в системе. Таким образом, в каждом до- и заэтектическом сплаве имеется некоторое содержание эвтектики, определяемое правилом отрезков. Примером сплава с подобным типом диаграммы состояния является сплав Pb-Sn. 17
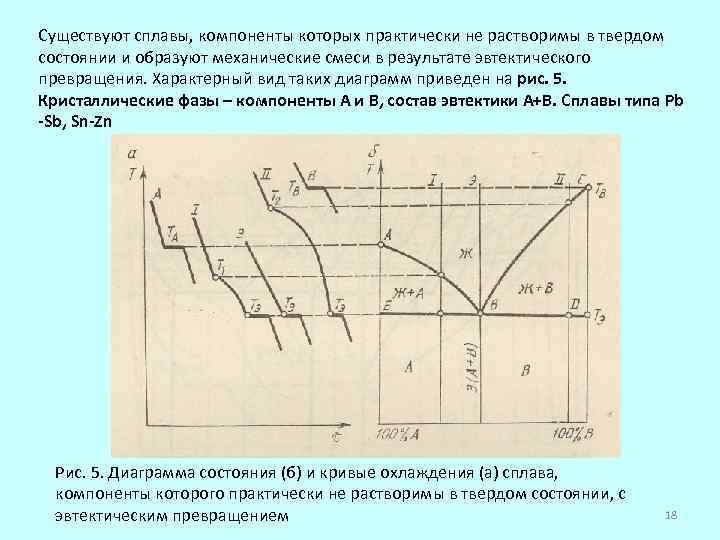 Существуют сплавы, компоненты которых практически не растворимы в твердом состоянии и образуют механические смеси в результате эвтектического превращения. Характерный вид таких диаграмм приведен на рис. 5. Кристаллические фазы – компоненты А и В, состав эвтектики А+В. Сплавы типа Pb -Sb, Sn-Zn Рис. 5. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого практически не растворимы в твердом состоянии, с эвтектическим превращением 18
Существуют сплавы, компоненты которых практически не растворимы в твердом состоянии и образуют механические смеси в результате эвтектического превращения. Характерный вид таких диаграмм приведен на рис. 5. Кристаллические фазы – компоненты А и В, состав эвтектики А+В. Сплавы типа Pb -Sb, Sn-Zn Рис. 5. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого практически не растворимы в твердом состоянии, с эвтектическим превращением 18
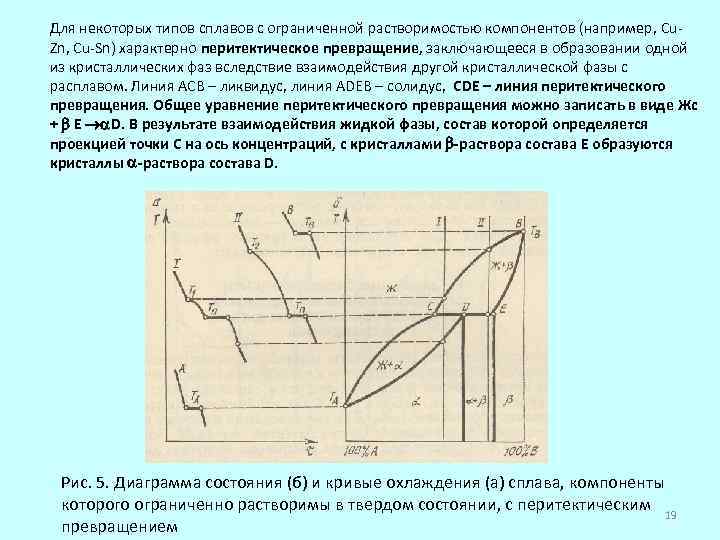 Для некоторых типов сплавов с ограниченной растворимостью компонентов (например, Cu. Zn, Cu-Sn) характерно перитектическое превращение, заключающееся в образовании одной из кристаллических фаз вследствие взаимодействия другой кристаллической фазы с расплавом. Линия АСВ – ликвидус, линия ADEB – солидус, CDE – линия перитектического превращения. Общее уравнение перитектического превращения можно записать в виде Жс + Е D. В результате взаимодействия жидкой фазы, состав которой определяется проекцией точки С на ось концентраций, с кристаллами -раствора состава Е образуются кристаллы -раствора состава D. Рис. 5. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого ограниченно растворимы в твердом состоянии, с перитектическим 19 превращением
Для некоторых типов сплавов с ограниченной растворимостью компонентов (например, Cu. Zn, Cu-Sn) характерно перитектическое превращение, заключающееся в образовании одной из кристаллических фаз вследствие взаимодействия другой кристаллической фазы с расплавом. Линия АСВ – ликвидус, линия ADEB – солидус, CDE – линия перитектического превращения. Общее уравнение перитектического превращения можно записать в виде Жс + Е D. В результате взаимодействия жидкой фазы, состав которой определяется проекцией точки С на ось концентраций, с кристаллами -раствора состава Е образуются кристаллы -раствора состава D. Рис. 5. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого ограниченно растворимы в твердом состоянии, с перитектическим 19 превращением
 При перитектическом превращении в системе существуют три фазы – жидкая и два твердых раствора. Вследствие нонвариантности системы перитектическое превращение протекает при постоянной температуре Тп. На кривых охлаждения сплавов I и II и перитектического появляется горизонтальный участок. Понижение температуры сплава I до Тп приводит к образованию кристаллической фазы -раствора. После окончания перитектического превращения в сплаве находятся кристаллы -раствора. Охлаждение сплава II ниже температур линии ликвидус вызывает кристаллизацию -раствора. Перитектическое превращение приводит к образованию -раствора. Ввиду того, что не весь -раствор израсходован на образование -раствора, после перитектического превращения сплав будет содержать - и -фазы. В сплаве металлов, ограниченно растворяющихся в твердом состоянии, могут образоваться ликвации – неоднородности химического состава. Для устранения этого вредного эффекта сплавы охлаждают с высокими скоростями, пермешивают. 20
При перитектическом превращении в системе существуют три фазы – жидкая и два твердых раствора. Вследствие нонвариантности системы перитектическое превращение протекает при постоянной температуре Тп. На кривых охлаждения сплавов I и II и перитектического появляется горизонтальный участок. Понижение температуры сплава I до Тп приводит к образованию кристаллической фазы -раствора. После окончания перитектического превращения в сплаве находятся кристаллы -раствора. Охлаждение сплава II ниже температур линии ликвидус вызывает кристаллизацию -раствора. Перитектическое превращение приводит к образованию -раствора. Ввиду того, что не весь -раствор израсходован на образование -раствора, после перитектического превращения сплав будет содержать - и -фазы. В сплаве металлов, ограниченно растворяющихся в твердом состоянии, могут образоваться ликвации – неоднородности химического состава. Для устранения этого вредного эффекта сплавы охлаждают с высокими скоростями, пермешивают. 20


