Материаловедение-Лекция3.ppt
- Количество слайдов: 19
 Материаловедение Лекция 3
Материаловедение Лекция 3
 Содержание лекции • Понятие о сплавах и методах их получения • Основные понятия в теории сплавов • Особенности строения, кристаллизации и свойств сплавов. Механические смеси, твердые растворы, химические соединения • Классификация сплавов твердых растворов • Кристаллизация сплавов • Диаграмма состояния 2 2
Содержание лекции • Понятие о сплавах и методах их получения • Основные понятия в теории сплавов • Особенности строения, кристаллизации и свойств сплавов. Механические смеси, твердые растворы, химические соединения • Классификация сплавов твердых растворов • Кристаллизация сплавов • Диаграмма состояния 2 2
 Понятие о сплавах и методах их получения Сплавы – сложные вещества, получаемые сплавлением металлов или металлов с неметаллами. Другие способы приготовления сплавов: - спекание; - электролиз; - плазменное напыление; - кристаллизация из паров; - восстановление из оксидов и др. Простые вещества, образующие сплав, называются компонентами сплава. Сплавы называются однородными (гомогенными), если их структура однофазная, и разнородными (гетерогенными), если структура их состоит из нескольких фаз. 3 3
Понятие о сплавах и методах их получения Сплавы – сложные вещества, получаемые сплавлением металлов или металлов с неметаллами. Другие способы приготовления сплавов: - спекание; - электролиз; - плазменное напыление; - кристаллизация из паров; - восстановление из оксидов и др. Простые вещества, образующие сплав, называются компонентами сплава. Сплавы называются однородными (гомогенными), если их структура однофазная, и разнородными (гетерогенными), если структура их состоит из нескольких фаз. 3 3
 Основные понятия в теории сплавов Система – группа тел, выделяемая для наблюдения и изучения В металловедении системами являются металлы и металлические сплавы. Чистый металл является однокомпонентной системой, сплав – сложной системой, состоящей из двух или более компонентов. Компоненты – вещества, образующие систему. В качестве компонентов выступают чистые вещества и химические соединения. Если они не диссоциируют на составные части в исследуемом интервале температур. Фаза – однородная часть системы, отделенная от других частей системы поверхностью раздела , при переходе через которую структура и свойства резко меняются. Вариантность (С) (число степеней свободы) – это число внутренних и внешних факторов (температура, давление, концентрация), которые можно изменять без изменения количества фаз в системе. Если вариантность С = 1 (моновариантная система), то возможно изменение одного из факторов в некоторых пределах без изменения числа фаз. Если вариантность С=0 (нонвариантная система), то внешние факторы изменять нельзя без изменения числа фаз в системе. Т. е. существует при определенных значениях р, Т, содержания каждой фазы. При С=0 система включает максимально возможное число фаз. 4
Основные понятия в теории сплавов Система – группа тел, выделяемая для наблюдения и изучения В металловедении системами являются металлы и металлические сплавы. Чистый металл является однокомпонентной системой, сплав – сложной системой, состоящей из двух или более компонентов. Компоненты – вещества, образующие систему. В качестве компонентов выступают чистые вещества и химические соединения. Если они не диссоциируют на составные части в исследуемом интервале температур. Фаза – однородная часть системы, отделенная от других частей системы поверхностью раздела , при переходе через которую структура и свойства резко меняются. Вариантность (С) (число степеней свободы) – это число внутренних и внешних факторов (температура, давление, концентрация), которые можно изменять без изменения количества фаз в системе. Если вариантность С = 1 (моновариантная система), то возможно изменение одного из факторов в некоторых пределах без изменения числа фаз. Если вариантность С=0 (нонвариантная система), то внешние факторы изменять нельзя без изменения числа фаз в системе. Т. е. существует при определенных значениях р, Т, содержания каждой фазы. При С=0 система включает максимально возможное число фаз. 4
 Основные понятия в теории сплавов Существует математическая связь между числом компонентов (К), числом фаз (Ф) и вариантностью системы (С). Это правило фаз или закон Гиббса: С=К–Ф+2 Если принять во внимание, что все превращения происходят при постоянном давлении, то число переменных уменьшится С=К–Ф+1 где С – число степеней свободы, К – число компонентов, Ф – число фаз, 1 – учитывает возможность изменения температуры. При кристаллизации элемента из расплава в системе существует две фазы – жидкая и твердая, что возможно только при постоянной температуре. Поэтому процесс кристаллизации является изотермическим (С=0). После полного исчезновения одной фазы в системе С=1. Параметр n характеризует внешние факторы (р, Т) оказывающие влияние на систему. Таким образом, n=2. В обычных условиях давленеи (атмосферное) не оказывает заметного влияния на состояние системы, поэтому принимают n=1. Из этого следует важный практический вывод: при постоянном давлении, равном атмосферному, число фаз, находящихся в равновесии, не может превышать больше, чем на единицу, число компонентов (К), т. е. Ф К+1. 5
Основные понятия в теории сплавов Существует математическая связь между числом компонентов (К), числом фаз (Ф) и вариантностью системы (С). Это правило фаз или закон Гиббса: С=К–Ф+2 Если принять во внимание, что все превращения происходят при постоянном давлении, то число переменных уменьшится С=К–Ф+1 где С – число степеней свободы, К – число компонентов, Ф – число фаз, 1 – учитывает возможность изменения температуры. При кристаллизации элемента из расплава в системе существует две фазы – жидкая и твердая, что возможно только при постоянной температуре. Поэтому процесс кристаллизации является изотермическим (С=0). После полного исчезновения одной фазы в системе С=1. Параметр n характеризует внешние факторы (р, Т) оказывающие влияние на систему. Таким образом, n=2. В обычных условиях давленеи (атмосферное) не оказывает заметного влияния на состояние системы, поэтому принимают n=1. Из этого следует важный практический вывод: при постоянном давлении, равном атмосферному, число фаз, находящихся в равновесии, не может превышать больше, чем на единицу, число компонентов (К), т. е. Ф К+1. 5
 Особенности строения, кристаллизации и свойств сплавов. Механические смеси, твердые растворы, химические соединения Строение металлического сплава зависит от того, в какие взаимодействия вступают компоненты, составляющие сплав. Почти все металлы в жидком состоянии растворяются друг в друге в любых соотношениях. При образовании сплавов в процессе их затвердевания возможно различное взаимодействие компонентов. В зависимости от характера взаимодействия компонентов различают сплавы: • Механические смеси; • Химические соединения; • Твердые растворы. 6
Особенности строения, кристаллизации и свойств сплавов. Механические смеси, твердые растворы, химические соединения Строение металлического сплава зависит от того, в какие взаимодействия вступают компоненты, составляющие сплав. Почти все металлы в жидком состоянии растворяются друг в друге в любых соотношениях. При образовании сплавов в процессе их затвердевания возможно различное взаимодействие компонентов. В зависимости от характера взаимодействия компонентов различают сплавы: • Механические смеси; • Химические соединения; • Твердые растворы. 6
 Механические смеси Сплавы механические смеси образуются, когда компоненты не способны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединения. Механические смеси образуются между элементами, значительно различающимися по строению и свойствам, когда сила взаимодействия между атомами одного элемента больше, чем между разнородными. Сплав состоит из кристаллов входящих в него компонентов. В сплавах сохраняются кристаллические решетки компонентов. Схема микроструктуры механической смеси 7
Механические смеси Сплавы механические смеси образуются, когда компоненты не способны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединения. Механические смеси образуются между элементами, значительно различающимися по строению и свойствам, когда сила взаимодействия между атомами одного элемента больше, чем между разнородными. Сплав состоит из кристаллов входящих в него компонентов. В сплавах сохраняются кристаллические решетки компонентов. Схема микроструктуры механической смеси 7
 Сплавы химические соединения В сплавах возможно образование фаз постоянного состава, соотношение элементов в которых подчиняется правилу валентности. Такие сплавы называются химическими соединениями. В сплавах существуют химические соединения переменного состава, не соответствующие правилу валентности, так называемые промежуточные фазы. Сплавы химические соединения образуются между элементами, значительно различающимися по строению и свойствам, если сила взаимодействия между разнородными атомами больше, чем между однородными. Особенности этих сплавов: • Постоянство состава, то есть сплав образуется при определенном соотношении компонентов, химическое соединение обозначается An. Bm; • Образуется специфическая, отличающаяся от решеток элементов, составляющих химическое соединение, кристаллическая решетка с правильным упорядоченным расположением атомов; • Ярко выраженные индивидуальные свойства; • Постоянство температуры кристаллизации, как у чистых компонентов 8
Сплавы химические соединения В сплавах возможно образование фаз постоянного состава, соотношение элементов в которых подчиняется правилу валентности. Такие сплавы называются химическими соединениями. В сплавах существуют химические соединения переменного состава, не соответствующие правилу валентности, так называемые промежуточные фазы. Сплавы химические соединения образуются между элементами, значительно различающимися по строению и свойствам, если сила взаимодействия между разнородными атомами больше, чем между однородными. Особенности этих сплавов: • Постоянство состава, то есть сплав образуется при определенном соотношении компонентов, химическое соединение обозначается An. Bm; • Образуется специфическая, отличающаяся от решеток элементов, составляющих химическое соединение, кристаллическая решетка с правильным упорядоченным расположением атомов; • Ярко выраженные индивидуальные свойства; • Постоянство температуры кристаллизации, как у чистых компонентов 8
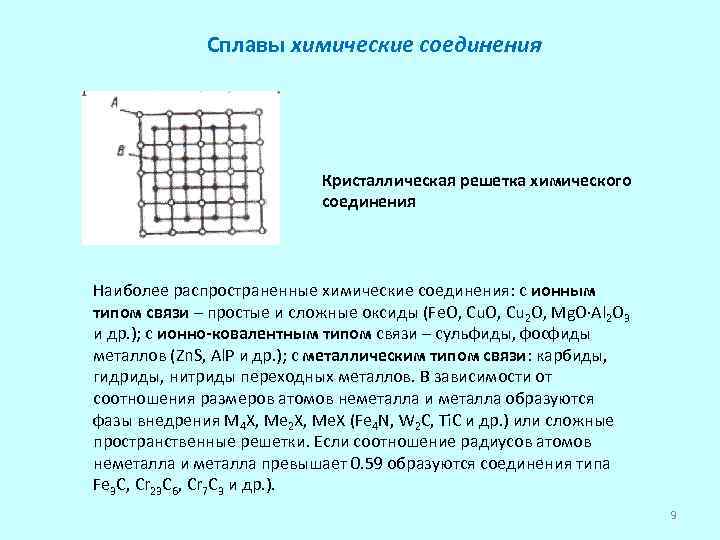 Сплавы химические соединения Кристаллическая решетка химического соединения Наиболее распространенные химические соединения: с ионным типом связи – простые и сложные оксиды (Fe. O, Cu 2 O, Mg. O Al 2 O 3 и др. ); с ионно-ковалентным типом связи – сульфиды, фосфиды металлов (Zn. S, Al. P и др. ); с металлическим типом связи: карбиды, гидриды, нитриды переходных металлов. В зависимости от соотношения размеров атомов неметалла и металла образуются фазы внедрения M 4 X, Me 2 X, Me. X (Fe 4 N, W 2 C, Ti. C и др. ) или сложные пространственные решетки. Если соотношение радиусов атомов неметалла и металла превышает 0. 59 образуются соединения типа Fe 3 C, Cr 23 C 6, Cr 7 C 3 и др. ). 9
Сплавы химические соединения Кристаллическая решетка химического соединения Наиболее распространенные химические соединения: с ионным типом связи – простые и сложные оксиды (Fe. O, Cu 2 O, Mg. O Al 2 O 3 и др. ); с ионно-ковалентным типом связи – сульфиды, фосфиды металлов (Zn. S, Al. P и др. ); с металлическим типом связи: карбиды, гидриды, нитриды переходных металлов. В зависимости от соотношения размеров атомов неметалла и металла образуются фазы внедрения M 4 X, Me 2 X, Me. X (Fe 4 N, W 2 C, Ti. C и др. ) или сложные пространственные решетки. Если соотношение радиусов атомов неметалла и металла превышает 0. 59 образуются соединения типа Fe 3 C, Cr 23 C 6, Cr 7 C 3 и др. ). 9
 Сплавы твердые растворы – это фаза, состоящая из двух или более компонентов, один из которых, сохраняя кристаллическую решетку, является растворителем, а другой (или другие) распределяются в решетке растворителя, не изменяя ее типа. Это кристаллические вещества. Характерная особенность твердых сплавов – наличие в их кристаллической решетке разнородных атомов, при сохранении типа решетки растворителя. Схема микроструктуры твердого раствора 10
Сплавы твердые растворы – это фаза, состоящая из двух или более компонентов, один из которых, сохраняя кристаллическую решетку, является растворителем, а другой (или другие) распределяются в решетке растворителя, не изменяя ее типа. Это кристаллические вещества. Характерная особенность твердых сплавов – наличие в их кристаллической решетке разнородных атомов, при сохранении типа решетки растворителя. Схема микроструктуры твердого раствора 10
 Классификация сплавов твердых растворов По степеням растворимости компонентов различают: - с неограниченной растворимостью компонентов; - с ограниченной растворимостью компонентов. При неограниченной растворимости компонентов кристаллическая решетка компонента растворителя по мере увеличения концентрации растворенного компонента плавно переходит в кристаллическую решетку растворенного компонента. Для образования растворов с неограниченной растворимостью компонентов необходимы: • Изоморфность (однотипность) кристаллических решеток компонентов; • Близость атомных радиусов компонентов, которые не должны отличаться более чем на 8 -13%; • Близость физико-химических свойств подобных по строению валентных оболочек атомов. Примерами таких сплавов являются сплавы Cu – Au, Cu – Ni, Ge – Si, Ag – Au, Mo – V. При ограниченной растворимости компонентов возможна концентрация растворенного вещества до определенного предела. При дальнейшем увеличении концентрации однородный твердый раствор распадается с образованием двухфазной смеси. 11
Классификация сплавов твердых растворов По степеням растворимости компонентов различают: - с неограниченной растворимостью компонентов; - с ограниченной растворимостью компонентов. При неограниченной растворимости компонентов кристаллическая решетка компонента растворителя по мере увеличения концентрации растворенного компонента плавно переходит в кристаллическую решетку растворенного компонента. Для образования растворов с неограниченной растворимостью компонентов необходимы: • Изоморфность (однотипность) кристаллических решеток компонентов; • Близость атомных радиусов компонентов, которые не должны отличаться более чем на 8 -13%; • Близость физико-химических свойств подобных по строению валентных оболочек атомов. Примерами таких сплавов являются сплавы Cu – Au, Cu – Ni, Ge – Si, Ag – Au, Mo – V. При ограниченной растворимости компонентов возможна концентрация растворенного вещества до определенного предела. При дальнейшем увеличении концентрации однородный твердый раствор распадается с образованием двухфазной смеси. 11
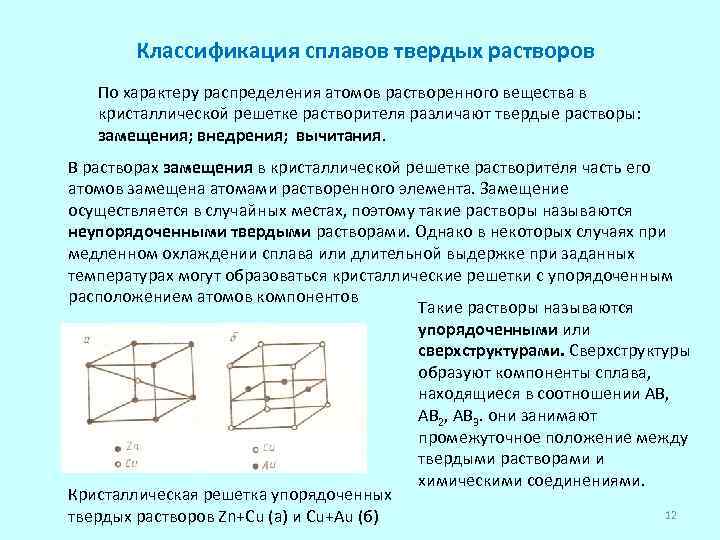 Классификация сплавов твердых растворов По характеру распределения атомов растворенного вещества в кристаллической решетке растворителя различают твердые растворы: замещения; внедрения; вычитания. В растворах замещения в кристаллической решетке растворителя часть его атомов замещена атомами растворенного элемента. Замещение осуществляется в случайных местах, поэтому такие растворы называются неупорядоченными твердыми растворами. Однако в некоторых случаях при медленном охлаждении сплава или длительной выдержке при заданных температурах могут образоваться кристаллические решетки с упорядоченным расположением атомов компонентов Такие растворы называются упорядоченными или сверхструктурами. Сверхструктуры образуют компоненты сплава, находящиеся в соотношении АВ, АВ 2, АВ 3. они занимают промежуточное положение между твердыми растворами и химическими соединениями. Кристаллическая решетка упорядоченных 12 твердых растворов Zn+Cu (a) и Cu+Au (б)
Классификация сплавов твердых растворов По характеру распределения атомов растворенного вещества в кристаллической решетке растворителя различают твердые растворы: замещения; внедрения; вычитания. В растворах замещения в кристаллической решетке растворителя часть его атомов замещена атомами растворенного элемента. Замещение осуществляется в случайных местах, поэтому такие растворы называются неупорядоченными твердыми растворами. Однако в некоторых случаях при медленном охлаждении сплава или длительной выдержке при заданных температурах могут образоваться кристаллические решетки с упорядоченным расположением атомов компонентов Такие растворы называются упорядоченными или сверхструктурами. Сверхструктуры образуют компоненты сплава, находящиеся в соотношении АВ, АВ 2, АВ 3. они занимают промежуточное положение между твердыми растворами и химическими соединениями. Кристаллическая решетка упорядоченных 12 твердых растворов Zn+Cu (a) и Cu+Au (б)
 Классификация сплавов твердых растворов При образовании растворов замещения периоды решетки изменяются в зависимости от разности атомных диаметров растворенного элемента и растворителя. Если атом растворенного элемента больше атома растворителя, то элементарные ячейки увеличиваются. Если меньше – сокращаются. В первом приближении это изменение пропорционально концентрации растворенного компонента. Изменение параметров решетки при образовании твердых растворов – важный момент, определяющий изменение свойств. Уменьшение параметра ведет к большему упрочнению, чем его увеличение. Образование твердых растворов приводит к увеличению их электрического сопротивления, снижает пластичность и вязкость. 13
Классификация сплавов твердых растворов При образовании растворов замещения периоды решетки изменяются в зависимости от разности атомных диаметров растворенного элемента и растворителя. Если атом растворенного элемента больше атома растворителя, то элементарные ячейки увеличиваются. Если меньше – сокращаются. В первом приближении это изменение пропорционально концентрации растворенного компонента. Изменение параметров решетки при образовании твердых растворов – важный момент, определяющий изменение свойств. Уменьшение параметра ведет к большему упрочнению, чем его увеличение. Образование твердых растворов приводит к увеличению их электрического сопротивления, снижает пластичность и вязкость. 13
 Классификация сплавов твердых растворов Твердые растворы внедрения образуются внедрением атомов растворенного компонента в междоузлия кристаллической решетки растворителя Схемы твердых растворов внедрения (а) и замещения (б) Образование таких растворов возможно, если атомы растворенного элемента имеют малые размеры. Такими являются элементы, находящиеся в начале периодической системы – углерод, водород, азот, бор. Размеры атомов превышают размеры межатомных промежутков в кристаллической решетке металла, это вызывает искажение решетки и в ней возникают напряжения. Концентрация таких растворов не превышает 2 -2. 5 %. Типичным примером раствора такого типа является твердый раствор углерода в Fe и Fe. В Fe углерод имеет незначительную растворимость – до 0. 02%, в Fe - до 2. 14%. 14
Классификация сплавов твердых растворов Твердые растворы внедрения образуются внедрением атомов растворенного компонента в междоузлия кристаллической решетки растворителя Схемы твердых растворов внедрения (а) и замещения (б) Образование таких растворов возможно, если атомы растворенного элемента имеют малые размеры. Такими являются элементы, находящиеся в начале периодической системы – углерод, водород, азот, бор. Размеры атомов превышают размеры межатомных промежутков в кристаллической решетке металла, это вызывает искажение решетки и в ней возникают напряжения. Концентрация таких растворов не превышает 2 -2. 5 %. Типичным примером раствора такого типа является твердый раствор углерода в Fe и Fe. В Fe углерод имеет незначительную растворимость – до 0. 02%, в Fe - до 2. 14%. 14
 Классификация сплавов твердых растворов Твердые растворы вычитания или растворы с дефектной структурой образуются на базе химических соединений, при этом возможна не только замена одних атомов в узлах кристаллической решетки другими, но и образование пустых, не занятых атомами узлов в решетке. К химическому соединению добавляют один из входящих в формулу элементов, его атомы занимают нормальное положение в решетке соединения, а места атомов другого элемента остаются незанятыми 15
Классификация сплавов твердых растворов Твердые растворы вычитания или растворы с дефектной структурой образуются на базе химических соединений, при этом возможна не только замена одних атомов в узлах кристаллической решетки другими, но и образование пустых, не занятых атомами узлов в решетке. К химическому соединению добавляют один из входящих в формулу элементов, его атомы занимают нормальное положение в решетке соединения, а места атомов другого элемента остаются незанятыми 15
 Кристаллизация сплавов подчиняется тем же закономерностям, что и кристаллизация чистых металлов. Необходимым условием является стремление системы в состояние с минимумом свободной энергии. Равновесное состояние достигается при небольших скоростях охлаждения или достаточно длительном нагреве сплава. Реальные сплавы находятся, как правило, в неравновесном (метастабильном) состоянии. Основным отличием является большая роль диффузионных процессов между жидкостью и кристаллизующейся фазой. Эти процессы необходимы для перераспределения разнородных атомов равномерно распределенных в жидкой фазе. В сплавах в твердых состояниях имеют место процессы перекристаллизации, обусловленные аллотропическими превращениями компонентов сплава, распадом твердых растворов, выделением из твердых растворов вторичных фаз, когда растворимость компонентов в твердом состоянии меняется с изменением температуры. Эти превращения называются фазовыми превращениями в твердом состоянии. При перекристаллизации в твердом состоянии образуются центры кристаллизации и происходит их рост. Обычно центры кристаллизации возникают по границам зерен старой фазы, где решетка имеет наиболее дефектное строение, и где имеются примеси, которые могут стать центрами новых кристаллов. У старой и новой фазы в течение некоторого времени имеются общие плоскости. Такая связь решеток называется когерентной связью. В случае различия строения старой и новой фаз превращение протекает с образованием промежуточных фаз. Нарушение когерентности и обособление кристаллов наступает когда они приобретут определенные размеры. Процессы кристаллизации сплавов описываются диаграммами состояния. 16
Кристаллизация сплавов подчиняется тем же закономерностям, что и кристаллизация чистых металлов. Необходимым условием является стремление системы в состояние с минимумом свободной энергии. Равновесное состояние достигается при небольших скоростях охлаждения или достаточно длительном нагреве сплава. Реальные сплавы находятся, как правило, в неравновесном (метастабильном) состоянии. Основным отличием является большая роль диффузионных процессов между жидкостью и кристаллизующейся фазой. Эти процессы необходимы для перераспределения разнородных атомов равномерно распределенных в жидкой фазе. В сплавах в твердых состояниях имеют место процессы перекристаллизации, обусловленные аллотропическими превращениями компонентов сплава, распадом твердых растворов, выделением из твердых растворов вторичных фаз, когда растворимость компонентов в твердом состоянии меняется с изменением температуры. Эти превращения называются фазовыми превращениями в твердом состоянии. При перекристаллизации в твердом состоянии образуются центры кристаллизации и происходит их рост. Обычно центры кристаллизации возникают по границам зерен старой фазы, где решетка имеет наиболее дефектное строение, и где имеются примеси, которые могут стать центрами новых кристаллов. У старой и новой фазы в течение некоторого времени имеются общие плоскости. Такая связь решеток называется когерентной связью. В случае различия строения старой и новой фаз превращение протекает с образованием промежуточных фаз. Нарушение когерентности и обособление кристаллов наступает когда они приобретут определенные размеры. Процессы кристаллизации сплавов описываются диаграммами состояния. 16
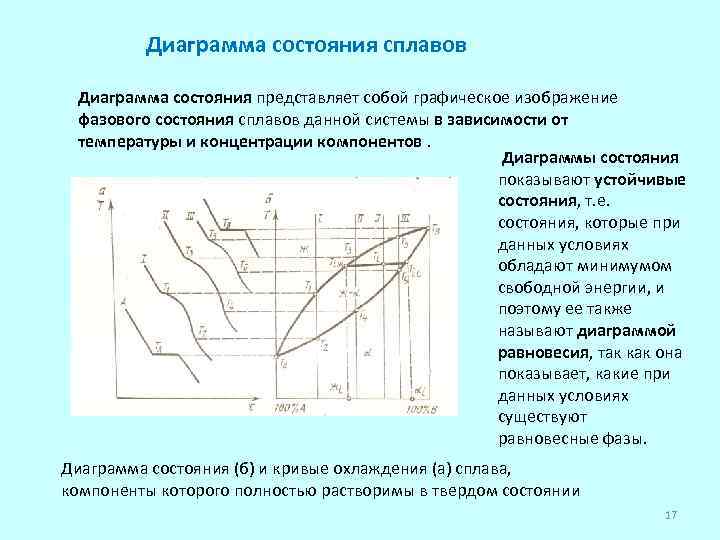 Диаграмма состояния сплавов Диаграмма состояния представляет собой графическое изображение фазового состояния сплавов данной системы в зависимости от температуры и концентрации компонентов. Диаграммы состояния показывают устойчивые состояния, т. е. состояния, которые при данных условиях обладают минимумом свободной энергии, и поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого полностью растворимы в твердом состоянии 17
Диаграмма состояния сплавов Диаграмма состояния представляет собой графическое изображение фазового состояния сплавов данной системы в зависимости от температуры и концентрации компонентов. Диаграммы состояния показывают устойчивые состояния, т. е. состояния, которые при данных условиях обладают минимумом свободной энергии, и поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы. Диаграмма состояния (б) и кривые охлаждения (а) сплава, компоненты которого полностью растворимы в твердом состоянии 17
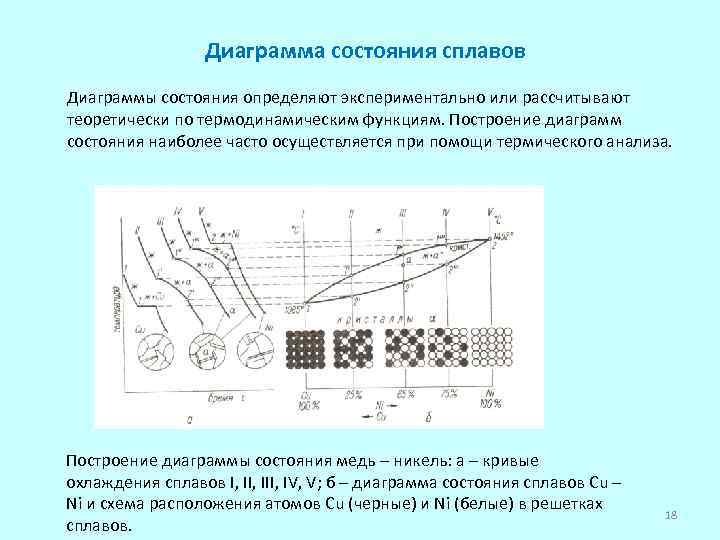 Диаграмма состояния сплавов Диаграммы состояния определяют экспериментально или рассчитывают теоретически по термодинамическим функциям. Построение диаграмм состояния наиболее часто осуществляется при помощи термического анализа. Построение диаграммы состояния медь – никель: а – кривые охлаждения сплавов I, III, IV, V; б – диаграмма состояния сплавов Cu – Ni и схема расположения атомов Cu (черные) и Ni (белые) в решетках сплавов. 18
Диаграмма состояния сплавов Диаграммы состояния определяют экспериментально или рассчитывают теоретически по термодинамическим функциям. Построение диаграмм состояния наиболее часто осуществляется при помощи термического анализа. Построение диаграммы состояния медь – никель: а – кривые охлаждения сплавов I, III, IV, V; б – диаграмма состояния сплавов Cu – Ni и схема расположения атомов Cu (черные) и Ni (белые) в решетках сплавов. 18
 Диаграмма состояния сплавов Для экспериментального построения диаграммы состояний сплавов, образованных компонентами А и В, необходимо изготовить серию сплавов, содержащих различные количества компонентов А и В. Для каждого такого сплава экспериментально строят кривые охлаждения и определяют по ним критические точки, т. е. температуры фазовых превращений. Некоторые критические точки имеют названия, например, точки, отвечающие началу кристаллизации, называют точками ликвидус, а концу кристаллизации – точками солидус. По кривым охлаждения строят диаграмму состава в координатах: по оси абсцисс – концентрация компонентов, по оси ординат – температура. Шкала концентраций показывает содержание компонента В. Левая крайняя точка на оси концентраций соответствует 100% содержанию компонента А. Процентное содержание второго компонента откладывается по этой оси слева направо. Правая крайняя точка соответствует 100 % содержанию второго компонента В. 19
Диаграмма состояния сплавов Для экспериментального построения диаграммы состояний сплавов, образованных компонентами А и В, необходимо изготовить серию сплавов, содержащих различные количества компонентов А и В. Для каждого такого сплава экспериментально строят кривые охлаждения и определяют по ним критические точки, т. е. температуры фазовых превращений. Некоторые критические точки имеют названия, например, точки, отвечающие началу кристаллизации, называют точками ликвидус, а концу кристаллизации – точками солидус. По кривым охлаждения строят диаграмму состава в координатах: по оси абсцисс – концентрация компонентов, по оси ординат – температура. Шкала концентраций показывает содержание компонента В. Левая крайняя точка на оси концентраций соответствует 100% содержанию компонента А. Процентное содержание второго компонента откладывается по этой оси слева направо. Правая крайняя точка соответствует 100 % содержанию второго компонента В. 19


