Материаловедение Лекция 2













 Материаловедение Лекция 2
Материаловедение Лекция 2
 Литература • Фетисов Г. П. , Карпман М. Г. , Матюнин В. М. и др. Материаловедение и технология конструкционных материалов. - М. : Металлургия, 2000, 2001 г. г. • 2. Абраимов Н. В. , Елисеев В. С. , Крымов В. В. Авиационное материаловедение и технология обработки металлов /Под ред. Н. В. Абраимова. - М. : Высшая школа, 1998. 444 с. • 3. Лахтин Ю. М. Металловедение и термическая обработка. – М. : Металлургия, 1993. • 4. Колачев Б. А. , Ливанов В. А. , Елагин В. И. Металловедение и термическая обработка цветных металлов и сплавов. - М. : МИСИС, 1999. • 5. Арзамасов Б. Н. Материаловедение : учеб. для вузов / Б. Н. Арзамасов [и др. ]. – М. : Изд-во МГТУ им Н. Э. Баумана, 2005. – 646 с. • 6. Адаскин, А. М. Материаловедение / А. М. Адаскин. – М. : Высш. • шк. , 2005. – 456 с. • 7. Шишкин, А. В. Материаловедение. Технология конструкционных • материалов : учеб. для вузов / А. В. Шишкин. – Новосибирск : Изд-во НГТУ, • 2004. • 8. Гусев А. И. , Ремпель А. А. Нанокристаллические материалы. - М. : ФИЗМАТЛИТ, 2000. - 224 с. • 9. Андриевский Р. А. , Рагуля А. В. Наноструктурные материалы. - М. : Издательский центр «Академия» , 2005. - 190 с. • 10. Помогайло А. Д. , Розенберг А. С. , Уфлянд И. Е. Наночастицы металлов в полимерах. Москва, Химия, с. 672, 2000 • Астафьева, Е. А. Лабораторный практикум по материаловедению / Е. А. Астафьева, А. М. Токмин, Л. А. Быконя. – Красноярск : ИПЦ КГТУ, 2002. – 110 с. • Темных, В. И. Теория и технология термической обработки металлов и сплавов / В. И. Темных, Л. А. Быконя. – Красноярск: ИПЦ КГТУ, 2000. – 176 с. • 3. Материаловедение и технология металлов / под ред. В. В. Атрощенко. – М. : Высш. шк. , 2000. – 625 с. 2
Литература • Фетисов Г. П. , Карпман М. Г. , Матюнин В. М. и др. Материаловедение и технология конструкционных материалов. - М. : Металлургия, 2000, 2001 г. г. • 2. Абраимов Н. В. , Елисеев В. С. , Крымов В. В. Авиационное материаловедение и технология обработки металлов /Под ред. Н. В. Абраимова. - М. : Высшая школа, 1998. 444 с. • 3. Лахтин Ю. М. Металловедение и термическая обработка. – М. : Металлургия, 1993. • 4. Колачев Б. А. , Ливанов В. А. , Елагин В. И. Металловедение и термическая обработка цветных металлов и сплавов. - М. : МИСИС, 1999. • 5. Арзамасов Б. Н. Материаловедение : учеб. для вузов / Б. Н. Арзамасов [и др. ]. – М. : Изд-во МГТУ им Н. Э. Баумана, 2005. – 646 с. • 6. Адаскин, А. М. Материаловедение / А. М. Адаскин. – М. : Высш. • шк. , 2005. – 456 с. • 7. Шишкин, А. В. Материаловедение. Технология конструкционных • материалов : учеб. для вузов / А. В. Шишкин. – Новосибирск : Изд-во НГТУ, • 2004. • 8. Гусев А. И. , Ремпель А. А. Нанокристаллические материалы. - М. : ФИЗМАТЛИТ, 2000. - 224 с. • 9. Андриевский Р. А. , Рагуля А. В. Наноструктурные материалы. - М. : Издательский центр «Академия» , 2005. - 190 с. • 10. Помогайло А. Д. , Розенберг А. С. , Уфлянд И. Е. Наночастицы металлов в полимерах. Москва, Химия, с. 672, 2000 • Астафьева, Е. А. Лабораторный практикум по материаловедению / Е. А. Астафьева, А. М. Токмин, Л. А. Быконя. – Красноярск : ИПЦ КГТУ, 2002. – 110 с. • Темных, В. И. Теория и технология термической обработки металлов и сплавов / В. И. Темных, Л. А. Быконя. – Красноярск: ИПЦ КГТУ, 2000. – 176 с. • 3. Материаловедение и технология металлов / под ред. В. В. Атрощенко. – М. : Высш. шк. , 2000. – 625 с. 2
 Содержание лекции • Строение реальных металлов • Дефекты кристаллического строения • Кристаллизация 3
Содержание лекции • Строение реальных металлов • Дефекты кристаллического строения • Кристаллизация 3
 Строение реальных кристаллов и дефекты кристаллической решетки Нарушая правильность строения кристаллов, дефекты термодинамически неустойчивы. Однако они не исчезают из-за отсутствия необходимых кинетических условий. 3 4
Строение реальных кристаллов и дефекты кристаллической решетки Нарушая правильность строения кристаллов, дефекты термодинамически неустойчивы. Однако они не исчезают из-за отсутствия необходимых кинетических условий. 3 4
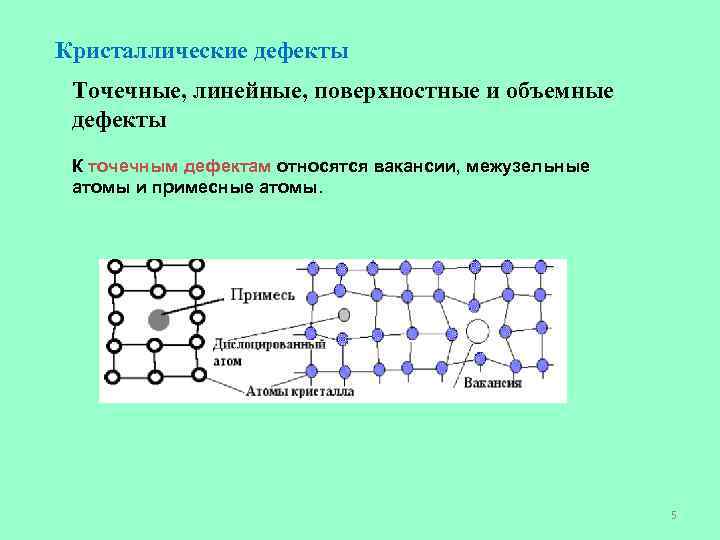
 Кристаллические дефекты Точечные, линейные, поверхностные и объемные дефекты К точечным дефектам относятся вакансии, межузельные атомы и примесные атомы. 5
Кристаллические дефекты Точечные, линейные, поверхностные и объемные дефекты К точечным дефектам относятся вакансии, межузельные атомы и примесные атомы. 5
 Схема искажения кристаллической решетки около точечных дефектов Вакансией называется пустой узел кристаллической решетки; межузельным атомом называется атом, перемещенный из узла в позицию между узлами; Примесные атомы размещаются либо в узлах решетки, либо между узлами и образуют соответственно твердые растворы замещения или внедрения. Вакансии и межузельные атомы образуются при любой температуре выше абсолютного нуля из-за тепловых колебаний атомов. На образование вакансий требуется энергия 1 -2 э. В, а на образование межузельного атома 5 -6 э. В. 6
Схема искажения кристаллической решетки около точечных дефектов Вакансией называется пустой узел кристаллической решетки; межузельным атомом называется атом, перемещенный из узла в позицию между узлами; Примесные атомы размещаются либо в узлах решетки, либо между узлами и образуют соответственно твердые растворы замещения или внедрения. Вакансии и межузельные атомы образуются при любой температуре выше абсолютного нуля из-за тепловых колебаний атомов. На образование вакансий требуется энергия 1 -2 э. В, а на образование межузельного атома 5 -6 э. В. 6
 Например, у меди при комнатной температуре имеется 10 -13 % вакансий, а вблизи т. пл. (1356 К) уже 0. 01% (1 вакансия на 104 атомов), межузельных атомов в 1020 раз меньше) В ионных кристаллах точечные дефекты возникают парами. Образования вакансий вследствие удаление ионов одного знака приводит к появлению в кристалле заряда противоположного знака. Нейтральность сохраняется, если ионы не удаляются из кристалла. В результате возникает пара вакансия – межузельная частица – дефекты Френкеля. Кристалл остается нейтральным и в том случае, когда при одинаковой валентности ионов анионные и катионные вакансии образуются в равных количествах – дефекты Шотки. 7
Например, у меди при комнатной температуре имеется 10 -13 % вакансий, а вблизи т. пл. (1356 К) уже 0. 01% (1 вакансия на 104 атомов), межузельных атомов в 1020 раз меньше) В ионных кристаллах точечные дефекты возникают парами. Образования вакансий вследствие удаление ионов одного знака приводит к появлению в кристалле заряда противоположного знака. Нейтральность сохраняется, если ионы не удаляются из кристалла. В результате возникает пара вакансия – межузельная частица – дефекты Френкеля. Кристалл остается нейтральным и в том случае, когда при одинаковой валентности ионов анионные и катионные вакансии образуются в равных количествах – дефекты Шотки. 7
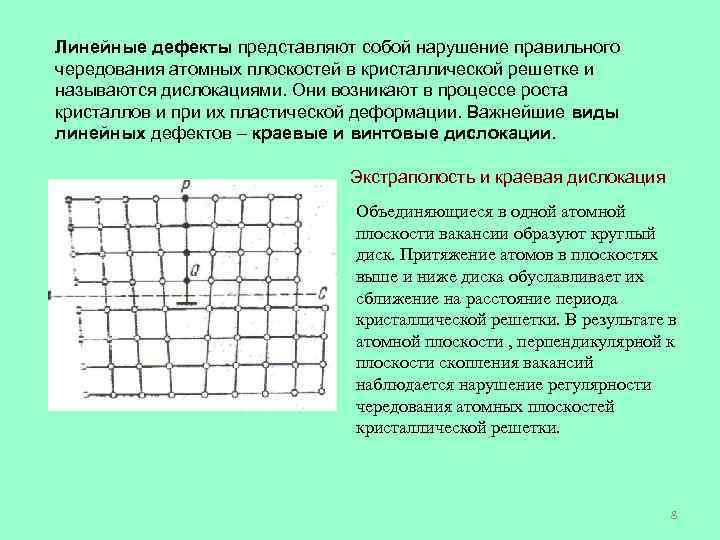
 Линейные дефекты представляют собой нарушение правильного чередования атомных плоскостей в кристаллической решетке и называются дислокациями. Они возникают в процессе роста кристаллов и при их пластической деформации. Важнейшие виды линейных дефектов – краевые и винтовые дислокации. Экстраполость и краевая дислокация Объединяющиеся в одной атомной плоскости вакансии образуют круглый диск. Притяжение атомов в плоскостях выше и ниже диска обуславливает их сближение на расстояние периода кристаллической решетки. В результате в атомной плоскости , перпендикулярной к плоскости скопления вакансий наблюдается нарушение регулярности чередования атомных плоскостей кристаллической решетки. 8
Линейные дефекты представляют собой нарушение правильного чередования атомных плоскостей в кристаллической решетке и называются дислокациями. Они возникают в процессе роста кристаллов и при их пластической деформации. Важнейшие виды линейных дефектов – краевые и винтовые дислокации. Экстраполость и краевая дислокация Объединяющиеся в одной атомной плоскости вакансии образуют круглый диск. Притяжение атомов в плоскостях выше и ниже диска обуславливает их сближение на расстояние периода кристаллической решетки. В результате в атомной плоскости , перпендикулярной к плоскости скопления вакансий наблюдается нарушение регулярности чередования атомных плоскостей кристаллической решетки. 8
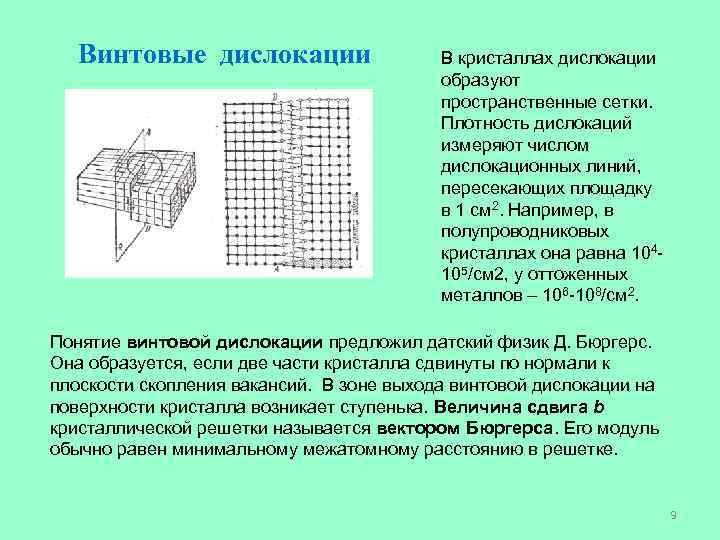
 Винтовые дислокации В кристаллах дислокации образуют пространственные сетки. Плотность дислокаций измеряют числом дислокационных линий, пересекающих площадку в 1 см 2. Например, в полупроводниковых кристаллах она равна 104 - 105/см 2, у оттоженных металлов – 106 -108/см 2. Понятие винтовой дислокации предложил датский физик Д. Бюргерс. Она образуется, если две части кристалла сдвинуты по нормали к плоскости скопления вакансий. В зоне выхода винтовой дислокации на поверхности кристалла возникает ступенька. Величина сдвига b кристаллической решетки называется вектором Бюргерса. Его модуль обычно равен минимальному межатомному расстоянию в решетке. 9
Винтовые дислокации В кристаллах дислокации образуют пространственные сетки. Плотность дислокаций измеряют числом дислокационных линий, пересекающих площадку в 1 см 2. Например, в полупроводниковых кристаллах она равна 104 - 105/см 2, у оттоженных металлов – 106 -108/см 2. Понятие винтовой дислокации предложил датский физик Д. Бюргерс. Она образуется, если две части кристалла сдвинуты по нормали к плоскости скопления вакансий. В зоне выхода винтовой дислокации на поверхности кристалла возникает ступенька. Величина сдвига b кристаллической решетки называется вектором Бюргерса. Его модуль обычно равен минимальному межатомному расстоянию в решетке. 9
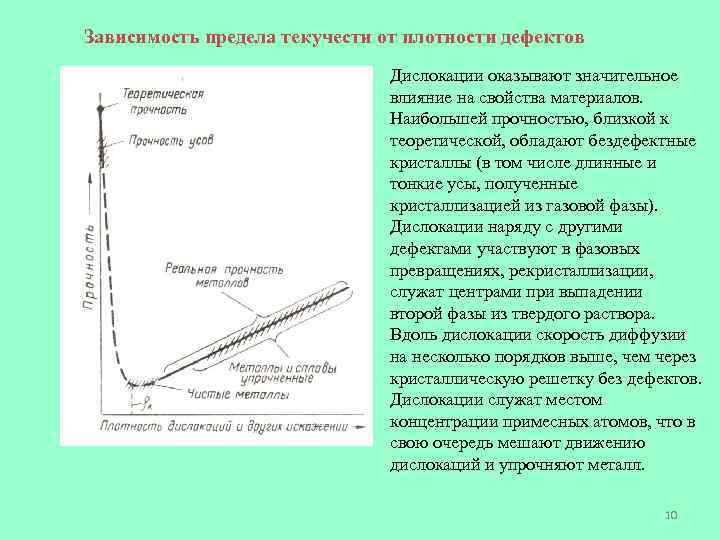
 Зависимость предела текучести от плотности дефектов Дислокации оказывают значительное влияние на свойства материалов. Наибольшей прочностью, близкой к теоретической, обладают бездефектные кристаллы (в том числе длинные и тонкие усы, полученные кристаллизацией из газовой фазы). Дислокации наряду с другими дефектами участвуют в фазовых превращениях, рекристаллизации, служат центрами при выпадении второй фазы из твердого раствора. Вдоль дислокации скорость диффузии на несколько порядков выше, чем через кристаллическую решетку без дефектов. Дислокации служат местом концентрации примесных атомов, что в свою очередь мешают движению дислокаций и упрочняют металл. 10
Зависимость предела текучести от плотности дефектов Дислокации оказывают значительное влияние на свойства материалов. Наибольшей прочностью, близкой к теоретической, обладают бездефектные кристаллы (в том числе длинные и тонкие усы, полученные кристаллизацией из газовой фазы). Дислокации наряду с другими дефектами участвуют в фазовых превращениях, рекристаллизации, служат центрами при выпадении второй фазы из твердого раствора. Вдоль дислокации скорость диффузии на несколько порядков выше, чем через кристаллическую решетку без дефектов. Дислокации служат местом концентрации примесных атомов, что в свою очередь мешают движению дислокаций и упрочняют металл. 10
 Кристаллизация Первичная кристаллизация. Вторичная кристаллизация. Форма кристаллов и строение слитка. Переход металла из жидкого или парообразного состояния в твердое с образованием кристаллической структуры называется первичной кристаллизацией. Образование новых кристаллов в твердом кристаллическом веществе называется вторичной кристаллизацией. Процесс кристаллизации состоит из двух одновременно идущих процессов: зарождения и роста кристаллов. Самопроизвольная первичная кристаллизация обусловлена стремлением вещества иметь более устойчивое состояние, характеризующееся уменьшением термодинамического потенциала Z. Энергетическое состояние вещества при равновесии характеризуется минимальным значением Z : Z= H – TS 11
Кристаллизация Первичная кристаллизация. Вторичная кристаллизация. Форма кристаллов и строение слитка. Переход металла из жидкого или парообразного состояния в твердое с образованием кристаллической структуры называется первичной кристаллизацией. Образование новых кристаллов в твердом кристаллическом веществе называется вторичной кристаллизацией. Процесс кристаллизации состоит из двух одновременно идущих процессов: зарождения и роста кристаллов. Самопроизвольная первичная кристаллизация обусловлена стремлением вещества иметь более устойчивое состояние, характеризующееся уменьшением термодинамического потенциала Z. Энергетическое состояние вещества при равновесии характеризуется минимальным значением Z : Z= H – TS 11
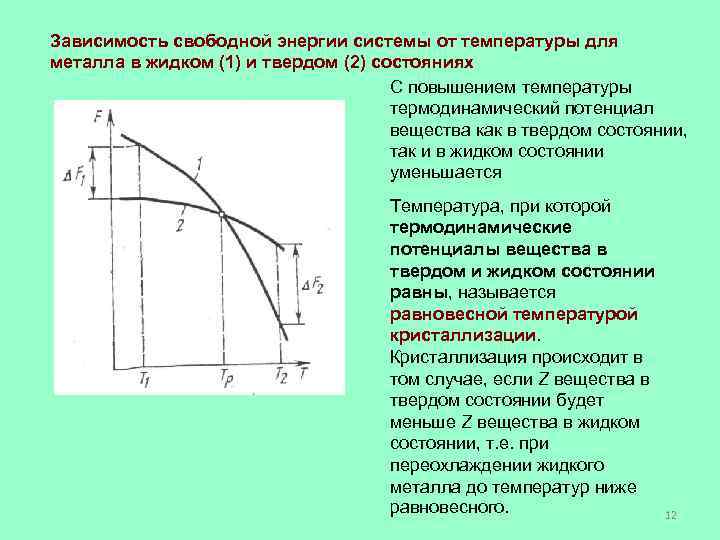
 Зависимость свободной энергии системы от температуры для металла в жидком (1) и твердом (2) состояниях С повышением температуры термодинамический потенциал вещества как в твердом состоянии, так и в жидком состоянии уменьшается Температура, при которой термодинамические потенциалы вещества в твердом и жидком состоянии равны, называется равновесной температурой кристаллизации. Кристаллизация происходит в том случае, если Z вещества в твердом состоянии будет меньше Z вещества в жидком состоянии, т. е. при переохлаждении жидкого металла до температур ниже равновесного. 12
Зависимость свободной энергии системы от температуры для металла в жидком (1) и твердом (2) состояниях С повышением температуры термодинамический потенциал вещества как в твердом состоянии, так и в жидком состоянии уменьшается Температура, при которой термодинамические потенциалы вещества в твердом и жидком состоянии равны, называется равновесной температурой кристаллизации. Кристаллизация происходит в том случае, если Z вещества в твердом состоянии будет меньше Z вещества в жидком состоянии, т. е. при переохлаждении жидкого металла до температур ниже равновесного. 12
 Характерный вид кривых охлаждения (1) и нагрева (2) чистого металла Плавление, процесс обратный кристаллизации, происходит при перегреве выше равновесной температуры. При кристаллизации выделяется теплота. Когда кристаллизуется чистый элемент, отвод теплоты, происходящей вследствие охлаждения, компенсируется теплотой кристаллизации. Поэтому на кривой охлаждения в координатах температура – время процессу кристаллизации соответствует горизонтальный участок. Разница между равновесной (Тs) и реальной (Тn) температурой кристаллизации называется степенью переохлаждения ( Т). Степень переохлаждения увеличивается с ростом скорости охлаждения. 13
Характерный вид кривых охлаждения (1) и нагрева (2) чистого металла Плавление, процесс обратный кристаллизации, происходит при перегреве выше равновесной температуры. При кристаллизации выделяется теплота. Когда кристаллизуется чистый элемент, отвод теплоты, происходящей вследствие охлаждения, компенсируется теплотой кристаллизации. Поэтому на кривой охлаждения в координатах температура – время процессу кристаллизации соответствует горизонтальный участок. Разница между равновесной (Тs) и реальной (Тn) температурой кристаллизации называется степенью переохлаждения ( Т). Степень переохлаждения увеличивается с ростом скорости охлаждения. 13
 В жидком состоянии атомы вещества перемещаются беспорядочно. В то же время в жидкости имеются группировки атомов, в которых расположение атомов во многом аналогично их расположению в решетке кристалла. При переохлаждении жидкости некоторые из них, наиболее крупные, становятся устойчивыми и способными к росту. Эти устойчивые группировки называются центрами кристаллизации или зародышами. Для данной степени переохлаждения имеется некоторый зародыш критического размера rкр. Все зародыши большего размера будут центрами кристаллизации, а зародыши меньшего размера окажутся неустойчивыми и вновь рассасываются в жидкости. Зарождение центра критического размера требует определенной энергии. Эта энергия передается от атомов жидкости, имеющих избыточную энергии, сверх некоторой средней из-за флуктуации энергии. Критический размер связан с термодинамическими параметрами: rкр = 2 / f, где - удельное (на см 2) поверхностное натяжение на границе жидкость – кристалл; f – удельное (на см 2) изменение свободной энергии при переходе жидкости в кристаллическое состояние. 14
В жидком состоянии атомы вещества перемещаются беспорядочно. В то же время в жидкости имеются группировки атомов, в которых расположение атомов во многом аналогично их расположению в решетке кристалла. При переохлаждении жидкости некоторые из них, наиболее крупные, становятся устойчивыми и способными к росту. Эти устойчивые группировки называются центрами кристаллизации или зародышами. Для данной степени переохлаждения имеется некоторый зародыш критического размера rкр. Все зародыши большего размера будут центрами кристаллизации, а зародыши меньшего размера окажутся неустойчивыми и вновь рассасываются в жидкости. Зарождение центра критического размера требует определенной энергии. Эта энергия передается от атомов жидкости, имеющих избыточную энергии, сверх некоторой средней из-за флуктуации энергии. Критический размер связан с термодинамическими параметрами: rкр = 2 / f, где - удельное (на см 2) поверхностное натяжение на границе жидкость – кристалл; f – удельное (на см 2) изменение свободной энергии при переходе жидкости в кристаллическое состояние. 14
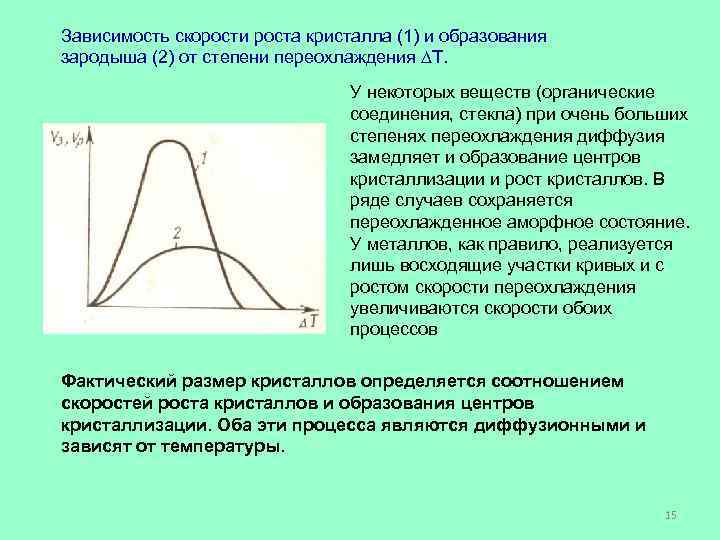
 Зависимость скорости роста кристалла (1) и образования зародыша (2) от степени переохлаждения Т. У некоторых веществ (органические соединения, стекла) при очень больших степенях переохлаждения диффузия замедляет и образование центров кристаллизации и рост кристаллов. В ряде случаев сохраняется переохлажденное аморфное состояние. У металлов, как правило, реализуется лишь восходящие участки кривых и с ростом скорости переохлаждения увеличиваются скорости обоих процессов Фактический размер кристаллов определяется соотношением скоростей роста кристаллов и образования центров кристаллизации. Оба эти процесса являются диффузионными и зависят от температуры. 15
Зависимость скорости роста кристалла (1) и образования зародыша (2) от степени переохлаждения Т. У некоторых веществ (органические соединения, стекла) при очень больших степенях переохлаждения диффузия замедляет и образование центров кристаллизации и рост кристаллов. В ряде случаев сохраняется переохлажденное аморфное состояние. У металлов, как правило, реализуется лишь восходящие участки кривых и с ростом скорости переохлаждения увеличиваются скорости обоих процессов Фактический размер кристаллов определяется соотношением скоростей роста кристаллов и образования центров кристаллизации. Оба эти процесса являются диффузионными и зависят от температуры. 15
 Форма кристаллов и строение слитков Форма зерен, образующихся при кристаллизации зависит от условий их роста, от скорости и направления отвода тепла и температуры жидкого металла, а также от примесей. Рост зерна происходит по дендритной схеме: Установлено, что наибольшая скорость роста кристаллов наблюдается по таким плоскостям и направлениям решетки, которые имеют наибольшую плотность упаковки атомов. В результате вырастают длинные ветви, которые называют осями первого порядка (I). Затем на этих осях растут ветви второго порядка (II) и т. д. одновременно идет кристаллизация в участках между осями дендритов. 16
Форма кристаллов и строение слитков Форма зерен, образующихся при кристаллизации зависит от условий их роста, от скорости и направления отвода тепла и температуры жидкого металла, а также от примесей. Рост зерна происходит по дендритной схеме: Установлено, что наибольшая скорость роста кристаллов наблюдается по таким плоскостям и направлениям решетки, которые имеют наибольшую плотность упаковки атомов. В результате вырастают длинные ветви, которые называют осями первого порядка (I). Затем на этих осях растут ветви второго порядка (II) и т. д. одновременно идет кристаллизация в участках между осями дендритов. 16
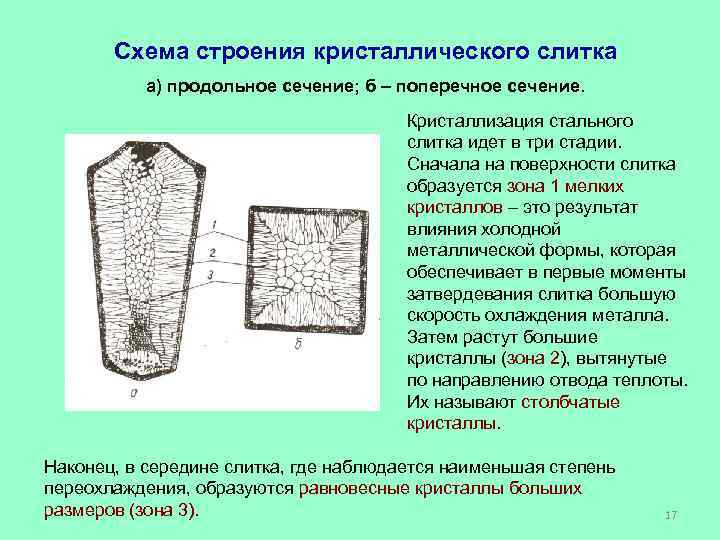
 Схема строения кристаллического слитка а) продольное сечение; б – поперечное сечение. Кристаллизация стального слитка идет в три стадии. Сначала на поверхности слитка образуется зона 1 мелких кристаллов – это результат влияния холодной металлической формы, которая обеспечивает в первые моменты затвердевания слитка большую скорость охлаждения металла. Затем растут большие кристаллы (зона 2), вытянутые по направлению отвода теплоты. Их называют столбчатые кристаллы. Наконец, в середине слитка, где наблюдается наименьшая степень переохлаждения, образуются равновесные кристаллы больших размеров (зона 3). 17
Схема строения кристаллического слитка а) продольное сечение; б – поперечное сечение. Кристаллизация стального слитка идет в три стадии. Сначала на поверхности слитка образуется зона 1 мелких кристаллов – это результат влияния холодной металлической формы, которая обеспечивает в первые моменты затвердевания слитка большую скорость охлаждения металла. Затем растут большие кристаллы (зона 2), вытянутые по направлению отвода теплоты. Их называют столбчатые кристаллы. Наконец, в середине слитка, где наблюдается наименьшая степень переохлаждения, образуются равновесные кристаллы больших размеров (зона 3). 17
 Вторичная кристаллизация Вторичной кристаллизацией называется процесс, в результате которого происходит полная замена одной кристаллической структуры на другую (аллотропное превращение) или частичное изменение структуры (выделение новой фазы из твердого раствора при изменении его концентрации). Обнаружены полиморфные модификации ряда металлов: Co- , Ti- , Zr- , Sn- , Fe- и др. Например, при температуре +18 С происходит превращение белого олова ( -модификация) с тетрагональной кристаллической структурой в серое ( -модификация) с кубической кристаллической структурой. Превращение сопровождается увеличением объема олова на 25%, что связано с уменьшением плотности от 7. 3 г/см 3 для белого олова до 5. 7 г/см 3 серого олова. Превращение сопровождается возникновением внутренних напряжений, металл по ходу теряет монолитность, и оловянный слиток превращается в порошок. В результате дефектных образований серого олова на поверхности белого ( «оловянная чума» ) изделия теряют прочность, пластичность, блеск и т. д. 18
Вторичная кристаллизация Вторичной кристаллизацией называется процесс, в результате которого происходит полная замена одной кристаллической структуры на другую (аллотропное превращение) или частичное изменение структуры (выделение новой фазы из твердого раствора при изменении его концентрации). Обнаружены полиморфные модификации ряда металлов: Co- , Ti- , Zr- , Sn- , Fe- и др. Например, при температуре +18 С происходит превращение белого олова ( -модификация) с тетрагональной кристаллической структурой в серое ( -модификация) с кубической кристаллической структурой. Превращение сопровождается увеличением объема олова на 25%, что связано с уменьшением плотности от 7. 3 г/см 3 для белого олова до 5. 7 г/см 3 серого олова. Превращение сопровождается возникновением внутренних напряжений, металл по ходу теряет монолитность, и оловянный слиток превращается в порошок. В результате дефектных образований серого олова на поверхности белого ( «оловянная чума» ) изделия теряют прочность, пластичность, блеск и т. д. 18
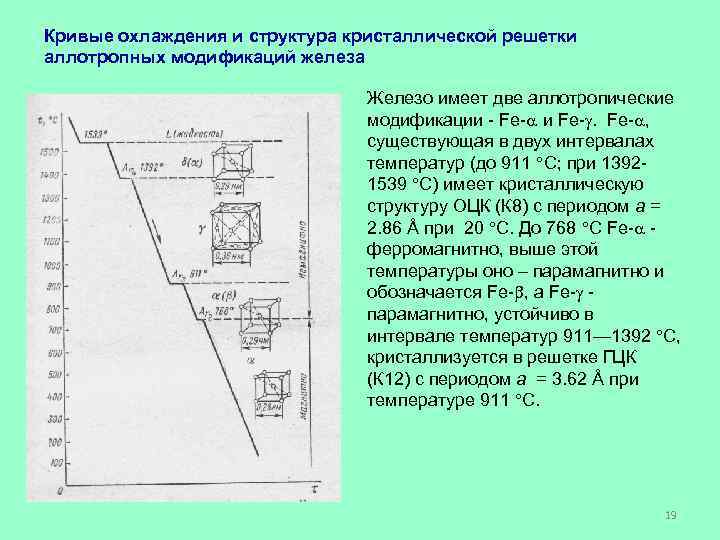
 Кривые охлаждения и структура кристаллической решетки аллотропных модификаций железа Железо имеет две аллотропические модификации - Fe- и Fe- , существующая в двух интервалах температур (до 911 С; при 1392 - 1539 С) имеет кристаллическую структуру ОЦК (К 8) с периодом а = 2. 86 Å при 20 С. До 768 С Fe- - ферромагнитно, выше этой температуры оно – парамагнитно и обозначается Fe- , а Fe- - парамагнитно, устойчиво в интервале температур 911— 1392 С, кристаллизуется в решетке ГЦК (К 12) с периодом а = 3. 62 Å при температуре 911 С. 19
Кривые охлаждения и структура кристаллической решетки аллотропных модификаций железа Железо имеет две аллотропические модификации - Fe- и Fe- , существующая в двух интервалах температур (до 911 С; при 1392 - 1539 С) имеет кристаллическую структуру ОЦК (К 8) с периодом а = 2. 86 Å при 20 С. До 768 С Fe- - ферромагнитно, выше этой температуры оно – парамагнитно и обозначается Fe- , а Fe- - парамагнитно, устойчиво в интервале температур 911— 1392 С, кристаллизуется в решетке ГЦК (К 12) с периодом а = 3. 62 Å при температуре 911 С. 19
 Различают нормальный и мартенситный механизм рост кристаллов. Первый наблюдается при медленном охлаждении металлов с высокими температурами полиморфного превращения. Новая кристаллическая фаза в этом случае возникает на границах исходных зерен и растет благодаря последовательному перемещению атомов из высокотемпературной модификации. Мартенситный механизм роста кристаллов присущ металлам с низкой температурой аллотропического превращения (например, Co). В металлах с высокой температурой аллотропического перехода (Fe, Ti, Zr) он наблюдается при больших переохлаждениях, т. е. также при низких температурах. Приблизительной температурной границей между реализацией нормального и мартенситного механизма можно считать 450 С. Вследствие малой подвижности атомов при низких температурах мартенситное превращение происходит путем совместного перемещения группы атомов на расстояния меньше межатомных. 20
Различают нормальный и мартенситный механизм рост кристаллов. Первый наблюдается при медленном охлаждении металлов с высокими температурами полиморфного превращения. Новая кристаллическая фаза в этом случае возникает на границах исходных зерен и растет благодаря последовательному перемещению атомов из высокотемпературной модификации. Мартенситный механизм роста кристаллов присущ металлам с низкой температурой аллотропического превращения (например, Co). В металлах с высокой температурой аллотропического перехода (Fe, Ti, Zr) он наблюдается при больших переохлаждениях, т. е. также при низких температурах. Приблизительной температурной границей между реализацией нормального и мартенситного механизма можно считать 450 С. Вследствие малой подвижности атомов при низких температурах мартенситное превращение происходит путем совместного перемещения группы атомов на расстояния меньше межатомных. 20
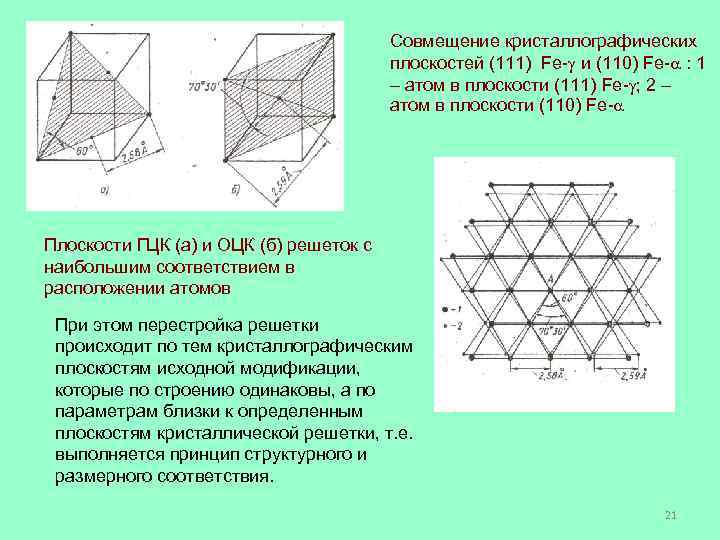
 Совмещение кристаллографических плоскостей (111) Fe- и (110) Fe- : 1 – атом в плоскости (111) Fe- ; 2 – атом в плоскости (110) Fe- Плоскости ГЦК (а) и ОЦК (б) решеток с наибольшим соответствием в расположении атомов При этом перестройка решетки происходит по тем кристаллографическим плоскостям исходной модификации, которые по строению одинаковы, а по параметрам близки к определенным плоскостям кристаллической решетки, т. е. выполняется принцип структурного и размерного соответствия. 21
Совмещение кристаллографических плоскостей (111) Fe- и (110) Fe- : 1 – атом в плоскости (111) Fe- ; 2 – атом в плоскости (110) Fe- Плоскости ГЦК (а) и ОЦК (б) решеток с наибольшим соответствием в расположении атомов При этом перестройка решетки происходит по тем кристаллографическим плоскостям исходной модификации, которые по строению одинаковы, а по параметрам близки к определенным плоскостям кристаллической решетки, т. е. выполняется принцип структурного и размерного соответствия. 21

