05 Вода порода.ppt
- Количество слайдов: 44

Массообмен минеральными компонентами • Удельная поверхность (Sуд, в - м 2·г-1 или Sуд, о- м-1) от 0, 1 до 1 103 м 2·г-1, (м 3·кг-1); (кг·м-3) Метод БЭТ (Брунауэр- Эммет- Теллера) 1 литр воды размазан по поверхности равной (м 2/л) • Минерально-солевой комплекс пород 1 - породообразующие реликтовые минералы, 2 - вторичные эпигенетические минералы (галогенные, карбонатные и сульфатные и др. ) 3 – ионно-солевой комплекс (вода физически связанная и в закрытых порах, вытяжки, поровые или горные растворы)
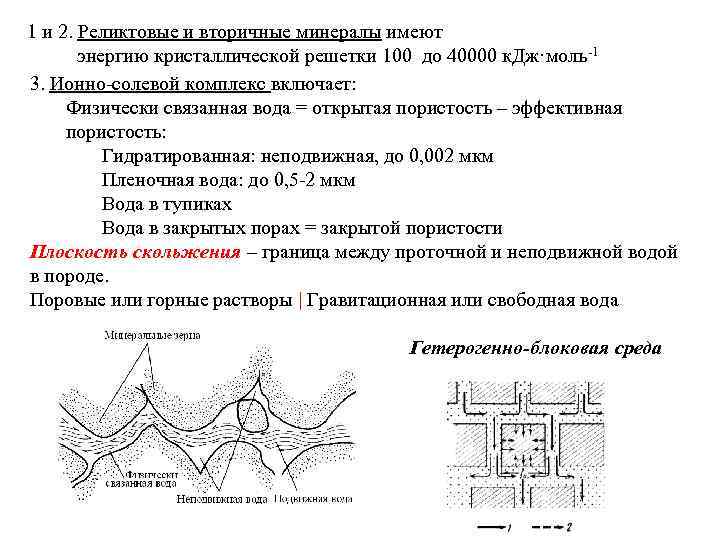
1 и 2. Реликтовые и вторичные минералы имеют энергию кристаллической решетки 100 до 40000 к. Дж·моль-1 3. Ионно-солевой комплекс включает: Физически связанная вода = открытая пористость – эффективная пористость: Гидратированная: неподвижная, до 0, 002 мкм Пленочная вода: до 0, 5 -2 мкм Вода в тупиках Вода в закрытых порах = закрытой пористости Плоскость скольжения – граница между проточной и неподвижной водой в породе. Поровые или горные растворы | Гравитационная или свободная вода Гетерогенно-блоковая среда

В неподвижной воде особенно активны: Электростатические силы действует далеко от поверхности раздела: сортирует ионы по знаку и величине заряда (ионный обмен) и способствует межмолекулярным взаимодействиям. Межмолекулярные силы действуют близко от поверхности раздела: гидролиз, комплексоообразование, растворение, минералообразование. Адсорбция -процесс концентрирования компонентов у поверхности раздела. Включает: тепловое (броуновское) движение, электростатическое взаимодействие, межатомное взаимодействие. Вызывают: хаотичное движение и перемешивание, сортировку ионов – ионный обмен, образованием координационных связей, комплексообразование При достижении равновесия формируется структура уравновешенного взаимодействия.

Представления об этой структуре – модели 2 электрических слоя – модель двойного электрического слоя Гельмогльца в 1853 2 (один диффузный) слоя – модель двойного диффузного слоя Гуи и Чапмана в 1910 -1913 3 (один диффузный) слоя - модель Штерна в 1924 4 (один диффузный) слоя – модель Грэм в 1947 4 (поверхность с диполями H 2 O) слоя – модель О’Мара Бокриса, Деванатана и Мюллера в 1963. Современная модель: 1. Гидратированная поверхность минерала 2. Слой Гильмгольца внутренний и внешний 3. Диффузный слой
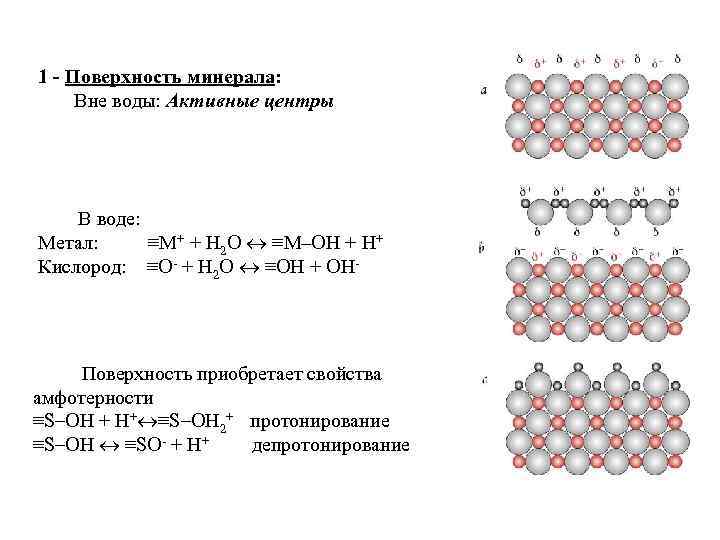
1 - Поверхность минерала: Вне воды: Активные центры В воде: Метал: ≡M+ + H 2 O ≡M‒OH + H+ Кислород: ≡O- + H 2 O ≡OH + OH- Поверхность приобретает свойства амфотерности ≡S‒OH + H+ ≡S‒OH 2+ протонирование ≡S‒OH ≡SO- + H+ депротонирование
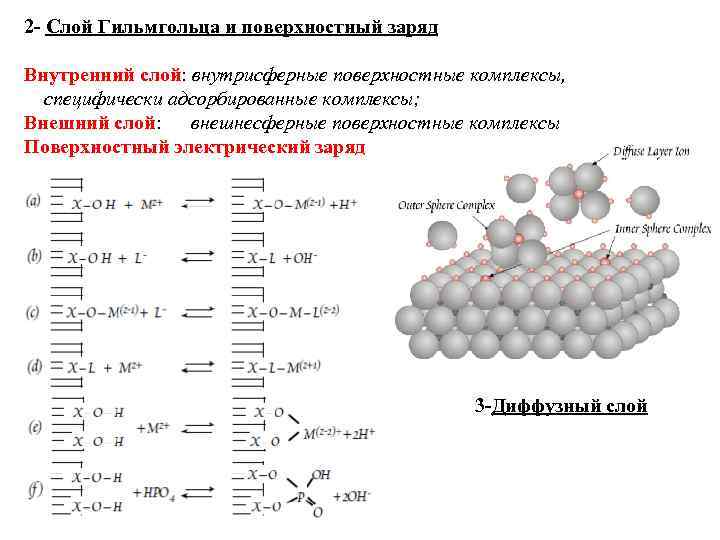
2 - Слой Гильмгольца и поверхностный заряд Внутренний слой: внутрисферные поверхностные комплексы, специфически адсорбированные комплексы; Внешний слой: внешнесферные поверхностные комплексы Поверхностный электрический заряд 3 -Диффузный слой

Поверхностный заряд: σin =σ0 + σH = -σi σпов. = σ0 + σH+ σi Если поверхностная избыточная концентрация (или гиббсовская поверхностная концентрация): где Φ – постоянная Фарадея (Кл· моль-1) Точка нулевого заряда (p. HPZC) - p. H, при которой σпов. = 0.

Минерал Кварц α-Si. O 2 p. I 2 -3, 5 Si. O 2 гель 1, 02, 5 2, 0 2 -4, 6 Альбит Na. Al. Si 3 O 8 Каолинит Al(Si 4 O 10)(OH)8 Монтмориллонит Гематит Fe 2 O 3 Магнетит Fe 3 O 4 Гётит Fe. OOH Fе(ОН)3 Корунд Al 2 O 3 Гиббсит Al(OH)3 Пиролюзит, δ-Мn. О 2 Рутил, Ti. O 2 В дистиллированной воде σi = 0, σпов. = σ0 + σH p. HPZC - нулевая точка только протонного заряда или изоэлектрическая точка, p. I ≤ 2, 5 5 -9 6, 5 6 -7 8, 5 8 -9 ~9 2, 2 5, 8 Если p. I > p. H, поверхность минерала + Eсли p. I< p. H, поверхность минерала ‒
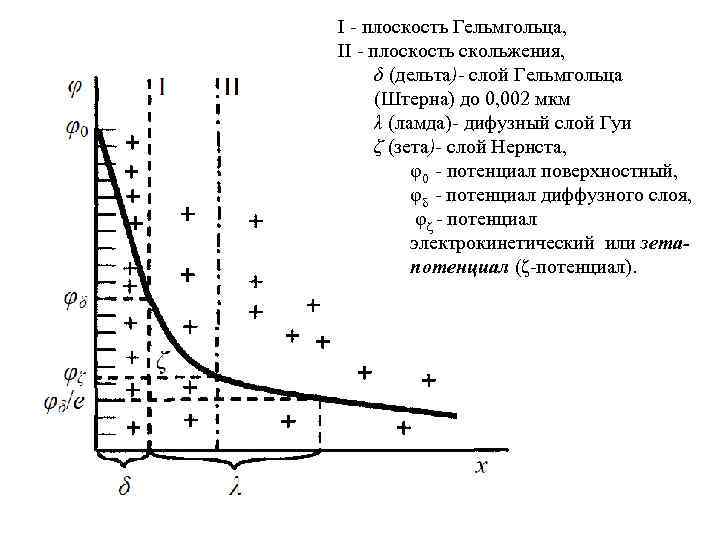
I - плоскость Гельмгольца, II - плоскость скольжения, δ (дельта)- слой Гельмгольца (Штерна) до 0, 002 мкм λ (ламда)- дифузный слой Гуи ζ (зета)- слой Нернста, φ0 - потенциал поверхностный, φδ - потенциал диффузного слоя, φζ - потенциал электрокинетический или зетапотенциал (ζ-потенциал).
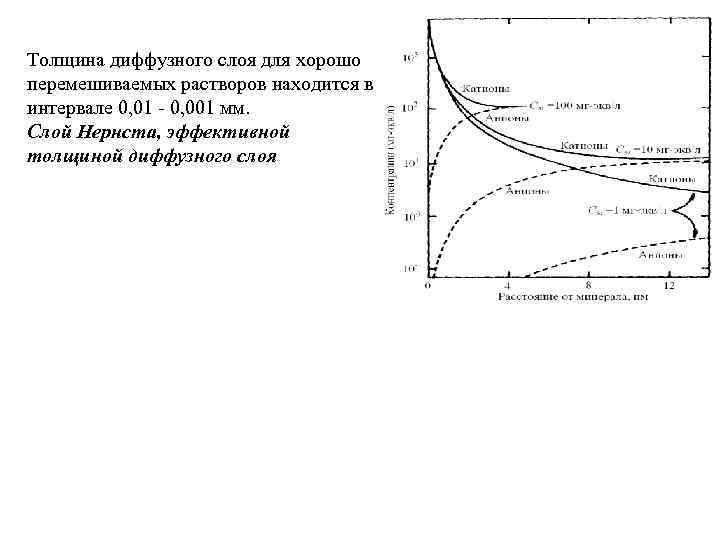
Толщина диффузного слоя для хорошо перемешиваемых растворов находится в интервале 0, 01 - 0, 001 мм. Слой Нернста, эффективной толщиной диффузного слоя

Поверхностное комплексообразование 2 семестр: Лекция 15. Поверхностные комплексы - метастабильные образования и раствора и минерала Взаимодействуют: Øфункциональные группы минерала (окиси и гидроокиси Al, Fe, Mn и Si) Øионы раствора Движущая сила комплексообразовния : Øвзаимодействие электростатических зарядов и Øхимическое сродство функциональных групп минералов и ионов раствора. Два уровня взаимодействий: Øвнутренний -сильных взаимодействий и Øвнешний - слабых взаимодействий Внутрисферный комплекс, образованный бифосфатом (HPO 42− ) и двумя Fe 3+ в гетите
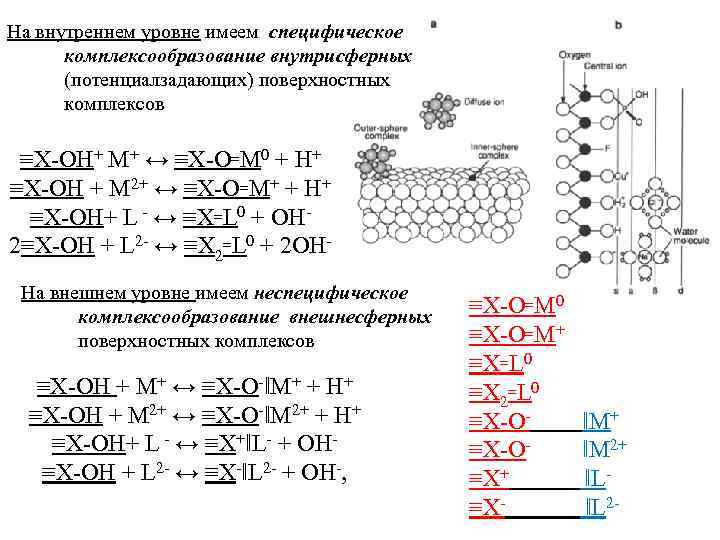
На внутреннем уровне имеем специфическое комплексообразование внутрисферных (потенциалзадающих) поверхностных комплексов ≡X-OH+ M+ ↔ ≡X-O꞊M 0 + H+ ≡X-OH + M 2+ ↔ ≡X-O꞊M+ + H+ ≡X-OH+ L - ↔ ≡X꞊L 0 + OH 2≡X-OH + L 2 - ↔ ≡X 2꞊L 0 + 2 OHНа внешнем уровне имеем неспецифическое комплексообразование внешнесферных поверхностных комплексов ≡X-OH + M+ ↔ ≡X-O-‖M+ + H+ ≡X-OH + M 2+ ↔ ≡X-O-‖M 2+ + H+ ≡X-OH+ L - ↔ ≡X+‖L- + OH≡X-OH + L 2 - ↔ ≡X-‖L 2 - + OH-, ≡X-O꞊M 0 ≡X-O꞊M+ ≡X꞊L 0 ≡X 2꞊L 0 ≡X-O- ‖M+ ≡X-O- ‖M 2+ ≡X+ ‖L≡X- ‖L 2 -

Электрическая нейтральность обеспечивается балансом зарядов в слое Штерна: σ0 + σH + σis+ σos + σd = 0 σ0 +σH+ σis+ σos = - σd Баланс активных центров на поверхности ≡X-O꞊M 0 ≡X-O꞊M+ ≡X꞊L 0 ≡X 2꞊L 0 ≡X-O- ‖M+ ≡X-O- ‖M 2+ ≡X+ ‖L≡X- ‖L 2 - Здесь Ȼ 0 – максимальное содержание одновалентных ионов способных уместиться на поверхности (моль·л-1), Cac и CM, ac– плотность активных центров на поверхности минерала (число мест·м-2 и моль·м-2 соответственно), NA –число Авагадро (6, 02205∙ 1023 моль-1), Sm/w – площадь поверхности минерала отнесенная к 1 литру воды (м 2∙м-3).

Среди них чаще всего используются: 1 – модель диффузного (двойного) слоя , 2 - модель постоянной емкости и 3 – модель тройного слоя.
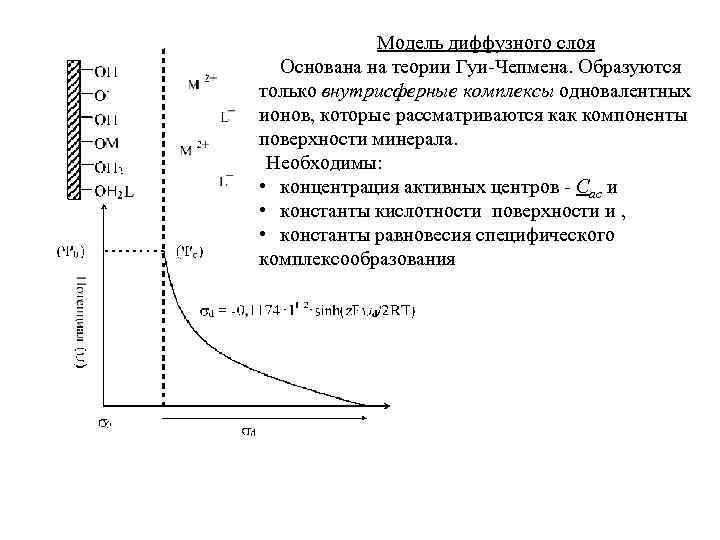
Модель диффузного слоя Основана на теории Гуи-Чепмена. Образуются только внутрисферные комплексы одновалентных ионов, которые рассматриваются как компоненты поверхности минерала. Необходимы: • концентрация активных центров - Cac и • константы кислотности поверхности и , • константы равновесия специфического комплексообразования

Модель постоянной емкости Основана на модели Г. Л. Гельмгольца. Образуются только внутрисферные комплексы, которые располагаются слоем на расстоянии от поверхности. Диффузный слой отсутствует. Необходимы: • концентрация активных центров - Cac , • константы кислотности, • электрическую емкость -Csp, s • константы равновесия специфического комплексообразования
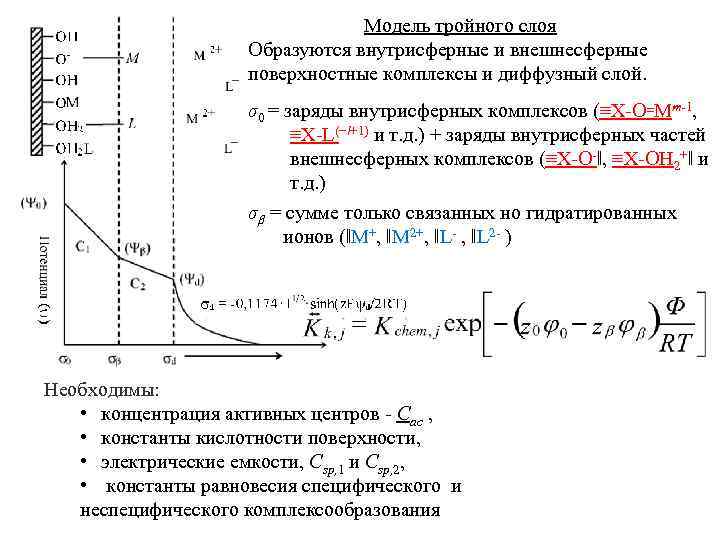
Модель тройного слоя Образуются внутрисферные и внешнесферные поверхностные комплексы и диффузный слой. σ0 = заряды внутрисферных комплексов (≡X-O꞊Mm-1, ≡X-L(−l+1) и т. д. ) + заряды внутрисферных частей внешнесферных комплексов (≡X-O-‖, ≡X-OH 2+‖ и т. д. ) σβ = сумме только связанных но гидратированных ионов (‖M+, ‖M 2+, ‖L- , ‖L 2 - ) Необходимы: • концентрация активных центров - Cac , • константы кислотности поверхности, • электрические емкости, Csp, 1 и Csp, 2, • константы равновесия специфического и неспецифического комплексообразования
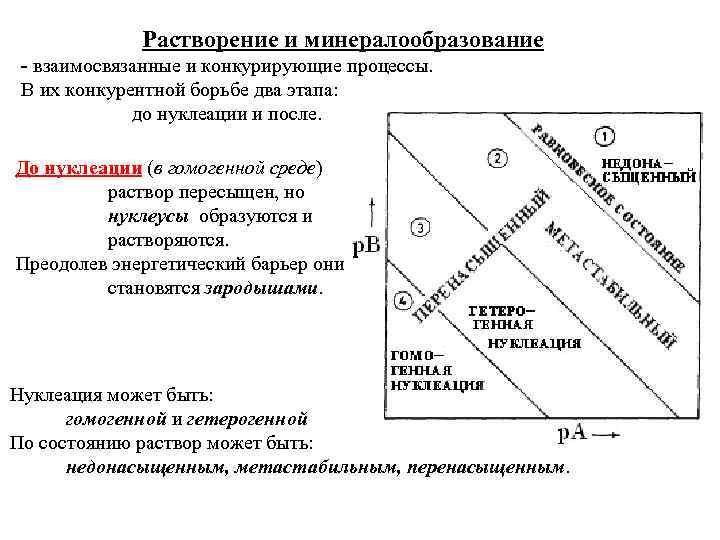
Растворение и минералообразование - взаимосвязанные и конкурирующие процессы. В их конкурентной борьбе два этапа: до нуклеации и после. До нуклеации (в гомогенной среде) раствор пересыщен, но нуклеусы образуются и растворяются. Преодолев энергетический барьер они становятся зародышами. Нуклеация может быть: гомогенной и гетерогенной По состоянию раствор может быть: недонасыщенным, метастабильным, перенасыщенным.

После неклюации (в гетерогенной среде). Лекция 2 Механизм включает: ионный обмен, адсорбцию, диффузию и поверхностное комплексообразование в слое Гельмгольца и на поверхности минерала. Сопровождается поглощением или выделением тепла - теплоты растворения (температура меняется). Принцип микроскопической обратимости реакций Растворение – минералообразование – сложный многоступенчатый процесс массообмена через поверхность раздела между водой и минералом. Минерал-реагент + Вода-реагент Вода-продукт Механизмы делятся на две части: химическую и диффузную. Химия определяет условия равновесия и направленность процесса Диффузия регулирует массообмен к поверхности раздела и от нее и влияет на скорость процесса Реакции: гидратация , электролитическая диссоциация или ассоциация, гидролиз, обмен лигандами, поверхностное комплексообразование и т. д.

Механизмы раствореия и минералообразования Растворение – минералообразование - массообмен между породой и подземной водой через поверхность раздела. Зависят от свойства минерала и состава воды. 2 основных химических процессов растворения: гидратация и гидролиз. Редко участвуют окислительно-восстановительные процессы Гидратация солей сильных кислот и оснований Na. Cl Na+ + Cl-; Ca. SO 4 2 H 2 O Ca 2+ + + 2 H 2 O; Незримый реагент - диполь H 2 O Конгруэнтное растворение Растворение начинается с гидратации: Li. Cl·H 2 O, Cu. Cl 2· 2 H 2 O, Fe. SO 4· 7 H 2 O, Fe(NO 3)3· 9 H 2 O, Na 2 SO 4· 10 H 2 O, Na 2 HPO 4· 12 H 2 O, и др. Осаждение увлекает H 2 O: Ca. SO 4· 2 H 2 O, Na 2 CO 3· 10 H 2 O и др.
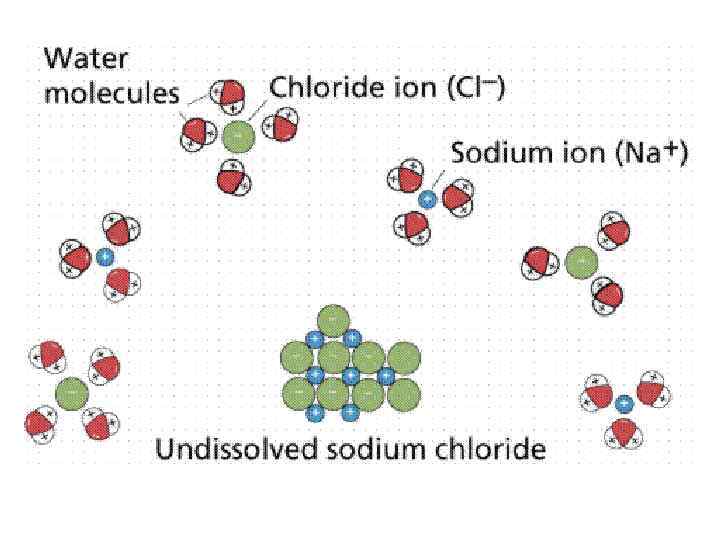
![Процесс растворения: Na. Cl(кристалл) → Na+(газ) + Cl-(газ) → [Na+n(H 2 O)]+ [Cl-n(H 2 Процесс растворения: Na. Cl(кристалл) → Na+(газ) + Cl-(газ) → [Na+n(H 2 O)]+ [Cl-n(H 2](https://present5.com/presentation/184980035_144560364/image-22.jpg)
Процесс растворения: Na. Cl(кристалл) → Na+(газ) + Cl-(газ) → [Na+n(H 2 O)]+ [Cl-n(H 2 O)] Теплота растворения ΔHгид - ΔHреш. = ΔHраст. При постоянной температуре ΔH = ΔZ
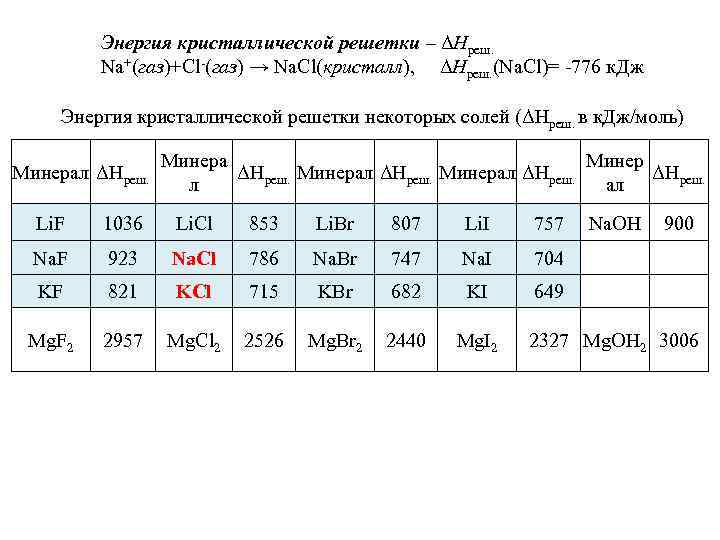
Энергия кристаллической решетки – ΔHреш. Na+(газ)+Cl-(газ) → Na. Cl(кристалл), ΔHреш. (Na. Cl)= -776 к. Дж Энергия кристаллической решетки некоторых солей (ΔHреш. в к. Дж/моль) Минерал ΔHреш. Минера Минер ΔHреш. Минерал ΔHреш. л ал Li. F 1036 Li. Cl 853 Li. Br 807 Li. I 757 Na. F 923 Na. Cl 786 Na. Br 747 Na. I 704 KF 821 KCl 715 KBr 682 KI 649 Mg. F 2 2957 Mg. Cl 2 2526 Mg. Br 2 2440 Mg. I 2 Na. OH 900 2327 Mg. OH 2 3006
![Энергия гидратации: Na+(газ) + n. H 2 O → [Na+n(H 2 O)], ΔHгид = Энергия гидратации: Na+(газ) + n. H 2 O → [Na+n(H 2 O)], ΔHгид =](https://present5.com/presentation/184980035_144560364/image-24.jpg)
Энергия гидратации: Na+(газ) + n. H 2 O → [Na+n(H 2 O)], ΔHгид = -406 к. Дж/моль; Cl-(газ) + n. H 2 O → [Cl-n(H 2 O)], ΔHгид = -363 к. Дж/моль. Энергия (энтальпия) гидратации ионов (Hhyd к. Дж/моль) Ионы H+ Li+ Na+ K+ Rb+ Cs+ Cr 2+ Co 2+ Zn 2+ Hhyd -1130 -520 -406 -322 -297 -276 -1904 -1996 -2046 Ion Al 3+ Be 2+ Mg 2+ Ca 2+ Sr 2+ Ba 2+ Mn 2+ Ni 2+ Cd 2+ Hhyd -4665 -2494 -1921 -1577 -1443 -1305 -1841 -2105 -1807 Ion Fe 3+ FCl. Br. ICl. O 4 Fe 2+ Cu 2+ Hg 2+ Для Na. Cl 776 - (406+363) = +7 к. Дж/моль Для KCl 715 - (322+363)= +30 к. Дж/моль Для Mg. Cl 2 2526 -1921 -363 = + 242 к. Дж/моль Hhyd -4430 -505 -363 -336 -295 -238 -1946 -2100 -1824
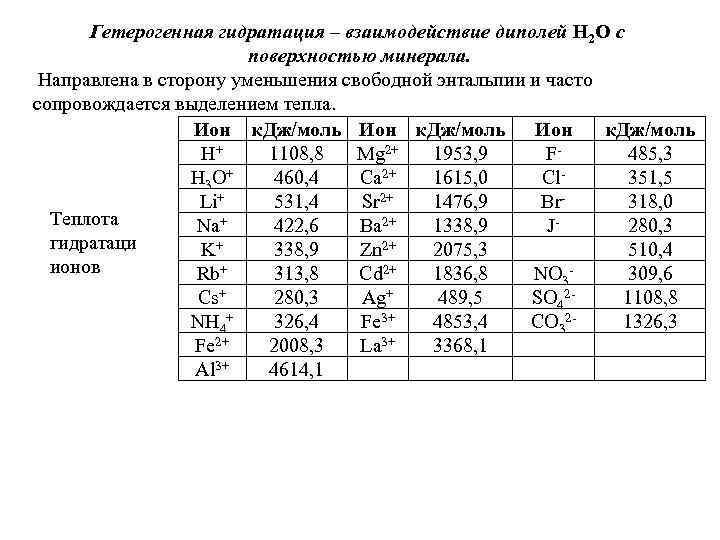
Гетерогенная гидратация – взаимодействие диполей H 2 O с поверхностью минерала. Направлена в сторону уменьшения свободной энтальпии и часто сопровождается выделением тепла. Ион к. Дж/моль H+ 1108, 8 Mg 2+ 1953, 9 F 485, 3 H 3 O+ 460, 4 Ca 2+ 1615, 0 Cl 351, 5 Li+ 531, 4 Sr 2+ 1476, 9 Br 318, 0 Теплота Na+ 422, 6 Ba 2+ 1338, 9 J 280, 3 гидратаци K+ 338, 9 Zn 2+ 2075, 3 510, 4 ионов Rb+ 313, 8 Cd 2+ 1836, 8 NO 3309, 6 Cs+ 280, 3 Ag+ 489, 5 SO 421108, 8 NH 4+ 326, 4 Fe 3+ 4853, 4 CO 321326, 3 Fe 2+ 2008, 3 La 3+ 3368, 1 Al 3+ 4614, 1

1 -Чем больше теплота гидратации, тем прочнее аквакомплексы. Энергия гидратации тем больше, чем меньше размер иона и чем больше его заряд, Энергии гидратации на поверхности минерала противостоит энергия кристаллической решетки. Когда энергия гидратация > энергии кристаллической решетки, идет процесс разрушения этой решётки. Когда энергия гидратации < энергии криталлической решетки формируется слой связанной воды. 2 - Минерализация мешает и уменьшает гидратацию. При высокой минерализации растворенные ионы способны выпадать в осадок, увлекая с собой диполи H 2 O. При кристаллизации H 2 O удаляется в составе кристаллогидратов: Li. Cl·H 2 O, Cu. Cl 2· 2 H 2 O, Ba(Cl. O 4)2· 3 H 2 O, Cd. Br 2· 4 H 2 O, Na 2 S 2 O 3· 5 H 2 O, Al. Cl 3· 6 H 2 O, Fe. SO 4· 7 H 2 O, Mg. I 2· 8 H 2 O, Fe(NO 3)3· 9 H 2 O, Na 2 SO 4· 10 H 2 O, Na 2 HPO 4· 12 H 2 O, Al 2(SO 4)3· 18 H 2 O и др, 3 - Температура уменьшает степень гидратации,
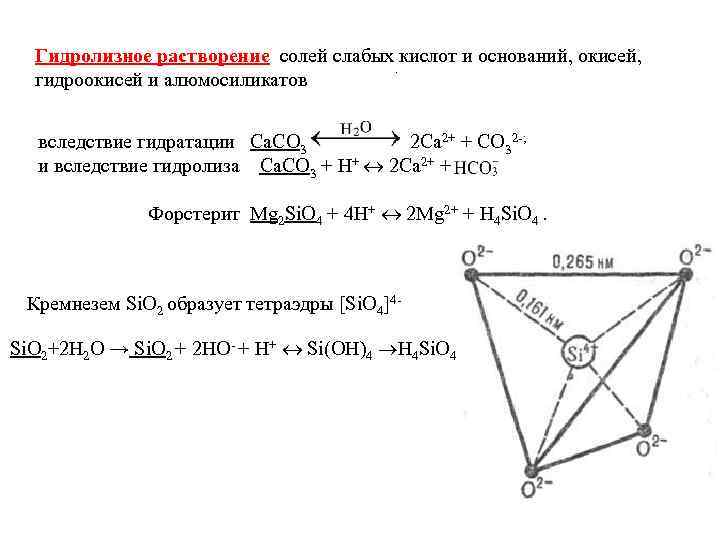
Гидролизное растворение солей слабых кислот и оснований, окисей, . гидроокисей и алюмосиликатов вследствие гидратации Ca. CO 3 2 Ca 2+ + CO 32 -; и вследствие гидролиза Ca. CO 3 + H+ 2 Ca 2+ + Форстерит Mg 2 Si. O 4 + 4 H+ 2 Mg 2+ + H 4 Si. O 4. Кремнезем Si. O 2 образует тетраэдры [Si. O 4]4 - Si. O 2+2 H 2 O → Si. O 2 + 2 HO- + H+ Si(OH)4 H 4 Si. O 4
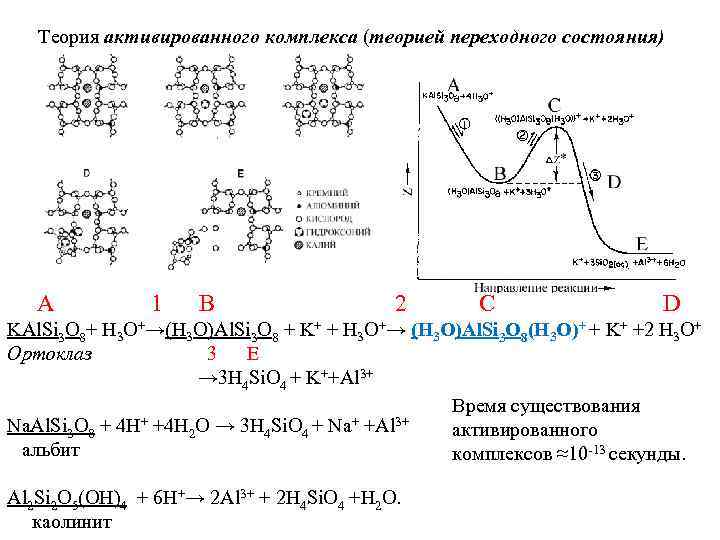
Теория активированного комплекса (теорией переходного состояния) A 1 B 2 C D KAl. Si 3 O 8+ H 3 O+→(H 3 O)Al. Si 3 O 8 + K+ + H 3 O+→ (H 3 O)Al. Si 3 O 8(H 3 O)+ + K+ +2 H 3 O+ Ортоклаз 3 E → 3 H 4 Si. O 4 + K++Al 3+ Время существования + +4 H O → 3 H Si. O + Na+ +Al 3+ Na. Al. Si 3 O 8 + 4 H активированного 2 4 4 альбит комплексов ≈10 -13 секунды. Al 2 Si 2 O 5(OH)4 + 6 H+→ 2 Al 3+ + 2 H 4 Si. O 4 +H 2 O. каолинит

Лекция 16. Условия равновесия Определяются: Произведением растворимости. Растворимостью. Эффективной растворимостью. Произведение растворимости – константа равновесия Для плохо растворимых минералов произведение растворимости

При гидратации у ангидрита: у малахита: При гидролизе у серпентина: Mg 3 Si 2 O 5(OH)4+6 H+=3 Mg 2+ + 2 H 4 Si. O 4 + H 2 O. серпентин

Посторонние компоненты Ингибиторы и катализаторы у кальцита: Если степень насыщения Ωj >1, т. е. Пa > Kr, j, Zr, j с +, минерал j образуется. Если степень насыщения Ωj <1, т. е. Пa < Kr, j, Zr, j с -, минерал j растворяется Индекс насыщения SIj с + показатель устойчивости минерала, Индекс насыщения SIj с - показатель агрессивности воды. Растворимость Максимальное количество минерала (а не иона), которое способно раствориться в единице объемы воды до её полного насыщения. ØРастворимость в чистой воде и стандартных условиях. ØЭффективная растворимость.

Растворимость в чистой воде Ba. SO 4 ↔ Ba 2+ + SO 42 -

Растворимые: соли сильных кислот и оснований с энергией кристаллической решетки (< 103 к. Дж/моль) и растворимостью >50 г/л (>0, 1 моль/л) (галит (Na. Cl), тенардит (Na 2 SO 4), мирабилит (Na 2 SO 4· 10 H 2 O), натрон - сода (Na 2 CO 3· 10 H 2 O), бура (Na 2 B 4 O 7· 10 H 2 O) и др. ) Плохо растворимые: соли слабых кислот и оснований с энергию кристаллической решётки < 104 к. Дж/моль и растворимостью 0, 01 -50 г/л (0, 1 -10 -4 моль/л). (гипс (Ca. SO 4· 2 H 2 O), ангидрит (Ca. SO 4), кальцит (Ca. CO 3) и доломит ((Ca, Mg)(CO 3)2), магнезит (Mg. CO 3), и др. ) Нерастворимые: окиси, гидроокиси и алюмосиликаты с энергию кристаллической решетки >104 к. Дж/моль и растворимостью < 0, 01 г/л (< 10 -4 моль/л). (Кварц, полевые шпаты, слюды, глины и т. д. ) Эффективная растворимость Зависит от состава воды, присутствующих минералов и температуры. Состав воды: свои и посторонние компоненты. 1. Свои, которые участвуют в реакции, входят в произведение растворимости и определяют степень насыщения. Ωj ≠ 0.
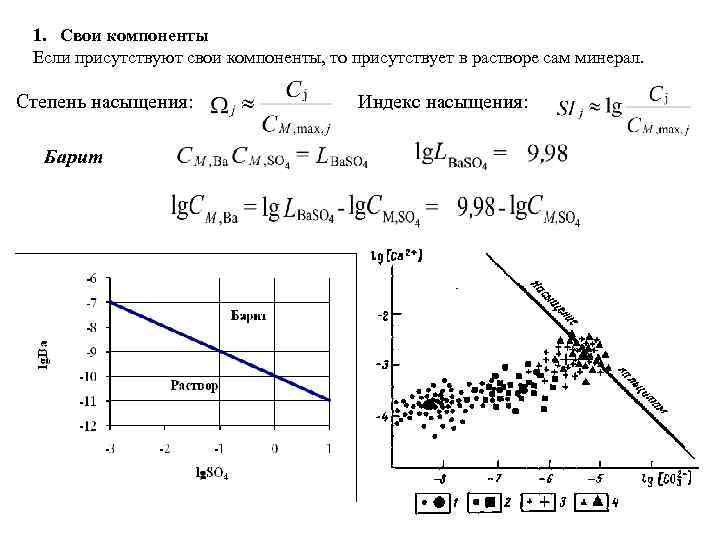
1. Свои компоненты Если присутствуют свои компоненты, то присутствует в растворе сам минерал. Степень насыщения: Индекс насыщения: Барит
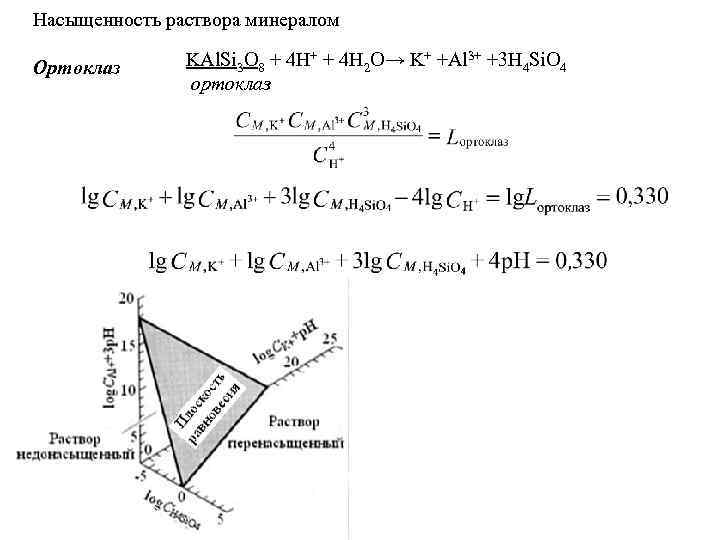
Насыщенность раствора минералом Ортоклаз KAl. Si 3 O 8 + 4 H+ + 4 H 2 O→ K+ +Al 3+ +3 H 4 Si. O 4 ортоклаз

2. Посторонние компоненты воды, которые отсутствуют в составе минерала (Ингибиторы и катализаторы). Они влияют, если взаимодействуют со компонентами минерала, т. е. образуют с ними комплексы. Пусть минерал j с составом Ml. Lm образует катион Mj и анион Lj. Их функции закомплексованности и или функции распределения и . Делаете кирпичи из глины, а их воруют.
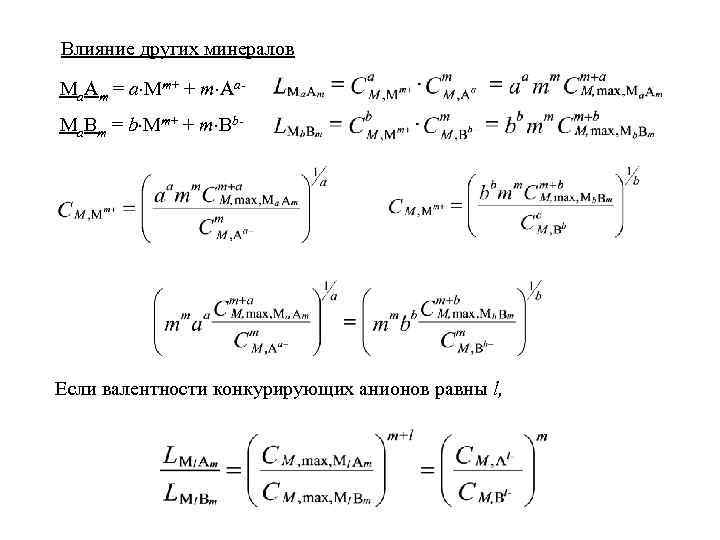
Влияние других минералов Ma. Am = a Mm+ + m Aa- Ma. Bm = b Mm+ + m Bb- Если валентности конкурирующих анионов равны l,
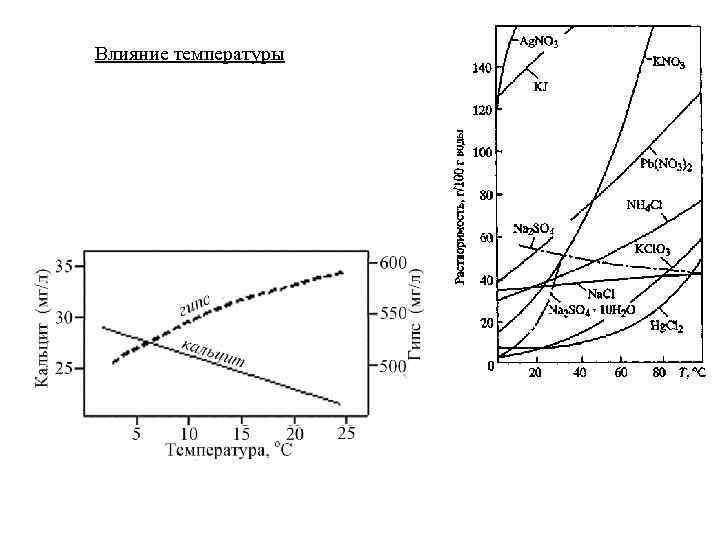
Влияние температуры

Скорость растворения Альмандин: Fe 3 Al 2(Si. O 4)3 +4 H+→ 3 Fe 2+ +2 Al 3+ + 3 H 4 Si. O 4. Согласно принципу микроскопической обратимости реакций прямая и обратная скорости принимаются равными. Растворение Минералообразование Если взаимодействуют объем воды Vj с минералом на площади Sj то: где – скорость, приведенная к площади раздела, – скорость, приведенная к объему раствора, Sm/w – площадь поверхности, отнесенная к единице объема воды.
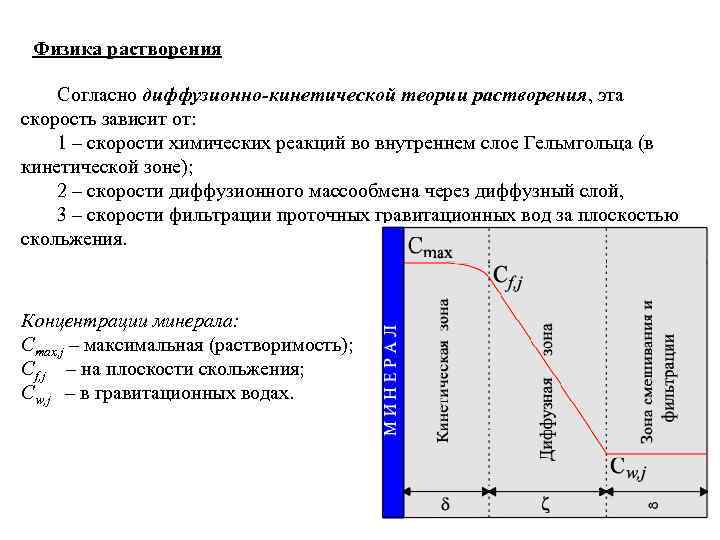
Физика растворения Согласно диффузионно-кинетической теории растворения, эта скорость зависит от: 1 – скорости химических реакций во внутреннем слое Гельмгольца (в кинетической зоне); 2 – скорости диффузионного массообмена через диффузный слой, 3 – скорости фильтрации проточных гравитационных вод за плоскостью скольжения. Концентрации минерала: Cmax, j – максимальная (растворимость); Cf, j – на плоскости скольжения; Cw, j – в гравитационных водах.

Скорости реакций Лекция 3 Преимущественно во внутреннем слое Гельмгольца (Штерна) Зависит от минерала, состава раствора и температуры. 1. Минерал: энергия кристаллической решетки и растворимость. 2. Состав воды: При гидратации: от концентрация отдельных ионов минерала, присутствия ингибиторов и катализаторов При гидратации растворение зависит от соотношения энергий кристаллической решетки и гидратаций и степени насыщения. При гидролизе растворение проходит стадию поверхностного комплексообразования. Теория активированного комплекса: взаимодействие минерала с раствором кислотно-щелочное и зависит от плотности активных центров : X-OH, X-OH 2+ и X-O- на поверхности раздела, т. е. p. H в воде.

Экспериментально установлено, что общую скорость растворения минералов можно представить, как сумму скоростей трех кислотнощелочных реакций : где , – константы скоростей, v -поряди скоростей реакции от 0 до 1, 5. 3. Температура: зависимость Арениуса Энергия активации реакций Ea, j , от 7 до 132 к. Дж/моль, в среднем близка к 71 к. Дж/моль. Лекция 2
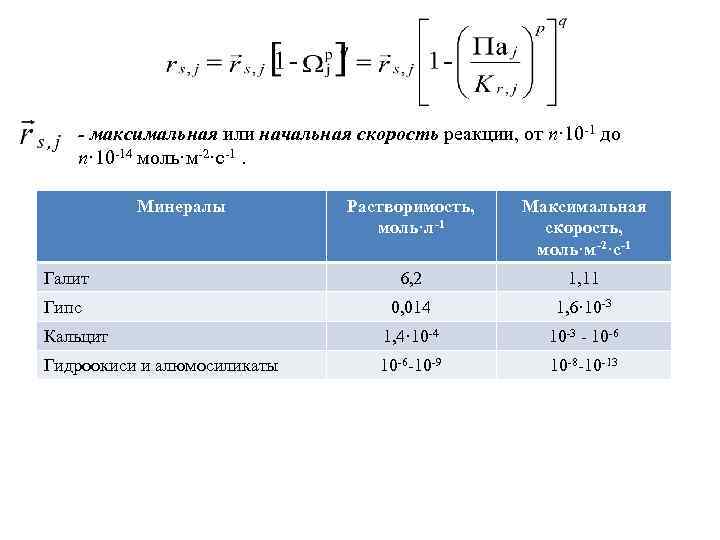
- максимальная или начальная скорость реакции, от n· 10 -1 до n· 10 -14 моль·м-2·с-1. Минералы Растворимость, моль·л-1 Максимальная скорость, моль·м-2·с-1 Галит 6, 2 1, 11 Гипс 0, 014 1, 6· 10 -3 Кальцит 1, 4· 10 -4 10 -3 - 10 -6 Гидроокиси и алюмосиликаты 10 -6 -10 -9 10 -8 -10 -13
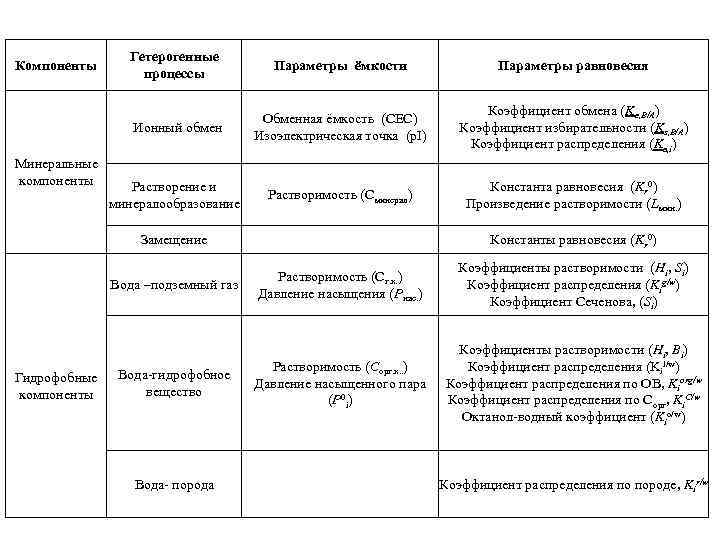
Параметры равновесия Обменная ёмкость (CEC) Изоэлектрическая точка (p. I) Коэффициент обмена (Ke, B/A) Коэффициент избирательности (Ks, B/A) Коэффициент распределения (Kв, i) Растворение и минералообразование Растворимость (Cминерал) Константа равновесия (Kr 0) Произведение растворимости (Lмин. ) Константы равновесия (Kr 0) Вода –подземный газ Гидрофобные компоненты Параметры ёмкости Замещение Минеральные компоненты Гетерогенные процессы Ионный обмен Компоненты Растворимость (Cг. к. ) Давление насыщения (Pнас. ) Коэффициенты растворимости (Hi, Si) Коэффициент распределения (Kig/w) Коэффициент Сеченова, (Si) Вода-гидрофобное вещество Растворимость (Cорг. к. . ) Давление насыщенного пара (P 0 i) Вода- порода Коэффициенты растворимости (Hi, Bi) Коэффициент распределения (Kil/w) Коэффициент распределения по ОВ, Kiorg/w Коэффициент распределения по Cорг, Ki. C/w Октанол-водный коэффициент (Kio/w) Коэффициент распределения по породе, Kir/w
05 Вода порода.ppt