 Масса молекул. Количество вещества. 10 класс
Масса молекул. Количество вещества. 10 класс
![Концентрация – число частиц в веществе. [n]=[1/м 3]=[м-3] Объем [V]=[м 3] Плотность [ƥ]=[кг/ м Концентрация – число частиц в веществе. [n]=[1/м 3]=[м-3] Объем [V]=[м 3] Плотность [ƥ]=[кг/ м](https://present5.com/presentation/8680553_335363581/image-2.jpg) Концентрация – число частиц в веществе. [n]=[1/м 3]=[м-3] Объем [V]=[м 3] Плотность [ƥ]=[кг/ м 3] Масса [m]=[кг] m 0 – масса одной молекулы m=m 0*N
Концентрация – число частиц в веществе. [n]=[1/м 3]=[м-3] Объем [V]=[м 3] Плотность [ƥ]=[кг/ м 3] Масса [m]=[кг] m 0 – масса одной молекулы m=m 0*N
 Относительная атомная масса вещества Ar (Находится в ПТХЭ) Относительная молекулярная масса вещества Mr (вычисляют, складывая относительные атомные массы элементов, входящих в состав молекулы вещества) Например: Mr(H 2 SO 4)=1*2+32+16*4=98
Относительная атомная масса вещества Ar (Находится в ПТХЭ) Относительная молекулярная масса вещества Mr (вычисляют, складывая относительные атомные массы элементов, входящих в состав молекулы вещества) Например: Mr(H 2 SO 4)=1*2+32+16*4=98
![Количество вещества [ν]=[моль] «ню» 1 моль – это количество вещества, в котором содержится столько Количество вещества [ν]=[моль] «ню» 1 моль – это количество вещества, в котором содержится столько](https://present5.com/presentation/8680553_335363581/image-4.jpg) Количество вещества [ν]=[моль] «ню» 1 моль – это количество вещества, в котором содержится столько же молекул или атомов, сколько атомов содержится в углероде массой 0, 012 кг. Постоянная Авогадро – число атомов в одном моле любого вещества. NA=6, 02*1023 моль-1
Количество вещества [ν]=[моль] «ню» 1 моль – это количество вещества, в котором содержится столько же молекул или атомов, сколько атомов содержится в углероде массой 0, 012 кг. Постоянная Авогадро – число атомов в одном моле любого вещества. NA=6, 02*1023 моль-1
 Количество вещества равно отношению числа молекул N в данном теле к постоянной Авогадро NA, т. е. к числу молекул в 1 моле вещества. ν= N/NA Молярная масса вещества – масса вещества, взятого в количестве 1 моль. [M]=[кг/моль] M=Mr*10 -3 кг/моль Например: M(H 2 SO 4)=98*10 -3 кг/моль
Количество вещества равно отношению числа молекул N в данном теле к постоянной Авогадро NA, т. е. к числу молекул в 1 моле вещества. ν= N/NA Молярная масса вещества – масса вещества, взятого в количестве 1 моль. [M]=[кг/моль] M=Mr*10 -3 кг/моль Например: M(H 2 SO 4)=98*10 -3 кг/моль
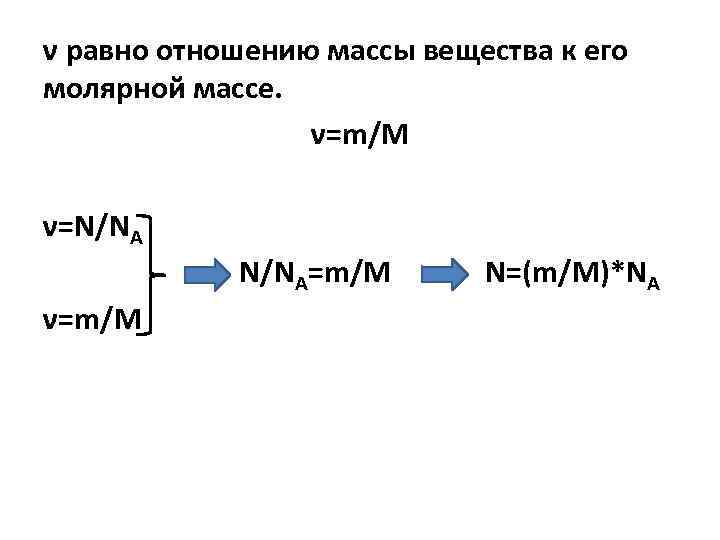 ν равно отношению массы вещества к его молярной массе. ν=m/M ν=N/NA=m/M ν=m/M N=(m/M)*NA
ν равно отношению массы вещества к его молярной массе. ν=m/M ν=N/NA=m/M ν=m/M N=(m/M)*NA