Масс-спектрометрия.ppt
- Количество слайдов: 21
 Масс-спектрометрия основана на разрушении молекулы под действием электронного удара и регистрации масс полученных осколков
Масс-спектрометрия основана на разрушении молекулы под действием электронного удара и регистрации масс полученных осколков
 При бомбардировке молекулы органического соединения электронами с энергией, несколько большей, чем значение первого потенциала ионизации вещества (около 10 э. В), происходит отрыв электрона от молекулы: Этот процесс называют ионизацией, а образующийся ион молекулярным ионом:
При бомбардировке молекулы органического соединения электронами с энергией, несколько большей, чем значение первого потенциала ионизации вещества (около 10 э. В), происходит отрыв электрона от молекулы: Этот процесс называют ионизацией, а образующийся ион молекулярным ионом:
 • Молекулярный ион является катион-радикалом, положительно заряжен и имеет нечетное количество электронов. Масса молекулярного иона практически равна массе молекулы, из которой он образуется. • Если бомбардировать молекулу электронами с энергией, значительно превышающей первый потенциал ионизации ( обычно используют 70 э. В), то образующийся молекулярный ион получает энергию, достаточную для разрыва в нем химических связей. Это приводит к распаду молекулярного иона на более мелкие фрагменты (осколочные ионы, радикалы). Такой процесс называют фрагментацией. • Помимо разрыва связей могут протекать внутримолекулярные перегруппировки • с образованием перегруппировочных ионов и радикалов.
• Молекулярный ион является катион-радикалом, положительно заряжен и имеет нечетное количество электронов. Масса молекулярного иона практически равна массе молекулы, из которой он образуется. • Если бомбардировать молекулу электронами с энергией, значительно превышающей первый потенциал ионизации ( обычно используют 70 э. В), то образующийся молекулярный ион получает энергию, достаточную для разрыва в нем химических связей. Это приводит к распаду молекулярного иона на более мелкие фрагменты (осколочные ионы, радикалы). Такой процесс называют фрагментацией. • Помимо разрыва связей могут протекать внутримолекулярные перегруппировки • с образованием перегруппировочных ионов и радикалов.
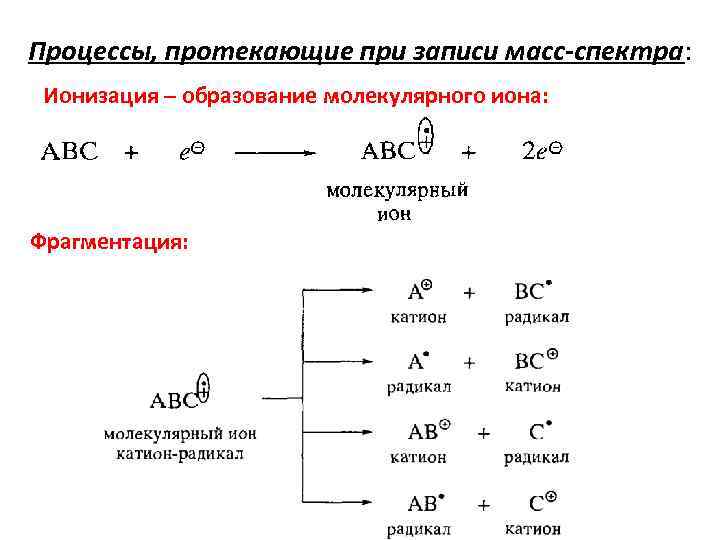 Процессы, протекающие при записи масс-спектра: Ионизация – образование молекулярного иона: Фрагментация:
Процессы, протекающие при записи масс-спектра: Ионизация – образование молекулярного иона: Фрагментация:
 Перегруппировки: Для получения масс-спектра пары вещества в глубоком вакууме (около 10 -6 мм. рт. ст. ) бомбардируют потоком электронов с энергией 70 э. В. Образующиеся при распаде молекулы частицы ускоряются сильным электрическим полем и попадают в магнитное поле, в котором нейтральные частицы не изменяют направления движения, а ионы изменяют траекторию своего движения в зависимости от отношения массы к заряду m/z, что позволяет распределить ионы по их массам, определить массы ионов и их количество.
Перегруппировки: Для получения масс-спектра пары вещества в глубоком вакууме (около 10 -6 мм. рт. ст. ) бомбардируют потоком электронов с энергией 70 э. В. Образующиеся при распаде молекулы частицы ускоряются сильным электрическим полем и попадают в магнитное поле, в котором нейтральные частицы не изменяют направления движения, а ионы изменяют траекторию своего движения в зависимости от отношения массы к заряду m/z, что позволяет распределить ионы по их массам, определить массы ионов и их количество.
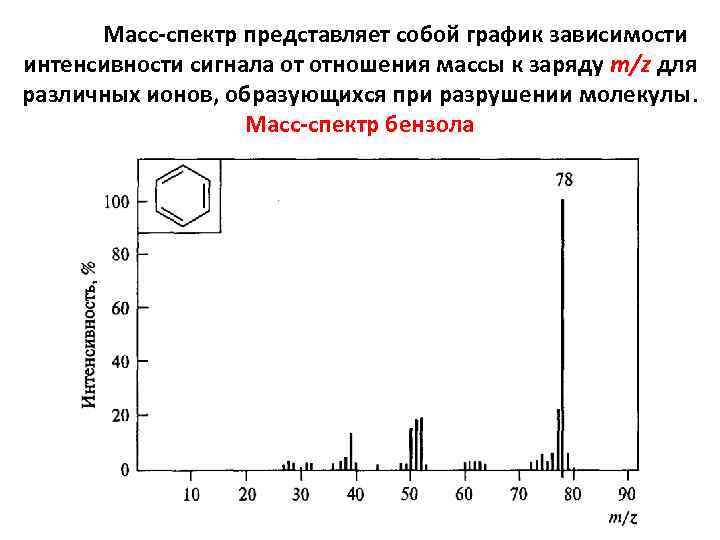 Масс-спектр представляет собой график зависимости интенсивности сигнала от отношения массы к заряду m/z для различных ионов, образующихся при разрушении молекулы. Масс-спектр бензола
Масс-спектр представляет собой график зависимости интенсивности сигнала от отношения массы к заряду m/z для различных ионов, образующихся при разрушении молекулы. Масс-спектр бензола
 • Высота пика с максимальной интенсивностью ( очевидно, это основной пик, соответствующий наиболее стабильному иону) принимается равной 100%. Интенсивность остальных пиков выражается в % от интенсивности основного пика. • Заряд образующихся ионов z обычно равен 1, поэтому отношение m/z совпадает с массой иона. • По масс спектру можно определить молекулярную массу, молекулярную формулу и структуру органического соединения.
• Высота пика с максимальной интенсивностью ( очевидно, это основной пик, соответствующий наиболее стабильному иону) принимается равной 100%. Интенсивность остальных пиков выражается в % от интенсивности основного пика. • Заряд образующихся ионов z обычно равен 1, поэтому отношение m/z совпадает с массой иона. • По масс спектру можно определить молекулярную массу, молекулярную формулу и структуру органического соединения.
 Определение молекулярной массы и молекулярной формулы • Наиболее интенсивный пик в спектре – необязательно пик молекулярного иона. Если при фрагментации молекулярного иона образуется более устойчивый карбокатион, стабилизированный электронными эффектами, то молекулярный пик имеет низкую интенсивность, а иногда может вообще отсутствовать в масс-спектре. • Для выявления молекулярного пика в случае его малой интенсивности следует иметь ввиду, что соединения, содержащие элементы С, H, O, S, галогены, имеют четное массовое число. В этом случае действует азотное правило: • Если в молекуле содержится нечетное число атомов азота, то массовое число молекулярного иона является нечетным. Если в молекуле содержится четное число атомов азота, то массовое число молекулярного иона является четным.
Определение молекулярной массы и молекулярной формулы • Наиболее интенсивный пик в спектре – необязательно пик молекулярного иона. Если при фрагментации молекулярного иона образуется более устойчивый карбокатион, стабилизированный электронными эффектами, то молекулярный пик имеет низкую интенсивность, а иногда может вообще отсутствовать в масс-спектре. • Для выявления молекулярного пика в случае его малой интенсивности следует иметь ввиду, что соединения, содержащие элементы С, H, O, S, галогены, имеют четное массовое число. В этом случае действует азотное правило: • Если в молекуле содержится нечетное число атомов азота, то массовое число молекулярного иона является нечетным. Если в молекуле содержится четное число атомов азота, то массовое число молекулярного иона является четным.
 Молекулярный ион (М+1) - присутствие изотопов 13 С и 2 Н Изотопный состав некоторых элементов
Молекулярный ион (М+1) - присутствие изотопов 13 С и 2 Н Изотопный состав некоторых элементов
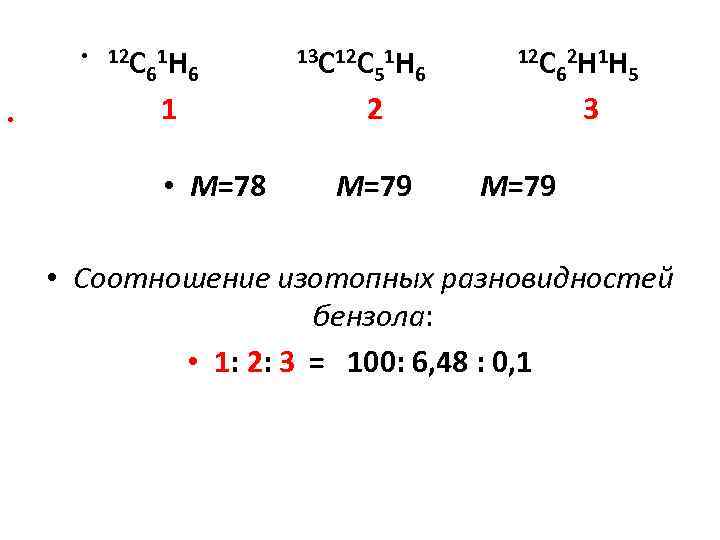 • 12 С 1 Н 6 6 • 1 • М=78 13 С 12 С 1 Н 5 6 12 С 2 Н 1 Н 6 5 2 М=79 3 М=79 • Соотношение изотопных разновидностей бензола: • 1: 2: 3 = 100: 6, 48 : 0, 1
• 12 С 1 Н 6 6 • 1 • М=78 13 С 12 С 1 Н 5 6 12 С 2 Н 1 Н 6 5 2 М=79 3 М=79 • Соотношение изотопных разновидностей бензола: • 1: 2: 3 = 100: 6, 48 : 0, 1
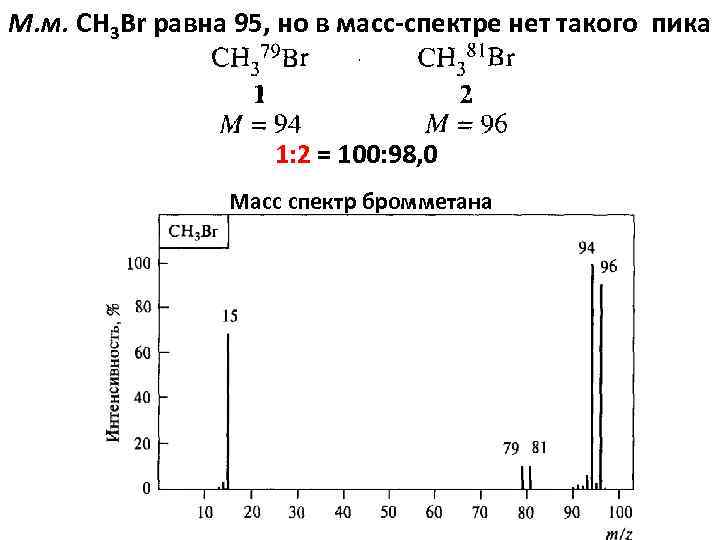 М. м. СH 3 Br равна 95, но в масс-спектре нет такого пика 1: 2 = 100: 98, 0 Масс спектр бромметана
М. м. СH 3 Br равна 95, но в масс-спектре нет такого пика 1: 2 = 100: 98, 0 Масс спектр бромметана
 Структуру органического соединения можно определить по результатам анализа осколочных и перегруппировочных ионов, образующихся при распаде молекулярного иона. • Направления фрагментации ионов определяется следующими факторами: • 1. Энергиями связи в анализируемой молекуле. При распаде ионов легче протекает разрыв связей с меньшей энергией. Энергия связи С-С < энергии связи С-Н, связи С-С легче разрываются, чем С=С. Связи С-Hal, С-О, C-N расщепляются легче, чем связи С-С. • 2. Стабильностью образующихся при фрагментации осколочных ионов и радикалов:
Структуру органического соединения можно определить по результатам анализа осколочных и перегруппировочных ионов, образующихся при распаде молекулярного иона. • Направления фрагментации ионов определяется следующими факторами: • 1. Энергиями связи в анализируемой молекуле. При распаде ионов легче протекает разрыв связей с меньшей энергией. Энергия связи С-С < энергии связи С-Н, связи С-С легче разрываются, чем С=С. Связи С-Hal, С-О, C-N расщепляются легче, чем связи С-С. • 2. Стабильностью образующихся при фрагментации осколочных ионов и радикалов:
 1. В алканах происходит разрыв С-С-связи у наиболее разветвленного атома С молекулярного иона с образованием наиболее стабильных третичных и вторичных карбкатионов: • Относительная интенсивность пиков образующихся осколочных ионов определяется стабильностью этих ионов.
1. В алканах происходит разрыв С-С-связи у наиболее разветвленного атома С молекулярного иона с образованием наиболее стабильных третичных и вторичных карбкатионов: • Относительная интенсивность пиков образующихся осколочных ионов определяется стабильностью этих ионов.
 2. В замещенных циклоалканах преимущественно наблюдается α-распад (разрыв связи в α-положении к циклу) молекулярного иона с отщеплением заместителя и образованием вторичного циклического карбокатиона: 3. Для алкенов характерен β-распад молекулярного иона с образованием резонансно-стабилизированного аллильного катиона m/z =41:
2. В замещенных циклоалканах преимущественно наблюдается α-распад (разрыв связи в α-положении к циклу) молекулярного иона с отщеплением заместителя и образованием вторичного циклического карбокатиона: 3. Для алкенов характерен β-распад молекулярного иона с образованием резонансно-стабилизированного аллильного катиона m/z =41:
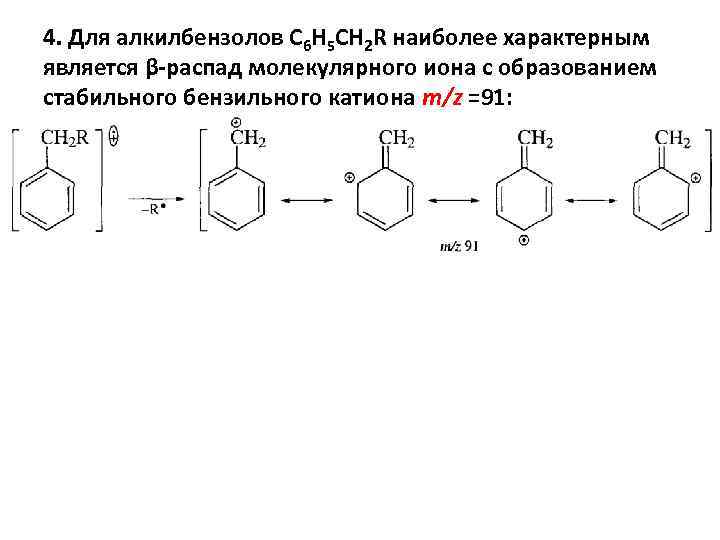 4. Для алкилбензолов С 6 Н 5 СН 2 R наиболее характерным является β-распад молекулярного иона с образованием стабильного бензильного катиона m/z =91:
4. Для алкилбензолов С 6 Н 5 СН 2 R наиболее характерным является β-распад молекулярного иона с образованием стабильного бензильного катиона m/z =91:
 5. В соединениях со связями С-O, C-S, C-N, C-Hal наблюдается α-распад, т. е. разрыв связи углерод- гетероатом молекулярного иона: • Интенсивный пик R+ наблюдается только для галогенпроизводных.
5. В соединениях со связями С-O, C-S, C-N, C-Hal наблюдается α-распад, т. е. разрыв связи углерод- гетероатом молекулярного иона: • Интенсивный пик R+ наблюдается только для галогенпроизводных.
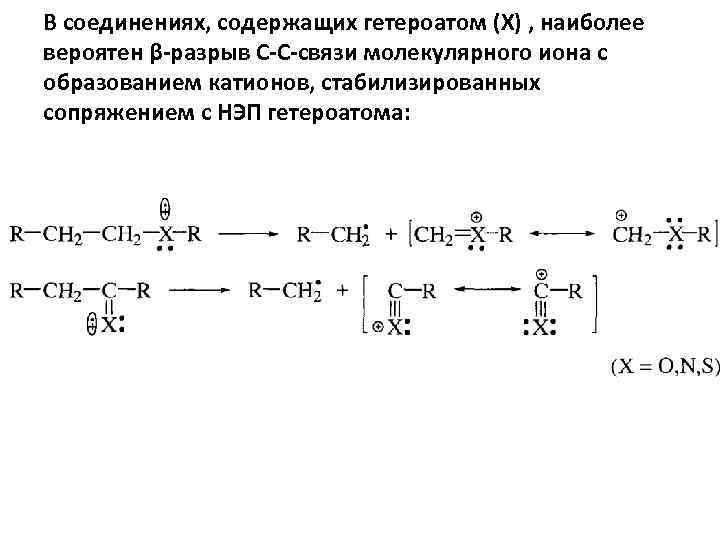 В соединениях, содержащих гетероатом (Х) , наиболее вероятен β-разрыв С-С-связи молекулярного иона с образованием катионов, стабилизированных сопряжением с НЭП гетероатома:
В соединениях, содержащих гетероатом (Х) , наиболее вероятен β-разрыв С-С-связи молекулярного иона с образованием катионов, стабилизированных сопряжением с НЭП гетероатома:
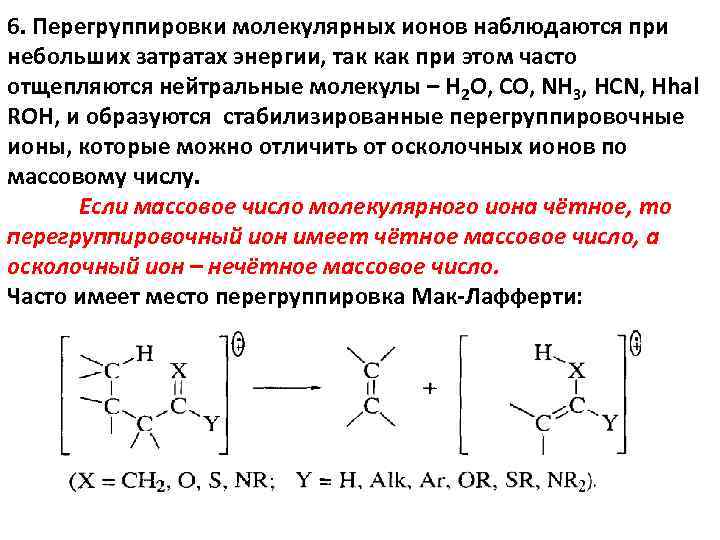 6. Перегруппировки молекулярных ионов наблюдаются при небольших затратах энергии, так как при этом часто отщепляются нейтральные молекулы – Н 2 О, CO, NH 3, HCN, Нhal ROH, и образуются стабилизированные перегруппировочные ионы, которые можно отличить от осколочных ионов по массовому числу. Если массовое число молекулярного иона чётное, то перегруппировочный ион имеет чётное массовое число, а осколочный ион – нечётное массовое число. Часто имеет место перегруппировка Мак-Лафферти:
6. Перегруппировки молекулярных ионов наблюдаются при небольших затратах энергии, так как при этом часто отщепляются нейтральные молекулы – Н 2 О, CO, NH 3, HCN, Нhal ROH, и образуются стабилизированные перегруппировочные ионы, которые можно отличить от осколочных ионов по массовому числу. Если массовое число молекулярного иона чётное, то перегруппировочный ион имеет чётное массовое число, а осколочный ион – нечётное массовое число. Часто имеет место перегруппировка Мак-Лафферти:
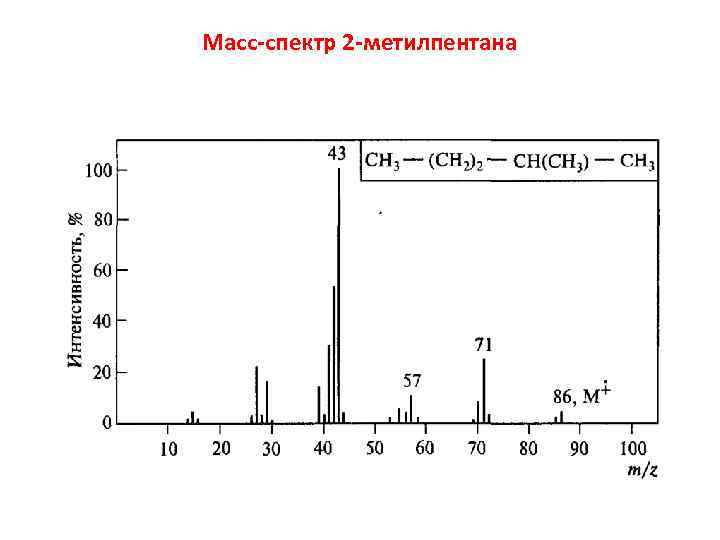 Масс-спектр 2 -метилпентана
Масс-спектр 2 -метилпентана
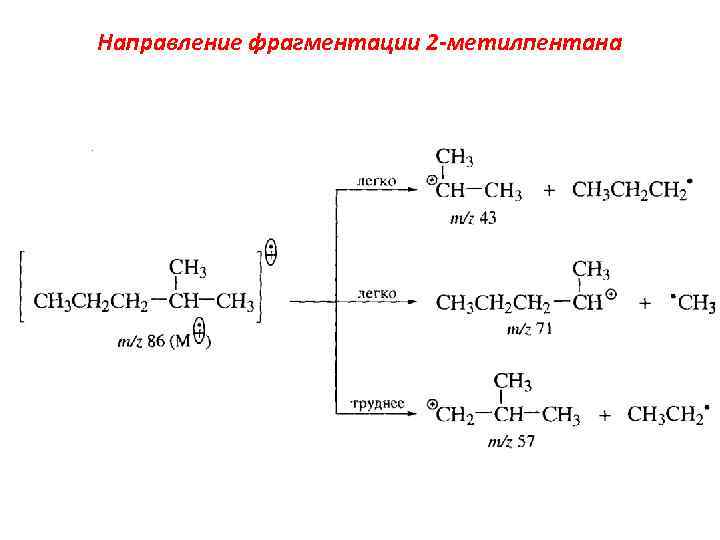 Направление фрагментации 2 -метилпентана
Направление фрагментации 2 -метилпентана
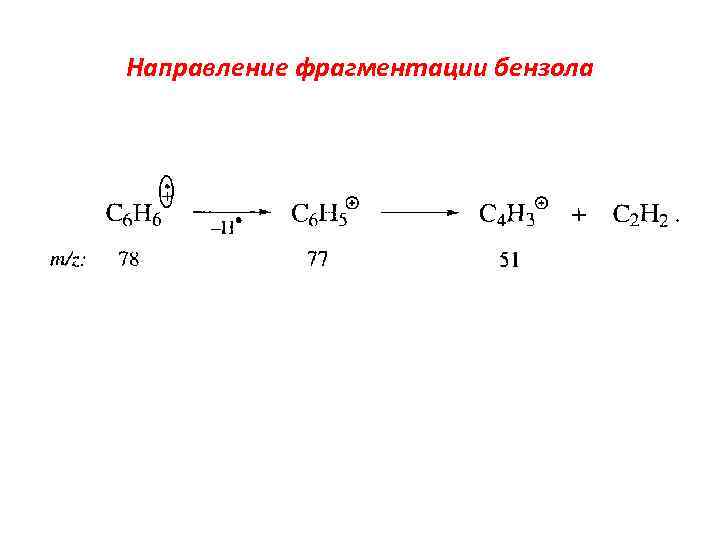 Направление фрагментации бензола
Направление фрагментации бензола


