масс - спектрометрия.ppt
- Количество слайдов: 39
 МАСС – СПЕКТРОМЕТРИЯ
МАСС – СПЕКТРОМЕТРИЯ
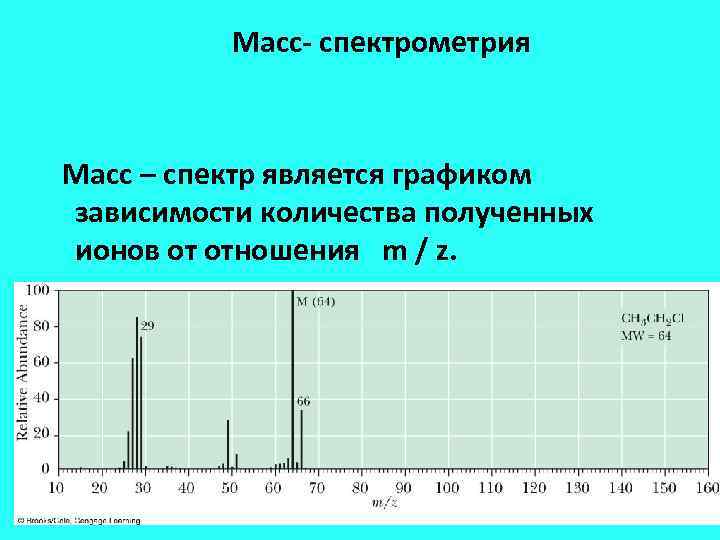 Масс- спектрометрия Масс – спектр является графиком зависимости количества полученных ионов от отношения m / z.
Масс- спектрометрия Масс – спектр является графиком зависимости количества полученных ионов от отношения m / z.
 Масс- спектроскопия Масс – спектрометрия решает следующие аналитические задачи: » определение структуры веществ » определение молярной массы » определение молекулярной формулы (элементного состава) » изучение механизмов реакций в органической химии » определение изотопного состава
Масс- спектроскопия Масс – спектрометрия решает следующие аналитические задачи: » определение структуры веществ » определение молярной массы » определение молекулярной формулы (элементного состава) » изучение механизмов реакций в органической химии » определение изотопного состава
 Основные узлы масс – спектрометра • • • система ввода пробы ионизатор масс – анализатор детектор регистрирующее устройство
Основные узлы масс – спектрометра • • • система ввода пробы ионизатор масс – анализатор детектор регистрирующее устройство
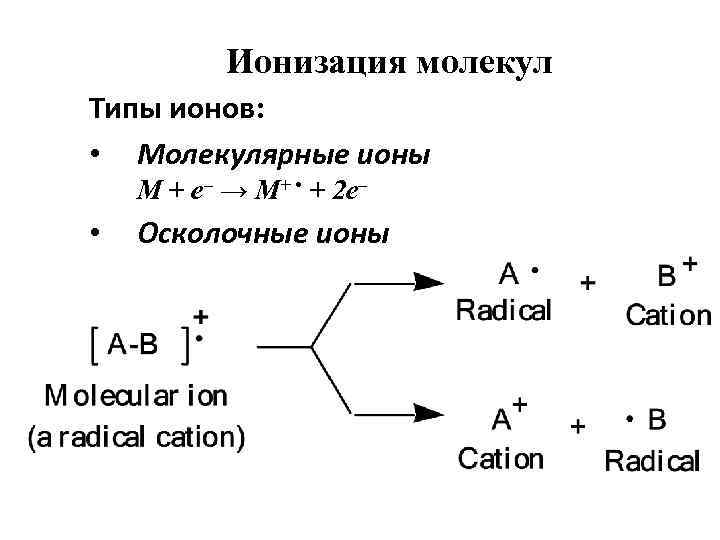 Ионизация молекул Типы ионов: • Молекулярные ионы М + е– → М+ • + 2 е– • Осколочные ионы
Ионизация молекул Типы ионов: • Молекулярные ионы М + е– → М+ • + 2 е– • Осколочные ионы
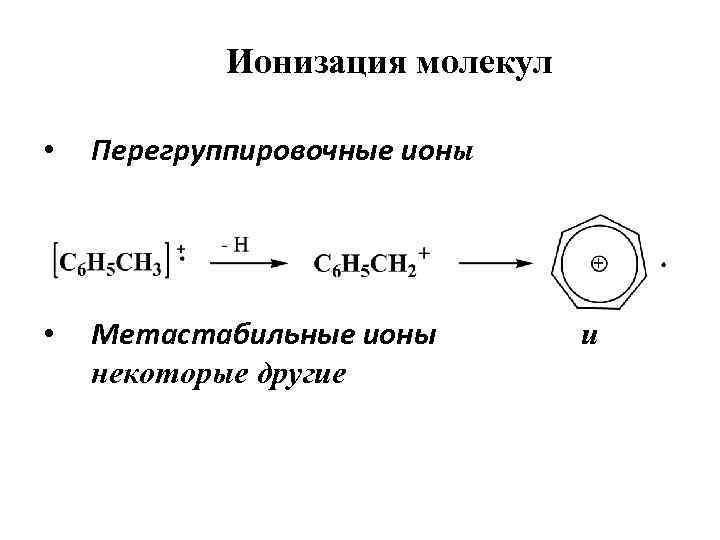 Ионизация молекул • Перегруппировочные ионы • Метастабильные ионы некоторые другие и
Ионизация молекул • Перегруппировочные ионы • Метастабильные ионы некоторые другие и
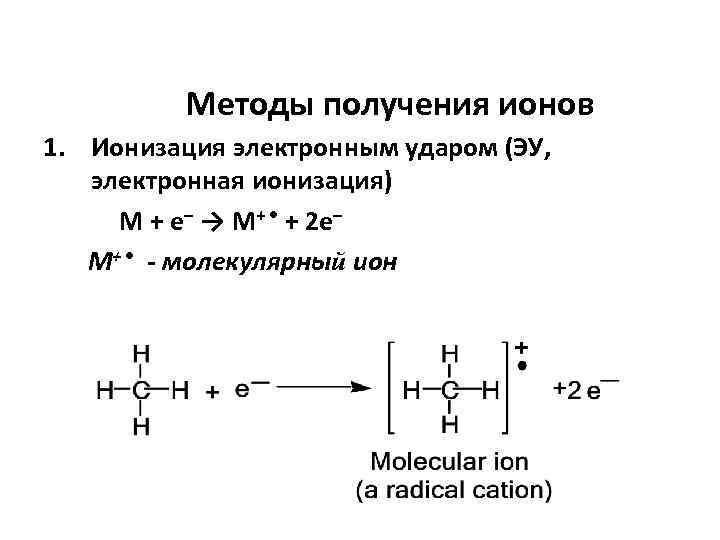 Методы получения ионов 1. Ионизация электронным ударом (ЭУ, электронная ионизация) М + е– → М+ • + 2 е– М+ • - молекулярный ион
Методы получения ионов 1. Ионизация электронным ударом (ЭУ, электронная ионизация) М + е– → М+ • + 2 е– М+ • - молекулярный ион
 Методы получения ионов 2. Химическая ионизация СН 4 → СН 4+ + ∙→ СН + + СН ∙ и т. д. СН 4 + СН 4 5 3 Возможные реакции ионов газа – реагента с молекулами анализируемого образца • протонирование M + СH 5+ = СH 4 + MH+ 2. электрофильное присоединение M + NH + = [M + NH ]+ 4 4
Методы получения ионов 2. Химическая ионизация СН 4 → СН 4+ + ∙→ СН + + СН ∙ и т. д. СН 4 + СН 4 5 3 Возможные реакции ионов газа – реагента с молекулами анализируемого образца • протонирование M + СH 5+ = СH 4 + MH+ 2. электрофильное присоединение M + NH + = [M + NH ]+ 4 4
 Методы получения ионов 3. Фотоионизация М + hν = М+ • + е– 4. Ионизация электрическим полем 5. Десорбционная ионизация 5. 1. Десорбционная химическая ионизация 5. 2. Бомбардировка быстрыми атомами 5. 3. Плазменная десорбция 5. 4. Лазерная десорбция – ионизация с помощью матрицы (MALDI) 5. 5. Полевая ионизация 5. 6. Полевая десорбция
Методы получения ионов 3. Фотоионизация М + hν = М+ • + е– 4. Ионизация электрическим полем 5. Десорбционная ионизация 5. 1. Десорбционная химическая ионизация 5. 2. Бомбардировка быстрыми атомами 5. 3. Плазменная десорбция 5. 4. Лазерная десорбция – ионизация с помощью матрицы (MALDI) 5. 5. Полевая ионизация 5. 6. Полевая десорбция
 Применение масс – спектрометрии • Определение молекулярной массы. • Определение элементного состава. «Азотное» правило. В молекуле с четной молекулярной массой число атомов азота четное или равно нулю. Нечетная молекулярная масса говорит о наличии нечетного числа атомов азота в молекуле. Эквивалент двойной связи показывает число двойных связей в молекуле. Можно рассчитать для соединений, содержащих атомы H, C, N, O, F, Cl, Br, I, зная элементный состав: ЭД = 1 + С − ½(H + F + Cl + I) + ½N
Применение масс – спектрометрии • Определение молекулярной массы. • Определение элементного состава. «Азотное» правило. В молекуле с четной молекулярной массой число атомов азота четное или равно нулю. Нечетная молекулярная масса говорит о наличии нечетного числа атомов азота в молекуле. Эквивалент двойной связи показывает число двойных связей в молекуле. Можно рассчитать для соединений, содержащих атомы H, C, N, O, F, Cl, Br, I, зная элементный состав: ЭД = 1 + С − ½(H + F + Cl + I) + ½N
 Установление структуры • Устойчивость и интенсивность пиков молекулярного иона: Ароматические соединения > сопряженные алкены > циклические соединения > органические сульфиды > короткие н-алканы >меркаптаны Кетоны > амины > сложные эфиры > простые эфиры > карбоновые кислоты, альдегиды, амиды.
Установление структуры • Устойчивость и интенсивность пиков молекулярного иона: Ароматические соединения > сопряженные алкены > циклические соединения > органические сульфиды > короткие н-алканы >меркаптаны Кетоны > амины > сложные эфиры > простые эфиры > карбоновые кислоты, альдегиды, амиды.
 Некоторые закономерности фрагментации • Спектр, содержащий много осколочных ионов, интенсивность которых увеличивается с уменьшением m/z, преимущественно соответствует алифатическому углеводороду или его производному
Некоторые закономерности фрагментации • Спектр, содержащий много осколочных ионов, интенсивность которых увеличивается с уменьшением m/z, преимущественно соответствует алифатическому углеводороду или его производному
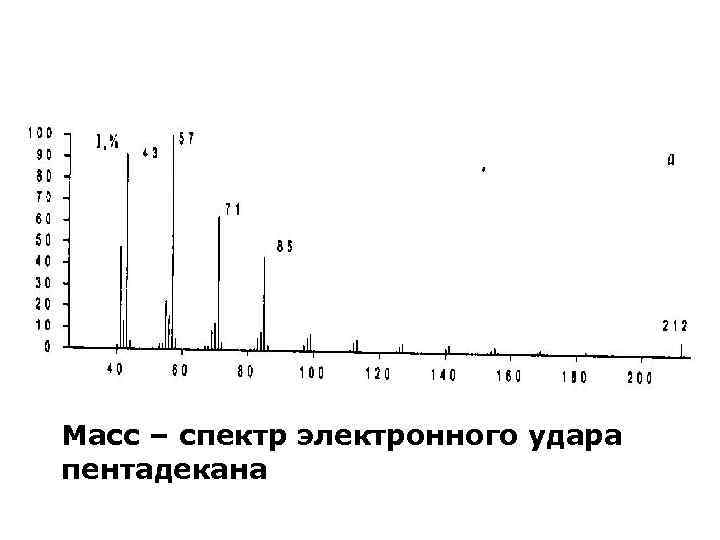 Масс – спектр электронного удара пентадекана
Масс – спектр электронного удара пентадекана
 Некоторые закономерности фрагментации • Интенсивность молекулярного иона уменьшается с увеличением разветвления в молекуле. • Ароматические соединения имеют интенсивный пик молекулярного иона
Некоторые закономерности фрагментации • Интенсивность молекулярного иона уменьшается с увеличением разветвления в молекуле. • Ароматические соединения имеют интенсивный пик молекулярного иона
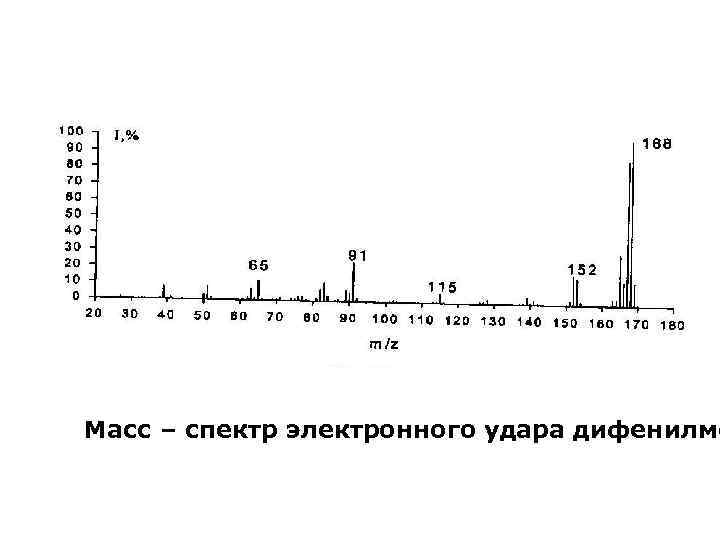 Масс – спектр электронного удара дифенилме
Масс – спектр электронного удара дифенилме
 Некоторые закономерности фрагментации • Интенсивность молекулярного иона в гомологическом ряду уменьшается с увеличением массы (исключение составляют жирные кислоты). • Вероятность разрыва связи С – Н уменьшается с увеличением длины цепи углеводорода.
Некоторые закономерности фрагментации • Интенсивность молекулярного иона в гомологическом ряду уменьшается с увеличением массы (исключение составляют жирные кислоты). • Вероятность разрыва связи С – Н уменьшается с увеличением длины цепи углеводорода.
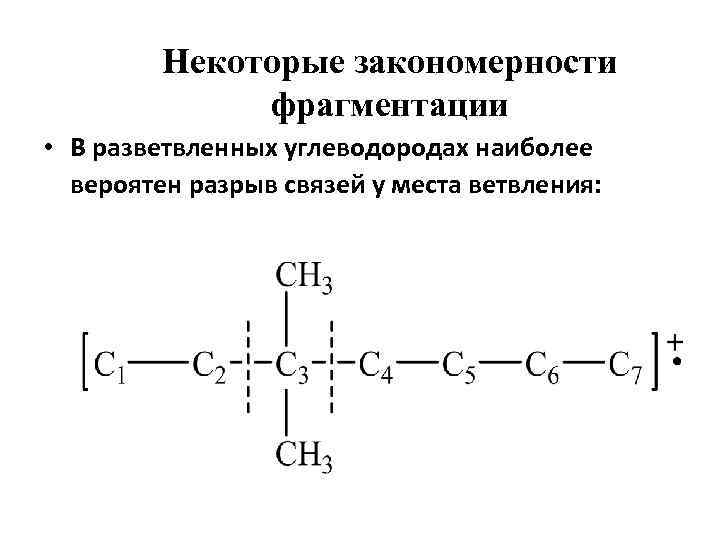 Некоторые закономерности фрагментации • В разветвленных углеводородах наиболее вероятен разрыв связей у места ветвления:
Некоторые закономерности фрагментации • В разветвленных углеводородах наиболее вероятен разрыв связей у места ветвления:
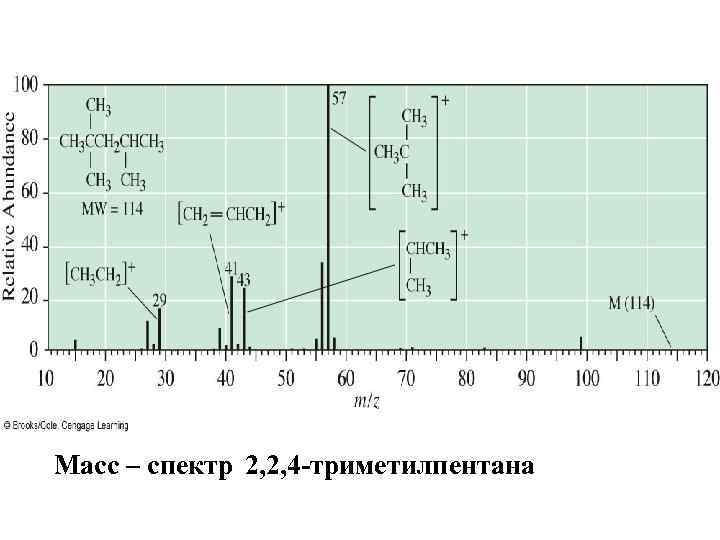 Масс – спектр 2, 2, 4 -триметилпентана
Масс – спектр 2, 2, 4 -триметилпентана
 Некоторые закономерности фрагментации • Отщепление по связи с алкильным заместителем возможно из-за устойчивости образующегося карбониевого иона: R 3 C+ > R 2 CH+ > RCH 2+ > CH 3+ Легче всего удаляется наиболее объемный заместитель. • Двойные связи и ароматические кольца стабилизируют молекулярный ион.
Некоторые закономерности фрагментации • Отщепление по связи с алкильным заместителем возможно из-за устойчивости образующегося карбониевого иона: R 3 C+ > R 2 CH+ > RCH 2+ > CH 3+ Легче всего удаляется наиболее объемный заместитель. • Двойные связи и ароматические кольца стабилизируют молекулярный ион.
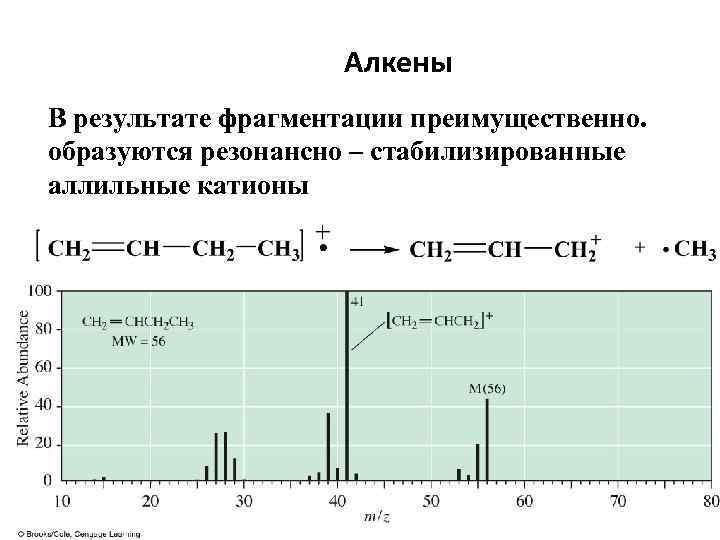 Алкены В результате фрагментации преимущественно. образуются резонансно – стабилизированные аллильные катионы
Алкены В результате фрагментации преимущественно. образуются резонансно – стабилизированные аллильные катионы
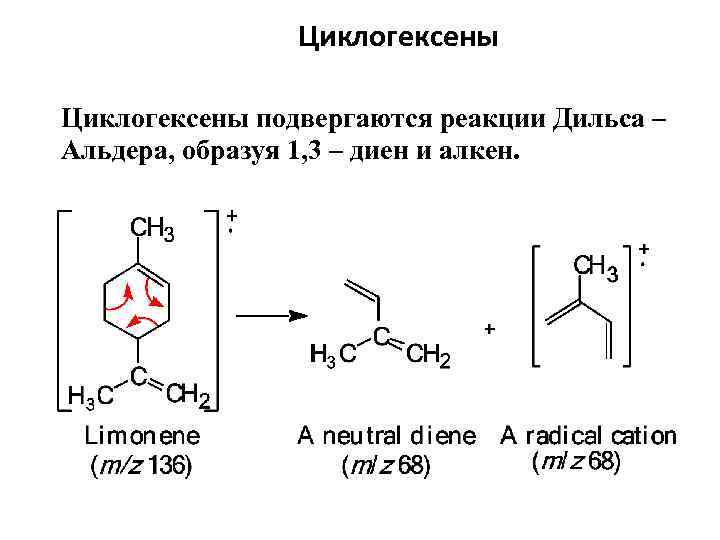 Циклогексены подвергаются реакции Дильса – Альдера, образуя 1, 3 – диен и алкен.
Циклогексены подвергаются реакции Дильса – Альдера, образуя 1, 3 – диен и алкен.
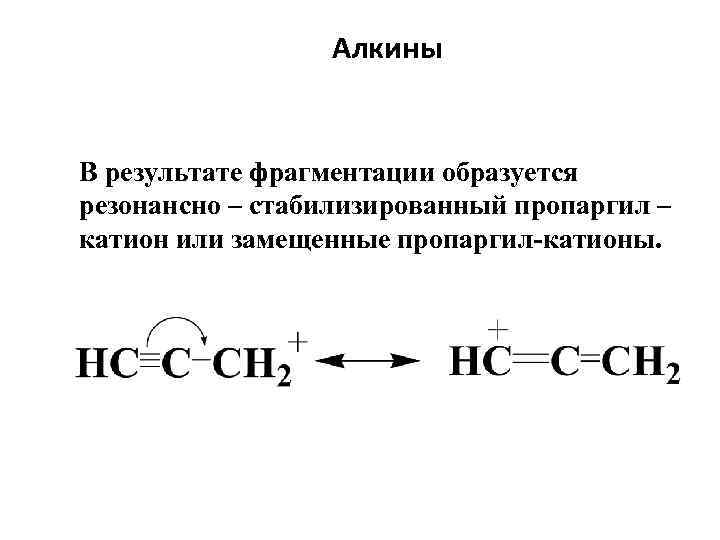 Алкины В результате фрагментации образуется резонансно – стабилизированный пропаргил – катион или замещенные пропаргил-катионы.
Алкины В результате фрагментации образуется резонансно – стабилизированный пропаргил – катион или замещенные пропаргил-катионы.
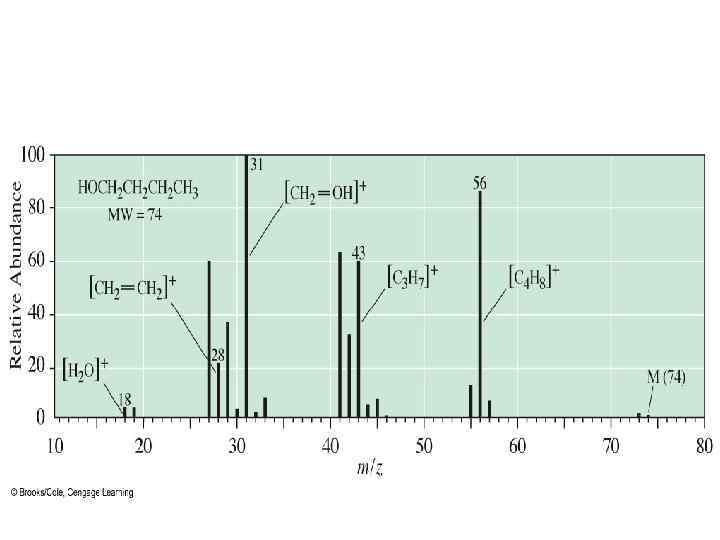
 Спирты • Одним из общих направлений фрагментации спиртов является потеря Н 2 О, с образованием соответствующего пика М – 18 • Другим направлением является отрыв алкильной группы от атома углерода, связанного с группой ОН, при этом образуется оксониевый ион с m/z = 31 [CH 2=OH+] и алкильный радикал
Спирты • Одним из общих направлений фрагментации спиртов является потеря Н 2 О, с образованием соответствующего пика М – 18 • Другим направлением является отрыв алкильной группы от атома углерода, связанного с группой ОН, при этом образуется оксониевый ион с m/z = 31 [CH 2=OH+] и алкильный радикал
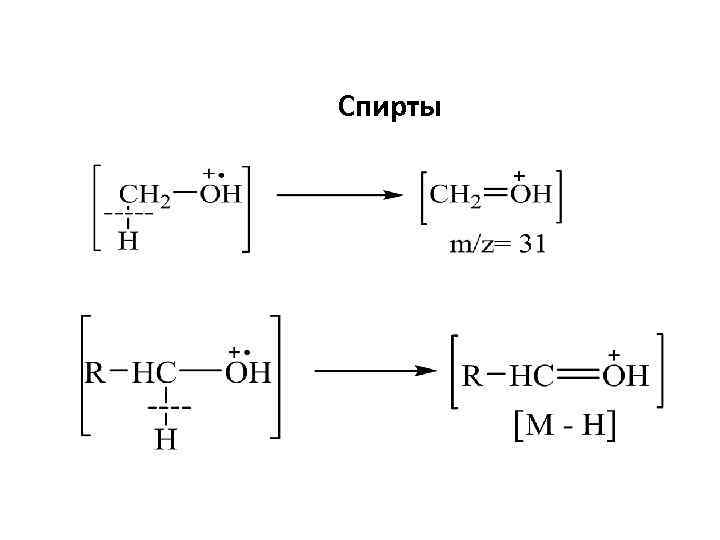 Спирты
Спирты
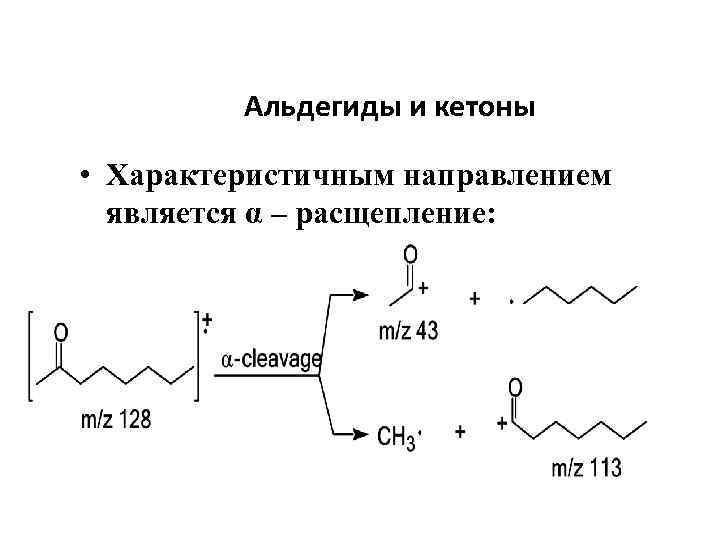 Альдегиды и кетоны • Характеристичным направлением является α – расщепление:
Альдегиды и кетоны • Характеристичным направлением является α – расщепление:
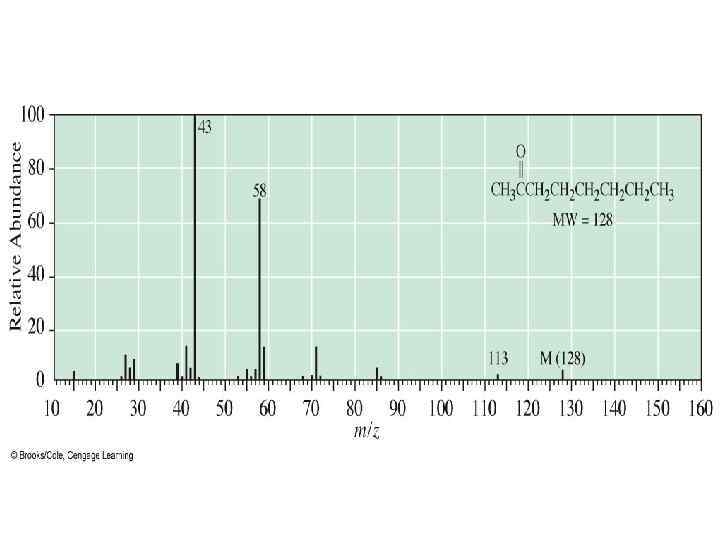
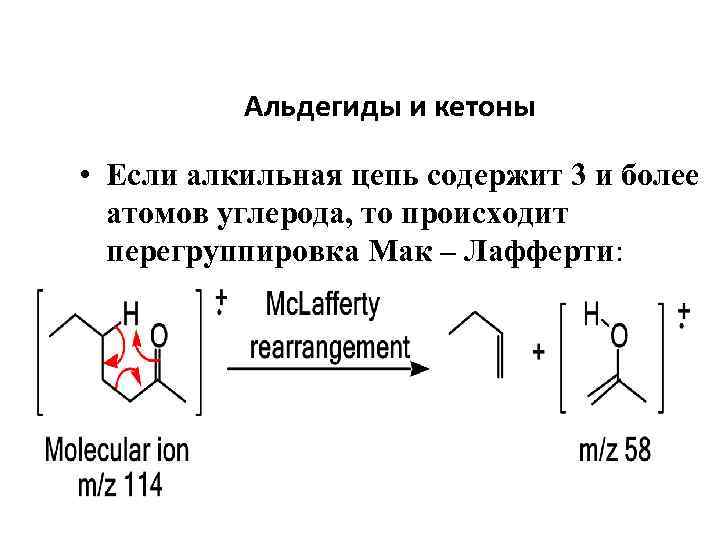 Альдегиды и кетоны • Если алкильная цепь содержит 3 и более атомов углерода, то происходит перегруппировка Мак – Лафферти:
Альдегиды и кетоны • Если алкильная цепь содержит 3 и более атомов углерода, то происходит перегруппировка Мак – Лафферти:
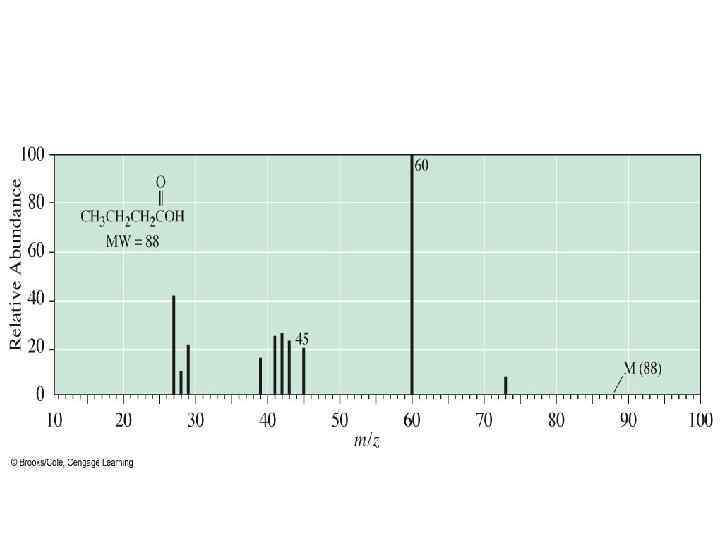
![Карбоновые кислоты Характеристичными направлениями являются: • α – расщепление с образованием иона [COOH+] c Карбоновые кислоты Характеристичными направлениями являются: • α – расщепление с образованием иона [COOH+] c](https://present5.com/presentation/127904055_384452550/image-29.jpg) Карбоновые кислоты Характеристичными направлениями являются: • α – расщепление с образованием иона [COOH+] c m/z = 45
Карбоновые кислоты Характеристичными направлениями являются: • α – расщепление с образованием иона [COOH+] c m/z = 45
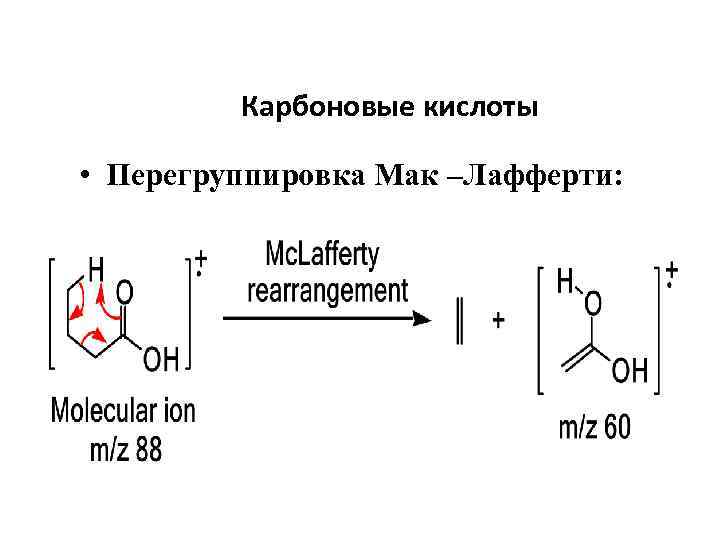 Карбоновые кислоты • Перегруппировка Мак –Лафферти:
Карбоновые кислоты • Перегруппировка Мак –Лафферти:
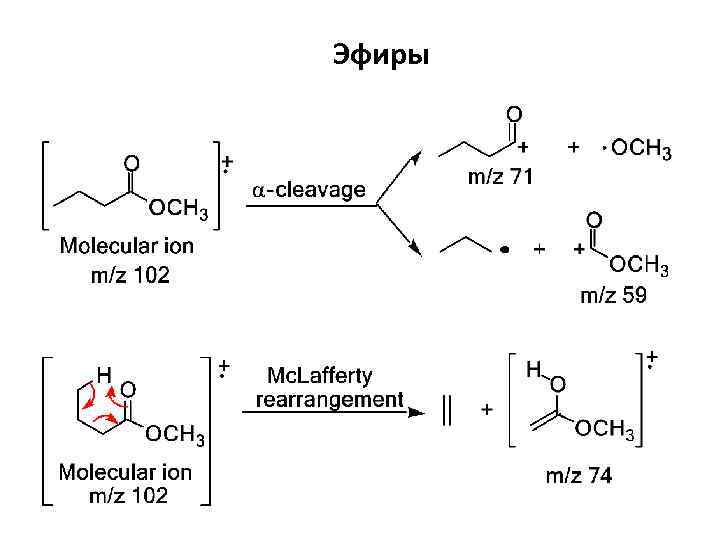
 Эфиры Характеристичными направлениями являются: • α – расщепление • Перегруппировка Мак –Лафферти:
Эфиры Характеристичными направлениями являются: • α – расщепление • Перегруппировка Мак –Лафферти:
 Эфиры
Эфиры
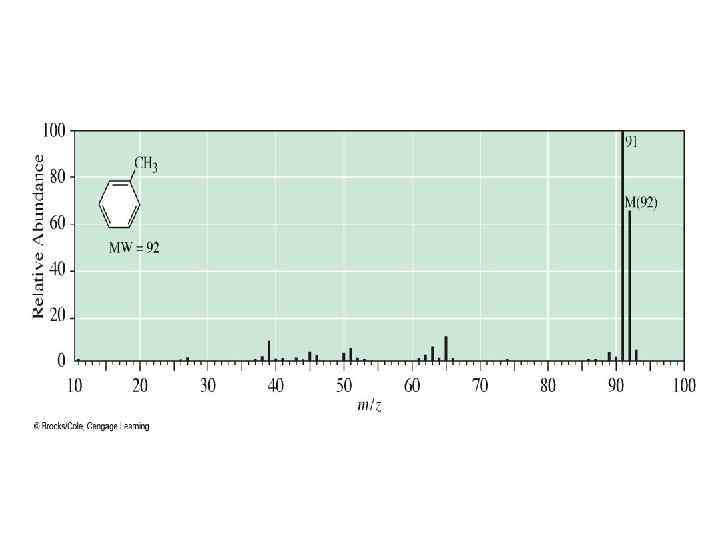
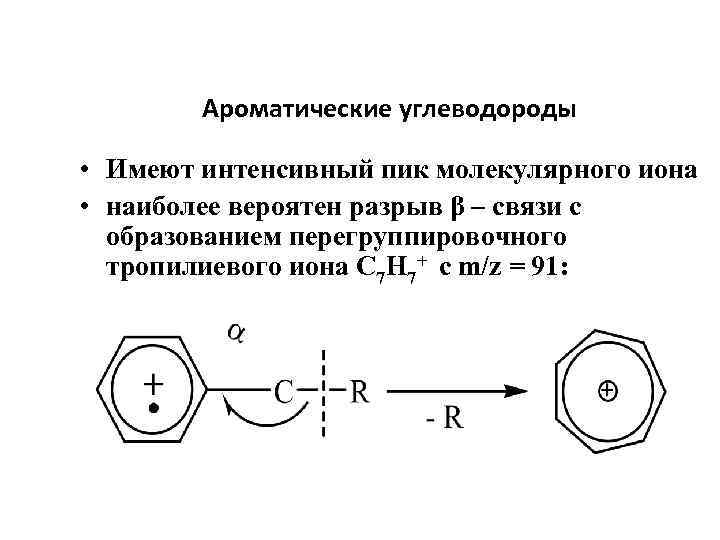 Ароматические углеводороды • Имеют интенсивный пик молекулярного иона • наиболее вероятен разрыв β – связи с образованием перегруппировочного тропилиевого иона С 7 Н 7+ c m/z = 91:
Ароматические углеводороды • Имеют интенсивный пик молекулярного иона • наиболее вероятен разрыв β – связи с образованием перегруппировочного тропилиевого иона С 7 Н 7+ c m/z = 91:
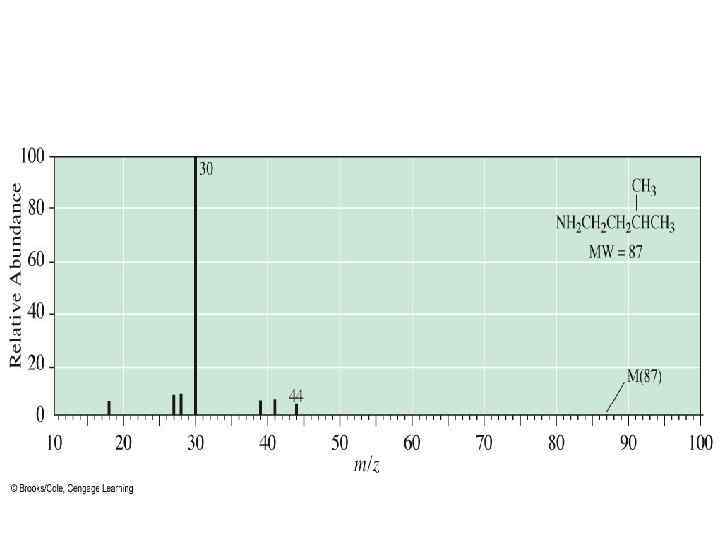
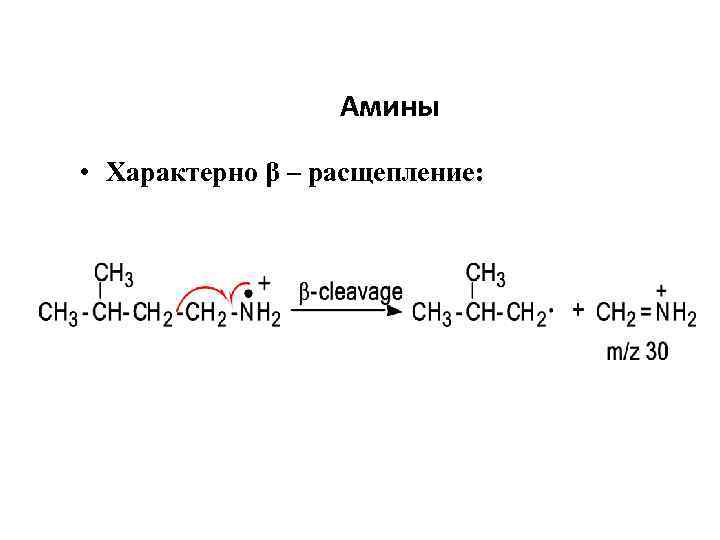 Амины • Характерно β – расщепление:
Амины • Характерно β – расщепление:
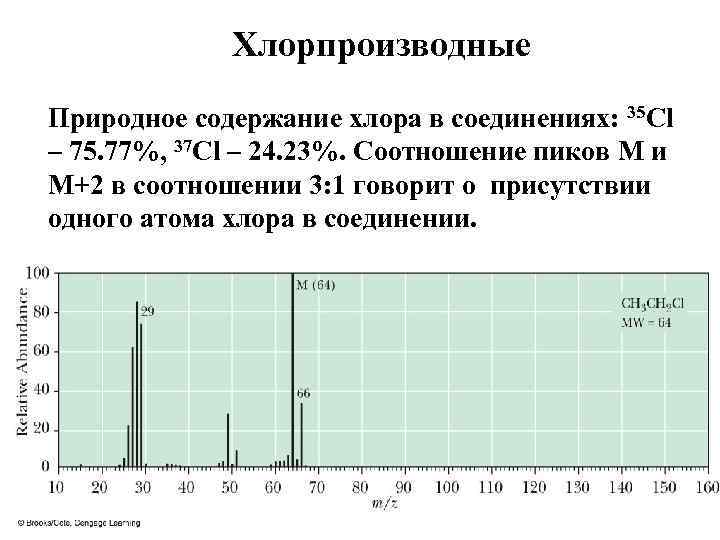 Хлорпроизводные Природное содержание хлора в соединениях: 35 Cl – 75. 77%, 37 Cl – 24. 23%. Соотношение пиков М и М+2 в соотношении 3: 1 говорит о присутствии одного атома хлора в соединении.
Хлорпроизводные Природное содержание хлора в соединениях: 35 Cl – 75. 77%, 37 Cl – 24. 23%. Соотношение пиков М и М+2 в соотношении 3: 1 говорит о присутствии одного атома хлора в соединении.
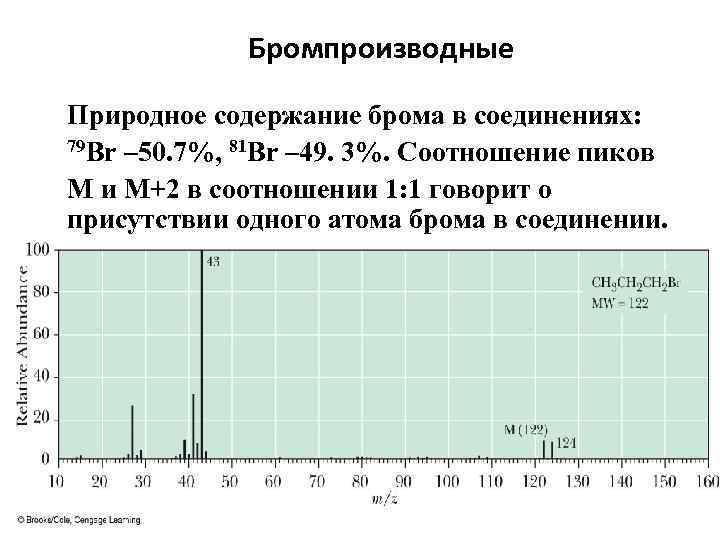 Бромпроизводные Природное содержание брома в соединениях: 79 Br – 50. 7%, 81 Br – 49. 3%. Соотношение пиков М и М+2 в соотношении 1: 1 говорит о присутствии одного атома брома в соединении.
Бромпроизводные Природное содержание брома в соединениях: 79 Br – 50. 7%, 81 Br – 49. 3%. Соотношение пиков М и М+2 в соотношении 1: 1 говорит о присутствии одного атома брома в соединении.


