15.Хромато-масс-спектрометрия.ppt
- Количество слайдов: 131
 Масс-спектрометрия и хромато-масс -спектрометрия высокого разрешения Лекция № 15
Масс-спектрометрия и хромато-масс -спектрометрия высокого разрешения Лекция № 15
 Хроматография – метод разделения веществ, основанный на разности распределения веществ между двумя фазами – подвижной (называемой еще элюентом) и неподвижной (обычно сорбент с развитой поверхностью, часто полимерной природы). Немного иное определение: метод основан на различии в скоростях движения концентрационных зон разных веществ, которые перемещаются в потоке элюента вдоль слоя неподвижной фазы, причем исследуемые соединения распределены между обеими фазами. Хроматография была открыта и предложена как метод исследования русским ученым Михаилом Семеновичем Цветом в 1903 г. В зависимости от агрегатного состояния элюента (подвижной фазы) хроматографию делят на газовую и жидкостную. В хромато-масс-спектрометрии применяются оба типа хроматографирования.
Хроматография – метод разделения веществ, основанный на разности распределения веществ между двумя фазами – подвижной (называемой еще элюентом) и неподвижной (обычно сорбент с развитой поверхностью, часто полимерной природы). Немного иное определение: метод основан на различии в скоростях движения концентрационных зон разных веществ, которые перемещаются в потоке элюента вдоль слоя неподвижной фазы, причем исследуемые соединения распределены между обеими фазами. Хроматография была открыта и предложена как метод исследования русским ученым Михаилом Семеновичем Цветом в 1903 г. В зависимости от агрегатного состояния элюента (подвижной фазы) хроматографию делят на газовую и жидкостную. В хромато-масс-спектрометрии применяются оба типа хроматографирования.
 Характеристики вещества, получаемые в хроматографическом методе Время удержания (время выхода) – время, проходящее между моментом ввода анализируемой пробы в колонку, и моментом выхода вершины пика вещества из колонки. Объем удержания – объем газа/жидкости-носителя, который проходит по хроматографической колонке с момента ввода анализируемой пробы в колонку до момента выхода вершины пика вещества из колонки. Индекс удержания – отношение времен удержания какого-то стандартного вещества (обычно для неполярных колонок какого -либо углеводорода известного строения) и определяемого вещества. Для одинаковых по химическому составу колонок является постоянной величиной. Площадь хроматографического пика – характеризующий количество вещества в пробе. параметр,
Характеристики вещества, получаемые в хроматографическом методе Время удержания (время выхода) – время, проходящее между моментом ввода анализируемой пробы в колонку, и моментом выхода вершины пика вещества из колонки. Объем удержания – объем газа/жидкости-носителя, который проходит по хроматографической колонке с момента ввода анализируемой пробы в колонку до момента выхода вершины пика вещества из колонки. Индекс удержания – отношение времен удержания какого-то стандартного вещества (обычно для неполярных колонок какого -либо углеводорода известного строения) и определяемого вещества. Для одинаковых по химическому составу колонок является постоянной величиной. Площадь хроматографического пика – характеризующий количество вещества в пробе. параметр,
 Стыковка хроматографа и масс-спектрометра, ограничения, накладываемые при этом на метод анализа Малые объемы пробы (1 -10 мкл), малая (<1%) концентрация образца (обусловлено высокой чувствительностью методов газовой хроматографии и масс-спектрального анализа Масс-анализатор с малым временем развертки масс-спектра Создание соединения-интерфейса между масс-анализатором и хроматографом: прогреваемое, инертное к проходящим через него соединениям Сохранение высокого вакуума в масс-анализаторе при стыковке с хроматографом Решение: капиллярная хроматографическая колонка, малый расход газа или раствора носителя, применение газовых молекулярных сепараторов, квадрупольный или времяпролетный масс-анализатор, анализ соединений по характеристическим ионам
Стыковка хроматографа и масс-спектрометра, ограничения, накладываемые при этом на метод анализа Малые объемы пробы (1 -10 мкл), малая (<1%) концентрация образца (обусловлено высокой чувствительностью методов газовой хроматографии и масс-спектрального анализа Масс-анализатор с малым временем развертки масс-спектра Создание соединения-интерфейса между масс-анализатором и хроматографом: прогреваемое, инертное к проходящим через него соединениям Сохранение высокого вакуума в масс-анализаторе при стыковке с хроматографом Решение: капиллярная хроматографическая колонка, малый расход газа или раствора носителя, применение газовых молекулярных сепараторов, квадрупольный или времяпролетный масс-анализатор, анализ соединений по характеристическим ионам
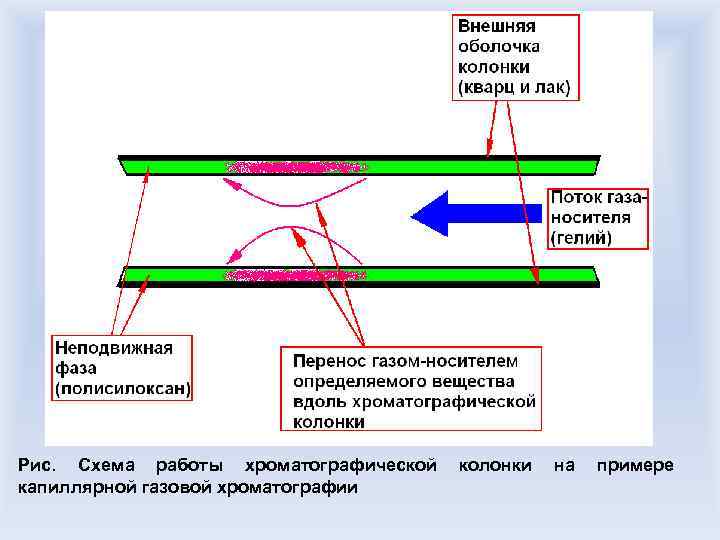 Рис. Схема работы хроматографической колонки на примере капиллярной газовой хроматографии
Рис. Схема работы хроматографической колонки на примере капиллярной газовой хроматографии
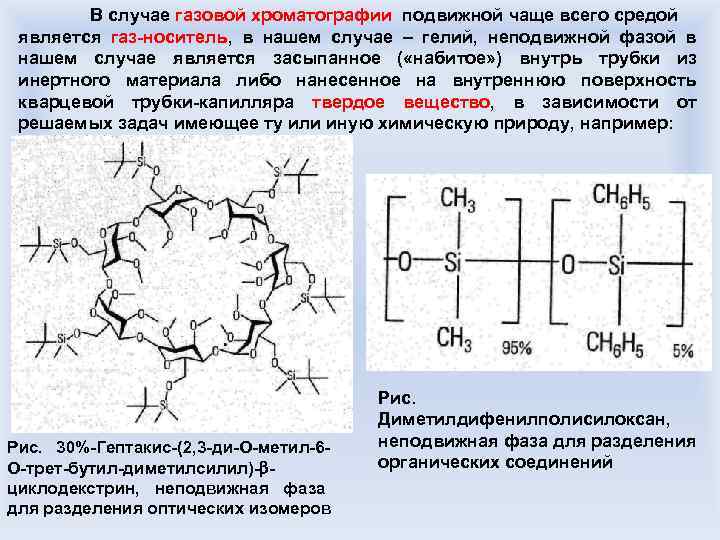 В случае газовой хроматографии подвижной чаще всего средой является газ-носитель, в нашем случае – гелий, неподвижной фазой в нашем случае является засыпанное ( «набитое» ) внутрь трубки из инертного материала либо нанесенное на внутреннюю поверхность кварцевой трубки-капилляра твердое вещество, в зависимости от решаемых задач имеющее ту или иную химическую природу, например: Рис. 30%-Гептакис-(2, 3 -ди-О-метил-6 О-трет-бутил-диметилсилил)- циклодекстрин, неподвижная фаза для разделения оптических изомеров Рис. Диметилдифенилполисилоксан, неподвижная фаза для разделения органических соединений
В случае газовой хроматографии подвижной чаще всего средой является газ-носитель, в нашем случае – гелий, неподвижной фазой в нашем случае является засыпанное ( «набитое» ) внутрь трубки из инертного материала либо нанесенное на внутреннюю поверхность кварцевой трубки-капилляра твердое вещество, в зависимости от решаемых задач имеющее ту или иную химическую природу, например: Рис. 30%-Гептакис-(2, 3 -ди-О-метил-6 О-трет-бутил-диметилсилил)- циклодекстрин, неподвижная фаза для разделения оптических изомеров Рис. Диметилдифенилполисилоксан, неподвижная фаза для разделения органических соединений
 Капиллярная газовая хроматографическая колонка HP-5 MS общего назначения, длина 30 м, внутреннний диаметр 0, 25 мм, внешний диаметр 0. 30 мм Капиллярная газовая хроматографическая колонка HP-5 MS, установленная в хроматограф
Капиллярная газовая хроматографическая колонка HP-5 MS общего назначения, длина 30 м, внутреннний диаметр 0, 25 мм, внешний диаметр 0. 30 мм Капиллярная газовая хроматографическая колонка HP-5 MS, установленная в хроматограф
 Возможности газовых хромато-массспектрометров 1. Автоматический ввод образца/серии образцов. 2. Диапазон измеряемых масс от 10 до 850 а. е. м. 3. Программируемое изменение хроматографической колонки от -50 до 400 С. температуры 4. Анализ жидких проб – веществ в растворе. 5. Возможность анализа легкокипящих образцов (температура кипения которых меньше либо больше температуры кипения растворителя). 6. Возможность подбора хроматографической колонки под узкоспециализированные задачи: анализ нефтепродуктов, лекарственных препаратов, разделение оптических изомеров и т. д. 7. Возможность подключения других модулей (в частности, термоаналитической приставки)
Возможности газовых хромато-массспектрометров 1. Автоматический ввод образца/серии образцов. 2. Диапазон измеряемых масс от 10 до 850 а. е. м. 3. Программируемое изменение хроматографической колонки от -50 до 400 С. температуры 4. Анализ жидких проб – веществ в растворе. 5. Возможность анализа легкокипящих образцов (температура кипения которых меньше либо больше температуры кипения растворителя). 6. Возможность подбора хроматографической колонки под узкоспециализированные задачи: анализ нефтепродуктов, лекарственных препаратов, разделение оптических изомеров и т. д. 7. Возможность подключения других модулей (в частности, термоаналитической приставки)
 Возможности масс-спектрометра высокого разрешения Thermo Electron DFS 1. При использовании штока прямого ввода для химической ионизации возможен нагрев образца до температуры 1600 С 2. При использовании штока прямого ввода возможен нагрев образца до температуры 360 С 3. Возможность ввода пробы через газовый хроматограф. 4. Диапазон измеряемых масс до 6 000 а. е. м. 5. Диапазон точно (до 4 знака после запятой) определяемых масс до 1 000 а. е. м. (зависит от наличия стандартов) 6. Ручной прямой ввод образца в масс-спектрометр 7. Ионизация электронным ударом 8. Малые количества веществ, расходуемых при проведении анализа
Возможности масс-спектрометра высокого разрешения Thermo Electron DFS 1. При использовании штока прямого ввода для химической ионизации возможен нагрев образца до температуры 1600 С 2. При использовании штока прямого ввода возможен нагрев образца до температуры 360 С 3. Возможность ввода пробы через газовый хроматограф. 4. Диапазон измеряемых масс до 6 000 а. е. м. 5. Диапазон точно (до 4 знака после запятой) определяемых масс до 1 000 а. е. м. (зависит от наличия стандартов) 6. Ручной прямой ввод образца в масс-спектрометр 7. Ионизация электронным ударом 8. Малые количества веществ, расходуемых при проведении анализа
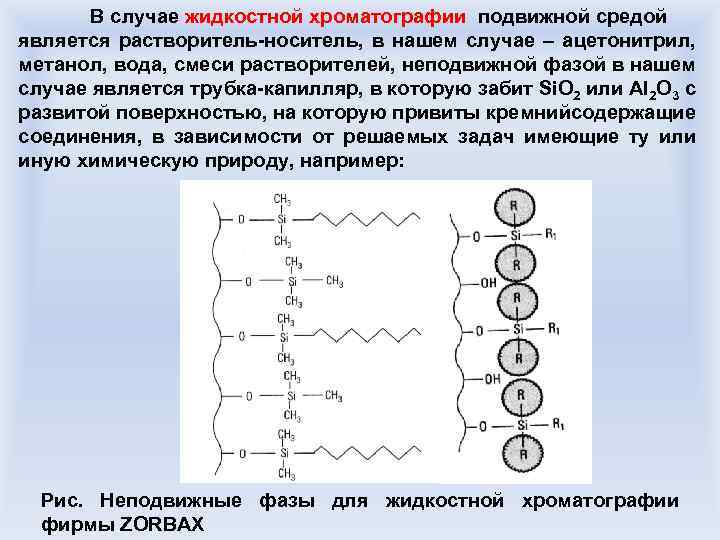 В случае жидкостной хроматографии подвижной средой является растворитель-носитель, в нашем случае – ацетонитрил, метанол, вода, смеси растворителей, неподвижной фазой в нашем случае является трубка-капилляр, в которую забит Si. O 2 или Al 2 O 3 с развитой поверхностью, на которую привиты кремнийсодержащие соединения, в зависимости от решаемых задач имеющие ту или иную химическую природу, например: Рис. Неподвижные фазы для жидкостной хроматографии фирмы ZORBAX
В случае жидкостной хроматографии подвижной средой является растворитель-носитель, в нашем случае – ацетонитрил, метанол, вода, смеси растворителей, неподвижной фазой в нашем случае является трубка-капилляр, в которую забит Si. O 2 или Al 2 O 3 с развитой поверхностью, на которую привиты кремнийсодержащие соединения, в зависимости от решаемых задач имеющие ту или иную химическую природу, например: Рис. Неподвижные фазы для жидкостной хроматографии фирмы ZORBAX
 Рис. Капиллярные хроматографические колонки для жидкостной хроматографии, слева – аналитическая колонка диаметром 5 микрон с предколонкой, справа – аналитическая колонка диаметром 1. 8 микрон
Рис. Капиллярные хроматографические колонки для жидкостной хроматографии, слева – аналитическая колонка диаметром 5 микрон с предколонкой, справа – аналитическая колонка диаметром 1. 8 микрон
 Возможности жидкостных хромато-масс-спектрометров 1. Автоматический и ручной ввод образца/ Серии образцов. 2. Диапазон измеряемых масс от 20 до 20000 а. е. м. и выше. 3. Программируемое изменение температуры хроматографической колонки до температуры кипения растворителя (обычно 25 -100 С). 4. Анализ жидких проб – веществ в растворе. 5. Возможность анализа полимеров, олигомеров, биологических объектов, полярных соединений, веществ, содержащих много ОН- и других ионогенных групп и т. д. , т. е. тех веществ, которые не проходят через хроматорафическую колонку газового хроматографа. 6. Возможность подбора хроматографической колонки под узкоспециализированные задачи: анализ нефтепродуктов, ароматических соединений, полярных веществ, лекарственных препаратов и т. д.
Возможности жидкостных хромато-масс-спектрометров 1. Автоматический и ручной ввод образца/ Серии образцов. 2. Диапазон измеряемых масс от 20 до 20000 а. е. м. и выше. 3. Программируемое изменение температуры хроматографической колонки до температуры кипения растворителя (обычно 25 -100 С). 4. Анализ жидких проб – веществ в растворе. 5. Возможность анализа полимеров, олигомеров, биологических объектов, полярных соединений, веществ, содержащих много ОН- и других ионогенных групп и т. д. , т. е. тех веществ, которые не проходят через хроматорафическую колонку газового хроматографа. 6. Возможность подбора хроматографической колонки под узкоспециализированные задачи: анализ нефтепродуктов, ароматических соединений, полярных веществ, лекарственных препаратов и т. д.
 Количественный масс-спектрометрический анализ Факторы, от которых зависит площадь пика: 1. Количество частиц. Масс-спектрометрический сигнал пропорционален потоку частиц. Если мы имели концентрацию анализируемого раствора 1% по массе фенола (М=94 г/моль) и 1% урсоловой кислоты (М=470 г/моль), то их пики по площади будут отличаться. 2. Сечение ионизации. Любое вещество характеризуется своей уникальной величиной сечения ионизации, т. е. количеством ионов, образовавшихся из молекул в условиях эксперимента. При электронном ударе примерно одна из 10 000 молекул ионизируется. Это «примерно» зависит от структуры соединения и может изменяться в широком диапазоне. Это означает, что одинаковые навески двух разных веществ после ионизации приведут к возникновению разного количества ионов. Как следствие, площади пиков на хроматограмме, пропорциональные величине полного ионного тока, на масс-хроматограммах будут существенно различаться. 3. Дискриминация по массе. Оказывается, что анализатор масс любого типа пропускает ионы с разными значениями m/z по-разному. В результате 100 ионов с m/z 56 дадут пик с интенсивностью, отличной от пика 100 ионов с m/z 326. Если два соединения в смеси имеют существенно различающиеся молекулярные массы, то дискриминация по массе скажется и на интенсивностях хроматографических пиков по полному ионному току.
Количественный масс-спектрометрический анализ Факторы, от которых зависит площадь пика: 1. Количество частиц. Масс-спектрометрический сигнал пропорционален потоку частиц. Если мы имели концентрацию анализируемого раствора 1% по массе фенола (М=94 г/моль) и 1% урсоловой кислоты (М=470 г/моль), то их пики по площади будут отличаться. 2. Сечение ионизации. Любое вещество характеризуется своей уникальной величиной сечения ионизации, т. е. количеством ионов, образовавшихся из молекул в условиях эксперимента. При электронном ударе примерно одна из 10 000 молекул ионизируется. Это «примерно» зависит от структуры соединения и может изменяться в широком диапазоне. Это означает, что одинаковые навески двух разных веществ после ионизации приведут к возникновению разного количества ионов. Как следствие, площади пиков на хроматограмме, пропорциональные величине полного ионного тока, на масс-хроматограммах будут существенно различаться. 3. Дискриминация по массе. Оказывается, что анализатор масс любого типа пропускает ионы с разными значениями m/z по-разному. В результате 100 ионов с m/z 56 дадут пик с интенсивностью, отличной от пика 100 ионов с m/z 326. Если два соединения в смеси имеют существенно различающиеся молекулярные массы, то дискриминация по массе скажется и на интенсивностях хроматографических пиков по полному ионному току.
 Количественный хромато-массспектрометрический анализ Метод внешнего стандарта: Для прибора, на котором производится анализ, готовится образец с заведомо известной концентрацией определяемого вещества. Для большей точности делается несколько разведений, записывают хроматограммы и получают калибровочную зависимость. Далее записывается проба с неизвестной концентрацией вещества и по величине площади хроматографического пика и калибровочной зависимости делается вывод о содержании в пробе вещества. Метод внутреннего стандарта: Также, как и в случае метода внешнего стандарта, приготовляются калибровочные растворы определяемого вещества и записываются их хроматограммы. Затем к образцу, имеющему в своем составе определяемое вещество, добавляется определенная порция определяемого вещества. Зная сигнал, который должен быть дан концентрацией, созданной добавлением вещества, определяют количество образца в исходной пробе.
Количественный хромато-массспектрометрический анализ Метод внешнего стандарта: Для прибора, на котором производится анализ, готовится образец с заведомо известной концентрацией определяемого вещества. Для большей точности делается несколько разведений, записывают хроматограммы и получают калибровочную зависимость. Далее записывается проба с неизвестной концентрацией вещества и по величине площади хроматографического пика и калибровочной зависимости делается вывод о содержании в пробе вещества. Метод внутреннего стандарта: Также, как и в случае метода внешнего стандарта, приготовляются калибровочные растворы определяемого вещества и записываются их хроматограммы. Затем к образцу, имеющему в своем составе определяемое вещество, добавляется определенная порция определяемого вещества. Зная сигнал, который должен быть дан концентрацией, созданной добавлением вещества, определяют количество образца в исходной пробе.
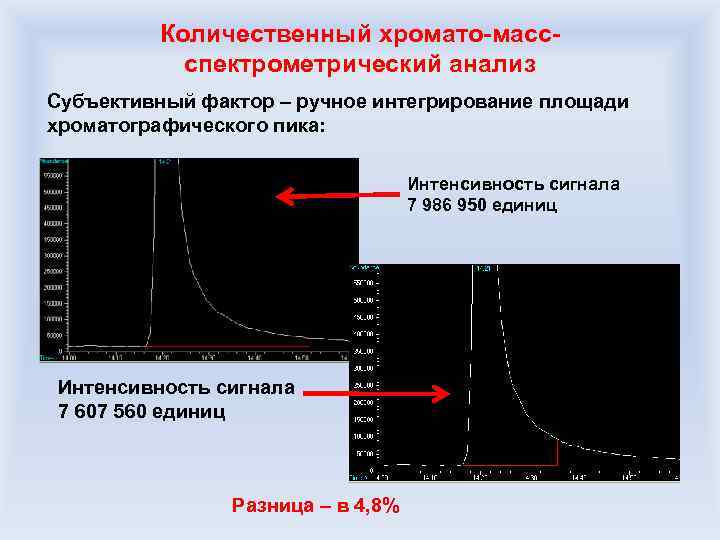 Количественный хромато-массспектрометрический анализ Субъективный фактор – ручное интегрирование площади хроматографического пика: Интенсивность сигнала 7 986 950 единиц DEPO Интенсивность сигнала 7 607 560 единиц Разница – в 4, 8%
Количественный хромато-массспектрометрический анализ Субъективный фактор – ручное интегрирование площади хроматографического пика: Интенсивность сигнала 7 986 950 единиц DEPO Интенсивность сигнала 7 607 560 единиц Разница – в 4, 8%
 ГАЗОВАЯ ХРОМАТО-МАСС-СПЕКТРОМЕТРИЯ
ГАЗОВАЯ ХРОМАТО-МАСС-СПЕКТРОМЕТРИЯ
 Требования к образцам на газовую хроматографию Общие требования: 1. Через хроматограф не проходят соли, полимеры, смолы, вещества с большой молекулярной массой (от 750 и выше). Поэтому такие соединения следует подвергать модификациям или же не приносить на хромато-масс-спектрометрический анализ – ничего разумного анализ показать не сможет. 2. Кислоты и их смеси желательно перевести в эфиры (желательно метиловые – они есть в базах масс-спектроскопических данных). Амины можно ацилировать. Иначе хроматографические пики на колонках с неполярной фазой получаются слишком широкие, и могут «закрывать» пики других соединений в смеси. 3. Не стоит приносить смеси с осадками, но если это неизбежно, то следует указать природу осадка. 4. Для образца в растворе: объем должен быть около 1 мл! Если есть опасность испарения растворителя, на емкости маркером следует оставить метку уровня растворителя. Если образца менее 1 мл, следует согласовать это с оператором хроматографа.
Требования к образцам на газовую хроматографию Общие требования: 1. Через хроматограф не проходят соли, полимеры, смолы, вещества с большой молекулярной массой (от 750 и выше). Поэтому такие соединения следует подвергать модификациям или же не приносить на хромато-масс-спектрометрический анализ – ничего разумного анализ показать не сможет. 2. Кислоты и их смеси желательно перевести в эфиры (желательно метиловые – они есть в базах масс-спектроскопических данных). Амины можно ацилировать. Иначе хроматографические пики на колонках с неполярной фазой получаются слишком широкие, и могут «закрывать» пики других соединений в смеси. 3. Не стоит приносить смеси с осадками, но если это неизбежно, то следует указать природу осадка. 4. Для образца в растворе: объем должен быть около 1 мл! Если есть опасность испарения растворителя, на емкости маркером следует оставить метку уровня растворителя. Если образца менее 1 мл, следует согласовать это с оператором хроматографа.
 Требования к образцам на газовую хроматографию Образцы в растворе: 1. Необходимо указать растворитель. При прочих равных лучше использовать более легкокипящий растворитель (метанол, хлороформ), т. к. в случае более высококипящего растворителя задержку включения масс-анализатора на проход фронта растворителя выставляют больше, до 8 мин. включительно, в результате чего все соединения, которые выходят до времени включения масс-анализатора, обычно остаются неопределенными. 2. Целесообразно проверить растворитель/растворители на наличие примесей. 3. В случае исследования результатов какого-то химического процесса целесообразно проверить на наличие примесей исходные вещества, особенно если в их чистоте имеются сомнения (вещества низкой квалификации по чистоте, с длительного хранения и т. д. ). 4. Необходимо как можно точнее указать концентрацию основного компонента в смеси. Желательно иметь это содержание около 0, 5% по массе. Иначе получите «зашкаленную пробу» .
Требования к образцам на газовую хроматографию Образцы в растворе: 1. Необходимо указать растворитель. При прочих равных лучше использовать более легкокипящий растворитель (метанол, хлороформ), т. к. в случае более высококипящего растворителя задержку включения масс-анализатора на проход фронта растворителя выставляют больше, до 8 мин. включительно, в результате чего все соединения, которые выходят до времени включения масс-анализатора, обычно остаются неопределенными. 2. Целесообразно проверить растворитель/растворители на наличие примесей. 3. В случае исследования результатов какого-то химического процесса целесообразно проверить на наличие примесей исходные вещества, особенно если в их чистоте имеются сомнения (вещества низкой квалификации по чистоте, с длительного хранения и т. д. ). 4. Необходимо как можно точнее указать концентрацию основного компонента в смеси. Желательно иметь это содержание около 0, 5% по массе. Иначе получите «зашкаленную пробу» .
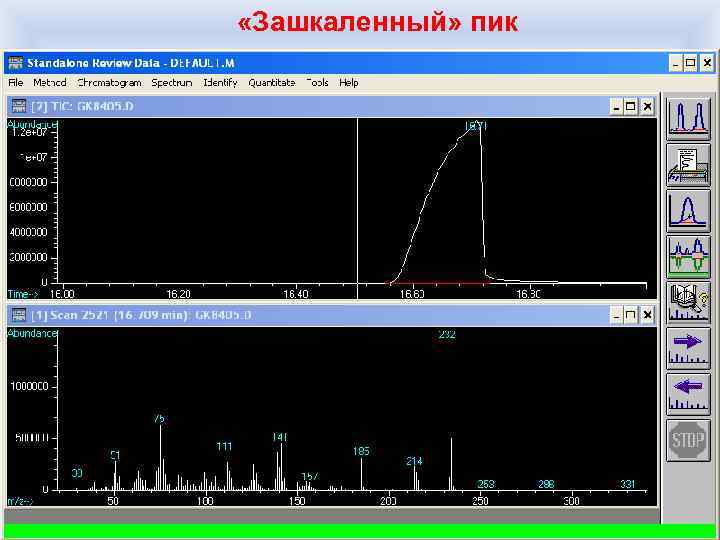 «Зашкаленный» пик
«Зашкаленный» пик
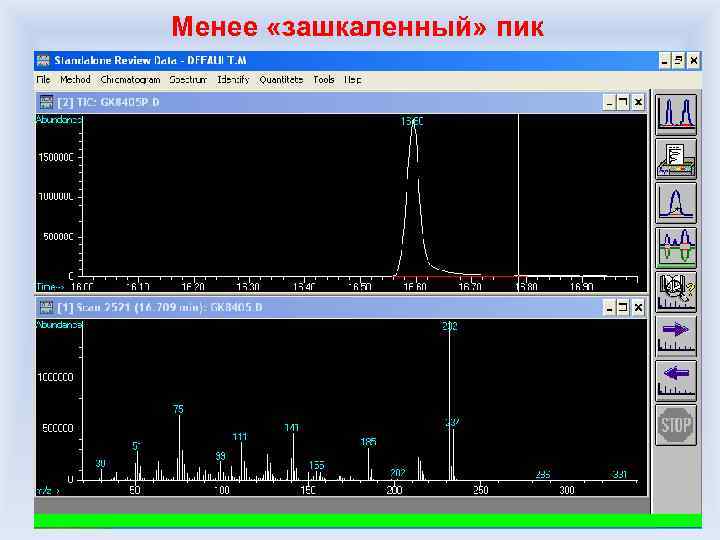 Менее «зашкаленный» пик
Менее «зашкаленный» пик
 Требования к образцам на газовую хроматографию Жидкие и твердые образцы веществ в чистом виде: 1. Необходимо указать растворитель (растворители), в котором возможно провести растворение образцов, при этом целесообразно указать особенности растворения – возможно, растворение происходит, но медленно, или растворение можно провести при нагревании и т. д. 2. Если образец представляет собой смесь веществ, желательно перечислить основные компоненты смеси и их примерное содержание. 3. Если для жидкого образца известна температура кипения, ее следует привести. 4. Указать, какие соединения могут оказаться в осадке при растворении в указанном заказчиком растворителе.
Требования к образцам на газовую хроматографию Жидкие и твердые образцы веществ в чистом виде: 1. Необходимо указать растворитель (растворители), в котором возможно провести растворение образцов, при этом целесообразно указать особенности растворения – возможно, растворение происходит, но медленно, или растворение можно провести при нагревании и т. д. 2. Если образец представляет собой смесь веществ, желательно перечислить основные компоненты смеси и их примерное содержание. 3. Если для жидкого образца известна температура кипения, ее следует привести. 4. Указать, какие соединения могут оказаться в осадке при растворении в указанном заказчиком растворителе.
 Требования к заявкам: ! ! Заявка должна быть оформлена возможно более полно, чем больше информации о предполагаемом составе и характере пробы у оператора, тем больше информации Шифр пробы должен быть не будет потом у заказчика. Следует не забывать указывать на заявке фамилию, телефон, e-mail, оператор может разрешить часть возникающих вопросов по телефону Структурные формулы следует приводить четко, на их основе потом определяется возможный путь фрагментации соединения под электронным ударом. Не следует упускать возможность написать возможную брутто-формулу соединений, оператор может, конечно, по структурной формуле написать брутто-формулу, но это не является его основной работой. Молекулярные массы целесообразно приводить с округлением в меньшую сторону до целых, если входят в соединение хлор или бром – то с учетом меньшего по массе изотопа (т. е. хлор – 35 а. е. м. , бром – 79 а. е. м. ). более 8 символов, применяются латиница, цифры, знаки «_» и «-»
Требования к заявкам: ! ! Заявка должна быть оформлена возможно более полно, чем больше информации о предполагаемом составе и характере пробы у оператора, тем больше информации Шифр пробы должен быть не будет потом у заказчика. Следует не забывать указывать на заявке фамилию, телефон, e-mail, оператор может разрешить часть возникающих вопросов по телефону Структурные формулы следует приводить четко, на их основе потом определяется возможный путь фрагментации соединения под электронным ударом. Не следует упускать возможность написать возможную брутто-формулу соединений, оператор может, конечно, по структурной формуле написать брутто-формулу, но это не является его основной работой. Молекулярные массы целесообразно приводить с округлением в меньшую сторону до целых, если входят в соединение хлор или бром – то с учетом меньшего по массе изотопа (т. е. хлор – 35 а. е. м. , бром – 79 а. е. м. ). более 8 символов, применяются латиница, цифры, знаки «_» и «-»
 Требования к заявкам: Указать особые условия для записи хроматомасс-спектрограммы - означает указать метод, которым произвести запись, требования к температуре источника и детектора, время, с которого проводить интегрирование пиков, их можно обсудить с оператором, чтобы понять, какой именно режим предпочтителен а) Записать и передать ХМС – означает передать файл, сгенерированный управляющим прибором компьютером при записи образца. Обработка его ведется уже химиком на своем компьютере при помощи специальной программы (Stand Alone Review Data) б) Идентифицировать компоненты смеси – означает провести идентификацию путем сравнения массспектров соединений смеси с имеющимися базами массспектральных данных (около 500 тыс. соединений) г) - Особые требования к представлению результатов (обсудить с оператором) в) Идентифицировать и интерпретировать компоненты смеси – означает провести идентификацию по базам данных для всех пиков, для которых это возможно, а для которых невозможно – предположить возможные структуры соединений на основе априорной информации и характера масс-спектра
Требования к заявкам: Указать особые условия для записи хроматомасс-спектрограммы - означает указать метод, которым произвести запись, требования к температуре источника и детектора, время, с которого проводить интегрирование пиков, их можно обсудить с оператором, чтобы понять, какой именно режим предпочтителен а) Записать и передать ХМС – означает передать файл, сгенерированный управляющим прибором компьютером при записи образца. Обработка его ведется уже химиком на своем компьютере при помощи специальной программы (Stand Alone Review Data) б) Идентифицировать компоненты смеси – означает провести идентификацию путем сравнения массспектров соединений смеси с имеющимися базами массспектральных данных (около 500 тыс. соединений) г) - Особые требования к представлению результатов (обсудить с оператором) в) Идентифицировать и интерпретировать компоненты смеси – означает провести идентификацию по базам данных для всех пиков, для которых это возможно, а для которых невозможно – предположить возможные структуры соединений на основе априорной информации и характера масс-спектра
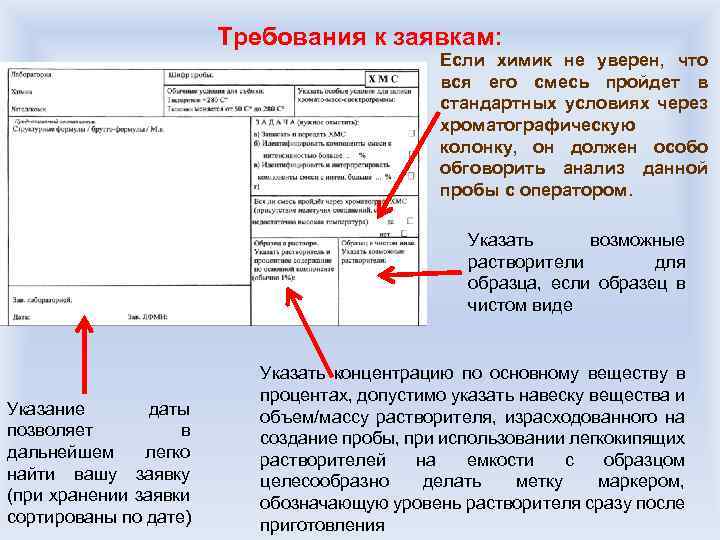 Требования к заявкам: Если химик не уверен, что вся его смесь пройдет в стандартных условиях через хроматографическую колонку, он должен особо обговорить анализ данной пробы с оператором. Указать возможные растворители для образца, если образец в чистом виде Указание даты позволяет в дальнейшем легко найти вашу заявку (при хранении заявки сортированы по дате) Указать концентрацию по основному веществу в процентах, допустимо указать навеску вещества и объем/массу растворителя, израсходованного на создание пробы, при использовании легкокипящих растворителей на емкости с образцом целесообразно делать метку маркером, обозначающую уровень растворителя сразу после приготовления
Требования к заявкам: Если химик не уверен, что вся его смесь пройдет в стандартных условиях через хроматографическую колонку, он должен особо обговорить анализ данной пробы с оператором. Указать возможные растворители для образца, если образец в чистом виде Указание даты позволяет в дальнейшем легко найти вашу заявку (при хранении заявки сортированы по дате) Указать концентрацию по основному веществу в процентах, допустимо указать навеску вещества и объем/массу растворителя, израсходованного на создание пробы, при использовании легкокипящих растворителей на емкости с образцом целесообразно делать метку маркером, обозначающую уровень растворителя сразу после приготовления
 ЖИДКОСТНАЯ МАСССПЕКТРОМЕТРИЯ ВЫСОКОГО РАЗРЕШЕНИЯ (ВЭЖХ -МС)
ЖИДКОСТНАЯ МАСССПЕКТРОМЕТРИЯ ВЫСОКОГО РАЗРЕШЕНИЯ (ВЭЖХ -МС)
 Требования к образцам на масс-спектрометрию высокого разрешения Твердые образцы: 1. Должны быть как можно более чистыми, если необходим массспектр. 2. Несмотря на высокую чувствительность метода и малое количество образца, необходимое для анализа, количество, предоставляемое химиком для записи масс-спектра, должно быть достаточным для того, чтобы образец удобно было помещать в кювету (обычно 10 мг достаточно). 3. Целесообразно проверить образец на наличие примесей (тонкослойной или иного вида хроматографии). 4. Указать растворители для образца, чтобы его отмывать от кюветы.
Требования к образцам на масс-спектрометрию высокого разрешения Твердые образцы: 1. Должны быть как можно более чистыми, если необходим массспектр. 2. Несмотря на высокую чувствительность метода и малое количество образца, необходимое для анализа, количество, предоставляемое химиком для записи масс-спектра, должно быть достаточным для того, чтобы образец удобно было помещать в кювету (обычно 10 мг достаточно). 3. Целесообразно проверить образец на наличие примесей (тонкослойной или иного вида хроматографии). 4. Указать растворители для образца, чтобы его отмывать от кюветы.
 Требования к заявкам на масс-спектрометрию высокого разрешения Целесообразно указать электронный адрес, помимо комнаты и телефона Обязательно указание, до какой температуры образец химически стабилен Обязательно указание растворителя, в котором образец хорошо растворим Указать молекулярный вес или интервал, где следует искать молекулярный ион образца
Требования к заявкам на масс-спектрометрию высокого разрешения Целесообразно указать электронный адрес, помимо комнаты и телефона Обязательно указание, до какой температуры образец химически стабилен Обязательно указание растворителя, в котором образец хорошо растворим Указать молекулярный вес или интервал, где следует искать молекулярный ион образца
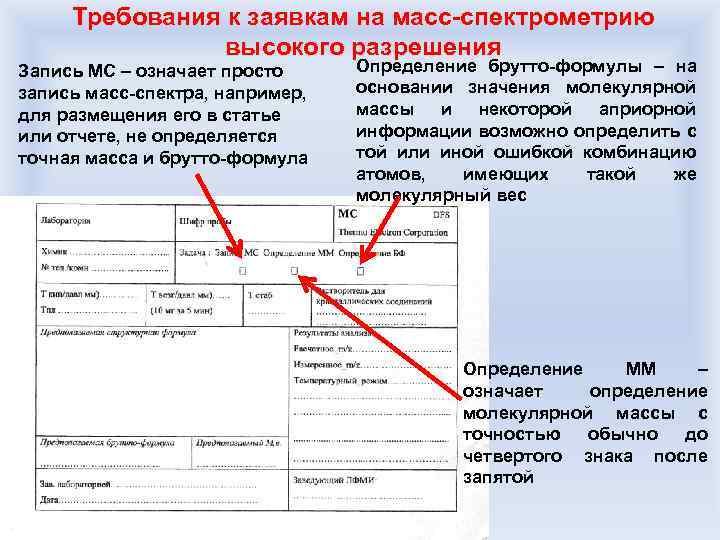 Требования к заявкам на масс-спектрометрию высокого разрешения Запись МС – означает просто запись масс-спектра, например, для размещения его в статье или отчете, не определяется точная масса и брутто-формула Определение брутто-формулы – на основании значения молекулярной массы и некоторой априорной информации возможно определить с той или иной ошибкой комбинацию атомов, имеющих такой же молекулярный вес Определение ММ – означает определение молекулярной массы с точностью обычно до четвертого знака после запятой
Требования к заявкам на масс-спектрометрию высокого разрешения Запись МС – означает просто запись масс-спектра, например, для размещения его в статье или отчете, не определяется точная масса и брутто-формула Определение брутто-формулы – на основании значения молекулярной массы и некоторой априорной информации возможно определить с той или иной ошибкой комбинацию атомов, имеющих такой же молекулярный вес Определение ММ – означает определение молекулярной массы с точностью обычно до четвертого знака после запятой
 МАСС-СПЕКТРОМЕТРИЯ ВЫСОКОГО РАЗРЕШЕНИЯ
МАСС-СПЕКТРОМЕТРИЯ ВЫСОКОГО РАЗРЕШЕНИЯ
 Специфика ВЭЖХ-МС анализа - пригоден для многих термолабильных и малолетучих веществ - не даёт стандартных масс-спектров - слабое разделение на колонках - проблема растворимости образца (лучше в Aс. CN, Me. OH, i-Pr. OH, H 2 O) Предпосылки к использованию ВЭЖХ-МС анализа • Проблемы с идентификацией, не решаемые другими физметодами • Надежда на наличие в молекуле ионогенных групп • Предварительный подбор условий ВЭЖХ-анализа (для смесей) • Заметная растворимость растворителях образца в неагрессивных
Специфика ВЭЖХ-МС анализа - пригоден для многих термолабильных и малолетучих веществ - не даёт стандартных масс-спектров - слабое разделение на колонках - проблема растворимости образца (лучше в Aс. CN, Me. OH, i-Pr. OH, H 2 O) Предпосылки к использованию ВЭЖХ-МС анализа • Проблемы с идентификацией, не решаемые другими физметодами • Надежда на наличие в молекуле ионогенных групп • Предварительный подбор условий ВЭЖХ-анализа (для смесей) • Заметная растворимость растворителях образца в неагрессивных
 Требования к образцам на жидкостную хроматографию Жидкие и твердые образцы веществ в чистом виде: 1. Необходимо указать растворитель (растворители), в котором возможно провести растворение образцов, при этом целесообразно указать особенности растворения – возможно, растворение происходит, но медленно, или растворение можно провести при нагревании и т. д. Целесообразно указать полярные растворители, в котором растворяется образец – метанол, ацетонитрил и т. д. – для обеспечения электроспрейионизации. 2. Если образец представляет собой смесь веществ, желательно перечислить основные компоненты смеси и их примерное содержание. 3. Если для жидкого образца известна температура кипения, ее следует привести. 4. Указать, какие соединения могут оказаться в осадке при растворении в указанном заказчиком растворителе.
Требования к образцам на жидкостную хроматографию Жидкие и твердые образцы веществ в чистом виде: 1. Необходимо указать растворитель (растворители), в котором возможно провести растворение образцов, при этом целесообразно указать особенности растворения – возможно, растворение происходит, но медленно, или растворение можно провести при нагревании и т. д. Целесообразно указать полярные растворители, в котором растворяется образец – метанол, ацетонитрил и т. д. – для обеспечения электроспрейионизации. 2. Если образец представляет собой смесь веществ, желательно перечислить основные компоненты смеси и их примерное содержание. 3. Если для жидкого образца известна температура кипения, ее следует привести. 4. Указать, какие соединения могут оказаться в осадке при растворении в указанном заказчиком растворителе.
 Пример масс-спектральной информации с жидкостного хромато-масс-спектрометра Agilent 1100 (квадрупольный масс-анализатор)
Пример масс-спектральной информации с жидкостного хромато-масс-спектрометра Agilent 1100 (квадрупольный масс-анализатор)
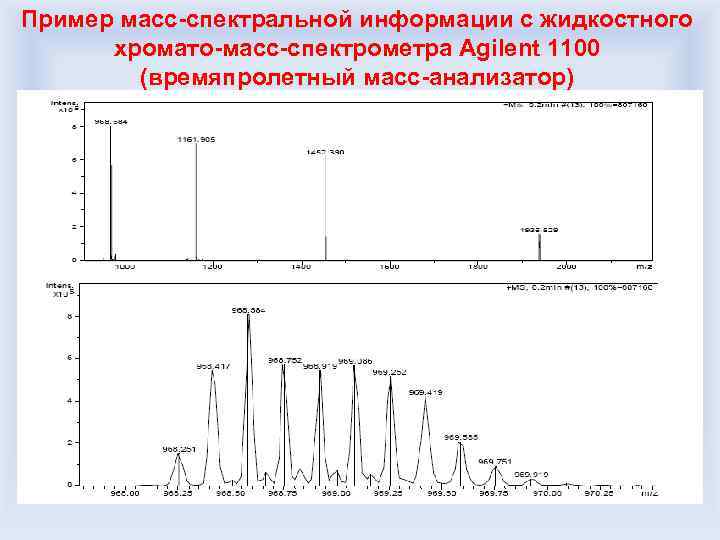 Пример масс-спектральной информации с жидкостного хромато-масс-спектрометра Agilent 1100 (времяпролетный масс-анализатор)
Пример масс-спектральной информации с жидкостного хромато-масс-спектрометра Agilent 1100 (времяпролетный масс-анализатор)
 ИНТЕРПРЕТАЦИЯ МАСС-СПЕКТРОВ
ИНТЕРПРЕТАЦИЯ МАСС-СПЕКТРОВ
 Состав масс-спектра Масс-спектр может состоять из нескольких типов ионов: 1. Молекулярный ион 2. Перегруппировочные ионы 3. Фрагментные ионы 4. Многозарядные ионы 5. Метастабильные ионы
Состав масс-спектра Масс-спектр может состоять из нескольких типов ионов: 1. Молекулярный ион 2. Перегруппировочные ионы 3. Фрагментные ионы 4. Многозарядные ионы 5. Метастабильные ионы
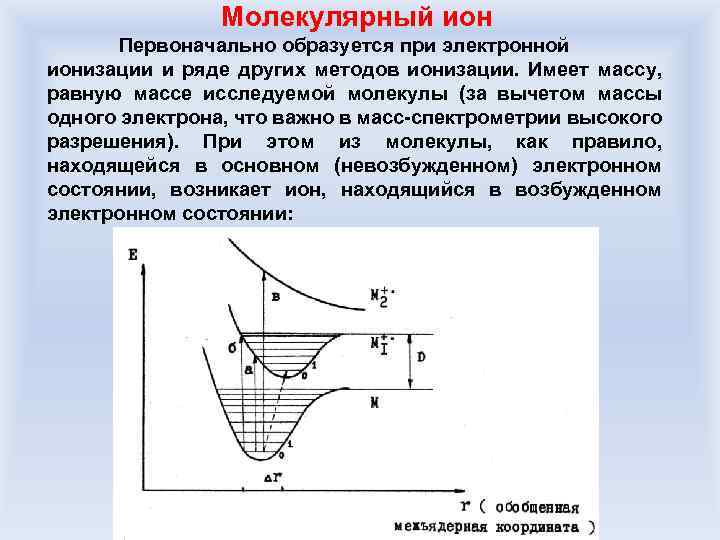 Молекулярный ион Первоначально образуется при электронной ионизации и ряде других методов ионизации. Имеет массу, равную массе исследуемой молекулы (за вычетом массы одного электрона, что важно в масс-спектрометрии высокого разрешения). При этом из молекулы, как правило, находящейся в основном (невозбужденном) электронном состоянии, возникает ион, находящийся в возбужденном электронном состоянии:
Молекулярный ион Первоначально образуется при электронной ионизации и ряде других методов ионизации. Имеет массу, равную массе исследуемой молекулы (за вычетом массы одного электрона, что важно в масс-спектрометрии высокого разрешения). При этом из молекулы, как правило, находящейся в основном (невозбужденном) электронном состоянии, возникает ион, находящийся в возбужденном электронном состоянии:
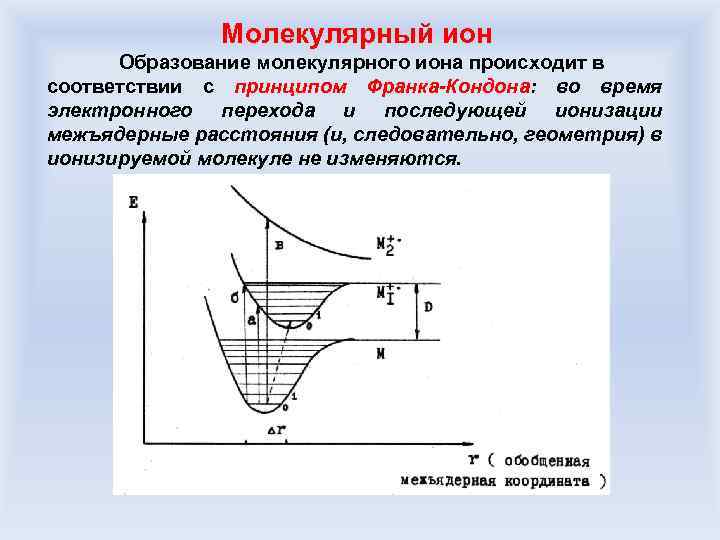 Молекулярный ион Образование молекулярного иона происходит в соответствии с принципом Франка-Кондона: во время электронного перехода и последующей ионизации межъядерные расстояния (и, следовательно, геометрия) в ионизируемой молекуле не изменяются.
Молекулярный ион Образование молекулярного иона происходит в соответствии с принципом Франка-Кондона: во время электронного перехода и последующей ионизации межъядерные расстояния (и, следовательно, геометрия) в ионизируемой молекуле не изменяются.
 Молекулярный ион Дает информацию о массе молекулы, в случае измерения точной массы или анализа интенсивности изотопных линий – о бруттоформуле молекулы. Молекулярный ион обязан: 1) иметь самую большую массу (m/z) в спектре. 2) быть нечетноэлектронным. 3) быть способным образовывать важнейшие фрагментные ионы с большой массой за счет выброса реальных нейтральных частиц. 4) включать все элементы, наличие которых можно увидеть по фрагментным ионам.
Молекулярный ион Дает информацию о массе молекулы, в случае измерения точной массы или анализа интенсивности изотопных линий – о бруттоформуле молекулы. Молекулярный ион обязан: 1) иметь самую большую массу (m/z) в спектре. 2) быть нечетноэлектронным. 3) быть способным образовывать важнейшие фрагментные ионы с большой массой за счет выброса реальных нейтральных частиц. 4) включать все элементы, наличие которых можно увидеть по фрагментным ионам.
 Повышение стабильности молекулярного иона возможно разными способами: 1) Изменение типа ионизации на более мягкий. 2) Снижение энергии электронной стандартных 70 до 20 -25 э. В, например). ионизации (со 3) введение в молекулу групп атомов с низким потенциалом ионизации или заменой дестабилизирующих молекулярный ион групп. Например: C 6 H 5 -, CH 3 O-, (CH 3)2 N- и т. п. Уменьшают стабильность молекулярного иона NO 2, ON=O, -O-NO 2, Cl, Br, I. 4) Понижение температуры образца – приводит к снижению внутренней энергии молекулярного иона, способного к фрагментации. Эффект велик для алифатических углеводородов, мал для ароматических. Здесь же – понижение температуры образца потребует увеличения его летучести, для чего модифицируют, переводя в эфиры, используя силилирование, ацетилирование и восстановление.
Повышение стабильности молекулярного иона возможно разными способами: 1) Изменение типа ионизации на более мягкий. 2) Снижение энергии электронной стандартных 70 до 20 -25 э. В, например). ионизации (со 3) введение в молекулу групп атомов с низким потенциалом ионизации или заменой дестабилизирующих молекулярный ион групп. Например: C 6 H 5 -, CH 3 O-, (CH 3)2 N- и т. п. Уменьшают стабильность молекулярного иона NO 2, ON=O, -O-NO 2, Cl, Br, I. 4) Понижение температуры образца – приводит к снижению внутренней энергии молекулярного иона, способного к фрагментации. Эффект велик для алифатических углеводородов, мал для ароматических. Здесь же – понижение температуры образца потребует увеличения его летучести, для чего модифицируют, переводя в эфиры, используя силилирование, ацетилирование и восстановление.
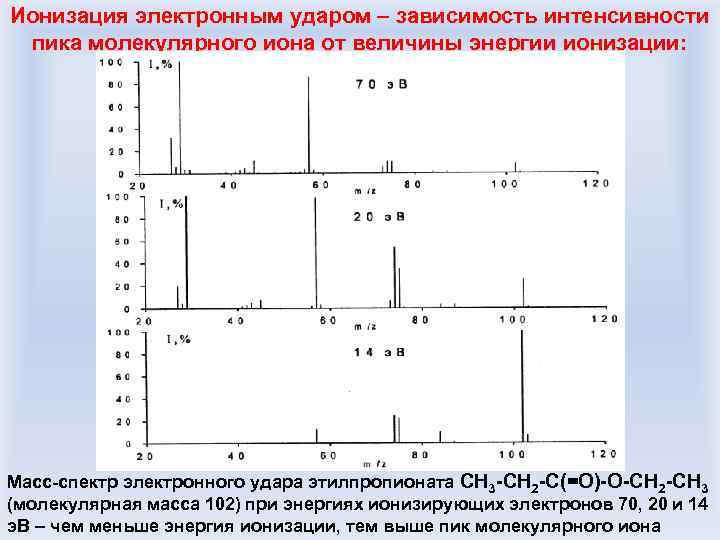 Ионизация электронным ударом – зависимость интенсивности пика молекулярного иона от величины энергии ионизации: Масс-спектр электронного удара этилпропионата CH 3 -CH 2 -C(=O)-O-CH 2 -CH 3 (молекулярная масса 102) при энергиях ионизирующих электронов 70, 20 и 14 э. В – чем меньше энергия ионизации, тем выше пик молекулярного иона
Ионизация электронным ударом – зависимость интенсивности пика молекулярного иона от величины энергии ионизации: Масс-спектр электронного удара этилпропионата CH 3 -CH 2 -C(=O)-O-CH 2 -CH 3 (молекулярная масса 102) при энергиях ионизирующих электронов 70, 20 и 14 э. В – чем меньше энергия ионизации, тем выше пик молекулярного иона
 Определение элементного состава по массспектру низкого разрешения Молекулярному иону сопутствуют так называемые «изотопные пики» , пики ионов, имеющих массу большую, чем молекулярный ион. Изотопные пики, как правило (исключение - бромсодержащие вещества), существенно менее интенсивны, чем молекулярный ион, и при этом их интенсивность подчиняется ряду закономерностей, что позволяет производить даже по спектру низкого разрешения элементный анализ образца или иона. Для этого производят анализ группы линий молекулярного иона: M+, (M+1)+, (M+2)+ и т. д. , сравнивая их интенсивности. Интенсивность изотопных спектральных линий, соответствующих определенному иону, зависит от элементного состава данного иона. Существует ряд правил, позволяющих извлечь много информации даже из масс-спектра низкого разрешения.
Определение элементного состава по массспектру низкого разрешения Молекулярному иону сопутствуют так называемые «изотопные пики» , пики ионов, имеющих массу большую, чем молекулярный ион. Изотопные пики, как правило (исключение - бромсодержащие вещества), существенно менее интенсивны, чем молекулярный ион, и при этом их интенсивность подчиняется ряду закономерностей, что позволяет производить даже по спектру низкого разрешения элементный анализ образца или иона. Для этого производят анализ группы линий молекулярного иона: M+, (M+1)+, (M+2)+ и т. д. , сравнивая их интенсивности. Интенсивность изотопных спектральных линий, соответствующих определенному иону, зависит от элементного состава данного иона. Существует ряд правил, позволяющих извлечь много информации даже из масс-спектра низкого разрешения.
 Определение элементного состава при помощи молекулярного иона при масс-спектре низкого разрешения: 1) Хлор, бром, сера и кремний легко детектируются благодаря характерной для каждого элемента мультиплетности сигнала, зависящей от природной распространенности изотопов соответствующих элементов, т. е. можно сразу сказать, какое количество атомов указанных галогенов находится в соединении
Определение элементного состава при помощи молекулярного иона при масс-спектре низкого разрешения: 1) Хлор, бром, сера и кремний легко детектируются благодаря характерной для каждого элемента мультиплетности сигнала, зависящей от природной распространенности изотопов соответствующих элементов, т. е. можно сразу сказать, какое количество атомов указанных галогенов находится в соединении
 Определение элементного состава при помощи молекулярного иона при масс-спектре низкого разрешения: 2) Если интенсивность пика М++2 составляет менее 3% от интенсивности пика М+, исследуемое соединение не содержит атомов хлора, брома, серы и кремния (правило применимо и для рассмотрения состава осколочных ионов). 3) Азотное правило Для молекулы и молекулярного иона: Если соединение содержит четное число атомов азота или азота в составе нет, его молекулярная масса четная; если число атомов азота нечетное, молекулярная масса тоже нечетная. Для фрагментных ионов: Нечетноэлектронный ион имеет четную массу, если содержит четное число атомов азота; четноэлектронный ион имеет четную массу, если содержит нечетное число атомов азота. 4) Интенсивность пика М+1 и М+2 для органических соединений прямо пропорциональна содержанию атомов углерода в молекуле анализируемого вещества.
Определение элементного состава при помощи молекулярного иона при масс-спектре низкого разрешения: 2) Если интенсивность пика М++2 составляет менее 3% от интенсивности пика М+, исследуемое соединение не содержит атомов хлора, брома, серы и кремния (правило применимо и для рассмотрения состава осколочных ионов). 3) Азотное правило Для молекулы и молекулярного иона: Если соединение содержит четное число атомов азота или азота в составе нет, его молекулярная масса четная; если число атомов азота нечетное, молекулярная масса тоже нечетная. Для фрагментных ионов: Нечетноэлектронный ион имеет четную массу, если содержит четное число атомов азота; четноэлектронный ион имеет четную массу, если содержит нечетное число атомов азота. 4) Интенсивность пика М+1 и М+2 для органических соединений прямо пропорциональна содержанию атомов углерода в молекуле анализируемого вещества.
 Определение элементного состава при помощи молекулярного иона при масс-спектре низкого разрешения: 5) Несмотря на относительно малую распространенность природного изотопа 18 О (примерно 0. 2% от основного 16 О) возможно делать определенные предположения об числе атомов кислорода в частице: если интенсивность пика иона (М+2)+ в спектре образца с небольшим числом атомов углерода в молекуле больше 0. 5% от интенсивности М+, можно предположить, что в состав соединения входит 1 или более атомов кислорода. Другими словами – каждый атом кислорода в частице повышает интенсивность сигнала (М+2)+ иона на 0. 2% от интенсивности сигнала М+.
Определение элементного состава при помощи молекулярного иона при масс-спектре низкого разрешения: 5) Несмотря на относительно малую распространенность природного изотопа 18 О (примерно 0. 2% от основного 16 О) возможно делать определенные предположения об числе атомов кислорода в частице: если интенсивность пика иона (М+2)+ в спектре образца с небольшим числом атомов углерода в молекуле больше 0. 5% от интенсивности М+, можно предположить, что в состав соединения входит 1 или более атомов кислорода. Другими словами – каждый атом кислорода в частице повышает интенсивность сигнала (М+2)+ иона на 0. 2% от интенсивности сигнала М+.
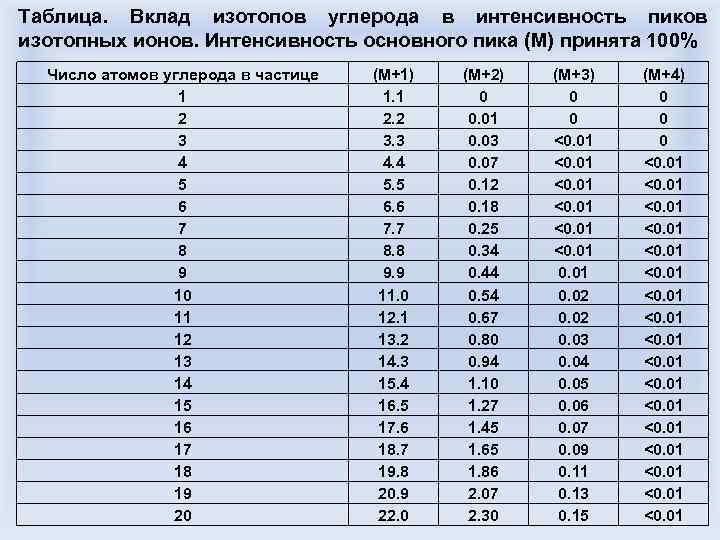 Таблица. Вклад изотопов углерода в интенсивность пиков изотопных ионов. Интенсивность основного пика (М) принята 100% Число атомов углерода в частице 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 (М+1) 1. 1 2. 2 3. 3 4. 4 5. 5 6. 6 7. 7 8. 8 9. 9 11. 0 12. 1 13. 2 14. 3 15. 4 16. 5 17. 6 18. 7 19. 8 20. 9 22. 0 (М+2) 0 0. 01 0. 03 0. 07 0. 12 0. 18 0. 25 0. 34 0. 44 0. 54 0. 67 0. 80 0. 94 1. 10 1. 27 1. 45 1. 65 1. 86 2. 07 2. 30 (М+3) 0 0 <0. 01 0. 02 0. 03 0. 04 0. 05 0. 06 0. 07 0. 09 0. 11 0. 13 0. 15 (М+4) 0 0 0 <0. 01 <0. 01
Таблица. Вклад изотопов углерода в интенсивность пиков изотопных ионов. Интенсивность основного пика (М) принята 100% Число атомов углерода в частице 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 (М+1) 1. 1 2. 2 3. 3 4. 4 5. 5 6. 6 7. 7 8. 8 9. 9 11. 0 12. 1 13. 2 14. 3 15. 4 16. 5 17. 6 18. 7 19. 8 20. 9 22. 0 (М+2) 0 0. 01 0. 03 0. 07 0. 12 0. 18 0. 25 0. 34 0. 44 0. 54 0. 67 0. 80 0. 94 1. 10 1. 27 1. 45 1. 65 1. 86 2. 07 2. 30 (М+3) 0 0 <0. 01 0. 02 0. 03 0. 04 0. 05 0. 06 0. 07 0. 09 0. 11 0. 13 0. 15 (М+4) 0 0 0 <0. 01 <0. 01
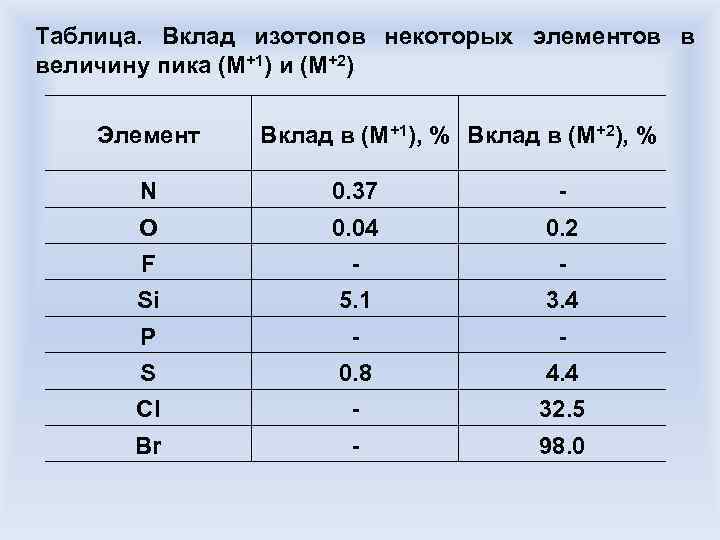 Таблица. Вклад изотопов некоторых элементов в величину пика (М+1) и (М+2) Элемент Вклад в (М+1), % Вклад в (М+2), % N 0. 37 - O 0. 04 0. 2 F - - Si 5. 1 3. 4 P - - S 0. 8 4. 4 Cl - 32. 5 Br - 98. 0
Таблица. Вклад изотопов некоторых элементов в величину пика (М+1) и (М+2) Элемент Вклад в (М+1), % Вклад в (М+2), % N 0. 37 - O 0. 04 0. 2 F - - Si 5. 1 3. 4 P - - S 0. 8 4. 4 Cl - 32. 5 Br - 98. 0
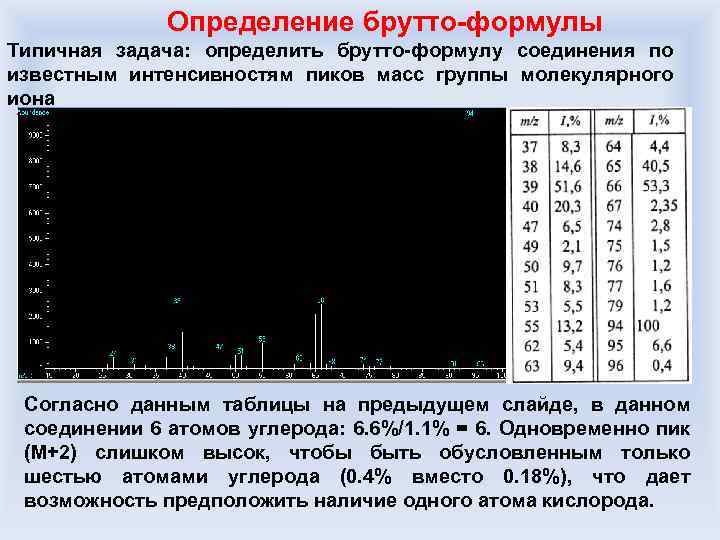 Определение брутто-формулы Типичная задача: определить брутто-формулу соединения по известным интенсивностям пиков масс группы молекулярного иона Согласно данным таблицы на предыдущем слайде, в данном соединении 6 атомов углерода: 6. 6%/1. 1% = 6. Одновременно пик (М+2) слишком высок, чтобы быть обусловленным только шестью атомами углерода (0. 4% вместо 0. 18%), что дает возможность предположить наличие одного атома кислорода.
Определение брутто-формулы Типичная задача: определить брутто-формулу соединения по известным интенсивностям пиков масс группы молекулярного иона Согласно данным таблицы на предыдущем слайде, в данном соединении 6 атомов углерода: 6. 6%/1. 1% = 6. Одновременно пик (М+2) слишком высок, чтобы быть обусловленным только шестью атомами углерода (0. 4% вместо 0. 18%), что дает возможность предположить наличие одного атома кислорода.
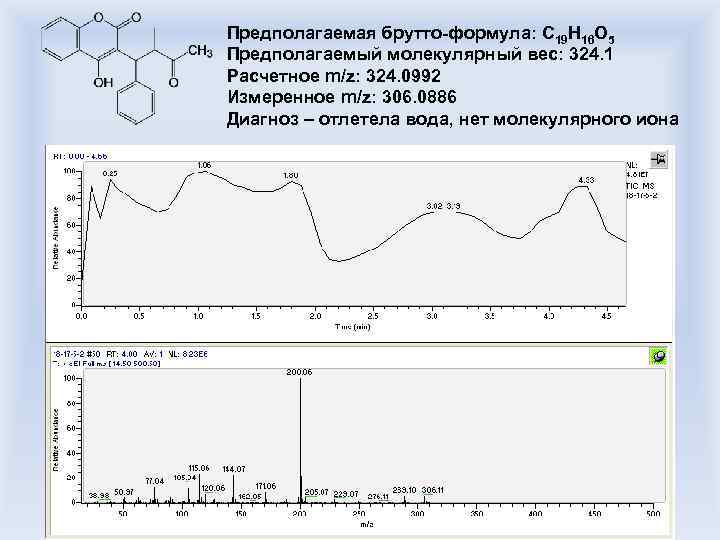 Предполагаемая брутто-формула: С 19 Н 16 О 5 Предполагаемый молекулярный вес: 324. 1 Расчетное m/z: 324. 0992 Измеренное m/z: 306. 0886 Диагноз – отлетела вода, нет молекулярного иона
Предполагаемая брутто-формула: С 19 Н 16 О 5 Предполагаемый молекулярный вес: 324. 1 Расчетное m/z: 324. 0992 Измеренное m/z: 306. 0886 Диагноз – отлетела вода, нет молекулярного иона
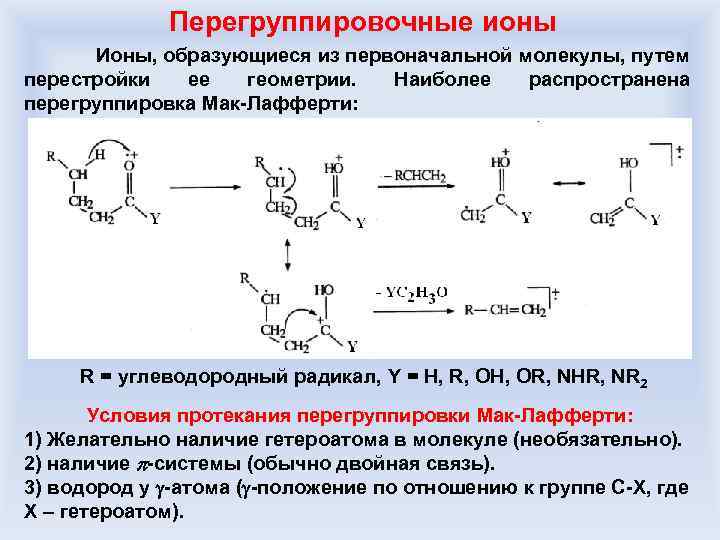 Перегруппировочные ионы Ионы, образующиеся из первоначальной молекулы, путем перестройки ее геометрии. Наиболее распространена перегруппировка Мак-Лафферти: R = углеводородный радикал, Y = H, R, OH, OR, NHR, NR 2 Условия протекания перегруппировки Мак-Лафферти: 1) Желательно наличие гетероатома в молекуле (необязательно). 2) наличие -системы (обычно двойная связь). 3) водород у -атома ( -положение по отношению к группе С-Х, где Х – гетероатом).
Перегруппировочные ионы Ионы, образующиеся из первоначальной молекулы, путем перестройки ее геометрии. Наиболее распространена перегруппировка Мак-Лафферти: R = углеводородный радикал, Y = H, R, OH, OR, NHR, NR 2 Условия протекания перегруппировки Мак-Лафферти: 1) Желательно наличие гетероатома в молекуле (необязательно). 2) наличие -системы (обычно двойная связь). 3) водород у -атома ( -положение по отношению к группе С-Х, где Х – гетероатом).
 Перегруппировочные ионы Перегруппировка атомов, не включающих атом водорода, называется скелетной. Примером перегруппировки с участием атомов водорода может служить перегруппировка неопентана: Следует отметить, что представления о механизме образования перегруппировочных ионов основаны на различных допущениях, требующих более строгого теоретического и экспериментального подтверждения. В частности, в случае неопентана возможны несколько различных механизмов образования этильного катион-радикала.
Перегруппировочные ионы Перегруппировка атомов, не включающих атом водорода, называется скелетной. Примером перегруппировки с участием атомов водорода может служить перегруппировка неопентана: Следует отметить, что представления о механизме образования перегруппировочных ионов основаны на различных допущениях, требующих более строгого теоретического и экспериментального подтверждения. В частности, в случае неопентана возможны несколько различных механизмов образования этильного катион-радикала.
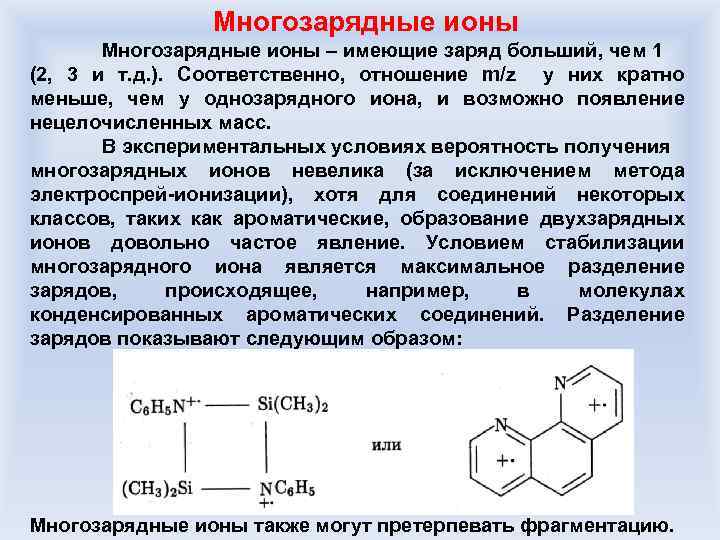 Многозарядные ионы – имеющие заряд больший, чем 1 (2, 3 и т. д. ). Соответственно, отношение m/z у них кратно меньше, чем у однозарядного иона, и возможно появление нецелочисленных масс. В экспериментальных условиях вероятность получения многозарядных ионов невелика (за исключением метода электроспрей-ионизации), хотя для соединений некоторых классов, таких как ароматические, образование двухзарядных ионов довольно частое явление. Условием стабилизации многозарядного иона является максимальное разделение зарядов, происходящее, например, в молекулах конденсированных ароматических соединений. Разделение зарядов показывают следующим образом: Многозарядные ионы также могут претерпевать фрагментацию.
Многозарядные ионы – имеющие заряд больший, чем 1 (2, 3 и т. д. ). Соответственно, отношение m/z у них кратно меньше, чем у однозарядного иона, и возможно появление нецелочисленных масс. В экспериментальных условиях вероятность получения многозарядных ионов невелика (за исключением метода электроспрей-ионизации), хотя для соединений некоторых классов, таких как ароматические, образование двухзарядных ионов довольно частое явление. Условием стабилизации многозарядного иона является максимальное разделение зарядов, происходящее, например, в молекулах конденсированных ароматических соединений. Разделение зарядов показывают следующим образом: Многозарядные ионы также могут претерпевать фрагментацию.
 Метастабильные ионы Ионы, имеющие время жизни порядка 10 -6 -10 -5 с, далее претерпевают распад на ион и нейтральную частицу. Время жизни метастабильных ионов короче, чем время пролета через масс-анализатор. В результате зарегистрированное детектором соотношение массы к заряду изменяется, что приводит к образованию слабого уширенного (размытого) пика, при этом максимум пика, как правило, соответствует нецелочисленным значениям массовых чисел. Регистрация в масс-спектре метабильного иона в ряде случаев является полезной, т. к. позволяет доказать протекание конкретной реакции, связывающей «родительский» и «дочерний» ионы.
Метастабильные ионы Ионы, имеющие время жизни порядка 10 -6 -10 -5 с, далее претерпевают распад на ион и нейтральную частицу. Время жизни метастабильных ионов короче, чем время пролета через масс-анализатор. В результате зарегистрированное детектором соотношение массы к заряду изменяется, что приводит к образованию слабого уширенного (размытого) пика, при этом максимум пика, как правило, соответствует нецелочисленным значениям массовых чисел. Регистрация в масс-спектре метабильного иона в ряде случаев является полезной, т. к. позволяет доказать протекание конкретной реакции, связывающей «родительский» и «дочерний» ионы.
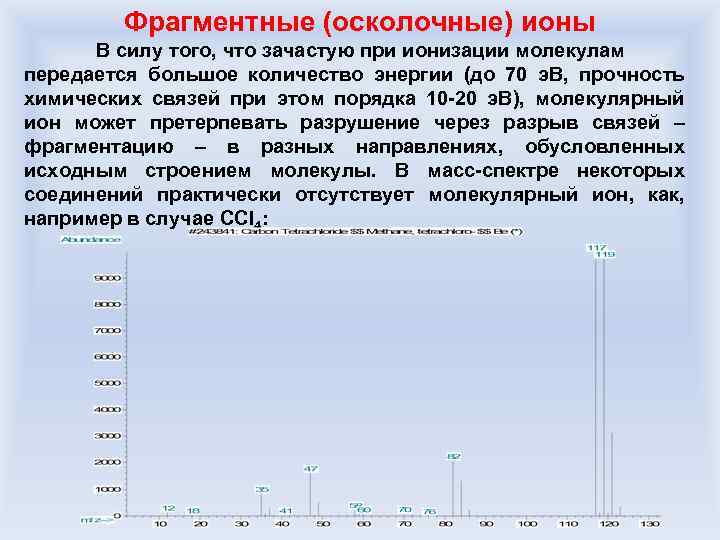 Фрагментные (осколочные) ионы В силу того, что зачастую при ионизации молекулам передается большое количество энергии (до 70 э. В, прочность химических связей при этом порядка 10 -20 э. В), молекулярный ион может претерпевать разрушение через разрыв связей – фрагментацию – в разных направлениях, обусловленных исходным строением молекулы. В масс-спектре некоторых соединений практически отсутствует молекулярный ион, как, например в случае CCl 4:
Фрагментные (осколочные) ионы В силу того, что зачастую при ионизации молекулам передается большое количество энергии (до 70 э. В, прочность химических связей при этом порядка 10 -20 э. В), молекулярный ион может претерпевать разрушение через разрыв связей – фрагментацию – в разных направлениях, обусловленных исходным строением молекулы. В масс-спектре некоторых соединений практически отсутствует молекулярный ион, как, например в случае CCl 4:
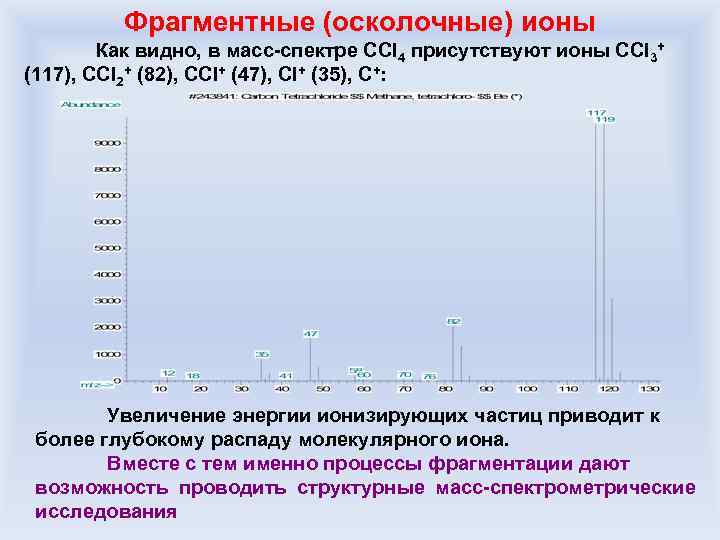 Фрагментные (осколочные) ионы Как видно, в масс-спектре CCl 4 присутствуют ионы CCl 3+ (117), CCl 2+ (82), CCl+ (47), Cl+ (35), C+: Увеличение энергии ионизирующих частиц приводит к более глубокому распаду молекулярного иона. Вместе с тем именно процессы фрагментации дают возможность проводить структурные масс-спектрометрические исследования
Фрагментные (осколочные) ионы Как видно, в масс-спектре CCl 4 присутствуют ионы CCl 3+ (117), CCl 2+ (82), CCl+ (47), Cl+ (35), C+: Увеличение энергии ионизирующих частиц приводит к более глубокому распаду молекулярного иона. Вместе с тем именно процессы фрагментации дают возможность проводить структурные масс-спектрометрические исследования
 ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Общая строгая теория распада молекулярного иона отсутствует, т. к. для описания фрагментации требуется знание электронных состояний ионов разных типов и вероятностей перехода между этими состояниями. Вместе с тем накопленный массив экспериментальных данных позволил сформировать качественные полуэмпирические представления о направлениях фрагментации, которые используют принципы сохранения структуры молекулы при ее ионизации (принцип Франка-Кондона) и минимума структурных изменений в результате разрыва связей при фрагментации.
ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Общая строгая теория распада молекулярного иона отсутствует, т. к. для описания фрагментации требуется знание электронных состояний ионов разных типов и вероятностей перехода между этими состояниями. Вместе с тем накопленный массив экспериментальных данных позволил сформировать качественные полуэмпирические представления о направлениях фрагментации, которые используют принципы сохранения структуры молекулы при ее ионизации (принцип Франка-Кондона) и минимума структурных изменений в результате разрыва связей при фрагментации.
 Фрагментные (осколочные) ионы: В органической масс-спектрометрии следует уделять пристальное внимание следующим фрагментным ионам: 1) Наиболее тяжелые ионы, образующиеся из М+. в результате выброса простейших частиц, т. е. без существенной перестройки в структуре исходной молекулы. 2) Ионы, характеризующиеся интенсивными пиками в спектре. наиболее 3) Характерные серии ионов, различающиеся на гомологическую разность, т. е. на 14 а. е. м. 4) Ионы с характерными изотопными пиками.
Фрагментные (осколочные) ионы: В органической масс-спектрометрии следует уделять пристальное внимание следующим фрагментным ионам: 1) Наиболее тяжелые ионы, образующиеся из М+. в результате выброса простейших частиц, т. е. без существенной перестройки в структуре исходной молекулы. 2) Ионы, характеризующиеся интенсивными пиками в спектре. наиболее 3) Характерные серии ионов, различающиеся на гомологическую разность, т. е. на 14 а. е. м. 4) Ионы с характерными изотопными пиками.
 ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 1) Для неразветвленных соединений относительная интенсивность молекулярного иона максимальна и понижается по мере увеличения разветвленности 2) С увеличением молекулярного веса в гомологическом ряду относительная интенсивность молекулярного иона обычно уменьшается (исключения: эфиры жирных кислот, которые часто встречаются, например, в экстрактах растений) 3) Распад идет преимущественно по разветвленным атомам углерода. Чем больше разветвление, тем вероятнее распад. Это результат повышения стабильности третичного карбониевого катиона по сравнению со вторичным, который, в свою очередь, стабильнее первичного: Порядок стабильности катионов: С+Н 3 < R`C+H 2 < R 2`C+H < R 3`C+
ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 1) Для неразветвленных соединений относительная интенсивность молекулярного иона максимальна и понижается по мере увеличения разветвленности 2) С увеличением молекулярного веса в гомологическом ряду относительная интенсивность молекулярного иона обычно уменьшается (исключения: эфиры жирных кислот, которые часто встречаются, например, в экстрактах растений) 3) Распад идет преимущественно по разветвленным атомам углерода. Чем больше разветвление, тем вероятнее распад. Это результат повышения стабильности третичного карбониевого катиона по сравнению со вторичным, который, в свою очередь, стабильнее первичного: Порядок стабильности катионов: С+Н 3 < R`C+H 2 < R 2`C+H < R 3`C+
 ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 4) Наибольший заместитель в разветвленной цепи отщепляется легче в виде радикала, т. к. радикал с длинной цепью может легче стабилизироваться за счет делокализации одного электрона 5) Двойные связи, циклические структуры и особенно ароматические и гетероароматические циклы стабилизируют молекулярный ион и таким образом повышают вероятность его появления (и уменьшают фрагментацию) 6) Двойные связи способствуют аллильному распаду и дают резонансно-стабилизированный аллильный карбониевый ион:
ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 4) Наибольший заместитель в разветвленной цепи отщепляется легче в виде радикала, т. к. радикал с длинной цепью может легче стабилизироваться за счет делокализации одного электрона 5) Двойные связи, циклические структуры и особенно ароматические и гетероароматические циклы стабилизируют молекулярный ион и таким образом повышают вероятность его появления (и уменьшают фрагментацию) 6) Двойные связи способствуют аллильному распаду и дают резонансно-стабилизированный аллильный карбониевый ион:
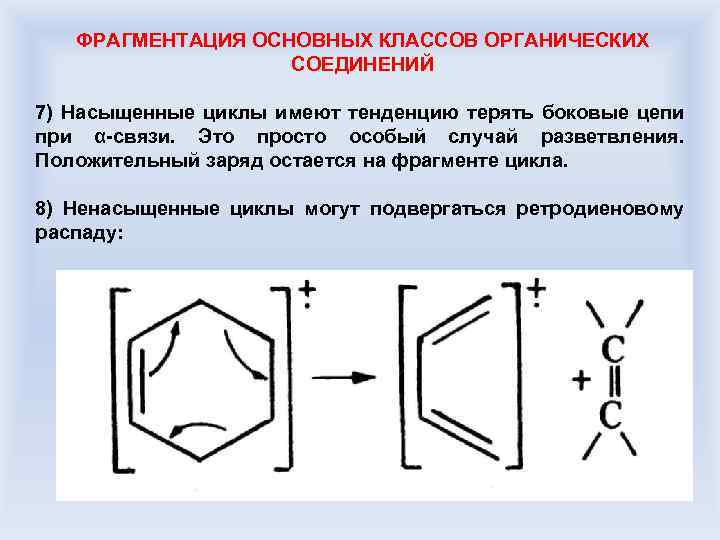 ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 7) Насыщенные циклы имеют тенденцию терять боковые цепи при α-связи. Это просто особый случай разветвления. Положительный заряд остается на фрагменте цикла. 8) Ненасыщенные циклы могут подвергаться ретродиеновому распаду:
ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 7) Насыщенные циклы имеют тенденцию терять боковые цепи при α-связи. Это просто особый случай разветвления. Положительный заряд остается на фрагменте цикла. 8) Ненасыщенные циклы могут подвергаться ретродиеновому распаду:
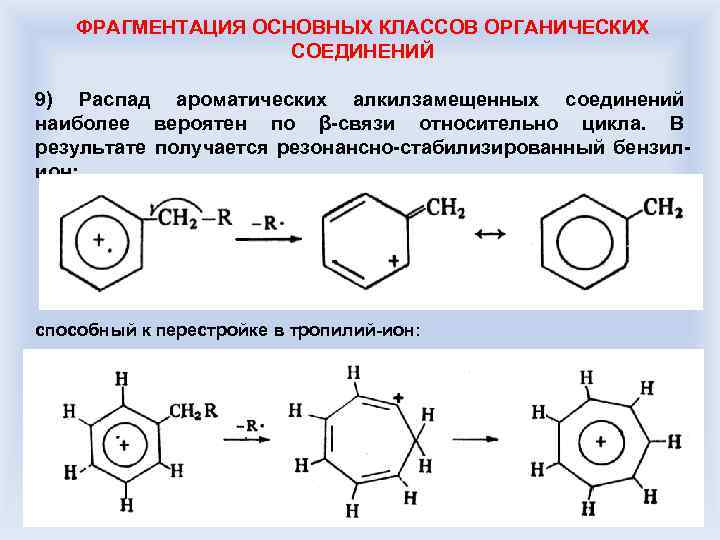 ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 9) Распад ароматических алкилзамещенных соединений наиболее вероятен по β-связи относительно цикла. В результате получается резонансно-стабилизированный бензилион: способный к перестройке в тропилий-ион:
ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 9) Распад ароматических алкилзамещенных соединений наиболее вероятен по β-связи относительно цикла. В результате получается резонансно-стабилизированный бензилион: способный к перестройке в тропилий-ион:
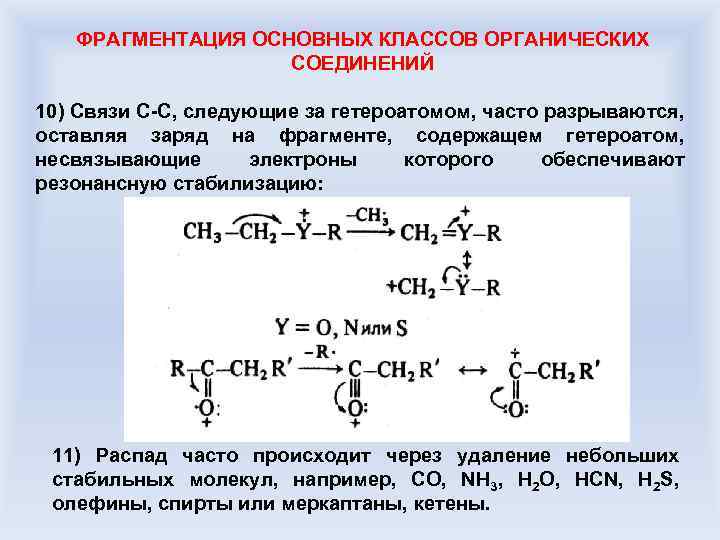 ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 10) Связи С-С, следующие за гетероатомом, часто разрываются, оставляя заряд на фрагменте, содержащем гетероатом, несвязывающие электроны которого обеспечивают резонансную стабилизацию: 11) Распад часто происходит через удаление небольших стабильных молекул, например, CO, NH 3, H 2 O, HCN, H 2 S, олефины, спирты или меркаптаны, кетены.
ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 10) Связи С-С, следующие за гетероатомом, часто разрываются, оставляя заряд на фрагменте, содержащем гетероатом, несвязывающие электроны которого обеспечивают резонансную стабилизацию: 11) Распад часто происходит через удаление небольших стабильных молекул, например, CO, NH 3, H 2 O, HCN, H 2 S, олефины, спирты или меркаптаны, кетены.
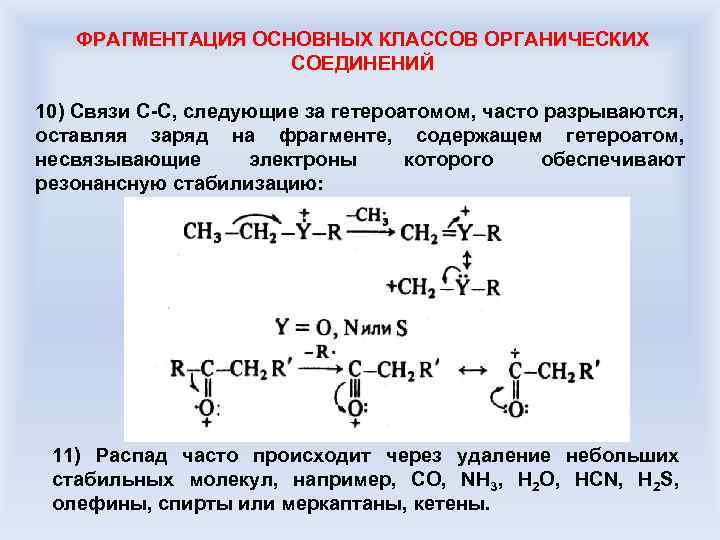 ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 10) Связи С-С, следующие за гетероатомом, часто разрываются, оставляя заряд на фрагменте, содержащем гетероатом, несвязывающие электроны которого обеспечивают резонансную стабилизацию: 11) Распад часто происходит через удаление небольших стабильных молекул, например, CO, NH 3, H 2 O, HCN, H 2 S, олефины, спирты или меркаптаны, кетены.
ФРАГМЕНТАЦИЯ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 10) Связи С-С, следующие за гетероатомом, часто разрываются, оставляя заряд на фрагменте, содержащем гетероатом, несвязывающие электроны которого обеспечивают резонансную стабилизацию: 11) Распад часто происходит через удаление небольших стабильных молекул, например, CO, NH 3, H 2 O, HCN, H 2 S, олефины, спирты или меркаптаны, кетены.
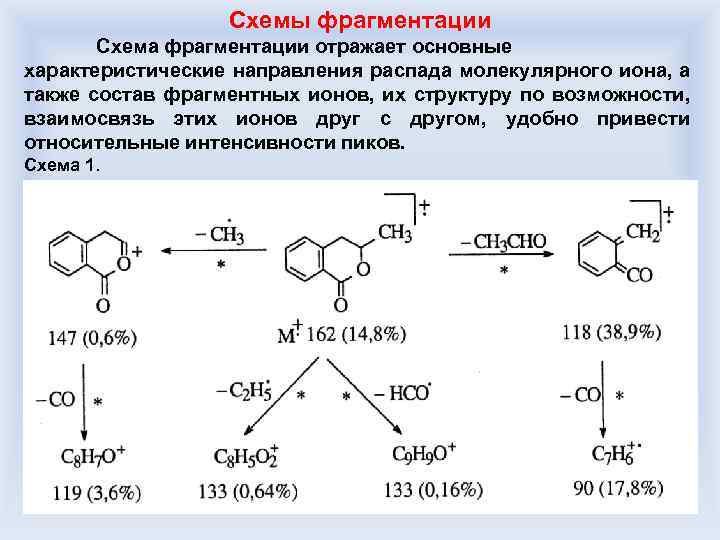 Схемы фрагментации Схема фрагментации отражает основные характеристические направления распада молекулярного иона, а также состав фрагментных ионов, их структуру по возможности, взаимосвязь этих ионов друг с другом, удобно привести относительные интенсивности пиков. Схема 1.
Схемы фрагментации Схема фрагментации отражает основные характеристические направления распада молекулярного иона, а также состав фрагментных ионов, их структуру по возможности, взаимосвязь этих ионов друг с другом, удобно привести относительные интенсивности пиков. Схема 1.
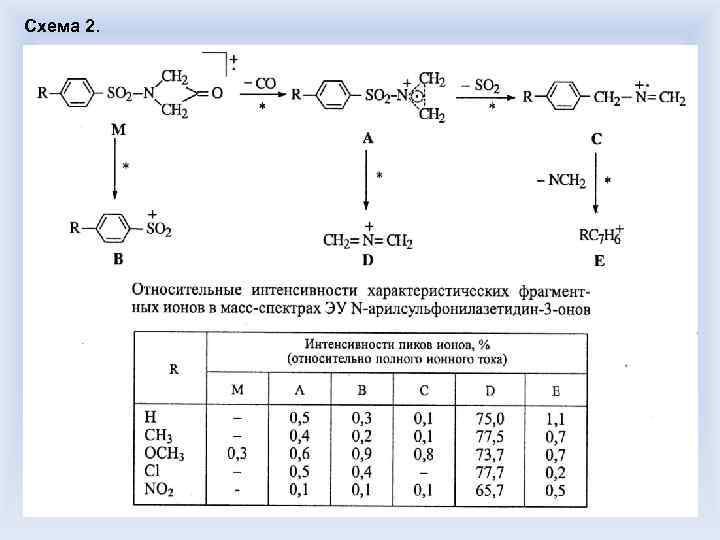 Схема 2.
Схема 2.
![Еще один вариант представления фрагментации Масс-спектр (NH 4+)2[5 -NATZ]2 - из работы Илюшин М. Еще один вариант представления фрагментации Масс-спектр (NH 4+)2[5 -NATZ]2 - из работы Илюшин М.](https://present5.com/presentation/18744133_169858409/image-65.jpg) Еще один вариант представления фрагментации Масс-спектр (NH 4+)2[5 -NATZ]2 - из работы Илюшин М. А. , Терпигорев А. Н. , Целинский И. В. Влияние изомерного строения (Nнитроамино)тетразолов на свойства их солей // ЖОХ. 1999. Т. 69. Вып. 10. С. 1727 -1730. Соль Осколочные ионы, m/z (% полного ионного тока) (NH 4+)2[5 -NATZ]2 M=164 г/моль 129(0. 4), 97(0. 7), 83(0. 7), 69(1. 2), 60(1. 2), 55(1. 6), 46(6. 5), 44(4. 0), 42(7. 0), 41(2. 6), 36(5. 7), 30(14. 0), 28(34. 1), 18(20. 3) 5 -нитраминотетразол (5 -NATZ):
Еще один вариант представления фрагментации Масс-спектр (NH 4+)2[5 -NATZ]2 - из работы Илюшин М. А. , Терпигорев А. Н. , Целинский И. В. Влияние изомерного строения (Nнитроамино)тетразолов на свойства их солей // ЖОХ. 1999. Т. 69. Вып. 10. С. 1727 -1730. Соль Осколочные ионы, m/z (% полного ионного тока) (NH 4+)2[5 -NATZ]2 M=164 г/моль 129(0. 4), 97(0. 7), 83(0. 7), 69(1. 2), 60(1. 2), 55(1. 6), 46(6. 5), 44(4. 0), 42(7. 0), 41(2. 6), 36(5. 7), 30(14. 0), 28(34. 1), 18(20. 3) 5 -нитраминотетразол (5 -NATZ):
 Схемы фрагментации Следует отметить, что в настоящий момент схемы фрагментации не корректно строить лишь на основании массспектра низкого разрешения, как это было в начале развития метода масс-спектрометрии. Во-первых, одному и тому же целому массовому числу может соответствовать несколько комбинаций атомов, порой встречающихся в одной молекуле. Во-вторых, возможна существенная перестройка фрагментных ионов, в результате чего сложно объяснить дальнейшие процессы фрагментации. Для корректного построения схемы фрагментации в настоящее время используется масс-спектрометрия высокого разрешения для определения брутто-формул фрагментных ионов, а также «тандемная» (MS-MS) масс-спектрометрия, которая позволяет прослеживать фрагментацию уже фрагментных ионов. Технически (если позволяет имеющееся экспеериментальное оборудование) такое исследование выполняется так: исследователь выбирает интересующий его ион и прослеживает только его превращения, при необходимости «накачивая» его энергией. Такой метод дает информацию о структуре изучаемого иона.
Схемы фрагментации Следует отметить, что в настоящий момент схемы фрагментации не корректно строить лишь на основании массспектра низкого разрешения, как это было в начале развития метода масс-спектрометрии. Во-первых, одному и тому же целому массовому числу может соответствовать несколько комбинаций атомов, порой встречающихся в одной молекуле. Во-вторых, возможна существенная перестройка фрагментных ионов, в результате чего сложно объяснить дальнейшие процессы фрагментации. Для корректного построения схемы фрагментации в настоящее время используется масс-спектрометрия высокого разрешения для определения брутто-формул фрагментных ионов, а также «тандемная» (MS-MS) масс-спектрометрия, которая позволяет прослеживать фрагментацию уже фрагментных ионов. Технически (если позволяет имеющееся экспеериментальное оборудование) такое исследование выполняется так: исследователь выбирает интересующий его ион и прослеживает только его превращения, при необходимости «накачивая» его энергией. Такой метод дает информацию о структуре изучаемого иона.
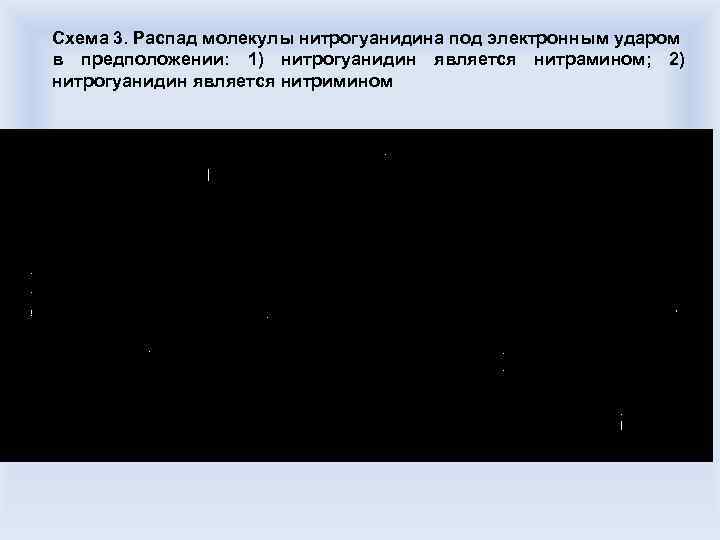 Схема 3. Распад молекулы нитрогуанидина под электронным ударом в предположении: 1) нитрогуанидин является нитрамином; 2) нитрогуанидин является нитримином
Схема 3. Распад молекулы нитрогуанидина под электронным ударом в предположении: 1) нитрогуанидин является нитрамином; 2) нитрогуанидин является нитримином
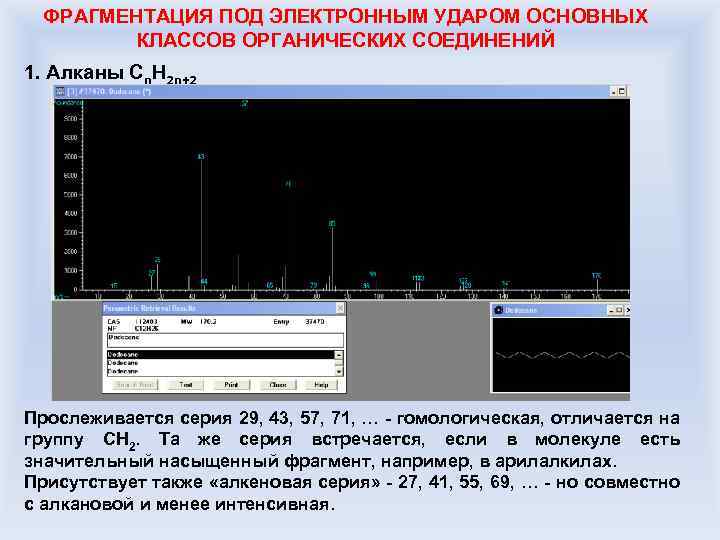 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 1. Алканы Cn. H 2 n+2 Прослеживается серия 29, 43, 57, 71, … - гомологическая, отличается на группу CH 2. Та же серия встречается, если в молекуле есть значительный насыщенный фрагмент, например, в арилалкилах. Присутствует также «алкеновая серия» - 27, 41, 55, 69, … - но совместно с алкановой и менее интенсивная.
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 1. Алканы Cn. H 2 n+2 Прослеживается серия 29, 43, 57, 71, … - гомологическая, отличается на группу CH 2. Та же серия встречается, если в молекуле есть значительный насыщенный фрагмент, например, в арилалкилах. Присутствует также «алкеновая серия» - 27, 41, 55, 69, … - но совместно с алкановой и менее интенсивная.
 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 2. Алкены и диены Прослеживается алкеновая серия 27, 41, 55, 69, … - гомологическая, отличается на группу CH 2. Присутствует также «алкановая серия» - 29, 43, 57, 71, …, но, в отличие от алканов, интенсивность «алкеновой серии» выше.
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 2. Алкены и диены Прослеживается алкеновая серия 27, 41, 55, 69, … - гомологическая, отличается на группу CH 2. Присутствует также «алкановая серия» - 29, 43, 57, 71, …, но, в отличие от алканов, интенсивность «алкеновой серии» выше.
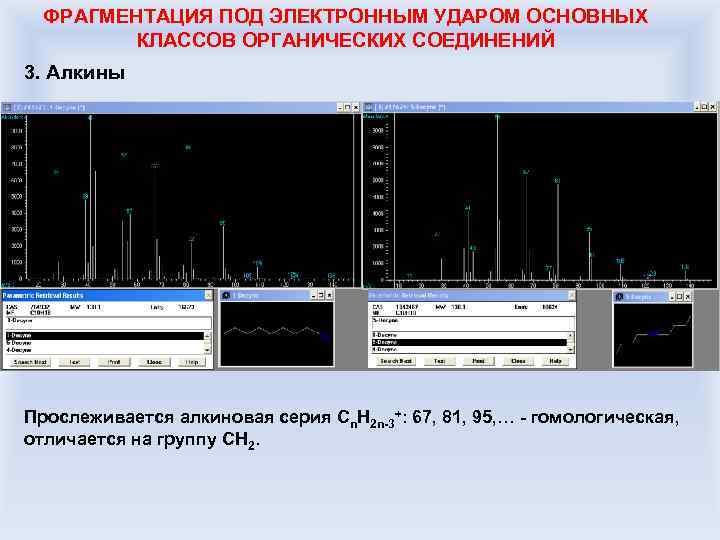 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 3. Алкины Прослеживается алкиновая серия Сn. H 2 n-3+: 67, 81, 95, … - гомологическая, отличается на группу CH 2.
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 3. Алкины Прослеживается алкиновая серия Сn. H 2 n-3+: 67, 81, 95, … - гомологическая, отличается на группу CH 2.
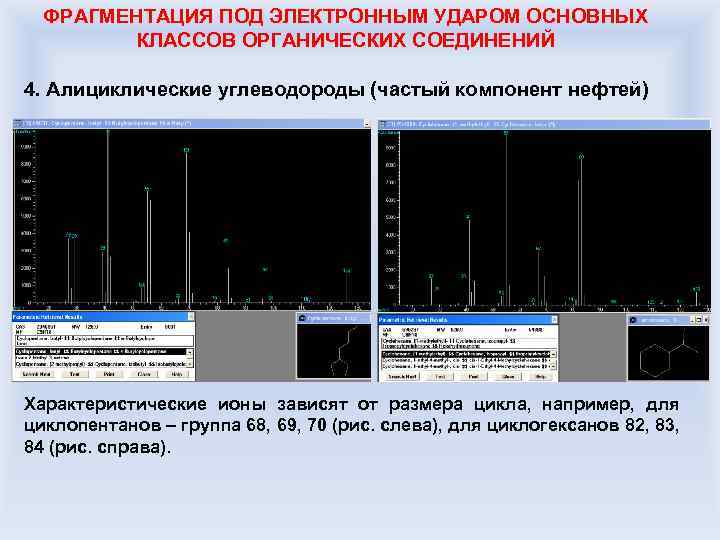 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 4. Алициклические углеводороды (частый компонент нефтей) Характеристические ионы зависят от размера цикла, например, для циклопентанов – группа 68, 69, 70 (рис. слева), для циклогексанов 82, 83, 84 (рис. справа).
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 4. Алициклические углеводороды (частый компонент нефтей) Характеристические ионы зависят от размера цикла, например, для циклопентанов – группа 68, 69, 70 (рис. слева), для циклогексанов 82, 83, 84 (рис. справа).
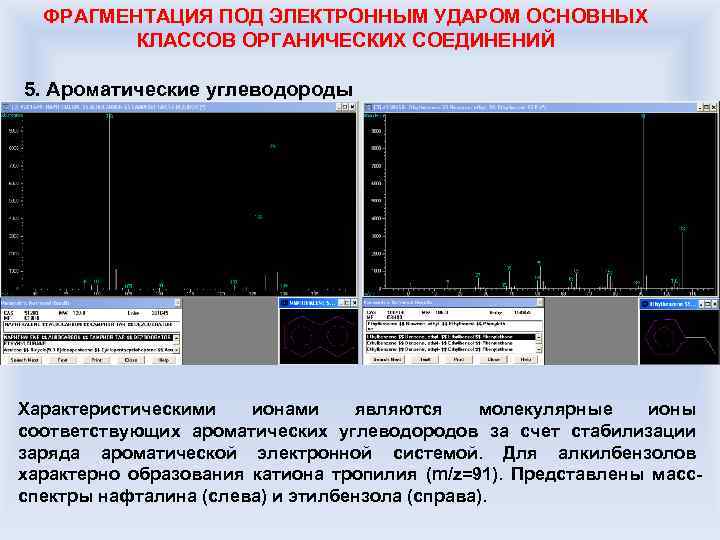 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 5. Ароматические углеводороды Характеристическими ионами являются молекулярные ионы соответствующих ароматических углеводородов за счет стабилизации заряда ароматической электронной системой. Для алкилбензолов характерно образования катиона тропилия (m/z=91). Представлены массспектры нафталина (слева) и этилбензола (справа).
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 5. Ароматические углеводороды Характеристическими ионами являются молекулярные ионы соответствующих ароматических углеводородов за счет стабилизации заряда ароматической электронной системой. Для алкилбензолов характерно образования катиона тропилия (m/z=91). Представлены массспектры нафталина (слева) и этилбензола (справа).
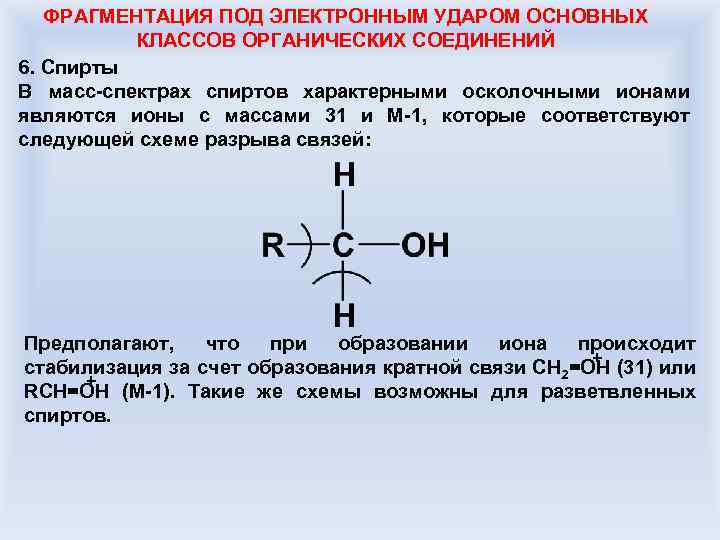 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 6. Спирты В масс-спектрах спиртов характерными осколочными ионами являются ионы с массами 31 и M-1, которые соответствуют следующей схеме разрыва связей: Предполагают, что при образовании иона происходит + стабилизация за счет образования кратной связи CH 2=OH (31) или + RCH=OH (M-1). Такие же схемы возможны для разветвленных спиртов.
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 6. Спирты В масс-спектрах спиртов характерными осколочными ионами являются ионы с массами 31 и M-1, которые соответствуют следующей схеме разрыва связей: Предполагают, что при образовании иона происходит + стабилизация за счет образования кратной связи CH 2=OH (31) или + RCH=OH (M-1). Такие же схемы возможны для разветвленных спиртов.
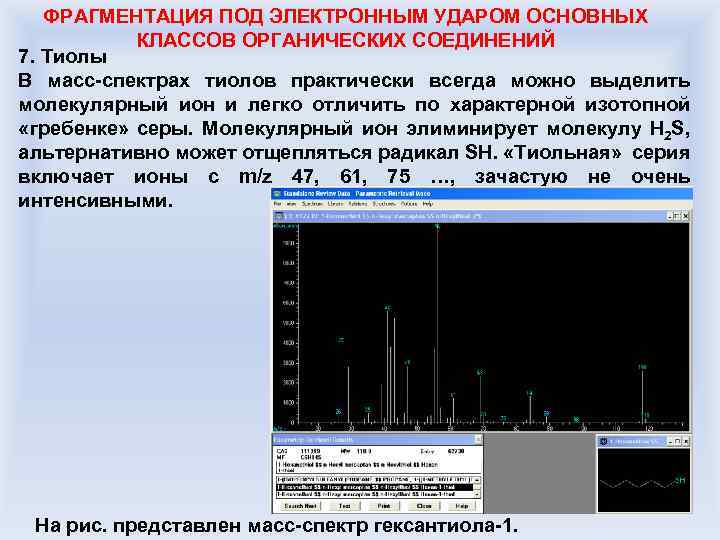 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 7. Тиолы В масс-спектрах тиолов практически всегда можно выделить молекулярный ион и легко отличить по характерной изотопной «гребенке» серы. Молекулярный ион элиминирует молекулу H 2 S, альтернативно может отщепляться радикал SH. «Тиольная» серия включает ионы с m/z 47, 61, 75 …, зачастую не очень интенсивными. На рис. представлен масс-спектр гексантиола-1.
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 7. Тиолы В масс-спектрах тиолов практически всегда можно выделить молекулярный ион и легко отличить по характерной изотопной «гребенке» серы. Молекулярный ион элиминирует молекулу H 2 S, альтернативно может отщепляться радикал SH. «Тиольная» серия включает ионы с m/z 47, 61, 75 …, зачастую не очень интенсивными. На рис. представлен масс-спектр гексантиола-1.
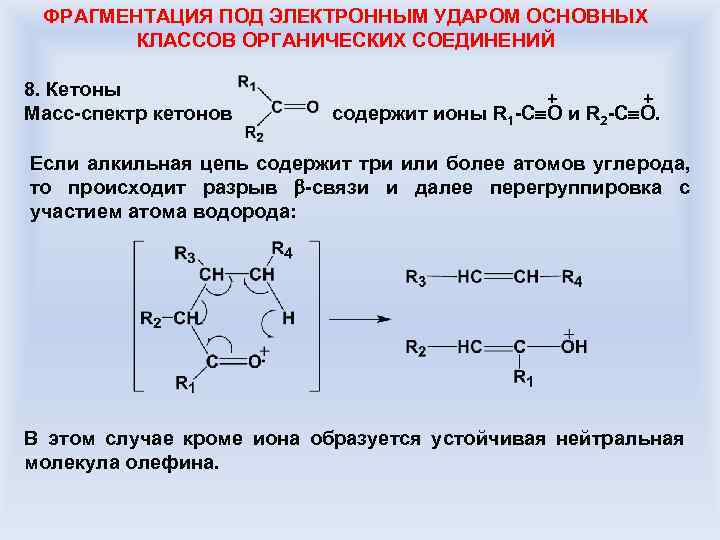 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 8. Кетоны + + Масс-спектр кетонов содержит ионы R 1 -C O и R 2 -C O. Если алкильная цепь содержит три или более атомов углерода, то происходит разрыв -связи и далее перегруппировка с участием атома водорода: В этом случае кроме иона образуется устойчивая нейтральная молекула олефина.
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 8. Кетоны + + Масс-спектр кетонов содержит ионы R 1 -C O и R 2 -C O. Если алкильная цепь содержит три или более атомов углерода, то происходит разрыв -связи и далее перегруппировка с участием атома водорода: В этом случае кроме иона образуется устойчивая нейтральная молекула олефина.
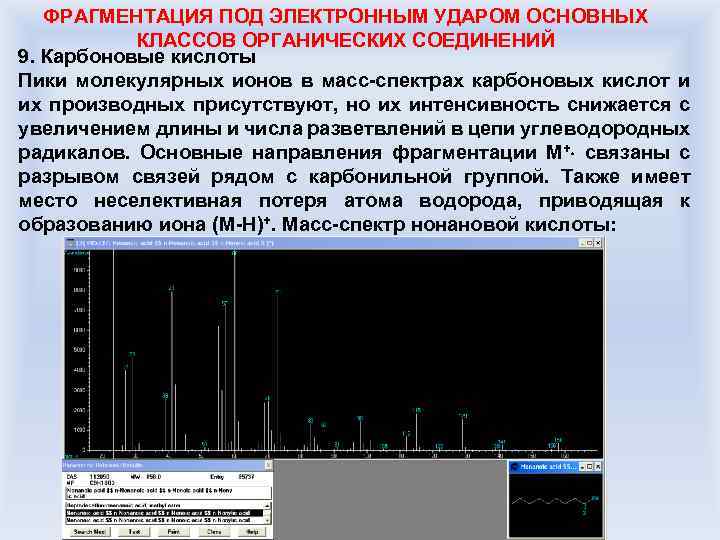 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 9. Карбоновые кислоты Пики молекулярных ионов в масс-спектрах карбоновых кислот и их производных присутствуют, но их интенсивность снижается с увеличением длины и числа разветвлений в цепи углеводородных радикалов. Основные направления фрагментации M+ связаны с разрывом связей рядом с карбонильной группой. Также имеет место неселективная потеря атома водорода, приводящая к образованию иона (M-H)+. Масс-спектр нонановой кислоты:
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 9. Карбоновые кислоты Пики молекулярных ионов в масс-спектрах карбоновых кислот и их производных присутствуют, но их интенсивность снижается с увеличением длины и числа разветвлений в цепи углеводородных радикалов. Основные направления фрагментации M+ связаны с разрывом связей рядом с карбонильной группой. Также имеет место неселективная потеря атома водорода, приводящая к образованию иона (M-H)+. Масс-спектр нонановой кислоты:
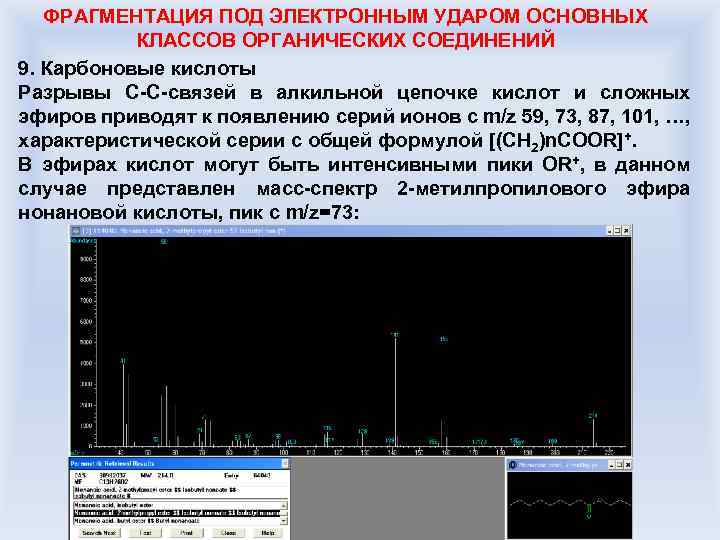 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 9. Карбоновые кислоты Разрывы C-C-связей в алкильной цепочке кислот и сложных эфиров приводят к появлению серий ионов с m/z 59, 73, 87, 101, …, характеристической серии с общей формулой [(CH 2)n. COOR]+. В эфирах кислот могут быть интенсивными пики OR+, в данном случае представлен масс-спектр 2 -метилпропилового эфира нонановой кислоты, пик с m/z=73:
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 9. Карбоновые кислоты Разрывы C-C-связей в алкильной цепочке кислот и сложных эфиров приводят к появлению серий ионов с m/z 59, 73, 87, 101, …, характеристической серии с общей формулой [(CH 2)n. COOR]+. В эфирах кислот могут быть интенсивными пики OR+, в данном случае представлен масс-спектр 2 -метилпропилового эфира нонановой кислоты, пик с m/z=73:
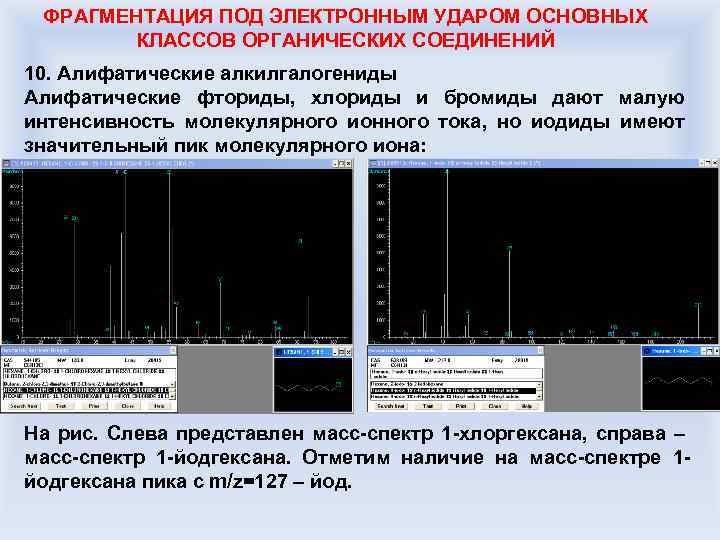 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 10. Алифатические алкилгалогениды Алифатические фториды, хлориды и бромиды дают малую интенсивность молекулярного ионного тока, но иодиды имеют значительный пик молекулярного иона: На рис. Слева представлен масс-спектр 1 -хлоргексана, справа – масс-спектр 1 -йодгексана. Отметим наличие на масс-спектре 1 йодгексана пика с m/z=127 – йод.
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 10. Алифатические алкилгалогениды Алифатические фториды, хлориды и бромиды дают малую интенсивность молекулярного ионного тока, но иодиды имеют значительный пик молекулярного иона: На рис. Слева представлен масс-спектр 1 -хлоргексана, справа – масс-спектр 1 -йодгексана. Отметим наличие на масс-спектре 1 йодгексана пика с m/z=127 – йод.
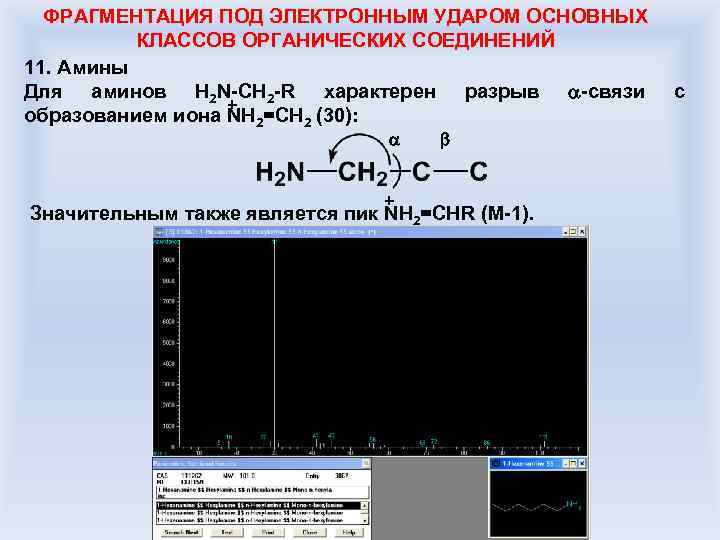 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 11. Амины Для аминов H 2 N-CH 2 -R характерен разрыв -связи с + образованием иона NH 2=CH 2 (30): + Значительным также является пик NH 2=CHR (M-1).
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 11. Амины Для аминов H 2 N-CH 2 -R характерен разрыв -связи с + образованием иона NH 2=CH 2 (30): + Значительным также является пик NH 2=CHR (M-1).
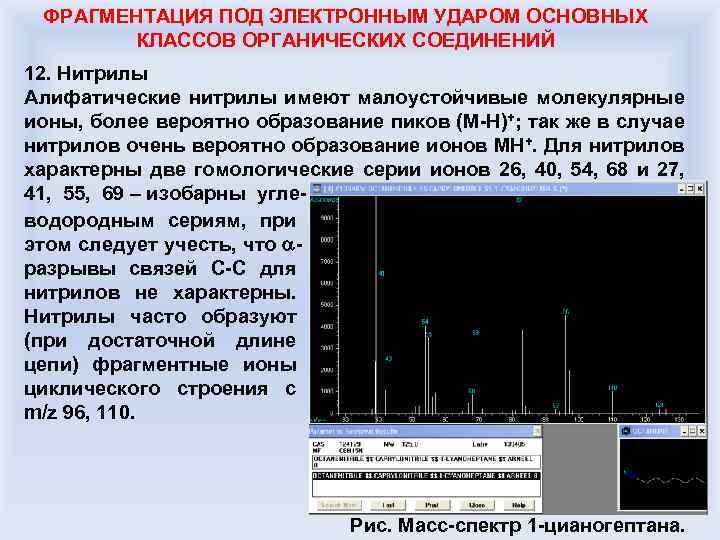 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 12. Нитрилы Алифатические нитрилы имеют малоустойчивые молекулярные ионы, более вероятно образование пиков (M-H)+; так же в случае нитрилов очень вероятно образование ионов MH+. Для нитрилов характерны две гомологические серии ионов 26, 40, 54, 68 и 27, 41, 55, 69 – изобарны углеводородным сериям, при этом следует учесть, что разрывы связей С-С для нитрилов не характерны. Нитрилы часто образуют (при достаточной длине цепи) фрагментные ионы циклического строения с m/z 96, 110. Рис. Масс-спектр 1 -цианогептана.
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 12. Нитрилы Алифатические нитрилы имеют малоустойчивые молекулярные ионы, более вероятно образование пиков (M-H)+; так же в случае нитрилов очень вероятно образование ионов MH+. Для нитрилов характерны две гомологические серии ионов 26, 40, 54, 68 и 27, 41, 55, 69 – изобарны углеводородным сериям, при этом следует учесть, что разрывы связей С-С для нитрилов не характерны. Нитрилы часто образуют (при достаточной длине цепи) фрагментные ионы циклического строения с m/z 96, 110. Рис. Масс-спектр 1 -цианогептана.
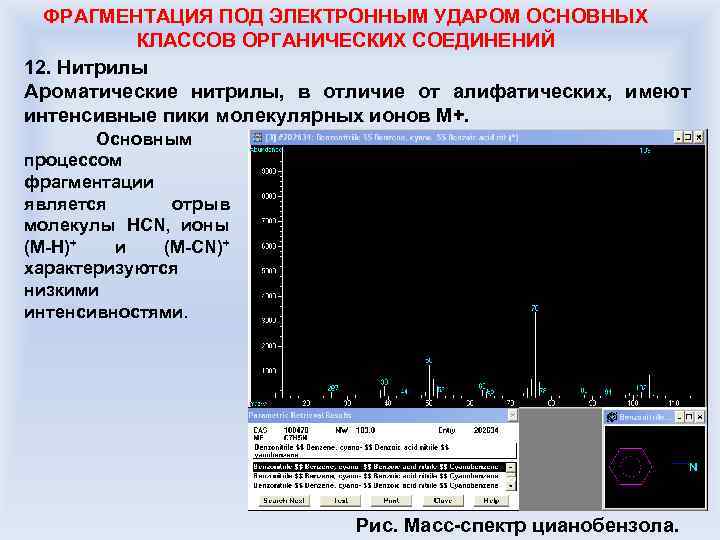 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 12. Нитрилы Ароматические нитрилы, в отличие от алифатических, имеют интенсивные пики молекулярных ионов М+. Основным процессом фрагментации является отрыв молекулы HCN, ионы (М-Н)+ и (M-CN)+ характеризуются низкими интенсивностями. Рис. Масс-спектр цианобензола.
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 12. Нитрилы Ароматические нитрилы, в отличие от алифатических, имеют интенсивные пики молекулярных ионов М+. Основным процессом фрагментации является отрыв молекулы HCN, ионы (М-Н)+ и (M-CN)+ характеризуются низкими интенсивностями. Рис. Масс-спектр цианобензола.
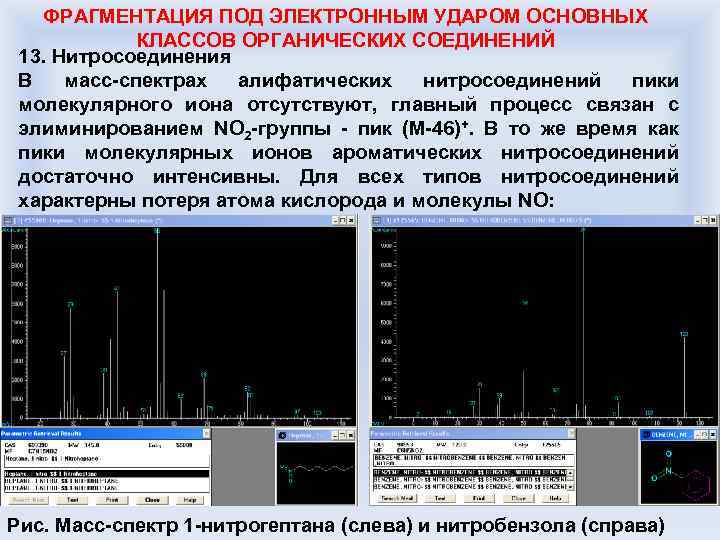 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 13. Нитросоединения В масс-спектрах алифатических нитросоединений пики молекулярного иона отсутствуют, главный процесс связан с элиминированием NO 2 -группы - пик (M-46)+. В то же время как пики молекулярных ионов ароматических нитросоединений достаточно интенсивны. Для всех типов нитросоединений характерны потеря атома кислорода и молекулы NO: Рис. Масс-спектр 1 -нитрогептана (слева) и нитробензола (справа)
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 13. Нитросоединения В масс-спектрах алифатических нитросоединений пики молекулярного иона отсутствуют, главный процесс связан с элиминированием NO 2 -группы - пик (M-46)+. В то же время как пики молекулярных ионов ароматических нитросоединений достаточно интенсивны. Для всех типов нитросоединений характерны потеря атома кислорода и молекулы NO: Рис. Масс-спектр 1 -нитрогептана (слева) и нитробензола (справа)
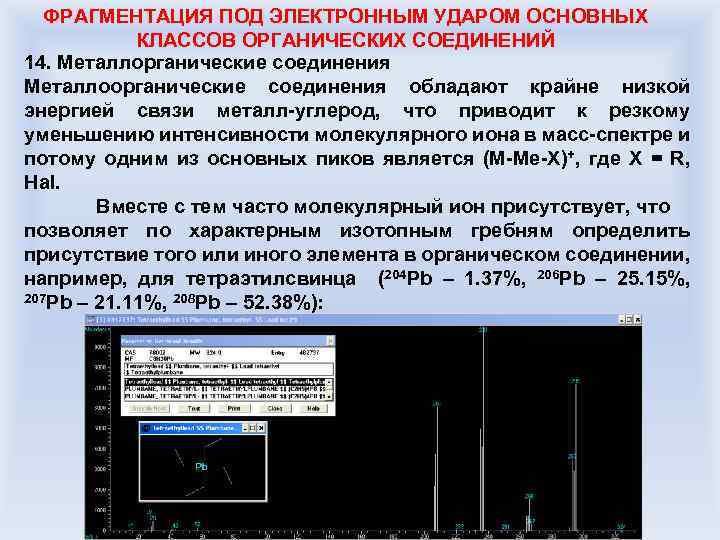 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 14. Металлорганические соединения Металлоорганические соединения обладают крайне низкой энергией связи металл-углерод, что приводит к резкому уменьшению интенсивности молекулярного иона в масс-спектре и потому одним из основных пиков является (М-Ме-X)+, где Х = R, Hal. Вместе с тем часто молекулярный ион присутствует, что позволяет по характерным изотопным гребням определить присутствие того или иного элемента в органическом соединении, например, для тетраэтилсвинца (204 Pb – 1. 37%, 206 Pb – 25. 15%, 207 Pb – 21. 11%, 208 Pb – 52. 38%):
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 14. Металлорганические соединения Металлоорганические соединения обладают крайне низкой энергией связи металл-углерод, что приводит к резкому уменьшению интенсивности молекулярного иона в масс-спектре и потому одним из основных пиков является (М-Ме-X)+, где Х = R, Hal. Вместе с тем часто молекулярный ион присутствует, что позволяет по характерным изотопным гребням определить присутствие того или иного элемента в органическом соединении, например, для тетраэтилсвинца (204 Pb – 1. 37%, 206 Pb – 25. 15%, 207 Pb – 21. 11%, 208 Pb – 52. 38%):
 ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Таблица. Характерные серии фрагментных ионов разных классов органических соединений Класс соединения Формула m/z Алканы Cn. H 2 n+1+ 15, 29, 43, 57, 71, 85… Алкены, нафтены Алкины, диены Cn. H 2 n-1+ Cn. H 2 n-3+ 27, 41, 55, 69, 83… 25, 39, 53, 67, 81… Спирты, простые эфиры Cn. H 2 n+1 O+ 31, 45, 59, 73, 87… Альдегиды, кетоны Кислоты, сложные эфиры Cn. H 2 n-1 O+ 29, 43, 57, 71, 85… Cn. H 2 n-1 O 2+ 45, 59, 73, 87, 101… Тиолы, сульфиды Амины Cn. H 2 n+1 S+ 47, 61, 75, 89, 103… (по 32 S) Cn. H 2 n+2 N+ 30, 44, 58, 72, 86, 100… Алкилхлориды Cn. H 2 n. Cl+ 35, 49, 63, 77, 91, 105… (по 35 Cl) Алкилфториды Алкилбромиды Cn. H 2 n. F+ Cn. H 2 n. Br+ 19, 33, 47, 61, 75… 79, 93, 107, 121… (по 79 Br) Алкилиодиды Нитрилы Cn. H 2 n. I+ Cn. H 2 n-2 N+ 127, 141, 155, 169… 40, 54, 68, 82, 96… Алкилбензолы 38, 39, 50 -52, 63 -65, 75 -78, 91, 105, 119…
ФРАГМЕНТАЦИЯ ПОД ЭЛЕКТРОННЫМ УДАРОМ ОСНОВНЫХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Таблица. Характерные серии фрагментных ионов разных классов органических соединений Класс соединения Формула m/z Алканы Cn. H 2 n+1+ 15, 29, 43, 57, 71, 85… Алкены, нафтены Алкины, диены Cn. H 2 n-1+ Cn. H 2 n-3+ 27, 41, 55, 69, 83… 25, 39, 53, 67, 81… Спирты, простые эфиры Cn. H 2 n+1 O+ 31, 45, 59, 73, 87… Альдегиды, кетоны Кислоты, сложные эфиры Cn. H 2 n-1 O+ 29, 43, 57, 71, 85… Cn. H 2 n-1 O 2+ 45, 59, 73, 87, 101… Тиолы, сульфиды Амины Cn. H 2 n+1 S+ 47, 61, 75, 89, 103… (по 32 S) Cn. H 2 n+2 N+ 30, 44, 58, 72, 86, 100… Алкилхлориды Cn. H 2 n. Cl+ 35, 49, 63, 77, 91, 105… (по 35 Cl) Алкилфториды Алкилбромиды Cn. H 2 n. F+ Cn. H 2 n. Br+ 19, 33, 47, 61, 75… 79, 93, 107, 121… (по 79 Br) Алкилиодиды Нитрилы Cn. H 2 n. I+ Cn. H 2 n-2 N+ 127, 141, 155, 169… 40, 54, 68, 82, 96… Алкилбензолы 38, 39, 50 -52, 63 -65, 75 -78, 91, 105, 119…
 Таким образом, опираясь на закономерности фрагментации органических соединений и данные таблицы на предыдущих слайдах, возможно в ряде случаев определить примерный класс анализируемого соединения или крупного фрагмента анализируемого соединения, что существенно упрощает задачу по установлению структуры. Целесообразно, при решении структурной задачи, определять брутто-состав фрагментных ионов. В целом, при работе с масс-спектральной информацией для решения структурных задач, полезно пользоваться алгоритмом, предложенным проф. Ф. Мак-Лафферти, представленном на следующем сайте.
Таким образом, опираясь на закономерности фрагментации органических соединений и данные таблицы на предыдущих слайдах, возможно в ряде случаев определить примерный класс анализируемого соединения или крупного фрагмента анализируемого соединения, что существенно упрощает задачу по установлению структуры. Целесообразно, при решении структурной задачи, определять брутто-состав фрагментных ионов. В целом, при работе с масс-спектральной информацией для решения структурных задач, полезно пользоваться алгоритмом, предложенным проф. Ф. Мак-Лафферти, представленном на следующем сайте.
 Алгоритм действий при интерпретации масс-спектра (Мак-Лафферти) 1) изучить всю имеющуюся информацию о веществе (спектральную, химическую, историю появления данного образца). Отметить все параметры съемки масс-спектра. Проверить значения m/z. 2) используя изотопные пики, вывести элементный состав всех фрагментов, для которых это возможно, подсчитать их степень ненасыщенности. Как вариант – использовать масс-спектрометрию высокого разрешения для определения элементного состава фрагментов. 3) Провести тест на молекулярный ион (максимальное значение m/z, нечетно-электронность, выбросы нейтральных частиц) 4) Отметить важнейшие нечетно-электронные ионы, обусловленные перегруппировочными процессами. 5) Изучить общий вид спектра (стабильность молекулярного иона, лабильность связей и т. д. ) 6) Приписать возможные структуры сериям ионов с низкой массой, важнейшим первичным нейтральным фрагментам, а также вторичным (по спектрам метастабильных ионов и активации соударением), важнейшим характеристическим ионам. 7) Постулировать структуру молекулы (тест по реальному спектру идентифицированного вещества из базы данных, например, по спектрам близких структур, по спектру, предсказанному теоретически).
Алгоритм действий при интерпретации масс-спектра (Мак-Лафферти) 1) изучить всю имеющуюся информацию о веществе (спектральную, химическую, историю появления данного образца). Отметить все параметры съемки масс-спектра. Проверить значения m/z. 2) используя изотопные пики, вывести элементный состав всех фрагментов, для которых это возможно, подсчитать их степень ненасыщенности. Как вариант – использовать масс-спектрометрию высокого разрешения для определения элементного состава фрагментов. 3) Провести тест на молекулярный ион (максимальное значение m/z, нечетно-электронность, выбросы нейтральных частиц) 4) Отметить важнейшие нечетно-электронные ионы, обусловленные перегруппировочными процессами. 5) Изучить общий вид спектра (стабильность молекулярного иона, лабильность связей и т. д. ) 6) Приписать возможные структуры сериям ионов с низкой массой, важнейшим первичным нейтральным фрагментам, а также вторичным (по спектрам метастабильных ионов и активации соударением), важнейшим характеристическим ионам. 7) Постулировать структуру молекулы (тест по реальному спектру идентифицированного вещества из базы данных, например, по спектрам близких структур, по спектру, предсказанному теоретически).
 Важнейшим инструментом для быстрой расшифровки результатов массспектрометрического анализа являются Библиотеки массспектральных данных
Важнейшим инструментом для быстрой расшифровки результатов массспектрометрического анализа являются Библиотеки массспектральных данных
 Библиотеки масс-спектральных данных NIST 07, NIST 08 – библиотеки масс-спектральных данных, созданные и поддерживаемые Национальным институтом стандартизации и технологии США, около 300 000 масс-спектров. WILEY 07 – библиотека масс-спектральных данных, созданная профессором Мак-Лафферти, при участии Национального бюро стандартов США, около 450 000 масс-спектров, во многом пересекается с библиотеками NIST. Библиотеки, созданные и поддерживаемые в НИОХ СО РАН, по природным соединениям, веществам, часто используемым в синтезах химиками НИОХ СО РАН, продуктам и полупродуктам синтезов – суммарно до 10 000 масс-спектров. Содержат, помимо самих масс-спектров, информацию о методе записи хроматограммы, из которой взят масс-спектр, время удержания или индекс удержания. Литературный поиск при помощи РЖХ, каталогов CAS и Belstein – в редких случаях.
Библиотеки масс-спектральных данных NIST 07, NIST 08 – библиотеки масс-спектральных данных, созданные и поддерживаемые Национальным институтом стандартизации и технологии США, около 300 000 масс-спектров. WILEY 07 – библиотека масс-спектральных данных, созданная профессором Мак-Лафферти, при участии Национального бюро стандартов США, около 450 000 масс-спектров, во многом пересекается с библиотеками NIST. Библиотеки, созданные и поддерживаемые в НИОХ СО РАН, по природным соединениям, веществам, часто используемым в синтезах химиками НИОХ СО РАН, продуктам и полупродуктам синтезов – суммарно до 10 000 масс-спектров. Содержат, помимо самих масс-спектров, информацию о методе записи хроматограммы, из которой взят масс-спектр, время удержания или индекс удержания. Литературный поиск при помощи РЖХ, каталогов CAS и Belstein – в редких случаях.
 Другие приложения массспектрометрии: кинетические и термодинамические массспектроскопические исследования
Другие приложения массспектрометрии: кинетические и термодинамические массспектроскопические исследования
 Кинетические исследования: 1. Определение механизмов химических процессов (в том числе по изотопным меткам). 2. Определение констант скоростей химических процессов. 3. Определение порядка и молекулярности реакции. Термодинамические исследования: 1. Определение потенциалов ионизации молекул и появления ионов. 2. Определение парциального давления паров вещества. 3. Определение теплоты сублимации. 4. Определение константы равновесия химической реакции и теплоты химической реакции. 5. Ион-молекулярные равновесия.
Кинетические исследования: 1. Определение механизмов химических процессов (в том числе по изотопным меткам). 2. Определение констант скоростей химических процессов. 3. Определение порядка и молекулярности реакции. Термодинамические исследования: 1. Определение потенциалов ионизации молекул и появления ионов. 2. Определение парциального давления паров вещества. 3. Определение теплоты сублимации. 4. Определение константы равновесия химической реакции и теплоты химической реакции. 5. Ион-молекулярные равновесия.
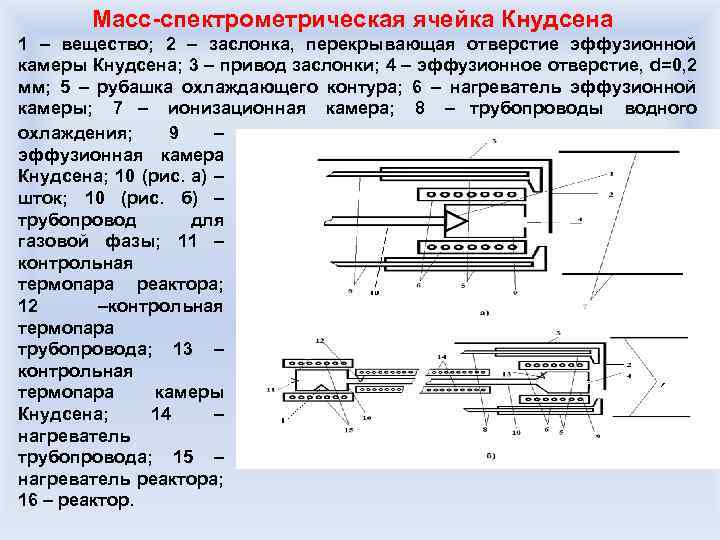 Масс-спектрометрическая ячейка Кнудсена 1 – вещество; 2 – заслонка, перекрывающая отверстие эффузионной камеры Кнудсена; 3 – привод заслонки; 4 – эффузионное отверстие, d=0, 2 мм; 5 – рубашка охлаждающего контура; 6 – нагреватель эффузионной камеры; 7 – ионизационная камера; 8 – трубопроводы водного охлаждения; 9 – эффузионная камера Кнудсена; 10 (рис. а) – шток; 10 (рис. б) – трубопровод для газовой фазы; 11 – контрольная термопара реактора; 12 –контрольная термопара трубопровода; 13 – контрольная термопара камеры Кнудсена; 14 – нагреватель трубопровода; 15 – нагреватель реактора; 16 – реактор.
Масс-спектрометрическая ячейка Кнудсена 1 – вещество; 2 – заслонка, перекрывающая отверстие эффузионной камеры Кнудсена; 3 – привод заслонки; 4 – эффузионное отверстие, d=0, 2 мм; 5 – рубашка охлаждающего контура; 6 – нагреватель эффузионной камеры; 7 – ионизационная камера; 8 – трубопроводы водного охлаждения; 9 – эффузионная камера Кнудсена; 10 (рис. а) – шток; 10 (рис. б) – трубопровод для газовой фазы; 11 – контрольная термопара реактора; 12 –контрольная термопара трубопровода; 13 – контрольная термопара камеры Кнудсена; 14 – нагреватель трубопровода; 15 – нагреватель реактора; 16 – реактор.
 Измерение теплот сублимации и испарения Уравнение Клапейрона-Клаузиуса Использование масс-спектрометрии позволяет определить теплоты сублимации (испарения) летучих веществ. Для этого измеряли интенсивность пика молекулярного иона при различных температурах, результаты вносили в интегрированную форму уравнения Клапейрона-Клаузиуса, где: I – интенсивность сигнала молекулярного иона (в произвольных единицах измерения); T – температура, K; R – универсальная газовая постоянная; H – теплота сублимации (испарения). Линеаризация этого уравнения в координатах ln(I T) от 1/Т дает возможность по углу наклона прямой определить теплоту сублимации (испарения) вещества.
Измерение теплот сублимации и испарения Уравнение Клапейрона-Клаузиуса Использование масс-спектрометрии позволяет определить теплоты сублимации (испарения) летучих веществ. Для этого измеряли интенсивность пика молекулярного иона при различных температурах, результаты вносили в интегрированную форму уравнения Клапейрона-Клаузиуса, где: I – интенсивность сигнала молекулярного иона (в произвольных единицах измерения); T – температура, K; R – универсальная газовая постоянная; H – теплота сублимации (испарения). Линеаризация этого уравнения в координатах ln(I T) от 1/Т дает возможность по углу наклона прямой определить теплоту сублимации (испарения) вещества.
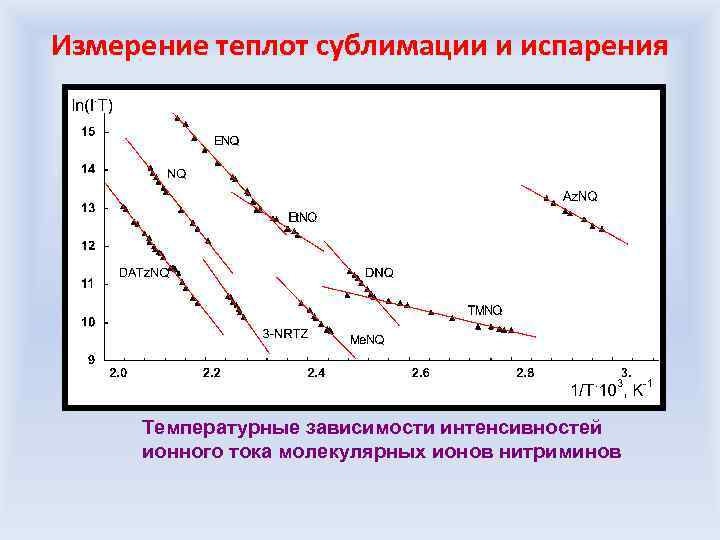 Измерение теплот сублимации и испарения Температурные зависимости интенсивностей ионного тока молекулярных ионов нитриминов
Измерение теплот сублимации и испарения Температурные зависимости интенсивностей ионного тока молекулярных ионов нитриминов
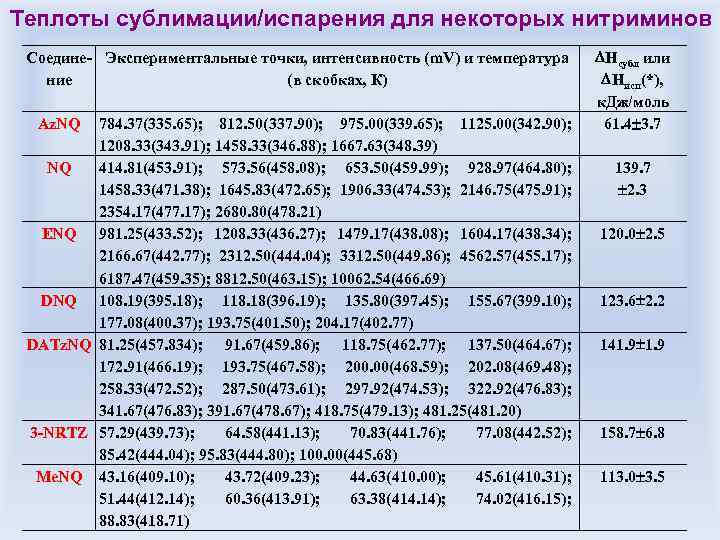 Теплоты сублимации/испарения для некоторых нитриминов Соедине- Экспериментальные точки, интенсивность (m. V) и температура ние (в скобках, К) Az. NQ 784. 37(335. 65); 812. 50(337. 90); 975. 00(339. 65); 1125. 00(342. 90); 1208. 33(343. 91); 1458. 33(346. 88); 1667. 63(348. 39) NQ 414. 81(453. 91); 573. 56(458. 08); 653. 50(459. 99); 928. 97(464. 80); 1458. 33(471. 38); 1645. 83(472. 65); 1906. 33(474. 53); 2146. 75(475. 91); 2354. 17(477. 17); 2680. 80(478. 21) ENQ 981. 25(433. 52); 1208. 33(436. 27); 1479. 17(438. 08); 1604. 17(438. 34); 2166. 67(442. 77); 2312. 50(444. 04); 3312. 50(449. 86); 4562. 57(455. 17); 6187. 47(459. 35); 8812. 50(463. 15); 10062. 54(466. 69) DNQ 108. 19(395. 18); 118. 18(396. 19); 135. 80(397. 45); 155. 67(399. 10); 177. 08(400. 37); 193. 75(401. 50); 204. 17(402. 77) DATz. NQ 81. 25(457. 834); 91. 67(459. 86); 118. 75(462. 77); 137. 50(464. 67); 172. 91(466. 19); 193. 75(467. 58); 200. 00(468. 59); 202. 08(469. 48); 258. 33(472. 52); 287. 50(473. 61); 297. 92(474. 53); 322. 92(476. 83); 341. 67(476. 83); 391. 67(478. 67); 418. 75(479. 13); 481. 25(481. 20) 3 -NRTZ 57. 29(439. 73); 64. 58(441. 13); 70. 83(441. 76); 77. 08(442. 52); 85. 42(444. 04); 95. 83(444. 80); 100. 00(445. 68) Me. NQ 43. 16(409. 10); 43. 72(409. 23); 44. 63(410. 00); 45. 61(410. 31); 51. 44(412. 14); 60. 36(413. 91); 63. 38(414. 14); 74. 02(416. 15); 88. 83(418. 71) Hсубл или Hисп(*), к. Дж/моль 61. 4 3. 7 139. 7 2. 3 120. 0 2. 5 123. 6 2. 2 141. 9 158. 7 6. 8 113. 0 3. 5
Теплоты сублимации/испарения для некоторых нитриминов Соедине- Экспериментальные точки, интенсивность (m. V) и температура ние (в скобках, К) Az. NQ 784. 37(335. 65); 812. 50(337. 90); 975. 00(339. 65); 1125. 00(342. 90); 1208. 33(343. 91); 1458. 33(346. 88); 1667. 63(348. 39) NQ 414. 81(453. 91); 573. 56(458. 08); 653. 50(459. 99); 928. 97(464. 80); 1458. 33(471. 38); 1645. 83(472. 65); 1906. 33(474. 53); 2146. 75(475. 91); 2354. 17(477. 17); 2680. 80(478. 21) ENQ 981. 25(433. 52); 1208. 33(436. 27); 1479. 17(438. 08); 1604. 17(438. 34); 2166. 67(442. 77); 2312. 50(444. 04); 3312. 50(449. 86); 4562. 57(455. 17); 6187. 47(459. 35); 8812. 50(463. 15); 10062. 54(466. 69) DNQ 108. 19(395. 18); 118. 18(396. 19); 135. 80(397. 45); 155. 67(399. 10); 177. 08(400. 37); 193. 75(401. 50); 204. 17(402. 77) DATz. NQ 81. 25(457. 834); 91. 67(459. 86); 118. 75(462. 77); 137. 50(464. 67); 172. 91(466. 19); 193. 75(467. 58); 200. 00(468. 59); 202. 08(469. 48); 258. 33(472. 52); 287. 50(473. 61); 297. 92(474. 53); 322. 92(476. 83); 341. 67(476. 83); 391. 67(478. 67); 418. 75(479. 13); 481. 25(481. 20) 3 -NRTZ 57. 29(439. 73); 64. 58(441. 13); 70. 83(441. 76); 77. 08(442. 52); 85. 42(444. 04); 95. 83(444. 80); 100. 00(445. 68) Me. NQ 43. 16(409. 10); 43. 72(409. 23); 44. 63(410. 00); 45. 61(410. 31); 51. 44(412. 14); 60. 36(413. 91); 63. 38(414. 14); 74. 02(416. 15); 88. 83(418. 71) Hсубл или Hисп(*), к. Дж/моль 61. 4 3. 7 139. 7 2. 3 120. 0 2. 5 123. 6 2. 2 141. 9 158. 7 6. 8 113. 0 3. 5
 Обработка хромато-массспектрограмм: компьютерная программа Standalone Review Data © HP
Обработка хромато-массспектрограмм: компьютерная программа Standalone Review Data © HP
 Программа обработки данных Standalone Review Data © HP Была разработана для использования в лабораториях и учебных заведениях, отличается простотой и удобством в обращении, при этом имеет весь необходимый функционал для работы с хромато-массспектрометрическими данными: позволяет обрабатывать хроматограммы, выбирать из них масс-спектры индивидуальных соединений, работать с готовыми базами данных масс-спектров и создавать свои библиотеки масс-спектров соединений.
Программа обработки данных Standalone Review Data © HP Была разработана для использования в лабораториях и учебных заведениях, отличается простотой и удобством в обращении, при этом имеет весь необходимый функционал для работы с хромато-массспектрометрическими данными: позволяет обрабатывать хроматограммы, выбирать из них масс-спектры индивидуальных соединений, работать с готовыми базами данных масс-спектров и создавать свои библиотеки масс-спектров соединений.
 Что требуется от слушателей в этой главе 1. Научиться использовать программу обработки массспектральных данных Standalone Review Data. 2. Получать информацию из хромато-масс-спектрограммы: содержание компонент в смеси, масс-спектр компонент в графическом и цифровом виде. 3. Уметь использовать базы данных масс-спектров для обработки результатов хромато-масс-спектрометрии, в том числе при работе с результатами анализа своих собственных образцов, полученных при лабораторных работах по другим курсам. 4. Знакомство с функционалом изучаемой программы обработки позволит впоследствии легко осваивать аналогичные программы, более современные или других производителей.
Что требуется от слушателей в этой главе 1. Научиться использовать программу обработки массспектральных данных Standalone Review Data. 2. Получать информацию из хромато-масс-спектрограммы: содержание компонент в смеси, масс-спектр компонент в графическом и цифровом виде. 3. Уметь использовать базы данных масс-спектров для обработки результатов хромато-масс-спектрометрии, в том числе при работе с результатами анализа своих собственных образцов, полученных при лабораторных работах по другим курсам. 4. Знакомство с функционалом изучаемой программы обработки позволит впоследствии легко осваивать аналогичные программы, более современные или других производителей.
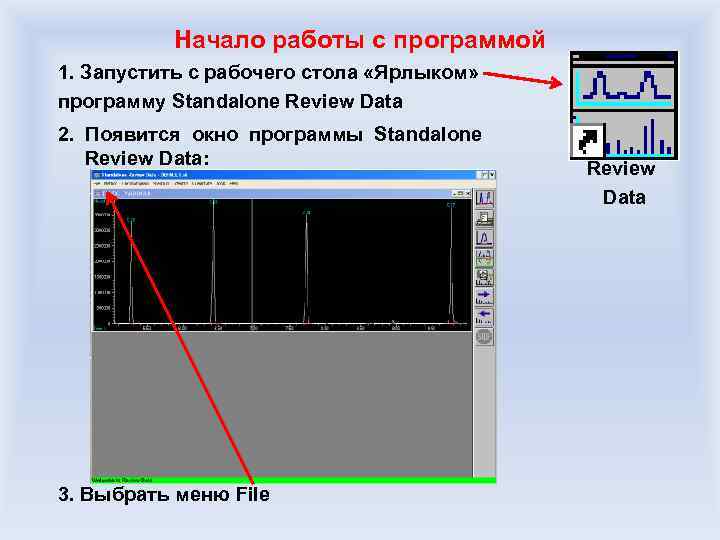 Начало работы с программой 1. Запустить с рабочего стола «Ярлыком» программу Standalone Review Data 2. Появится окно программы Standalone Review Data: 3. Выбрать меню File Review Data
Начало работы с программой 1. Запустить с рабочего стола «Ярлыком» программу Standalone Review Data 2. Появится окно программы Standalone Review Data: 3. Выбрать меню File Review Data
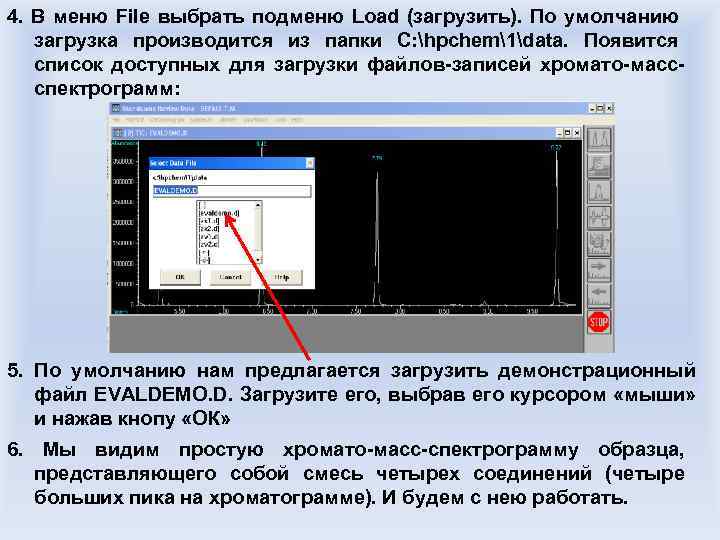 4. В меню File выбрать подменю Load (загрузить). По умолчанию загрузка производится из папки C: hpchem1data. Появится список доступных для загрузки файлов-записей хромато-массспектрограмм: 5. По умолчанию нам предлагается загрузить демонстрационный файл EVALDEMO. D. Загрузите его, выбрав его курсором «мыши» и нажав кнопу «ОК» 6. Мы видим простую хромато-масс-спектрограмму образца, представляющего собой смесь четырех соединений (четыре больших пика на хроматограмме). И будем с нею работать.
4. В меню File выбрать подменю Load (загрузить). По умолчанию загрузка производится из папки C: hpchem1data. Появится список доступных для загрузки файлов-записей хромато-массспектрограмм: 5. По умолчанию нам предлагается загрузить демонстрационный файл EVALDEMO. D. Загрузите его, выбрав его курсором «мыши» и нажав кнопу «ОК» 6. Мы видим простую хромато-масс-спектрограмму образца, представляющего собой смесь четырех соединений (четыре больших пика на хроматограмме). И будем с нею работать.
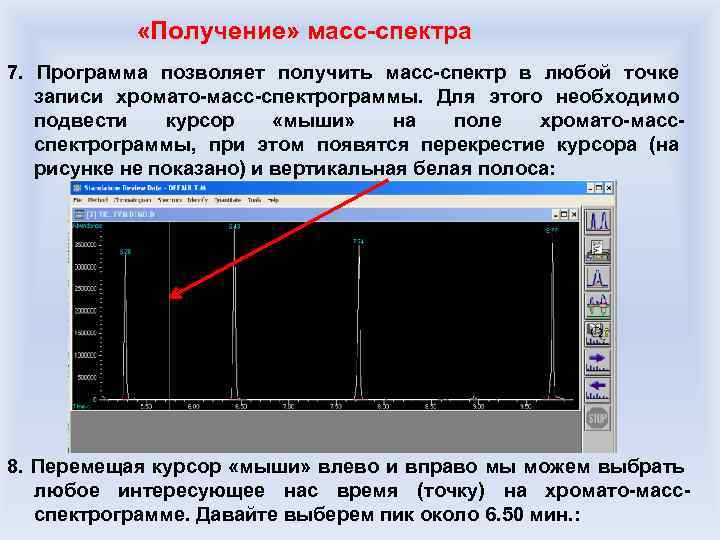 «Получение» масс-спектра 7. Программа позволяет получить масс-спектр в любой точке записи хромато-масс-спектрограммы. Для этого необходимо подвести курсор «мыши» на поле хромато-массспектрограммы, при этом появятся перекрестие курсора (на рисунке не показано) и вертикальная белая полоса: 8. Перемещая курсор «мыши» влево и вправо мы можем выбрать любое интересующее нас время (точку) на хромато-массспектрограмме. Давайте выберем пик около 6. 50 мин. :
«Получение» масс-спектра 7. Программа позволяет получить масс-спектр в любой точке записи хромато-масс-спектрограммы. Для этого необходимо подвести курсор «мыши» на поле хромато-массспектрограммы, при этом появятся перекрестие курсора (на рисунке не показано) и вертикальная белая полоса: 8. Перемещая курсор «мыши» влево и вправо мы можем выбрать любое интересующее нас время (точку) на хромато-массспектрограмме. Давайте выберем пик около 6. 50 мин. :
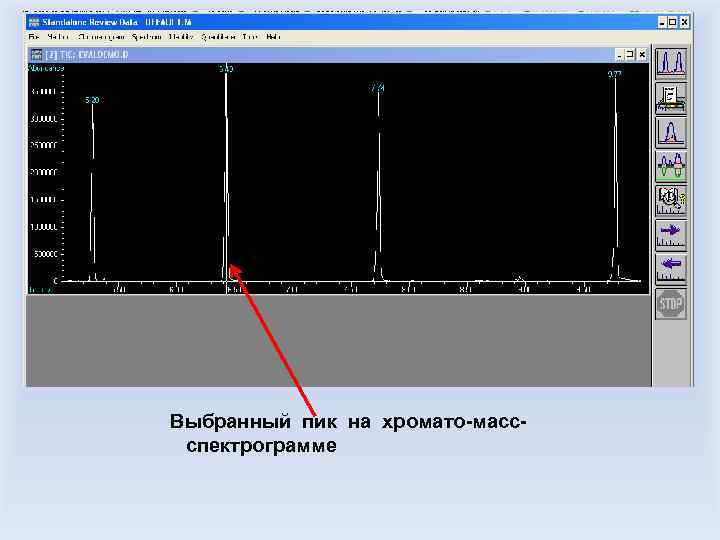 Выбранный пик на хромато-массспектрограмме
Выбранный пик на хромато-массспектрограмме
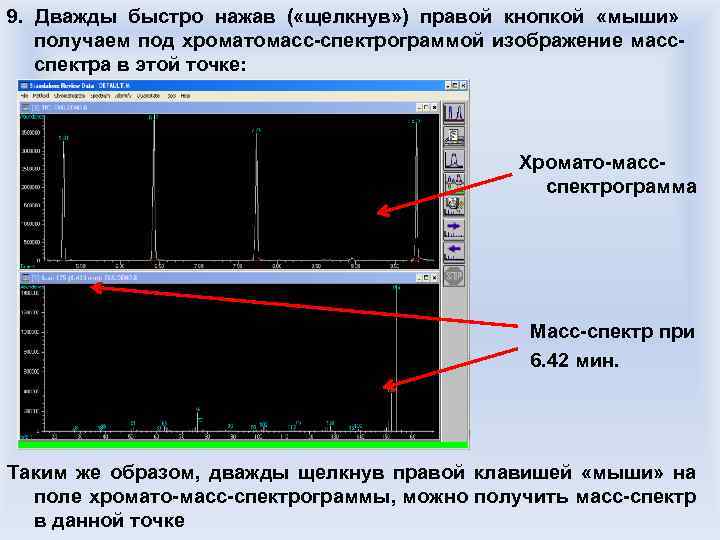 9. Дважды быстро нажав ( «щелкнув» ) правой кнопкой «мыши» получаем под хроматомасс-спектрограммой изображение массспектра в этой точке: Хромато-массспектрограмма Масс-спектр при 6. 42 мин. Таким же образом, дважды щелкнув правой клавишей «мыши» на поле хромато-масс-спектрограммы, можно получить масс-спектр в данной точке
9. Дважды быстро нажав ( «щелкнув» ) правой кнопкой «мыши» получаем под хроматомасс-спектрограммой изображение массспектра в этой точке: Хромато-массспектрограмма Масс-спектр при 6. 42 мин. Таким же образом, дважды щелкнув правой клавишей «мыши» на поле хромато-масс-спектрограммы, можно получить масс-спектр в данной точке
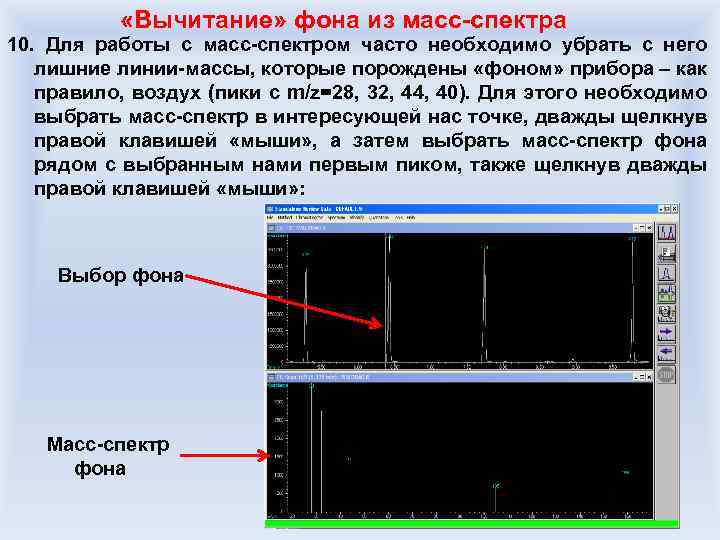 «Вычитание» фона из масс-спектра 10. Для работы с масс-спектром часто необходимо убрать с него лишние линии-массы, которые порождены «фоном» прибора – как правило, воздух (пики с m/z=28, 32, 44, 40). Для этого необходимо выбрать масс-спектр в интересующей нас точке, дважды щелкнув правой клавишей «мыши» , а затем выбрать масс-спектр фона рядом с выбранным нами первым пиком, также щелкнув дважды правой клавишей «мыши» : Выбор фона Масс-спектр фона
«Вычитание» фона из масс-спектра 10. Для работы с масс-спектром часто необходимо убрать с него лишние линии-массы, которые порождены «фоном» прибора – как правило, воздух (пики с m/z=28, 32, 44, 40). Для этого необходимо выбрать масс-спектр в интересующей нас точке, дважды щелкнув правой клавишей «мыши» , а затем выбрать масс-спектр фона рядом с выбранным нами первым пиком, также щелкнув дважды правой клавишей «мыши» : Выбор фона Масс-спектр фона
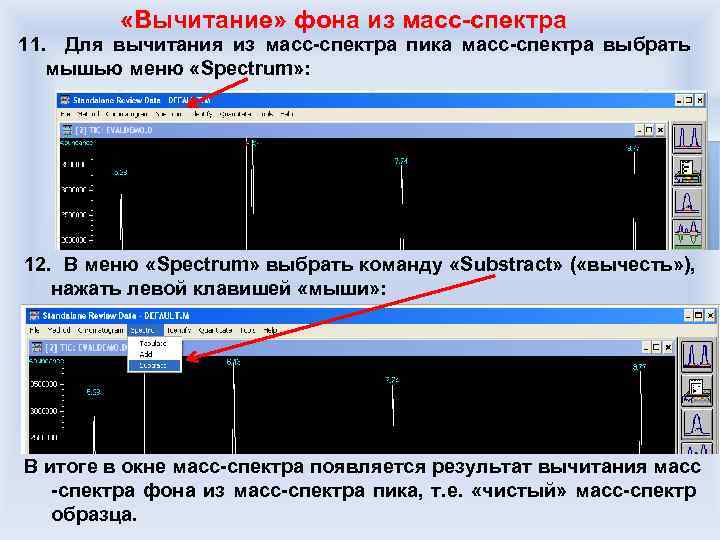 «Вычитание» фона из масс-спектра 11. Для вычитания из масс-спектра пика масс-спектра выбрать мышью меню «Spectrum» : 12. В меню «Spectrum» выбрать команду «Substract» ( «вычесть» ), нажать левой клавишей «мыши» : В итоге в окне масс-спектра появляется результат вычитания масс -спектра фона из масс-спектра пика, т. е. «чистый» масс-спектр образца.
«Вычитание» фона из масс-спектра 11. Для вычитания из масс-спектра пика масс-спектра выбрать мышью меню «Spectrum» : 12. В меню «Spectrum» выбрать команду «Substract» ( «вычесть» ), нажать левой клавишей «мыши» : В итоге в окне масс-спектра появляется результат вычитания масс -спектра фона из масс-спектра пика, т. е. «чистый» масс-спектр образца.
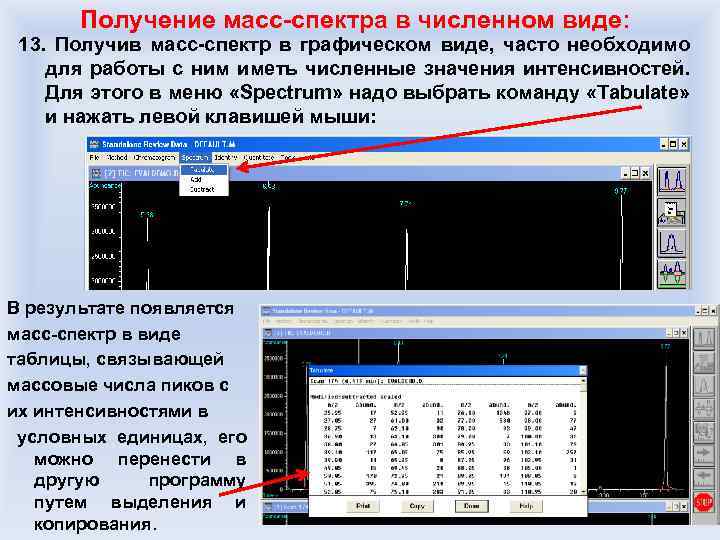 Получение масс-спектра в численном виде: 13. Получив масс-спектр в графическом виде, часто необходимо для работы с ним иметь численные значения интенсивностей. Для этого в меню «Spectrum» надо выбрать команду «Tabulate» и нажать левой клавишей мыши: В результате появляется масс-спектр в виде таблицы, связывающей массовые числа пиков с их интенсивностями в условных единицах, его можно перенести в другую программу путем выделения и копирования.
Получение масс-спектра в численном виде: 13. Получив масс-спектр в графическом виде, часто необходимо для работы с ним иметь численные значения интенсивностей. Для этого в меню «Spectrum» надо выбрать команду «Tabulate» и нажать левой клавишей мыши: В результате появляется масс-спектр в виде таблицы, связывающей массовые числа пиков с их интенсивностями в условных единицах, его можно перенести в другую программу путем выделения и копирования.
 Получение масс-спектра в численном виде: 14. Масс-спектр в численном виде необходим для: А) получения брутто-формулу соединения или его фрагмента по так называемым «изотопным» пикам Б) оформления статей и отчетов – часто требуется не графический, а численный вид масс-спектра, как, например, в работе Илюшин М. А. , Терпигорев А. Н. , Целинский И. В. Влияние изомерного строения (N-нитроамино)тетразолов на свойства их солей // ЖОХ. 1999. Т. 69. Вып. 10. С. 1727 -1730: Масс-спектр (NH 4+)2[5 -NATZ]2 Соль Осколочные ионы, m/z (% полного ионного тока) (NH 4+)2[5 -NATZ]2 - 129(0. 4), 97(0. 7), 83(0. 7), 69(1. 2), 60(1. 2), M=164 г/моль 55(1. 6), 46(6. 5), 44(4. 0), 42(7. 0), 41(2. 6), 36(5. 7), 30(14. 0), 28(34. 1), 18(20. 3)
Получение масс-спектра в численном виде: 14. Масс-спектр в численном виде необходим для: А) получения брутто-формулу соединения или его фрагмента по так называемым «изотопным» пикам Б) оформления статей и отчетов – часто требуется не графический, а численный вид масс-спектра, как, например, в работе Илюшин М. А. , Терпигорев А. Н. , Целинский И. В. Влияние изомерного строения (N-нитроамино)тетразолов на свойства их солей // ЖОХ. 1999. Т. 69. Вып. 10. С. 1727 -1730: Масс-спектр (NH 4+)2[5 -NATZ]2 Соль Осколочные ионы, m/z (% полного ионного тока) (NH 4+)2[5 -NATZ]2 - 129(0. 4), 97(0. 7), 83(0. 7), 69(1. 2), 60(1. 2), M=164 г/моль 55(1. 6), 46(6. 5), 44(4. 0), 42(7. 0), 41(2. 6), 36(5. 7), 30(14. 0), 28(34. 1), 18(20. 3)
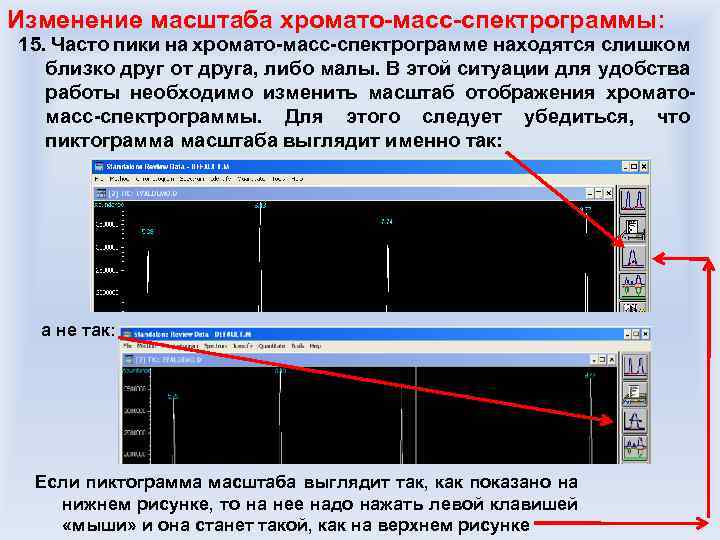 Изменение масштаба хромато-масс-спектрограммы: 15. Часто пики на хромато-масс-спектрограмме находятся слишком близко друг от друга, либо малы. В этой ситуации для удобства работы необходимо изменить масштаб отображения хроматомасс-спектрограммы. Для этого следует убедиться, что пиктограмма масштаба выглядит именно так: а не так: Если пиктограмма масштаба выглядит так, как показано на нижнем рисунке, то на нее надо нажать левой клавишей «мыши» и она станет такой, как на верхнем рисунке
Изменение масштаба хромато-масс-спектрограммы: 15. Часто пики на хромато-масс-спектрограмме находятся слишком близко друг от друга, либо малы. В этой ситуации для удобства работы необходимо изменить масштаб отображения хроматомасс-спектрограммы. Для этого следует убедиться, что пиктограмма масштаба выглядит именно так: а не так: Если пиктограмма масштаба выглядит так, как показано на нижнем рисунке, то на нее надо нажать левой клавишей «мыши» и она станет такой, как на верхнем рисунке
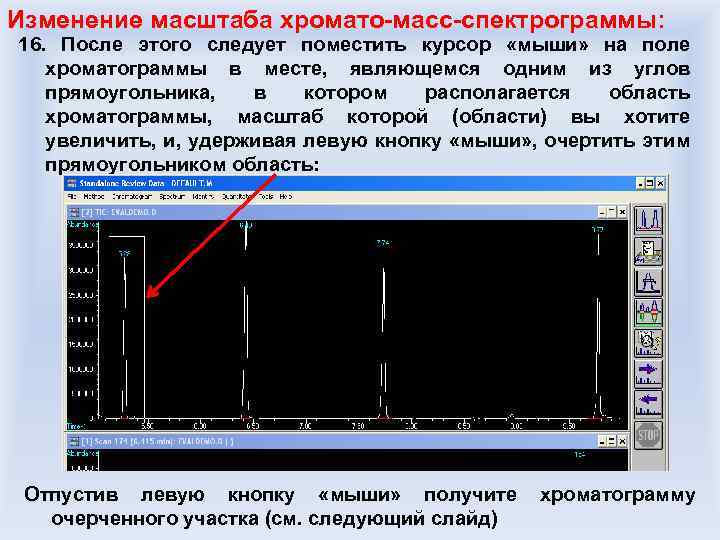 Изменение масштаба хромато-масс-спектрограммы: 16. После этого следует поместить курсор «мыши» на поле хроматограммы в месте, являющемся одним из углов прямоугольника, в котором располагается область хроматограммы, масштаб которой (области) вы хотите увеличить, и, удерживая левую кнопку «мыши» , очертить этим прямоугольником область: Отпустив левую кнопку «мыши» получите хроматограмму очерченного участка (см. следующий слайд)
Изменение масштаба хромато-масс-спектрограммы: 16. После этого следует поместить курсор «мыши» на поле хроматограммы в месте, являющемся одним из углов прямоугольника, в котором располагается область хроматограммы, масштаб которой (области) вы хотите увеличить, и, удерживая левую кнопку «мыши» , очертить этим прямоугольником область: Отпустив левую кнопку «мыши» получите хроматограмму очерченного участка (см. следующий слайд)
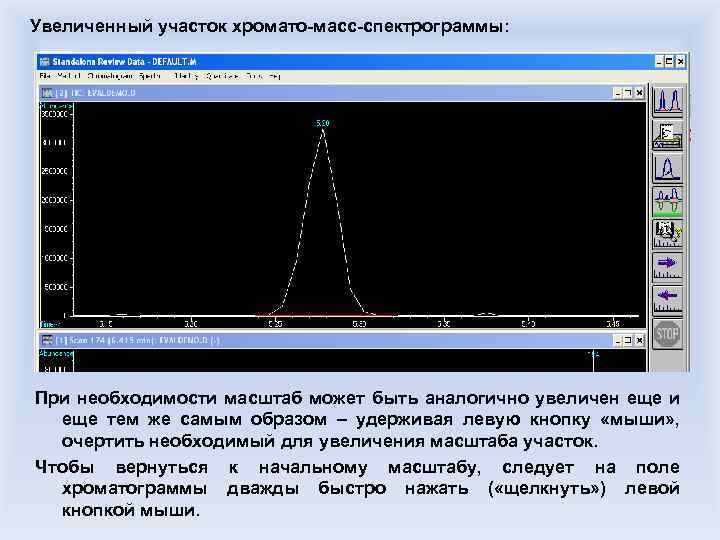 Увеличенный участок хромато-масс-спектрограммы: При необходимости масштаб может быть аналогично увеличен еще и еще тем же самым образом – удерживая левую кнопку «мыши» , очертить необходимый для увеличения масштаба участок. Чтобы вернуться к начальному масштабу, следует на поле хроматограммы дважды быстро нажать ( «щелкнуть» ) левой кнопкой мыши.
Увеличенный участок хромато-масс-спектрограммы: При необходимости масштаб может быть аналогично увеличен еще и еще тем же самым образом – удерживая левую кнопку «мыши» , очертить необходимый для увеличения масштаба участок. Чтобы вернуться к начальному масштабу, следует на поле хроматограммы дважды быстро нажать ( «щелкнуть» ) левой кнопкой мыши.
 Изменение масштаба хромато-масс-спектрограммы: 17. Аналогичным образом можно изменить масштаб самого массспектра, очерчивая прямоугольником необходимый участок на поле масс-спектра. Вернуться к первоначальному масштабу можно аналогично – дважды быстро нажав ( «щелкнув» ) левой кнопкой «мыши» на поле масс-спектра. Использование подключенных спектральных данных баз масс- 18. Масс-спектральные базы данных позволяют производить идентификацию соединений путем сравнения имеющегося в базе масс-спектра с масс-спектром, полученным в ходе эксперимента. Способ сранения примерно аналогичен сличению отпечатков пальцев – программа сравнивает интенсивности массовых линий в экспериментальном массспектре с интенсивностью масс-спектральных линий массспектров, находящихся у нее в картотеке, и выдает наиболее близкие, по ее мнению, результаты.
Изменение масштаба хромато-масс-спектрограммы: 17. Аналогичным образом можно изменить масштаб самого массспектра, очерчивая прямоугольником необходимый участок на поле масс-спектра. Вернуться к первоначальному масштабу можно аналогично – дважды быстро нажав ( «щелкнув» ) левой кнопкой «мыши» на поле масс-спектра. Использование подключенных спектральных данных баз масс- 18. Масс-спектральные базы данных позволяют производить идентификацию соединений путем сравнения имеющегося в базе масс-спектра с масс-спектром, полученным в ходе эксперимента. Способ сранения примерно аналогичен сличению отпечатков пальцев – программа сравнивает интенсивности массовых линий в экспериментальном массспектре с интенсивностью масс-спектральных линий массспектров, находящихся у нее в картотеке, и выдает наиболее близкие, по ее мнению, результаты.
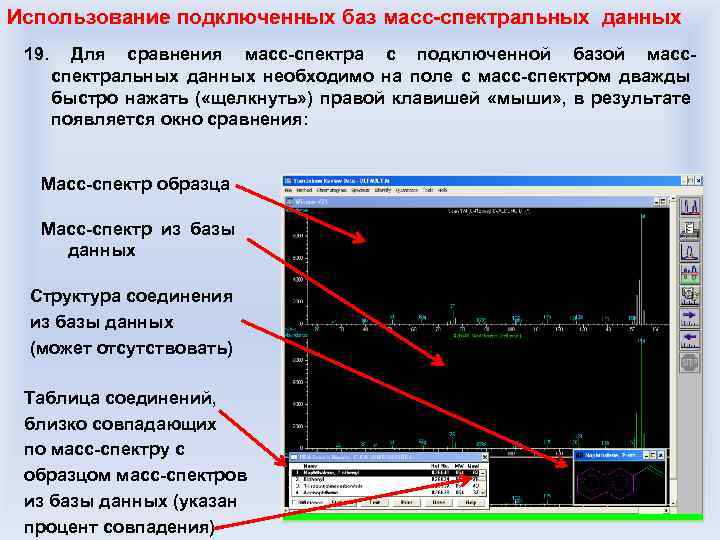 Использование подключенных баз масс-спектральных данных 19. Для сравнения масс-спектра с подключенной базой массспектральных данных необходимо на поле с масс-спектром дважды быстро нажать ( «щелкнуть» ) правой клавишей «мыши» , в результате появляется окно сравнения: Масс-спектр образца Масс-спектр из базы данных Структура соединения из базы данных (может отсутствовать) Таблица соединений, близко совпадающих по масс-спектру с образцом масс-спектров из базы данных (указан процент совпадения)
Использование подключенных баз масс-спектральных данных 19. Для сравнения масс-спектра с подключенной базой массспектральных данных необходимо на поле с масс-спектром дважды быстро нажать ( «щелкнуть» ) правой клавишей «мыши» , в результате появляется окно сравнения: Масс-спектр образца Масс-спектр из базы данных Структура соединения из базы данных (может отсутствовать) Таблица соединений, близко совпадающих по масс-спектру с образцом масс-спектров из базы данных (указан процент совпадения)
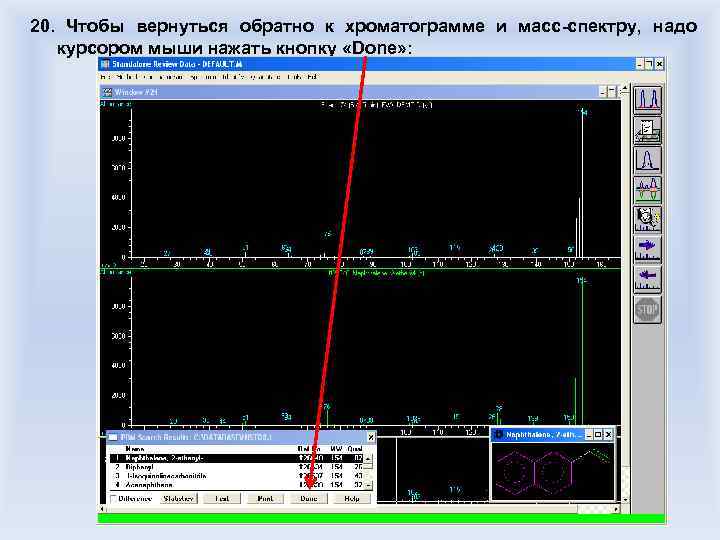 20. Чтобы вернуться обратно к хроматограмме и масс-спектру, надо курсором мыши нажать кнопку «Done» :
20. Чтобы вернуться обратно к хроматограмме и масс-спектру, надо курсором мыши нажать кнопку «Done» :
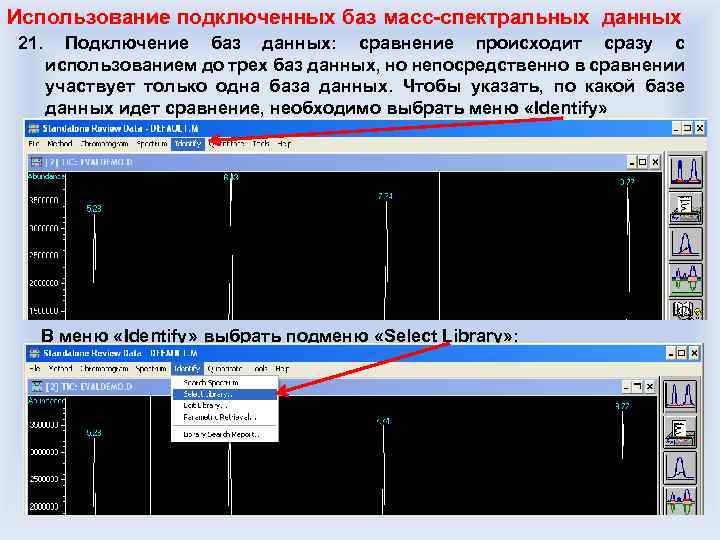 Использование подключенных баз масс-спектральных данных 21. Подключение баз данных: сравнение происходит сразу с использованием до трех баз данных, но непосредственно в сравнении участвует только одна база данных. Чтобы указать, по какой базе данных идет сравнение, необходимо выбрать меню «Identify» В меню «Identify» выбрать подменю «Select Library» :
Использование подключенных баз масс-спектральных данных 21. Подключение баз данных: сравнение происходит сразу с использованием до трех баз данных, но непосредственно в сравнении участвует только одна база данных. Чтобы указать, по какой базе данных идет сравнение, необходимо выбрать меню «Identify» В меню «Identify» выбрать подменю «Select Library» :
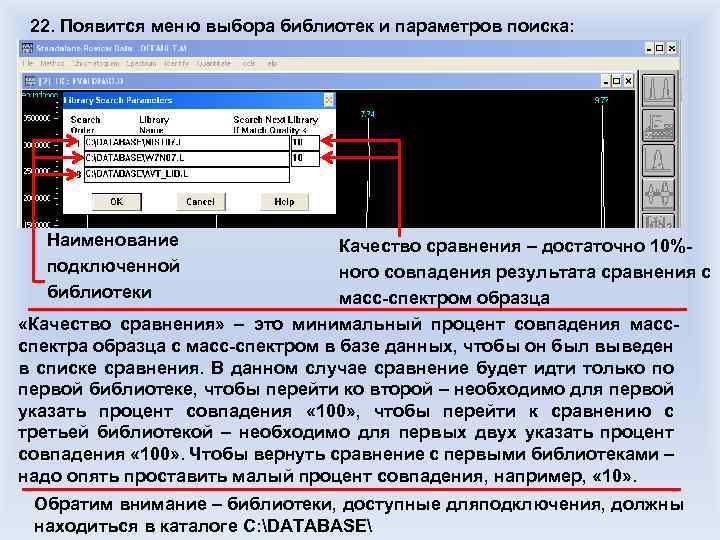 22. Появится меню выбора библиотек и параметров поиска: Наименование подключенной библиотеки Качество сравнения – достаточно 10%ного совпадения результата сравнения с масс-спектром образца «Качество сравнения» – это минимальный процент совпадения массспектра образца с масс-спектром в базе данных, чтобы он был выведен в списке сравнения. В данном случае сравнение будет идти только по первой библиотеке, чтобы перейти ко второй – необходимо для первой указать процент совпадения « 100» , чтобы перейти к сравнению с третьей библиотекой – необходимо для первых двух указать процент совпадения « 100» . Чтобы вернуть сравнение с первыми библиотеками – надо опять проставить малый процент совпадения, например, « 10» . Обратим внимание – библиотеки, доступные дляподключения, должны находиться в каталоге C: DATABASE
22. Появится меню выбора библиотек и параметров поиска: Наименование подключенной библиотеки Качество сравнения – достаточно 10%ного совпадения результата сравнения с масс-спектром образца «Качество сравнения» – это минимальный процент совпадения массспектра образца с масс-спектром в базе данных, чтобы он был выведен в списке сравнения. В данном случае сравнение будет идти только по первой библиотеке, чтобы перейти ко второй – необходимо для первой указать процент совпадения « 100» , чтобы перейти к сравнению с третьей библиотекой – необходимо для первых двух указать процент совпадения « 100» . Чтобы вернуть сравнение с первыми библиотеками – надо опять проставить малый процент совпадения, например, « 10» . Обратим внимание – библиотеки, доступные дляподключения, должны находиться в каталоге C: DATABASE
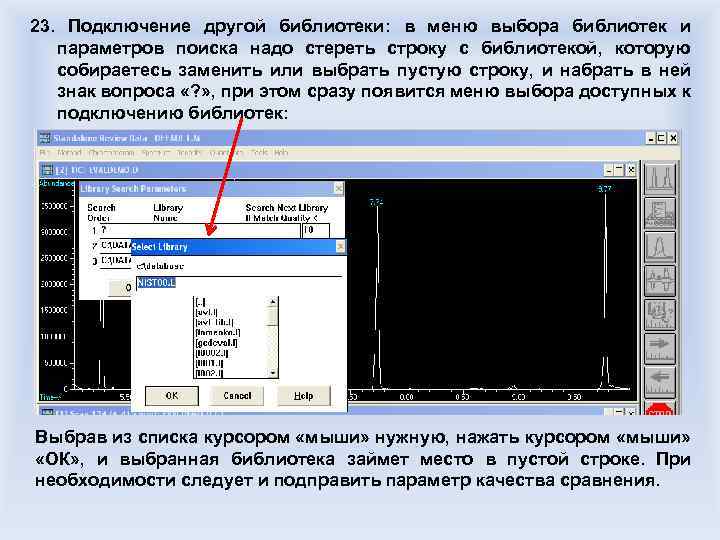 23. Подключение другой библиотеки: в меню выбора библиотек и параметров поиска надо стереть строку с библиотекой, которую собираетесь заменить или выбрать пустую строку, и набрать в ней знак вопроса «? » , при этом сразу появится меню выбора доступных к подключению библиотек: Выбрав из списка курсором «мыши» нужную, нажать курсором «мыши» «ОК» , и выбранная библиотека займет место в пустой строке. При необходимости следует и подправить параметр качества сравнения.
23. Подключение другой библиотеки: в меню выбора библиотек и параметров поиска надо стереть строку с библиотекой, которую собираетесь заменить или выбрать пустую строку, и набрать в ней знак вопроса «? » , при этом сразу появится меню выбора доступных к подключению библиотек: Выбрав из списка курсором «мыши» нужную, нажать курсором «мыши» «ОК» , и выбранная библиотека займет место в пустой строке. При необходимости следует и подправить параметр качества сравнения.
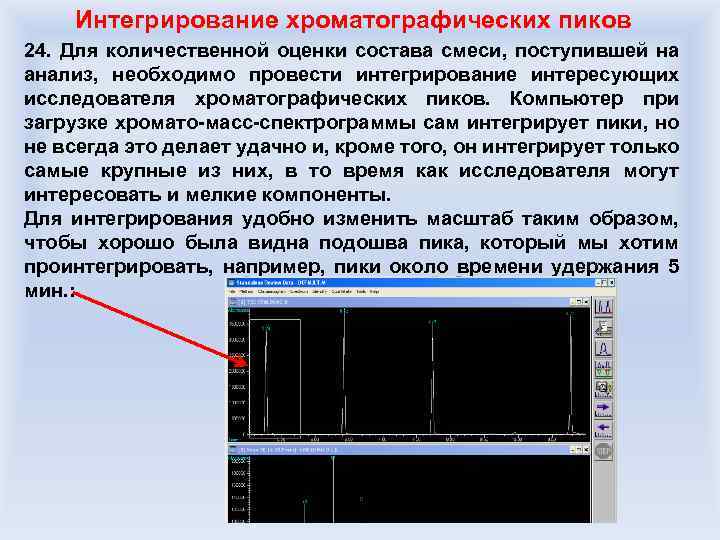 Интегрирование хроматографических пиков 24. Для количественной оценки состава смеси, поступившей на анализ, необходимо провести интегрирование интересующих исследователя хроматографических пиков. Компьютер при загрузке хромато-масс-спектрограммы сам интегрирует пики, но не всегда это делает удачно и, кроме того, он интегрирует только самые крупные из них, в то время как исследователя могут интересовать и мелкие компоненты. Для интегрирования удобно изменить масштаб таким образом, чтобы хорошо была видна подошва пика, который мы хотим проинтегрировать, например, пики около времени удержания 5 мин. :
Интегрирование хроматографических пиков 24. Для количественной оценки состава смеси, поступившей на анализ, необходимо провести интегрирование интересующих исследователя хроматографических пиков. Компьютер при загрузке хромато-масс-спектрограммы сам интегрирует пики, но не всегда это делает удачно и, кроме того, он интегрирует только самые крупные из них, в то время как исследователя могут интересовать и мелкие компоненты. Для интегрирования удобно изменить масштаб таким образом, чтобы хорошо была видна подошва пика, который мы хотим проинтегрировать, например, пики около времени удержания 5 мин. :
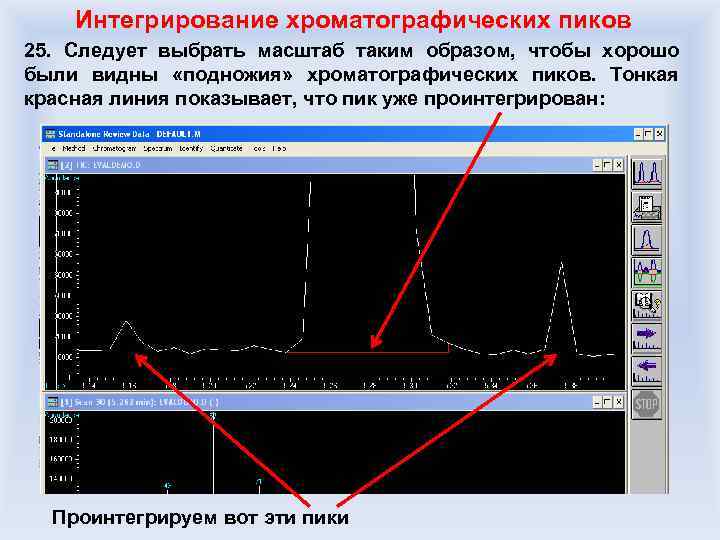 Интегрирование хроматографических пиков 25. Следует выбрать масштаб таким образом, чтобы хорошо были видны «подножия» хроматографических пиков. Тонкая красная линия показывает, что пик уже проинтегрирован: Проинтегрируем вот эти пики
Интегрирование хроматографических пиков 25. Следует выбрать масштаб таким образом, чтобы хорошо были видны «подножия» хроматографических пиков. Тонкая красная линия показывает, что пик уже проинтегрирован: Проинтегрируем вот эти пики
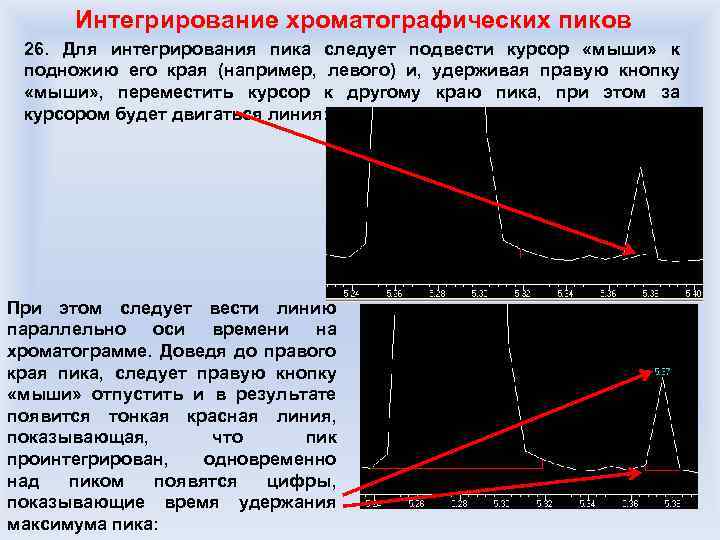 Интегрирование хроматографических пиков 26. Для интегрирования пика следует подвести курсор «мыши» к подножию его края (например, левого) и, удерживая правую кнопку «мыши» , переместить курсор к другому краю пика, при этом за курсором будет двигаться линия: При этом следует вести линию параллельно оси времени на хроматограмме. Доведя до правого края пика, следует правую кнопку «мыши» отпустить и в результате появится тонкая красная линия, показывающая, что пик проинтегрирован, одновременно над пиком появятся цифры, показывающие время удержания максимума пика:
Интегрирование хроматографических пиков 26. Для интегрирования пика следует подвести курсор «мыши» к подножию его края (например, левого) и, удерживая правую кнопку «мыши» , переместить курсор к другому краю пика, при этом за курсором будет двигаться линия: При этом следует вести линию параллельно оси времени на хроматограмме. Доведя до правого края пика, следует правую кнопку «мыши» отпустить и в результате появится тонкая красная линия, показывающая, что пик проинтегрирован, одновременно над пиком появятся цифры, показывающие время удержания максимума пика:
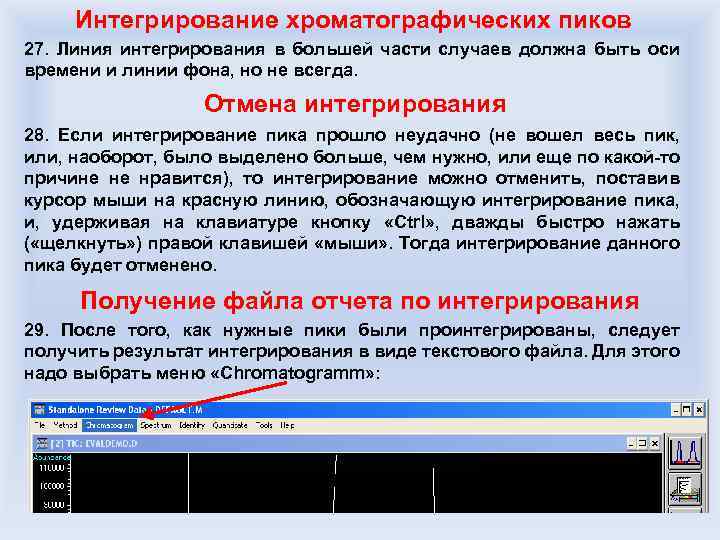 Интегрирование хроматографических пиков 27. Линия интегрирования в большей части случаев должна быть оси времени и линии фона, но не всегда. Отмена интегрирования 28. Если интегрирование пика прошло неудачно (не вошел весь пик, или, наоборот, было выделено больше, чем нужно, или еще по какой-то причине не нравится), то интегрирование можно отменить, поставив курсор мыши на красную линию, обозначающую интегрирование пика, и, удерживая на клавиатуре кнопку «Ctrl» , дважды быстро нажать ( «щелкнуть» ) правой клавишей «мыши» . Тогда интегрирование данного пика будет отменено. Получение файла отчета по интегрирования 29. После того, как нужные пики были проинтегрированы, следует получить результат интегрирования в виде текстового файла. Для этого надо выбрать меню «Chromatogramm» :
Интегрирование хроматографических пиков 27. Линия интегрирования в большей части случаев должна быть оси времени и линии фона, но не всегда. Отмена интегрирования 28. Если интегрирование пика прошло неудачно (не вошел весь пик, или, наоборот, было выделено больше, чем нужно, или еще по какой-то причине не нравится), то интегрирование можно отменить, поставив курсор мыши на красную линию, обозначающую интегрирование пика, и, удерживая на клавиатуре кнопку «Ctrl» , дважды быстро нажать ( «щелкнуть» ) правой клавишей «мыши» . Тогда интегрирование данного пика будет отменено. Получение файла отчета по интегрирования 29. После того, как нужные пики были проинтегрированы, следует получить результат интегрирования в виде текстового файла. Для этого надо выбрать меню «Chromatogramm» :
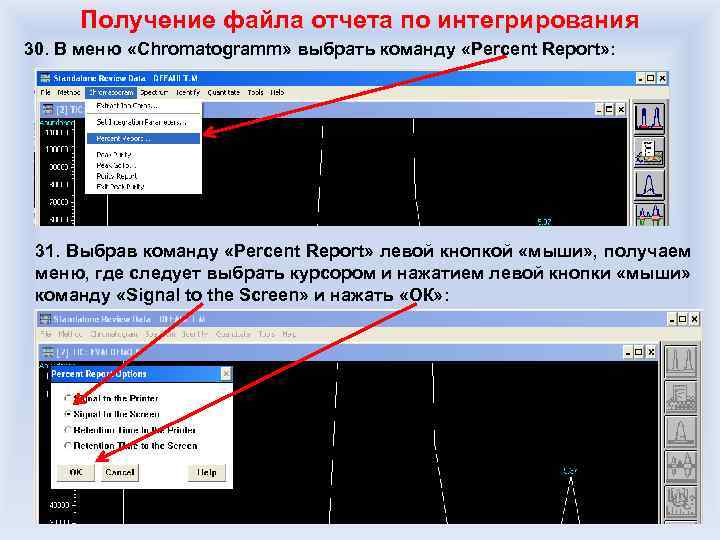 Получение файла отчета по интегрирования 30. В меню «Chromatogramm» выбрать команду «Percent Report» : 31. Выбрав команду «Percent Report» левой кнопкой «мыши» , получаем меню, где следует выбрать курсором и нажатием левой кнопки «мыши» команду «Signal to the Screen» и нажать «ОК» :
Получение файла отчета по интегрирования 30. В меню «Chromatogramm» выбрать команду «Percent Report» : 31. Выбрав команду «Percent Report» левой кнопкой «мыши» , получаем меню, где следует выбрать курсором и нажатием левой кнопки «мыши» команду «Signal to the Screen» и нажать «ОК» :
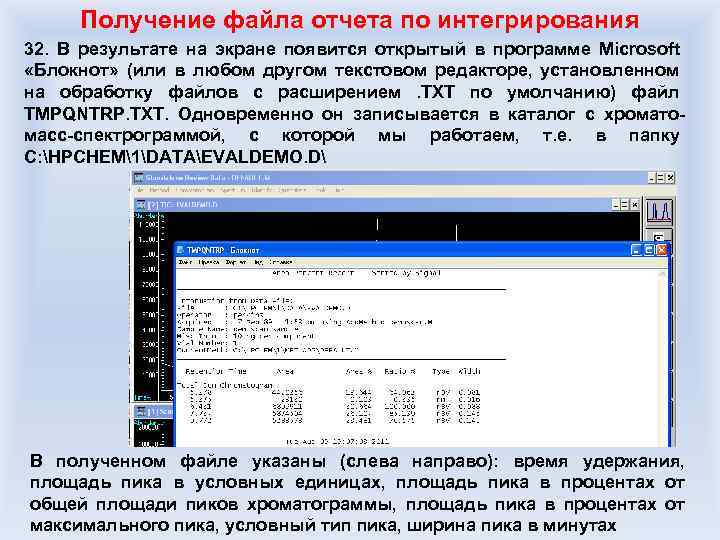 Получение файла отчета по интегрирования 32. В результате на экране появится открытый в программе Microsoft «Блокнот» (или в любом другом текстовом редакторе, установленном на обработку файлов с расширением . TXT по умолчанию) файл TMPQNTRP. TXT. Одновременно он записывается в каталог с хроматомасс-спектрограммой, с которой мы работаем, т. е. в папку C: HPCHEM1DATAEVALDEMO. D В полученном файле указаны (слева направо): время удержания, площадь пика в условных единицах, площадь пика в процентах от общей площади пиков хроматограммы, площадь пика в процентах от максимального пика, условный тип пика, ширина пика в минутах
Получение файла отчета по интегрирования 32. В результате на экране появится открытый в программе Microsoft «Блокнот» (или в любом другом текстовом редакторе, установленном на обработку файлов с расширением . TXT по умолчанию) файл TMPQNTRP. TXT. Одновременно он записывается в каталог с хроматомасс-спектрограммой, с которой мы работаем, т. е. в папку C: HPCHEM1DATAEVALDEMO. D В полученном файле указаны (слева направо): время удержания, площадь пика в условных единицах, площадь пика в процентах от общей площади пиков хроматограммы, площадь пика в процентах от максимального пика, условный тип пика, ширина пика в минутах
 Программа Enter_Spec 33. Для более удобного отображения наиболее важных параметров хроматографических пиков, подвергшихся интегрированию, а именно – времени удержания, площади пика в условных единицах, площади пика в процентах от полной площади всех интегрированных пиков, удобно использовать программу Enter_Spec. Ее следует запустить с рабочего стола при помощи ярлыка Enter_Spec После запуска на рабочем столе Windows появится окно программы, в нем надо будет выбрать меню «Задание» и в нем – «Ввод док. 2» Окно программы Enter_Spec
Программа Enter_Spec 33. Для более удобного отображения наиболее важных параметров хроматографических пиков, подвергшихся интегрированию, а именно – времени удержания, площади пика в условных единицах, площади пика в процентах от полной площади всех интегрированных пиков, удобно использовать программу Enter_Spec. Ее следует запустить с рабочего стола при помощи ярлыка Enter_Spec После запуска на рабочем столе Windows появится окно программы, в нем надо будет выбрать меню «Задание» и в нем – «Ввод док. 2» Окно программы Enter_Spec
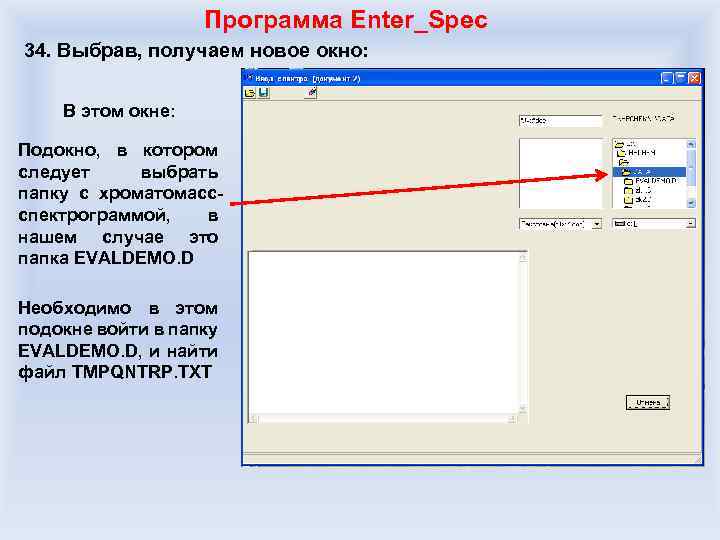 Программа Enter_Spec 34. Выбрав, получаем новое окно: В этом окне: Подокно, в котором следует выбрать папку с хроматомассспектрограммой, в нашем случае это папка EVALDEMO. D Необходимо в этом подокне войти в папку EVALDEMO. D, и найти файл TMPQNTRP. TXT
Программа Enter_Spec 34. Выбрав, получаем новое окно: В этом окне: Подокно, в котором следует выбрать папку с хроматомассспектрограммой, в нашем случае это папка EVALDEMO. D Необходимо в этом подокне войти в папку EVALDEMO. D, и найти файл TMPQNTRP. TXT
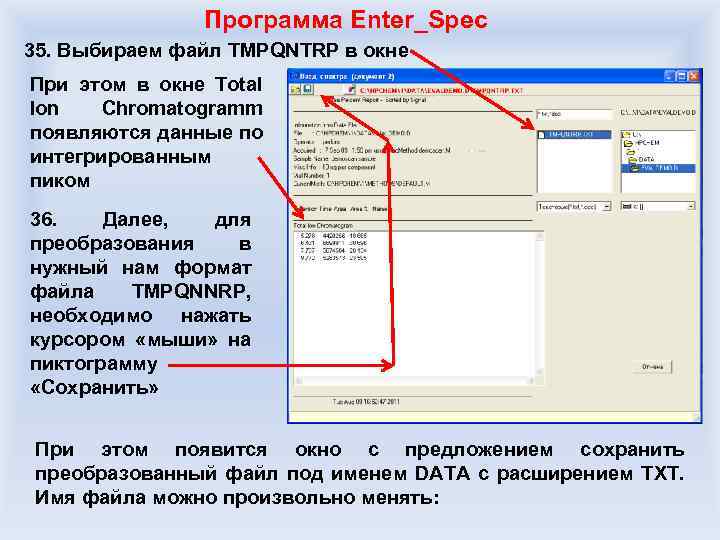 Программа Enter_Spec 35. Выбираем файл TMPQNTRP в окне При этом в окне Total Ion Chromatogramm появляются данные по интегрированным пиком 36. Далее, для преобразования в нужный нам формат файла TMPQNNRP, необходимо нажать курсором «мыши» на пиктограмму «Сохранить» При этом появится окно с предложением сохранить преобразованный файл под именем DATA с расширением TXT. Имя файла можно произвольно менять:
Программа Enter_Spec 35. Выбираем файл TMPQNTRP в окне При этом в окне Total Ion Chromatogramm появляются данные по интегрированным пиком 36. Далее, для преобразования в нужный нам формат файла TMPQNNRP, необходимо нажать курсором «мыши» на пиктограмму «Сохранить» При этом появится окно с предложением сохранить преобразованный файл под именем DATA с расширением TXT. Имя файла можно произвольно менять:
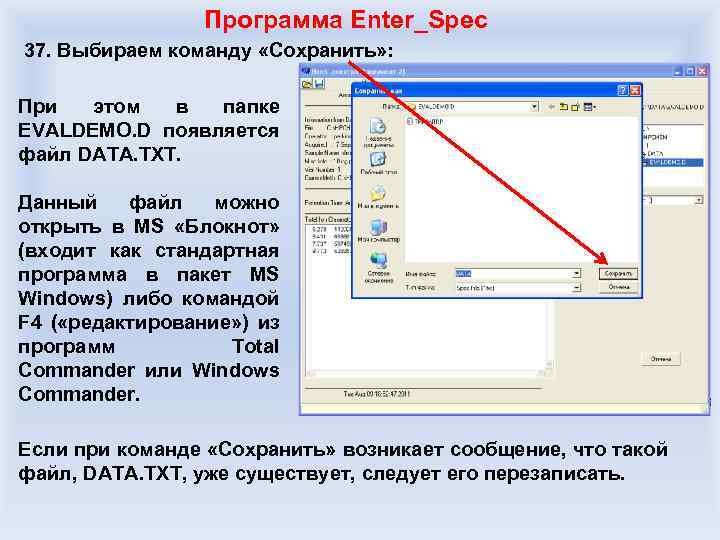 Программа Enter_Spec 37. Выбираем команду «Сохранить» : При этом в папке EVALDEMO. D появляется файл DATA. TXT. Данный файл можно открыть в MS «Блокнот» (входит как стандартная программа в пакет MS Windows) либо командой F 4 ( «редактирование» ) из программ Total Commander или Windows Commander. Если при команде «Сохранить» возникает сообщение, что такой файл, DATA. TXT, уже существует, следует его перезаписать.
Программа Enter_Spec 37. Выбираем команду «Сохранить» : При этом в папке EVALDEMO. D появляется файл DATA. TXT. Данный файл можно открыть в MS «Блокнот» (входит как стандартная программа в пакет MS Windows) либо командой F 4 ( «редактирование» ) из программ Total Commander или Windows Commander. Если при команде «Сохранить» возникает сообщение, что такой файл, DATA. TXT, уже существует, следует его перезаписать.
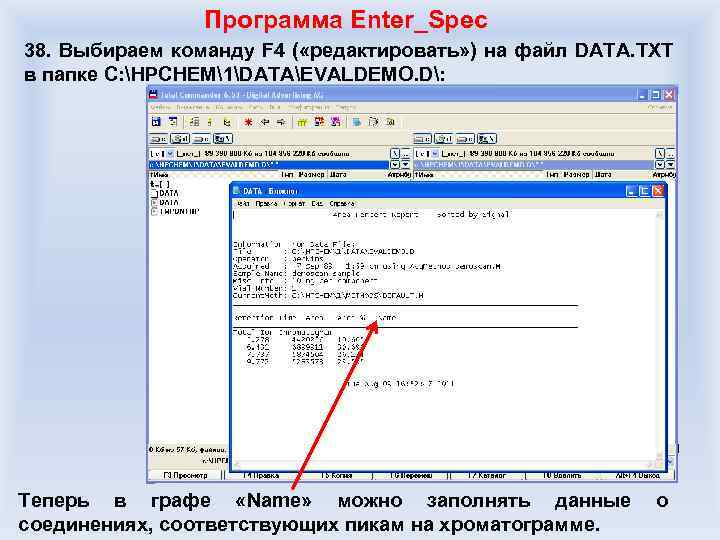 Программа Enter_Spec 38. Выбираем команду F 4 ( «редактировать» ) на файл DATA. TXT в папке C: HPCHEM1DATAEVALDEMO. D: Теперь в графе «Name» можно заполнять данные о соединениях, соответствующих пикам на хроматограмме.
Программа Enter_Spec 38. Выбираем команду F 4 ( «редактировать» ) на файл DATA. TXT в папке C: HPCHEM1DATAEVALDEMO. D: Теперь в графе «Name» можно заполнять данные о соединениях, соответствующих пикам на хроматограмме.
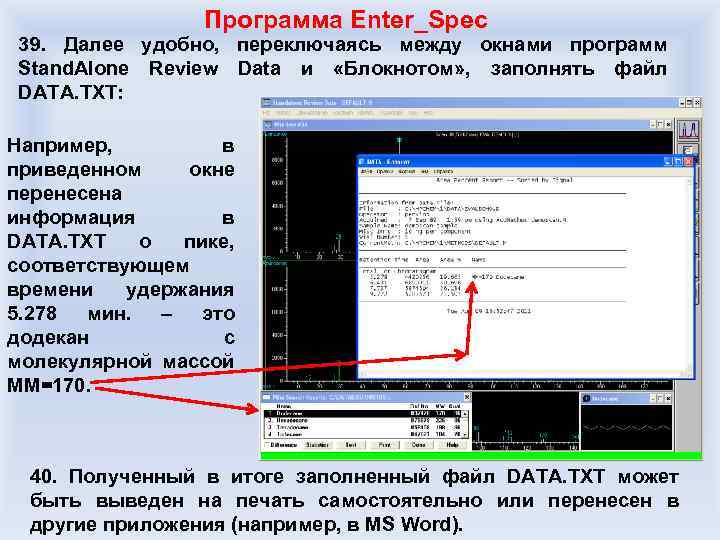 Программа Enter_Spec 39. Далее удобно, переключаясь между окнами программ Stand. Alone Review Data и «Блокнотом» , заполнять файл DATA. TXT: Например, в приведенном окне перенесена информация в DATA. TXT о пике, соответствующем времени удержания 5. 278 мин. – это додекан с молекулярной массой ММ=170. 40. Полученный в итоге заполненный файл DATA. TXT может быть выведен на печать самостоятельно или перенесен в другие приложения (например, в MS Word).
Программа Enter_Spec 39. Далее удобно, переключаясь между окнами программ Stand. Alone Review Data и «Блокнотом» , заполнять файл DATA. TXT: Например, в приведенном окне перенесена информация в DATA. TXT о пике, соответствующем времени удержания 5. 278 мин. – это додекан с молекулярной массой ММ=170. 40. Полученный в итоге заполненный файл DATA. TXT может быть выведен на печать самостоятельно или перенесен в другие приложения (например, в MS Word).
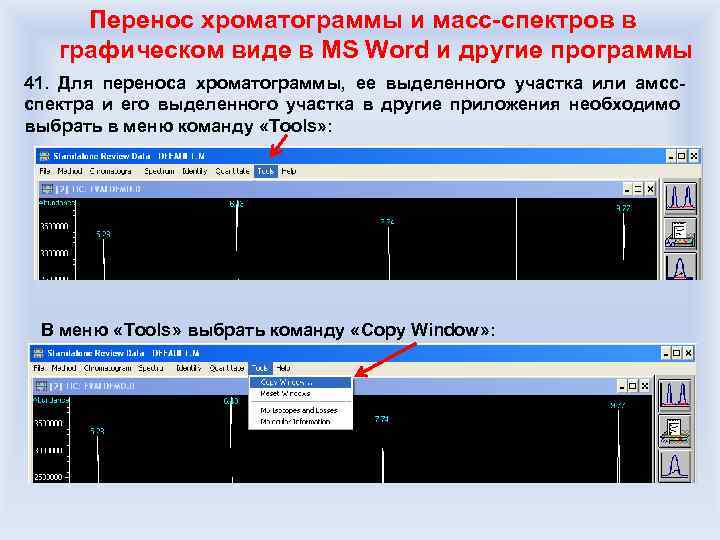 Перенос хроматограммы и масс-спектров в графическом виде в MS Word и другие программы 41. Для переноса хроматограммы, ее выделенного участка или амссспектра и его выделенного участка в другие приложения необходимо выбрать в меню команду «Tools» : В меню «Tools» выбрать команду «Copy Window» :
Перенос хроматограммы и масс-спектров в графическом виде в MS Word и другие программы 41. Для переноса хроматограммы, ее выделенного участка или амссспектра и его выделенного участка в другие приложения необходимо выбрать в меню команду «Tools» : В меню «Tools» выбрать команду «Copy Window» :
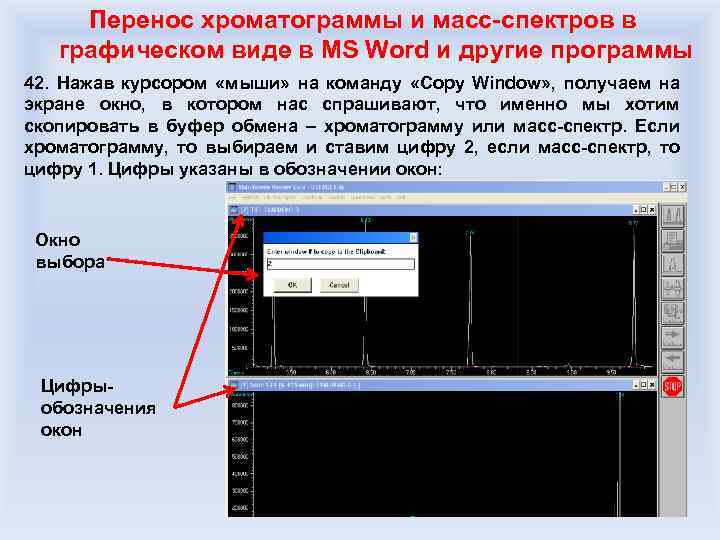 Перенос хроматограммы и масс-спектров в графическом виде в MS Word и другие программы 42. Нажав курсором «мыши» на команду «Copy Window» , получаем на экране окно, в котором нас спрашивают, что именно мы хотим скопировать в буфер обмена – хроматограмму или масс-спектр. Если хроматограмму, то выбираем и ставим цифру 2, если масс-спектр, то цифру 1. Цифры указаны в обозначении окон: Окно выбора Цифрыобозначения окон
Перенос хроматограммы и масс-спектров в графическом виде в MS Word и другие программы 42. Нажав курсором «мыши» на команду «Copy Window» , получаем на экране окно, в котором нас спрашивают, что именно мы хотим скопировать в буфер обмена – хроматограмму или масс-спектр. Если хроматограмму, то выбираем и ставим цифру 2, если масс-спектр, то цифру 1. Цифры указаны в обозначении окон: Окно выбора Цифрыобозначения окон
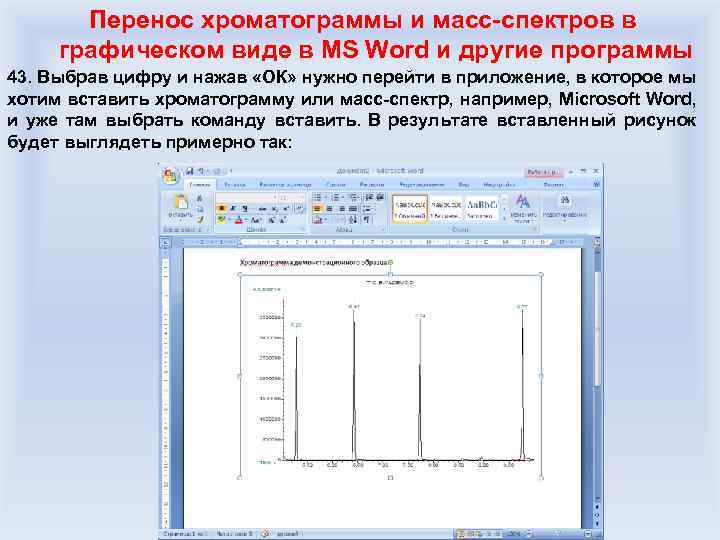 Перенос хроматограммы и масс-спектров в графическом виде в MS Word и другие программы 43. Выбрав цифру и нажав «ОК» нужно перейти в приложение, в которое мы хотим вставить хроматограмму или масс-спектр, например, Microsoft Word, и уже там выбрать команду вставить. В результате вставленный рисунок будет выглядеть примерно так:
Перенос хроматограммы и масс-спектров в графическом виде в MS Word и другие программы 43. Выбрав цифру и нажав «ОК» нужно перейти в приложение, в которое мы хотим вставить хроматограмму или масс-спектр, например, Microsoft Word, и уже там выбрать команду вставить. В результате вставленный рисунок будет выглядеть примерно так:
 Перенос хроматограммы и масс-спектров в графическом виде в MS Word и другие программы 44. Рисунок, перенесенный из программы «Stand. Alone Review Data» , можно уже в MS Word «растянуть/сузить» для корректного отображения надписей и цифр, также, как это делается с обычным рисунком. Программа Stand Alone Review Data доступна для установки на любой компьютер НИОХ СО РАН под управлением операционных систем Windows 95, 98, 2000, NT 4, XP
Перенос хроматограммы и масс-спектров в графическом виде в MS Word и другие программы 44. Рисунок, перенесенный из программы «Stand. Alone Review Data» , можно уже в MS Word «растянуть/сузить» для корректного отображения надписей и цифр, также, как это делается с обычным рисунком. Программа Stand Alone Review Data доступна для установки на любой компьютер НИОХ СО РАН под управлением операционных систем Windows 95, 98, 2000, NT 4, XP


