Масс-спектрометрия.pptx
- Количество слайдов: 50
 Масс-спектрометрия
Масс-спектрометрия
 2 Масс-спектрометрия метод основан на ионизации атомов и молекул вещества и последующем разделении образующихся ионов в соответствии с их массовым числом m/z - отношением массы иона к его заряду - в электрическом или магнитном поле.
2 Масс-спектрометрия метод основан на ионизации атомов и молекул вещества и последующем разделении образующихся ионов в соответствии с их массовым числом m/z - отношением массы иона к его заряду - в электрическом или магнитном поле.
 3 МС позволяет определить: 1. Молекулярную массу вещества. 2. Молекулярную формулу вещества. 3. Строение вещества.
3 МС позволяет определить: 1. Молекулярную массу вещества. 2. Молекулярную формулу вещества. 3. Строение вещества.
 4 Масс-спектр уксусной кислоты 100 H 3 C C O 43 I, % O H 3 C C OH 60 C O CH 3 15 50 28 m/z 10 20 30 40 50 60 1. Молекулярная масса – 60. 2. Молекулярная формула – С 2 Н 4 О 2. 3. Строение вещества – СН 3 СООН.
4 Масс-спектр уксусной кислоты 100 H 3 C C O 43 I, % O H 3 C C OH 60 C O CH 3 15 50 28 m/z 10 20 30 40 50 60 1. Молекулярная масса – 60. 2. Молекулярная формула – С 2 Н 4 О 2. 3. Строение вещества – СН 3 СООН.
 5 Масс-спектр уксусной кислоты Основной ион Фрагментные ионы 100 H 3 C C O 43 I, % O H 3 C C OH 60 C O CH 3 15 50 Молекулярный ион 28 m/z 10 20 30 40 50 60
5 Масс-спектр уксусной кислоты Основной ион Фрагментные ионы 100 H 3 C C O 43 I, % O H 3 C C OH 60 C O CH 3 15 50 Молекулярный ион 28 m/z 10 20 30 40 50 60
 6 Типы ионов в масс-спектрах 1. Молекулярный ион – молекула с положительным зарядом (катион-радикал), полученным за счёт отрыва одного электрона от нейтральной молекулы. 2. Основной ион – ион, интенсивность которого в масс-спектре максимальна. 3. Фрагментный ион – ион, образующийся при распаде молекулярного иона с разрывом связей и миграцией атомов.
6 Типы ионов в масс-спектрах 1. Молекулярный ион – молекула с положительным зарядом (катион-радикал), полученным за счёт отрыва одного электрона от нейтральной молекулы. 2. Основной ион – ион, интенсивность которого в масс-спектре максимальна. 3. Фрагментный ион – ион, образующийся при распаде молекулярного иона с разрывом связей и миграцией атомов.
 7 Масс-спектрометрия – совокупность трёх отдельных процессов: 1. Ионизация молекулы. 2. Разделение ионов по массам. 3. Детектирование ионов.
7 Масс-спектрометрия – совокупность трёх отдельных процессов: 1. Ионизация молекулы. 2. Разделение ионов по массам. 3. Детектирование ионов.
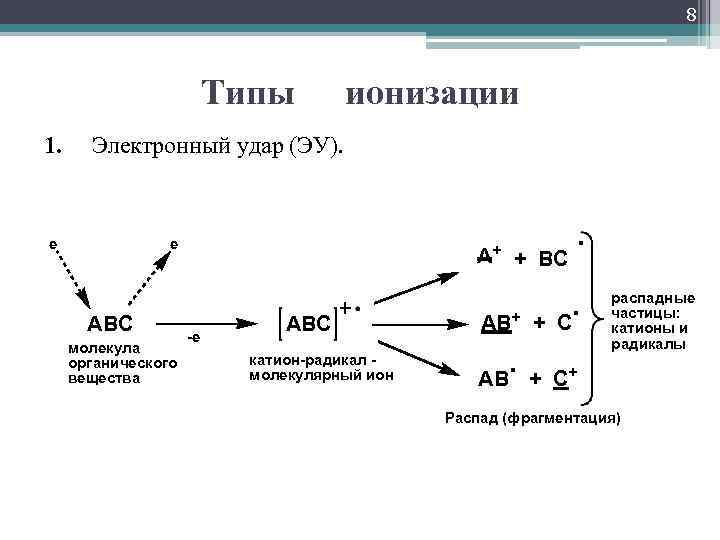 8 Типы 1. ионизации Электронный удар (ЭУ). e e ABC молекула органического вещества A+ -e ABC катион-радикал молекулярный ион . + BC . AB+ + C . распадные частицы: катионы и радикалы AB + C+ Распад (фрагментация)
8 Типы 1. ионизации Электронный удар (ЭУ). e e ABC молекула органического вещества A+ -e ABC катион-радикал молекулярный ион . + BC . AB+ + C . распадные частицы: катионы и радикалы AB + C+ Распад (фрагментация)
 9 Достоинства метода • дает богатые фрагментами масс-спектры, которые однозначно характеризуют структуру молекулы • высокочувствительный метод анализа, позволяет анализировать пикомольные количества вещества (моль 10− 12) • Существуют "библиотеки" масс-спектров, содержащие спектры более 70000 органических соединений, по которым можно проводить их идентификацию с применением ЭВМ
9 Достоинства метода • дает богатые фрагментами масс-спектры, которые однозначно характеризуют структуру молекулы • высокочувствительный метод анализа, позволяет анализировать пикомольные количества вещества (моль 10− 12) • Существуют "библиотеки" масс-спектров, содержащие спектры более 70000 органических соединений, по которым можно проводить их идентификацию с применением ЭВМ
 10 Недостатки метода: • Молекулярные ионы образуются лишь у 20% органических соединений • Определение легколетучих термически стабильных соединений; • Ионы с большими значениями m/z, дающие информацию о молекулярной массе и наличии функциональных групп обеспечивают небольшой вклад в значения полного ионного тока
10 Недостатки метода: • Молекулярные ионы образуются лишь у 20% органических соединений • Определение легколетучих термически стабильных соединений; • Ионы с большими значениями m/z, дающие информацию о молекулярной массе и наличии функциональных групп обеспечивают небольшой вклад в значения полного ионного тока
 11 Типы ионизации 2. Химическая ионизация. Органическое вещество ионизируется газом реагентом: метаном, аммиаком, изобутаном Определяемые молекулы АВ ионизируются непосредственно ионами реагентного газа за счет ряда реакций: CH 5+ + АВ → АH 2+ + CH 4 Далее протонированная молекула образца выталкивается электрическим полем в сторону масс-анализатора
11 Типы ионизации 2. Химическая ионизация. Органическое вещество ионизируется газом реагентом: метаном, аммиаком, изобутаном Определяемые молекулы АВ ионизируются непосредственно ионами реагентного газа за счет ряда реакций: CH 5+ + АВ → АH 2+ + CH 4 Далее протонированная молекула образца выталкивается электрическим полем в сторону масс-анализатора
 12 Достоинства: 1. Мягкий метод ионизации, молекуле образца передается около 5 э. В избыточной энергии, что препятствует процессам распада и позволяет подвергать анализу нестойкие молекулы 2. Интенсивный пик молекулярного иона, что позволяет определить молекулярную массу
12 Достоинства: 1. Мягкий метод ионизации, молекуле образца передается около 5 э. В избыточной энергии, что препятствует процессам распада и позволяет подвергать анализу нестойкие молекулы 2. Интенсивный пик молекулярного иона, что позволяет определить молекулярную массу
 13 Недостатки: 1. Отсутствие распада, очень простые массспектры, что не позволяет судить о структуре вещества и сравнить спектр с базами массспектральных данных 2. Анализ только газовых веществ.
13 Недостатки: 1. Отсутствие распада, очень простые массспектры, что не позволяет судить о структуре вещества и сравнить спектр с базами массспектральных данных 2. Анализ только газовых веществ.
 14 Типы ионизации 3. Бомбардировка ускоренными атомами. Ионизация ионами инертных газов: аргона, ксенона. • пробу помещают в ионизатор непосредственно или предварительно, растворяют в подходящей нелетучей матрице (обычно, в глицерине) • облучение потоком нейтральных высокоэнергетических атомов, например, Аг или Хе • образование положительных и отрицательных ионов, которые в результате десорбции отрываются от поверхности
14 Типы ионизации 3. Бомбардировка ускоренными атомами. Ионизация ионами инертных газов: аргона, ксенона. • пробу помещают в ионизатор непосредственно или предварительно, растворяют в подходящей нелетучей матрице (обычно, в глицерине) • облучение потоком нейтральных высокоэнергетических атомов, например, Аг или Хе • образование положительных и отрицательных ионов, которые в результате десорбции отрываются от поверхности
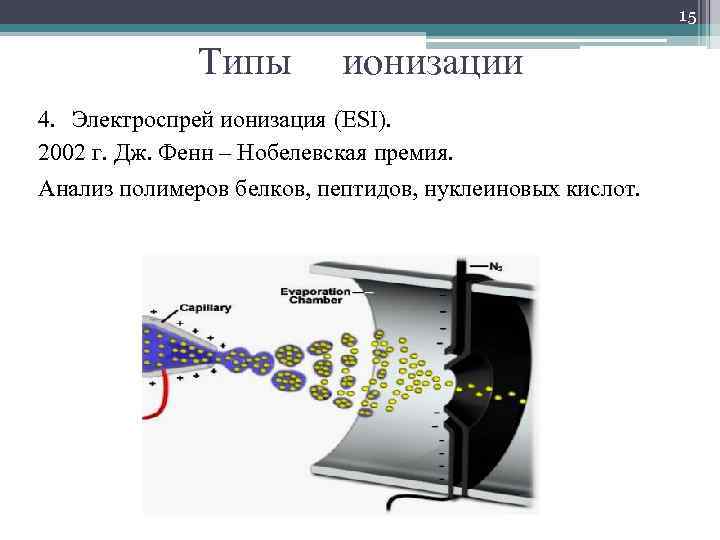 15 Типы ионизации 4. Электроспрей ионизация (ESI). 2002 г. Дж. Фенн – Нобелевская премия. Анализ полимеров белков, пептидов, нуклеиновых кислот.
15 Типы ионизации 4. Электроспрей ионизация (ESI). 2002 г. Дж. Фенн – Нобелевская премия. Анализ полимеров белков, пептидов, нуклеиновых кислот.
 16 Достоинства: • Метод позволяет работать с веществами, которые нельзя перевести в газовую фазу • Удобен для сочетания масс-спектрометра с жидкостным хроматографом • Возможность анализа крупных молекул • Мягкое (низкоэнергетическое) ионизационное воздействие
16 Достоинства: • Метод позволяет работать с веществами, которые нельзя перевести в газовую фазу • Удобен для сочетания масс-спектрометра с жидкостным хроматографом • Возможность анализа крупных молекул • Мягкое (низкоэнергетическое) ионизационное воздействие
 17 Недостатки: • Вещество должно быть растворимо в полярных растворителях • масс-спектр малоинформативен, как правило, присутствуют лишь пики комплексов молекулярного иона с катионом (H+ , Na+ , K+), многозарядных ионов таких комплексов
17 Недостатки: • Вещество должно быть растворимо в полярных растворителях • масс-спектр малоинформативен, как правило, присутствуют лишь пики комплексов молекулярного иона с катионом (H+ , Na+ , K+), многозарядных ионов таких комплексов
 18 Типы ионизации 5. Матричная лазерная десорбционная ионизация МЛДИ (MALDI). 2002 г. К. Танаке – Нобелевская премия. Анализ полимерных молекул: полипептидов, белков, нуклеотидов, полисахаридов, гуминовых веществ, лигнинов, синтетических полимеров.
18 Типы ионизации 5. Матричная лазерная десорбционная ионизация МЛДИ (MALDI). 2002 г. К. Танаке – Нобелевская премия. Анализ полимерных молекул: полипептидов, белков, нуклеотидов, полисахаридов, гуминовых веществ, лигнинов, синтетических полимеров.
 19 Взаимодействие лазерного импульса с образцом МЛДИ лазерный импульс (337 нм, 3. 68 э. В, 0. 1 нс)
19 Взаимодействие лазерного импульса с образцом МЛДИ лазерный импульс (337 нм, 3. 68 э. В, 0. 1 нс)
 20 Достоинства: 1. Возможность анализа крупных молекул. 2. Мягкая ионизация образца. 3. Возможность анализа загрязненных примесями образцов Недостатки: 1. Малоинформативный масс-спектр – присутствуют лишь пики молекулярного иона и его «мультимеров» - частиц, состоящих из нескольких молекул образца с зарядом +1 2. Долгая подготовка пробы и необходимость подбора условий под образец - подбирать вещество для матрицы
20 Достоинства: 1. Возможность анализа крупных молекул. 2. Мягкая ионизация образца. 3. Возможность анализа загрязненных примесями образцов Недостатки: 1. Малоинформативный масс-спектр – присутствуют лишь пики молекулярного иона и его «мультимеров» - частиц, состоящих из нескольких молекул образца с зарядом +1 2. Долгая подготовка пробы и необходимость подбора условий под образец - подбирать вещество для матрицы
 21 Типы ионизации 6. Полевая ионизация • Ионизация происходит под действием электрического поля высокой напряженности (до 108 В/см). • Происходит на эмиттере – вольфрамовой проволоке, покрытой пиролитическим углеродом. Частицы углерода увеличивают локальную напряженность поля и способствуют ионизации. • Метод относится к мягким способам ионизации. • Количество образующихся фрагментов невелико. • Спектр достаточно простой и содержит молекулярный пик. • Требуют предварительного испарения пробы (~500 °С).
21 Типы ионизации 6. Полевая ионизация • Ионизация происходит под действием электрического поля высокой напряженности (до 108 В/см). • Происходит на эмиттере – вольфрамовой проволоке, покрытой пиролитическим углеродом. Частицы углерода увеличивают локальную напряженность поля и способствуют ионизации. • Метод относится к мягким способам ионизации. • Количество образующихся фрагментов невелико. • Спектр достаточно простой и содержит молекулярный пик. • Требуют предварительного испарения пробы (~500 °С).
 22 Способы ввода пробы: • Непрямой способ - пробу вводят в ионизатор в газообразном состоянии. Жидкие и твердые пробы испаряют(~500 °С) в вакуумной камере • Прямой способ - используется для труднолетучих проб. Образец непосредственно вводят в ионизатор с помощью штанги через систему шлюзовых камер. • Анализируемое вещество поступает в массспектрометр в ходе хроматографического разделения.
22 Способы ввода пробы: • Непрямой способ - пробу вводят в ионизатор в газообразном состоянии. Жидкие и твердые пробы испаряют(~500 °С) в вакуумной камере • Прямой способ - используется для труднолетучих проб. Образец непосредственно вводят в ионизатор с помощью штанги через систему шлюзовых камер. • Анализируемое вещество поступает в массспектрометр в ходе хроматографического разделения.
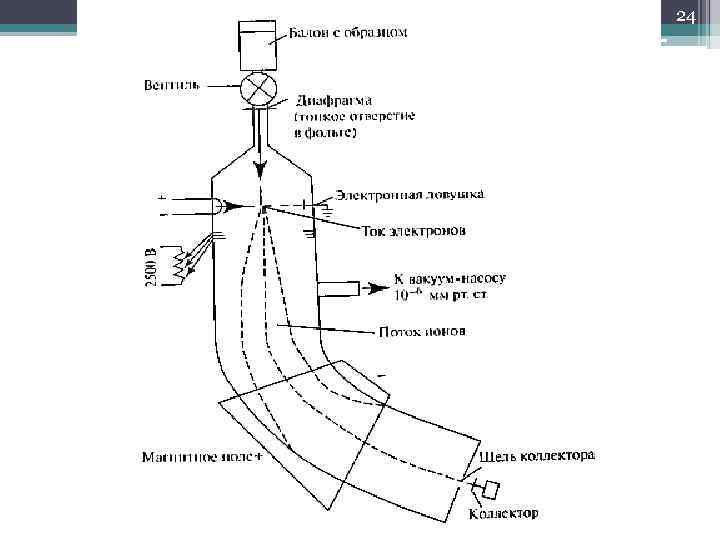
 23 Масс-спектрометрия под действием электронного удара
23 Масс-спектрометрия под действием электронного удара
 24
24
 25 Движение заряженной частицы в магнитном поле 2 2 m Br z 2 V m – масса иона; z – заряд иона; B– напряжённость магнитного поля; V – ускоряющее напряжение; r – радиус кривизны движения иона.
25 Движение заряженной частицы в магнитном поле 2 2 m Br z 2 V m – масса иона; z – заряд иона; B– напряжённость магнитного поля; V – ускоряющее напряжение; r – радиус кривизны движения иона.
 26 В масс-спектрометрии регистрируются только заряженные частицы: катион-радикалы АВС+. и катионы А+, АВ+, С+. Незаряженные радикальные частицы ВС. , АВ. не регистрируются.
26 В масс-спектрометрии регистрируются только заряженные частицы: катион-радикалы АВС+. и катионы А+, АВ+, С+. Незаряженные радикальные частицы ВС. , АВ. не регистрируются.
 27 Масс - анализатор Масс –анализатор – устройство для разделения ионов в соответствии с отношением m/z Основные типы масс-анализаторов: 1. магнитные 2. квадрупольные 3. времяпролетные
27 Масс - анализатор Масс –анализатор – устройство для разделения ионов в соответствии с отношением m/z Основные типы масс-анализаторов: 1. магнитные 2. квадрупольные 3. времяпролетные
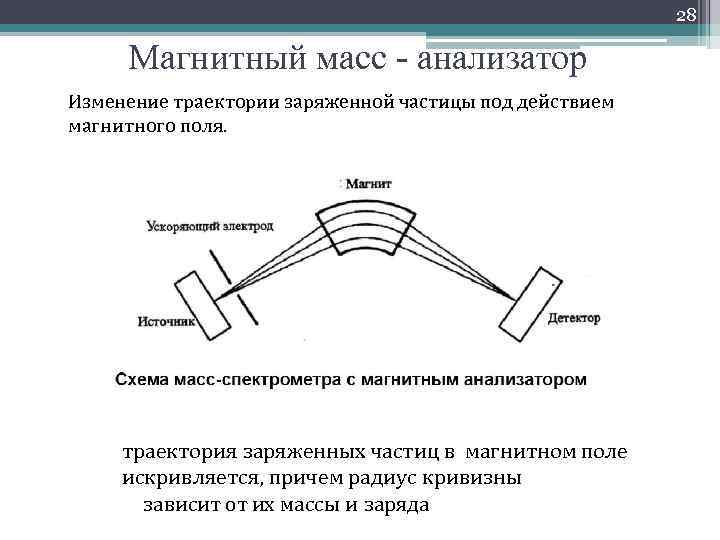 28 Магнитный масс - анализатор Изменение траектории заряженной частицы под действием магнитного поля. r 1 H 2 U 0 m / z траектория заряженных частиц в магнитном поле искривляется, причем радиус кривизны зависит от их массы и заряда 31
28 Магнитный масс - анализатор Изменение траектории заряженной частицы под действием магнитного поля. r 1 H 2 U 0 m / z траектория заряженных частиц в магнитном поле искривляется, причем радиус кривизны зависит от их массы и заряда 31
 29 Достоинства: высокое разрешение, чувствительность, большой диапазон детектируемых масс Основной недостаток – большой размер приборов и высокая стоимость
29 Достоинства: высокое разрешение, чувствительность, большой диапазон детектируемых масс Основной недостаток – большой размер приборов и высокая стоимость
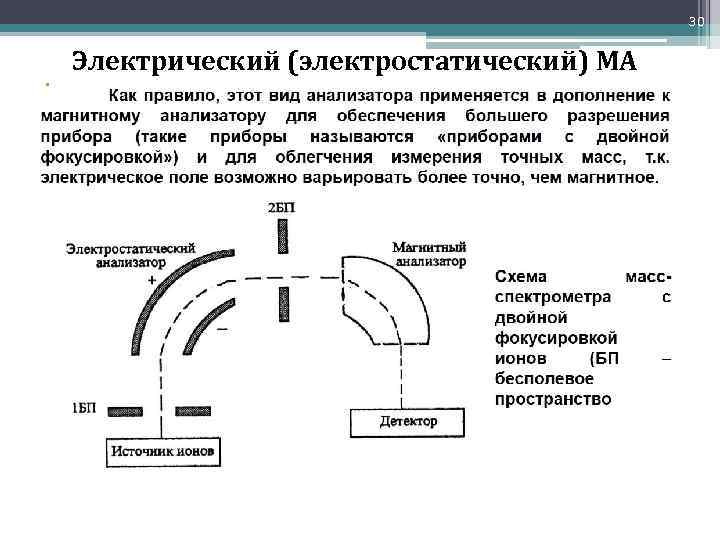 30 Электрический (электростатический) МА
30 Электрический (электростатический) МА
 31 Квадрупольный анализатор
31 Квадрупольный анализатор
 32
32
 33 Действие времяпролетных масс-анализаторов основано на зависимости скорости движения ионов от их массы. Особенность: ионы движутся в бесполевом пространстве После ускорителя все ионы обладают одинаковой кинетической энергией E = mv 2/2 , следовательно, чем больше их масса, тем меньше скорость, тем больше время пролета иона через анализатор Метод применим для определения массы больших молекул (десятки и сотни тысяч атомных единиц)
33 Действие времяпролетных масс-анализаторов основано на зависимости скорости движения ионов от их массы. Особенность: ионы движутся в бесполевом пространстве После ускорителя все ионы обладают одинаковой кинетической энергией E = mv 2/2 , следовательно, чем больше их масса, тем меньше скорость, тем больше время пролета иона через анализатор Метод применим для определения массы больших молекул (десятки и сотни тысяч атомных единиц)
 34 ЖИДКОСТНАЯ ХРОМАТО-МАСССПЕКТРОМЕТРИЯ • Сочетание ВЭЖХ и МС. • Анализ смесей труднолетучих, полярных веществ, не поддающихся анализу методом газожидкостной хроматографии.
34 ЖИДКОСТНАЯ ХРОМАТО-МАСССПЕКТРОМЕТРИЯ • Сочетание ВЭЖХ и МС. • Анализ смесей труднолетучих, полярных веществ, не поддающихся анализу методом газожидкостной хроматографии.
 35
35
 36 Детекторы ионов Сначала использовалась фотопластинка. В настоящее время применяют динодные вторично-электронные умножители, в которых ион, попадая на первый динод выбивает из него пучок электронов, которые в свою очередь, попадая на следующий динод, выбивают из него ещё большее количество электронов и т. д. микроканальные умножители, системы типа диодных матриц и коллекторы, собирающие все ионы, попавшие в данную точку пространства (коллекторы Фарадея)
36 Детекторы ионов Сначала использовалась фотопластинка. В настоящее время применяют динодные вторично-электронные умножители, в которых ион, попадая на первый динод выбивает из него пучок электронов, которые в свою очередь, попадая на следующий динод, выбивают из него ещё большее количество электронов и т. д. микроканальные умножители, системы типа диодных матриц и коллекторы, собирающие все ионы, попавшие в данную точку пространства (коллекторы Фарадея)
 37 Для МС характерны Использование небольших навесок ( 1 мг и меньше) Высокая чувствительность все элементы периодической системы определяют с чувствительностью 10 -12 г при использовании лазерных источников ионизации достигается чувствительность 10 -19 г Универсальность – возможность анализа широкого круга объектов от элементов до сложных белковых молекул Высокая специфичность и селективность Недостаток масс-спектрометрии: это деструктивный 62 метод анализа, и используемый образец нельзя восстановить для дальнейшего анализа или синтеза
37 Для МС характерны Использование небольших навесок ( 1 мг и меньше) Высокая чувствительность все элементы периодической системы определяют с чувствительностью 10 -12 г при использовании лазерных источников ионизации достигается чувствительность 10 -19 г Универсальность – возможность анализа широкого круга объектов от элементов до сложных белковых молекул Высокая специфичность и селективность Недостаток масс-спектрометрии: это деструктивный 62 метод анализа, и используемый образец нельзя восстановить для дальнейшего анализа или синтеза
 Области применения МС Ядерная энергетика Археология Нефтехимия Геохимия (изотопная геохронология) Агрохимия Химическая промышленность Анализ полупроводниковых материалов, особо чистых металлов, тонких пленок и порошков (например, оксидов U и РЗЭ) Фармацевтика - для контроля качества производимых лекарств и выявления фальсификатов Медицинская диагностика Биохимия – идентификация белков, исследование метаболизма лекарственных средств 38
Области применения МС Ядерная энергетика Археология Нефтехимия Геохимия (изотопная геохронология) Агрохимия Химическая промышленность Анализ полупроводниковых материалов, особо чистых металлов, тонких пленок и порошков (например, оксидов U и РЗЭ) Фармацевтика - для контроля качества производимых лекарств и выявления фальсификатов Медицинская диагностика Биохимия – идентификация белков, исследование метаболизма лекарственных средств 38
 39 Масс-спектрометрическая характеристика различных классов органических соединений
39 Масс-спектрометрическая характеристика различных классов органических соединений
 40 Алканы Обычно дают малоинтенсивные пики М+. В масс-спектрах характерно присутствие гомологичных ионов [Cn. H 2 n+1]+. Самые интенсивные пики m/z 43 [C 3 H 7]+ и m/z 57 [C 4 H 9]+.
40 Алканы Обычно дают малоинтенсивные пики М+. В масс-спектрах характерно присутствие гомологичных ионов [Cn. H 2 n+1]+. Самые интенсивные пики m/z 43 [C 3 H 7]+ и m/z 57 [C 4 H 9]+.
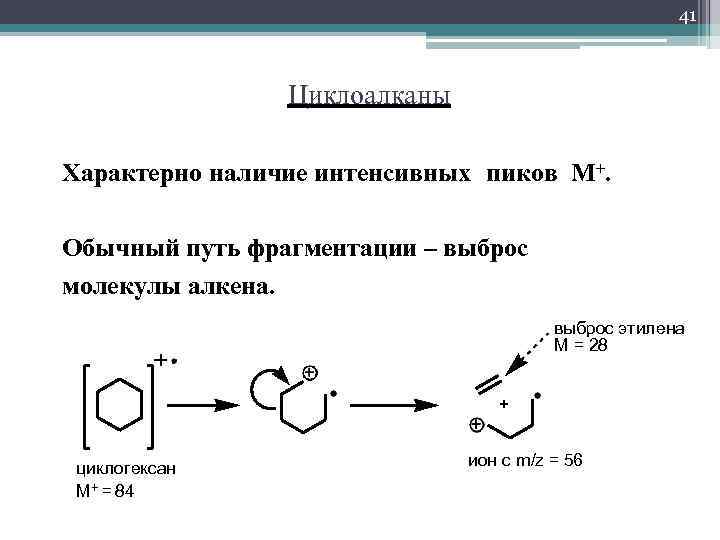 41 Циклоалканы Характерно наличие интенсивных пиков М+. Обычный путь фрагментации – выброс молекулы алкена. выброс этилена M = 28 циклогексан M+ = 84 ион с m/z = 56
41 Циклоалканы Характерно наличие интенсивных пиков М+. Обычный путь фрагментации – выброс молекулы алкена. выброс этилена M = 28 циклогексан M+ = 84 ион с m/z = 56
 42 Алкены и алкины Пики М+ обычно более интенсивны, чем у алканов. В масс-спектрах характерно присутствие гомологичных ионов [Cn. H 2 n-1]+ и [Cn. H 2 n-3]+. Распад молекул сопровождается перегруппировками с миграцией кратной связи.
42 Алкены и алкины Пики М+ обычно более интенсивны, чем у алканов. В масс-спектрах характерно присутствие гомологичных ионов [Cn. H 2 n-1]+ и [Cn. H 2 n-3]+. Распад молекул сопровождается перегруппировками с миграцией кратной связи.
 43 Спирты Молекулярные ионы М+ образуются при потере электрона от неподелённой электронной пары атома кислорода. Основные пути распада: - элиминирование молекулы Н 2 О; - разрыв α-β связи.
43 Спирты Молекулярные ионы М+ образуются при потере электрона от неподелённой электронной пары атома кислорода. Основные пути распада: - элиминирование молекулы Н 2 О; - разрыв α-β связи.
![44 Масс-спектр бутанола-1 100 [+CH 2 OH] 31 I, % 56 = 74 -18 44 Масс-спектр бутанола-1 100 [+CH 2 OH] 31 I, % 56 = 74 -18](https://present5.com/presentation/40744259_456078862/image-44.jpg) 44 Масс-спектр бутанола-1 100 [+CH 2 OH] 31 I, % 56 = 74 -18 = M+- H 2 O [C 3 H 5]+ 41 [C 3 H 7]+ 43 50 M+ OH 74 m/z 10 20 30 40 50 60 70
44 Масс-спектр бутанола-1 100 [+CH 2 OH] 31 I, % 56 = 74 -18 = M+- H 2 O [C 3 H 5]+ 41 [C 3 H 7]+ 43 50 M+ OH 74 m/z 10 20 30 40 50 60 70
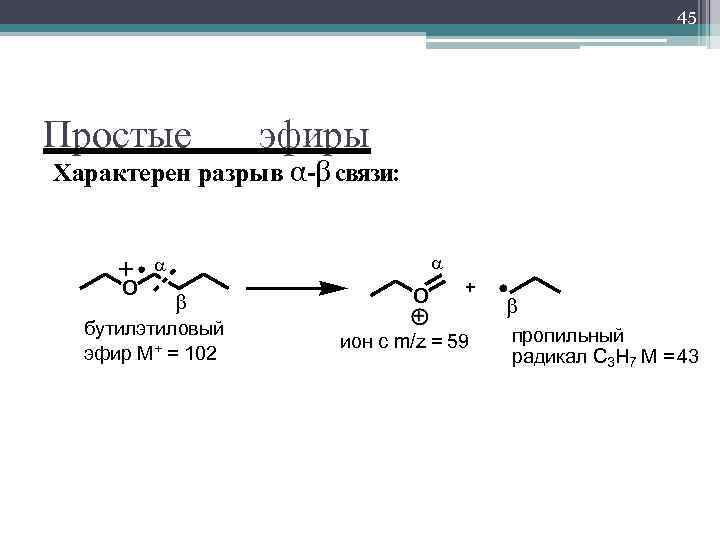 45 Простые эфиры Характерен разрыв α-β связи: O бутилэтиловый эфир M+ = 102 O ион с m/z = 59 пропильный радикал С 3 Н 7 M = 43
45 Простые эфиры Характерен разрыв α-β связи: O бутилэтиловый эфир M+ = 102 O ион с m/z = 59 пропильный радикал С 3 Н 7 M = 43
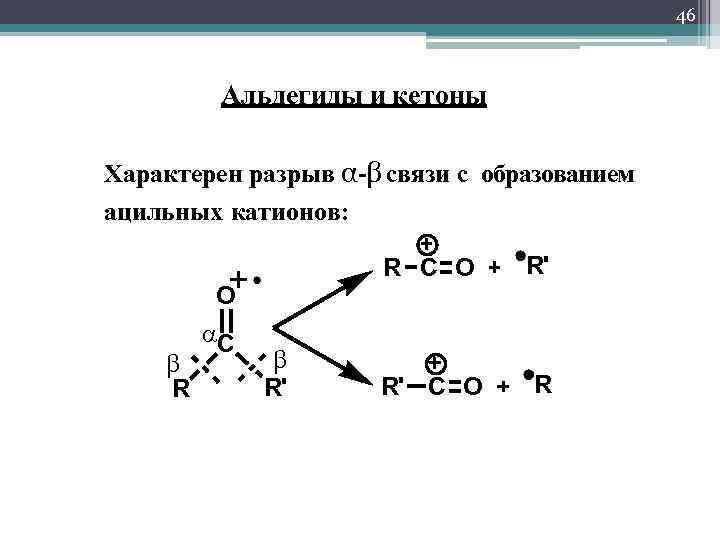 46 Альдегиды и кетоны Характерен разрыв α-β связи с образованием ацильных катионов: R C O O R C R' R' R' C O R
46 Альдегиды и кетоны Характерен разрыв α-β связи с образованием ацильных катионов: R C O O R C R' R' R' C O R
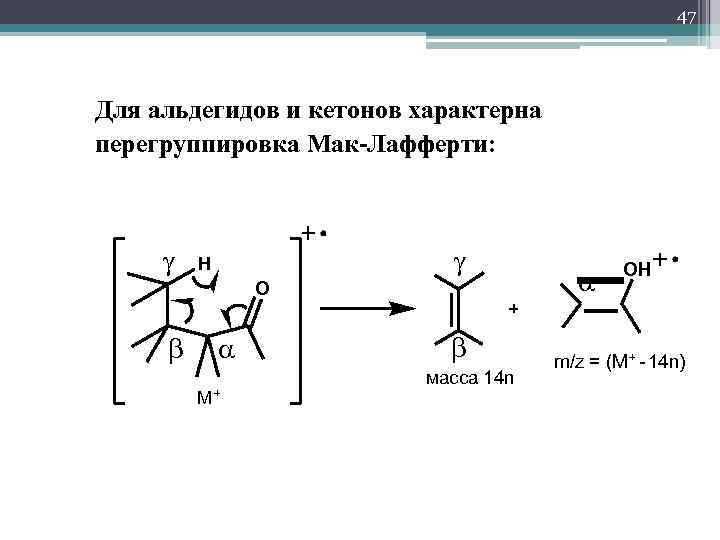 47 Для альдегидов и кетонов характерна перегруппировка Мак-Лафферти: H O M+ масса 14 n OH m/z = (M+ - 14 n)
47 Для альдегидов и кетонов характерна перегруппировка Мак-Лафферти: H O M+ масса 14 n OH m/z = (M+ - 14 n)
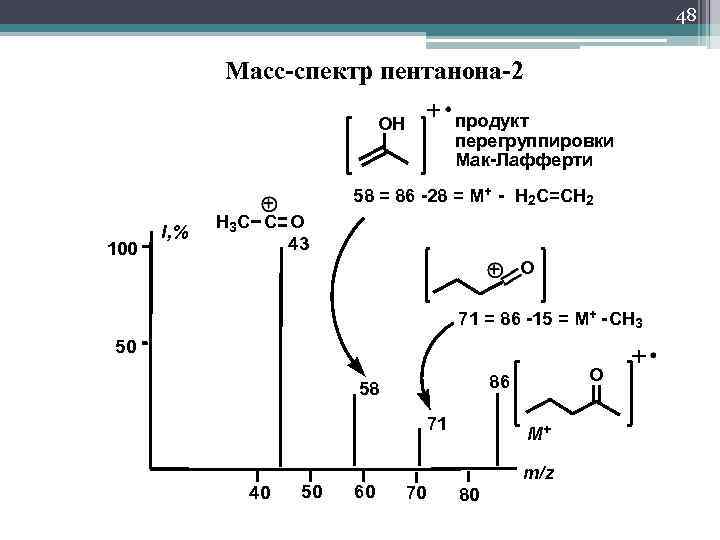 48 Масс-спектр пентанона-2 продукт перегруппировки Мак-Лафферти OH 58 = 86 -28 = M+ - H 2 C=CH 2 100 I, % H 3 C C O 43 O 71 = 86 -15 = M+ - CH 3 50 71 40 50 60 O 86 58 70 M+ m/z 80
48 Масс-спектр пентанона-2 продукт перегруппировки Мак-Лафферти OH 58 = 86 -28 = M+ - H 2 C=CH 2 100 I, % H 3 C C O 43 O 71 = 86 -15 = M+ - CH 3 50 71 40 50 60 O 86 58 70 M+ m/z 80
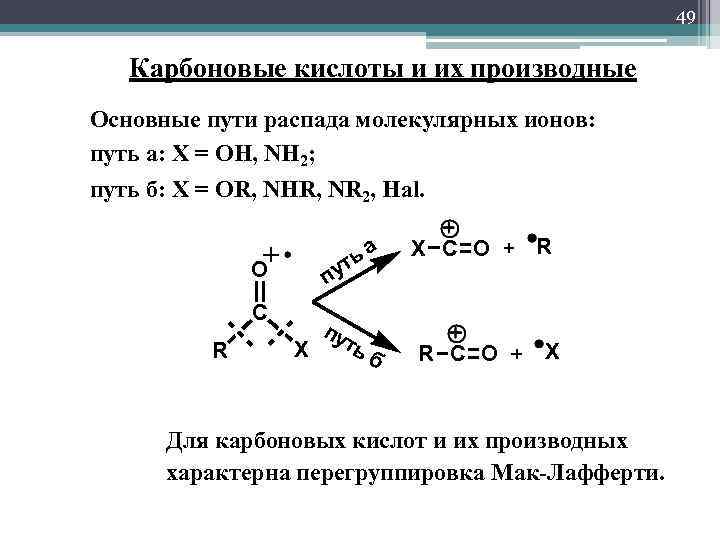 49 Карбоновые кислоты и их производные Основные пути распада молекулярных ионов: путь а: Х = OH, NH 2; путь б: Х = OR, NHR, NR 2, Hal. O C R ьа ут п пу ть X б X C O R X Для карбоновых кислот и их производных характерна перегруппировка Мак-Лафферти.
49 Карбоновые кислоты и их производные Основные пути распада молекулярных ионов: путь а: Х = OH, NH 2; путь б: Х = OR, NHR, NR 2, Hal. O C R ьа ут п пу ть X б X C O R X Для карбоновых кислот и их производных характерна перегруппировка Мак-Лафферти.
 50 Ароматические соединения Характерно образование стабильных высоко интенсивных молекулярных ионов М+. В масс-спектрах производных бензола содержатся характеристичные пики с m/z 78 -76, 65 -63, 52 -50, 39 -37. Характер масс-спектрометрического распада аренов определяется заместителями в ароматическом кольце.
50 Ароматические соединения Характерно образование стабильных высоко интенсивных молекулярных ионов М+. В масс-спектрах производных бензола содержатся характеристичные пики с m/z 78 -76, 65 -63, 52 -50, 39 -37. Характер масс-спектрометрического распада аренов определяется заместителями в ароматическом кольце.


