подгруппа марганца.ppt
- Количество слайдов: 23
 МАРГАНЕЦ Нахождение в природе: В земной коре - 0, 03%. Минерал – пиролюзит (Мn. О 2·Н 2 О). Физические свойства: Мn – серебристо-белый металл, плотность 7, 2 г/см 3, твердый, хрупкий, при 12600 С плавится, а при 21200 С закипает. На воздухе покрывается пестрыми пятнами оксидной пленки. Получение: t 1) 3 Мn. О 2 = Мn 3 О 4 + О 2 пиролюзит 2) 3 Мn 3 О 4 + 8 А 1 = 4 А 12 О 3 + 9 Мn Fе 2 О 3 + Мn. О 2 + 5 С = 2 Fе·Мn + 5 СО ферромарганец 3) Электролиз расплава Мn. SО 4.
МАРГАНЕЦ Нахождение в природе: В земной коре - 0, 03%. Минерал – пиролюзит (Мn. О 2·Н 2 О). Физические свойства: Мn – серебристо-белый металл, плотность 7, 2 г/см 3, твердый, хрупкий, при 12600 С плавится, а при 21200 С закипает. На воздухе покрывается пестрыми пятнами оксидной пленки. Получение: t 1) 3 Мn. О 2 = Мn 3 О 4 + О 2 пиролюзит 2) 3 Мn 3 О 4 + 8 А 1 = 4 А 12 О 3 + 9 Мn Fе 2 О 3 + Мn. О 2 + 5 С = 2 Fе·Мn + 5 СО ферромарганец 3) Электролиз расплава Мn. SО 4.
 Химические свойства: Образует соединения в с. о. +2, +3, +4, +6, +7. 1) Легко растворяется в воде в присутствии соединений, дающих при гидролизе кислую среду: Мn + 2 Н 2 О + 2 NН 4 С 1 = Мn. С 12 + 2 NН 4 ОН + Н 2 2) Взаимодействует с неметаллами. Мn + С 12 = Мn С 12 (хлорид) 2 Мn + Si = Мn 2 Si (силицид) 3) Растворяется в кислотах не окислителях с выделением водорода: Мn + 2 НС 1 = Мn. С 12 + Н 2 4) Пассивируется при действии холодной НNО 3. 5) На воздухе брусок покрывается прочной оксидной пленкой. Мелко раздробленный окисляется легко. Применение: Марганец в виде ферромарганца используют в черной металлургии.
Химические свойства: Образует соединения в с. о. +2, +3, +4, +6, +7. 1) Легко растворяется в воде в присутствии соединений, дающих при гидролизе кислую среду: Мn + 2 Н 2 О + 2 NН 4 С 1 = Мn. С 12 + 2 NН 4 ОН + Н 2 2) Взаимодействует с неметаллами. Мn + С 12 = Мn С 12 (хлорид) 2 Мn + Si = Мn 2 Si (силицид) 3) Растворяется в кислотах не окислителях с выделением водорода: Мn + 2 НС 1 = Мn. С 12 + Н 2 4) Пассивируется при действии холодной НNО 3. 5) На воздухе брусок покрывается прочной оксидной пленкой. Мелко раздробленный окисляется легко. Применение: Марганец в виде ферромарганца используют в черной металлургии.
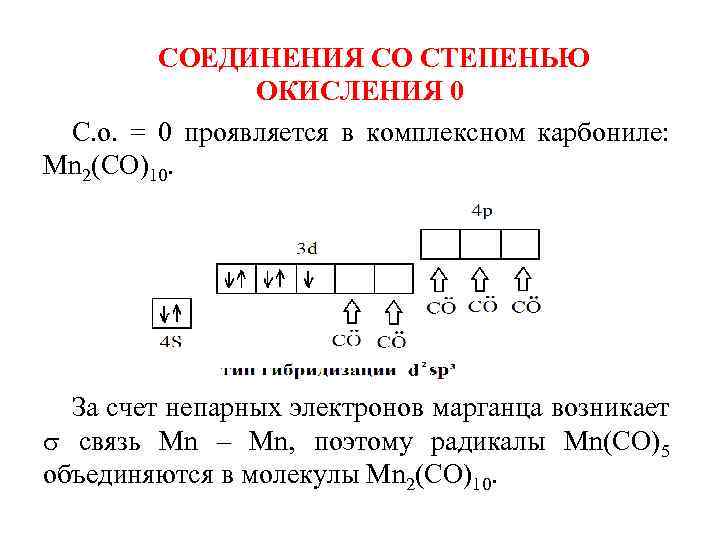 СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ 0 С. о. = 0 проявляется в комплексном карбониле: Mn 2(СО)10. За счет непарных электронов марганца возникает связь Мn – Мn, поэтому радикалы Мn(СО)5 объединяются в молекулы Мn 2(СО)10.
СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ 0 С. о. = 0 проявляется в комплексном карбониле: Mn 2(СО)10. За счет непарных электронов марганца возникает связь Мn – Мn, поэтому радикалы Мn(СО)5 объединяются в молекулы Мn 2(СО)10.
 КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ Оксиды: Мn. О Мn 2 О 3 Мn. О 2 Мn. О 3 Мn 2 О 7 и гидроксиды Мn(ОН)2 Мn(ОН)3 Мn(ОН)4 Н 2 Мn. О 4 НМn. О 4 ---------------------------- кислотные свойства увеличиваются
КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ Оксиды: Мn. О Мn 2 О 3 Мn. О 2 Мn. О 3 Мn 2 О 7 и гидроксиды Мn(ОН)2 Мn(ОН)3 Мn(ОН)4 Н 2 Мn. О 4 НМn. О 4 ---------------------------- кислотные свойства увеличиваются
 СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +2 Физические свойства: Мn. О–серо-зеленый, Тпл=17800 С имеет переменный состав (Мn. О–Мn. О 1, 5), полупроводник. Получение: Реакции протекают при нагревании: 1) Мn. О 2 +Н 2 = Mn. О +Н 2 О 2) Мn. СО 3=Mn. О+СО 2 Химические свойства: 1) С водой не взаимодействует, Мn(ОН)2 получают косвенно: Мn. SО 4 + 2 КОН = Мn(ОН)2 + К 2 SО 4 2) Мn. О взаимодействует с кислотами: Мn. О + 2 Н 3 О+ + 3 Н 2 О = [Мn(Н 2 О)6]2+ 3) Со щелочами при длительном и сильном нагревании: Мn(ОН)2 + 4 ОН- = [Мn(ОН)6]4 Соли иона Мn 2+ хорошо растворимы в воде , кроме Мn. S, Мn. СО 3 и Мn 3(РО 4)2. В воде соли диссоциируют, образуя ион [Мn(Н 2 О)6]2+, имеющий розовую окраску.
СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +2 Физические свойства: Мn. О–серо-зеленый, Тпл=17800 С имеет переменный состав (Мn. О–Мn. О 1, 5), полупроводник. Получение: Реакции протекают при нагревании: 1) Мn. О 2 +Н 2 = Mn. О +Н 2 О 2) Мn. СО 3=Mn. О+СО 2 Химические свойства: 1) С водой не взаимодействует, Мn(ОН)2 получают косвенно: Мn. SО 4 + 2 КОН = Мn(ОН)2 + К 2 SО 4 2) Мn. О взаимодействует с кислотами: Мn. О + 2 Н 3 О+ + 3 Н 2 О = [Мn(Н 2 О)6]2+ 3) Со щелочами при длительном и сильном нагревании: Мn(ОН)2 + 4 ОН- = [Мn(ОН)6]4 Соли иона Мn 2+ хорошо растворимы в воде , кроме Мn. S, Мn. СО 3 и Мn 3(РО 4)2. В воде соли диссоциируют, образуя ион [Мn(Н 2 О)6]2+, имеющий розовую окраску.
 Получение солей Mn 2+: 4 НС 1+Mn. O 2=Mn. C 12+2 H 2 O
Получение солей Mn 2+: 4 НС 1+Mn. O 2=Mn. C 12+2 H 2 O
 При действии сильных является восстановителем. окислителей Мn 2+
При действии сильных является восстановителем. окислителей Мn 2+
 Взаимодействие с пероксидом водорода Mn 2++H 2 O 2=Mn 3++H 2 O Mn 3+ CH 2(COOH)2+HIO 3 HI → I 2 желтый → = HI+CO 2+H 2 O I 2·[C 6 H 12 O 6] синий → HIO 3 бесцветный
Взаимодействие с пероксидом водорода Mn 2++H 2 O 2=Mn 3++H 2 O Mn 3+ CH 2(COOH)2+HIO 3 HI → I 2 желтый → = HI+CO 2+H 2 O I 2·[C 6 H 12 O 6] синий → HIO 3 бесцветный
 В щелочной среде Мn(ОН)2 окисляется кислородом воздуха и быстро темнеет: 2 Мn(ОН)2+О 2 +2 Н 2 О = 2 Мn(ОН)4 В сильно щелочной среде окисление сопровождается образованием манганатов: сплавление 3 Мn. SО 4+2 О 3+12 КОН=3 К 2 Мn. О 4+ 3 К 2 SО 4+6 Н 2 О Сильные окислители (Рb. О 2) в кислой среде переводят Мn 2+ в Мn. О 4 -: 2 Мn. SО 4+5 Рb. О 2+6 НNО 3=2 НМn. О 4+3 Рb(NО 3)2+2 Рb. SО 4+2 Н 2 О
В щелочной среде Мn(ОН)2 окисляется кислородом воздуха и быстро темнеет: 2 Мn(ОН)2+О 2 +2 Н 2 О = 2 Мn(ОН)4 В сильно щелочной среде окисление сопровождается образованием манганатов: сплавление 3 Мn. SО 4+2 О 3+12 КОН=3 К 2 Мn. О 4+ 3 К 2 SО 4+6 Н 2 О Сильные окислители (Рb. О 2) в кислой среде переводят Мn 2+ в Мn. О 4 -: 2 Мn. SО 4+5 Рb. О 2+6 НNО 3=2 НМn. О 4+3 Рb(NО 3)2+2 Рb. SО 4+2 Н 2 О
 СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +4. Физические свойства: Мn. О 2 – черно-бурое вещество, переменного состава в воде не растворяется, инертен – без нагревания устойчив к действию большинства кислот. Химические свойства: 1)Амфотерен. Основным признаком отвечает черная соль Мn(SО 4)2 получают: Мn. SО 4+О 3+H 2 SO 4=Мn(SО 4)2+Н 2 О+O 2 Мn(SО 4)2 гидролизуется на цело: Мn(SО 4)2+2 Н 2 О = 2 H 2 SO 4+Mn. O 2 2) При сплавлении со щелочами или основными оксидами Мn. О 2 - кислотный оксид: Мn. О 2 + Са. О = Са. Мn. О 3 – образуются манганиты.
СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +4. Физические свойства: Мn. О 2 – черно-бурое вещество, переменного состава в воде не растворяется, инертен – без нагревания устойчив к действию большинства кислот. Химические свойства: 1)Амфотерен. Основным признаком отвечает черная соль Мn(SО 4)2 получают: Мn. SО 4+О 3+H 2 SO 4=Мn(SО 4)2+Н 2 О+O 2 Мn(SО 4)2 гидролизуется на цело: Мn(SО 4)2+2 Н 2 О = 2 H 2 SO 4+Mn. O 2 2) При сплавлении со щелочами или основными оксидами Мn. О 2 - кислотный оксид: Мn. О 2 + Са. О = Са. Мn. О 3 – образуются манганиты.
 Соединение Мn 4+ - сильные окислители: Мn. О 2+4 Н++2 е=Мn 2++2 Н 2 О; Е =1, 23 В. Окисляют НС 1(к): Мn. О 2+4 НС 1(к)=Мn. С 12+2 Н 2 О
Соединение Мn 4+ - сильные окислители: Мn. О 2+4 Н++2 е=Мn 2++2 Н 2 О; Е =1, 23 В. Окисляют НС 1(к): Мn. О 2+4 НС 1(к)=Мn. С 12+2 Н 2 О
 При взаимодействии с более сильными окислителями образуют производные Мn+6 и Мn+7: сплавление 3 Мn. О 2+КС 1 О 3+6 КОН=3 К 2 Мn. О 4+КС 1+3 Н 2 О 2 Мn. О 2+3 Рb. О 2+6 НNО 3=2 НМn. О 4+3 Рb(NО 3)2+2 Н 2 О
При взаимодействии с более сильными окислителями образуют производные Мn+6 и Мn+7: сплавление 3 Мn. О 2+КС 1 О 3+6 КОН=3 К 2 Мn. О 4+КС 1+3 Н 2 О 2 Мn. О 2+3 Рb. О 2+6 НNО 3=2 НМn. О 4+3 Рb(NО 3)2+2 Н 2 О
 СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +6 Мn. О 42 - существуют в избытке щелочей, иначе диспропорционируют: 3 ЭО 42 -+2 Н 2 О=2 ЭО 4 -+ЭО 2+4 ОНПроцесс легко идет в кислой среде, поэтому Н 2 Mn. О 4 на образуется. Соединения Мn+6 – сильные окислители, особенно в кислых средах: Мn. О 42 -+4 Н++2 е=Мn. О 2+2 Н 2 О, Е = 2, 26 В При действии более сильных окислителей превращаются в перманганаты: 2 К 2 Мn. О 4 + С 12 = 2 КМn. О 4 + 2 КС 1
СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +6 Мn. О 42 - существуют в избытке щелочей, иначе диспропорционируют: 3 ЭО 42 -+2 Н 2 О=2 ЭО 4 -+ЭО 2+4 ОНПроцесс легко идет в кислой среде, поэтому Н 2 Mn. О 4 на образуется. Соединения Мn+6 – сильные окислители, особенно в кислых средах: Мn. О 42 -+4 Н++2 е=Мn. О 2+2 Н 2 О, Е = 2, 26 В При действии более сильных окислителей превращаются в перманганаты: 2 К 2 Мn. О 4 + С 12 = 2 КМn. О 4 + 2 КС 1
 СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +7 Мn 2 О 7 – неустойчив, темнозеленая маслянистая жидкость. Получают: 2 КМn. О 4 + Н 2 SО 4 = Мn 2 О 7 + К 2 SО 4 + Н 2 О
СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +7 Мn 2 О 7 – неустойчив, темнозеленая маслянистая жидкость. Получают: 2 КМn. О 4 + Н 2 SО 4 = Мn 2 О 7 + К 2 SО 4 + Н 2 О
 Если не применять специальных мер Мn 2 О 7 разлагаются со взрывом: 2 Мn 2 О 7 = 4 Мn. О 2 + 3 О 2
Если не применять специальных мер Мn 2 О 7 разлагаются со взрывом: 2 Мn 2 О 7 = 4 Мn. О 2 + 3 О 2
 КМn. О 4 – сильный органические вещества. окислитель. Окисляет
КМn. О 4 – сильный органические вещества. окислитель. Окисляет
 В кислой среде восстанавливаются до Мn 2+: 2 КМn. О 4+10 КВr+8 Н 2 SО 4=2 Мn. SО 4+6 Н 2 SО 4+5 Вr 2+8 Н 2 О, Е 0=1, 58 В В щелочной среде до Мn. О 42 -: 2 КМn. О 4+К 2 SО 3+2 КОН=К 2 SО 4+2 К 2 Мn. О 4+Н 2 О, Е 0=0, 56 В В нейтральной до Мn. О 2: 2 КМn. О 4+С 6 Н 5 СН 3=2 КОН+2 Мn. О 2+С 6 Н 5 СООН, Е 0=0, 6 В
В кислой среде восстанавливаются до Мn 2+: 2 КМn. О 4+10 КВr+8 Н 2 SО 4=2 Мn. SО 4+6 Н 2 SО 4+5 Вr 2+8 Н 2 О, Е 0=1, 58 В В щелочной среде до Мn. О 42 -: 2 КМn. О 4+К 2 SО 3+2 КОН=К 2 SО 4+2 К 2 Мn. О 4+Н 2 О, Е 0=0, 56 В В нейтральной до Мn. О 2: 2 КМn. О 4+С 6 Н 5 СН 3=2 КОН+2 Мn. О 2+С 6 Н 5 СООН, Е 0=0, 6 В
 Взаимодействие перманганата в разных средах
Взаимодействие перманганата в разных средах
 При нагревании КМn. О 4 разлагаются: 2 КМn. О 4 = К 2 Мn. О 4 + Мn. О 2 + О 2
При нагревании КМn. О 4 разлагаются: 2 КМn. О 4 = К 2 Мn. О 4 + Мn. О 2 + О 2
 Применение: КМn. О 4 для отбелки текстильных материалов, осветления масел, окисления органических веществ. Получение: Раньше: 1)Мn. О 2+КNО 3+2 КОН = К 2 Мn. О 4 + КNО 2 + Н 2 О 3 К 2 Мn. О 4 + 2 Н 2 О = 2 КМn. О 4 + Мn. О 2 + 4 КОН 2) 2 К 2 Мn. О 4 + С 12 = 2 КМn. О 4 + 2 КС 1 Сейчас: электролитическое окисление манганатов: Мn. О 42 - -е = Мn. О 4 -
Применение: КМn. О 4 для отбелки текстильных материалов, осветления масел, окисления органических веществ. Получение: Раньше: 1)Мn. О 2+КNО 3+2 КОН = К 2 Мn. О 4 + КNО 2 + Н 2 О 3 К 2 Мn. О 4 + 2 Н 2 О = 2 КМn. О 4 + Мn. О 2 + 4 КОН 2) 2 К 2 Мn. О 4 + С 12 = 2 КМn. О 4 + 2 КС 1 Сейчас: электролитическое окисление манганатов: Мn. О 42 - -е = Мn. О 4 -
 Технеций и рений Технеций (Тс) и рений (Re) полные электронные аналоги. Электронная конфигурация внешнего уровня: (n-1)d 5 ns 2. Атомные радиусы Тс и Re близки из-за лантаноидного сжатия, их свойства сходны друг с другом, чем с марганцем. Для Тс устойчивая с. о. +8, к. ч. для Тс и Re равно 7, 8, 9. Тс – первый искусственный элемент. Физические свойства: В ряду Мn – Тс – Re доля ковалентной связи, образованной за счет электронов (n-1)d орбиталей увеличивается, увеличивается энергия возгонки, температура плавления и кипения. По тугоплавкости Re уступает только вольфраму.
Технеций и рений Технеций (Тс) и рений (Re) полные электронные аналоги. Электронная конфигурация внешнего уровня: (n-1)d 5 ns 2. Атомные радиусы Тс и Re близки из-за лантаноидного сжатия, их свойства сходны друг с другом, чем с марганцем. Для Тс устойчивая с. о. +8, к. ч. для Тс и Re равно 7, 8, 9. Тс – первый искусственный элемент. Физические свойства: В ряду Мn – Тс – Re доля ковалентной связи, образованной за счет электронов (n-1)d орбиталей увеличивается, увеличивается энергия возгонки, температура плавления и кипения. По тугоплавкости Re уступает только вольфраму.
 Химические свойства: В ряду Мn – Тс – Re химическая активность падает. Марганец в ряду напряжений до водорода, Тс и Re после. 1) Мn взаимодействует с НС 1(р) и Н 2 SО 4(р), а Тс и Re реагируют только с НNО 3. 2) При нагревании Тс и Re реагируют с неметаллами. 3) В атмосфере кислорода сгорают, образуя Э 2 О 7. Получение: Источник получения Тс – продукты деления урана.
Химические свойства: В ряду Мn – Тс – Re химическая активность падает. Марганец в ряду напряжений до водорода, Тс и Re после. 1) Мn взаимодействует с НС 1(р) и Н 2 SО 4(р), а Тс и Re реагируют только с НNО 3. 2) При нагревании Тс и Re реагируют с неметаллами. 3) В атмосфере кислорода сгорают, образуя Э 2 О 7. Получение: Источник получения Тс – продукты деления урана.
 Степень окисления +2 не характерна. Производные Тс4+ устойчивее однотипных соединений Мn+4 и Re+4. Более устойчивы соединения Re и Тс в с. о. +6. Галогениды и оксиды Тс и Re (VI) – кислотные соединения. Устойчивость соединений в ряду Мn+7–Тс+7–Re+7 увеличивается. Тс2 О 7 и Re 2 О 7 устойчивые кристаллические вещества желтого цвета. Тс2 О 7 разлагается при t = 2600 С, а Re 2 О 7 кипит при t = 3590 С без разложения. Получение Тс2 О 7 и Re 2 О: 4 Э+7 О 2=2 Э 2 О 7 Применение: Катализаторы.
Степень окисления +2 не характерна. Производные Тс4+ устойчивее однотипных соединений Мn+4 и Re+4. Более устойчивы соединения Re и Тс в с. о. +6. Галогениды и оксиды Тс и Re (VI) – кислотные соединения. Устойчивость соединений в ряду Мn+7–Тс+7–Re+7 увеличивается. Тс2 О 7 и Re 2 О 7 устойчивые кристаллические вещества желтого цвета. Тс2 О 7 разлагается при t = 2600 С, а Re 2 О 7 кипит при t = 3590 С без разложения. Получение Тс2 О 7 и Re 2 О: 4 Э+7 О 2=2 Э 2 О 7 Применение: Катализаторы.


