МАКРОМОЛЕКУЛЯРНЫЕ КОМПЛЕКСЫ. РИБОСОМЫ Сапунов Г.


МАКРОМОЛЕКУЛЯРНЫЕ КОМПЛЕКСЫ. РИБОСОМЫ Сапунов Г. А.

Рибосомы важнейший немембранный органоид В эукариотических клетках живой клетки сферической или слегка рибосомы располагаются на эллипсоидной формы, диаметром 10— мембранах эндоплазматической 20 нанометров, состоящий из большой сети, хотя могут быть локализованы и малой субъединиц. и в неприкрепленной форме в Рибосомы служат для биосинтеза белка цитоплазме. из аминокислот по заданной матрице на основе генетической информации, Нередко с одной молекулой м. РНК предоставляемой матричной РНК. Этот ассоциировано несколько рибосом, процесс называется трансляцией. такая структура называется полирибосомой (полисомой). Синтез рибосом у эукариот происходит в специальной внутриядерной структуре — ядрышке.
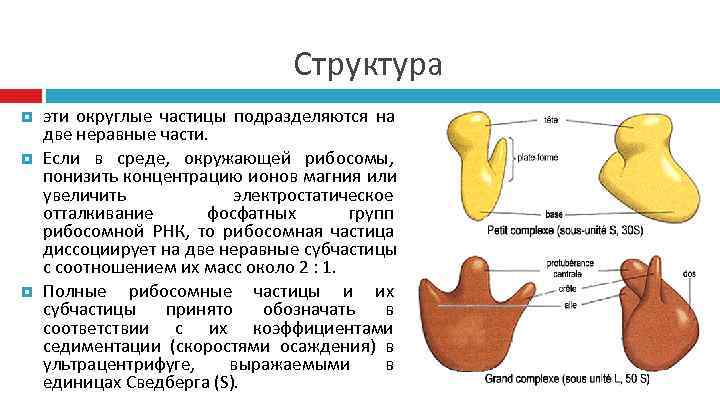
Структура эти округлые частицы подразделяются на две неравные части. Если в среде, окружающей рибосомы, понизить концентрацию ионов магния или увеличить электростатическое отталкивание фосфатных групп рибосомной РНК, то рибосомная частица диссоциирует на две неравные субчастицы с соотношением их масс около 2 : 1. Полные рибосомные частицы и их субчастицы принято обозначать в соответствии с их коэффициентами седиментации (скоростями осаждения) в ультрацентрифуге, выражаемыми в единицах Сведберга (S).
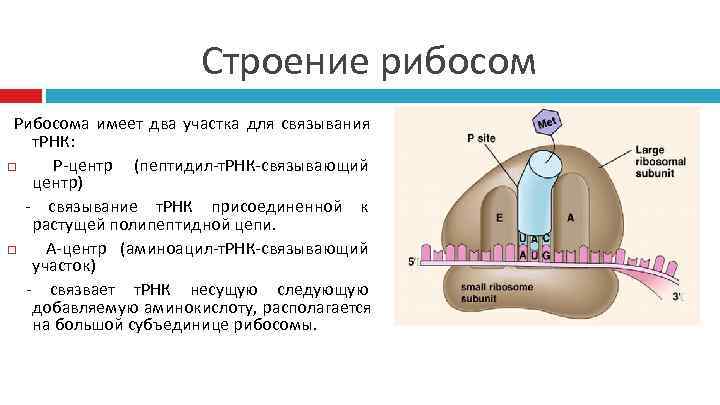
Строение рибосом Рибосома имеет два участка для связывания т. РНК: Р-центр (пептидил-т. РНК-связывающий центр) - связывание т. РНК присоединенной к растущей полипептидной цепи. А-центр (аминоацил-т. РНК-связывающий участок) - связвает т. РНК несущую следующую добавляемую аминокислоту, располагается на большой субъединице рибосомы.
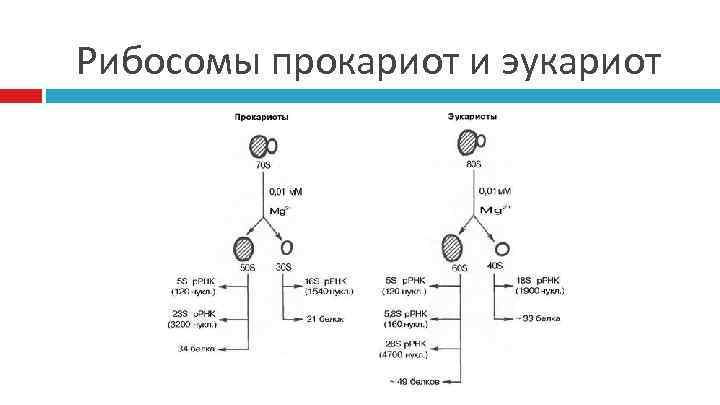
Рибосомы прокариот и эукариот
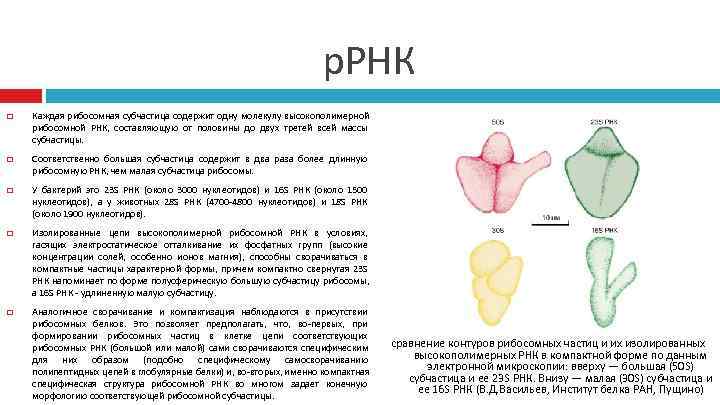
р. РНК Каждая рибосомная субчастица содержит одну молекулу высокополимерной рибосомной РНК, составляющую от половины до двух третей всей массы субчастицы. Соответственно большая субчастица содержит в два раза более длинную рибосомную РНК, чем малая субчастица рибосомы. У бактерий это 23 S РНК (около 3000 нуклеотидов) и 16 S РНК (около 1500 нуклеотидов), а у животных 28 S РНК (4700 -4800 нуклеотидов) и 18 S РНК (около 1900 нуклеотидов). Изолированные цепи высокополимерной рибосомной РНК в условиях, гасящих электростатическое отталкивание их фосфатных групп (высокие концентрации солей, особенно ионов магния), способны сворачиваться в компактные частицы характерной формы, причем компактно свернутая 23 S РНК напоминает по форме полусферическую большую субчастицу рибосомы, а 16 S РНК - удлиненную малую субчастицу. Аналогичное сворачивание и компактизация наблюдаются в присутствии рибосомных белков. Это позволяет предполагать, что, во-первых, при формировании рибосомных частиц в клетке цепи соответствующих рибосомных РНК (большой или малой) сами сворачиваются специфическим сравнение контуров рибосомных частиц и их изолированных для них образом (подобно специфическому самосворачиванию высокополимерных РНК в компактной форме по данным полипептидных цепей в глобулярные белки) и, во-вторых, именно компактная электронной микроскопии: вверху — большая (50 S) специфическая структура рибосомной РНК во многом задает конечную субчастица и ее 23 S РНК. Внизу — малая (30 S) субчастица и ее 16 S РНК (В. Д. Васильев, Институт белка РАН, Пущино) морфологию соответствующей рибосомной субчастицы.

Разнообразие р. РНК Физические исследования пространственного Помимо высокополимерной РНК распределения РНК и белка в рибосомных большая рибосомная субчастицах, проведенные с помощью рассеяния нейтронов, показали, что рибосомная РНК содержит одну или две молекулы концентрируется в основном ближе к центру относительно низкомолекулярных частиц, тогда как масса рибосомных белков РНК - это 5 S РНК в случае бактерий занимает в среднем более периферическое положение. и других прокариот или 5 S РНК и Можно сделать вывод, что свернутая молекула 5, 8 S РНК в случае эукариотических высокополимерной рибосомной РНК - это организмов. Указанные малые структурное ядро рибосомной субчастицы, рибосомные РНК сопоставимы по определяющее и ее компактность, и ее форму, и размерам с рибосомными организацию на ней рибосомных белков. белками и вместе с ними Следовательно, рибосома есть прежде всего ее располагаются на ядре РНК. высокополимерной рибосомной Согласно большинству современных РНК как на каркасе. эволюционных концепций, примитивный предшественник рибосомы мог состоять только из РНК и лишь в ходе эволюции постепенно дополняться белками.

Рибосомные белки Каждая рибосомная субчастица содержит много молекул рибосомных белков, и все они разные. В этом отношении рибосомный РНП принципиально отличается от вирусного, где белковая оболочка строится из однотипных белков за счет их симметричной слоевой упаковки на поверхности РНК. Самосборка четвертичной структуры - физический механизм реализации симметричной упаковки идентичных белковых молекул в слое, характерной для вирусных нуклеопротеидов. Однако такая белковая самосборка невозможна в случае разнородных белковых молекул, каковыми являются рибосомные белки. Здесь реализуется другой принцип: каждый рибосомный белок имеет свою персональную посадочную площадку на рибосомной РНК - свой "шесток". Белок специфически узнает только этот участок РНК и садится на него. Так, на рибосомной РНК рассаживаются все разнотипные рибосомные белки. На 23 S РНК бактериальной рибосомы за счет такого специфического РНК-белкового узнавания рассаживаются 32 различные белковые молекулы, а на 16 S РНК - 21 белок. Разделение индивидуальных белков бактериальной (Escherichia coli) 70 S рибосомы путем двумерного электрофореза в полиакриламидном геле. Буквой S (small) обозначаются белки малой (30 S) субчастицы, а буквой L (large) — большой (50 S) субчастицы рибосомы

Роль рибосомных белков Локализация белков, экранирование РНК 1. могут непосредственно участвовать в Во-первых, в рибосомах белка по массе функциях связывания субстратов и относительно много меньше, чем в вирусах, и его каталитических функциях рибосомы, просто не может хватить, чтобы покрыть всю локализуясь в соответствующих рибосомную РНК; рибосомная РНК может быть функциональных центрах и обеспечивая лишь "полуодета". их своими активными группами. Во-вторых, рибосомные белки, скорее всего, не 2. могут служить стабилизаторами или формируют поверхностных слоев, а организованы в группы - трехмерные кластеры, модификаторами определенных где часть белков оказывается под другими локальных структур рибосомной РНК и белками и не экспонирована на поверхности. таким образом поддерживать их в В-третьих, периферические структурные функционально активном состоянии или образования рибосомной РНК могут быть способствовать их переключениям из участниками этих кластеров наравне с белками и одного состояния в другое. в некоторых случаях прикрывать белки с поверхности.
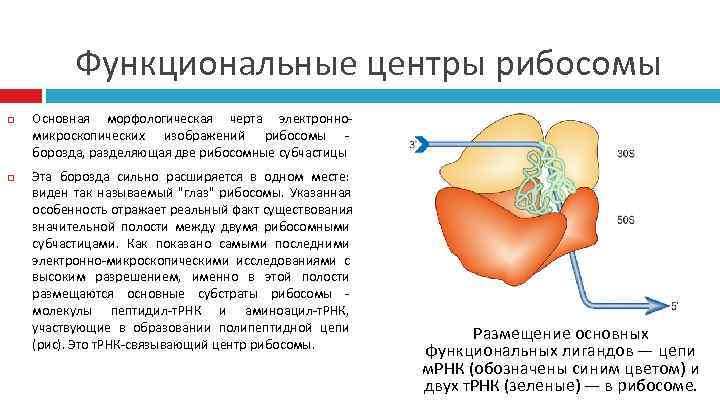
Функциональные центры рибосомы Основная морфологическая черта электронно- микроскопических изображений рибосомы - борозда, разделяющая две рибосомные субчастицы Эта борозда сильно расширяется в одном месте: виден так называемый "глаз" рибосомы. Указанная особенность отражает реальный факт существования значительной полости между двумя рибосомными субчастицами. Как показано самыми последними электронно-микроскопическими исследованиями с высоким разрешением, именно в этой полости размещаются основные субстраты рибосомы - молекулы пептидил-т. РНК и аминоацил-т. РНК, участвующие в образовании полипептидной цепи Размещение основных (рис). Это т. РНК-связывающий центр рибосомы. функциональных лигандов — цепи м. РНК (обозначены синим цветом) и двух т. РНК (зеленые) — в рибосоме.
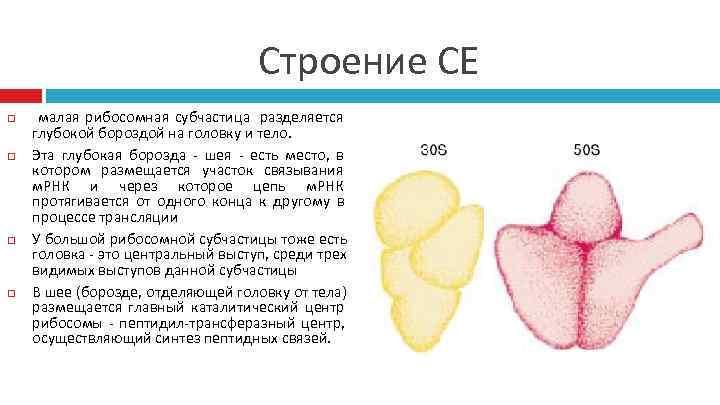
Строение СЕ малая рибосомная субчастица разделяется глубокой бороздой на головку и тело. Эта глубокая борозда - шея - есть место, в котором размещается участок связывания м. РНК и через которое цепь м. РНК протягивается от одного конца к другому в процессе трансляции У большой рибосомной субчастицы тоже есть головка - это центральный выступ, среди трех видимых выступов данной субчастицы В шее (борозде, отделяющей головку от тела) размещается главный каталитический центр рибосомы - пептидил-трансферазный центр, осуществляющий синтез пептидных связей.
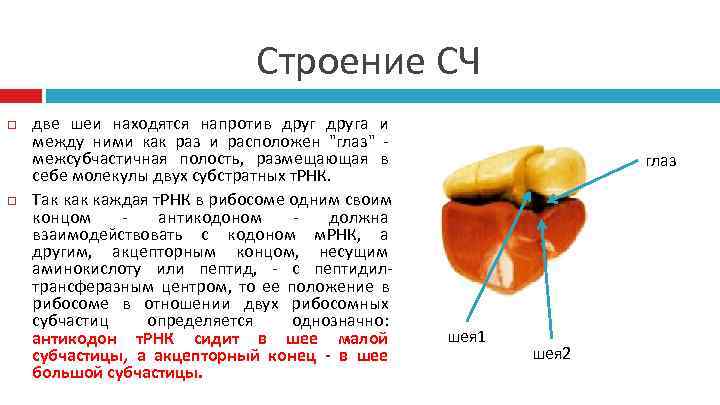
Строение СЧ две шеи находятся напротив друга и между ними как раз и расположен "глаз" - межсубчастичная полость, размещающая в глаз себе молекулы двух субстратных т. РНК. Так каждая т. РНК в рибосоме одним своим концом - антикодоном - должна взаимодействовать с кодоном м. РНК, а другим, акцепторным концом, несущим аминокислоту или пептид, - с пептидил- трансферазным центром, то ее положение в рибосоме в отношении двух рибосомных субчастиц определяется однозначно: антикодон т. РНК сидит в шее малой шея 1 субчастицы, а акцепторный конец - в шее шея 2 большой субчастицы.
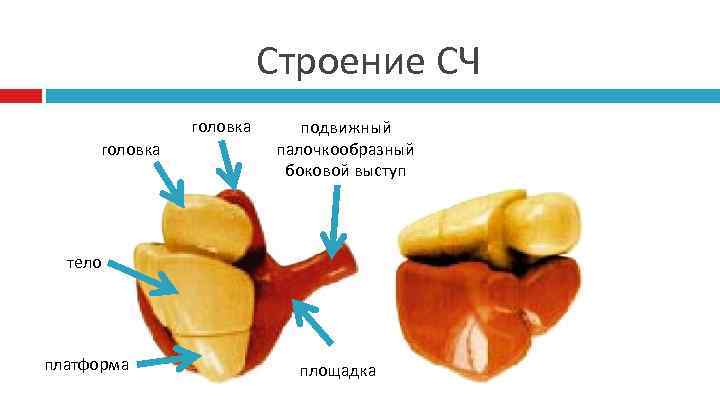
Строение СЧ головка подвижный головка палочкообразный боковой выступ тело платформа площадка

Ассоциация СЧ площадка принимает на себя поступающую в рибосому новую аминоацил- т. РНК в комплексе со специальным белком - фактором элонгации 1 (EF 1). При этом палочкообразный отросток взаимодействует с фактором и ориентируется более или менее перпендикулярно плоскости раздела между субчастицами. В результате образуется карман между непокрытой площадкой большой субчастицы, боковой поверхностью малой субчастицы и палочкообразным отростком. Этот же карман может принимать другой белок - фактор элонгации 2 (EF 2), связывающийся с рибосомой для производства механического акта - транслокации. Третий – левый выступ большой субчастицы и примыкающая к нему лопасть (боковое "ребро"), по-видимому, непосредственно участвуют в ассоциации рибосомных субчастиц. Со стороны малой рибосомной субчастицы в ассоциации субчастиц участвует боковая лопасть ее "тела"

Механизм действия Биосинтез белка имеет два аспекта: химический и генетический. Белок строится из аминокислот путем последовательного добавления аминокислотных остатков к одному из концов растущей полипептидной цепи (удлинения) с одновременным сканированием матричного полинуклеотида (м. РНК), задающего порядок добавления различных аминокислотных остатков. Три последовательные химические реакции приводят к включению (добавлению) аминокислоты в полипептидную цепь строящегося белка: 1. аминокислота + АТФ >> аминоацил-аденилат + пирофосфат, 2. аминоацил-аденилат + т. РНК' >>аминоацил-т. РНК' + АМФ, 3. пептидил(n)-т. РНК + аминоацил-т. РНК' >> т. РНК + пептидил(n + 1)-т. РНК‘.

Биосинтез белка Первая реакция - активация аминокислоты за счет образования ангидридной связи между ее карбоксилом и фосфатом адениловой кислоты в процессе биосинтеза белка вторая реакция - акцептирование аминоацильного остатка молекулой т. РНК с образованием сложноэфирной связи между карбоксилом аминокислоты и гидроксилом концевого рибозного остатка т. РНК – рибосома: Третья реакция - транспептидация, то есть перенос карбоксильной группы растущего полипептида от гидроксила рибозного остатка т. РНК, принесшей предыдущий принимает кодированную аминокислотный остаток в цепь, на аминогруппу аминокислотного остатка аминоацил-т. РНК - генетическую информацию 1 и 2 происходят вне рибосомы, и обе реакции катализируется ферментом аминоацил-т. РНК-синтетазой. от ДНК в виде м. РНК и 3 осуществляется в рибосоме и катализируется самой рибосомой, без постороннего фермента. расшифровывает ее, Таким образом, именно молекулы аминоацил-т. РНК являются формой поступления аминокислотных остатков в рибосомы. катализирует образование Генетическая сторона биосинтеза белка определяется тем, что поступление аминоацил-т. РНК в рибосому строго детерминировано матричной РНК (м. РНК), пептидных связей в реакции являющейся копией гена, и порядок чередования кодирующих триплетов (кодонов) вдоль цепи м. РНК однозначно задает структуру синтезируемого белка. Для этого транспептидации рибосома сканирует цепь м. РНК по триплетам и последовательно выбирает из раствора аминоацил-т. РНК с соответствующими аминокислотными остатками, выбрасывая отработанные, деацилированные т. РНК. передвигает цепь м. РНК и молекулы т. РНК (транслокация).
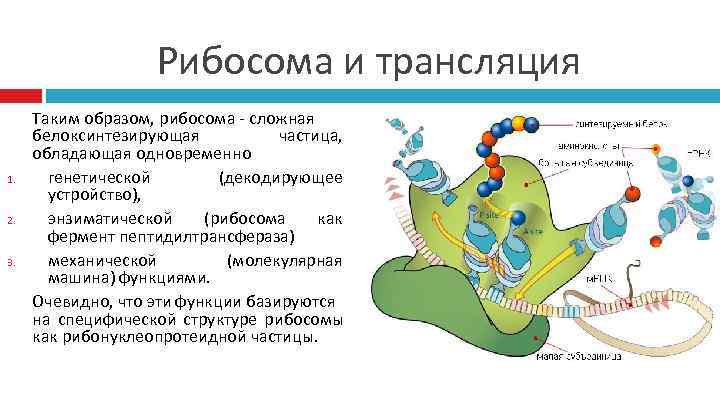
Рибосома и трансляция Таким образом, рибосома - сложная белоксинтезирующая частица, обладающая одновременно 1. генетической (декодирующее устройство), 2. энзиматической (рибосома как фермент пептидилтрансфераза) 3. механической (молекулярная машина) функциями. Очевидно, что эти функции базируются на специфической структуре рибосомы как рибонуклеопротеидной частицы.
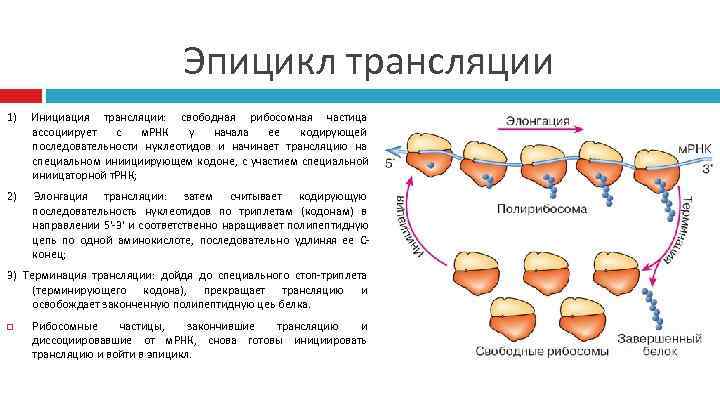
Эпицикл трансляции 1) Инициация трансляции: свободная рибосомная частица ассоциирует с м. РНК у начала ее кодирующей последовательности нуклеотидов и начинает трансляцию на специальном иниициирующем кодоне, с участием специальной иниицаторной т. РНК; 2) Элонгация трансляции: затем считывает кодирующую последовательность нуклеотидов по триплетам (кодонам) в направлении 5'-3' и соответственно наращивает полипептидную цепь по одной аминокислоте, последовательно удлиняя ее С- конец; 3) Терминация трансляции: дойдя до специального стоп-триплета (терминирующего кодона), прекращает трансляцию и освобождает законченную полипептидную цеь белка. Рибосомные частицы, закончившие трансляцию и диссоциировавшие от м. РНК, снова готовы инициировать трансляцию и войти в эпицикл.
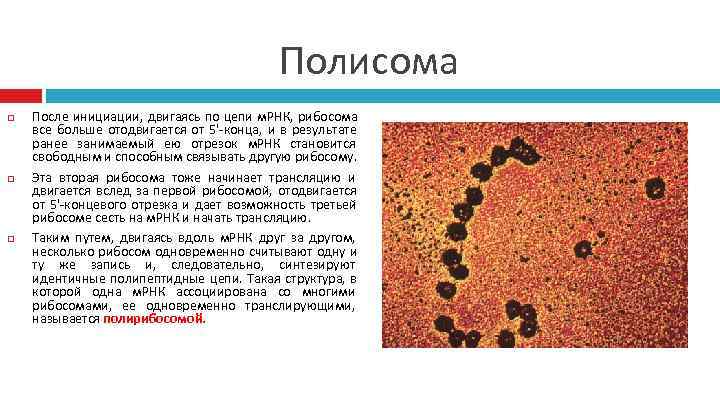
Полисома После инициации, двигаясь по цепи м. РНК, рибосома все больше отодвигается от 5'-конца, и в результате ранее занимаемый ею отрезок м. РНК становится свободным и способным связывать другую рибосому. Эта вторая рибосома тоже начинает трансляцию и двигается вслед за первой рибосомой, отодвигается от 5'-концевого отрезка и дает возможность третьей рибосоме сесть на м. РНК и начать трансляцию. Таким путем, двигаясь вдоль м. РНК друг за другом, несколько рибосом одновременно считывают одну и ту же запись и, следовательно, синтезируют идентичные полипептидные цепи. Такая структура, в которой одна м. РНК ассоциирована со многими рибосомами, ее одновременно транслирующими, называется полирибосомой.
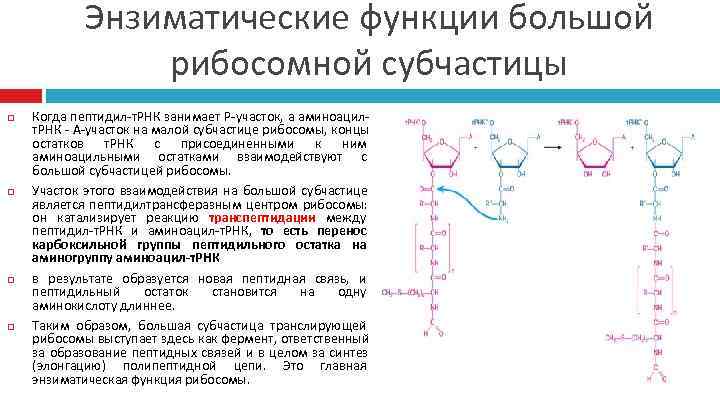
Энзиматические функции большой рибосомной субчастицы Когда пептидил-т. РНК занимает Р-участок, а аминоацил- т. РНК - А-участок на малой субчастице рибосомы, концы остатков т. РНК с присоединенными к ним аминоацильными остатками взаимодействуют с большой субчастицей рибосомы. Участок этого взаимодействия на большой субчастице является пептидилтрансферазным центром рибосомы: он катализирует реакцию транспептидации между пептидил-т. РНК и аминоацил-т. РНК, то есть перенос карбоксильной группы пептидильного остатка на аминогруппу аминоацил-т. РНК в результате образуется новая пептидная связь, и пептидильный остаток становится на одну аминокислоту длиннее. Таким образом, большая субчастица транслирующей рибосомы выступает здесь как фермент, ответственный за образование пептидных связей и в целом за синтез (элонгацию) полипептидной цепи. Это главная энзиматическая функция рибосомы.

Обратите внимание! Никакого отдельного от рибосомы белка-фермента, катализирующего образование пептидных связей на рибосоме, не существует. Не найдено и никакого специального белка в составе рибосомы, который бы обладал такой энзиматической функцией. Транспептидация катализируется пептидилтрансферазным центром самой рибосомы как интегральной частью большой рибосомной субчастицы, и основной вклад в организацию центра вносит, по-видимому, рибосомная РНК субчастицы. транспептидация - экзергоническая реакция, способная "накормить" энергией работающую рибосому и обеспечить спонтанное прохождение элонгационного цикла. прямой гидролиз ГТФ представляется необходимым для "энзиматического" (фактор -промотируемого) катализа нековалентных конформационных переходов в элонгационном цикле. Основная роль этого гидролиза - разрушение лиганда, обеспечивающего сродство катализатора к переходному конформационному состоянию, чтобы дать возможность выйти из этого промежуточного комплекса и перейти к следующему - продуктивному — состоянию.
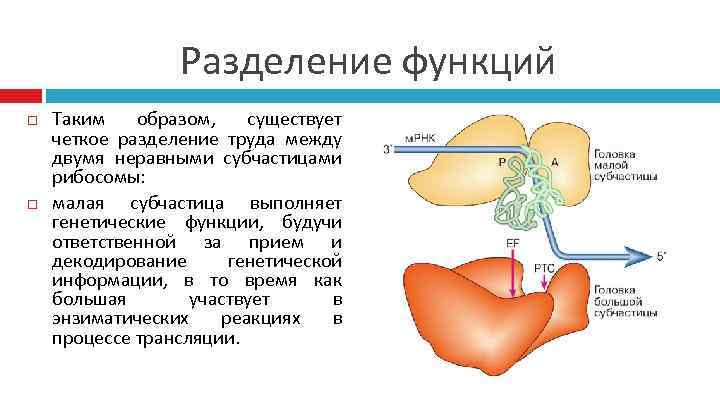
Разделение функций Таким образом, существует четкое разделение труда между двумя неравными субчастицами рибосомы: малая субчастица выполняет генетические функции, будучи ответственной за прием и декодирование генетической информации, в то время как большая участвует в энзиматических реакциях в процессе трансляции.
3 D-модель рибосомы на атомном уровне: Нобелевская премия 2009 по химии Рамакришнан и Йонат выявили строение рибосомы бактерии Haloarcula marismortui на атомном уровне
Макромолекулярные комплексы.ppt
- Количество слайдов: 23

