 МАГНИТНЫЕ СВОЙСТВА АТОМОВ Магнитные свойства атомов Эффект Зеемана Спин электрона Опыты Штерна и Герлаха Принцип тождественности одинаковых частиц Распределение электронов по энергетическим уровням атома
МАГНИТНЫЕ СВОЙСТВА АТОМОВ Магнитные свойства атомов Эффект Зеемана Спин электрона Опыты Штерна и Герлаха Принцип тождественности одинаковых частиц Распределение электронов по энергетическим уровням атома
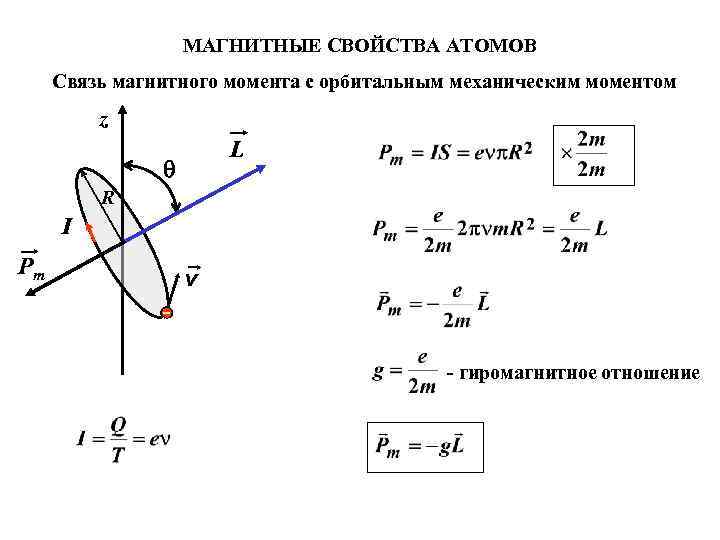 МАГНИТНЫЕ СВОЙСТВА АТОМОВ Связь магнитного момента с орбитальным механическим моментом z L R I Pm v - гиромагнитное отношение
МАГНИТНЫЕ СВОЙСТВА АТОМОВ Связь магнитного момента с орбитальным механическим моментом z L R I Pm v - гиромагнитное отношение
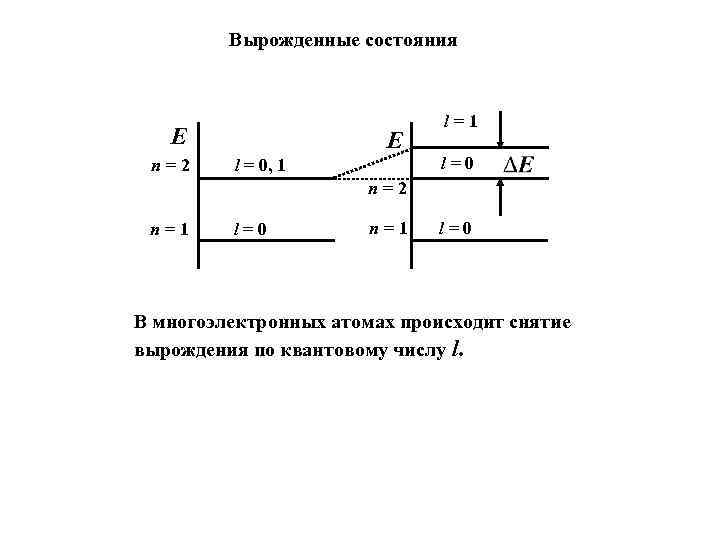 Вырожденные состояния E n=2 E l = 0, 1 l=0 n=2 n=1 l=0 В многоэлектронных атомах происходит снятие вырождения по квантовому числу l.
Вырожденные состояния E n=2 E l = 0, 1 l=0 n=2 n=1 l=0 В многоэлектронных атомах происходит снятие вырождения по квантовому числу l.
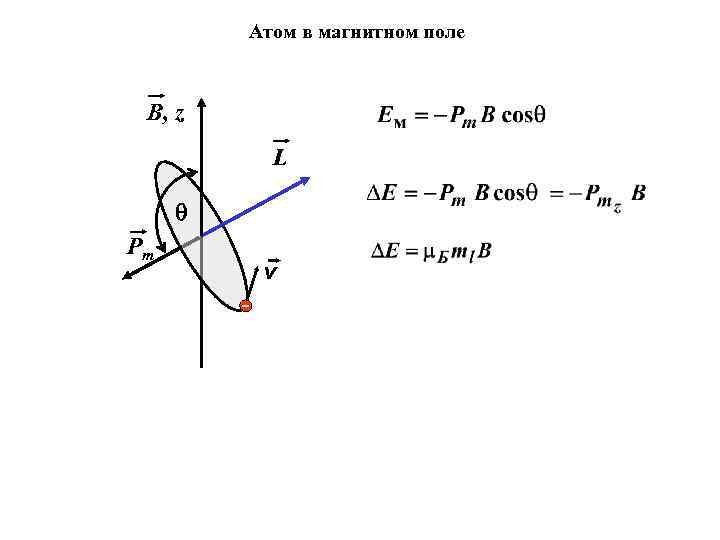 Атом в магнитном поле B, z L Pm v
Атом в магнитном поле B, z L Pm v
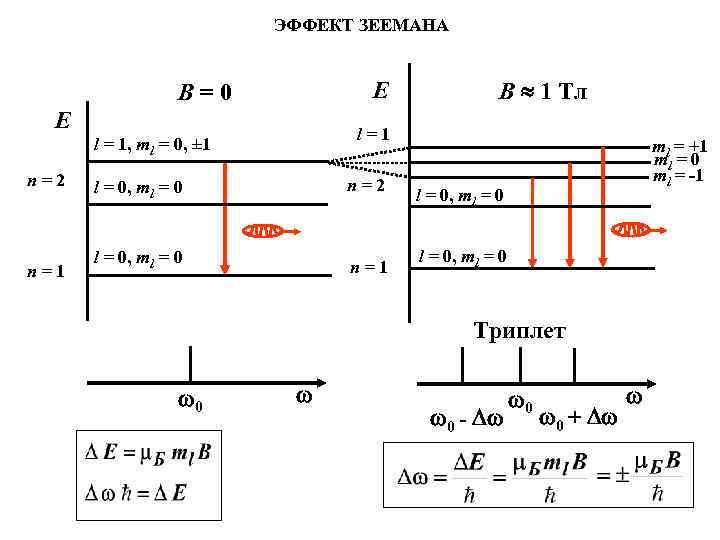 ЭФФЕКТ ЗЕЕМАНА E B=0 E l=1 l = 1, ml = 0, ± 1 n=2 n=1 B 1 Тл l = 0, ml = 0 n=2 l = 0, ml = 0 n=1 ml = +1 ml = 0 ml = -1 l = 0, ml = 0 Триплет 0 0 - 0 0 +
ЭФФЕКТ ЗЕЕМАНА E B=0 E l=1 l = 1, ml = 0, ± 1 n=2 n=1 B 1 Тл l = 0, ml = 0 n=2 l = 0, ml = 0 n=1 ml = +1 ml = 0 ml = -1 l = 0, ml = 0 Триплет 0 0 - 0 0 +
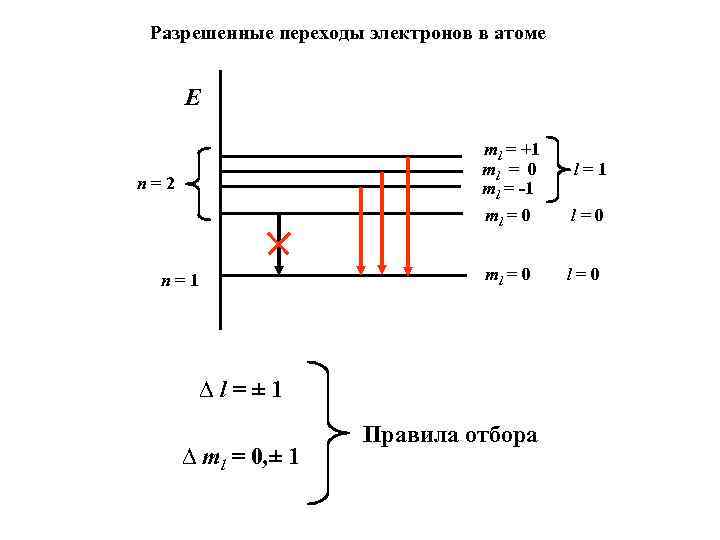 Разрешенные переходы электронов в атоме E ml = +1 ml = 0 ml = -1 ml = 0 n=2 n=1 l=0 ml = 0 l=0 l=± 1 ml = 0, ± 1 Правила отбора l=1
Разрешенные переходы электронов в атоме E ml = +1 ml = 0 ml = -1 ml = 0 n=2 n=1 l=0 ml = 0 l=0 l=± 1 ml = 0, ± 1 Правила отбора l=1
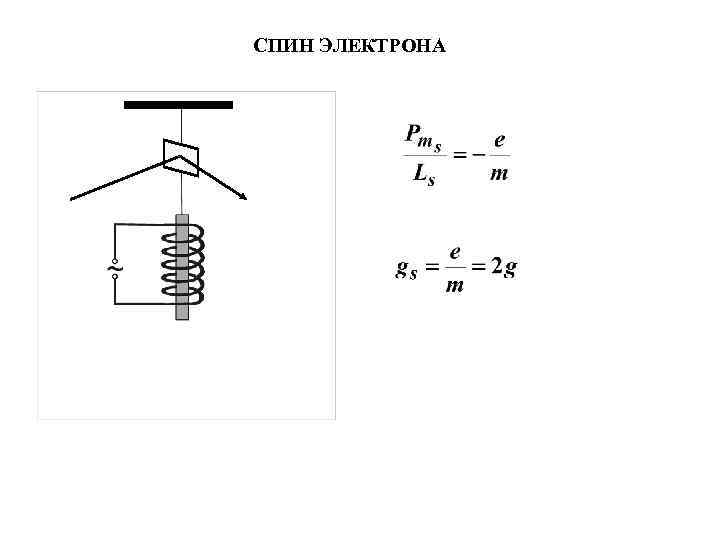 СПИН ЭЛЕКТРОНА
СПИН ЭЛЕКТРОНА
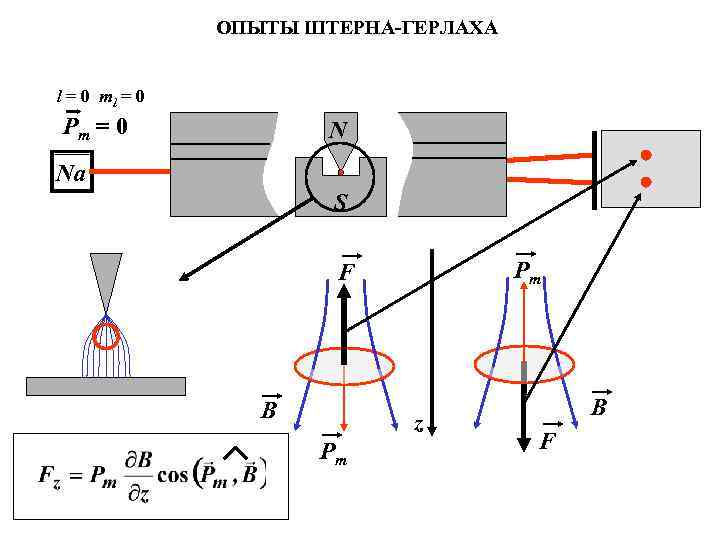 ОПЫТЫ ШТЕРНА-ГЕРЛАХА l = 0 ml = 0 Pm = 0 N Na S Pm F B z Pm B F
ОПЫТЫ ШТЕРНА-ГЕРЛАХА l = 0 ml = 0 Pm = 0 N Na S Pm F B z Pm B F
 s - спиновое квантовое число всего состояний магнитное спиновое квантовое число
s - спиновое квантовое число всего состояний магнитное спиновое квантовое число
 Квантовые числа n = 1, 2, 3, …. … l = 0, 1, 2…. , n − 1 ml = 0, 1, 2, …, l – главное квантовое число – азимутальное – магнитное − кратность вырождения Правила отбора n = 1, 2, 3, …. l= 1 ml = 0, 1 ms = 0
Квантовые числа n = 1, 2, 3, …. … l = 0, 1, 2…. , n − 1 ml = 0, 1, 2, …, l – главное квантовое число – азимутальное – магнитное − кратность вырождения Правила отбора n = 1, 2, 3, …. l= 1 ml = 0, 1 ms = 0
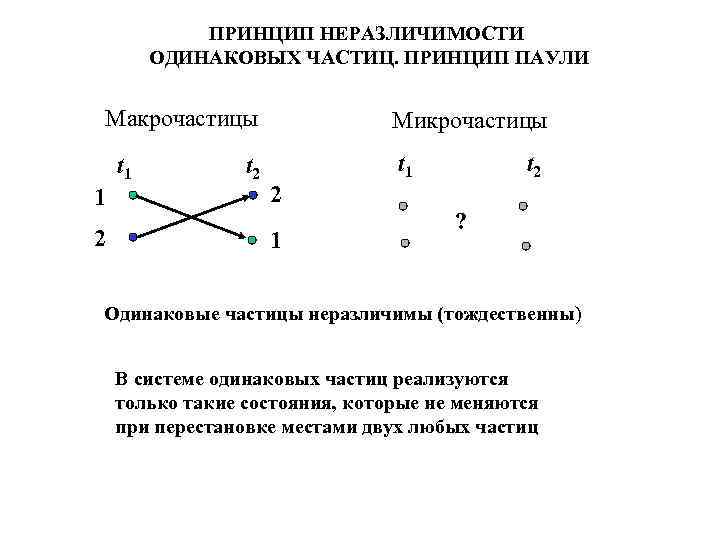 ПРИНЦИП НЕРАЗЛИЧИМОСТИ ОДИНАКОВЫХ ЧАСТИЦ. ПРИНЦИП ПАУЛИ Макрочастицы t 1 t 2 Микрочастицы t 1 1 2 2 1 t 2 ? Одинаковые частицы неразличимы (тождественны) В системе одинаковых частиц реализуются только такие состояния, которые не меняются при перестановке местами двух любых частиц
ПРИНЦИП НЕРАЗЛИЧИМОСТИ ОДИНАКОВЫХ ЧАСТИЦ. ПРИНЦИП ПАУЛИ Макрочастицы t 1 t 2 Микрочастицы t 1 1 2 2 1 t 2 ? Одинаковые частицы неразличимы (тождественны) В системе одинаковых частиц реализуются только такие состояния, которые не меняются при перестановке местами двух любых частиц
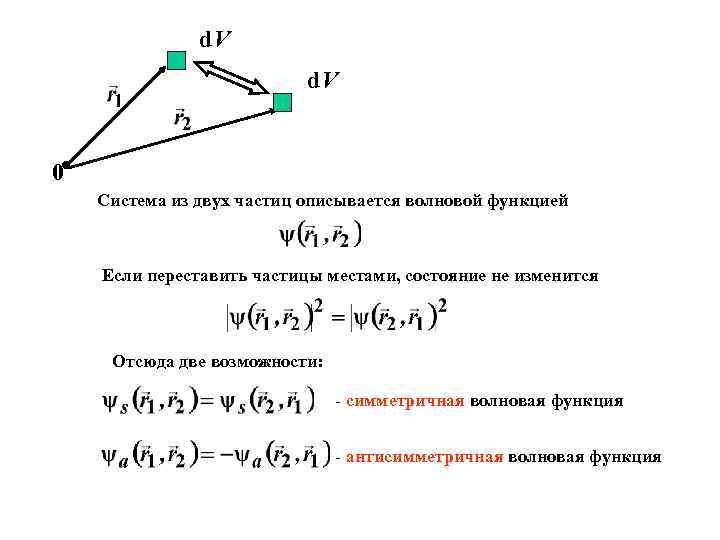 d. V 0 Система из двух частиц описывается волновой функцией Если переставить частицы местами, состояние не изменится Отсюда две возможности: - симметричная волновая функция - антисимметричная волновая функция
d. V 0 Система из двух частиц описывается волновой функцией Если переставить частицы местами, состояние не изменится Отсюда две возможности: - симметричная волновая функция - антисимметричная волновая функция
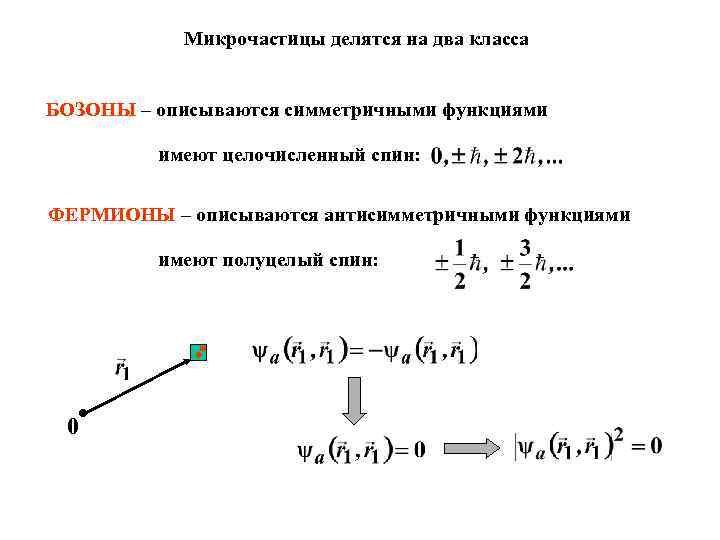 Микрочастицы делятся на два класса БОЗОНЫ – описываются симметричными функциями имеют целочисленный спин: ФЕРМИОНЫ – описываются антисимметричными функциями имеют полуцелый спин: 0
Микрочастицы делятся на два класса БОЗОНЫ – описываются симметричными функциями имеют целочисленный спин: ФЕРМИОНЫ – описываются антисимметричными функциями имеют полуцелый спин: 0
 ПРИНЦИП ПАУЛИ В системе тождественных фермионов не может быть двух частиц, находящихся в одном и том же состоянии В атоме не может быть двух электронов, характеризующихся одинаковой четверкой квантовых чисел
ПРИНЦИП ПАУЛИ В системе тождественных фермионов не может быть двух частиц, находящихся в одном и том же состоянии В атоме не может быть двух электронов, характеризующихся одинаковой четверкой квантовых чисел
 РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОНОВ ПО ЭНЕРГЕТИЧЕСКИМ УРОВНЯМ АТОМА 1. Принцип запрета Паули ms = 1/2 в квантовом состоянии (n, l, ml) может находиться не более двух электронов 2. Принцип наименьшей энергии n оболочка 1 2 3 4 5 K LMN O l 0 1 2 3 4 подоболочка s p d f g
РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОНОВ ПО ЭНЕРГЕТИЧЕСКИМ УРОВНЯМ АТОМА 1. Принцип запрета Паули ms = 1/2 в квантовом состоянии (n, l, ml) может находиться не более двух электронов 2. Принцип наименьшей энергии n оболочка 1 2 3 4 5 K LMN O l 0 1 2 3 4 подоболочка s p d f g
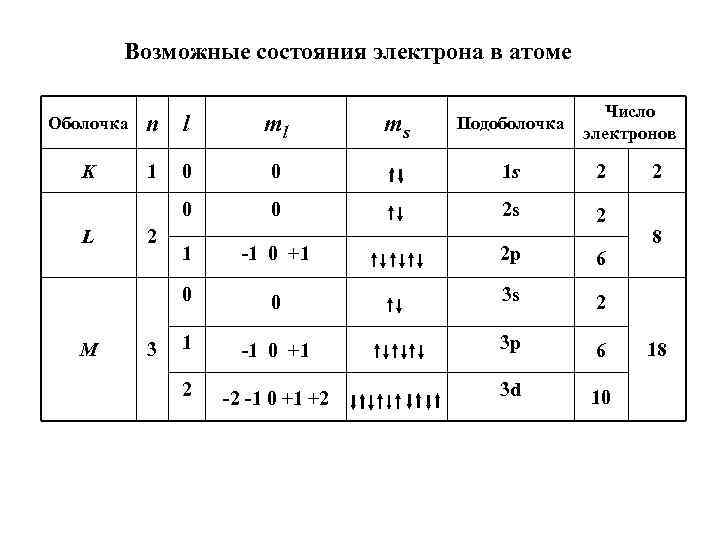 Возможные состояния электрона в атоме n l ml K 1 0 0 1 s 2 0 0 2 s 2 L 2 ms Число электронов Оболочка Подоболочка 3 -1 0 +1 2 p 6 0 M 1 0 3 s -1 0 +1 3 p 6 2 -2 -1 0 +1 +2 3 d 10 8 2 18
Возможные состояния электрона в атоме n l ml K 1 0 0 1 s 2 0 0 2 s 2 L 2 ms Число электронов Оболочка Подоболочка 3 -1 0 +1 2 p 6 0 M 1 0 3 s -1 0 +1 3 p 6 2 -2 -1 0 +1 +2 3 d 10 8 2 18
 Структура электронных оболочек атомов Z=1 H n = 1, l = 0, ml = 0 1 s 1 Z = 2 He 1 s 2 Z = 3 Li 1 s 2 2 s 1 Z = 4 Be 1 s 2 2 s 2 Z = 10 Ne 1 s 2 2 s 22 p 6
Структура электронных оболочек атомов Z=1 H n = 1, l = 0, ml = 0 1 s 1 Z = 2 He 1 s 2 Z = 3 Li 1 s 2 2 s 1 Z = 4 Be 1 s 2 2 s 2 Z = 10 Ne 1 s 2 2 s 22 p 6