 «Магний»
«Магний»
 Электронное строение атома Mg 24 +12 Mg 0 2 e p+ = 12 e- = 12 n 0 = 12 8 e Порядок заполнения 2 e 3 s 2 2 p 6 1 s 2 Краткая электронная запись 2
Электронное строение атома Mg 24 +12 Mg 0 2 e p+ = 12 e- = 12 n 0 = 12 8 e Порядок заполнения 2 e 3 s 2 2 p 6 1 s 2 Краткая электронная запись 2
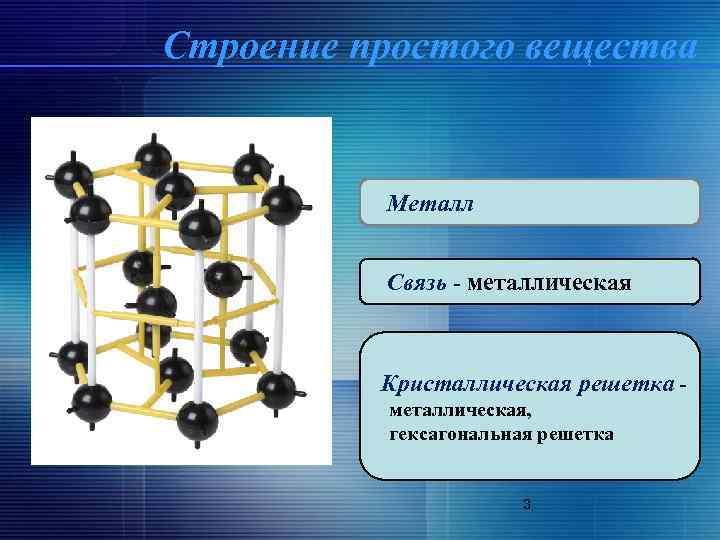 Строение простого вещества Металл Связь - металлическая Кристаллическая решетка металлическая, гексагональная решетка 3
Строение простого вещества Металл Связь - металлическая Кристаллическая решетка металлическая, гексагональная решетка 3
 Физические свойства Mg Цвет – блестящий, серебристо-белый t пл. = 651°C. t кип. ≈ 1107°C. Электропроводный Легкий, плотность ρ = 1, 74 г/см 3 Относительно мягкий, пластичный. 4
Физические свойства Mg Цвет – блестящий, серебристо-белый t пл. = 651°C. t кип. ≈ 1107°C. Электропроводный Легкий, плотность ρ = 1, 74 г/см 3 Относительно мягкий, пластичный. 4
 Химические свойства Mg C неметаллами ( кислородом, серой) C неметаллами ( галогенами, азотом) C водой C кислотами C оксидами металлов Mg ++2 HCl O=Mg Cl 2 + H 2↑ 4 Mg. Mg++ 422=4 Mg. Cl+ 3 Fe Fe 3 Cl= =Mg O 2 2 Mg O 2 Mg. O t Mg + 2 H 2 4=4 Mg. SO 4+H + H 2↑ 4 Mg+5 H 2 SOO = Mg(OH)2 2 S+4 H 2 O Mg O S = Mg 3 3 Mg + Al 2+ N== Mg ON 2 2 Al 3 Mg + 3 2 3 Mg S + 5
Химические свойства Mg C неметаллами ( кислородом, серой) C неметаллами ( галогенами, азотом) C водой C кислотами C оксидами металлов Mg ++2 HCl O=Mg Cl 2 + H 2↑ 4 Mg. Mg++ 422=4 Mg. Cl+ 3 Fe Fe 3 Cl= =Mg O 2 2 Mg O 2 Mg. O t Mg + 2 H 2 4=4 Mg. SO 4+H + H 2↑ 4 Mg+5 H 2 SOO = Mg(OH)2 2 S+4 H 2 O Mg O S = Mg 3 3 Mg + Al 2+ N== Mg ON 2 2 Al 3 Mg + 3 2 3 Mg S + 5
 Горение Mg в кислороде 2 Mg + O 2 = 2 Mg. O 6
Горение Mg в кислороде 2 Mg + O 2 = 2 Mg. O 6
 Горение Mg в воде Что будет, если тушить магний водой? На заводе по переработке вторичного сырья в Уолтон Хиллс, штат Огайо возник пожар. В здании было большое количество металлов, среди них титан, сталь и магний. Пожарные, опасаясь, что огонь перекинется на соседнюю бензозаправку решили залить горящее здание водой. Результат не заставил себя ждать - произошел сильный взрыв, во все стороны разлетелись куски раскаленного добела магния. Ослепительный огонь поднялся на высоту 50 м. Однако пожарных это ни чему не научило - они продолжили заливать здание, что вызвало новые взрывы магния. Пожарные вынуждены были отступать под дождем горящего магния. От жара огня начали плавиться стены здания. Единственный способ погасить пожар магния - засыпать металл большим количеством песка, что было в данном случае технически невозможно, но это не повод заливать горящий магний водой. Некомпетентные действия пожарных значительно усугубили масштаб аварии. Mg + 2 H 2 O = Mg(OH)2 + H 2 7
Горение Mg в воде Что будет, если тушить магний водой? На заводе по переработке вторичного сырья в Уолтон Хиллс, штат Огайо возник пожар. В здании было большое количество металлов, среди них титан, сталь и магний. Пожарные, опасаясь, что огонь перекинется на соседнюю бензозаправку решили залить горящее здание водой. Результат не заставил себя ждать - произошел сильный взрыв, во все стороны разлетелись куски раскаленного добела магния. Ослепительный огонь поднялся на высоту 50 м. Однако пожарных это ни чему не научило - они продолжили заливать здание, что вызвало новые взрывы магния. Пожарные вынуждены были отступать под дождем горящего магния. От жара огня начали плавиться стены здания. Единственный способ погасить пожар магния - засыпать металл большим количеством песка, что было в данном случае технически невозможно, но это не повод заливать горящий магний водой. Некомпетентные действия пожарных значительно усугубили масштаб аварии. Mg + 2 H 2 O = Mg(OH)2 + H 2 7
 Горение Mg в хлоре Mg + Cl 2 = Mg. Cl 2 8
Горение Mg в хлоре Mg + Cl 2 = Mg. Cl 2 8
 Вспышка смеси Mg + Ag. NO 3 от капли воды 3 Mg + Ag. NO 3 = 3 Mg. O + 0. 5 N 2 + Ag 9
Вспышка смеси Mg + Ag. NO 3 от капли воды 3 Mg + Ag. NO 3 = 3 Mg. O + 0. 5 N 2 + Ag 9
 Лабораторная работа: «Горение магния на воздухе» 2 Mg + O 2 = 2 Mg. O 10
Лабораторная работа: «Горение магния на воздухе» 2 Mg + O 2 = 2 Mg. O 10
 Магнийтермия – получение металлов восстановлением оксидов металлов магнием, которое сопровождается выделением значительного количества теплоты. 4 Mg+ Fe 3 O 4 = 4 Mg. O + 3 Fe 3 Mg + Al 2 O 3 = 3 Mg. O + 2 Al 11
Магнийтермия – получение металлов восстановлением оксидов металлов магнием, которое сопровождается выделением значительного количества теплоты. 4 Mg+ Fe 3 O 4 = 4 Mg. O + 3 Fe 3 Mg + Al 2 O 3 = 3 Mg. O + 2 Al 11
 Нахождение Mg в земной коре Сульфаты Кизерит Mg. SO 4×H 2 O (17, 6% Mg) Лангбейнит 2 Mg. SO 4×K 2 SO 4 (11, 7% Mg) Каинит Mg. SO 4×KCI× 3 H 2 O (9, 8% Mg) Карбонаты Магнезит Mg. CO 3 (28, 8% Mg) Доломит Mg. CO 3×Ca. CO 3 (18, 2% Mg) Брусит Mg(OH)2 (Mg 41, 7%) Бишофит Mg. Cl 2× 6 H 2 O (12, 0% Mg) 12
Нахождение Mg в земной коре Сульфаты Кизерит Mg. SO 4×H 2 O (17, 6% Mg) Лангбейнит 2 Mg. SO 4×K 2 SO 4 (11, 7% Mg) Каинит Mg. SO 4×KCI× 3 H 2 O (9, 8% Mg) Карбонаты Магнезит Mg. CO 3 (28, 8% Mg) Доломит Mg. CO 3×Ca. CO 3 (18, 2% Mg) Брусит Mg(OH)2 (Mg 41, 7%) Бишофит Mg. Cl 2× 6 H 2 O (12, 0% Mg) 12
 Получение Mg 1830 год М. Фарадей: Mg. Cl 2 = Mg + Cl 2 В 1852 году метод был усовершенствован Р. Бунзеном В России электролитический метод получения магния впервые разработал П. П. Федотьев в 1914 г. в Петроградском политехническом институте 13
Получение Mg 1830 год М. Фарадей: Mg. Cl 2 = Mg + Cl 2 В 1852 году метод был усовершенствован Р. Бунзеном В России электролитический метод получения магния впервые разработал П. П. Федотьев в 1914 г. в Петроградском политехническом институте 13
 Применение Mg и его сплавов 14
Применение Mg и его сплавов 14
 Выводы Магний – химический элемент II группы ПСХЭ Д. И. Менделеева, в химическом отношении – весьма активный металл, соединения магния имеют основной характер. Магний – характерный элемент мантии Земли, минералы магния многочисленны. Более половины из них образовались в биосфере – на дне морей, озер, в почвах. В промышленности наибольшее количество магния получают электролизом расплава хлорида магния. Широко применяются сплавы магния в промышленности. Магний – постоянная часть растительных и животных организмов. Из препаратов магния в медицинской практике применяют: сульфат магния (как успокаивающее, противосудорожное, спазмолитическое, слабительное и желчегонное средство), магнезию жженую (магния оксид) и карбонат магния (легкое слабительное). 15
Выводы Магний – химический элемент II группы ПСХЭ Д. И. Менделеева, в химическом отношении – весьма активный металл, соединения магния имеют основной характер. Магний – характерный элемент мантии Земли, минералы магния многочисленны. Более половины из них образовались в биосфере – на дне морей, озер, в почвах. В промышленности наибольшее количество магния получают электролизом расплава хлорида магния. Широко применяются сплавы магния в промышленности. Магний – постоянная часть растительных и животных организмов. Из препаратов магния в медицинской практике применяют: сульфат магния (как успокаивающее, противосудорожное, спазмолитическое, слабительное и желчегонное средство), магнезию жженую (магния оксид) и карбонат магния (легкое слабительное). 15


