Luminescence.ppt
- Количество слайдов: 77
 Люминесценция: основные понятия ■ Упоминание о люминесценции датируется XV веком, когда было описано свечение неорганических кристаллов. Возникновение люминесценции многие связывают с моментом выхода работы Давида Брустера, который в 1833 году описал красную флуоресценцию хлорофилла. ■ The Hound of the Baskervilles (Конан Дойл Артур).
Люминесценция: основные понятия ■ Упоминание о люминесценции датируется XV веком, когда было описано свечение неорганических кристаллов. Возникновение люминесценции многие связывают с моментом выхода работы Давида Брустера, который в 1833 году описал красную флуоресценцию хлорофилла. ■ The Hound of the Baskervilles (Конан Дойл Артур).
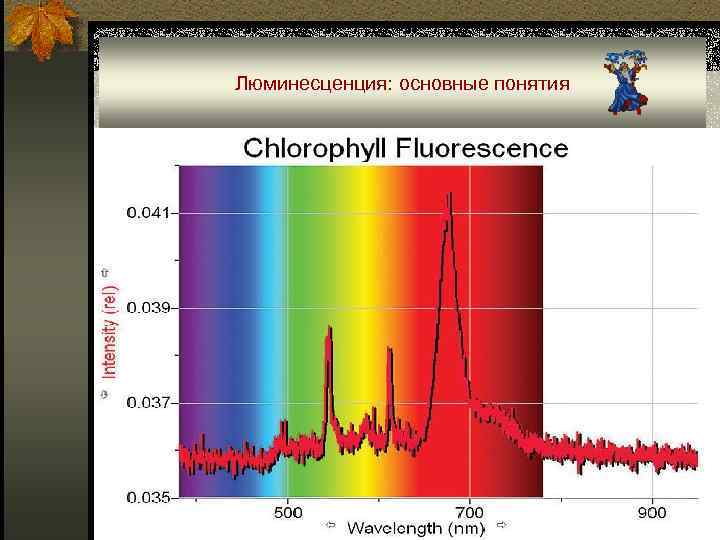 Люминесценция: основные понятия
Люминесценция: основные понятия
 Люминесцения : основные понятия ■ Итак, что такое люминесценция? Определение этого понятия довольно сложно и исходит из сопоставления свойств люминесцентного излучения и законов теплового равновесного излучения. Под тепловым излучением понимают электромагнитное излучение, обусловленное возбуждением частиц вещества (атомов, молекул, ионов) вследствие их теплового движения. Чтобы вызвать люминесценцию вещества к нему необходимо подвести извне определенное количество энергии. ■ Люминесценция – это свечение атомов, молекул и других более сложных комплексов, возникающего в результате электронного перехода в этих частицах при их возвращении из возбужденного состояния в нормальное (В. Л. Левшин).
Люминесцения : основные понятия ■ Итак, что такое люминесценция? Определение этого понятия довольно сложно и исходит из сопоставления свойств люминесцентного излучения и законов теплового равновесного излучения. Под тепловым излучением понимают электромагнитное излучение, обусловленное возбуждением частиц вещества (атомов, молекул, ионов) вследствие их теплового движения. Чтобы вызвать люминесценцию вещества к нему необходимо подвести извне определенное количество энергии. ■ Люминесценция – это свечение атомов, молекул и других более сложных комплексов, возникающего в результате электронного перехода в этих частицах при их возвращении из возбужденного состояния в нормальное (В. Л. Левшин).
 Люминесцения : основные понятия ■ Люминесценция – это излучение (B`v, T), представляющее собой избыток над тепловым излучением (Bv, T) вещества при данной температуре и имеющее длительность (>10 -10 c), значительно превышающую период световых волн (Видеман - Вавилов).
Люминесцения : основные понятия ■ Люминесценция – это излучение (B`v, T), представляющее собой избыток над тепловым излучением (Bv, T) вещества при данной температуре и имеющее длительность (>10 -10 c), значительно превышающую период световых волн (Видеман - Вавилов).
 Классификация видов люминесценции n По длительности свечения: флуоресценция (~10 -8 c), фосфоресценция (>10 -6 с). n По способу возбуждения (таблица). n По механизму свечения: • свечение дискретных центров – поглощающими и излучающими центрами являются одни и те же частицы (атомы, молекулы, ионы); • рекомбинационное свечение – процессы поглощения и излучения разделены во времени и в пространстве. В процессе возбуждения происходит разделение частицы вещества на две противоположно заряженные части. Последующая их рекомбинация сопровождается выделением энергии.
Классификация видов люминесценции n По длительности свечения: флуоресценция (~10 -8 c), фосфоресценция (>10 -6 с). n По способу возбуждения (таблица). n По механизму свечения: • свечение дискретных центров – поглощающими и излучающими центрами являются одни и те же частицы (атомы, молекулы, ионы); • рекомбинационное свечение – процессы поглощения и излучения разделены во времени и в пространстве. В процессе возбуждения происходит разделение частицы вещества на две противоположно заряженные части. Последующая их рекомбинация сопровождается выделением энергии.
 Классификация методов люминесценции по способам возбуждения
Классификация методов люминесценции по способам возбуждения
 Люминесценция дискретных центров
Люминесценция дискретных центров
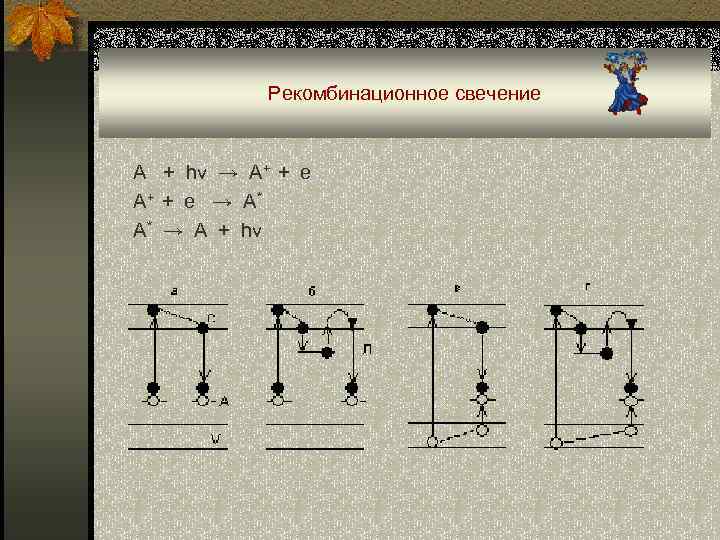 Рекомбинационное свечение А + hv → A+ + e → A* A* → A + hv
Рекомбинационное свечение А + hv → A+ + e → A* A* → A + hv
 Основные характеристики люминесценции n Спектры поглощения: A = f(λ); A = f(v); T, % = f(λ); T, % = f(v). n Cпектры люминесценции: I = f(λ); I = f(v). n Спектры возбуждения: зависимости интенсивности люминесценции (I) от частоты (волнового числа) или длины волны возбуждающего света; у частиц, люминесцирующих по типу дискретных центров, спектры возбуждения идентичны спектрам поглощения. n Энергетический выход люминесценции. n Квантовый выход люминесценции. n Время жизни возбужденного люминесцентного центра.
Основные характеристики люминесценции n Спектры поглощения: A = f(λ); A = f(v); T, % = f(λ); T, % = f(v). n Cпектры люминесценции: I = f(λ); I = f(v). n Спектры возбуждения: зависимости интенсивности люминесценции (I) от частоты (волнового числа) или длины волны возбуждающего света; у частиц, люминесцирующих по типу дискретных центров, спектры возбуждения идентичны спектрам поглощения. n Энергетический выход люминесценции. n Квантовый выход люминесценции. n Время жизни возбужденного люминесцентного центра.
 Фотолюминесцеция
Фотолюминесцеция
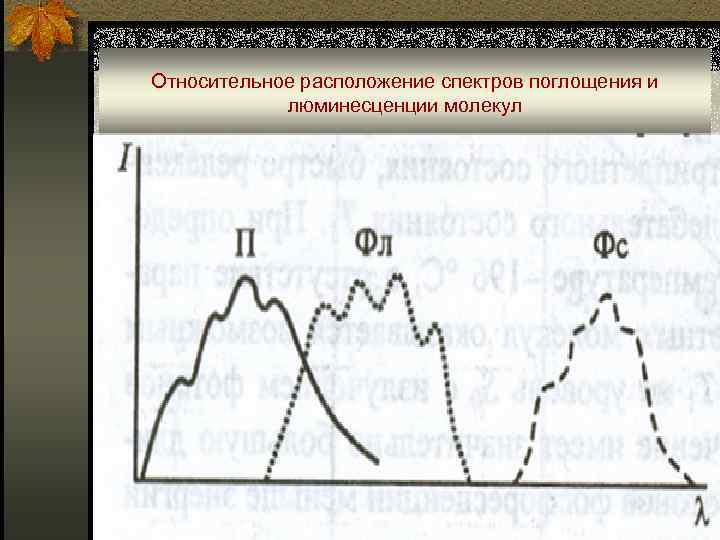 Относительное расположение спектров поглощения и люминесценции молекул
Относительное расположение спектров поглощения и люминесценции молекул
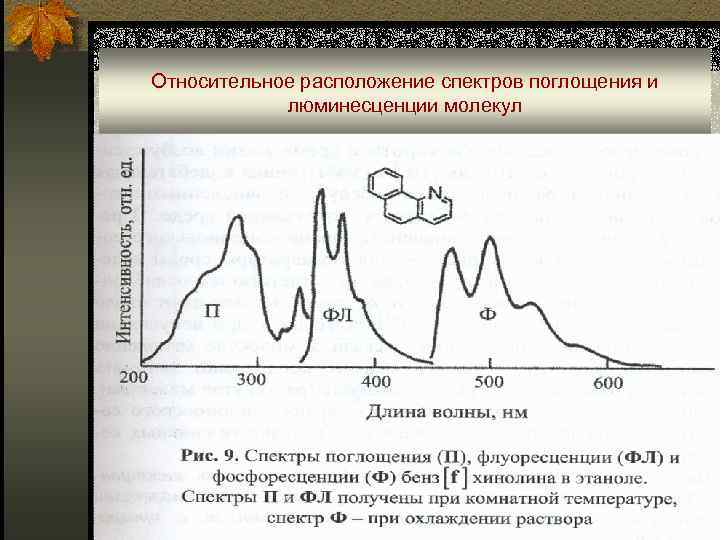 Относительное расположение спектров поглощения и люминесценции молекул
Относительное расположение спектров поглощения и люминесценции молекул
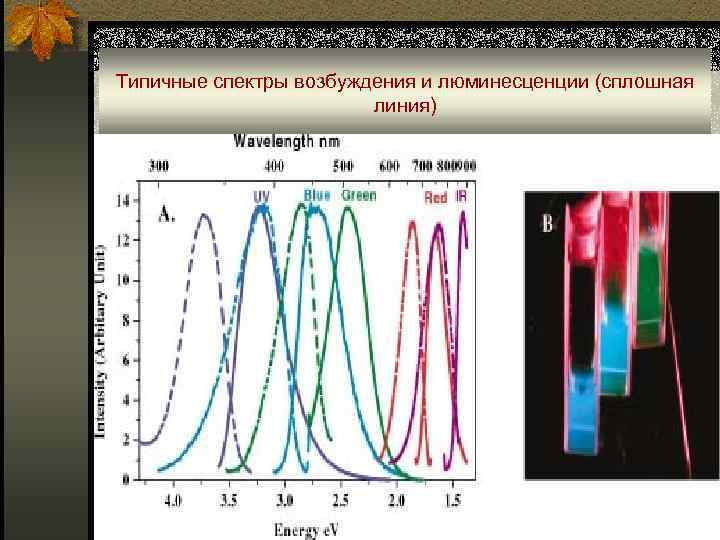 Типичные спектры возбуждения и люминесценции (сплошная линия)
Типичные спектры возбуждения и люминесценции (сплошная линия)
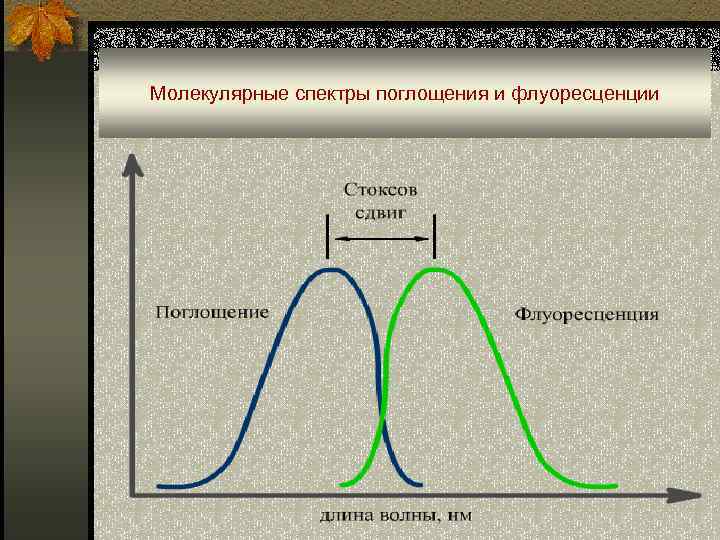 Молекулярные спектры поглощения и флуоресценции
Молекулярные спектры поглощения и флуоресценции
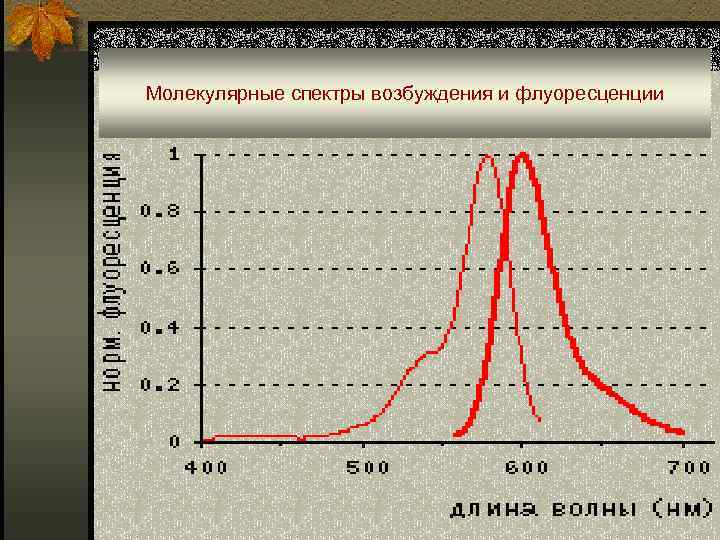 Молекулярные спектры возбуждения и флуоресценции
Молекулярные спектры возбуждения и флуоресценции
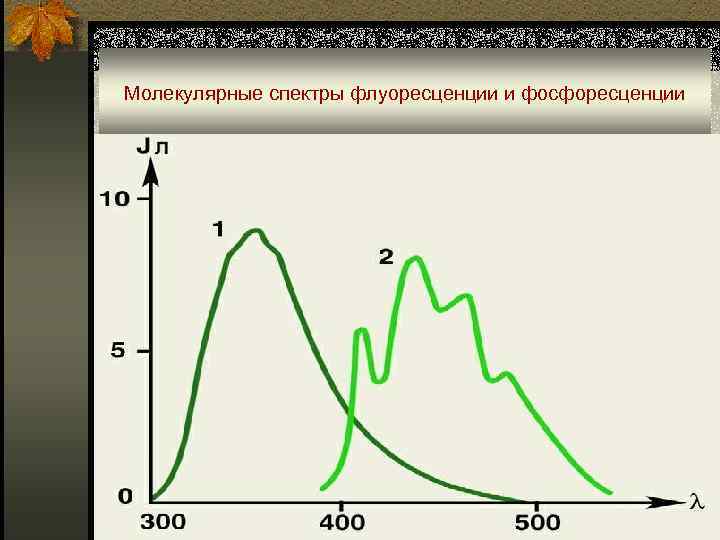 Молекулярные спектры флуоресценции и фосфоресценции
Молекулярные спектры флуоресценции и фосфоресценции
 Выход люминесценции n Способность вещества к люминесценции в данной среде характеризуется величиной выхода люминесценции. n Различают абсолютный квантовый и энергетический выходы люминесценции и относительный выход люминесценции. n Абсолютным квантовым выходом люминесценции (φкв) называют отношение числа квантов Nл, излученных веществом, к числу поглощенных квантов возбуждающего света Nп: φкв = Nл / Nп ■ φкв определяется соотношением между вероятностями излучательного (α) и безызлучательного (β): φкв = α / α + β
Выход люминесценции n Способность вещества к люминесценции в данной среде характеризуется величиной выхода люминесценции. n Различают абсолютный квантовый и энергетический выходы люминесценции и относительный выход люминесценции. n Абсолютным квантовым выходом люминесценции (φкв) называют отношение числа квантов Nл, излученных веществом, к числу поглощенных квантов возбуждающего света Nп: φкв = Nл / Nп ■ φкв определяется соотношением между вероятностями излучательного (α) и безызлучательного (β): φкв = α / α + β
 Выход люминесценции n Абсолютным энергетическим выходом люминесценции (φэн) называют отношение излучаемой веществом энергии Ел к поглощенной энергии возбуждения Еп: φэн = Ел / Еп ■ Абсолютный энергетический и квантовые выходы связаны простым соотношением: φэн = Ел / Еп = Nл • hvл / Nп • hvп = φкв • (vл / vп) или φэн = φкв • (λп / λл); φкв = φэн • (λл / λп) ■ Измерение абсолютных выходов люминесценции представляет трудную задачу, поэтому на практике чаще измеряют относительный выход люминесценции.
Выход люминесценции n Абсолютным энергетическим выходом люминесценции (φэн) называют отношение излучаемой веществом энергии Ел к поглощенной энергии возбуждения Еп: φэн = Ел / Еп ■ Абсолютный энергетический и квантовые выходы связаны простым соотношением: φэн = Ел / Еп = Nл • hvл / Nп • hvп = φкв • (vл / vп) или φэн = φкв • (λп / λл); φкв = φэн • (λл / λп) ■ Измерение абсолютных выходов люминесценции представляет трудную задачу, поэтому на практике чаще измеряют относительный выход люминесценции.
 Время жизни возбужденного люминесцентного центра n В случае люминесцентных дискретных центров число возбужденных центров n после прекращения возбуждения в отсутствии безызлучательных процессов дезактивации будет уменьшаться со временем: -dn/dt = k 1 n, где k 1 – константа скорости мономолекулярного излучательного процесса. ■ Среднее излучательное время жизни (τ0) люминесцентного центра определяется выражением: τ0 = 1/ k 1
Время жизни возбужденного люминесцентного центра n В случае люминесцентных дискретных центров число возбужденных центров n после прекращения возбуждения в отсутствии безызлучательных процессов дезактивации будет уменьшаться со временем: -dn/dt = k 1 n, где k 1 – константа скорости мономолекулярного излучательного процесса. ■ Среднее излучательное время жизни (τ0) люминесцентного центра определяется выражением: τ0 = 1/ k 1
 Время жизни возбужденного люминесцентного центра n Для грубых оценок применимо соотношение: 10 -4 τ0 ≈ ———— ε(λmax) n Таким образом, среднее излучательное время жизни возбужденного состояния тем меньше, чем интенсивнее поглощение, приводящее к его возникновению. n Поскольку имеют место безызлучательные процессы, измеряемые времена жизни τ всегда меньше τ0 : 1 τ = —————— k 1 + k 2 + k 3
Время жизни возбужденного люминесцентного центра n Для грубых оценок применимо соотношение: 10 -4 τ0 ≈ ———— ε(λmax) n Таким образом, среднее излучательное время жизни возбужденного состояния тем меньше, чем интенсивнее поглощение, приводящее к его возникновению. n Поскольку имеют место безызлучательные процессы, измеряемые времена жизни τ всегда меньше τ0 : 1 τ = —————— k 1 + k 2 + k 3
 Энергетические переходы в молекуле n При комнатной температуре молекула обычно находится в n n основном S 0 синглетном состоянии. При поглощении энергии молекула оказывается в возбужденном электронном состоянии S 2. Далее практически мгновенно (~10 -12 с) в результате колебательной релаксации (КР) достигается невозбужденный колебательный уровень S 2. Далее также практически мгновенно (~10 -11 с) вследствие внутренней конверсии молекула перейдет в более низкое электронно-возбужденное состояние S 1. Переход S 1 → S 0 с испусканием фотона (10 -6 - 10 -9 с) – флуоресценция.
Энергетические переходы в молекуле n При комнатной температуре молекула обычно находится в n n основном S 0 синглетном состоянии. При поглощении энергии молекула оказывается в возбужденном электронном состоянии S 2. Далее практически мгновенно (~10 -12 с) в результате колебательной релаксации (КР) достигается невозбужденный колебательный уровень S 2. Далее также практически мгновенно (~10 -11 с) вследствие внутренней конверсии молекула перейдет в более низкое электронно-возбужденное состояние S 1. Переход S 1 → S 0 с испусканием фотона (10 -6 - 10 -9 с) – флуоресценция.
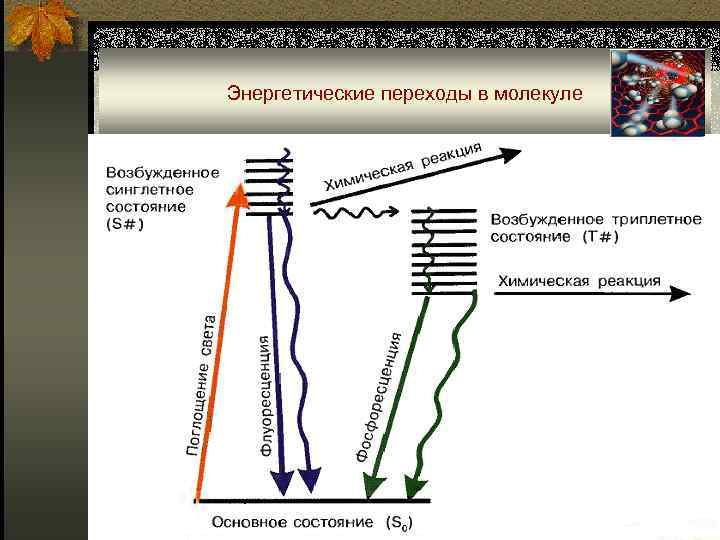 Энергетические переходы в молекуле
Энергетические переходы в молекуле
 Энергетические переходы в молекуле
Энергетические переходы в молекуле
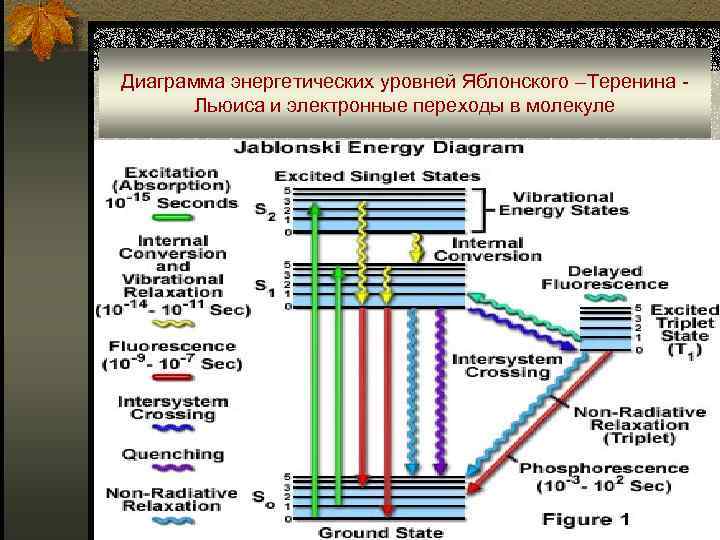 Диаграмма энергетических уровней Яблонского –Теренина - Льюиса и электронные переходы в молекуле
Диаграмма энергетических уровней Яблонского –Теренина - Льюиса и электронные переходы в молекуле
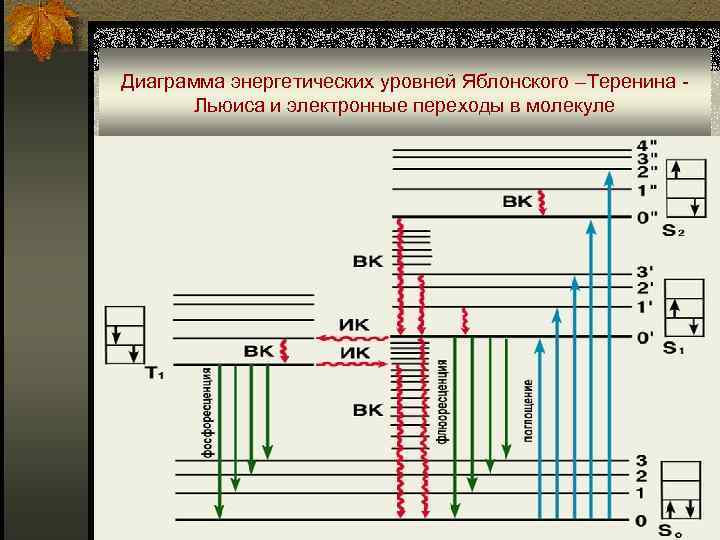 Диаграмма энергетических уровней Яблонского –Теренина - Льюиса и электронные переходы в молекуле
Диаграмма энергетических уровней Яблонского –Теренина - Льюиса и электронные переходы в молекуле
 Энергетические переходы в молекуле ■ Безызлучательный переход S 1 → T 1 с изменением спина электрона – интеркомбинационная конверсия. n Переход T 1 → S 0 с испусканием фотона (>10 -4 c) – фосфоресценция.
Энергетические переходы в молекуле ■ Безызлучательный переход S 1 → T 1 с изменением спина электрона – интеркомбинационная конверсия. n Переход T 1 → S 0 с испусканием фотона (>10 -4 c) – фосфоресценция.
 Замедленная флуоресценция n Помимо флуоресценции и фосфоресценции существует еще один вид люминесценции – замедленная флуоресценция. n Этот вид молекулярной люминесценции наблюдается в весьма ограниченных диапазонах температур, вязкостей и концентраций растворов. n По сравнению с флуоресценцией и фосфоресценцией ее интенсивность невелика и достигает максимальных значений при комнатной и более высоких температурах, заметно ослабевая с понижением температуры. n Различают замедленную флуоресценцию Е – типа.
Замедленная флуоресценция n Помимо флуоресценции и фосфоресценции существует еще один вид люминесценции – замедленная флуоресценция. n Этот вид молекулярной люминесценции наблюдается в весьма ограниченных диапазонах температур, вязкостей и концентраций растворов. n По сравнению с флуоресценцией и фосфоресценцией ее интенсивность невелика и достигает максимальных значений при комнатной и более высоких температурах, заметно ослабевая с понижением температуры. n Различают замедленную флуоресценцию Е – типа.
 Замедленная флуоресценция Е - типа n Замедленная флуоресценция Е – типа: за счет термической активации молекул в состоянии Т 1 происходит их переход на более высокие колебательные уровни, которые могут перекрываться с колебательными уровнями S 1 и и становится возможным переход Т 1 → S 1.
Замедленная флуоресценция Е - типа n Замедленная флуоресценция Е – типа: за счет термической активации молекул в состоянии Т 1 происходит их переход на более высокие колебательные уровни, которые могут перекрываться с колебательными уровнями S 1 и и становится возможным переход Т 1 → S 1.
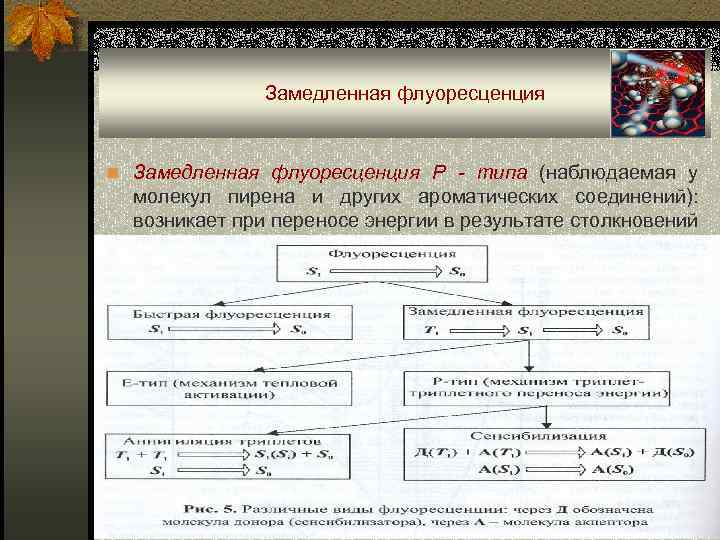 Замедленная флуоресценция n Замедленная флуоресценция Р - типа (наблюдаемая у молекул пирена и других ароматических соединений): возникает при переносе энергии в результате столкновений
Замедленная флуоресценция n Замедленная флуоресценция Р - типа (наблюдаемая у молекул пирена и других ароматических соединений): возникает при переносе энергии в результате столкновений
 Диаграмма потенциальной энергии n При рассмотрении люминесценции полезно рассмотрение диаграммы потенциальной энергии. n Ограничимся двумерными диаграммами, относящимися, строго говоря, к случаю двухатомной молекулы.
Диаграмма потенциальной энергии n При рассмотрении люминесценции полезно рассмотрение диаграммы потенциальной энергии. n Ограничимся двумерными диаграммами, относящимися, строго говоря, к случаю двухатомной молекулы.
 Диаграмма потенциальной энергии n Кривые потенциальной энергии состояний S 1 и T 1 пересекаются в некоторой точке. n В этой точке положение и импульсы атомных ядер одни и те же, т. е. возможен S 1 → T 1 переход. n В сложных многоатомных молекулах многомерные потенциальные поверхности могут пересекаться во многих точках, что увеличивает вероятность ИК. n Принцип Франка – Кондона. Согласно этому принципу электронные переходы являются настолько быстрыми процессами (10 -13 с) по сравнению с движением ядер (10 -12 с), что за время электронного перехода ядра не успевают изменить ни своей скорости ни своего взаимного расположения.
Диаграмма потенциальной энергии n Кривые потенциальной энергии состояний S 1 и T 1 пересекаются в некоторой точке. n В этой точке положение и импульсы атомных ядер одни и те же, т. е. возможен S 1 → T 1 переход. n В сложных многоатомных молекулах многомерные потенциальные поверхности могут пересекаться во многих точках, что увеличивает вероятность ИК. n Принцип Франка – Кондона. Согласно этому принципу электронные переходы являются настолько быстрыми процессами (10 -13 с) по сравнению с движением ядер (10 -12 с), что за время электронного перехода ядра не успевают изменить ни своей скорости ни своего взаимного расположения.
 Принцип Франка - Кондона n Поэтому прежнее положение ядер будет соответствовать изменившимся в результате электронного перехода силам только в том случае, если молекула будет совершать достаточные колебания. n Так, при электронном возбуждении молекулы прочность связи мгновенно ослабевает, а ядра в первый момент продолжают занимать прежнее близкое друг к другу положение (сжатая молекула). n Такое несоответствие приводит к тому, что молекула начинает совершать колебания. n За короткое время жизни возбужденного состояния (10 -9 с) избыточная колебательная энергия успевает распределиться между многочисленными колебаниями молекулы или передаться окружающей среде.
Принцип Франка - Кондона n Поэтому прежнее положение ядер будет соответствовать изменившимся в результате электронного перехода силам только в том случае, если молекула будет совершать достаточные колебания. n Так, при электронном возбуждении молекулы прочность связи мгновенно ослабевает, а ядра в первый момент продолжают занимать прежнее близкое друг к другу положение (сжатая молекула). n Такое несоответствие приводит к тому, что молекула начинает совершать колебания. n За короткое время жизни возбужденного состояния (10 -9 с) избыточная колебательная энергия успевает распределиться между многочисленными колебаниями молекулы или передаться окружающей среде.
 Принцип Франка - Кондона n В результате молекула из неравновесного Франк – Кондоновского состояния переходит в равновесное, в котором ядра в соответствии с ослабленной связью разнесены друг от друга и совершают относительно этого положения колебания. n Далее – при испускании кванта люминесценции прочность связи в молекуле мгновенно усиливается, ядра же в первый момент продолжают занимать прежнее, далекое друг от друга положение (растянутая молекула). n И снова – переход из неравновесного Франк - Кондоновского состояния в равновесное осуществляется в результате колебаний.
Принцип Франка - Кондона n В результате молекула из неравновесного Франк – Кондоновского состояния переходит в равновесное, в котором ядра в соответствии с ослабленной связью разнесены друг от друга и совершают относительно этого положения колебания. n Далее – при испускании кванта люминесценции прочность связи в молекуле мгновенно усиливается, ядра же в первый момент продолжают занимать прежнее, далекое друг от друга положение (растянутая молекула). n И снова – переход из неравновесного Франк - Кондоновского состояния в равновесное осуществляется в результате колебаний.
 Принцип Франка - Кондона n Итак, согласно принципу Франка - Кондона, при электронном возбуждении внутримолекулярные связи, как правило, ослабляются. n Это приводит к тому, что минимум потенциальной кривой возбужденного состояния расположен при несколько большем межъядерном расстоянии, чем у основного состояния. n Как следует из квантовой механики, наиболее вероятное межъядерное расстояние для молекулы с нулевой колебательной энергией соответствует средней точке АВ или CD.
Принцип Франка - Кондона n Итак, согласно принципу Франка - Кондона, при электронном возбуждении внутримолекулярные связи, как правило, ослабляются. n Это приводит к тому, что минимум потенциальной кривой возбужденного состояния расположен при несколько большем межъядерном расстоянии, чем у основного состояния. n Как следует из квантовой механики, наиболее вероятное межъядерное расстояние для молекулы с нулевой колебательной энергией соответствует средней точке АВ или CD.
 Принцип Франка - Кондона n Наиболее вероятными будут переходы, отвечающие вертикальным линиям, проведенным из середины отрезков АВ (поглощение)или CD (испускание) до пересечения с соответствующими потенциальными кривыми:
Принцип Франка - Кондона n Наиболее вероятными будут переходы, отвечающие вертикальным линиям, проведенным из середины отрезков АВ (поглощение)или CD (испускание) до пересечения с соответствующими потенциальными кривыми:
 Принцип Франка - Кондона
Принцип Франка - Кондона
 Фотолюминесценция n Способность веществ к люминесценции, как и к поглощению излучения, связана с их электронным строением. n Например, если низшее возбужденное синглетное состояние органической молекулы обусловлено π → π* переходом, то она часто имеет высокие выходы и флуоресценции и фосфоресценции. n В тех же случаях, когда низшее возбужденное синглетное состояние возникает в результате n → π* перехода, то молекула обычно обладает малым выходом флуоресценции , но может обладать высоким выходом фосфоресценции при низкой температуре. n Обычно переход n → π* является наиболее длинноволновым переходом.
Фотолюминесценция n Способность веществ к люминесценции, как и к поглощению излучения, связана с их электронным строением. n Например, если низшее возбужденное синглетное состояние органической молекулы обусловлено π → π* переходом, то она часто имеет высокие выходы и флуоресценции и фосфоресценции. n В тех же случаях, когда низшее возбужденное синглетное состояние возникает в результате n → π* перехода, то молекула обычно обладает малым выходом флуоресценции , но может обладать высоким выходом фосфоресценции при низкой температуре. n Обычно переход n → π* является наиболее длинноволновым переходом.
 Электронная структура и оптические свойства молекулы (классификация Каши)
Электронная структура и оптические свойства молекулы (классификация Каши)
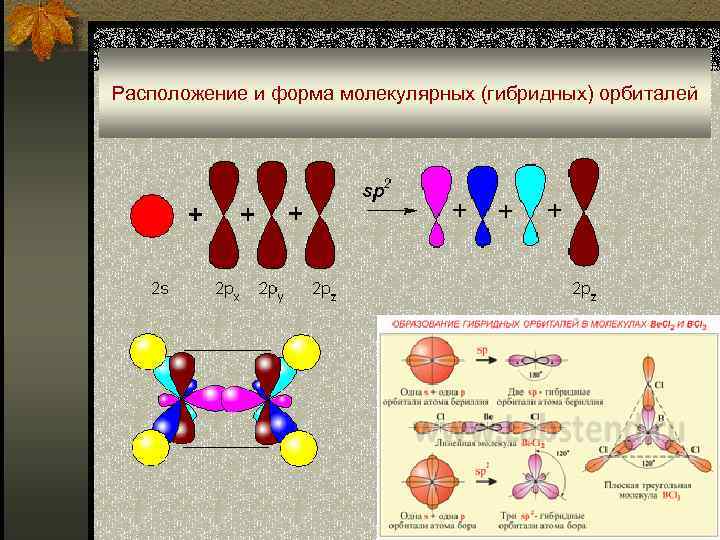 Расположение и форма молекулярных (гибридных) орбиталей
Расположение и форма молекулярных (гибридных) орбиталей
 Фотолюминесценция n Вероятность такого перехода мала (ε λmax ~ (1 - 2) • 103 M -1 • см-1), а время жизни возбужденного синглетного состояния n , π*, а значит и вероятность безызлучательной дезактивации велики. n Экспериментально установлено, что разница в энергиях S 1 ↔ T 1 для состояния n , π* в 2 - 4 раза меньше, чем для состояния π, π*. n Все это приводит к тому, что часто соединения, содержащие n - электроны, слабо или вовсе не флуоресцируют, но сильно фосфоресцируют.
Фотолюминесценция n Вероятность такого перехода мала (ε λmax ~ (1 - 2) • 103 M -1 • см-1), а время жизни возбужденного синглетного состояния n , π*, а значит и вероятность безызлучательной дезактивации велики. n Экспериментально установлено, что разница в энергиях S 1 ↔ T 1 для состояния n , π* в 2 - 4 раза меньше, чем для состояния π, π*. n Все это приводит к тому, что часто соединения, содержащие n - электроны, слабо или вовсе не флуоресцируют, но сильно фосфоресцируют.
 Электронная структура и оптические свойства молекулы (классификация Каши)
Электронная структура и оптические свойства молекулы (классификация Каши)
 Структура и оптические свойства молекул n Замечено, что наибольшей способностью к люминесценции обладают симметричные молекулы с протяженной системой сопряженных связей, склонные к образованию орто - и пара - хиноидных колец. n Одним из наиболее важных факторов, обуславливающих люминесценцию, является требование о наличии жесткой и плоской структуры. n По - видимому, относительное вращение частей «гибкой» молекулы возмущает электронные оболочки и облегчает безызлучательные переходы. n Например, известный гормон адреналин не люминесцирует, но при окислении превращается в ярко люминесцирующий триоксидон.
Структура и оптические свойства молекул n Замечено, что наибольшей способностью к люминесценции обладают симметричные молекулы с протяженной системой сопряженных связей, склонные к образованию орто - и пара - хиноидных колец. n Одним из наиболее важных факторов, обуславливающих люминесценцию, является требование о наличии жесткой и плоской структуры. n По - видимому, относительное вращение частей «гибкой» молекулы возмущает электронные оболочки и облегчает безызлучательные переходы. n Например, известный гормон адреналин не люминесцирует, но при окислении превращается в ярко люминесцирующий триоксидон.
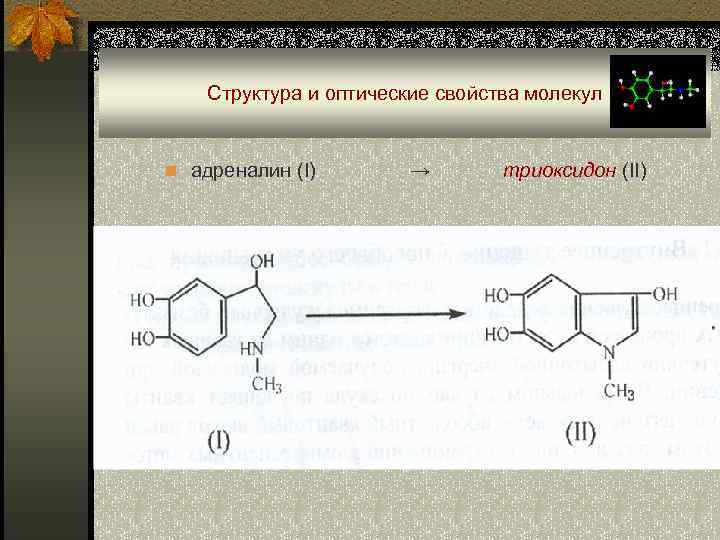 Структура и оптические свойства молекул n адреналин (I) → триоксидон (II)
Структура и оптические свойства молекул n адреналин (I) → триоксидон (II)
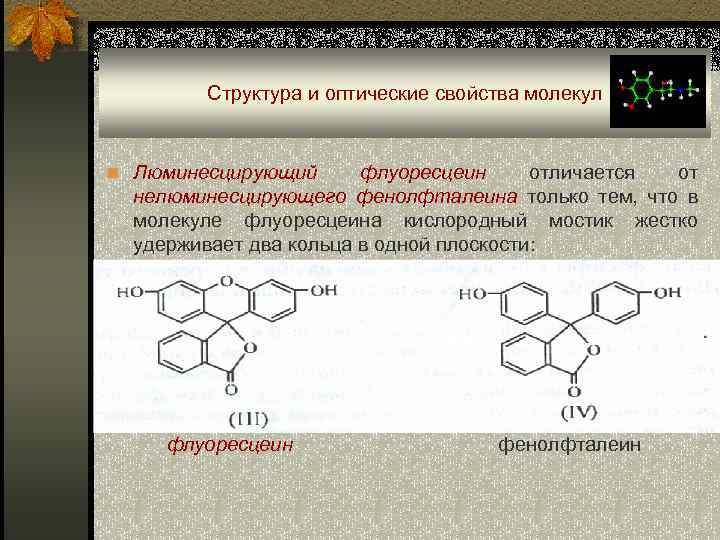 Структура и оптические свойства молекул n Люминесцирующий флуоресцеин отличается от нелюминесцирующего фенолфталеина только тем, что в молекуле флуоресцеина кислородный мостик жестко удерживает два кольца в одной плоскости: флуоресцеин фенолфталеин
Структура и оптические свойства молекул n Люминесцирующий флуоресцеин отличается от нелюминесцирующего фенолфталеина только тем, что в молекуле флуоресцеина кислородный мостик жестко удерживает два кольца в одной плоскости: флуоресцеин фенолфталеин
 Основные закономерности молекулярной люминесценции n Правило Каши: форма спектра люминесценции не зависит от длины волны возбуждающего света. n Закон Стокса - Ломмеля: спектр люминесценции в целом и его максимум сдвинут со спектром поглощения и его максимумом в длинноволновую область. n Правило Левшина (правило зеркальной симметрии): нормированные спектры поглощения и флуоресценции, представленные в виде графиков ε = f(v) и I/v = f(v), зеркально симметричны относительно прямой, перпендикулярной к оси частот и проходящей через точку пересечения спектров v 0.
Основные закономерности молекулярной люминесценции n Правило Каши: форма спектра люминесценции не зависит от длины волны возбуждающего света. n Закон Стокса - Ломмеля: спектр люминесценции в целом и его максимум сдвинут со спектром поглощения и его максимумом в длинноволновую область. n Правило Левшина (правило зеркальной симметрии): нормированные спектры поглощения и флуоресценции, представленные в виде графиков ε = f(v) и I/v = f(v), зеркально симметричны относительно прямой, перпендикулярной к оси частот и проходящей через точку пересечения спектров v 0.
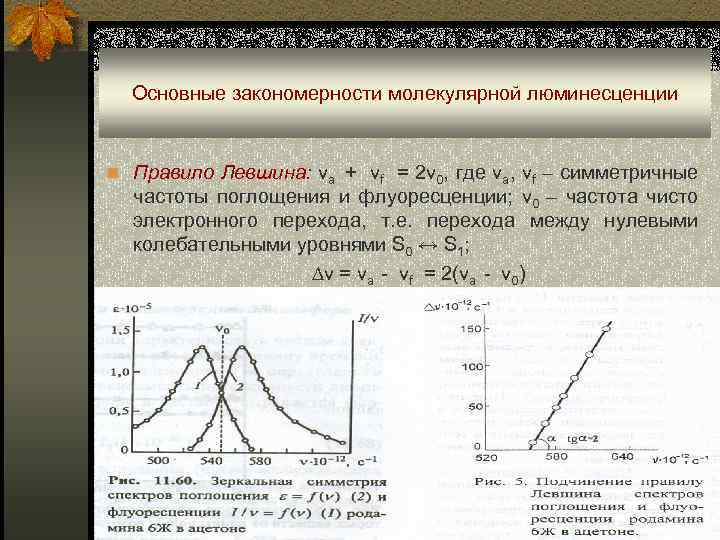 Основные закономерности молекулярной люминесценции n Правило Левшина: va + vf = 2 v 0, где va, vf – симметричные частоты поглощения и флуоресценции; v 0 – частота чисто электронного перехода, т. е. перехода между нулевыми колебательными уровнями S 0 ↔ S 1; ∆v = va - vf = 2(va - v 0)
Основные закономерности молекулярной люминесценции n Правило Левшина: va + vf = 2 v 0, где va, vf – симметричные частоты поглощения и флуоресценции; v 0 – частота чисто электронного перехода, т. е. перехода между нулевыми колебательными уровнями S 0 ↔ S 1; ∆v = va - vf = 2(va - v 0)
 Основные закономерности молекулярной люминесценции n Закон Вавилова: по мере увеличения λв энергетический выход флуоресценции возрастает, сохраняет постоянную величину и затем уменьшается.
Основные закономерности молекулярной люминесценции n Закон Вавилова: по мере увеличения λв энергетический выход флуоресценции возрастает, сохраняет постоянную величину и затем уменьшается.
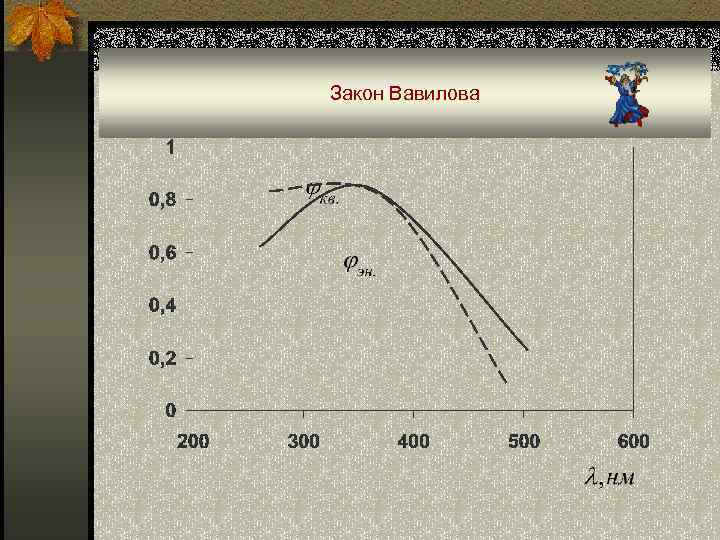 Закон Вавилова
Закон Вавилова
 Закон затухания люминесценции n Для интенсивности люминесценции Iл, определяемой скоростью испускания квантов люминесценции, имеем: dn Iл = - ——— = k 1 • n 0 • e-k 1 t = Iл 0 • e-k 1 t, dt где Iл 0 – интенсивность люминесценции в первый момент после прекращения возбуждения. n Таким образом, интенсивность люминесценции дискретного центра уменьшается со временем по экспоненциальному закону. n Затухание рекомбинационного свечения происходит по более сложному гиперболическому закону.
Закон затухания люминесценции n Для интенсивности люминесценции Iл, определяемой скоростью испускания квантов люминесценции, имеем: dn Iл = - ——— = k 1 • n 0 • e-k 1 t = Iл 0 • e-k 1 t, dt где Iл 0 – интенсивность люминесценции в первый момент после прекращения возбуждения. n Таким образом, интенсивность люминесценции дискретного центра уменьшается со временем по экспоненциальному закону. n Затухание рекомбинационного свечения происходит по более сложному гиперболическому закону.
 Зависимость интенсивности люминесценции от концентрации n При стационарном (непрерывном) возбуждении образца и отсутствии тушения: Iл = k 1 • φкв • Nп (Nп – число поглощенных квантов); Nп = k 2 • (I 0 – I); I = I 0 • 10 -εℓC; Iл = k • φкв • I 0 (1 - 10 -εℓC), где k – коэффициент пропорциональности; Разложение 10 -εℓC в ряд дает: (2, 3εℓC) 2 (2, 3εℓC)3 1 - 2, 3εℓC + ———— - ———— + ……. ; 2! 3!
Зависимость интенсивности люминесценции от концентрации n При стационарном (непрерывном) возбуждении образца и отсутствии тушения: Iл = k 1 • φкв • Nп (Nп – число поглощенных квантов); Nп = k 2 • (I 0 – I); I = I 0 • 10 -εℓC; Iл = k • φкв • I 0 (1 - 10 -εℓC), где k – коэффициент пропорциональности; Разложение 10 -εℓC в ряд дает: (2, 3εℓC) 2 (2, 3εℓC)3 1 - 2, 3εℓC + ———— - ———— + ……. ; 2! 3!
 Зависимость интенсивности люминесценции от концентрации ■ При εℓC ≤ 10 -2 вклад третьего и последующих членов разложения незначительны: Iл = 2, 3 • k • φкв • I 0 • ε • ℓ • C; Iл = k • C; обычно ε ~ 103 – 104, тогда при ℓ = 1 см Сi = 10 -5 – 10 -6 M
Зависимость интенсивности люминесценции от концентрации ■ При εℓC ≤ 10 -2 вклад третьего и последующих членов разложения незначительны: Iл = 2, 3 • k • φкв • I 0 • ε • ℓ • C; Iл = k • C; обычно ε ~ 103 – 104, тогда при ℓ = 1 см Сi = 10 -5 – 10 -6 M
 Причины отклонения зависимости Iл = k. C от линейности ■ Эффект внутреннего фильтра связан с поглощением части возбуждающего излучения при прохождении через слой люминофора; ■ Самопоглощение – поглощение люминофором части люминесцентного излучения; ■ Тушение люминесценции: • концентрационное тушение (образование нелюминесцирующих агрегатов, миграция энергии от возбужденных молекул к невозбужденным); • температурное тушение (внутримолекулярный процесс, обусловленный значительным увеличением колебательной энергии при повышении Т);
Причины отклонения зависимости Iл = k. C от линейности ■ Эффект внутреннего фильтра связан с поглощением части возбуждающего излучения при прохождении через слой люминофора; ■ Самопоглощение – поглощение люминофором части люминесцентного излучения; ■ Тушение люминесценции: • концентрационное тушение (образование нелюминесцирующих агрегатов, миграция энергии от возбужденных молекул к невозбужденным); • температурное тушение (внутримолекулярный процесс, обусловленный значительным увеличением колебательной энергии при повышении Т);
 Тушение люминесценции ■ Тушение люминесценции: • тушение посторонними веществами ( тяжелые ионы: I-, Br-, Cs+, Cu+; парамагнитные Mn 2+, O 2; молекулы растворителя); • статическое тушение (примесное вещество образует с невозбужденным люминофором нелюминесцирующие продукты); • динамическое тушение (примесное вещество образует с возбужденным люминофором нелюминесцирующие продукты).
Тушение люминесценции ■ Тушение люминесценции: • тушение посторонними веществами ( тяжелые ионы: I-, Br-, Cs+, Cu+; парамагнитные Mn 2+, O 2; молекулы растворителя); • статическое тушение (примесное вещество образует с невозбужденным люминофором нелюминесцирующие продукты); • динамическое тушение (примесное вещество образует с возбужденным люминофором нелюминесцирующие продукты).
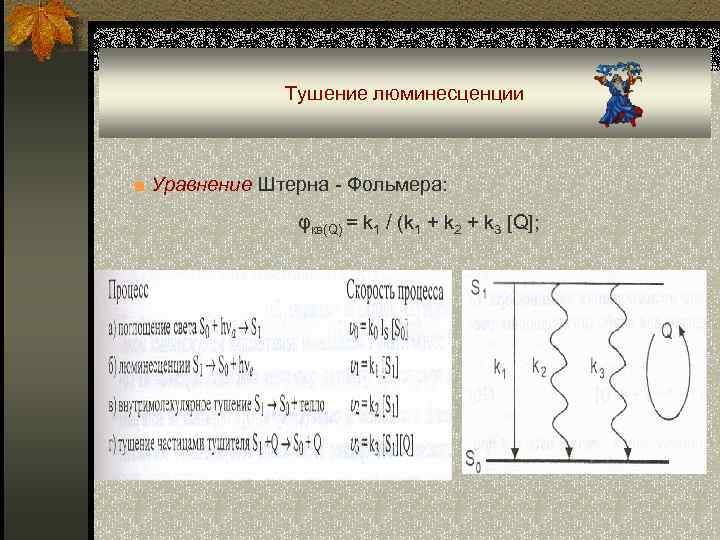 Тушение люминесценции ■ Уравнение Штерна - Фольмера: φкв(Q) = k 1 / (k 1 + k 2 + k 3 [Q];
Тушение люминесценции ■ Уравнение Штерна - Фольмера: φкв(Q) = k 1 / (k 1 + k 2 + k 3 [Q];
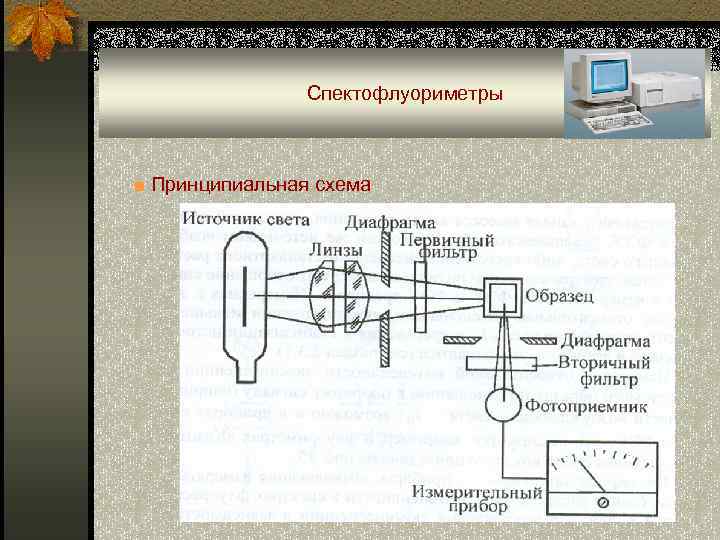 Спектофлуориметры ■ Принципиальная схема
Спектофлуориметры ■ Принципиальная схема
 Спектофлуориметры ■ Принципиальная схема
Спектофлуориметры ■ Принципиальная схема
 Практическое применение люминесценции ■ Принципиальная схема
Практическое применение люминесценции ■ Принципиальная схема
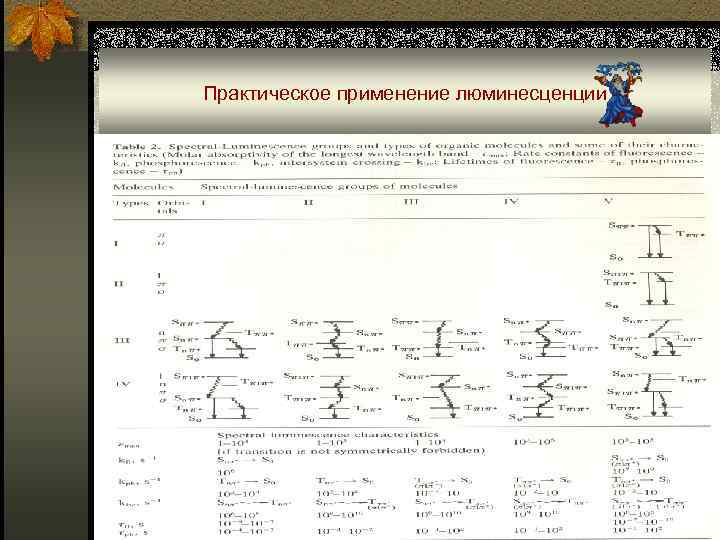 Практическое применение люминесценции ■ Принципиальная схема
Практическое применение люминесценции ■ Принципиальная схема
 Практическое применение люминесценции Флуориметрические определения: cобственная люминесценция (UO 22+, комплексные галогениды тяжелых металлов Tl+, Sn 2+, Sb 3+, Te(IV), Pb 2+, Bi 3+, In 3+ и др. , кристаллофосфоры, органические соединения); флуоресценция комплексных соединений ионов металлов с органическими реагентами. ■ Фосфориметрические определения. ■ Временная селекция. ■ Синхронное сканирование спектров (производные спектры). ■ Хемилюминесцентный анализ. ■
Практическое применение люминесценции Флуориметрические определения: cобственная люминесценция (UO 22+, комплексные галогениды тяжелых металлов Tl+, Sn 2+, Sb 3+, Te(IV), Pb 2+, Bi 3+, In 3+ и др. , кристаллофосфоры, органические соединения); флуоресценция комплексных соединений ионов металлов с органическими реагентами. ■ Фосфориметрические определения. ■ Временная селекция. ■ Синхронное сканирование спектров (производные спектры). ■ Хемилюминесцентный анализ. ■
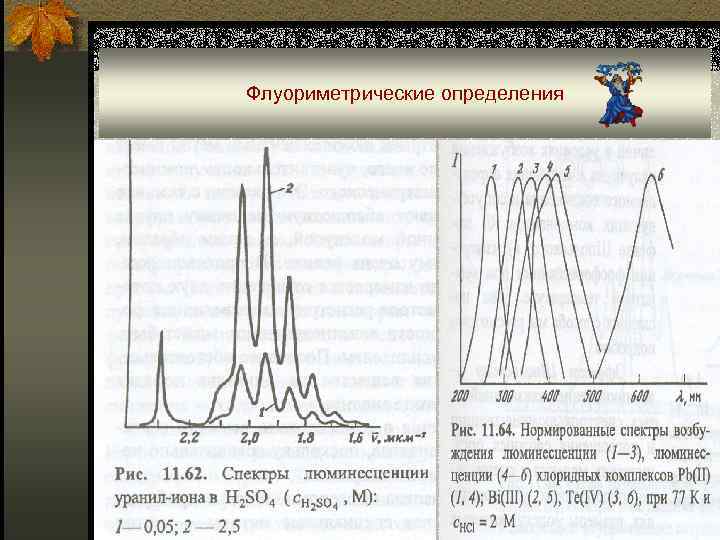 Флуориметрические определения
Флуориметрические определения
 Флуориметрические определения
Флуориметрические определения
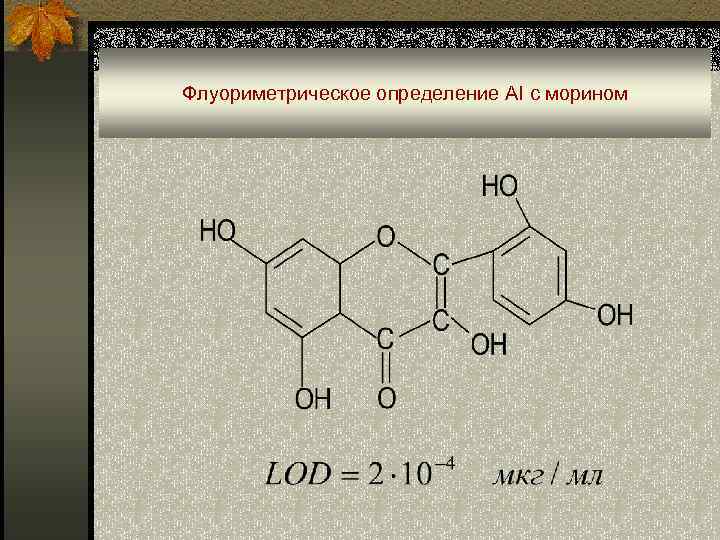 Флуориметрическое определение AI с морином
Флуориметрическое определение AI с морином
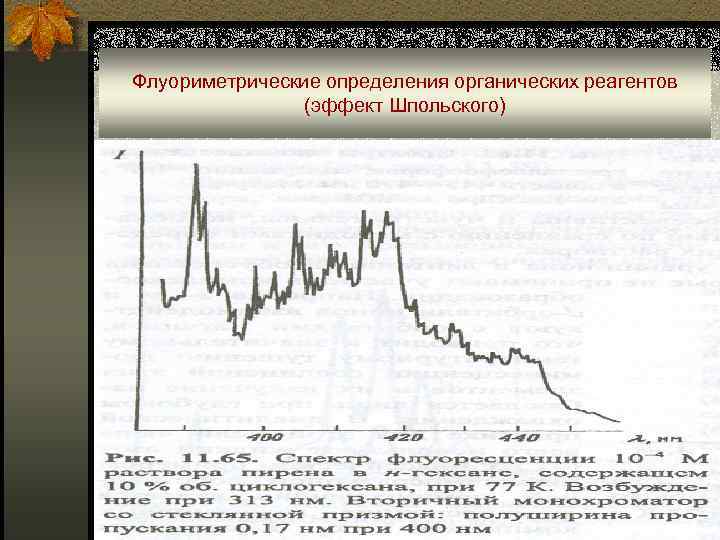 Флуориметрические определения органических реагентов (эффект Шпольского)
Флуориметрические определения органических реагентов (эффект Шпольского)
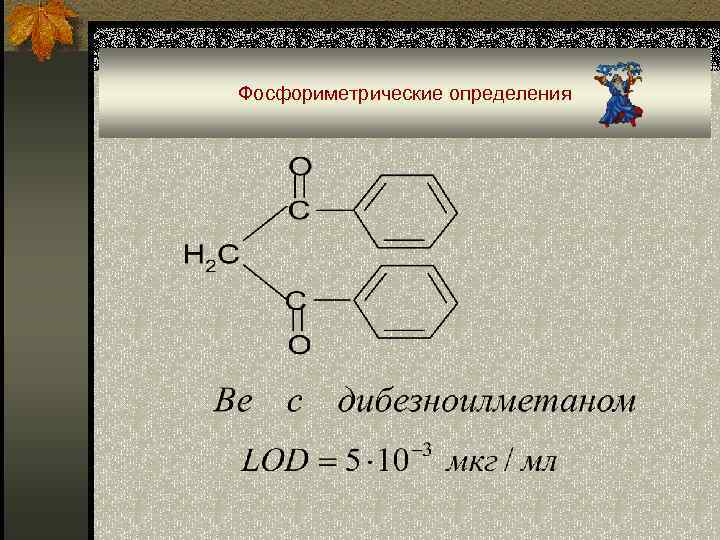 Фосфориметрические определения
Фосфориметрические определения
 Синхронные спектры ■ Синхронные спектры получают при одновременном (синхронном) сканировании (изменении) длин волн возбуждения и испускания с постоянным сдвигом Δλ между ними. ■ При этом наблюдается значительное упрощение спектров люминесценции сложных молекул, сужение их полос и, как следствие, повышение селективности определений, а также уменьшение фонового свечения за счет подавления релеевского и комбинационного рассеяния растворителя. ■ Оптимальным условием для достижения наиболее интенсивного сигнала и наименьшей полуширины линии является синхронное сканирование с условием: Δλ = λисп (макс. ) - λвозб (макс. )
Синхронные спектры ■ Синхронные спектры получают при одновременном (синхронном) сканировании (изменении) длин волн возбуждения и испускания с постоянным сдвигом Δλ между ними. ■ При этом наблюдается значительное упрощение спектров люминесценции сложных молекул, сужение их полос и, как следствие, повышение селективности определений, а также уменьшение фонового свечения за счет подавления релеевского и комбинационного рассеяния растворителя. ■ Оптимальным условием для достижения наиболее интенсивного сигнала и наименьшей полуширины линии является синхронное сканирование с условием: Δλ = λисп (макс. ) - λвозб (макс. )
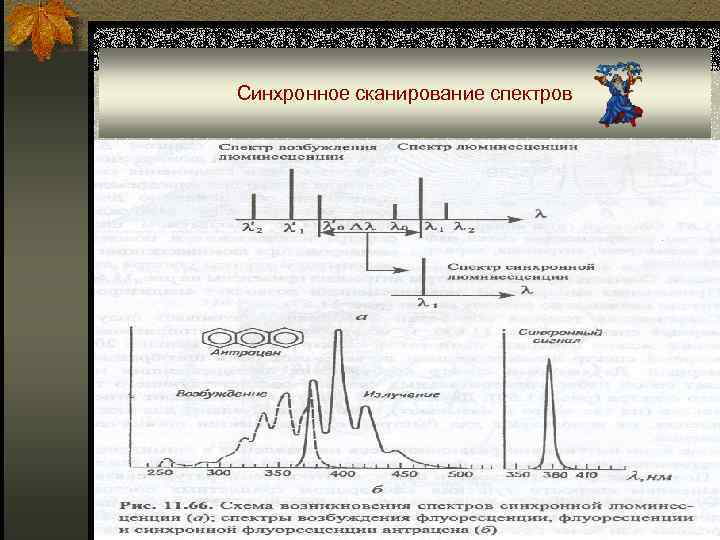 Синхронное сканирование спектров
Синхронное сканирование спектров
 Трехмерные спектры ■ Трехмерные спектры представляют собой зависимость интенсивности люминесценции как от длины волны возбуждения, так и от длины волны испускания. ■ Трехмерные спектры имеют вид «горной гряды» . Каждая строка такой гряды представляет собой спектр излучения, а каждый столбец – спектр возбуждения. ■ Такие спектры получают из большого числа (обычно не менее 50) индивидуальных спектров люминесценции, записанных через определенные промежутки длин волн возбуждения. ■ Трехмерные спектры дают полную картину спектральных свойств исследуемого образца.
Трехмерные спектры ■ Трехмерные спектры представляют собой зависимость интенсивности люминесценции как от длины волны возбуждения, так и от длины волны испускания. ■ Трехмерные спектры имеют вид «горной гряды» . Каждая строка такой гряды представляет собой спектр излучения, а каждый столбец – спектр возбуждения. ■ Такие спектры получают из большого числа (обычно не менее 50) индивидуальных спектров люминесценции, записанных через определенные промежутки длин волн возбуждения. ■ Трехмерные спектры дают полную картину спектральных свойств исследуемого образца.
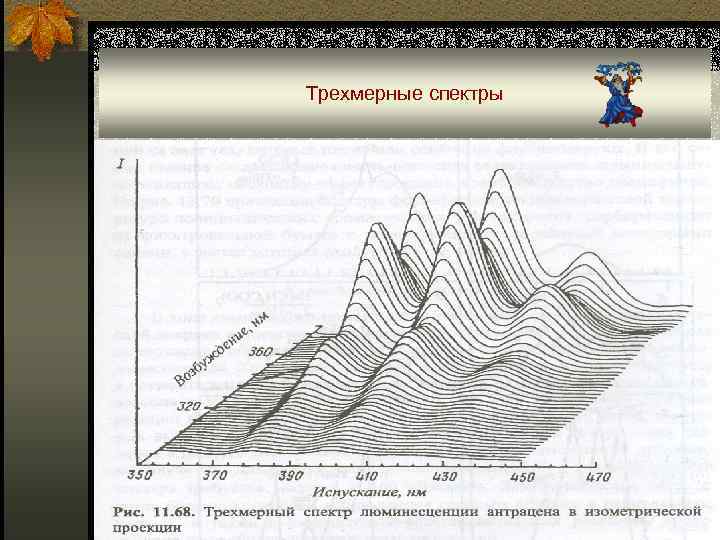 Трехмерные спектры
Трехмерные спектры
 Контурные (двумерные) спектры ■ Использование трехмерных спектров для анализа смесей, содержащих более трех компонентов, и имеющих широкие размытые полосы в одной и той же спектральной области, представляет неразрешимую задачу. ■ В данном случае более перспективным является использование контурных спектров – результат сечения трехмерного спектра плоскостями, параллельными плоскости ХОУ, с последующим объединением полученных сечений в одной плоскости ХОУ. ■ Получающиеся изображения напоминают контурные карты (контурные спектры), которые являются «отпечатками пальцев» индивидуального соединения.
Контурные (двумерные) спектры ■ Использование трехмерных спектров для анализа смесей, содержащих более трех компонентов, и имеющих широкие размытые полосы в одной и той же спектральной области, представляет неразрешимую задачу. ■ В данном случае более перспективным является использование контурных спектров – результат сечения трехмерного спектра плоскостями, параллельными плоскости ХОУ, с последующим объединением полученных сечений в одной плоскости ХОУ. ■ Получающиеся изображения напоминают контурные карты (контурные спектры), которые являются «отпечатками пальцев» индивидуального соединения.
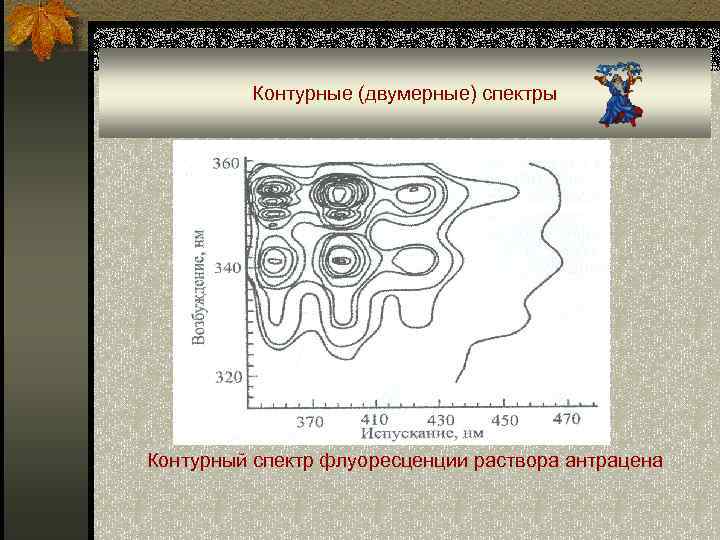 Контурные (двумерные) спектры Контурный спектр флуоресценции раствора антрацена
Контурные (двумерные) спектры Контурный спектр флуоресценции раствора антрацена
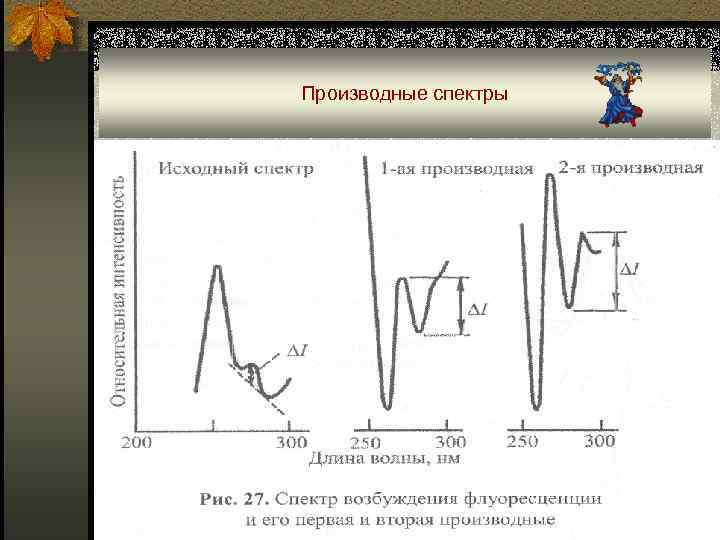 Производные спектры
Производные спектры
 Хемилюминесцентный анализ ■ Хемилюминесцентный анализ основан на явлении хемилюминесценции (ХЛ). Этот вид свечения не требует внешнего источника возбуждения, а возникает за счет энергии экзотермических химических процессов: A + B → P* + C P* → P + hvcl n В растворах ХЛ наблюдается главным образом в реакциях окисления органических веществ кислородом или пероксидом водорода. n Образование продуктов реакции происходит чаще всего по сложному радикально-цепному механизму. n Так, многие полагают, что окисление люминола (I) протекает с участием радикалов HO 2*, HO*, O 2*.
Хемилюминесцентный анализ ■ Хемилюминесцентный анализ основан на явлении хемилюминесценции (ХЛ). Этот вид свечения не требует внешнего источника возбуждения, а возникает за счет энергии экзотермических химических процессов: A + B → P* + C P* → P + hvcl n В растворах ХЛ наблюдается главным образом в реакциях окисления органических веществ кислородом или пероксидом водорода. n Образование продуктов реакции происходит чаще всего по сложному радикально-цепному механизму. n Так, многие полагают, что окисление люминола (I) протекает с участием радикалов HO 2*, HO*, O 2*.
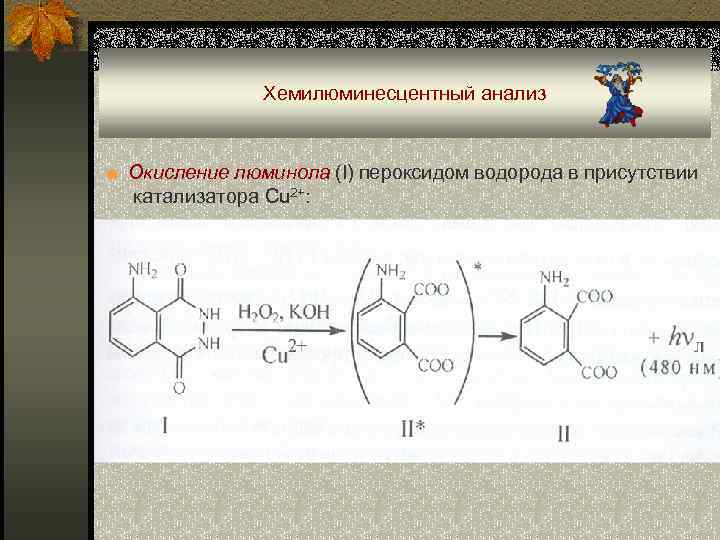 Хемилюминесцентный анализ ■ Окисление люминола (I) пероксидом водорода в присутствии катализатора Cu 2+:
Хемилюминесцентный анализ ■ Окисление люминола (I) пероксидом водорода в присутствии катализатора Cu 2+:
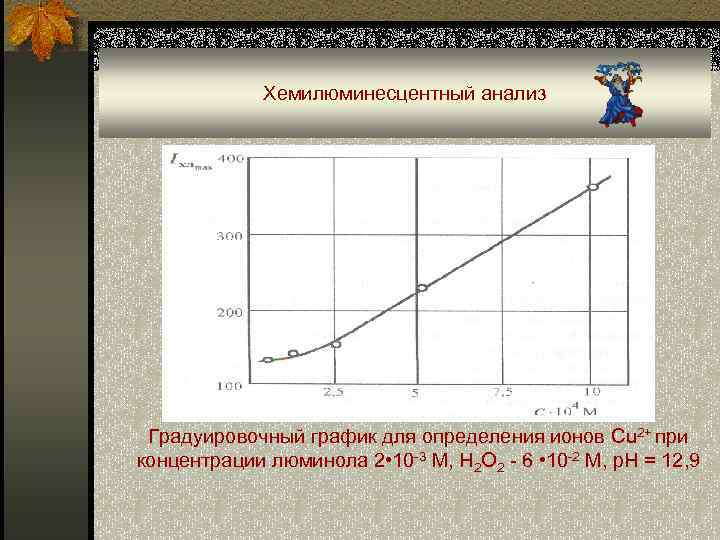 Хемилюминесцентный анализ Градуировочный график для определения ионов Cu 2+ при концентрации люминола 2 • 10 -3 М, Н 2 О 2 - 6 • 10 -2 М, р. Н = 12, 9
Хемилюминесцентный анализ Градуировочный график для определения ионов Cu 2+ при концентрации люминола 2 • 10 -3 М, Н 2 О 2 - 6 • 10 -2 М, р. Н = 12, 9
 Хемилюминесцентный анализ ■ Основные группы определяемых соединений: • хемилюминесцентные соединения, которые при окислении излучают свет (люминол, люцигенин, лофин и др. ); • окислители (пероксид водорода, гипохлориты, гипобромиты, персулфаты, перманганат калия, молекулярный кислород и др. ); • катализаторы индикаторных реакций (ионы меди, кобальта, марганца, никеля, железа и др. ); • ингибиторы индикаторных реакций (ароматические соединения, содержащие фенольные и аминогруппы); • соединения, изменяющие р. Н среды (щелочи, карбонаты, органические основания и др. ). ■ Сортовой ХЛ анализ и индикаторные методы.
Хемилюминесцентный анализ ■ Основные группы определяемых соединений: • хемилюминесцентные соединения, которые при окислении излучают свет (люминол, люцигенин, лофин и др. ); • окислители (пероксид водорода, гипохлориты, гипобромиты, персулфаты, перманганат калия, молекулярный кислород и др. ); • катализаторы индикаторных реакций (ионы меди, кобальта, марганца, никеля, железа и др. ); • ингибиторы индикаторных реакций (ароматические соединения, содержащие фенольные и аминогруппы); • соединения, изменяющие р. Н среды (щелочи, карбонаты, органические основания и др. ). ■ Сортовой ХЛ анализ и индикаторные методы.
 Хемилюминесцентный анализ ■ Сортовой ХЛ анализ применяется при испытаниях вин, соков плодов и овощей, мясных экстрактов и т. д. Так, по реакции окисления люминола в присутствии катализатора - комплекса ионов меди с α-аминокислотами, содержащимися в соке картофеля, можно улавливать сортовые различия картофеля: сорта различаются по содержанию аминокислот. ■ К индикаторным методам ХЛ анализа относятся различные виды титрования с использованием хемилюминесцентных индикаторов (ХЛИ). В отличии от флуоресцентных индикаторов для работы с ХЛИ не требуется источника возбуждения.
Хемилюминесцентный анализ ■ Сортовой ХЛ анализ применяется при испытаниях вин, соков плодов и овощей, мясных экстрактов и т. д. Так, по реакции окисления люминола в присутствии катализатора - комплекса ионов меди с α-аминокислотами, содержащимися в соке картофеля, можно улавливать сортовые различия картофеля: сорта различаются по содержанию аминокислот. ■ К индикаторным методам ХЛ анализа относятся различные виды титрования с использованием хемилюминесцентных индикаторов (ХЛИ). В отличии от флуоресцентных индикаторов для работы с ХЛИ не требуется источника возбуждения.
 Хемилюминесцентный анализ (аналитические характеристики) ■ Большей частью ХЛ – определения отличаются высокой чувствительностью: пределы обнаружения 10 -10 – 10 -4 г/мл при конечном объеме 2 – 5 мл. ■ Селективность ХЛ – определений, как правило, невысока, так как многие вещества влияют на скорость индикаторной реакции. Однако варьирование условий определения или применение маскирующих агентов позволяет «смягчить» этот недостаток. ■ Простота, доступность и дешевизна аппаратуры, используемой в ХЛ, в сочетании с возможностью экспрессного, высокочувствительного, а при определенных условиях, и селективного определения большого круга соединений обуславливает распространенность ХЛ.
Хемилюминесцентный анализ (аналитические характеристики) ■ Большей частью ХЛ – определения отличаются высокой чувствительностью: пределы обнаружения 10 -10 – 10 -4 г/мл при конечном объеме 2 – 5 мл. ■ Селективность ХЛ – определений, как правило, невысока, так как многие вещества влияют на скорость индикаторной реакции. Однако варьирование условий определения или применение маскирующих агентов позволяет «смягчить» этот недостаток. ■ Простота, доступность и дешевизна аппаратуры, используемой в ХЛ, в сочетании с возможностью экспрессного, высокочувствительного, а при определенных условиях, и селективного определения большого круга соединений обуславливает распространенность ХЛ.


