d-элементы 2 вер.ppt
- Количество слайдов: 48

Лёвкин А. Н. Некоторые d-элементы
IA IIIB IVB VB VIIB VIIIB IB IIIA IVA VA VIIA H Li VIIIA He Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Sc Ti Rb Sr Y Cs Ba Fr Ra V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn Ac Rf Db Sg Bh Hs Mt Ds Rg
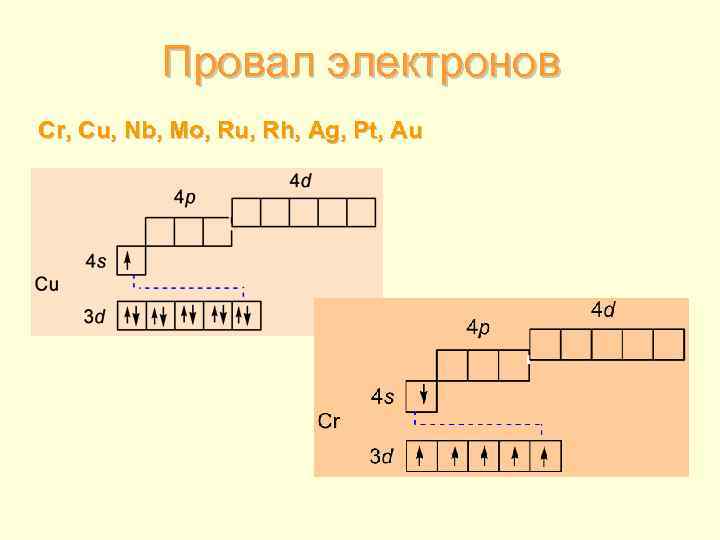
Провал электронов Cr, Cu, Nb, Mo, Ru, Rh, Ag, Pt, Au
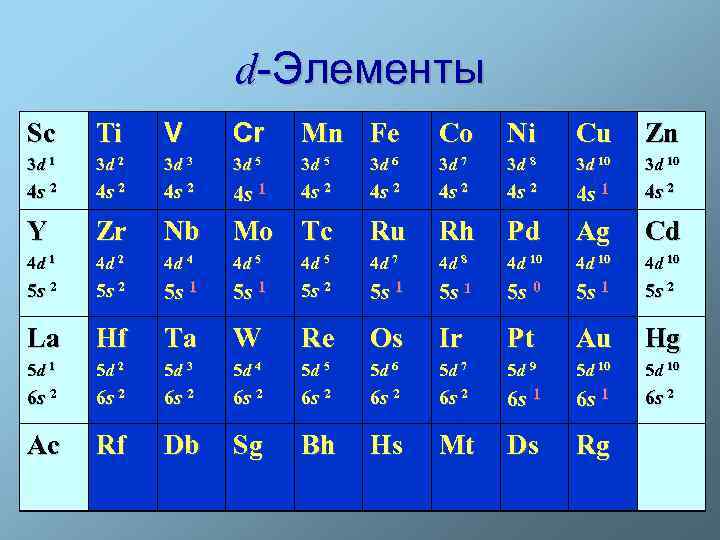
d-Элементы Sc Ti V Cr Mn Fe Co Ni Cu Zn 3 d 1 3 d 2 3 d 3 3 d 5 3 d 6 3 d 7 3 d 8 3 d 10 4 s 2 4 s 2 4 s 1 4 s 2 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd 4 d 1 4 d 2 4 d 4 4 d 5 4 d 7 4 d 8 4 d 10 5 s 2 5 s 1 5 s 0 5 s 1 5 s 2 La Hf Ta W Re Os Ir Pt Au Hg 5 d 1 5 d 2 5 d 3 5 d 4 5 d 5 5 d 6 5 d 7 5 d 9 5 d 10 6 s 2 6 s 2 6 s 1 6 s 2 Ac Rf Db Sg Bh Hs Mt Ds Rg
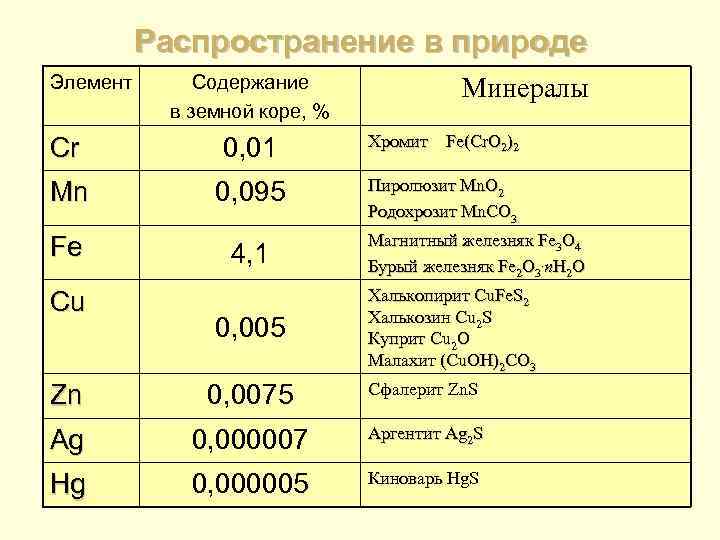
Распространение в природе Элемент Содержание в земной коре, % Минералы Cr 0, 01 Хромит Fe(Cr. O 2)2 Mn 0, 095 Пиролюзит Mn. O 2 Родохрозит Mn. CO 3 Fe Cu 4, 1 0, 005 Магнитный железняк Fe 3 O 4 Бурый железняк Fe 2 O 3. n. H 2 O Халькопирит Cu. Fe. S 2 Халькозин Cu 2 S Куприт Cu 2 O Малахит (Cu. OH)2 CO 3 Zn 0, 0075 Сфалерит Zn. S Ag 0, 000007 Аргентит Ag 2 S Hg 0, 000005 Киноварь Hg. S

Минералы Лимонит Fe 2 O 3∙n. H 2 O Смитсонит Zn. CO 3 Магнетит Fe 3 O 4 Сфалерит Zn. S Гематит Fe 2 O 3 Пирит Fe. S 2

Минералы Малахит (Cu. OH)2 CO 3 Хромит (Fe, Cr 2)O 4 Крокоит Pb. Cr. O 4

Минералы Киноварь Hg. S Пиролюзит Mn. O 2 Серебро Ag
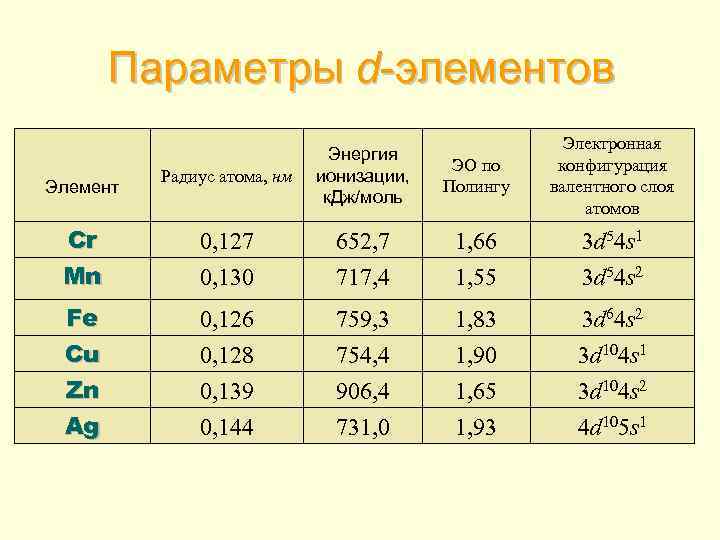
Параметры d-элементов Радиус атома, нм Энергия ионизации, к. Дж/моль ЭО по Полингу Электронная конфигурация валентного слоя атомов Cr Mn 0, 127 652, 7 1, 66 3 d 54 s 1 0, 130 717, 4 1, 55 3 d 54 s 2 Fe Cu Zn Ag 0, 126 0, 128 0, 139 0, 144 759, 3 754, 4 906, 4 731, 0 1, 83 1, 90 1, 65 1, 93 3 d 64 s 2 3 d 104 s 1 3 d 104 s 2 4 d 105 s 1 Элемент
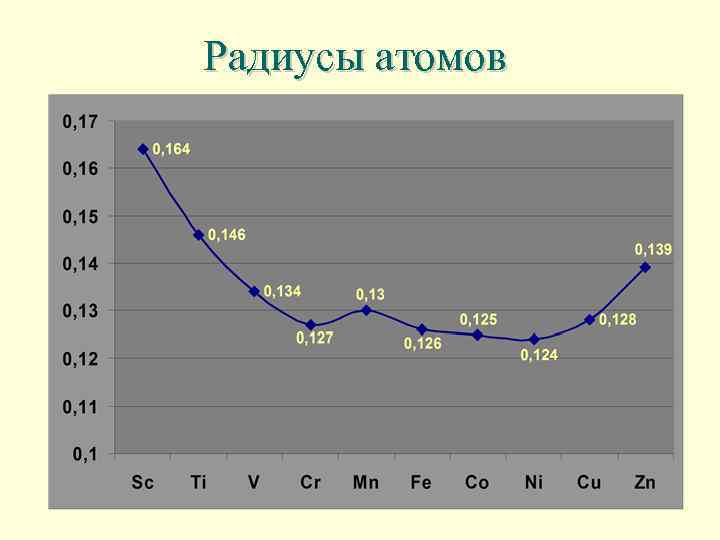
Радиусы атомов
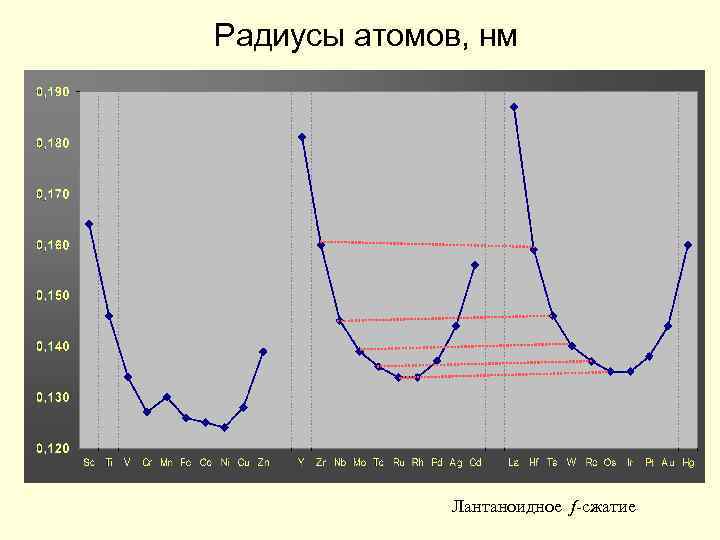
Радиусы атомов, нм Лантаноидное f-сжатие
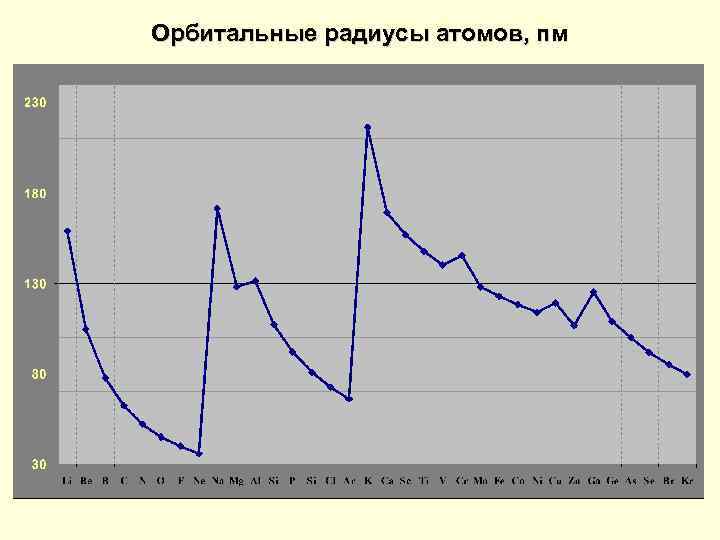
Орбитальные радиусы атомов, пм
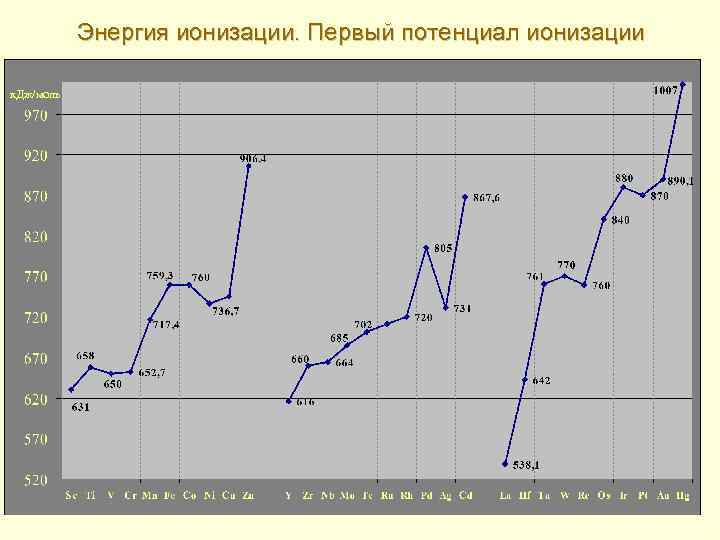
Энергия ионизации. Первый потенциал ионизации к. Дж/моль
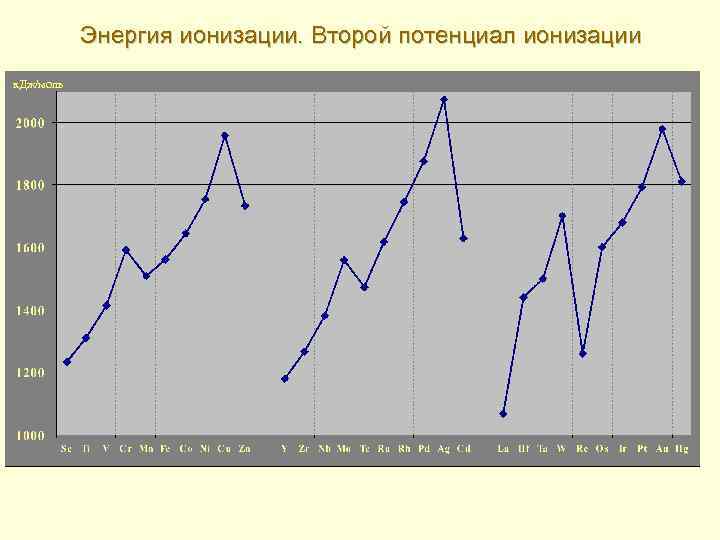
Энергия ионизации. Второй потенциал ионизации к. Дж/моль
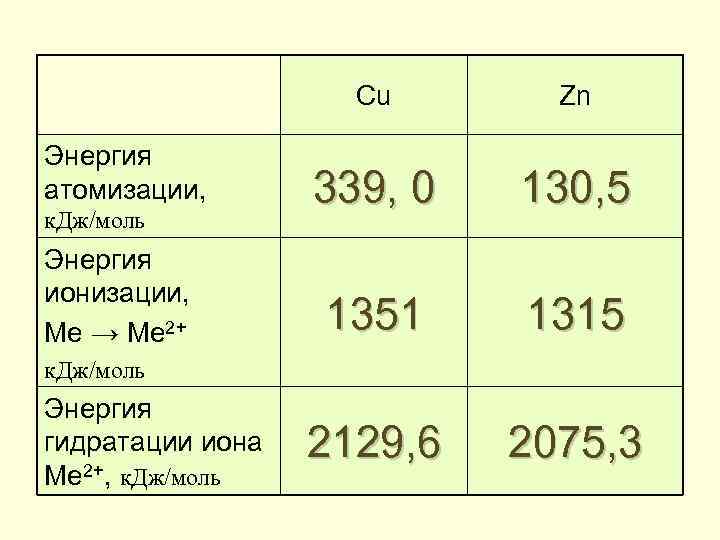
Cu Энергия атомизации, к. Дж/моль Энергия ионизации, Me → Me 2+ Zn 339, 0 130, 5 1351 1315 2129, 6 2075, 3 к. Дж/моль Энергия гидратации иона Ме 2+, к. Дж/моль
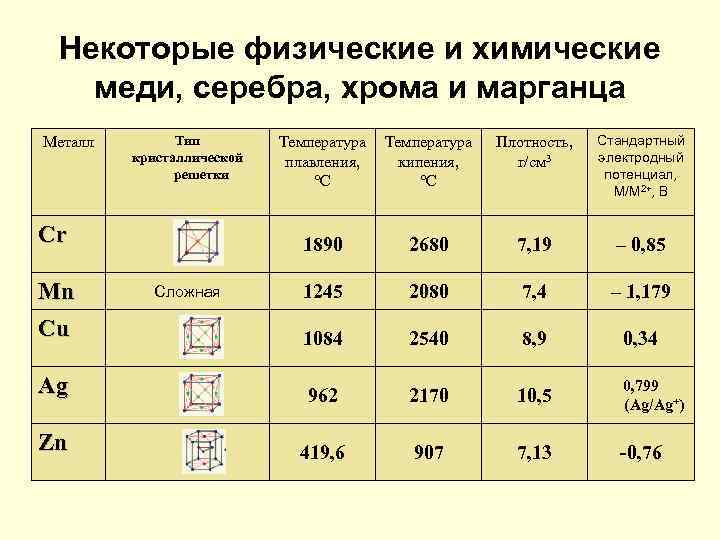
Некоторые физические и химические меди, серебра, хрома и марганца Температура плавления, °С Температура кипения, °С Плотность, г/см 3 Стандартный электродный потенциал, М/М 2+, В 1890 2680 7, 19 – 0, 85 1245 2080 7, 4 – 1, 179 Cu 1084 2540 8, 9 0, 34 Ag 962 2170 10, 5 0, 799 (Ag/Ag+) Zn 419, 6 907 7, 13 -0, 76 Металл Тип кристаллической решетки Cr Mn Сложная
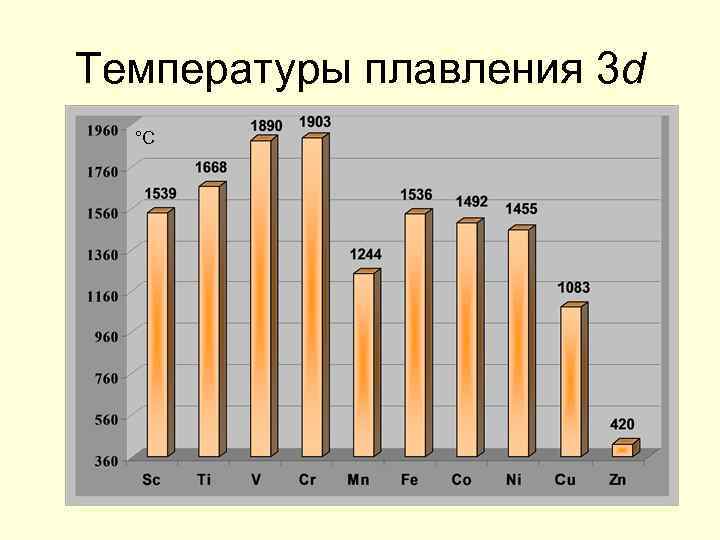
Температуры плавления 3 d °С
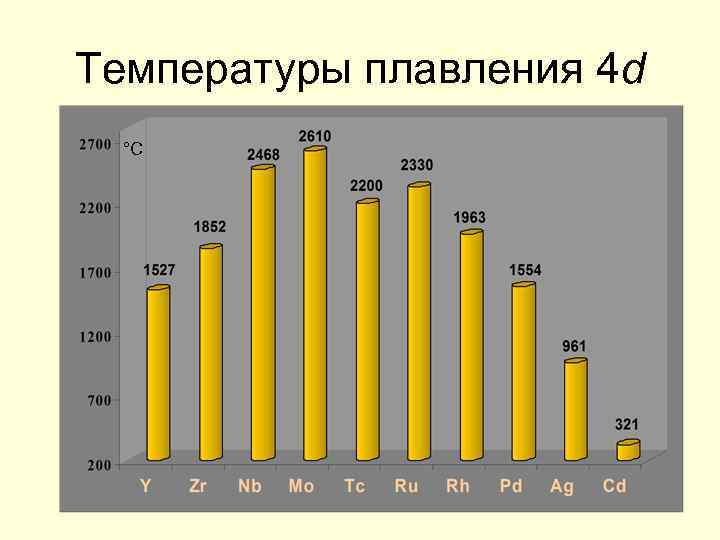
Температуры плавления 4 d °С
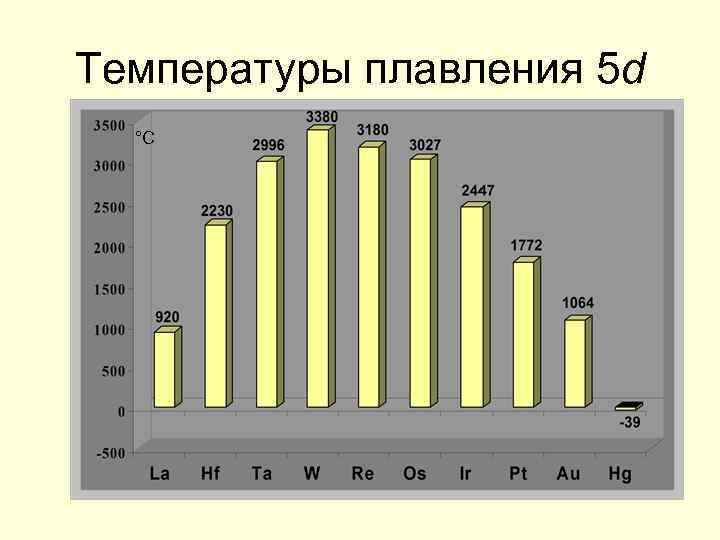
Температуры плавления 5 d °С
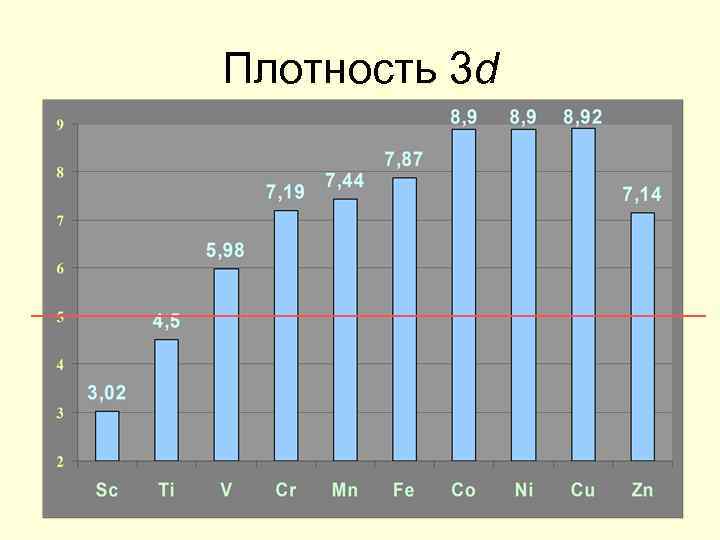
Плотность 3 d
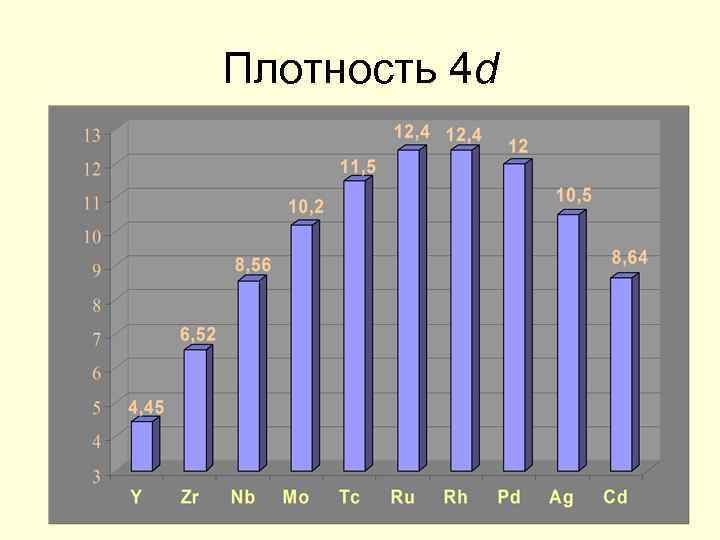
Плотность 4 d
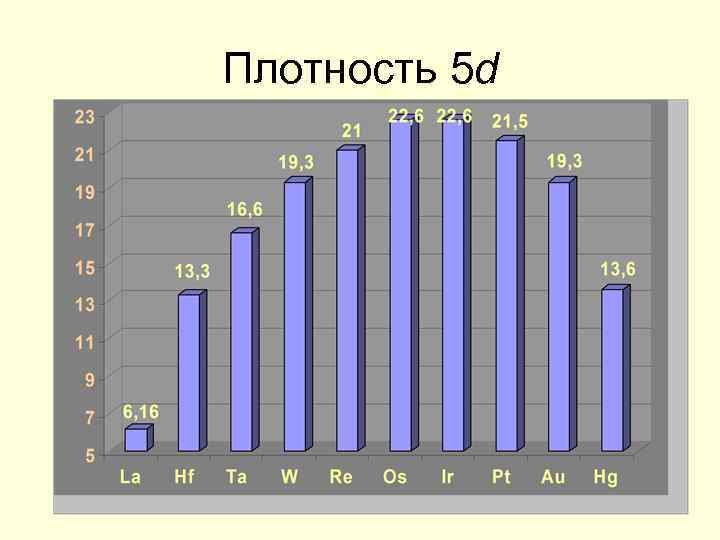
Плотность 5 d
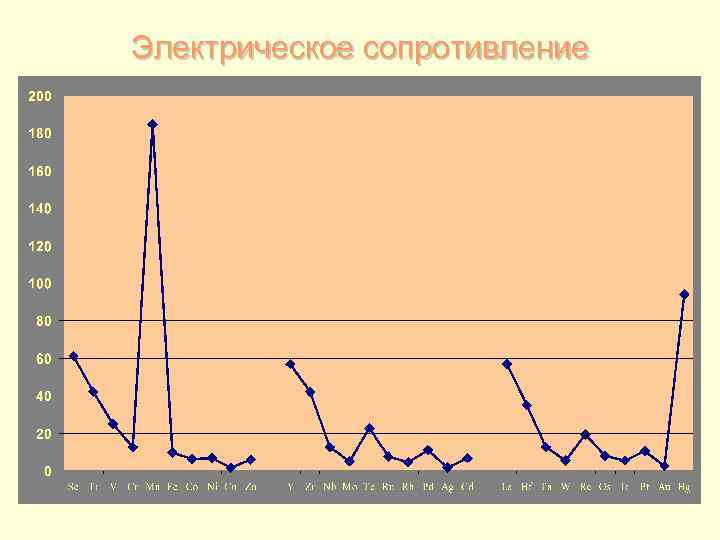
Электрическое сопротивление
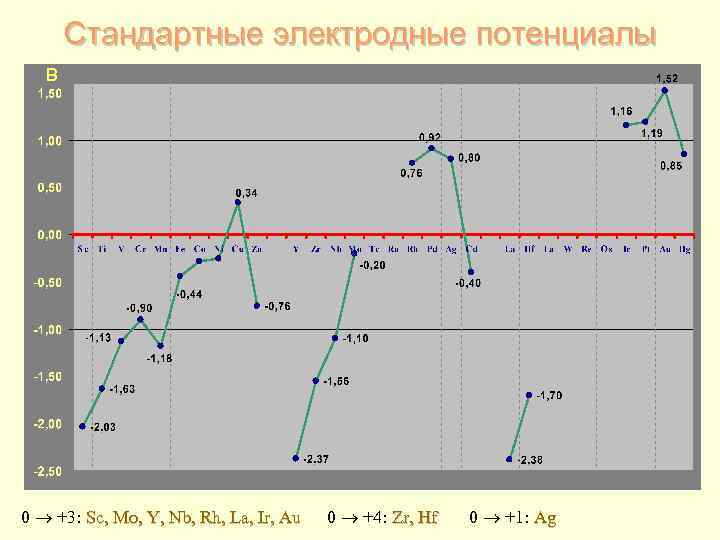
Стандартные электродные потенциалы В 0 +3: Sc, Mo, Y, Nb, Rh, La, Ir, Au 0 +4: Zr, Hf 0 +1: Ag
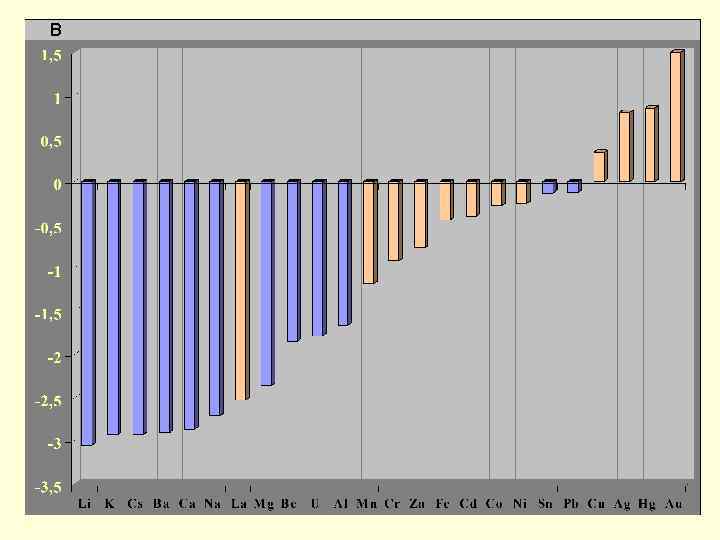
В
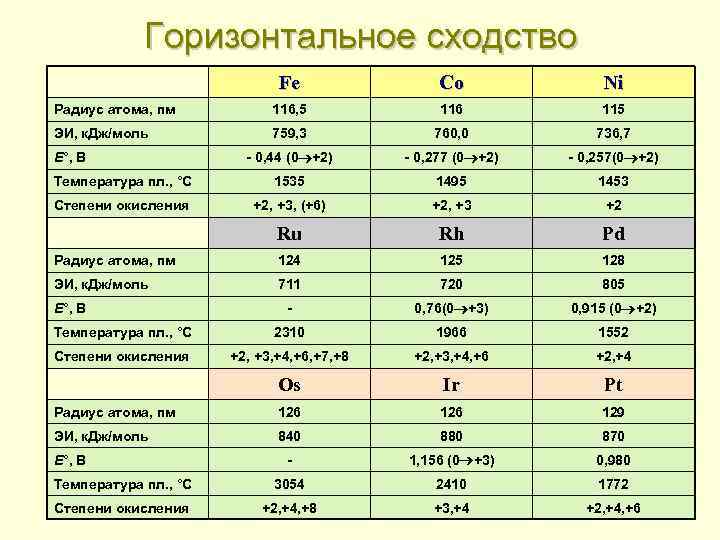
Горизонтальное сходство Fe Co Ni Радиус атома, пм 116, 5 116 115 ЭИ, к. Дж/моль 759, 3 760, 0 736, 7 - 0, 44 (0 +2) - 0, 277 (0 +2) - 0, 257(0 +2) Температура пл. , °С 1535 1495 1453 Степени окисления +2, +3, (+6) +2, +3 +2 Ru Rh Pd Радиус атома, пм 124 125 128 ЭИ, к. Дж/моль 711 720 805 - 0, 76(0 +3) 0, 915 (0 +2) Температура пл. , °С 2310 1966 1552 Степени окисления +2, +3, +4, +6, +7, +8 +2, +3, +4, +6 +2, +4 Os Ir Pt Радиус атома, пм 126 129 ЭИ, к. Дж/моль 840 880 870 - 1, 156 (0 +3) 0, 980 Температура пл. , °С 3054 2410 1772 Степени окисления +2, +4, +8 +3, +4 +2, +4, +6 E°, В

Устойчивость высшей степени окисления +3 4 Cr(порошок) + 3 O 2 = 2 Cr 2 O 3 +6 (медленно) 2 Mo + 3 O 2 = 2 Mo. O 3 (600 -700 °C) 2 W + 3 O 2 = 2 WO 3 (выше 500 °С) +2, +3 3 Fe + 2 O 2 = Fe 3 O 4 +4 Ru + O 2 = Ru. O 2 +8 Os + 2 O 2 = Os. O 4 Чем обусловлена устойчивость высшей степени окисления У 4 d- и 5 d-элементов? (150 -600 °С, сгорание на воздухе) (400 °С) (400 °C, сгорание на воздухе) Mn. O 4 - / Mn. O 2 Tc. O 4 - / Tc. O 2 Re. O 4 - / Re. O 2 Экранирующее влияние электронов на f-подуровне! 1, 69 В 0, 74 В 0, 51 В

Химические свойства меди 2 Cu + O 2 = 2 Cu. O Cu + Cl 2 = Cu. Cl 2 2 Cu + S = Cu 2 S Cu + 2 H 2 SO 4 (конц. ) = Cu. SO 4 + SO 2 + 2 H 2 O Cu + 4 HNO 3 (конц. ) = Cu(NO 3)2 + 2 NO 2 + 2 H 2 O 3 Cu + 8 HNO 3 (разб. ) = 3 Cu(NO 3)2 + 2 NO + 4 H 2 O 2 Cu + O 2 + CO 2 + H 2 O = (Cu. OH)2 CO 3 Опыт: горение меди в хлоре Опыт: взаимодействие меди с азотной кислотой Опыт: взаимодействие меди с серной концентрированной кислотой

Химические свойства серебра 2 Ag + Cl 2 = 2 Ag. Cl 2 Ag + S = Ag 2 S 2 Ag + 2 H 2 SO 4 (конц. , гор. ) = Ag 2 SO 4 + SO 2 + 2 H 2 O 3 Ag + 4 HNO 3 (разб. ) = 3 Ag. NO 3 + NO + 2 H 2 O 4 Ag + 2 H 2 S + O 2 = 2 Ag 2 S + 2 H 2 O Ag + F 2 = Ag. F 2 (>300 °C)

Химические свойства цинка 2 Zn + O 2 = 2 Zn. O Zn + Cl 2 = Zn. Cl 2 Zn + S = Zn. S Zn + H 2 O (пар) = Zn. O + H 2 Zn + 2 HCl = Zn. Cl 2 + H 2 Zn + H 2 SO 4 = Zn. SO 4 + H 2 4 Zn + 5 H 2 SO 4(конц. ) = 4 Zn. SO 4 + H 2 S + 4 H 2 O 4 Zn + 10 HNO 3 (оч. разб. , гор. ) = 4 Zn(NO 3)2 + NH 4 NO 3 + 3 H 2 O Zn + H 3 PO 4 (конц. , гор. ) = Zn. HPO 4 + H 2 Zn + 2 Na. OH + 2 H 2 O = Na 2[Zn(OH)4] + H 2 Zn + 4 NH 3. H 2 O = [Zn(NH 3)4](OH)2 + H 2 + 2 H 2 O

Химические свойства ртути 2 Hg + O 2 = 2 Hg. O 250 -350 °C Hg + Cl 2 = Hg. Cl 2 70 -120 °C Hg + Hg. Cl 2 = Hg 2 Cl 2 250 -300 °C Hg + S = Hg. S 2 Hg + 2 H 2 SO 4 = Hg 2 SO 4 + SO 2 + 2 H 2 O конц. , гор. Hg + 2 H 2 SO 4 = Hg. SO 4 + SO 2 + H 2 O конц. 6 Hg + 8 HNO 3 = 3 Hg 2(NO 3)2 + 2 NO + 4 H 2 O разб. , хол. Hg + 4 HNO 3 = Hg(NO 3)2 + 2 NO 2 + 2 H 2 O конц. , гор. Опыт: взаимодействие ртути с азотной кислотой Hg + 4 HI = H 2[Hg. I 4] + H 2 конц.

Химические свойства хрома Не реагирует с холодной водой, щелочами, гидратом аммиака, пассивируется в концентрированной и разбавленной азотной кислоте, «царской водке» . 4 Cr (порошок) + 3 O 2 = 2 Cr 2 O 3. Cr + 2 F 2 = Cr. F 4 (350 -500 °C) 2 Cr + 3 H 2 O (пар) = Cr 2 O 3 + 3 H 2 Cr + H 2 SO 4 (разб. ) = Cr. SO 4 + H 2 Cr + 2 HCl = Cr. Cl 2 + H 2

Химические свойства марганца Mn + Cl 2 = Mn. Cl 2 Mn + O 2 = Mn. O 2 Mn + S = Mn. S Mn (порошок) + 2 H 2 O (пар) = Mn(OH)2 + H 2 Mn + 2 HCl = Mn. Cl 2 + H 2 Mn + H 2 SO 4 = Mn. SO 4 + H 2 Mn + 2 H 2 SO 4 (конц. ) = Mn. SO 4 + SO 2 + 2 H 2 O 3 Mn + 8 HNO 3 (конц. ) = 3 Mn(NO 3)2 + 2 NO + 4 H 2 O
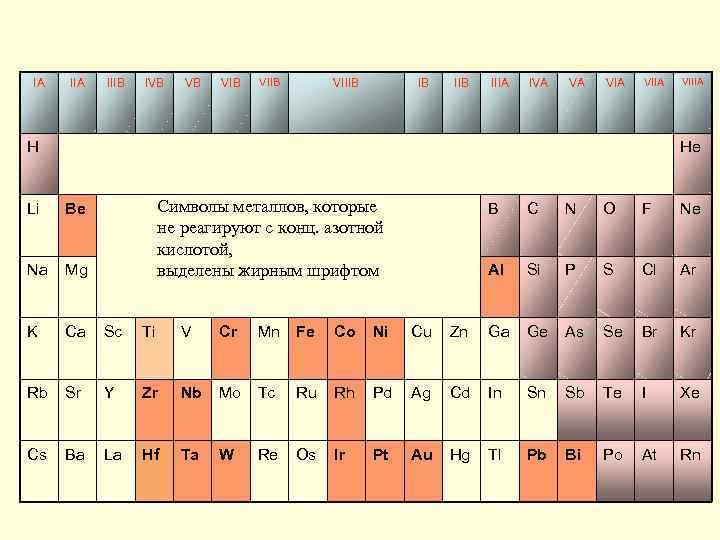
IA IIIB IVB VB VIIB VIIIB IB IIIA IVA VA VIIA H VIIIA He Символы металлов, которые не реагируют с конц. азотной кислотой, выделены жирным шрифтом Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn
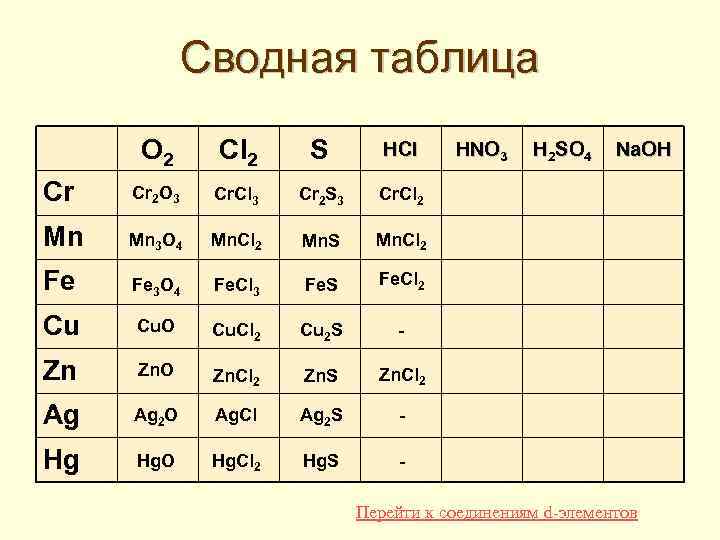
Сводная таблица O 2 Cl 2 S HCl Cr Cr 2 O 3 Cr. Cl 3 Cr 2 S 3 Cr. Cl 2 Mn Mn 3 O 4 Mn. Cl 2 Mn. S Mn. Cl 2 Fe Fe 3 O 4 Fe. Cl 3 Fe. S Fe. Cl 2 Cu Cu. O Cu. Cl 2 Cu 2 S - Zn Zn. O Zn. Cl 2 Zn. S Zn. Cl 2 Ag Ag 2 O Ag. Cl Ag 2 S - Hg Hg. O Hg. Cl 2 Hg. S - HNO 3 H 2 SO 4 Na. OH Перейти к соединениям d-элементов

Окраска высших оксидов d-элементов Sc 2 O 3 Ti. O 2 Y 2 O 3 V 2 O 5 Cr. O 3 Mn 2 O 7 Fe 2 O 3 Co 3 O 4 Ni. O Cu. O Zn. O Zr. O 2 Nb 2 O 5 Mo. O 3 Tc 2 O 7 Ru. O 4 Rh 2 O 3 Pd. O Ag 2 O Cd. O La 2 O 3 Hf. O 2 Ta 2 O 5 WO 3 Re 2 O 7 Os. O 4 Ir 2 O 3 Pt. O 2 Au 2 O 3 Hg. O

Соединения d-элементов Кислотно-основный характер оксидов и гидроксидов Кислотность в о з р а с т а е т Cr. O Cr 2 O 3 Cr. O 3 с повышением степени окисления Cr(OH)2 Cr(OH)3 H 2 Cr. O 4 с повышением степени окисления Hg. O Cd. O Zn. O по подгруппе с убыванием Z Zn Cd Hg Sc 2 O 3 Ti. O 2 V 2 O 5 Cr. O 3 Mn 2 O 7 по периоду с повышением степени окисления
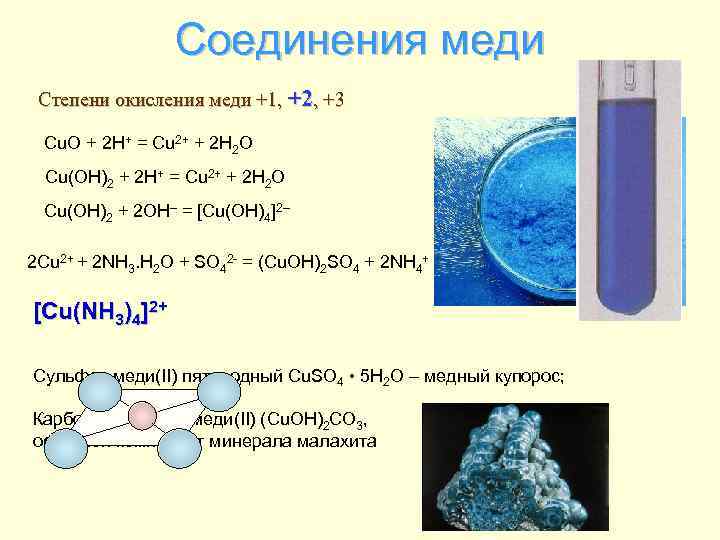
Соединения меди Степени окисления меди +1, +2, +3 Cu. O + 2 H+ = Cu 2+ + 2 H 2 O Cu(OH)2 + 2 OH– = [Cu(OH)4]2– 2 Cu 2+ + 2 NH 3. H 2 O + SO 42 - = (Cu. OH)2 SO 4 + 2 NH 4+ [Cu(NH 3)4]2+ Сульфат меди(II) пятиводный Cu. SO 4 • 5 H 2 O – медный купорос; Карбонат гидроксомеди(II) (Cu. OH)2 CO 3, основной компонент минерала малахита
![Полезная информация к практикуму 2 Cu 2+ + [Fe(CN)6]4 - = Cu 2[Fe(CN)6]↓ Cu Полезная информация к практикуму 2 Cu 2+ + [Fe(CN)6]4 - = Cu 2[Fe(CN)6]↓ Cu](https://present5.com/presentation/1514994_443145689/image-39.jpg)
Полезная информация к практикуму 2 Cu 2+ + [Fe(CN)6]4 - = Cu 2[Fe(CN)6]↓ Cu 2+ + S 2 - = Cu. S↓ Cu. S + 2 H+ -X Cu. SO 4 + H 2 S = Cu. S↓ + H 2 SO 4 3 Cu. SO 4 + 2 Al = Al 2(SO 4)3 + 3 Cu. Cl 2 + 2 Al = 2 Al. Cl 3 + 3 Cu

Соединения серебра Степени окисления серебра Ag 2 O +1, +2, +3 ПР = 1, 6· 10 -8 2 Ag. NO 3 + 2 Na. OH = Ag 2 O +2 Na. NO 3 + H 2 O Ag. NO 3 Соль Растворимость 225, 5 г/100 г Н 2 О при 20 °С ПР Ag. Cl 1, 8· 10 -10 Ag. Br 6· 10 -13 Ag. I 1, 1· 10 -16 Ag 3 PO 4 1· 10 -20 Ag 2 CO 3 Ag. Cl + 2 NH 3 = [Ag(NH 3)2]Cl К. ч. = 2 8, 2· 10 -12 Ag 2 S 6· 10 -50 Ag 2 SO 4 2· 10 -5 Ag 2 Cr. O 4 4· 10 -12 [Ag(NH 3)2]OH реактив Толленса Ag. I + Na 2 S 2 O 3 = Na 3[Ag(S 2 O 3)2] + Na. I

Соединения хрома Хром был открыт в минерале крокоите Pb. Cr. O 4 Луи Вокленом в 1797 г.

Соединения хрома Степени окисления хрома +2, +3, +4, +6 Cr. O 4 Cr. Cl 2 + 4 HCl + O 2 = 4 Cr. Cl 3 + 2 H 2 O Cr(OH)3 + 3 H+ = Cr 3+ + 3 H 2 O Cr(OH)2 +3 Cr 2 O 3 Cr(OH)3 +6 Cr. O(OH) Cr. O 3 H 2 Cr. O 4 Кислотность +2 Cr(OH)2 + 2 H+ = Cr 2+ + 2 H 2 O Cr(OH)3 + 3 OH– = [Cr(OH)6]3– Cr. O 3 + H 2 O = H 2 Cr. O 42– + 2 H+ Cr 2 O 72– + H 2 O K 2 Cr 2 O 7 + 14 HCl = 2 KCl + 2 Cr. Cl 3 + 3 Cl 2 + 7 H 2 O K 2 Cr 2 O 7 + K 2 SO 3 + H 2 SO 4 = Cr 2(SO 4)3 + K 2 SO 4 + H 2 O 2 Na 3[Cr(OH)6] + 3 Br 2 + 4 Na. OH = 2 Na 2 Cr. O 4 + 6 Na. Br + H 2 O Cr. O 2 ферромагнитен

Соединения марганца Степени окисления марганца +2, +3, +4, +6, +7 Mn. CO 3 = Mn. O + CO 2 Mn. O 2 + H 2 = Mn. O + H 2 O +4 Mn. O + 2 HCl = Mn. Cl 2 + H 2 O Mn(OH)2 +7 2 Mn(OH)2 + O 2 + H 2 O = 2 Mn. O(OH)2 Mn. O 2 + 4 HCl (конц. ) = Mn. Cl 2 + 2 H 2 O Mn. O 2 + KNO 3 + 2 KOH = K 2 Mn. O 4 + KNO 2 + H 2 O 2 Mn. O 2 + 2 H 2 SO 4 = 2 Mn. SO 4 + 2 H 2 O + O 2 2 Mn. O 2 + 4 KOH + O 2 = 2 K 2 Mn. O 4 + 2 H 2 O. Mn 2 O 7 + H 2 O = 2 HMn. O 4 Mn 2 O 7 + 2 Na. OH = 2 Na. Mn. O 4 + H 2 O Mn. O 2 Mn. O(OH)2 Mn 2 O 7 HMn. O 4 Кислотность +2

Окислительные свойства перманганата +7 +2 2 KMn. O 4 + 5 K 2 SO 3 + 3 H 2 SO 4 = 2 Mn. SO 4 + 6 K 2 SO 4 + 3 H 2 O +7 +4 2 KMn. O 4 + 3 K 2 SO 3 + H 2 O = 2 Mn. O 2 + 3 K 2 SO 4 + 2 KOH +6 +7 2 KMn. O 4 + K 2 SO 3 + 2 KOH = 2 K 2 Mn. O 4 + K 2 SO 4 + H 2 O +6 +7 +4 2 K 2 Mn. O 4 + 2 H 2 O 2 KMn. O 4 + Mn. O 2 + 4 KOH +4 +6 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 +7 Опыт: восстановление перманганата в кислой среде Опыт: восстановление перманганата в нейтральн. ср. Опыт: восстановление перманганата в щелочной среде
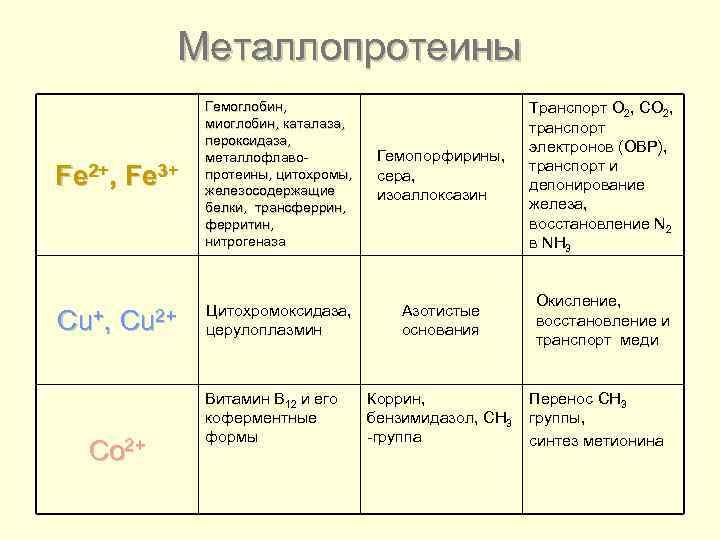
Металлопротеины Fe 2+, Fe 3+ Гемоглобин, миоглобин, каталаза, пероксидаза, металлофлавопротеины, цитохромы, железосодержащие белки, трансферрин, ферритин, нитрогеназа Гемопорфирины, сера, изоаллоксазин Транспорт О 2, СО 2, транспорт электронов (ОВР), транспорт и депонирование железа, восстановление N 2 в NH 3 Cu+, Cu 2+ Цитохромоксидаза, церулоплазмин Азотистые основания Окисление, восстановление и транспорт меди Co 2+ Витамин В 12 и его коферментные формы Коррин, бензимидазол, СН 3 -группа Перенос СН 3 группы, синтез метионина
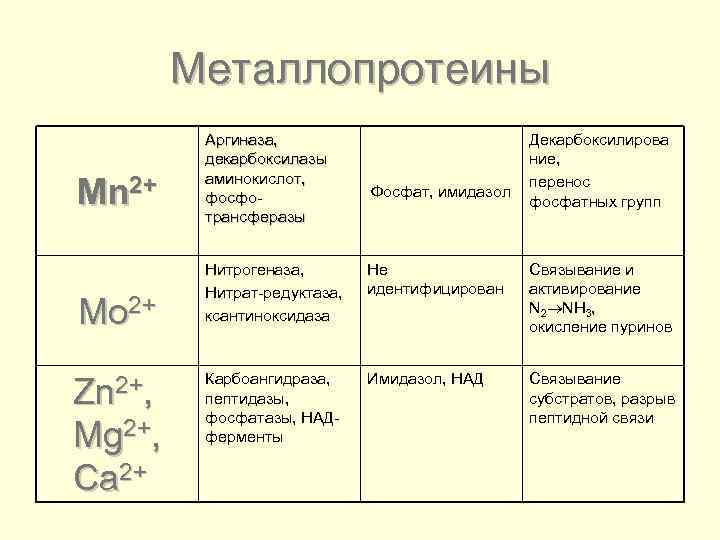
Металлопротеины Mn 2+ Mo 2+ Zn 2+, Mg 2+, Ca 2+ Аргиназа, декарбоксилазы аминокислот, фосфотрансферазы Фосфат, имидазол Декарбоксилирова ние, перенос фосфатных групп Нитрогеназа, Нитрат-редуктаза, ксантиноксидаза Не идентифицирован Связывание и активирование N 2 NH 3, окисление пуринов Карбоангидраза, пептидазы, фосфатазы, НАДферменты Имидазол, НАД Связывание субстратов, разрыв пептидной связи

Применение Металл Области применения Mn Сплавы, легирующая добавка к стали. Cu Проводники электрического тока, сплавы (латунь, бронза, мельхиор и др. ), теплообменники. Ag Электротехнические контакты, зеркальные покрытия, ювелирные изделия, производство фотографических материалов. Cr Сплавы, легирующая добавка к стали, антикоррозийные и декоративные покрытия. Zn Гальванические элементы, антикоррозийные покрытия, сплавы.

Спасибо за внимание!
d-элементы 2 вер.ppt