лучевая терапия злокачественный образований.ppt
- Количество слайдов: 76

Лучевая терапия злокачественных опухолей. Бондарь Д. В. Кафедра онкологии ИГИУВ, Иркутск

Роль лучевой терапии в лечении злокачественных опухолей Основной метод консервативного лечения n Компонент комплексного и комбинированного лечения n 50% всех онкологических больных получают лучевую терапию n 30% больных получают лучевую терапию в монорежиме n Один из основных методов симптоматической и паллиативной помощи n

Ионизирующее излучение Излучение, образующее при взаимодействии с веществом заряды разных знаков, называют ионизирующим.

История лучевой терапии n 1895 г. открытие рентгеновского излучения (Вильгельм Конрад Рентген) n 1886 г. Открытие естественной радиоактивности (Анри Беккрель) n 1934 г. открытие искусственной радиоактивности (Фредерик и Ирэн Жолио. Кюри)

Виды ионизирующих излучений n • • • Фотонное излучение Рентгеновские лучи (до 300 кэ. В) Гамма-лучи (0, 4 – 1, 7 Мэ. В) Мегавольтное излучение (4 – 25 Мэ. В) n • • Корпускулярное излучение Электроны (5 -20 Мэ. В) Протоны (150 -250 Мэ. В) Нейтроны (2, 35 – 14 Мэ. В) Тяжелые ионы (1001000 Мэ. В)

Виды лучевой терапии Дистанционная лучевая терапия n Контактная лучевая терапия (брахитерапия) • Внутриполостная терапия • Внутритканевая терапия • Аппликационная n Радиофармпрепараты n

Источники излучения Естественные и искусственные радиоактивные элементы (Со 60, Ir 192, Сf 252, Cs 137 и т. д. ) n Электрофизические машины (генераторы рентгеновского излучения, линейные ускорители, ускорители электронов и тяжелых частиц) n

Источники внешнего излучения Источник излучения Энергия Низковольтные рентгеновские Менее 100 кэ. В установки Кобальт 60 1, 25 Мэ. В 8 -20 Мэ. В Вид излучения Рентгеновское Гамма-лучи Рентгеновское Ускорители 6 -20 Мэ. В Электроны Применение Поверхностные и подкожные образования Образования на средней и большой глубине Глубоко расположенные опухоли Опухоли расположенные до 6 см от поверхности
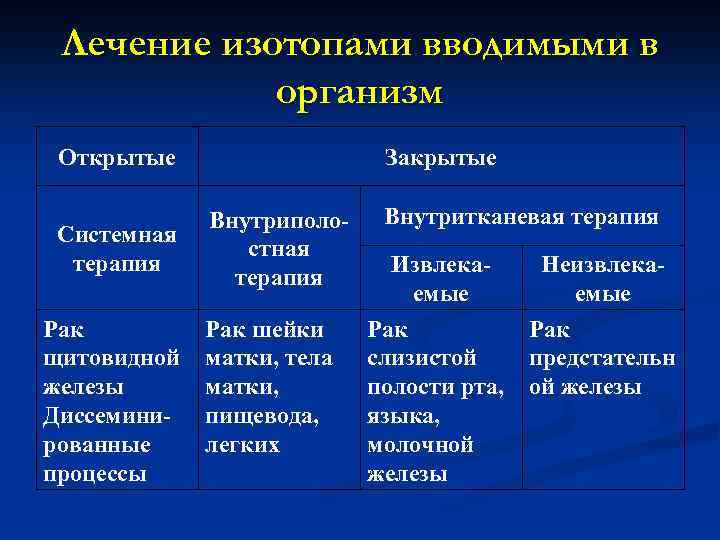
Лечение изотопами вводимыми в организм Открытые Системная терапия Рак щитовидной железы Диссеминированные процессы Закрытые Внутриполостная терапия Рак шейки матки, тела матки, пищевода, легких Внутритканевая терапия Извлекаемые Неизвлекаемые Рак слизистой полости рта, языка, молочной железы Рак предстательн ой железы

Единицы измерения поглощенной дозы 1 Гр = 1 Дж/1 кг 1 Гр = 100 рад

Лучевые повреждения n Летальные – приводят к гибели клетки n Сублетальные – гибель клетки или репарация и востановление функций n Потенциально летальные - могут приводить гибели клетки или репарация и репопуляция через 2 -2, 5 недели.

Радиобиологические эффекты физический уровень 1. прямое действие - молекула ионизируется при прохождении через нее электрона или фотона 2. косвенное действие - молекула не поглощает энергию фотона, а получает ее от другой молекулы

Радиобиологические эффекты химический уровень Инактивация жизненно важных биологически активных молекул n Разрушение внутриклеточных барьеров и дезорганизация, ведущие к распаду клетки n Образование под действием излучения новых веществ, являющихся чрезвычайно токсичными n

Радиобиологические эффекты клеточный уровень Мутации, в том числе соматические n Задержка митоза n Репродуктивная гибель, наступающая после одного или нескольких делений n Гибель в интерфазе, после облучения, без предварительного деления n

Успех лучевой терапии зависит от: n Радиочувствительности опухоли – 50 % n Аппаратного оснащения – 25 % n Точности выбора плана и лечения и его исполнения – 25 %

КТ - топометрия

Планирование

Фиксирующая маска

Виды фракционирования n n n Классическое: РОД – 1. 8 -2. 2 Гр, 1 раз в день, 5 раз в неделю Гиперфракционирование: РОД – 1 -1. 25 Гр, 2 раза в день, интервал 4 -5 часов, 5 р/неделю Гипофракционирование: РОД – 4 -10 Гр, 1 -3 раза в неделю Ускоренное: РОД - 1. 2 -2 Гр, ежедневно 2 -3 раза день интервал 4 -5 часов, 5 раз внеделю Динамическое: РОД изменяется во время курса лечения
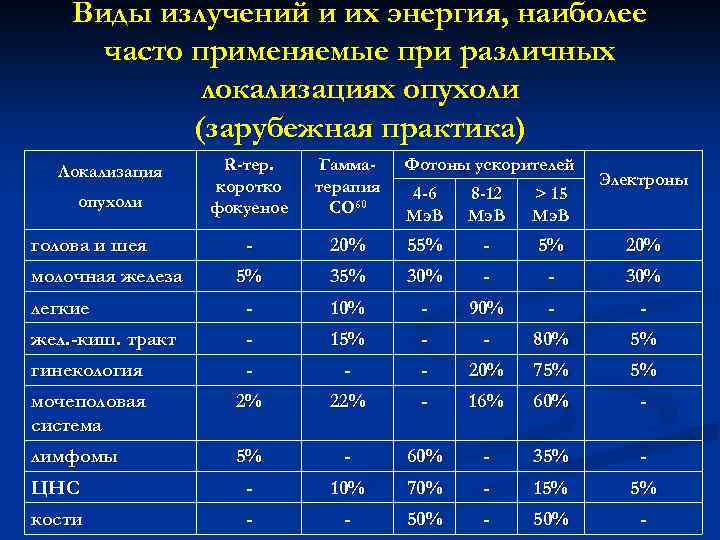
Виды излучений и их энергия, наиболее часто применяемые при различных локализациях опухоли (зарубежная практика) Локализация R-тер. коротко фокуеное Гамматерапия СО 60 - Фотоны ускорителей Электроны 4 -6 Мэ. В 8 -12 Мэ. В > 15 Мэ. В 20% 55% - 5% 20% 5% 30% - - 30% легкие - 10% - 90% - - жел. -киш. тракт - 15% - - 80% 5% гинекология - - - 20% 75% 5% мочеполовая система 2% 22% - 16% 60% - лимфомы 5% - 60% - 35% - ЦНС - 10% 70% - 15% 5% кости - - 50% - опухоли голова и шея молочная железа

Основные направления современной ЛТ в лечении злокачественных опухолей. Ø Ø Ø комбинация с хирургическим лечением - улучшение результатов и расширение возможности выполнения радикальных, органо-сохраняющих, функционально щадящих операций; в самостоятельном варианте или в комплексе с противоопухолевыми химиотерапевтическими препаратами - эффективное консервативное радикальное или паллиативное лечение некоторых форм злокачественных опухолей; совершенствование техники и технологии на всех этапах ЛТ: предлучевой топометрии, компьютерного планирования и управления процессом облучения, что позволяет осуществлять прецизионное облучение мишени и избегать развития серьёзных осложнений.

КЛАССИФИКАЦИЯ ОПУХОЛЕЙ ПО ПРИЗНАКУ РАДИОЧУВСТВИТЕЛЬНОСТИ

Опухоль гетерогенна по: n Степени дифференцировки (низкая, высокая) n Оксигенотопографии, т. е. степени кислородного насыщения n Фазам клеточного цикла

По радиочувствительности любая опухоль представляется гетерогенной Радиочувствительность отдельных клеток неодинакова в разных фазах клеточного цикла: n наибольшая чувствительность в фазе М (митоза) n наибольшая резистентность в фазе S (синтеза ДНК)

Факторы определяющие радиорезистентность опухоли 1. Гистогенез. Происхождение из тканей с низкой 2. 3. 4. 5. радиочувствительностью. Кровоснабжение и локализация. Высокий процент гипоксичных или аноксичных клеток. Способность к репарации сублетальных повреждений. Размер опухоли. Репопуляция.

Способы преодоления радиорезистентности 1. Насыщение опухоли кислородом 2. 3. 4. 5. 6. (ГБО). Повышение дозы на опухоль при защите нормальных тканей. Терморадиотерапия. Нестандартное фракционирование дозы. Электронакцепторные соединения. Сочетание с лекарственными противоопухолевыми препаратами.
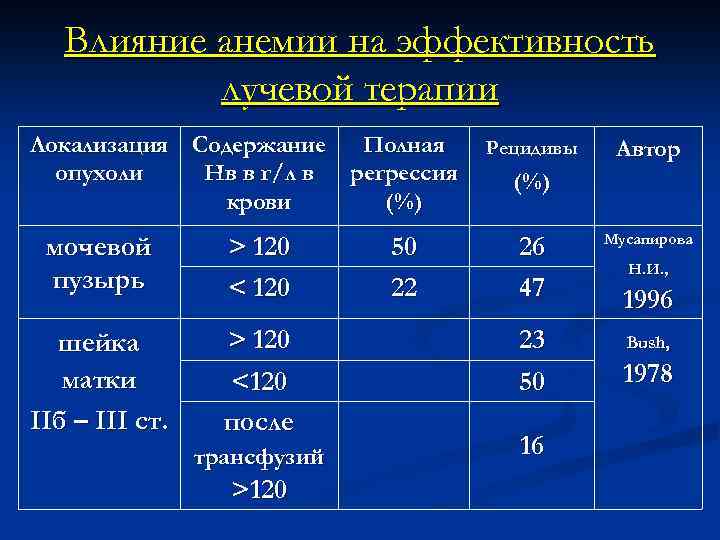
Влияние анемии на эффективность лучевой терапии Локализация Содержание Полная опухоли Нв в г/л в регрессия крови (%) мочевой пузырь > 120 < 120 шейка матки IIб – III ст. > 120 <120 после трансфузий >120 50 22 Рецидивы Автор (%) 26 47 23 50 16 Мусапирова Н. И. , 1996 Bush, 1978

МЕХАНИЗМЫ УСИЛЕНИЯ ПРОТИВООПУХОЛЕВОГО ЭФФЕКТА ПРИ ХИМИОЛУЧЕВОЙ ТЕРАПИИ. 1. 2. 3. 4. 5. 6. Подавление репопуляции опухолевых клеток. Реоксигенация опухоли за счет быстрой её регрессии. Активность некоторых препаратов в отношении гипоксичных клеток и фазы «S» . Частичная синхронизация кл. цикла с накоплением клеток в фазах M и G 1(винка-алкалоиды, таксаны, 5 FU, и др. ) Подавление процессов репарации сублетальных повреждений (платина, антрациклины, антиметаболиты и др. ). Воздействие химиопреаратов на субликические диссеминаты.

ЛЕЧЕБНЫЕ (радикальные) ДОЗЫ ДЛЯ РАЗЛИЧНЫХ ОПУХОЛЕЙ Лечебная доза (Гр) Характер опухоли 20 -30 семинома; ЦНС- при ОЛЛ 30 -40 семинома, оп. Вильмса, нейробластома 40 -50 семинома, ЛГМ, лимфосаркома, базалиома эмбриональный рак, ретинобластома, оп. 50 -60 Юинга, медуллобластома плоскоклеточный рак шейки матки, головы и 60 -65 шеи < 2 см, метастазы в л/у < 2 см рак полости рта (2 -4 см), оп. гортани и глотки, 70 -75 рак мочевого пузыря, шейки и тела матки, рак легкого (< 3 см), метастазы в л/у (< 3 см) 80 или > 80 оп. головы и шеи (> 4 см), оп. молочной железы (> 5 см), остеогенная саркома, меланома, оп. мягких тканей (> 5 см), оп. щитовидной железы, метастазы в л/у > 5 см

Суммарные дозы излучения при химиолучевом лечении 1. При гемобластозах и некоторых солидных опухолях с высокой чувствительностью к лекарственному лечению ЛТ используют как адъювантное средство и СОД могут быть уменьшены на 30 -40% и сост. 30 -50 Гр. 2. Для большинства местнораспространенных ОП, не отличающихся высокой чувствительностью к химиопрепаратам, ЛТ является базовым методом и СОД подводятся на уровне канцерицидных.
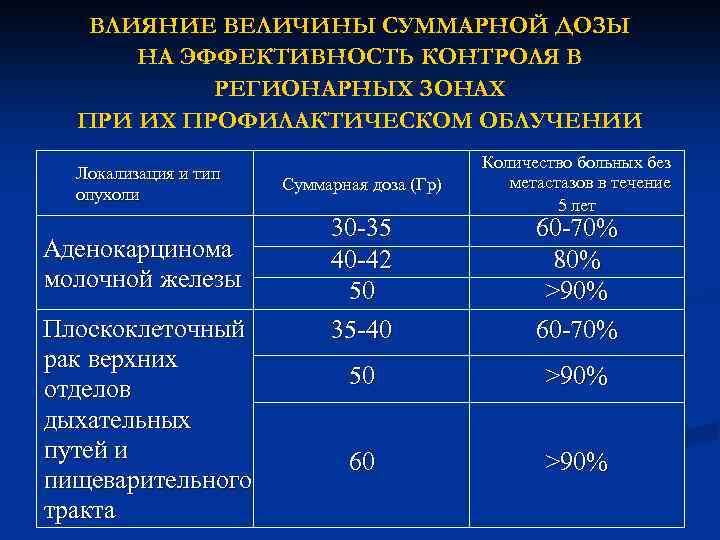
ВЛИЯНИЕ ВЕЛИЧИНЫ СУММАРНОЙ ДОЗЫ НА ЭФФЕКТИВНОСТЬ КОНТРОЛЯ В РЕГИОНАРНЫХ ЗОНАХ ПРИ ИХ ПРОФИЛАКТИЧЕСКОМ ОБЛУЧЕНИИ Локализация и тип опухоли Аденокарцинома молочной железы Плоскоклеточный рак верхних отделов дыхательных путей и пищеварительного тракта Суммарная доза (Гр) 30 -35 40 -42 50 35 -40 Количество больных без метастазов в течение 5 лет 60 -70% 80% >90% 60 -70% 50 >90% 60 >90%

Противопоказания к лучевой терапии n n n n Общее тяжелое состояние пациента (индекс Карновского менее 70) Обширное распространение опухоли, склонной к распаду, кровотечению, серозный выпот, множественные метастазы Активный туберкулез, инфаркт миокарда, острая и хроническая сердечная недостаточность, дыхательная недостаточность 2 -3 степени. Острые инфекционные заболевания Хронические заболевания в стадии декомпенсации Лейкопения Тромбоцитопения Анемия

Современные тенденции в комбинированном лечении злокачественных опухолей n Предоперационное интенсивно-концентрированное облучение (гипофракционирование) при ранних стадиях заболевания стало применяться редко. Продолжает применяться этот вид предоперационной ЛТ при раке прямой кишки. После морфологического уточнения распространенности процесса решается вопрос о дополнительном послеоперационном облучении. При опухолях I-II ст. большинства локализаций на I этапе выполняется операция. Вопрос о целесообразности послеоперационной ЛТ решается по результатам гистологии. n При местно-распространенных опухолях, а также опухолях головы и шеи даже I-II ст. наиболее целесообразна пролонгированная предоперационная ЛТ. Для опухолей чувствительных к ХТ – предоперационная ХЛТ.
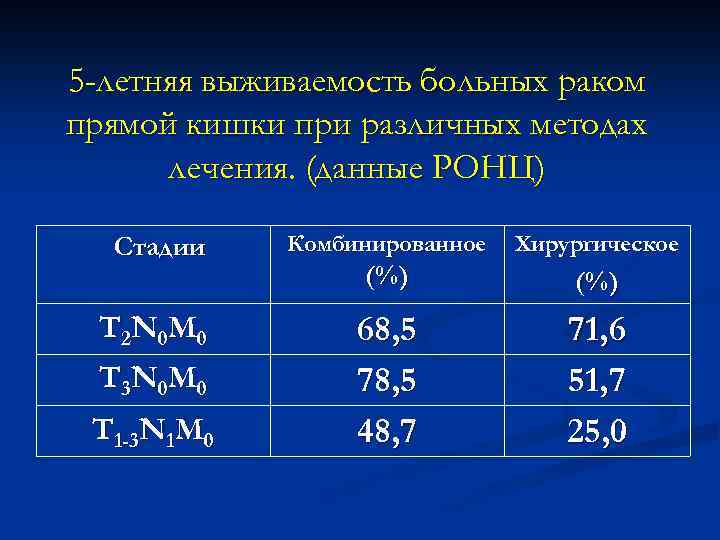
5 -летняя выживаемость больных раком прямой кишки при различных методах лечения. (данные РОНЦ) Стадии T 2 N 0 M 0 T 3 N 0 M 0 T 1 -3 N 1 M 0 Комбинированное Хирургическое (%) 68, 5 78, 5 48, 7 71, 6 51, 7 25, 0
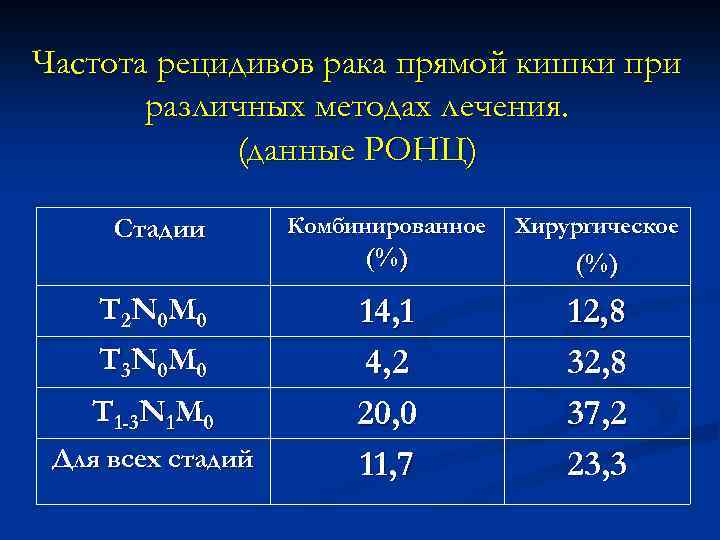
Частота рецидивов рака прямой кишки при различных методах лечения. (данные РОНЦ) Стадии T 2 N 0 M 0 T 3 N 0 M 0 T 1 -3 N 1 M 0 Для всех стадий Комбинированное Хирургическое (%) 14, 1 4, 2 20, 0 11, 7 12, 8 37, 2 23, 3

Сравнительные результаты лечения рака прямой кишки без метастазов в регионарные л/у (Т 2 -3 N 0 M 0). Данные РОНЦ. 5 -лет. выж-сть Рецидивы (%) Отдаленные метастазы (%) I хирургическое 57, 2 23, 3 12, 3 II предоперац. ЛТ + операция (5 Гр х 5 Фр = 25 Гр) 72, 7 13, 4 9, 2 III предоперац. ЛТ с лок. ГТ + операция 82, 3 3, 3 4, 3 Вариант лечения

5 -летняя выживаемость больных раком прямой кишки с метастазами в регионарные л/у (Т 1 -3 N 1 M 0) при различных методах лечения. (данные РОНЦ) Хирургический - 25% Луч. терапия + операция - 48% Луч. терапия + операция + п/операц. ЛТ - 64%

Частота рецидивов у больных нижне-ампулярным раком при различных методах лечения (данные РОНЦ) Хирургическое лечение - 20, 4% Предоперационная ЛТ + операция - 10, 4% ЛТ с локальной ГТ + операция - 5, 6%

Комплексная неоадъювантная терапия рака прямой кишки. Методика ИООД. n Нижнеампулярный отдел и анальный канал Классическое фракционирование, СОД – 44 -46 Гр; прямая кишка, параректальные и паховые лимфоузлы; 5 фторурацил 250 мг в дни облучения. n Среднеампулярный отдел Динамическое фракционирование, СОД – 44 Гр(ВДФ); прямая кишка и внутритазовые лимфоузлы; цисплатин 30 мг 3 дня + 5 ФУ 750 мг 5 дней

Комплексная неоадъювантная терапия рака прямой кишки. Методика ИООД. n Вернеампулярный и ректосигмоидный отдел Среднее фракционирование, РОД – 5, 4 Гр 4 фракции; опухоль толстой кишки; оперативное вмешательство через 24 -48 часов; ПХТ по результатам ПГЗ.

Комплексная неоадъювантная терапия рака прямой кишки. Зарубежная практика. Среднее фракционирование, РОД – 5 Гр 5 фракций; оперативное лечение в день окончания лучевой терапии; ПХТ по результатам ПГЗ.
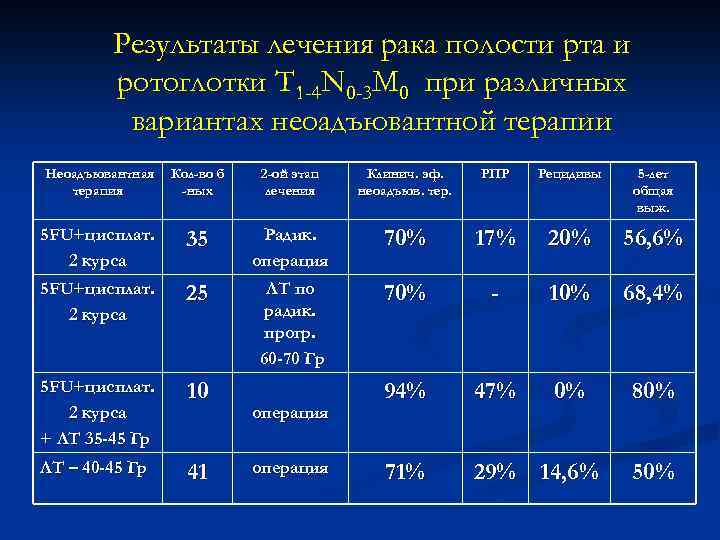
Результаты лечения рака полости рта и ротоглотки T 1 -4 N 0 -3 M 0 при различных вариантах неоадъювантной терапии Неоадъювантная терапия Кол-во б -ных 2 -ой этап лечения Клинич. эф. неоадъюв. тер. РПР Рецидивы 5 -лет общая выж. 5 FU+цисплат. 2 курса 35 Радик. операция 70% 17% 20% 56, 6% 5 FU+цисплат. 2 курса 25 ЛТ по радик. прогр. 60 -70 Гр 70% - 10% 68, 4% 5 FU+цисплат. 2 курса + ЛТ 35 -45 Гр 10 94% 47% 0% 80% ЛТ – 40 -45 Гр 41 71% 29% 14, 6% операция 50%
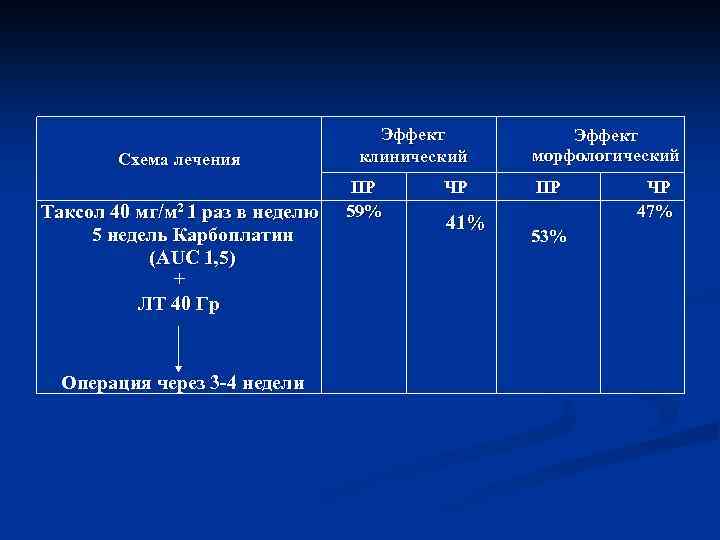
Схема лечения Таксол 40 мг/м 2 1 раз в неделю 5 недель Карбоплатин (AUC 1, 5) + ЛТ 40 Гр Операция через 3 -4 недели Эффект клинический ПР 59% ЧР 41% Эффект морфологический ПР 53% ЧР 47%
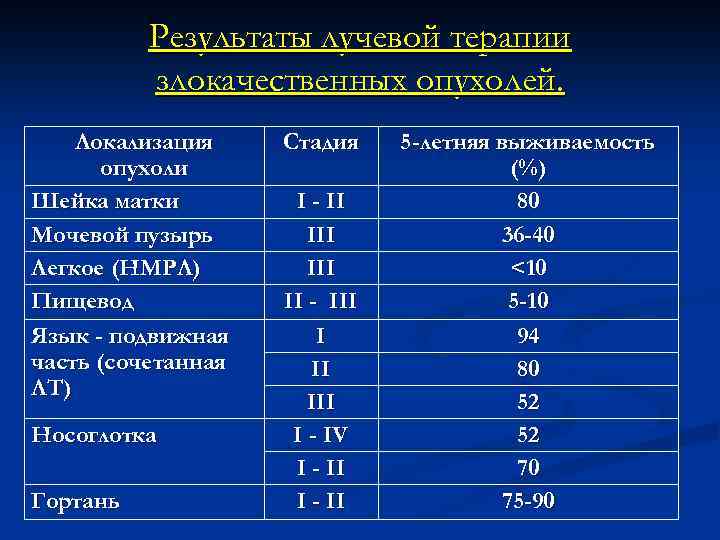
Результаты лучевой терапии злокачественных опухолей. Локализация опухоли Шейка матки Мочевой пузырь Легкое (НМРЛ) Пищевод Язык - подвижная часть (сочетанная ЛТ) Носоглотка Гортань Стадия I - II III II - III I - IV I - II 5 -летняя выживаемость (%) 80 36 -40 <10 5 -10 94 80 52 52 70 75 -90
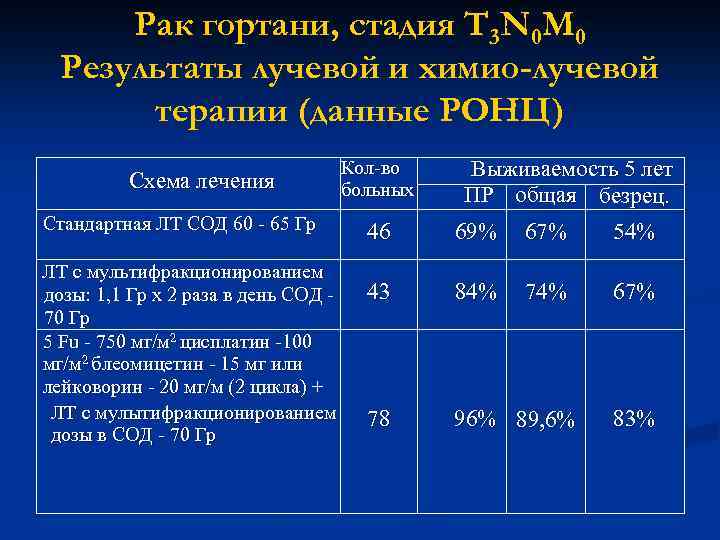
Рак гортани, стадия T 3 N 0 M 0 Результаты лучевой и химио-лучевой терапии (данные РОНЦ) Схема лечения Стандартная ЛТ СОД 60 - 65 Гр ЛТ с мультифракционированием дозы: 1, 1 Гр х 2 раза в день СОД 70 Гр 5 Fu - 750 мг/м 2 цисплатин -100 мг/м 2 блеомицетин - 15 мг или лейковорин - 20 мг/м (2 цикла) + ЛТ с мулытифракционированием дозы в СОД - 70 Гр Кол-во больных Выживаемость 5 лет ПР общая безрец. 46 69% 67% 54% 43 84% 74% 67% 78 96% 89, 6% 83%

Сравнительная эффективность химио-лучевой терапии с одной ЛТ при местно-распространенном раке носоглотки (рандомизированное исследование) Схема лечения ЛТ - - 60 Гр на носоглотку и per. зоны + буст + цисплатин 40 мг/м 21 раз в неделю (8 недель) ЛТ (конвенциональная) Безрецидивная выживаемость 2 года 78% Побочные эффекты Местные лучевые реакции одинаковы в обеих группах. Общая токсичность: тошнота, рвота и миелосупрессия чаще в 1 группе. 62% * ХЛТ может улучшить не только контроль первичной опухоли, но и отдаленных метастазов AT Chan, Гон-Конг, 2000
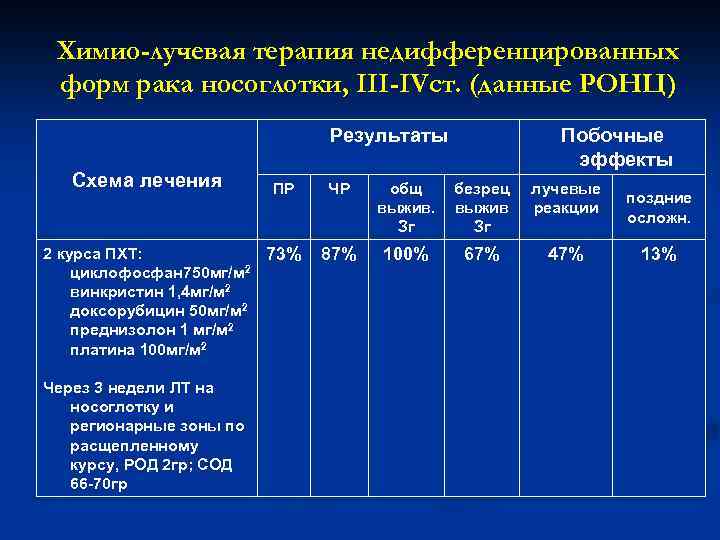
Химио-лучевая терапия недифференцированных форм рака носоглотки, III-IVcт. (данные РОНЦ) Результаты Схема лечения ПР 2 курса ПХТ: 73% 2 циклофосфан 750 мг/м винкристин 1, 4 мг/м 2 доксорубицин 50 мг/м 2 преднизолон 1 мг/м 2 платина 100 мг/м 2 Через 3 недели ЛТ на носоглотку и регионарные зоны по расщепленному курсу, РОД 2 гр; СОД 66 -70 гр Побочные эффекты ЧР общ выжив. Зг безрец выжив Зг лучевые реакции 87% 100% 67% 47% поздние осложн. 13%

Химио-лучевая терапия анального рака Схема лечения 5 Fu-750 мг/м 2 в дни 1 -4 цисплатин 100 мг/м 2 день - 1 3 курса через каждые 21 день Кол-во больны х 12(Т 2 -3) Результаты ПР у 10 из 12 83% безрецидивная выживаемо сть 3 года 10 83% + ЛТ одновременно с XT наружное облучение промежностным полем и на паховые лимфоузлы, РОД 2 Гр, СОД - 44 Гр за 4 недели +внутриполостная терапия РОД – 3 Гр, СОД – 24 -27 Гр * 2 больных с N+ оперированы на лимфопутях

Тактика лечения инвазивного рака мочевого пузыря (Т 2 -4 Nх. М 0) Неоадьювантная ХЛТ ПР продолжение ХЛТ ЧР цистэктомия 5 -летняя выживаемость у больных с ПР на I этапе при Т 2 -4 - 55 -60% только Т 2 - 64 -68% Zietman A. Annu. Meet. ASCO; 1998 Educational BOOK, 329 -336
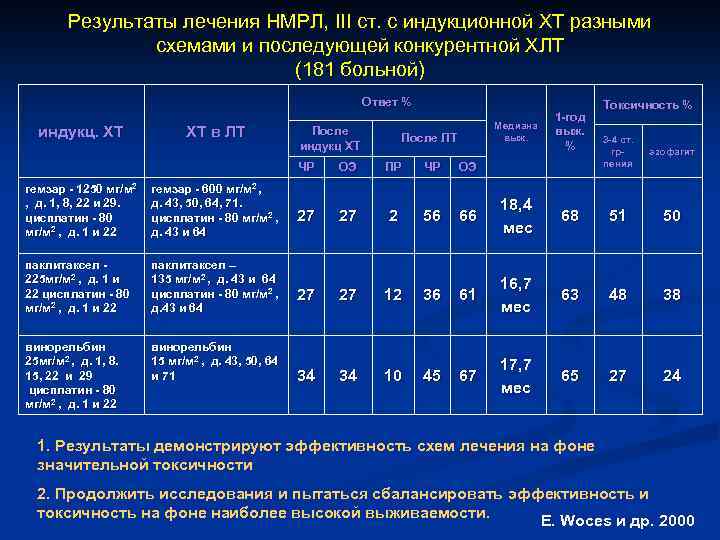
Результаты лечения НМРЛ, III ст. с индукционной ХТ разными схемами и последующей конкурентной ХЛТ (181 больной) Ответ % индукц. ХТ ХТ в ЛТ После индукц ХТ Медиана выж. После ЛТ 1 -год выж. % Токсичность % 3 -4 ст. грпения эзофагит ЧР гемзар - 1250 мг/м 2 , д. 1, 8, 22 и 29. цисплатин - 80 мг/м 2 , д. 1 и 22 гемзар - 600 мг/м 2 , д. 43, 50, 64, 71. цисплатин - 80 мг/м 2 , д. 43 и 64 паклитаксел 225 мг/м 2 , д. 1 и 22 цисплатин - 80 мг/м 2 , д. 1 и 22 паклитаксел – 135 мг/м 2 , д. 43 и 64 цисплатин - 80 мг/м 2 , д. 43 и 64 винорельбин 25 мг/м 2 , д. 1, 8. 15, 22 и 29 цисплатин - 80 мг/м 2 , д. 1 и 22 винорельбин 15 мг/м 2 , д. 43, 50, 64 и 71 ОЭ ПР ЧР ОЭ 27 27 2 56 66 18, 4 мес 68 51 50 27 27 12 36 61 16, 7 мес 63 48 38 34 34 10 45 67 17, 7 мес 65 27 24 1. Результаты демонстрируют эффективность схем лечения на фоне значительной токсичности 2. Продолжить исследования и пытаться сбалансировать эффективность и токсичность на фоне наиболее высокой выживаемости. E. Woces и др. 2000

Химио-лучевая терапия НМРЛ III ст. с консолидацией эффекта таксотером в сравнении с др. схемами Схема лечения Медиана выжив. Выживаемость 1 г 2 г 3 г 39% 58% 34% 17% 78% 50% 40% ЕР/ЛТ операция 17 мес. ЕР/ЛТ РЕ 15 мес. ЕР/ЛТ таксотер 22 мес. 3 цикла ЕР: цисплатин 50 мг/м 2 дни 1, 8 и 29, 36 этопозид 50 мг/м 2 дни 1 -5 и 29 -36 ЛТ – 45 Гр + буст 16 Гр Таксотер 75 мг/м 2 день 71; 92; 113 (3 цикла) ASCO, 2002

Мелкоклеточный рак легкого Для успешного лечения необходимо: 1. Интенсивная терапия сочетанием нескольких препаратов с разным механизмом действия (2 -4 курса). 2. Комбинация с лучевой терапией в дозе 45 -50 Гр. Наиболее часто применяют схемы: CDE; CAV; САМ Эффект ХЛТ: ПР+ЧР - 80 - 90% Полное излечение 5 -10% ПР -30 -50%

Химио-лучевая терапия в сравнении с одной ЛТ у больных раком пищевода Схема лечения Кол-во б-ных Результаты лечения/выживаемость 12 мес 24 мес Медиана 61 50 38 13 мес 62 33 10 9 мес Цисплатин 75 мг/м 2 - 1 ый день 5 Fu - 1000 мг/м 2 с 1 по 4 дни (2 курса с интервалом 4 нед. ) + ЛТ (параллельно с XT) в СОД от 50 до 64 Гр + Адьювантная ХТ 2 курса по той же схеме с интервалом 3 недели после окончания ЛТ ЛТ M. AL - Saraff et al. 1996

Конкурентная химио-лучевая терапия местнораспространенного рака поджелудочной железы Схема ХТ Гемзар 250 мг/м 2 1 р. в неделю кол-во б-х Выживаемость 6 мес. 42 88% токсичность гематол. негематол. 4 ст. 5% 33% + ЛТ, РОД 1, 8 Гр СОД 50, 4 Гр T. Okusaka, 2003
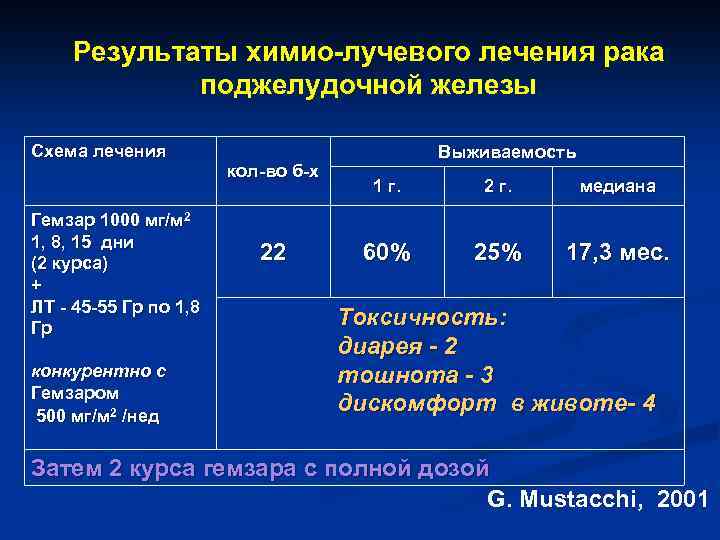
Результаты химио-лучевого лечения рака поджелудочной железы Схема лечения Гемзар 1000 мг/м 2 1, 8, 15 дни (2 курса) + ЛТ - 45 -55 Гр по 1, 8 Гр конкурентно с Гемзаром 500 мг/м 2 /нед кол-во б-х 22 Выживаемость 1 г. 2 г. медиана 60% 25% 17, 3 мес. Токсичность: диарея - 2 тошнота - 3 дискомфорт в животе- 4 Затем 2 курса гемзара с полной дозой G. Mustacchi, 2001
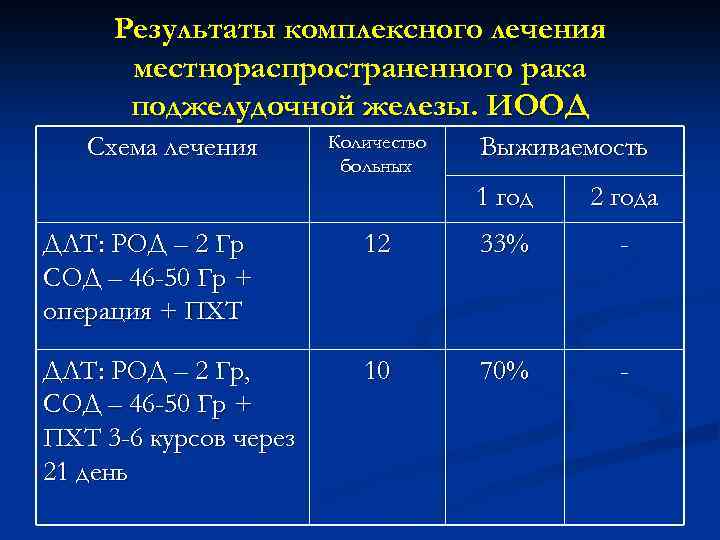
Результаты комплексного лечения местнораспространенного рака поджелудочной железы. ИООД Схема лечения Количество больных Выживаемость 1 год 2 года ДЛТ: РОД – 2 Гр СОД – 46 -50 Гр + операция + ПХТ 12 33% - ДЛТ: РОД – 2 Гр, СОД – 46 -50 Гр + ПХТ 3 -6 курсов через 21 день 10 70% -

Рациональная лучевая терапия операбельного рака молочной железы.

Рациональная лучевая терапия операбельного рака молочной железы (РМЖ) Ø Возросшие технические возможности метода позволяют подводить необходимые дозы излучения как к первичному очагу в МЖ, так и к регионарному лимфатическому коллектору без тяжелых лучевых повреждений нормальных тканей Ø Роль ЛТ в лечении РМЖ за последние десятилетия значительно изменилась: это обусловлено внедрением органосохранных операций; значительным расширением арсенала лекарственной терапии Ø Реже стало применяться послеоперационное облучение после радикальной мастэктомии и значительно возросла роль после органосохранных операций

Адьювантное облучение после радикальной резекции (ИООД) Ø В зону лучевого воздействия включается оставшаяся часть МЖ, РОД 2 Гр, СОД 50 Гр. Буст на ложе опухоли в СОД 10 Гр подводится при повышенном риске рецидива Ø Регионарные зоны рекомендуется облучать в следующих случаях: § при медиальной и центральной локализации - облучение парастернального коллектора, при обнаружении метастазов в аксиллярных л/у -дополнительно надключичного; § при наружной локализации, в случае поражения Зх и более аксиллярных л/у и неблагоприятных морфологических признаках - облучение надключичного и парастернального коллектора; СОД на регионарные зоны 45 -50 Гр Ø Начало послеоперационной ЛТ - через 4 недели после операции
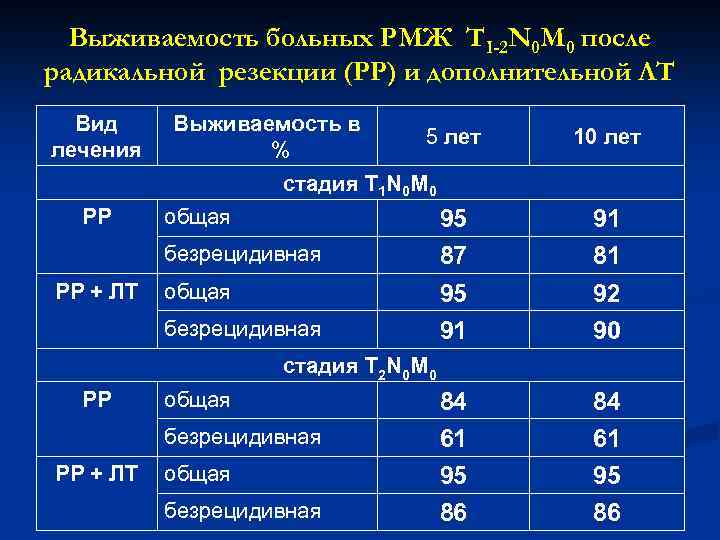
Выживаемость больных РМЖ TI-2 N 0 M 0 после радикальной резекции (РР) и дополнительной ЛТ Вид лечения Выживаемость в % 5 лет 10 лет стадия Т 1 N 0 М 0 РР общая безрецидивная РР + ЛТ общая безрецидивная 95 87 95 91 91 81 92 90 84 61 95 86 стадия T 2 N 0 M 0 РР общая безрецидивная РР + ЛТ общая безрецидивная
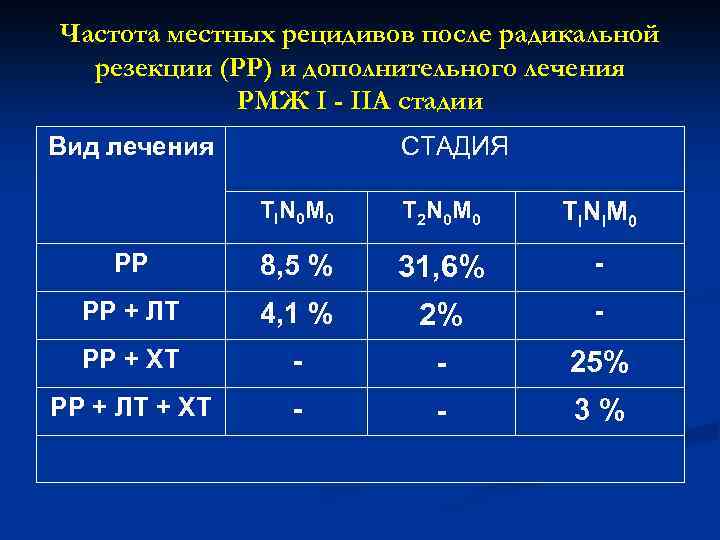
Частота местных рецидивов после радикальной резекции (РР) и дополнительного лечения РМЖ I - IIА стадии Вид лечения СТАДИЯ T I N 0 M 0 T 2 N 0 M 0 Т I N I М 0 РР 8, 5 % 31, 6% - РР + ЛТ 4, 1 % 2% - РР + ХТ - - 25% РР + ЛТ + XT - - 3%
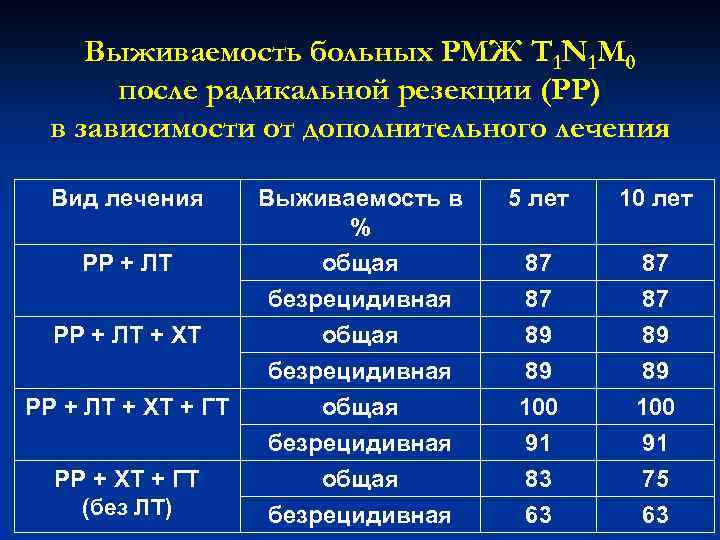
Выживаемость больных РМЖ T 1 N 1 M 0 после радикальной резекции (РР) в зависимости от дополнительного лечения Вид лечения Выживаемость в % 5 лет 10 лет РР + ЛТ общая 87 87 безрецидивная общая безрецидивная 87 89 89 100 91 83 63 87 89 89 100 91 75 63 РР + ЛТ + XT + ГТ РР + XT + ГТ (без ЛТ)
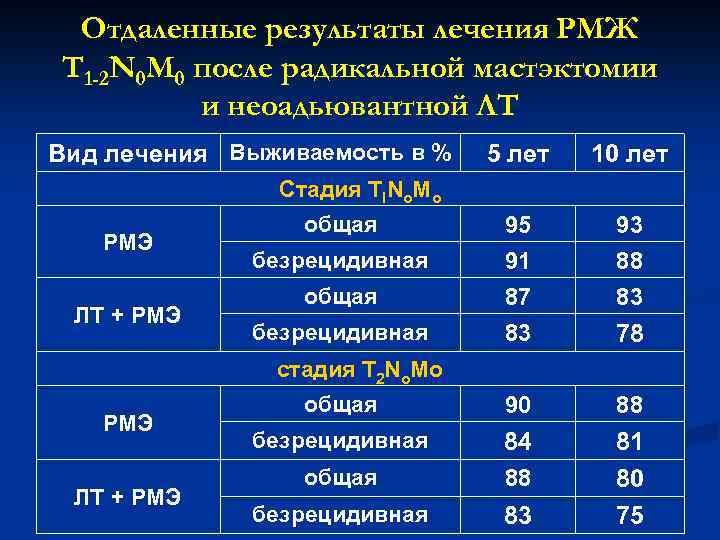
Отдаленные результаты лечения РМЖ T 1 -2 N 0 M 0 после радикальной мастэктомии и неоадьювантной ЛТ Вид лечения Выживаемость в % 5 лет 10 лет 95 91 87 83 93 88 83 78 общая 90 88 безрецидивная общая 84 88 безрецидивная 83 81 80 75 Стадия TINo. Mo РМЭ ЛТ + РМЭ общая безрецидивная стадия T 2 No. Mo РМЭ ЛТ + РМЭ
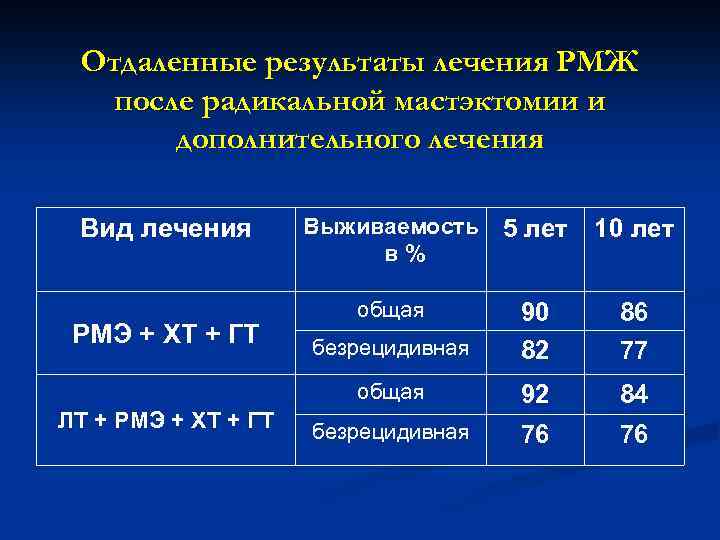
Отдаленные результаты лечения РМЖ после радикальной мастэктомии и дополнительного лечения РМЭ + XT + ГТ ЛТ + РМЭ + XT + ГТ Выживаемость в% 5 лет 10 лет общая безрецидивная 90 82 86 77 общая Вид лечения 92 84 безрецидивная 76 76

Рациональная ЛТ при ранних стадиях (I - IIА) РМЖ n n ЛТ должна быть обязательным компонентом после радикальной резекции рака молочной железы в случае выполнения радикальной мастэктомии -применение интенсивной неоадьювантной ЛТ рака молочной железы I - II А ст. нецелесообразно

Методика лечения начальных форм рака молочной железы Т 1 -2 N 0 М 0 (ИООД) n • РР N – ДЛТ на молочную железу РОД – 2 Гр СОД – 46 -50 Гр PP N + ДЛТ на молочную железу, шейно-надключичные и парастернальные л/у РОД – 2 Гр, СОД – 46 -50 Гр + 4 курса ПХТ n • РМЭ N – наблюдение РМЭ N + ДЛТ на шейнонадключичные и парастернальные лимфоузлы РОД – 2 Гр СОД – 46 Гр
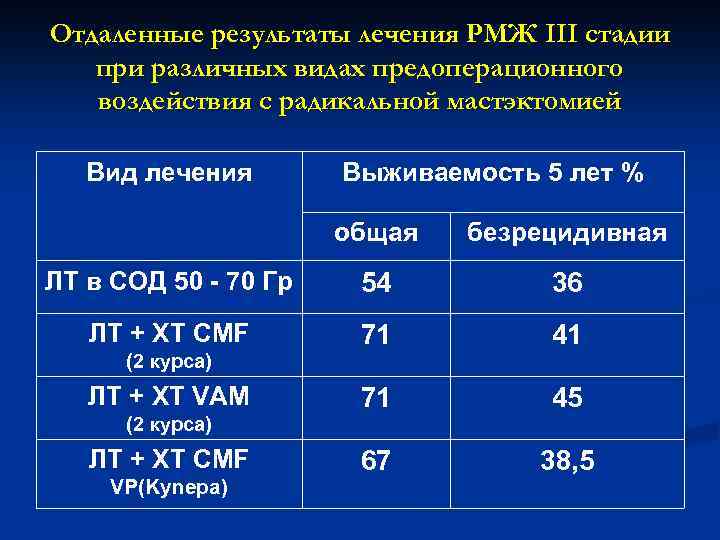
Отдаленные результаты лечения РМЖ III стадии при различных видах предоперационного воздействия с радикальной мастэктомией Вид лечения Выживаемость 5 лет % общая безрецидивная ЛТ в СОД 50 - 70 Гр 54 36 ЛТ + XT CMF 71 41 71 45 67 38, 5 (2 курса) ЛТ + XT VAM (2 курса) ЛТ + XT CMF VP(Kynepa)
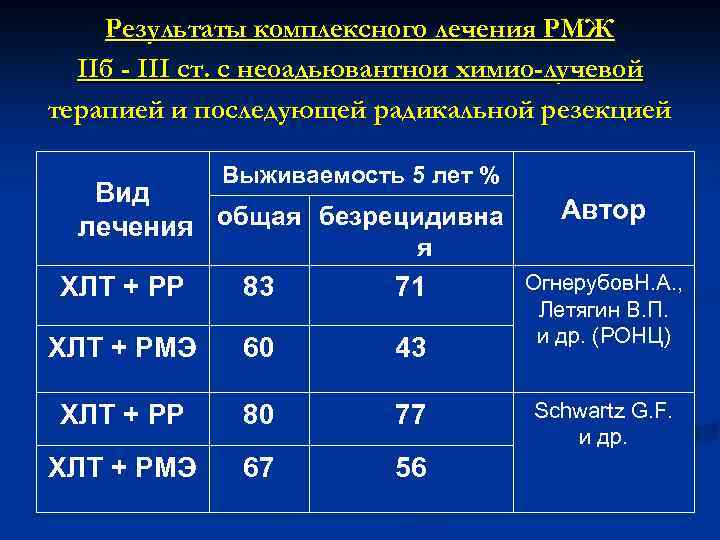
Результаты комплексного лечения РМЖ IIб - III ст. с неоадьювантнои химио-лучевой терапией и последующей радикальной резекцией Выживаемость 5 лет % Вид лечения общая безрецидивна Автор я ХЛТ + РР 83 71 ХЛТ + РМЭ 60 43 ХЛТ + РР 80 77 ХЛТ + РМЭ 67 56 Огнерубов. Н. А. , Летягин В. П. и др. (РОНЦ) Schwartz G. F. и др.

Рак молочной железы -местнораспространенный (T 2 -3 N 1 -2 M 0) методика РОНЦ Комплексное лечение с неоадьювантной ХЛТ уменьшение оп. до 2 см оп > 2 см радикальная резекция радикальная мастэктомия адъювантная XT 5 лет. выживаемость Общая - 83%, безрец. - 71% Схемы XT: ЛТ: 5 лет. выживаемость Общая - 62%, безрец. - 40% CAF, AC, FAC, VAM РОД 2 Гр, СОД 46 -50 Гр.

В лечении местно распространенного РМЖ, наиболее целесообразно использовать ЛТ в комбинации с лекарственными препаратами предоперационно: ü Достигается наибольшая регрессия опухоли ü Наблюдается наиболее выраженный патоморфоз ü Создается возможность выполнить операцию у больных с первично неоперабельными опухолями ü В ряде случаев создается возможность выполнить органосохранную операцию ü Достигается увеличение продолжительности жизни больных

Лечение местнораспространенного рака молочной железы Т 1 -4 N 1 -3 М 0 (ИООД) 6 курсов неоадъювантной ПХТ n ДЛТ РОД – 2 Гр на молочную железу и все группы лимфоузлов СОД – 46 -50 Гр на фоне проведения ДЛТ – 2 курса ПХТ n Радикальная операция n 2 -4 курса адъювантной ПХТ n

Местнораспространенный РМЖ. Послеоперационная ЛТ У больных с неоадьювантной XT послеоперационная ЛТ целесообразна: n на зоны регионарного метастазирования при множественных метастазах в лимфатические узлы, наличии конгломератов, «условной радикальности» их удаления, СОД 46 - 50 Гр n облучение послеоперационного рубца целесообразно при наличии необходимой техники
лучевая терапия злокачественный образований.ppt