3 Соединеия кислорода и серы.ppt
- Количество слайдов: 32
 ЛС, производные Vl группы. Производные кислорода и серы. Вода очищенная. Кислород. Пероксид водорода, пероксид магния. Требования к качеству. Методы оценки качества (фармакопейный анализ). Условия хранения. Применение.
ЛС, производные Vl группы. Производные кислорода и серы. Вода очищенная. Кислород. Пероксид водорода, пероксид магния. Требования к качеству. Методы оценки качества (фармакопейный анализ). Условия хранения. Применение.
 Aqua purificata – Вода очищенная Aqua pro injectionibus – Вода для инъекций H 2 O Ткип = 100 о. С, плотность 1 г/см 3 1. р. Н = 5, 0 – 7, 0 (потенциометрически) 2. сухой остаток (нелетучие примеси) 3. Восстанавливающие вещества (недопустимая примесь) Mn. O 4 - + 8 H+ + 5ē → Mn 2+ + 4 H 2 O розовый бесцв 4. примесь диоксида углерода – углекислого газа (недопустимая примесь) СО 2 + Са(ОН)2 → Са. СО 3 ↓ + Н 2 О
Aqua purificata – Вода очищенная Aqua pro injectionibus – Вода для инъекций H 2 O Ткип = 100 о. С, плотность 1 г/см 3 1. р. Н = 5, 0 – 7, 0 (потенциометрически) 2. сухой остаток (нелетучие примеси) 3. Восстанавливающие вещества (недопустимая примесь) Mn. O 4 - + 8 H+ + 5ē → Mn 2+ + 4 H 2 O розовый бесцв 4. примесь диоксида углерода – углекислого газа (недопустимая примесь) СО 2 + Са(ОН)2 → Са. СО 3 ↓ + Н 2 О
 5. Нитраты и нитриты (недопустимая примесь) 6. ионы аммония (допустимая примесь) не более 0, 00002%, т. е. эталон разводят в 10 раз. 7 -10. соли тяжелых металлов, хлориды, сульфаты и ионы кальция (недопустимые примеси). • микробиологическая чистота - не более 100 микроорганизмов в 1 мл при отсутствии бактерий сем. Enterobacteriaceae, Staphylococcus aureus, Pseudomonas aeruqinosa.
5. Нитраты и нитриты (недопустимая примесь) 6. ионы аммония (допустимая примесь) не более 0, 00002%, т. е. эталон разводят в 10 раз. 7 -10. соли тяжелых металлов, хлориды, сульфаты и ионы кальция (недопустимые примеси). • микробиологическая чистота - не более 100 микроорганизмов в 1 мл при отсутствии бактерий сем. Enterobacteriaceae, Staphylococcus aureus, Pseudomonas aeruqinosa.
 • Вода для инъекций дополнительно должна быть апирогенной, не содержать антимикробных веществ и других добавок. № 309 «Об утверждении инструкции по санитарному режиму аптеки» № 214 «О контроле качества ЛС, изготовляемых в аптеках» хранят в асептических условиях. Вода очищенная – не более 3 суток. Вода для инъекций – не более суток при температуре 5 -10 о. С либо 80 -90 о. С.
• Вода для инъекций дополнительно должна быть апирогенной, не содержать антимикробных веществ и других добавок. № 309 «Об утверждении инструкции по санитарному режиму аптеки» № 214 «О контроле качества ЛС, изготовляемых в аптеках» хранят в асептических условиях. Вода очищенная – не более 3 суток. Вода для инъекций – не более суток при температуре 5 -10 о. С либо 80 -90 о. С.
 Кислород Oxygenium О 2 Получение Катод: | Анод: 2 К+ + 2ē → 2 К 2 ОН- - 2ē → 2 ОН 2 К + 2 Н 2 О → 2 КОН + Н 2 2 ОН → Н 2 О + ½ О 2
Кислород Oxygenium О 2 Получение Катод: | Анод: 2 К+ + 2ē → 2 К 2 ОН- - 2ē → 2 ОН 2 К + 2 Н 2 О → 2 КОН + Н 2 2 ОН → Н 2 О + ½ О 2
 Подлинность 1. тлеющая лучина, внесенная в сосуд с кислородом, вспыхивает и ярко горит 2. «лисий хвост» - выделение оранжевокрасного газа оксида азота (IV). O 2 + 2 NO → 2 NO 2 оранжево- красный O 2 + 2 N 2 O ≠ чистота испытание на содержание газообразных примесей: оксида и диоксида углерода, оксидов азота (II, IV), молекулярного хлора, озона, хлороводорода.
Подлинность 1. тлеющая лучина, внесенная в сосуд с кислородом, вспыхивает и ярко горит 2. «лисий хвост» - выделение оранжевокрасного газа оксида азота (IV). O 2 + 2 NO → 2 NO 2 оранжево- красный O 2 + 2 N 2 O ≠ чистота испытание на содержание газообразных примесей: оксида и диоксида углерода, оксидов азота (II, IV), молекулярного хлора, озона, хлороводорода.
 1. диоксид углерода СО 2 (недопустимая примесь) Ва(ОН)2 + СО 2 → Ва. СО 3 ↓ + Н 2 О Са(ОН)2 + СО 2 → Са. СО 3 ↓ + Н 2 О 2. оксид углерода СО (недопустимая примесь) CO + 2[Ag(NH 3)2]NO 3 + 2 H 2 O → 2 Ag↓ + 2 NH 4 NO 3 + (NH 4)2 CO 3
1. диоксид углерода СО 2 (недопустимая примесь) Ва(ОН)2 + СО 2 → Ва. СО 3 ↓ + Н 2 О Са(ОН)2 + СО 2 → Са. СО 3 ↓ + Н 2 О 2. оксид углерода СО (недопустимая примесь) CO + 2[Ag(NH 3)2]NO 3 + 2 H 2 O → 2 Ag↓ + 2 NH 4 NO 3 + (NH 4)2 CO 3
 3. оксиды азота (II, IV) NO и NO 2 NO + NO 2 + 2 KOH → 2 KNO 2 + H 2 O 2 KNO 2 + H 2 SO 4 → 2 HNO 2 + 2 K 2 SO 4 2 KI + H 2 SO 4 → 2 HI + K 2 SO 4 2 HNO 2 + 2 HI → I 2 + 2 NO↑+ 2 H 2 O 4. хлор и озон Cl 2 + 2 KI → I 2 + 2 KCl O 3 + 2 KI + H 2 O → I 2 + O 2↑ +2 KOH 5. Хлороводород H 2 O+ метиловый красный
3. оксиды азота (II, IV) NO и NO 2 NO + NO 2 + 2 KOH → 2 KNO 2 + H 2 O 2 KNO 2 + H 2 SO 4 → 2 HNO 2 + 2 K 2 SO 4 2 KI + H 2 SO 4 → 2 HI + K 2 SO 4 2 HNO 2 + 2 HI → I 2 + 2 NO↑+ 2 H 2 O 4. хлор и озон Cl 2 + 2 KI → I 2 + 2 KCl O 3 + 2 KI + H 2 O → I 2 + O 2↑ +2 KOH 5. Хлороводород H 2 O+ метиловый красный
 Количественное определение Поглотительный раствор (Cu, NH 4 OH, NH 4 Cl) в приборе Гемпеля 2 Cu + O 2 → 2 Cu. O + 2 NH 4 OH + 2 NH 4 Cl → [Cu(NH 3)4]Cl + 3 H 2 O
Количественное определение Поглотительный раствор (Cu, NH 4 OH, NH 4 Cl) в приборе Гемпеля 2 Cu + O 2 → 2 Cu. O + 2 NH 4 OH + 2 NH 4 Cl → [Cu(NH 3)4]Cl + 3 H 2 O
 Раствор водорода пероксида – Solutio Hydrogenii peroxydi diluta Н 2 О 2 3% (2, 7%-3, 3%) Состав: Раствора водорода пероксида концентрированного (пергидроля) 27, 5 – 31 % от 7, 5 до 11 г (в зависимости от фактического содержания); Натрия бензоата 0, 05 г; Воды очищенной до 100 мл Solutio Hydrogenii peroxydi concentrate (Perhydrolum) 30%, 27, 5 – 31%
Раствор водорода пероксида – Solutio Hydrogenii peroxydi diluta Н 2 О 2 3% (2, 7%-3, 3%) Состав: Раствора водорода пероксида концентрированного (пергидроля) 27, 5 – 31 % от 7, 5 до 11 г (в зависимости от фактического содержания); Натрия бензоата 0, 05 г; Воды очищенной до 100 мл Solutio Hydrogenii peroxydi concentrate (Perhydrolum) 30%, 27, 5 – 31%
 Получение: впервые Луи Тенаром в 1818. Ba. O 2 + 2 HCl H 2 O 2 + Ba. Cl 2 Промышленный способ – электролитический: H 2 SO 4 + H 2 O ↔H 3 O+ + HSO 4 Катод: 2 H 3 O++ 2ē → 2 H 3 O → 2 H 2 O + H 2↑ Анод: 2 HSO 4 - - 2ē→ 2 HSO 4 → H 2 S 2 O 8 пероксодисерная кислота
Получение: впервые Луи Тенаром в 1818. Ba. O 2 + 2 HCl H 2 O 2 + Ba. Cl 2 Промышленный способ – электролитический: H 2 SO 4 + H 2 O ↔H 3 O+ + HSO 4 Катод: 2 H 3 O++ 2ē → 2 H 3 O → 2 H 2 O + H 2↑ Анод: 2 HSO 4 - - 2ē→ 2 HSO 4 → H 2 S 2 O 8 пероксодисерная кислота
 Суммарно 2 H 2 SO 4 → H 2 S 2 O 8 + H 2↑ электролиз H 2 S 2 O 8 + 2 H 2 O → 2 H 2 SO 4 + H 2 O 2 концентрируют путем перегонки в вакууме до получения 27, 5 - 40% раствора (раствор водорода пероксида концентрированный; пергидроль) Химические свойства 1. Кислотно-основные: слабая кислота р. Н 3, 8 – 5, 6 (потенциометрически) Н 2 О 2 ↔ Н+ + НО 2 -
Суммарно 2 H 2 SO 4 → H 2 S 2 O 8 + H 2↑ электролиз H 2 S 2 O 8 + 2 H 2 O → 2 H 2 SO 4 + H 2 O 2 концентрируют путем перегонки в вакууме до получения 27, 5 - 40% раствора (раствор водорода пероксида концентрированный; пергидроль) Химические свойства 1. Кислотно-основные: слабая кислота р. Н 3, 8 – 5, 6 (потенциометрически) Н 2 О 2 ↔ Н+ + НО 2 -
 Образует соли с гидроксидами металлов: Ва(ОН)2 + Н 2 О 2 → Ва. О 2↓ + 2 Н 2 О Na. OH + H 2 O 2 → Na. HO 2 + Н 2 О Соли неустойчивы Na. HO 2 +HCl → H 2 O 2 + Na. Cl Mg. O 2 + H 2 SO 4 → H 2 O 2 + Mg. SO 4 2. Легко разлагается (реакции разложения) Н 2 О 2 + 2 Н+ + 2ē → 2 Н 2 О H 2 O 2 - 2ē → O 2↑ + 2 H+ 2 Н 2 О 2 ↔ О 2↑ + 2 Н 2 О
Образует соли с гидроксидами металлов: Ва(ОН)2 + Н 2 О 2 → Ва. О 2↓ + 2 Н 2 О Na. OH + H 2 O 2 → Na. HO 2 + Н 2 О Соли неустойчивы Na. HO 2 +HCl → H 2 O 2 + Na. Cl Mg. O 2 + H 2 SO 4 → H 2 O 2 + Mg. SO 4 2. Легко разлагается (реакции разложения) Н 2 О 2 + 2 Н+ + 2ē → 2 Н 2 О H 2 O 2 - 2ē → O 2↑ + 2 H+ 2 Н 2 О 2 ↔ О 2↑ + 2 Н 2 О
 Факторы (катализаторы) разложения: свет, нагревание, окислители и восстановители, щелочи, металлы (железо, медь, марганец и др). натрия бензоат - стабилизатор по ФС 3. Окислительно-восстановительные: является и окислителем и восстановителем, более характерны окислительные свойства (окислительный распад):
Факторы (катализаторы) разложения: свет, нагревание, окислители и восстановители, щелочи, металлы (железо, медь, марганец и др). натрия бензоат - стабилизатор по ФС 3. Окислительно-восстановительные: является и окислителем и восстановителем, более характерны окислительные свойства (окислительный распад):
 Окислительный распад Н 2 О 2 + 2 Н+ + 2ē → 2 Н 2 О в кислой среде H 2 O 2 + 2 KI + H 2 SO 4 → I 2 + K 2 SO 4 + 2 H 2 O в щелочной среде 3 H 2 O 2 + Cr 2(SO 4)3 + 10 Na. OH → 2 Na 2 Cr. O 4 + 3 Na 2 SO 4 + 8 H 2 O Восстановительный распад H 2 O 2 - 2ē → O 2↑ + 2 H+ 2 KMn. O 4 + 5 H 2 O 2 + 3 H 2 SO 4 → 2 Mn. SO 4 + 5 O 2↑ + K 2 SO 4 + 8 H 2 O
Окислительный распад Н 2 О 2 + 2 Н+ + 2ē → 2 Н 2 О в кислой среде H 2 O 2 + 2 KI + H 2 SO 4 → I 2 + K 2 SO 4 + 2 H 2 O в щелочной среде 3 H 2 O 2 + Cr 2(SO 4)3 + 10 Na. OH → 2 Na 2 Cr. O 4 + 3 Na 2 SO 4 + 8 H 2 O Восстановительный распад H 2 O 2 - 2ē → O 2↑ + 2 H+ 2 KMn. O 4 + 5 H 2 O 2 + 3 H 2 SO 4 → 2 Mn. SO 4 + 5 O 2↑ + K 2 SO 4 + 8 H 2 O
 реакция диспропорционирования Окислительный распад H 2 O 2 + 2 H+ + 2ē → 2 H 2 O Восстановительный распад H 2 O 2 - 2ē → 2 H+ + O 2 Суммарно: 2 H 2 O 2 → 2 H 2 O + O 2↑ Подлинность: ФС специфическая, общая для группы – реакция образования надхромовых кислот (окислительный распад):
реакция диспропорционирования Окислительный распад H 2 O 2 + 2 H+ + 2ē → 2 H 2 O Восстановительный распад H 2 O 2 - 2ē → 2 H+ + O 2 Суммарно: 2 H 2 O 2 → 2 H 2 O + O 2↑ Подлинность: ФС специфическая, общая для группы – реакция образования надхромовых кислот (окислительный распад):
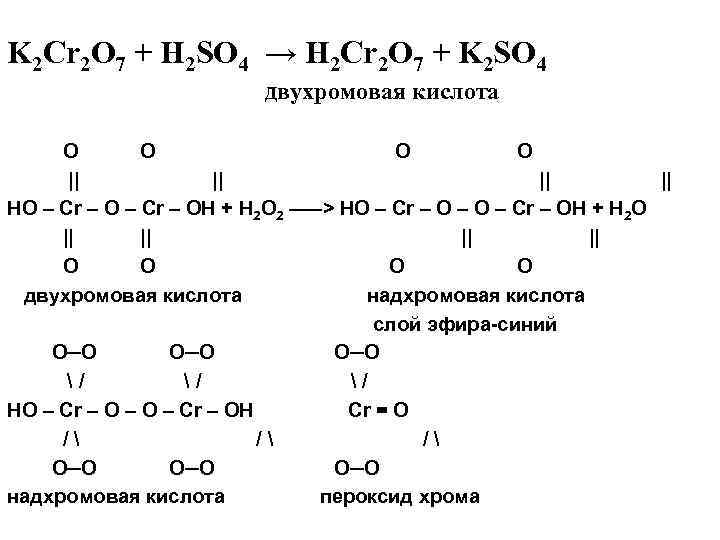 K 2 Cr 2 O 7 + H 2 SO 4 → H 2 Cr 2 O 7 + K 2 SO 4 двухромовая кислота O O O || || || HO – Cr – OH + H 2 O 2 –––> HO – Cr – OH + H 2 O || || || O O O двухромовая кислота надхромовая кислота слой эфира-синий O─O / HO – Cr – OH Cr = O / O─O O─O надхромовая кислота пероксид хрома
K 2 Cr 2 O 7 + H 2 SO 4 → H 2 Cr 2 O 7 + K 2 SO 4 двухромовая кислота O O O || || || HO – Cr – OH + H 2 O 2 –––> HO – Cr – OH + H 2 O || || || O O O двухромовая кислота надхромовая кислота слой эфира-синий O─O / HO – Cr – OH Cr = O / O─O O─O надхромовая кислота пероксид хрома
 Количественное определение 1. Фармакопейный - перманганатометрия в среде разведенной серной кислоты (восстановительный распад) 2. Иодометрия в среде разведенной серной кислоты (окислительный распад) Расчеты концентрации в титриметрии. рельные частицы (РЧ) условные частицы (УЧ)
Количественное определение 1. Фармакопейный - перманганатометрия в среде разведенной серной кислоты (восстановительный распад) 2. Иодометрия в среде разведенной серной кислоты (окислительный распад) Расчеты концентрации в титриметрии. рельные частицы (РЧ) условные частицы (УЧ)
 Растворы с молярной концентрацией вещества (РЧ) 1 Раствор хлористоводородной кислоты(HCl) 2 Раствор хлорной кислоты(HCl. O 4) 3 Раствор натра едкого(Na. OH) 4 Раствор кали едкого(KOH) 5 Раствор натрия метилата(CH 3 ONa) 6 Раствор серебра нитрата(Ag. NO 3) 7 Раствор аммония роданида(NH 4 SCN) 8 Раствор трилона Б (Tr Б) 9 Раствор натрия нитрита (Na. NO 2) 10 Раствор натрия тиосульфата(Na 2 S 2 O 3) 11 Раствор церия сульфата (Ce(SO ) )
Растворы с молярной концентрацией вещества (РЧ) 1 Раствор хлористоводородной кислоты(HCl) 2 Раствор хлорной кислоты(HCl. O 4) 3 Раствор натра едкого(Na. OH) 4 Раствор кали едкого(KOH) 5 Раствор натрия метилата(CH 3 ONa) 6 Раствор серебра нитрата(Ag. NO 3) 7 Раствор аммония роданида(NH 4 SCN) 8 Раствор трилона Б (Tr Б) 9 Раствор натрия нитрита (Na. NO 2) 10 Раствор натрия тиосульфата(Na 2 S 2 O 3) 11 Раствор церия сульфата (Ce(SO ) )
 Растворы с молярной концентрацией эквивалента вещества (УЧ) 1 Раствор серной кислоты УЧ (½ H 2 SO 4) 2 Р-р ртути окисной нитрата УЧ [½ Hg(NO 3)2] 3 Раствор йода УЧ (½ I 2) 4 Раствор йодмонохлорида УЧ (½ ICl) 5 Раствор калия йодата УЧ (1/6 KIO 3) 6 Раствор калия бромата УЧ (1/6 KBr. O 3) 7 Раствор калия перманганата УЧ (1/5 KMn. O 4)
Растворы с молярной концентрацией эквивалента вещества (УЧ) 1 Раствор серной кислоты УЧ (½ H 2 SO 4) 2 Р-р ртути окисной нитрата УЧ [½ Hg(NO 3)2] 3 Раствор йода УЧ (½ I 2) 4 Раствор йодмонохлорида УЧ (½ ICl) 5 Раствор калия йодата УЧ (1/6 KIO 3) 6 Раствор калия бромата УЧ (1/6 KBr. O 3) 7 Раствор калия перманганата УЧ (1/5 KMn. O 4)
 1. Коэффициент стехиометричности К стех = n моль вещества n моль титранта 2. Фактор эквивалентности (fэкв) если титрант РЧ, то fэкв = Кстех если титрант УЧ, то fэкв = Кстех · УЧ 3. Молярная масса эквивалента, (Э или Мэ) М. э = fэкв · М. м 4. Титр (Т) Т = М. э · Ст-та /1000 г/мл 5. Составление расчетной формулы С% = V· К· T· 100 % а
1. Коэффициент стехиометричности К стех = n моль вещества n моль титранта 2. Фактор эквивалентности (fэкв) если титрант РЧ, то fэкв = Кстех если титрант УЧ, то fэкв = Кстех · УЧ 3. Молярная масса эквивалента, (Э или Мэ) М. э = fэкв · М. м 4. Титр (Т) Т = М. э · Ст-та /1000 г/мл 5. Составление расчетной формулы С% = V· К· T· 100 % а
 Где: С –концентрация определенного вещества в % V – объем титранта в мл К – коэффициент поправки на титрант Т – титр по определенному веществу а – масса в гр или объем в мл анализируемого вещества, взятый для анализа Если расчет в гр на объем или массу ЛФ С = V · К · T · Р а , где Р – объем или масса ЛФ Если титрование обратное V = (V 1· К 1 – V 2 · К 2)
Где: С –концентрация определенного вещества в % V – объем титранта в мл К – коэффициент поправки на титрант Т – титр по определенному веществу а – масса в гр или объем в мл анализируемого вещества, взятый для анализа Если расчет в гр на объем или массу ЛФ С = V · К · T · Р а , где Р – объем или масса ЛФ Если титрование обратное V = (V 1· К 1 – V 2 · К 2)
 С = (V 1· К 1 – V 2 · К 2) · T · 100% а Если предварительно сделали разведение и титровали часть полученного разведения С% = V· К· T· Vк · 100% а · Vпр Vк – объем мерной колбы в мл Vпр – объем разведения, взятый для титрования (аликвотная доля), в мл
С = (V 1· К 1 – V 2 · К 2) · T · 100% а Если предварительно сделали разведение и титровали часть полученного разведения С% = V· К· T· Vк · 100% а · Vпр Vк – объем мерной колбы в мл Vпр – объем разведения, взятый для титрования (аликвотная доля), в мл
 1. Перманганатометрия H 2 O 2 2 KMn. O 4 + 5 H 2 O 2 + 3 H 2 SO 4 → 2 Mn. SO 4 + 5 O 2↑+K 2 SO 4 + 8 H 2 O Восст. распад H 2 O 2 - 2ē → 2 H+ + O 2 Кстех = 5 моль H 2 O 2 . = 5/2; 2 моль KMn. O 4 fэкв = Кстех · УЧ=5/2 · 1/5 = ½ ; М. м Н 2 О 2 = 34, 02 М. э (Э) = fэкв · М. м Н 2 О 2 = ½ М. м Н 2 О 2 = 34, 01 / 2 = 17, 01
1. Перманганатометрия H 2 O 2 2 KMn. O 4 + 5 H 2 O 2 + 3 H 2 SO 4 → 2 Mn. SO 4 + 5 O 2↑+K 2 SO 4 + 8 H 2 O Восст. распад H 2 O 2 - 2ē → 2 H+ + O 2 Кстех = 5 моль H 2 O 2 . = 5/2; 2 моль KMn. O 4 fэкв = Кстех · УЧ=5/2 · 1/5 = ½ ; М. м Н 2 О 2 = 34, 02 М. э (Э) = fэкв · М. м Н 2 О 2 = ½ М. м Н 2 О 2 = 34, 01 / 2 = 17, 01
 Т = Ст-та · М. э = 17, 01· 0, 1 / 1000 = 0, 001701 1000 С% =V KMn. O 4 · К KMn. O 4· TH 2 O 2/0, 1 н KMn. O 4 · 100% 10 · 10 2. Йодометрический метод H 2 O 2 + 2 KI + H 2 SO 4 → I 2 + K 2 SO 4 + 2 H 2 O I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6 1 моль пероксида → 1 моль йода→ 2 моль тиосульфата натрия → Кстех = 1 моль пероксида/2 моль тиосульфата натрия = ½
Т = Ст-та · М. э = 17, 01· 0, 1 / 1000 = 0, 001701 1000 С% =V KMn. O 4 · К KMn. O 4· TH 2 O 2/0, 1 н KMn. O 4 · 100% 10 · 10 2. Йодометрический метод H 2 O 2 + 2 KI + H 2 SO 4 → I 2 + K 2 SO 4 + 2 H 2 O I 2 + 2 Na 2 S 2 O 3 → 2 Na. I + Na 2 S 4 O 6 1 моль пероксида → 1 моль йода→ 2 моль тиосульфата натрия → Кстех = 1 моль пероксида/2 моль тиосульфата натрия = ½
 Кстех = 1 моль H 2 O 2 . = ½; 2 моль Na 2 S 2 O 3 fэкв = Кстех· РЧ = ½ · 1. = ½ ; М. э = fэкв · М. м Н 2 О 2 = ½ М. м Н 2 О 2 Magnesii peroxydum – Магния пероксид смесь оксида и пероксида магния Mg. O+Mg. O 2 Получение Mg. Cl 2 + KOH → Mg. O + 2 KCl + H 2 O Mg. O + H 2 O 2 → Mg. O 2 + H 2 O
Кстех = 1 моль H 2 O 2 . = ½; 2 моль Na 2 S 2 O 3 fэкв = Кстех· РЧ = ½ · 1. = ½ ; М. э = fэкв · М. м Н 2 О 2 = ½ М. м Н 2 О 2 Magnesii peroxydum – Магния пероксид смесь оксида и пероксида магния Mg. O+Mg. O 2 Получение Mg. Cl 2 + KOH → Mg. O + 2 KCl + H 2 O Mg. O + H 2 O 2 → Mg. O 2 + H 2 O
 Подлинность предварительное растворение в разв. кислотах Mg. O 2 + 2 HCl → Mg. Cl 2 + H 2 O 2 Mg. O + 2 HCl → Mg. Cl 2 + H 2 O 1. Ион магния с гидрофосфатом натрия в щелочной среде раствора аммиака в присутствии аммония хлорида: Mg. Cl 2 + Na 2 HPO 4 + NH 4 OH + NH 4 Cl → Mg. NH 4 PO 4↓ +2 Na. Cl + H 2 O Белый крист. 2. Пероксид водорода – по реакции образования надхромовых кислот;
Подлинность предварительное растворение в разв. кислотах Mg. O 2 + 2 HCl → Mg. Cl 2 + H 2 O 2 Mg. O + 2 HCl → Mg. Cl 2 + H 2 O 1. Ион магния с гидрофосфатом натрия в щелочной среде раствора аммиака в присутствии аммония хлорида: Mg. Cl 2 + Na 2 HPO 4 + NH 4 OH + NH 4 Cl → Mg. NH 4 PO 4↓ +2 Na. Cl + H 2 O Белый крист. 2. Пероксид водорода – по реакции образования надхромовых кислот;
 Количественное определение Mg. O 2 + 2 HCl → Mg. Cl 2 + H 2 O 2 перманганатометрия (см. пероксид водорода) Hydroperitum – Гидроперит H 2 O 2 • H 2 N-CO-NH 2 + лимоная кислота
Количественное определение Mg. O 2 + 2 HCl → Mg. Cl 2 + H 2 O 2 перманганатометрия (см. пероксид водорода) Hydroperitum – Гидроперит H 2 O 2 • H 2 N-CO-NH 2 + лимоная кислота
 Натрия тиосульфат Natrii thiosulfas Na 2 S 2 O 3 • 5 H 2 O Sodium thiosulfate (MHH) Натриевая соль тиосерной кислоты 1799 г Химические свойства. Реакция разложения Na 2 S 2 O 3 + CO 2 + H 2 O → Na 2 CO 3 + H 2 S 2 O 3 → S↓ + SO 2↑ + H 2 O желтый (муть) запах Подлинность 1. реакции на ион натрия (см. катины-анионы) 2. Реакции на тиосульфат-ион
Натрия тиосульфат Natrii thiosulfas Na 2 S 2 O 3 • 5 H 2 O Sodium thiosulfate (MHH) Натриевая соль тиосерной кислоты 1799 г Химические свойства. Реакция разложения Na 2 S 2 O 3 + CO 2 + H 2 O → Na 2 CO 3 + H 2 S 2 O 3 → S↓ + SO 2↑ + H 2 O желтый (муть) запах Подлинность 1. реакции на ион натрия (см. катины-анионы) 2. Реакции на тиосульфат-ион
 А. Реакция разложения с кислотой хлороводородной разведенной Na 2 S 2 O 3 + 2 НСl → 2 Na. Cl + SO 2↑ + S↓+ H 2 O S 2 - - 2ē = S↓ запах желтый(муть) S 6+ + 2ē = S 4+ Б. Реакция с раствором серебра нитрата. Na 2 S 2 O 3 + 2 Ag. N 03 → Ag 2 S 2 O 3 ↓ + 2 Na. N 03 белый Ag 2 S 2 O 3 → Ag 2 SO 3↓ + S↓желтый осадок Ag 2 SO 3 + S + H 2 O → Ag 2 S↓ + H 2 SO 4 черный белый → желтый → бурый → черный
А. Реакция разложения с кислотой хлороводородной разведенной Na 2 S 2 O 3 + 2 НСl → 2 Na. Cl + SO 2↑ + S↓+ H 2 O S 2 - - 2ē = S↓ запах желтый(муть) S 6+ + 2ē = S 4+ Б. Реакция с раствором серебра нитрата. Na 2 S 2 O 3 + 2 Ag. N 03 → Ag 2 S 2 O 3 ↓ + 2 Na. N 03 белый Ag 2 S 2 O 3 → Ag 2 SO 3↓ + S↓желтый осадок Ag 2 SO 3 + S + H 2 O → Ag 2 S↓ + H 2 SO 4 черный белый → желтый → бурый → черный
 Чистота -недопустимые примеси 1. Сульфиты и сульфаты SO 32 - + I 2 + H 2 O → SO 42 - + 2 HI SO 42 - + Ва(NO 3)2 → Ва. SO 4↓ + 2 NO 3 белый 2. Сульфиды – с натрия нитропруссидом Na 2 S + Na 2[Fe(CN)5 NO] → Na 4[Fe(CN)5 NOS] фиолетовое окрашивание Количественное определение 2 Na 2 S 2 O 3 + I 2 → Na 2 S 4 O 6 + 2 Na. I 2 S 2 O 32 - - 2ē → S 4 O 62 -; I 2 + 2ē → 2 IИндикатор – крахмал (до синего окрашивания)
Чистота -недопустимые примеси 1. Сульфиты и сульфаты SO 32 - + I 2 + H 2 O → SO 42 - + 2 HI SO 42 - + Ва(NO 3)2 → Ва. SO 4↓ + 2 NO 3 белый 2. Сульфиды – с натрия нитропруссидом Na 2 S + Na 2[Fe(CN)5 NO] → Na 4[Fe(CN)5 NOS] фиолетовое окрашивание Количественное определение 2 Na 2 S 2 O 3 + I 2 → Na 2 S 4 O 6 + 2 Na. I 2 S 2 O 32 - - 2ē → S 4 O 62 -; I 2 + 2ē → 2 IИндикатор – крахмал (до синего окрашивания)
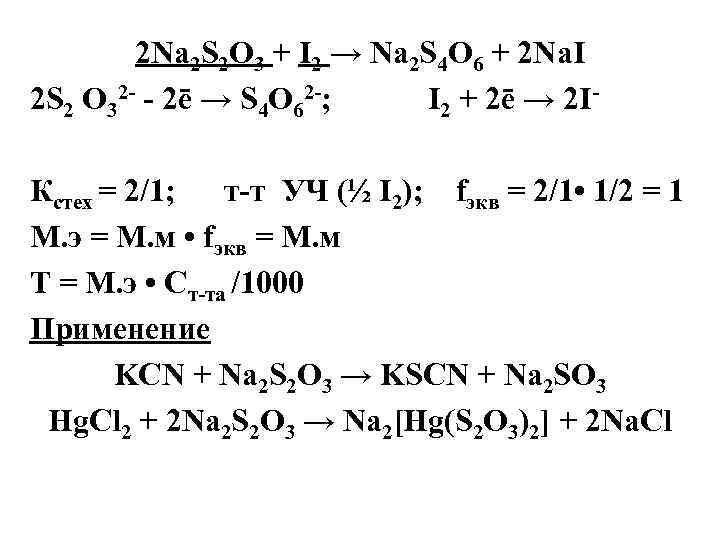 2 Na 2 S 2 O 3 + I 2 → Na 2 S 4 O 6 + 2 Na. I 2 S 2 O 32 - - 2ē → S 4 O 62 -; I 2 + 2ē → 2 I- Кстех = 2/1; т-т УЧ (½ I 2); fэкв = 2/1 • 1/2 = 1 М. э = М. м • fэкв = М. м Т = М. э • Ст-та /1000 Применение KCN + Na 2 S 2 O 3 → KSCN + Na 2 SO 3 Hg. Cl 2 + 2 Na 2 S 2 O 3 → Na 2[Hg(S 2 O 3)2] + 2 Na. Cl
2 Na 2 S 2 O 3 + I 2 → Na 2 S 4 O 6 + 2 Na. I 2 S 2 O 32 - - 2ē → S 4 O 62 -; I 2 + 2ē → 2 I- Кстех = 2/1; т-т УЧ (½ I 2); fэкв = 2/1 • 1/2 = 1 М. э = М. м • fэкв = М. м Т = М. э • Ст-та /1000 Применение KCN + Na 2 S 2 O 3 → KSCN + Na 2 SO 3 Hg. Cl 2 + 2 Na 2 S 2 O 3 → Na 2[Hg(S 2 O 3)2] + 2 Na. Cl


