Lecture 1-2 Первый закон.ppt
- Количество слайдов: 86
 ЛОМОНОСОВ МИХАИЛ ВАСИЛЬЕВИЧ 1711 - 1765 Термин «Физическая химия» принадлежит М. В. Ломоносову, который в 1752 г. впервые читал студентам Петербургского университета «Курс истинной физической химии»
ЛОМОНОСОВ МИХАИЛ ВАСИЛЬЕВИЧ 1711 - 1765 Термин «Физическая химия» принадлежит М. В. Ломоносову, который в 1752 г. впервые читал студентам Петербургского университета «Курс истинной физической химии»
 БЕКЕТОВ НИКОЛАЙ НИКОЛАЕВИЧ 1827 - 1911 Следующий курс физической химии читал Н. Н. Бекетов в Харьковском университете в 1865 году 2
БЕКЕТОВ НИКОЛАЙ НИКОЛАЕВИЧ 1827 - 1911 Следующий курс физической химии читал Н. Н. Бекетов в Харьковском университете в 1865 году 2
 3
3
 ФИЗИЧЕСКАЯ ХИМИЯ - ФИЗИЧЕСКАЯ ХИМИЯ наука об общих законах физики и химии Исследует химические явления с помощью теоретических и экспериментальных методов химии и физики 4
ФИЗИЧЕСКАЯ ХИМИЯ - ФИЗИЧЕСКАЯ ХИМИЯ наука об общих законах физики и химии Исследует химические явления с помощью теоретических и экспериментальных методов химии и физики 4
 РАЗДЕЛЫ ФИЗИЧЕСКОЙ ХИМИИ • ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА • ХИМИЧЕСКОЕ РАВНОВЕСИЕ • ФАЗОВЫЕ РАВНОВЕСИЯ • РАСТВОРЫ ЭЛЕКТРОЛИТОВ И НЕЭЛЕКТРОЛИТОВ • ЭЛЕКТРОХИМИЯ РАСТВОРОВ • БУФЕРНЫЕ РАСТВОРЫ • ЭЛЕКТРОДВИЖУЩИЕ СИЛЫ И ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ • ХИМИЧЕСКАЯ КИНЕТИКА И КАТАЛИЗ 5
РАЗДЕЛЫ ФИЗИЧЕСКОЙ ХИМИИ • ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА • ХИМИЧЕСКОЕ РАВНОВЕСИЕ • ФАЗОВЫЕ РАВНОВЕСИЯ • РАСТВОРЫ ЭЛЕКТРОЛИТОВ И НЕЭЛЕКТРОЛИТОВ • ЭЛЕКТРОХИМИЯ РАСТВОРОВ • БУФЕРНЫЕ РАСТВОРЫ • ЭЛЕКТРОДВИЖУЩИЕ СИЛЫ И ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ • ХИМИЧЕСКАЯ КИНЕТИКА И КАТАЛИЗ 5
 Термодинамика – это раздел физической химии об использовании и превращениях энергии 6
Термодинамика – это раздел физической химии об использовании и превращениях энергии 6
 Эйнштейн А. (1879 -1955) «Классическая термодинамика – это термодинамика единственная общая физическая теория. И я убежден, что в рамках применения своих основных положений она никогда не будет опровергнута…» (1949)
Эйнштейн А. (1879 -1955) «Классическая термодинамика – это термодинамика единственная общая физическая теория. И я убежден, что в рамках применения своих основных положений она никогда не будет опровергнута…» (1949)
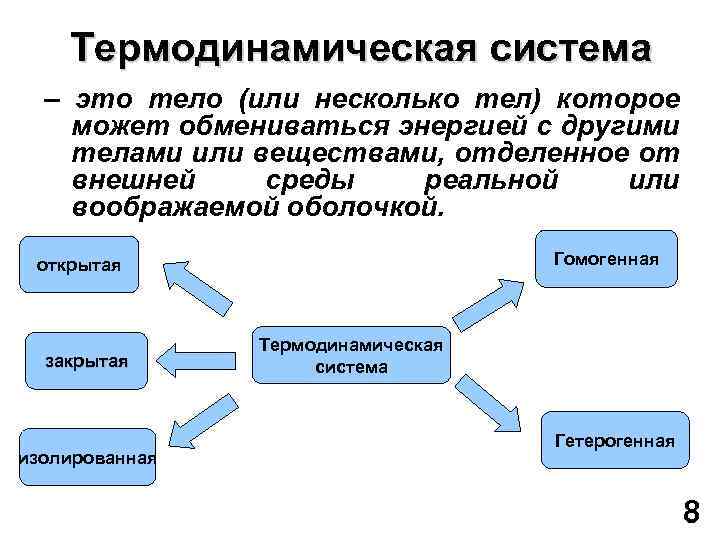 Термодинамическая система – это тело (или несколько тел) которое может обмениваться энергией с другими телами или веществами, отделенное от внешней среды реальной или воображаемой оболочкой. Гомогенная открытая закрытая изолированная Термодинамическая система Гетерогенная 8
Термодинамическая система – это тело (или несколько тел) которое может обмениваться энергией с другими телами или веществами, отделенное от внешней среды реальной или воображаемой оболочкой. Гомогенная открытая закрытая изолированная Термодинамическая система Гетерогенная 8
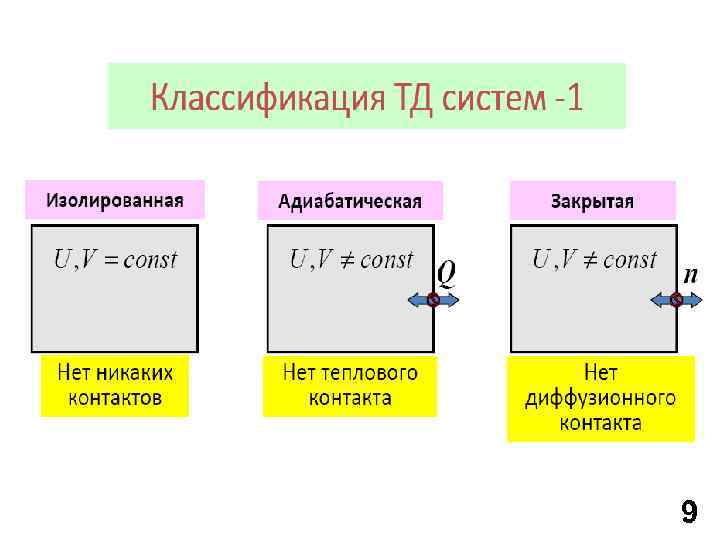 9
9
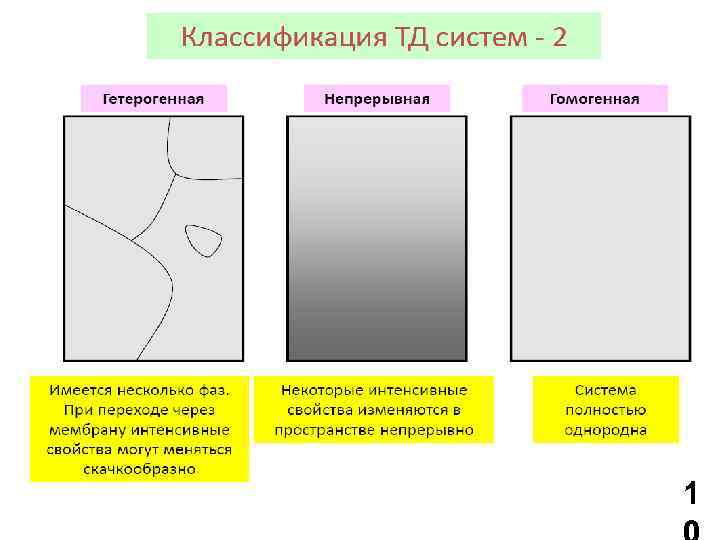 1
1
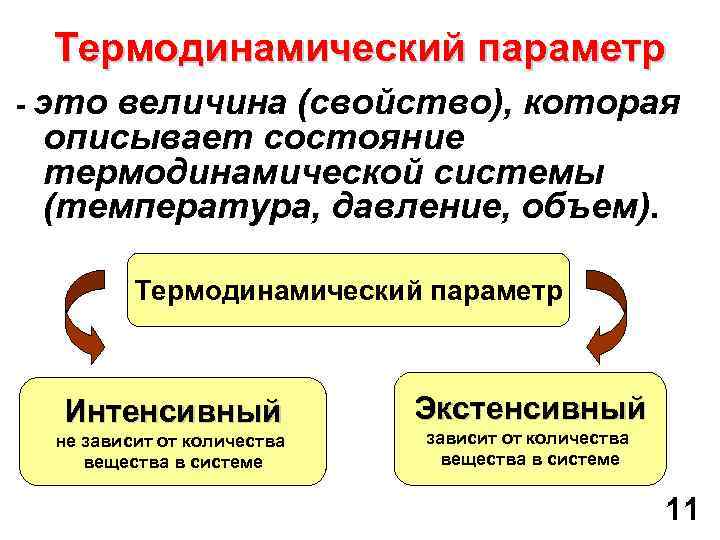 Термодинамический параметр - это величина (свойство), которая описывает состояние термодинамической системы (температура, давление, объем). Термодинамический параметр Интенсивный не зависит от количества вещества в системе Экстенсивный зависит от количества вещества в системе 11
Термодинамический параметр - это величина (свойство), которая описывает состояние термодинамической системы (температура, давление, объем). Термодинамический параметр Интенсивный не зависит от количества вещества в системе Экстенсивный зависит от количества вещества в системе 11
 12
12
 13
13
 14
14
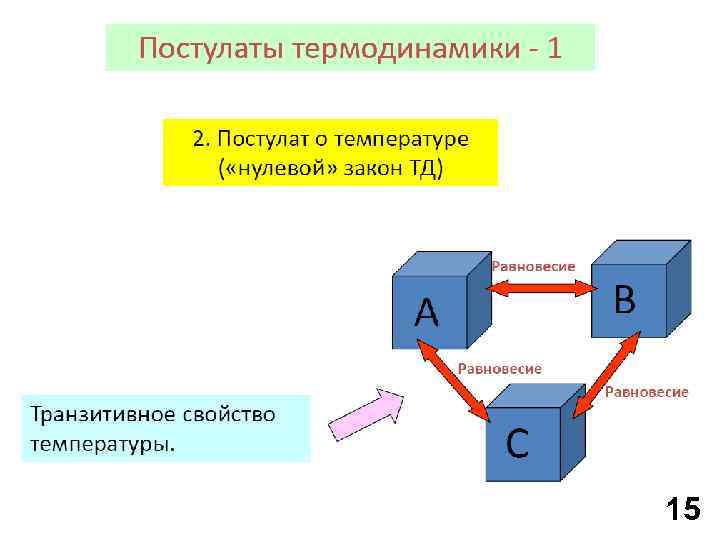 15
15
 16
16
 ТЕРМОДИНАМИЧЕСКИЙ ПРОЦЕСС – это изменение состояния термодинамической системы, которое сопровождается изменением хотя бы одного из параметров. 17
ТЕРМОДИНАМИЧЕСКИЙ ПРОЦЕСС – это изменение состояния термодинамической системы, которое сопровождается изменением хотя бы одного из параметров. 17
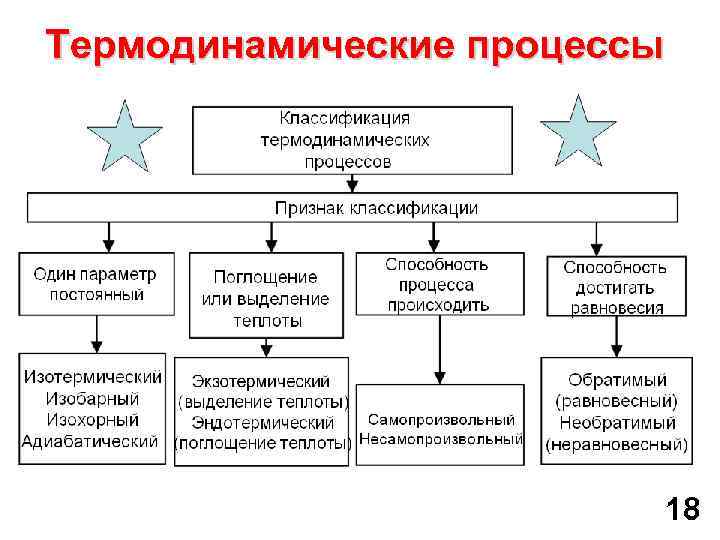 Термодинамические процессы 18
Термодинамические процессы 18
 19
19
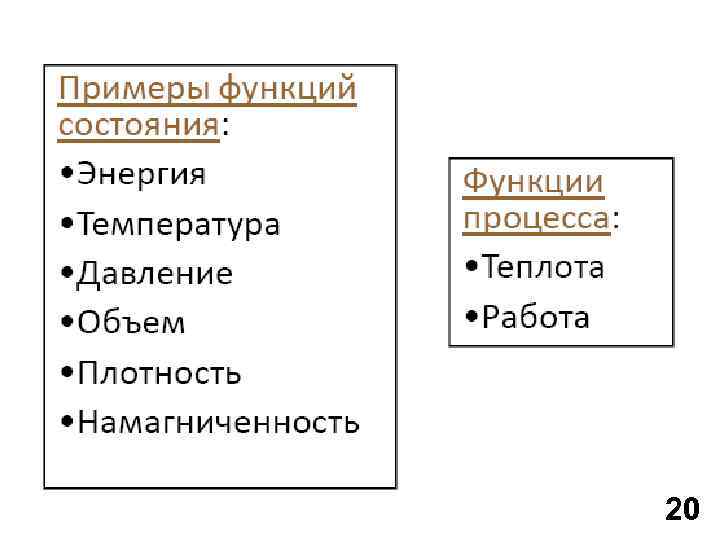 20
20
 Закон Менделеева-Клапейрона • p. V = const × n. T • p. V = n. RT • R – газовая постоянная 21
Закон Менделеева-Клапейрона • p. V = const × n. T • p. V = n. RT • R – газовая постоянная 21
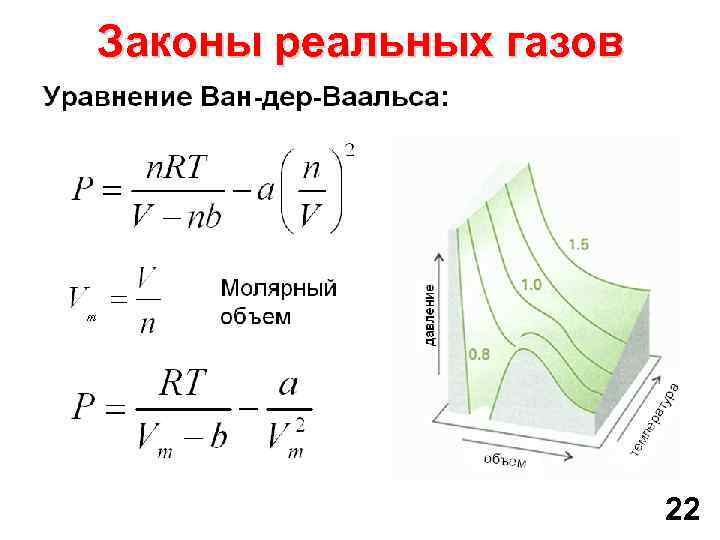 Законы реальных газов 22
Законы реальных газов 22
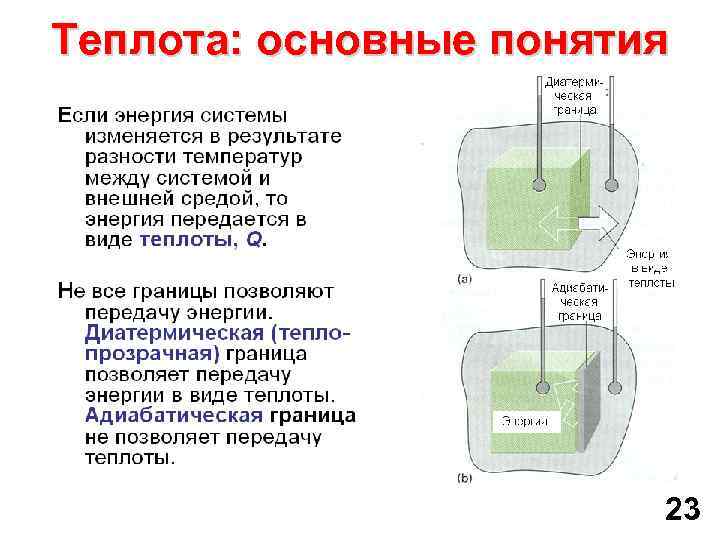 Теплота: основные понятия 23
Теплота: основные понятия 23
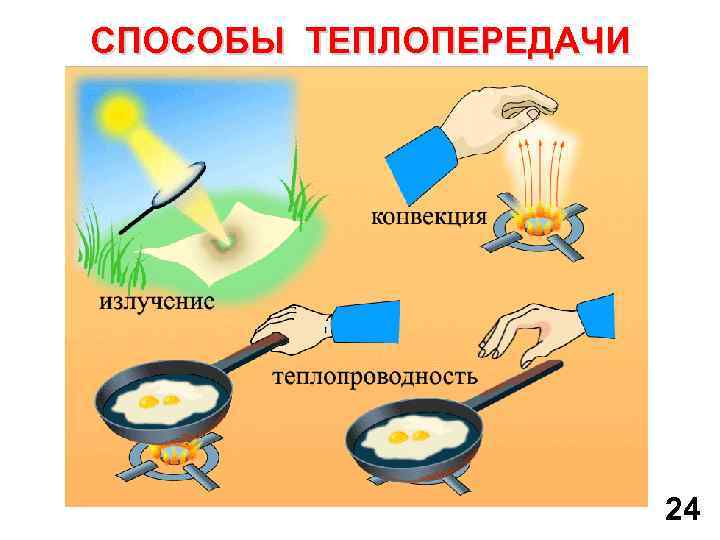 СПОСОБЫ ТЕПЛОПЕРЕДАЧИ 24
СПОСОБЫ ТЕПЛОПЕРЕДАЧИ 24
 СУБЪЕКТИВНОСТЬ ВОСПРИЯТИЯ ТЕПЛА И ХОЛОДА 25
СУБЪЕКТИВНОСТЬ ВОСПРИЯТИЯ ТЕПЛА И ХОЛОДА 25
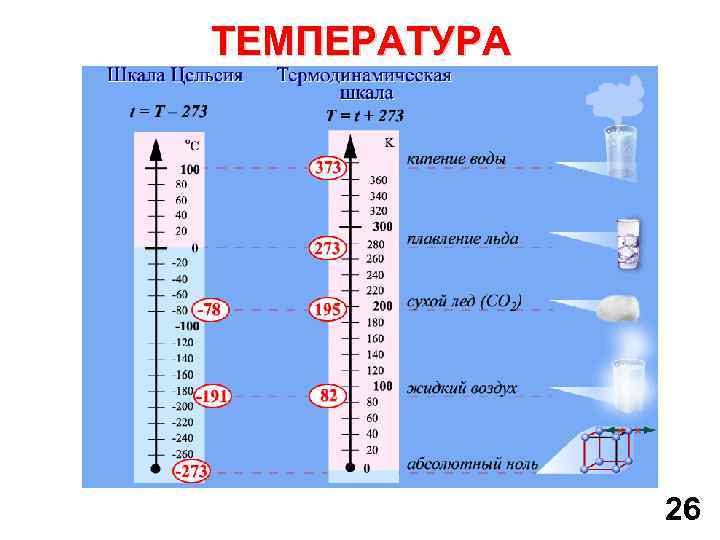 ТЕМПЕРАТУРА 26
ТЕМПЕРАТУРА 26
 Работа: основные понятия 27
Работа: основные понятия 27
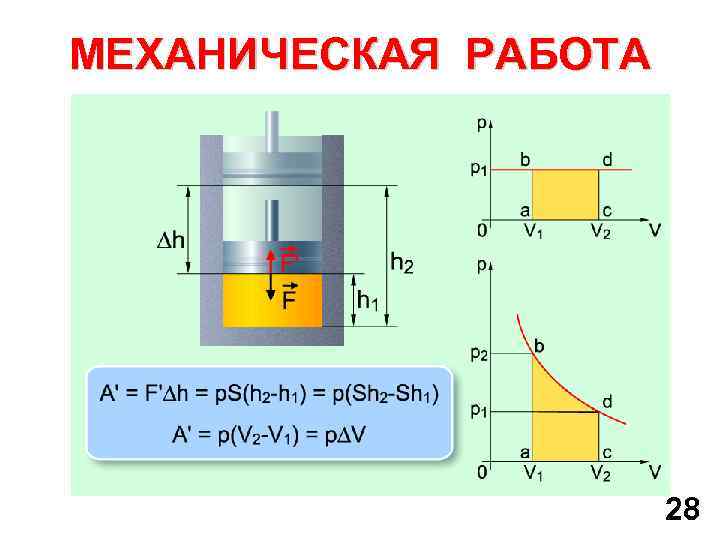 МЕХАНИЧЕСКАЯ РАБОТА 28
МЕХАНИЧЕСКАЯ РАБОТА 28
 В чем разница между работой и теплотой? Обоснование на молекулярном уровне Теплота это передача энергии Теплота вследствие хаотичного (беспорядочного) движения молекул (теплового движения) Работа это передача энергии Работа вследствие организованного (упорядоченного ) движения молекул 29
В чем разница между работой и теплотой? Обоснование на молекулярном уровне Теплота это передача энергии Теплота вследствие хаотичного (беспорядочного) движения молекул (теплового движения) Работа это передача энергии Работа вследствие организованного (упорядоченного ) движения молекул 29
 Внутренняя энергия: основные понятия 1 Общая энергия системы называется ее внутренней энергией. Внутренняя энергия системы - это сумма общей кинетической и потенциальной энергий молекул, составляющих систему. 30
Внутренняя энергия: основные понятия 1 Общая энергия системы называется ее внутренней энергией. Внутренняя энергия системы - это сумма общей кинетической и потенциальной энергий молекул, составляющих систему. 30
 Внутренняя энергия: основные понятия 2 ΔU - изменение внутренней энергии. Если система переходит из начального состояния (U 1) в конечное состояние (U 2): ΔU = U 2 – U 1 31
Внутренняя энергия: основные понятия 2 ΔU - изменение внутренней энергии. Если система переходит из начального состояния (U 1) в конечное состояние (U 2): ΔU = U 2 – U 1 31
 Внутренняя энергия: основные понятия 3 Внутренняя энергия является функцией состояния (переменной состояния). Изменение термодинамических параметров приводит к изменению внутренней энергии. В термодинамике энергия процесса считается положительной, если внутренняя энергия системы увеличивается в ходе процесса. 32
Внутренняя энергия: основные понятия 3 Внутренняя энергия является функцией состояния (переменной состояния). Изменение термодинамических параметров приводит к изменению внутренней энергии. В термодинамике энергия процесса считается положительной, если внутренняя энергия системы увеличивается в ходе процесса. 32
 Внутренняя энергия: основные понятия 4 • Переменная (функция) состояния – величина, которая зависит только от свойств системы в начальном и конечном состоянии и не зависит от пути процесса. 33
Внутренняя энергия: основные понятия 4 • Переменная (функция) состояния – величина, которая зависит только от свойств системы в начальном и конечном состоянии и не зависит от пути процесса. 33
 Закон сохранения энергии Энергия не возникает и не исчезает, а только переходит из одной формы в другую. В любой изолированной системе запас энергии остается постоянным. Разные формы энергии переходят друг в друга в строго эквивалентных количествах. 34
Закон сохранения энергии Энергия не возникает и не исчезает, а только переходит из одной формы в другую. В любой изолированной системе запас энергии остается постоянным. Разные формы энергии переходят друг в друга в строго эквивалентных количествах. 34
 ПEРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Энергия изолированной адиабатической системы постоянна. В неизолированной системе энергия может изменяться за счет: а) совершения работы над окружающей средой; б) теплообмена с окружающей средой. 35
ПEРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Энергия изолированной адиабатической системы постоянна. В неизолированной системе энергия может изменяться за счет: а) совершения работы над окружающей средой; б) теплообмена с окружающей средой. 35
 36
36
 37
37
 38
38
 ПEРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ • механическая работа: А = -pdv; • A - полезная работа: электрическая А´ = dq, химическая А´ = dn, поверхностная А´ = d 39
ПEРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ • механическая работа: А = -pdv; • A - полезная работа: электрическая А´ = dq, химическая А´ = dn, поверхностная А´ = d 39
 40
40
 41
41
 ЭНТАЛЬПИЯ • QP = U + p V = (U + p. V) = H • Только в двух случаях – при изобарном и изохорном процессах, теплота приобретает свойства функции состояния QP = H, QV = U • В общем случае для любого процесса H = U + (p. V) = U + p V + V p 42
ЭНТАЛЬПИЯ • QP = U + p V = (U + p. V) = H • Только в двух случаях – при изобарном и изохорном процессах, теплота приобретает свойства функции состояния QP = H, QV = U • В общем случае для любого процесса H = U + (p. V) = U + p V + V p 42
 Энтальпия: основные понятия δQР = d. U + Pd. V δQР = d(U + PV) Теплота, которая выделяется при постоянном давлении равна изменению энтальпии, H. 43
Энтальпия: основные понятия δQР = d. U + Pd. V δQР = d(U + PV) Теплота, которая выделяется при постоянном давлении равна изменению энтальпии, H. 43
 Энтальпия идеального газа PV = Δn. RT H = U + PV = U + Δn. RT Δn – изменение моль молекул газа в реакции. 2 H 2(г) + O 2(г) = 2 H 2 O(ж) Δn = -3 моль ΔH – ΔU = Δn. RT = -3 8. 31 298 = -7. 5 k. Дж 44
Энтальпия идеального газа PV = Δn. RT H = U + PV = U + Δn. RT Δn – изменение моль молекул газа в реакции. 2 H 2(г) + O 2(г) = 2 H 2 O(ж) Δn = -3 моль ΔH – ΔU = Δn. RT = -3 8. 31 298 = -7. 5 k. Дж 44
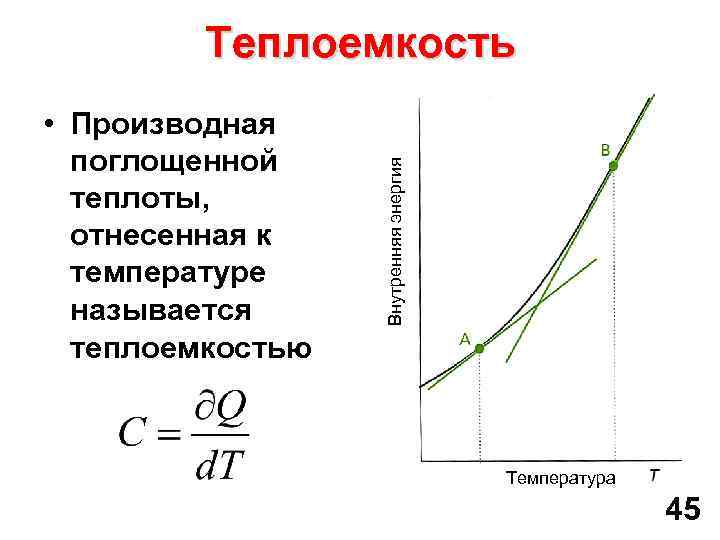 • Производная поглощенной теплоты, отнесенная к температуре называется теплоемкостью Внутренняя энергия Теплоемкость Температура 45
• Производная поглощенной теплоты, отнесенная к температуре называется теплоемкостью Внутренняя энергия Теплоемкость Температура 45
 Теплоемкость при постоянном объеме Внутренняя энергия системы и объем изменяются при изменении температуры. Теплоемкость при постоянном объеме обозначается CV и определяется как: 46
Теплоемкость при постоянном объеме Внутренняя энергия системы и объем изменяются при изменении температуры. Теплоемкость при постоянном объеме обозначается CV и определяется как: 46
 Расчет CV Для идеального одноатомного газа: Для идеального двухатомного газа: 47
Расчет CV Для идеального одноатомного газа: Для идеального двухатомного газа: 47
 • Теплоемкость при постоянном Теплоемкость объеме может быть использована, чтобы найти изменение внутренней энергии при изменении температуры (при V = const): 48
• Теплоемкость при постоянном Теплоемкость объеме может быть использована, чтобы найти изменение внутренней энергии при изменении температуры (при V = const): 48
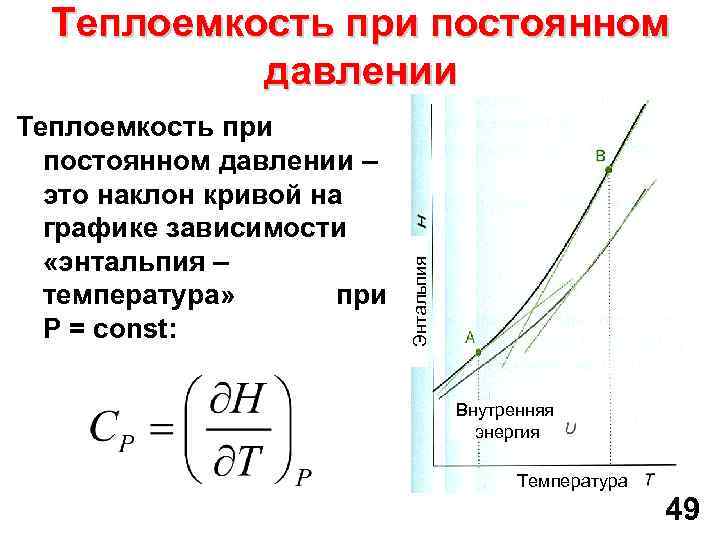 Теплоемкость при постоянном давлении – это наклон кривой на графике зависимости «энтальпия – температура» при P = const: Энтальпия Теплоемкость при постоянном давлении Внутренняя энергия Температура 49
Теплоемкость при постоянном давлении – это наклон кривой на графике зависимости «энтальпия – температура» при P = const: Энтальпия Теплоемкость при постоянном давлении Внутренняя энергия Температура 49
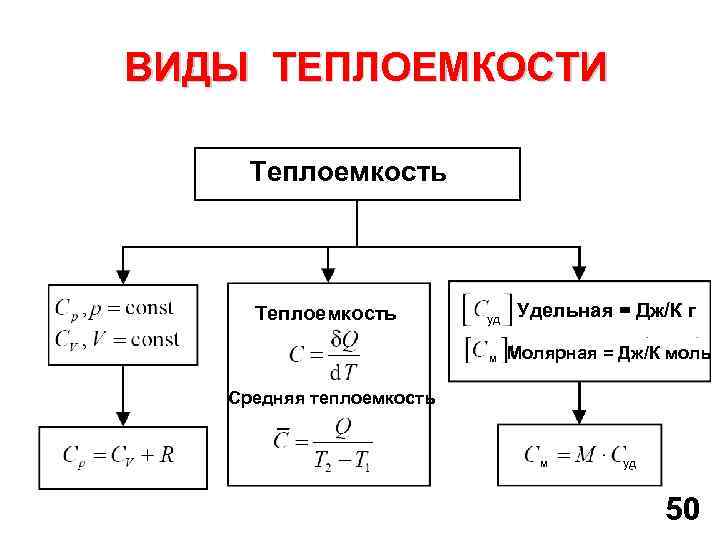 ВИДЫ ТЕПЛОЕМКОСТИ Теплоемкость уд Удельная = Дж/К г м Теплоемкость Молярная = Дж/К моль Средняя теплоемкость м уд 50
ВИДЫ ТЕПЛОЕМКОСТИ Теплоемкость уд Удельная = Дж/К г м Теплоемкость Молярная = Дж/К моль Средняя теплоемкость м уд 50
 Связь между средней и истинной теплоемкостями 51
Связь между средней и истинной теплоемкостями 51
 Связь между Сp и СV для идеальных газов 52
Связь между Сp и СV для идеальных газов 52
 Зависимость теплоемкости от температуры В общем случае эмпирическая зависимость теплоемкости от температуры выражается полиномом: 53
Зависимость теплоемкости от температуры В общем случае эмпирическая зависимость теплоемкости от температуры выражается полиномом: 53
 Определение d. U Теплоемкость при постоянном объеме используется для расчета изменения внутренней энергии при изменении температуры при постоянном объеме: d. U = CV d. T 54
Определение d. U Теплоемкость при постоянном объеме используется для расчета изменения внутренней энергии при изменении температуры при постоянном объеме: d. U = CV d. T 54
 Определение d. H Теплоемкость при постоянном давлении используется для расчета изменения энтальпии при изменении температуры при постоянном давлении: d. H = Cp d. T 55
Определение d. H Теплоемкость при постоянном давлении используется для расчета изменения энтальпии при изменении температуры при постоянном давлении: d. H = Cp d. T 55
 Термохимия 1 Типы энтальпии Теплоемкость Закон Кирхгофа Закон Гесса 56
Термохимия 1 Типы энтальпии Теплоемкость Закон Кирхгофа Закон Гесса 56
 Термохимия 2 57
Термохимия 2 57
 ТИПЫ ПРОЦЕССОВ 58
ТИПЫ ПРОЦЕССОВ 58
 Изменение энтальпии в экзотермических и эндотермических процессах Выделение теплоты приводит к уменьшению энтальпии системы (при Р = const). Поэтому для экзотермического процесса: ΔH < 0 Поглощение теплоты приводит к увеличению энтальпии системы (при Р = const). Поэтому для эндотермического процесса: ΔH > 0 59
Изменение энтальпии в экзотермических и эндотермических процессах Выделение теплоты приводит к уменьшению энтальпии системы (при Р = const). Поэтому для экзотермического процесса: ΔH < 0 Поглощение теплоты приводит к увеличению энтальпии системы (при Р = const). Поэтому для эндотермического процесса: ΔH > 0 59
 Измерение теплоты химической реакции Калориметрия - это метод, который используется для измерения теплоты, которая поглощается или выделяется в ходе химической реакции. 60
Измерение теплоты химической реакции Калориметрия - это метод, который используется для измерения теплоты, которая поглощается или выделяется в ходе химической реакции. 60
 Измерение теплоты химической реакции При постоянном объеме количество теплоты будет равно изменению внутренней энергии. ΔU = Qv (V=const) При постоянном давлении количество теплоты будет равно изменению энтальпии ΔH = QP (P=const) 61
Измерение теплоты химической реакции При постоянном объеме количество теплоты будет равно изменению внутренней энергии. ΔU = Qv (V=const) При постоянном давлении количество теплоты будет равно изменению энтальпии ΔH = QP (P=const) 61
 Стандартная энтальпия и стандартное состояние Стандартное изменение энтальпии ΔH° - это изменение энтальпии для процесса, в котором исходные вещества и продукты находятся в стандартном состоянии. Стандартное состояние вещества при определенной температуре - это его состояние при стандартном давлении. (1 aтм, или 1. 01325 × 105 Пa). 62
Стандартная энтальпия и стандартное состояние Стандартное изменение энтальпии ΔH° - это изменение энтальпии для процесса, в котором исходные вещества и продукты находятся в стандартном состоянии. Стандартное состояние вещества при определенной температуре - это его состояние при стандартном давлении. (1 aтм, или 1. 01325 × 105 Пa). 62
 Стандартная энтальпия и стандартное состояние Примеры: стандартное состояние жидкого этанола - это жидкий этанол при 298 K и 1 aтм; стандартное состояние твердого железа – это железо при 500 K и 1 aтм. 63
Стандартная энтальпия и стандартное состояние Примеры: стандартное состояние жидкого этанола - это жидкий этанол при 298 K и 1 aтм; стандартное состояние твердого железа – это железо при 500 K и 1 aтм. 63
 Энтальпия физических превращений 1 Стандартная энтальпия образования вещества Δf. H° - это стандартная энтальпия химической реакции образования вещества из простых веществ. Стандартная энтальпия сгорания вещества Δc. H° - это стандартная энтальпия полного окисления органического вещества до CO 2 и H 2 O. 64
Энтальпия физических превращений 1 Стандартная энтальпия образования вещества Δf. H° - это стандартная энтальпия химической реакции образования вещества из простых веществ. Стандартная энтальпия сгорания вещества Δc. H° - это стандартная энтальпия полного окисления органического вещества до CO 2 и H 2 O. 64
 Энтальпия физических превращений 2 Стандартная энтальпия перехода Δtrs. H° – это фазового изменение стандартной энтальпии при изменении физического состояния вещества. Примеры изменения физического состояния вещества: испарение; конденсация; плавление кристаллизация; сублимация 65
Энтальпия физических превращений 2 Стандартная энтальпия перехода Δtrs. H° – это фазового изменение стандартной энтальпии при изменении физического состояния вещества. Примеры изменения физического состояния вещества: испарение; конденсация; плавление кристаллизация; сублимация 65
 Энтальпия физических превращений 3 Стандартная энтальпия испарения, Δvap. H°, это изменение энтальпии при испарении 1 моль чистой жидкости при 1 атм Пример : H 2 O(ж) → H 2 O(г) + Δvap. H°(373 K) = +40. 66 k. Дж/моль 66
Энтальпия физических превращений 3 Стандартная энтальпия испарения, Δvap. H°, это изменение энтальпии при испарении 1 моль чистой жидкости при 1 атм Пример : H 2 O(ж) → H 2 O(г) + Δvap. H°(373 K) = +40. 66 k. Дж/моль 66
 Энтальпия физических превращений 4 Стандартная энтальпия плавления Δfus. H°, это изменение энтальпии при переходе 1 моль твердого вещества в жидкость. Пример: H 2 O(тв) → H 2 O(ж) + Δfus. H°(273 K) = +6. 01 k. Дж/моль 67
Энтальпия физических превращений 4 Стандартная энтальпия плавления Δfus. H°, это изменение энтальпии при переходе 1 моль твердого вещества в жидкость. Пример: H 2 O(тв) → H 2 O(ж) + Δfus. H°(273 K) = +6. 01 k. Дж/моль 67
 Стандартная энтальпия возгонки H 2 O(тв) → H 2 O(г) + Δsub. H° Два этапа: H 2 O(тв) → H 2 O(ж) + Δfus. H° H 2 O(ж) → H 2 O(г) + Δvap. H° Δsub. H° = Δfus. H° + Δvap. H° 68
Стандартная энтальпия возгонки H 2 O(тв) → H 2 O(г) + Δsub. H° Два этапа: H 2 O(тв) → H 2 O(ж) + Δfus. H° H 2 O(ж) → H 2 O(г) + Δvap. H° Δsub. H° = Δfus. H° + Δvap. H° 68
 Энтальпия прямого и обратного процесса Энтальпия – это функция состояния ΔH° (A B) = -ΔH° (A B) Пример: Энтальпия испарения воды равна + 44 k. Дж/моль. Энтальпия конденсации воды равна - 44 k. Дж/моль. 69
Энтальпия прямого и обратного процесса Энтальпия – это функция состояния ΔH° (A B) = -ΔH° (A B) Пример: Энтальпия испарения воды равна + 44 k. Дж/моль. Энтальпия конденсации воды равна - 44 k. Дж/моль. 69
 Энтальпия химической реакции Стандартная энтальпия химической реакции, Δr. H° - это изменение энтальпии когда реагенты в стандартном состоянии переходят в продукты реакции в стандартном состоянии. 70
Энтальпия химической реакции Стандартная энтальпия химической реакции, Δr. H° - это изменение энтальпии когда реагенты в стандартном состоянии переходят в продукты реакции в стандартном состоянии. 70
 Энтальпия химической реакции 71
Энтальпия химической реакции 71
 Энтальпия химической реакции Расчет энтальпии химической реакции с использованием стандартных энтальпий сгорания веществ: Пример : C 6 H 12 O 6(тв) + 6 O 2(г) = 6 CO 2(г)+ 6 H 2 O(ж) реагенты продукты Δr. Hо = -2808 k. Дж/моль 72
Энтальпия химической реакции Расчет энтальпии химической реакции с использованием стандартных энтальпий сгорания веществ: Пример : C 6 H 12 O 6(тв) + 6 O 2(г) = 6 CO 2(г)+ 6 H 2 O(ж) реагенты продукты Δr. Hо = -2808 k. Дж/моль 72
 Закон Гесса Стандартная энтальпия реакции может быть определена как сумма стандартных энтальпий реакций, из которых можно получить данную реакцию Термодинамическая основа закона Гесса – это независимость энтальпии реакции от пути получения продукта из реагентов. 73
Закон Гесса Стандартная энтальпия реакции может быть определена как сумма стандартных энтальпий реакций, из которых можно получить данную реакцию Термодинамическая основа закона Гесса – это независимость энтальпии реакции от пути получения продукта из реагентов. 73
 Применение закона Гесса Метод Пример Метод термохимических схем Метод термохимических уравнений 74
Применение закона Гесса Метод Пример Метод термохимических схем Метод термохимических уравнений 74
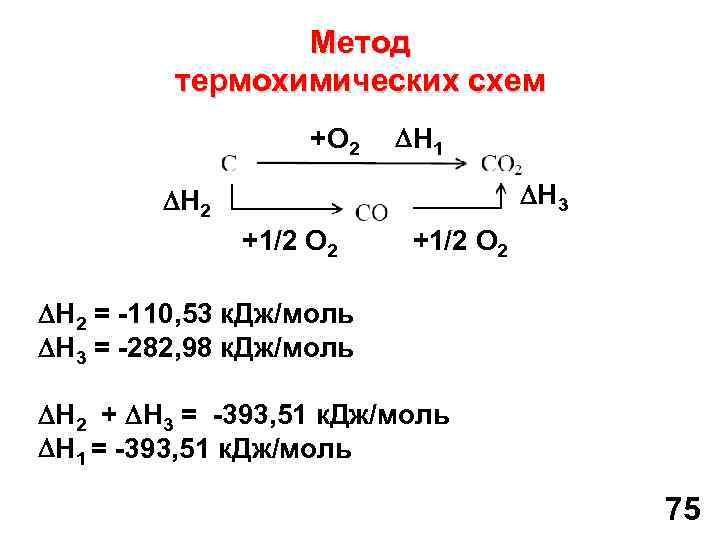 Метод термохимических схем +О 2 Н 1 Н 3 Н 2 +1/2 О 2 Н 2 = -110, 53 к. Дж/моль Н 3 = -282, 98 к. Дж/моль Н 2 + Н 3 = -393, 51 к. Дж/моль Н 1 = -393, 51 к. Дж/моль 75
Метод термохимических схем +О 2 Н 1 Н 3 Н 2 +1/2 О 2 Н 2 = -110, 53 к. Дж/моль Н 3 = -282, 98 к. Дж/моль Н 2 + Н 3 = -393, 51 к. Дж/моль Н 1 = -393, 51 к. Дж/моль 75
 Метод термохимических уравнений (1) (2) (3) Сложение уравнений (2) и (3) дает уравнение (1). Поэтому: Н 1= Н 2 + Н 3 76
Метод термохимических уравнений (1) (2) (3) Сложение уравнений (2) и (3) дает уравнение (1). Поэтому: Н 1= Н 2 + Н 3 76
 Зависимость энтальпии от температуры (1) 77
Зависимость энтальпии от температуры (1) 77
 Зависимость энтальпии от температуры (2) 78
Зависимость энтальпии от температуры (2) 78
 Закон Кирхгофа для химической реакции (1) Для химической реакции: 79
Закон Кирхгофа для химической реакции (1) Для химической реакции: 79
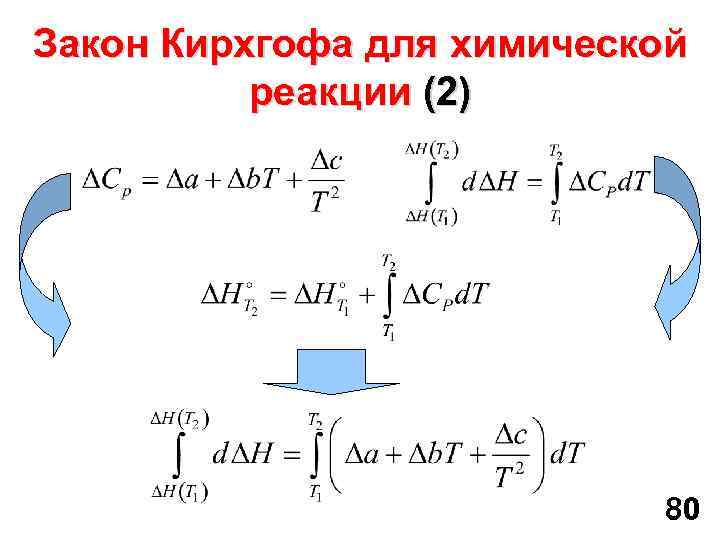 Закон Кирхгофа для химической реакции (2) 80
Закон Кирхгофа для химической реакции (2) 80
 Энтальпия образования ионов в растворе Тепловой эффект образования химического соединения в растворе, диссоциирующего на ионы, определяется по энтальпиям образования ионов в растворе. Пример: Теплота образования иона SO 42 - равна энтальпии реакции: S(тв) + 2 O 2(г) + H 2 O(ж) + 2 e = SO 42 -(aq) 81
Энтальпия образования ионов в растворе Тепловой эффект образования химического соединения в растворе, диссоциирующего на ионы, определяется по энтальпиям образования ионов в растворе. Пример: Теплота образования иона SO 42 - равна энтальпии реакции: S(тв) + 2 O 2(г) + H 2 O(ж) + 2 e = SO 42 -(aq) 81
 Теплота растворения Теплота, которая поглощается или выделяется при образовании раствора определенной концентрации (моляльности) – интегральная теплота растворения. Теплота растворения зависит от: – теплоты разрушения кристаллической решетки – теплоты сольватации (гидратации) 82
Теплота растворения Теплота, которая поглощается или выделяется при образовании раствора определенной концентрации (моляльности) – интегральная теплота растворения. Теплота растворения зависит от: – теплоты разрушения кристаллической решетки – теплоты сольватации (гидратации) 82
 Моляльность – способ выражения состава раствора. Моляльность показывает количество молей растворенного вещества в 1000 г растворителя. 83
Моляльность – способ выражения состава раствора. Моляльность показывает количество молей растворенного вещества в 1000 г растворителя. 83
 Интегральная теплота растворения ∆Н 0 – первая интегральная теплота растворения. Это тепловой эффект при растворении 1 моль вещества в бесконечно большом объеме растворителя. ∆Нs – полная интегральная теплота растворения. Это теплота растворения 1 моль вещества в таком объеме растворителя, чтобы образовался насыщенный раствор. 84
Интегральная теплота растворения ∆Н 0 – первая интегральная теплота растворения. Это тепловой эффект при растворении 1 моль вещества в бесконечно большом объеме растворителя. ∆Нs – полная интегральная теплота растворения. Это теплота растворения 1 моль вещества в таком объеме растворителя, чтобы образовался насыщенный раствор. 84
 Промежуточная теплота разведения – это тепловой эффект разбавления раствора, содержащего 1 моль вещества от концентрации m 2 до меньшей концентрации m 1. 85
Промежуточная теплота разведения – это тепловой эффект разбавления раствора, содержащего 1 моль вещества от концентрации m 2 до меньшей концентрации m 1. 85
 Промежуточная теплота раcтворения – это тепловой эффект, который сопровождает концентрирование раствора от концентрации m 1 до большей концентрации m 2. 86
Промежуточная теплота раcтворения – это тепловой эффект, который сопровождает концентрирование раствора от концентрации m 1 до большей концентрации m 2. 86


