Лекция 2 Поверхносное натяжение.ppt
- Количество слайдов: 33
 Литература Основная 1. И. П. Суздалев. Физикохимия нанокластеров, наноструктур и наноматериалов. –М. : Комкнига. , 2005. - 589 с. 2. Пул, Оуэнс. Нанотехнологии. 3. Р. А. Андриевский, А. В. Рагуля. Наноструктурные материалы. М. : Изд. центр «Академия» . -2005. -192 с. Дополнительная литература 1. Сергеев Г. Б. Нанохимия. - М. : К. д. » Университет» . - 2007. -335 с. 2. Старостин 3. Помогайло 1
Литература Основная 1. И. П. Суздалев. Физикохимия нанокластеров, наноструктур и наноматериалов. –М. : Комкнига. , 2005. - 589 с. 2. Пул, Оуэнс. Нанотехнологии. 3. Р. А. Андриевский, А. В. Рагуля. Наноструктурные материалы. М. : Изд. центр «Академия» . -2005. -192 с. Дополнительная литература 1. Сергеев Г. Б. Нанохимия. - М. : К. д. » Университет» . - 2007. -335 с. 2. Старостин 3. Помогайло 1
 Основные понятия и определения Продолжение лек 1 Фаза Структура Агрегатное состояние относятся к макроскопическим, бесконечно протяженным) телам С уменьшением размера тела становятся менее определенными (а фазовый переход более размытым) Изолированная частица (1 нм) обладающая четко выраженной структурой нельзя сказать, в каком агрегатном состоянии она находится, хотя и можно говорить (по данным, например, спектроскопии) о ее жидкоподобном или твердоподобном поведении 2
Основные понятия и определения Продолжение лек 1 Фаза Структура Агрегатное состояние относятся к макроскопическим, бесконечно протяженным) телам С уменьшением размера тела становятся менее определенными (а фазовый переход более размытым) Изолированная частица (1 нм) обладающая четко выраженной структурой нельзя сказать, в каком агрегатном состоянии она находится, хотя и можно говорить (по данным, например, спектроскопии) о ее жидкоподобном или твердоподобном поведении 2
 Структура Фаза Агрегатное состояние относятся к макроскопическим, бесконечно протяженным) телам Изолированная частица (1 нм) В каком состоянии она находится ? 3
Структура Фаза Агрегатное состояние относятся к макроскопическим, бесконечно протяженным) телам Изолированная частица (1 нм) В каком состоянии она находится ? 3
 Для выделения наноразмерных эффектов следует обратиться к специфике малых систем Чем меньше частицы вещества, тем большую роль играют в них поверхностные явления В средней части поверхностного слоя наблюдаются очень большие градиенты свойств, которые различны в соприкасающихся фазах Н 2 О изменение плотности в тысячу раз на границе воды с воздухом осуществляется на расстоянии в 1 нм 4
Для выделения наноразмерных эффектов следует обратиться к специфике малых систем Чем меньше частицы вещества, тем большую роль играют в них поверхностные явления В средней части поверхностного слоя наблюдаются очень большие градиенты свойств, которые различны в соприкасающихся фазах Н 2 О изменение плотности в тысячу раз на границе воды с воздухом осуществляется на расстоянии в 1 нм 4
 Удельная поверхность тела объем дисперсной фазы для систем кубических частиц с размером ребра l и сферических диаметром d имеем: в общем виде где k - коэффициент формы части, D - дисперсность Зависимость удельной поверхности Sуд дисперсных систем от размера частиц а и дисперсности D 5
Удельная поверхность тела объем дисперсной фазы для систем кубических частиц с размером ребра l и сферических диаметром d имеем: в общем виде где k - коэффициент формы части, D - дисперсность Зависимость удельной поверхности Sуд дисперсных систем от размера частиц а и дисперсности D 5
 Изменение удельной поверхности от дисперсности (размера) nдля пленки nдля бруска возрастает коэффициент формы k • для куба кривизна поверхности Н Найдем Н для сферической частицы радиусом r: 6
Изменение удельной поверхности от дисперсности (размера) nдля пленки nдля бруска возрастает коэффициент формы k • для куба кривизна поверхности Н Найдем Н для сферической частицы радиусом r: 6
 специфика малых систем но Для выделения наноразмерных эффектов следует обратиться к специфике малых систем Она состоит в том, что чем меньше частицы вещества, тем большую относительную роль играют в них поверхностные явления на свойства поверхностей существенно влияют Условие существования межфазных поверхностей – наличие в системе жидкой или твердой фазы, определяющих форму и строение поверхностного слоя • большая подвижность молекул жидкости и 7 • практическая неподвижность молекул и атомов твердого тела
специфика малых систем но Для выделения наноразмерных эффектов следует обратиться к специфике малых систем Она состоит в том, что чем меньше частицы вещества, тем большую относительную роль играют в них поверхностные явления на свойства поверхностей существенно влияют Условие существования межфазных поверхностей – наличие в системе жидкой или твердой фазы, определяющих форму и строение поверхностного слоя • большая подвижность молекул жидкости и 7 • практическая неподвижность молекул и атомов твердого тела
 Поверхностный слой жидкости непрерывно обновляется вследствие • подвижности молекул в объеме, а также в результате • постоянно протекающих процессов испарения и конденсации Н 2 О среднее время жизни на поверхности ≈ 10 -7 с Плотность граничного слоя изменяется непрерывно от плотности жидкой воды до плотности ее пара Вследствие подвижности жидкости имеют гладкие и сплошные, или эквипотенциальные, поверхности время жизни атомов на поверхности вольфрама составляет 1032 с с термодинамических позиций все точки поверхности жидкости энергетически эквивалентны 8 Поверхность твердого тела редко бывает эквипотенциальной
Поверхностный слой жидкости непрерывно обновляется вследствие • подвижности молекул в объеме, а также в результате • постоянно протекающих процессов испарения и конденсации Н 2 О среднее время жизни на поверхности ≈ 10 -7 с Плотность граничного слоя изменяется непрерывно от плотности жидкой воды до плотности ее пара Вследствие подвижности жидкости имеют гладкие и сплошные, или эквипотенциальные, поверхности время жизни атомов на поверхности вольфрама составляет 1032 с с термодинамических позиций все точки поверхности жидкости энергетически эквивалентны 8 Поверхность твердого тела редко бывает эквипотенциальной
 Поверхностные (межфазные) явления состоят в том, что на границе между соприкасающимися фазами располагается узкая переходная зона - поверхностный слой, свойства которого отличаются от свойств объемных фаз Эффективная толщина поверхностного слоя приближается к молекулярным размерам В средней части поверхностного слоя наблюдаются очень большие градиенты тех локальных свойств, которые различны в соприкасающихся фазах Например, изменение плотности в тысячу раз на границе конденсированной фазы с воздухом осуществляется на расстоянии в 1 нм Высокая неоднородность поверхностных слоев причина их анизотропии 9
Поверхностные (межфазные) явления состоят в том, что на границе между соприкасающимися фазами располагается узкая переходная зона - поверхностный слой, свойства которого отличаются от свойств объемных фаз Эффективная толщина поверхностного слоя приближается к молекулярным размерам В средней части поверхностного слоя наблюдаются очень большие градиенты тех локальных свойств, которые различны в соприкасающихся фазах Например, изменение плотности в тысячу раз на границе конденсированной фазы с воздухом осуществляется на расстоянии в 1 нм Высокая неоднородность поверхностных слоев причина их анизотропии 9
 термодинамическое состояния вещества в поверхностных слоях - в избыточной поверхностной энергии - в ненасыщенности химических связей и определенных физических сил, характерных для конденсированных фаз Для жидкостей и большинства твердых тел межмолекулярное взаимодействие обусловлено ван-дер-ваальсовыми и водородными связями Разрыв связей Поверхность способная образовывать ван-дер-ваальсовы и водородные связи 10
термодинамическое состояния вещества в поверхностных слоях - в избыточной поверхностной энергии - в ненасыщенности химических связей и определенных физических сил, характерных для конденсированных фаз Для жидкостей и большинства твердых тел межмолекулярное взаимодействие обусловлено ван-дер-ваальсовыми и водородными связями Разрыв связей Поверхность способная образовывать ван-дер-ваальсовы и водородные связи 10
 При разрушении твердых тел с атомной кристаллической решеткой (С, Ge, Si и др. ) разрываются ковалентные связи В условиях вакуума способны образовывать между собой двойные связи на воздухе реагируют с кислородом, образуя на поверхности оксидные пленки У ионных кристаллов распределение электрического заряда на поверхности значительно отличается от его распределения в объеме реакционная способность поверхности повышена относительно ионов противоположного заряда 11
При разрушении твердых тел с атомной кристаллической решеткой (С, Ge, Si и др. ) разрываются ковалентные связи В условиях вакуума способны образовывать между собой двойные связи на воздухе реагируют с кислородом, образуя на поверхности оксидные пленки У ионных кристаллов распределение электрического заряда на поверхности значительно отличается от его распределения в объеме реакционная способность поверхности повышена относительно ионов противоположного заряда 11
 Поверхностная энергия Может быть представлена в виде произведения поверхностного натяжения (обобщенная сила) на площадь поверхности (обобщенная координата) Геометрические параметры Удельная поверхность тела, как и дисперсной системы определяется отношением площади его поверхности S 1/2 между фазами 1 и 2 к объему тела V: Обычно объем дисперсной фазы, редко - дисперсионной среды 12
Поверхностная энергия Может быть представлена в виде произведения поверхностного натяжения (обобщенная сила) на площадь поверхности (обобщенная координата) Геометрические параметры Удельная поверхность тела, как и дисперсной системы определяется отношением площади его поверхности S 1/2 между фазами 1 и 2 к объему тела V: Обычно объем дисперсной фазы, редко - дисперсионной среды 12
 Твердые вещества Для большинства твердых веществ химические связи оказываются смешанными В оксидах металлов могут содержаться различные доли ионной и ковалентной связей Неоднозначность реакционной способности поверхности 13
Твердые вещества Для большинства твердых веществ химические связи оказываются смешанными В оксидах металлов могут содержаться различные доли ионной и ковалентной связей Неоднозначность реакционной способности поверхности 13
 Поверхностное натяжение σ Можно рассматривать 1 Как работу переноса молекул из объема тела на поверхность, связанную с разрывом межмолекулярных связей 2 Как силу, направленную тангенциально к поверхности и приходящуюся на единицу длины периметра, ограничивающего поверхность 3 Как работу образования единицы поверхности γ - поверхностное натяжение для твердых тел - обратимая работа по созданию новой поверхности путем добавления других атомов на поверхности 14
Поверхностное натяжение σ Можно рассматривать 1 Как работу переноса молекул из объема тела на поверхность, связанную с разрывом межмолекулярных связей 2 Как силу, направленную тангенциально к поверхности и приходящуюся на единицу длины периметра, ограничивающего поверхность 3 Как работу образования единицы поверхности γ - поверхностное натяжение для твердых тел - обратимая работа по созданию новой поверхности путем добавления других атомов на поверхности 14
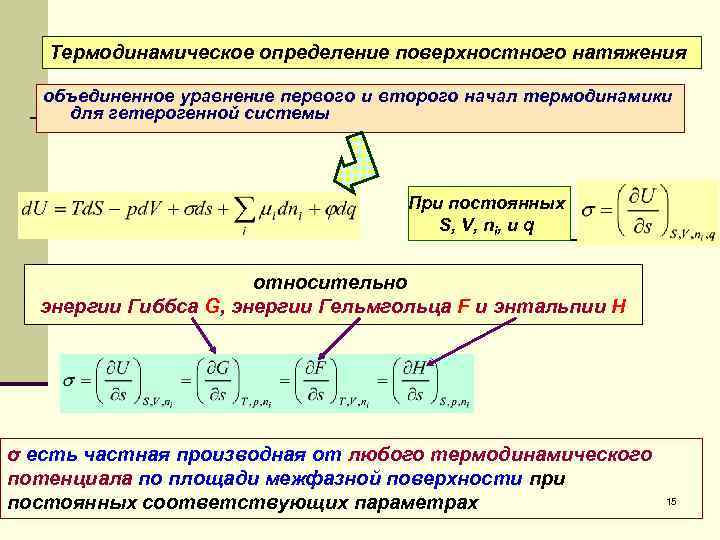 Термодинамическое определение поверхностного натяжения объединенное уравнение первого и второго начал термодинамики для гетерогенной системы При постоянных S, V, ni, и q относительно энергии Гиббса G, энергии Гельмгольца F и энтальпии Н σ есть частная производная от любого термодинамического потенциала по площади межфазной поверхности при постоянных соответствующих параметрах 15
Термодинамическое определение поверхностного натяжения объединенное уравнение первого и второго начал термодинамики для гетерогенной системы При постоянных S, V, ni, и q относительно энергии Гиббса G, энергии Гельмгольца F и энтальпии Н σ есть частная производная от любого термодинамического потенциала по площади межфазной поверхности при постоянных соответствующих параметрах 15
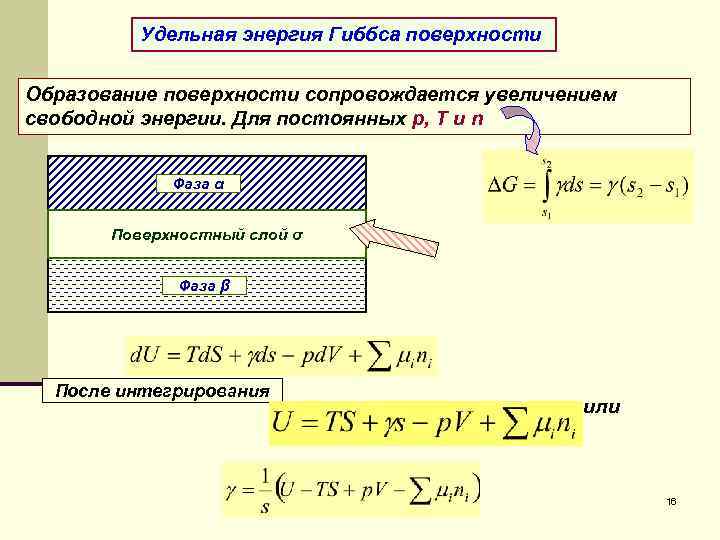 Удельная энергия Гиббса поверхности Образование поверхности сопровождается увеличением свободной энергии. Для постоянных р, Т и n Фаза α Поверхностный слой σ Фаза β После интегрирования или 16
Удельная энергия Гиббса поверхности Образование поверхности сопровождается увеличением свободной энергии. Для постоянных р, Т и n Фаза α Поверхностный слой σ Фаза β После интегрирования или 16
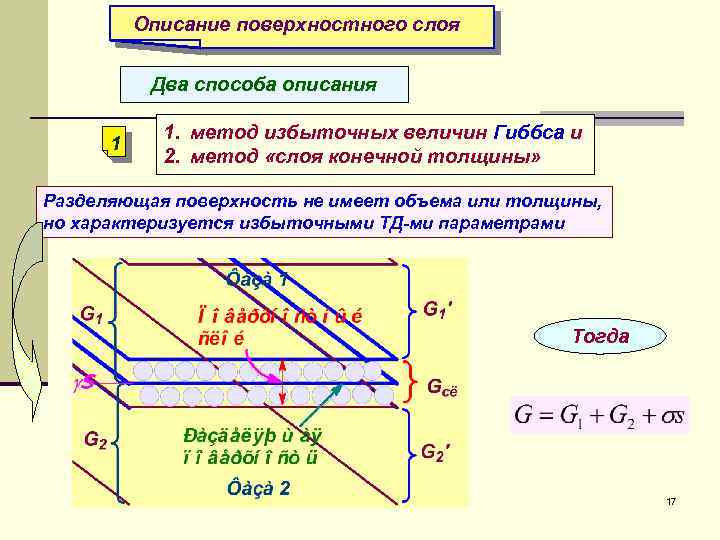 Описание поверхностного слоя Два способа описания 1 1. метод избыточных величин Гиббса и 2. метод «слоя конечной толщины» Разделяющая поверхность не имеет объема или толщины, но характеризуется избыточными ТД-ми параметрами Тогда 17
Описание поверхностного слоя Два способа описания 1 1. метод избыточных величин Гиббса и 2. метод «слоя конечной толщины» Разделяющая поверхность не имеет объема или толщины, но характеризуется избыточными ТД-ми параметрами Тогда 17
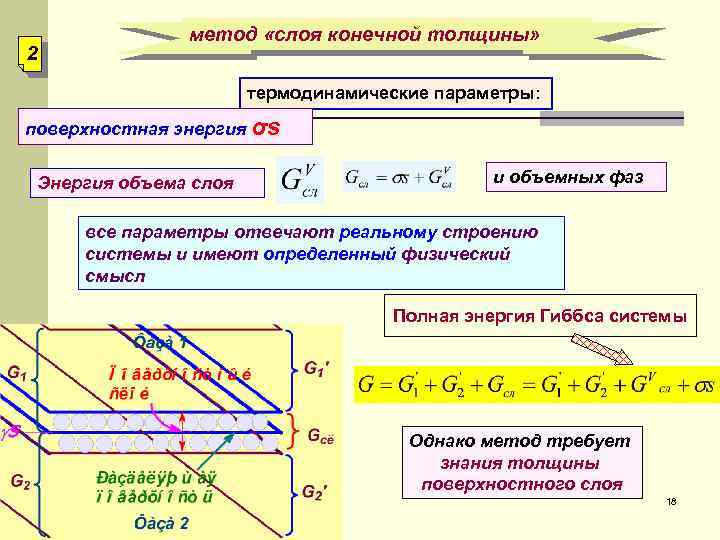 2 метод «слоя конечной толщины» термодинамические параметры: поверхностная энергия σs Энергия объема слоя и объемных фаз все параметры отвечают реальному строению системы и имеют определенный физический смысл Полная энергия Гиббса системы Однако метод требует знания толщины поверхностного слоя 18
2 метод «слоя конечной толщины» термодинамические параметры: поверхностная энергия σs Энергия объема слоя и объемных фаз все параметры отвечают реальному строению системы и имеют определенный физический смысл Полная энергия Гиббса системы Однако метод требует знания толщины поверхностного слоя 18
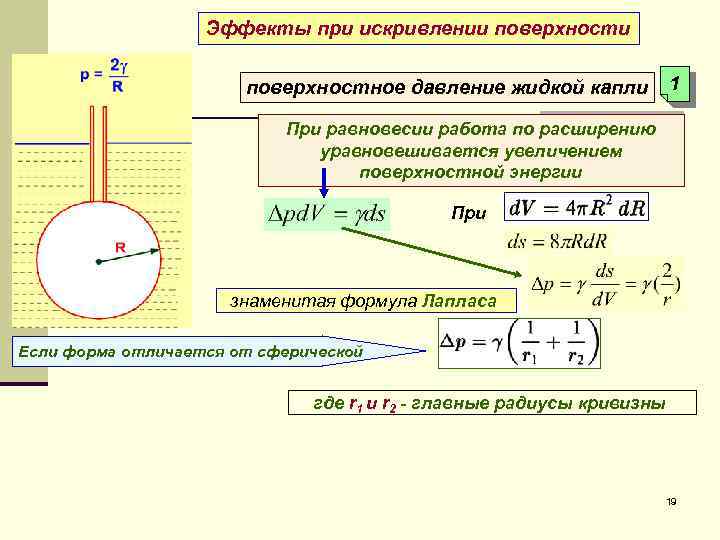 Эффекты при искривлении поверхности 1 поверхностное давление жидкой капли При равновесии работа по расширению уравновешивается увеличением поверхностной энергии При знаменитая формула Лапласа Если форма отличается от сферической где r 1 и r 2 - главные радиусы кривизны 19
Эффекты при искривлении поверхности 1 поверхностное давление жидкой капли При равновесии работа по расширению уравновешивается увеличением поверхностной энергии При знаменитая формула Лапласа Если форма отличается от сферической где r 1 и r 2 - главные радиусы кривизны 19
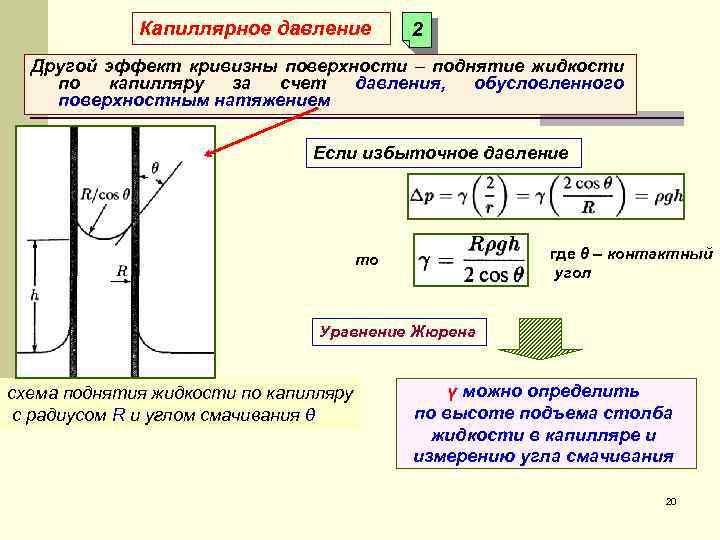 Капиллярное давление 2 Другой эффект кривизны поверхности – поднятие жидкости по капилляру за счет давления, обусловленного поверхностным натяжением Если избыточное давление где θ – контактный угол то Уравнение Жюрена схема поднятия жидкости по капилляру с радиусом R и углом смачивания θ γ можно определить по высоте подъема столба жидкости в капилляре и измерению угла смачивания 20
Капиллярное давление 2 Другой эффект кривизны поверхности – поднятие жидкости по капилляру за счет давления, обусловленного поверхностным натяжением Если избыточное давление где θ – контактный угол то Уравнение Жюрена схема поднятия жидкости по капилляру с радиусом R и углом смачивания θ γ можно определить по высоте подъема столба жидкости в капилляре и измерению угла смачивания 20
 Давление пара над искривленной поверхностью увеличивается по сравнению с плоской поверхностью Работа увеличения давления пара благодаря приложенному давлению Δр соответствует 1 Где V - молярный объем, р - давление пара над искривленной поверхностью, ро - давление пара над плоской поверхностью Уравнение тогда Кельвина (Томсона) где R - газовая постоянная, Т - температура, М - молекулярный вес, р - плотность Аналогичное выражение можно получить, рассматривая перенос 1 -ой молекулы в-ва из плоской поверхности через фазу пара на сферическую поверхность 21
Давление пара над искривленной поверхностью увеличивается по сравнению с плоской поверхностью Работа увеличения давления пара благодаря приложенному давлению Δр соответствует 1 Где V - молярный объем, р - давление пара над искривленной поверхностью, ро - давление пара над плоской поверхностью Уравнение тогда Кельвина (Томсона) где R - газовая постоянная, Т - температура, М - молекулярный вес, р - плотность Аналогичное выражение можно получить, рассматривая перенос 1 -ой молекулы в-ва из плоской поверхности через фазу пара на сферическую поверхность 21
 Работа переноса моля вещества на искривленную пов-ть 2 работа должна быть равна произведению поверхностной энергии на изменение площади поверхности Т. к. изменение объема соответствует dv = 4πr 2 dr то изменение радиуса при переносе 1 моля dr = V/(4πr 2) Увеличение давления паров над искривленной поверхностью может быть существенным для нанокластеров Например, для твердых нанокластеров Al 2 O 3 с размерами 100 нм при 1850°С давление превышает 2 %, а для 10 нм - уже 20 % 22
Работа переноса моля вещества на искривленную пов-ть 2 работа должна быть равна произведению поверхностной энергии на изменение площади поверхности Т. к. изменение объема соответствует dv = 4πr 2 dr то изменение радиуса при переносе 1 моля dr = V/(4πr 2) Увеличение давления паров над искривленной поверхностью может быть существенным для нанокластеров Например, для твердых нанокластеров Al 2 O 3 с размерами 100 нм при 1850°С давление превышает 2 %, а для 10 нм - уже 20 % 22
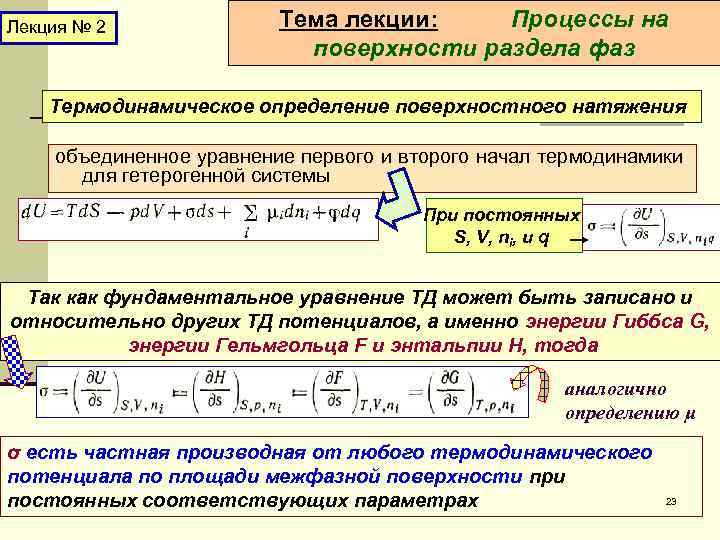 Лекция № 2 Тема лекции: Процессы на поверхности раздела фаз Термодинамическое определение поверхностного натяжения объединенное уравнение первого и второго начал термодинамики для гетерогенной системы При постоянных S, V, ni, и q Так как фундаментальное уравнение ТД может быть записано и относительно других ТД потенциалов, а именно энергии Гиббса G, энергии Гельмгольца F и энтальпии Н, тогда аналогично определению μ σ есть частная производная от любого термодинамического потенциала по площади межфазной поверхности при постоянных соответствующих параметрах 23
Лекция № 2 Тема лекции: Процессы на поверхности раздела фаз Термодинамическое определение поверхностного натяжения объединенное уравнение первого и второго начал термодинамики для гетерогенной системы При постоянных S, V, ni, и q Так как фундаментальное уравнение ТД может быть записано и относительно других ТД потенциалов, а именно энергии Гиббса G, энергии Гельмгольца F и энтальпии Н, тогда аналогично определению μ σ есть частная производная от любого термодинамического потенциала по площади межфазной поверхности при постоянных соответствующих параметрах 23
 Удельная энергия Гиббса для поверхности Изменение энергии Гиббса поверхности можно представить через энергию Гиббса, приходящуюся на единицу площади поверхности Gs, тогда Для индивидуальных веществ (d. Gs/ds = 0) Термодинамические потенциалы единицы поверхности не изменяются с изменением площади поверхности σ индивидуальных веществ является в то же время удельной энергией Гиббса поверхности общая энергия Гиббса поверхности линейно связана с площадью поверхности Удельная энергия Гиббса растворов зависит от удельной поверхности (d. Gs/ds ≠ 0) 24
Удельная энергия Гиббса для поверхности Изменение энергии Гиббса поверхности можно представить через энергию Гиббса, приходящуюся на единицу площади поверхности Gs, тогда Для индивидуальных веществ (d. Gs/ds = 0) Термодинамические потенциалы единицы поверхности не изменяются с изменением площади поверхности σ индивидуальных веществ является в то же время удельной энергией Гиббса поверхности общая энергия Гиббса поверхности линейно связана с площадью поверхности Удельная энергия Гиббса растворов зависит от удельной поверхности (d. Gs/ds ≠ 0) 24
 Поверхностное натяжение σ можно рассматривать 1 Как работу переноса молекул из объема тела на поверхность, связанную с разрывом межмолекулярных связей поверхностное натяжение меньше у неполярных жидкостей, имеющих слабые межмолекулярные связи, и больше у полярных жидкостей (Н 2 О) 2 Как силу, направленную тангенциально к поверхности и приходящуюся на единицу длины периметра, ограничивающего эту поверхность поверхностные молекулы, обладая некомпенсированной энергией, стремятся уйти в глубь конденсированной фазы и тем самым сжимают поверхность 25
Поверхностное натяжение σ можно рассматривать 1 Как работу переноса молекул из объема тела на поверхность, связанную с разрывом межмолекулярных связей поверхностное натяжение меньше у неполярных жидкостей, имеющих слабые межмолекулярные связи, и больше у полярных жидкостей (Н 2 О) 2 Как силу, направленную тангенциально к поверхности и приходящуюся на единицу длины периметра, ограничивающего эту поверхность поверхностные молекулы, обладая некомпенсированной энергией, стремятся уйти в глубь конденсированной фазы и тем самым сжимают поверхность 25
 В твердых телах переход поверхностных атомов и молекул в равновесное состояние может продолжаться очень долго вследствие их малой подвижности 3 Наиболее четким по физическому смыслу является представление о поверхностном натяжении как о работе образования единицы поверхности У тел в твердом состоянии по сравнению с жидким силы межмолекулярного и межатомного взаимодействия больше на величину, определяемую энтальпией плавления (затвердевания). 26
В твердых телах переход поверхностных атомов и молекул в равновесное состояние может продолжаться очень долго вследствие их малой подвижности 3 Наиболее четким по физическому смыслу является представление о поверхностном натяжении как о работе образования единицы поверхности У тел в твердом состоянии по сравнению с жидким силы межмолекулярного и межатомного взаимодействия больше на величину, определяемую энтальпией плавления (затвердевания). 26
 Когезионные и поверхностные силы Когезия - взаимодействие молекул, атомов, ионов внутри одной фазы, обусловленное силами притяжения различной природы и определяет существование веществ в конденсированном состоянии. Работа когезии - энергия обратимого изотермического разрыва тела по сечению, равному единице площади ! Когезия характеризуется такими параметрами, как энергия кристаллической решетки, внутреннее давление, энергия парообразования, температура кипения, летучесть Эти же параметры количественно характеризуют и поверхностное натяжение тел на границе с газом В уравнение Ван-дер-Ваальса для реальных газов входит внутреннее давление В жидкостях 1/V 2 >> чем для газов. Поэтому можно пренебречь 27 р уравнении Ван-дер-Ваальса. Тогда
Когезионные и поверхностные силы Когезия - взаимодействие молекул, атомов, ионов внутри одной фазы, обусловленное силами притяжения различной природы и определяет существование веществ в конденсированном состоянии. Работа когезии - энергия обратимого изотермического разрыва тела по сечению, равному единице площади ! Когезия характеризуется такими параметрами, как энергия кристаллической решетки, внутреннее давление, энергия парообразования, температура кипения, летучесть Эти же параметры количественно характеризуют и поверхностное натяжение тел на границе с газом В уравнение Ван-дер-Ваальса для реальных газов входит внутреннее давление В жидкостях 1/V 2 >> чем для газов. Поэтому можно пренебречь 27 р уравнении Ван-дер-Ваальса. Тогда
 Энергия парообразования работа когезии определяется энтальпией парообразования: Энтальпия парообразования твердых тел равна энергии кристаллической решетки В условиях равновесия при p и T = const ∆Gn = 0 и тогда Так как и при кипении р/рат. М = 1 Тогда где L - энтальпия парообразования при Ткип Т. О. , когезию жидкостей (и поверхностное натяжение) можно оценивать и сравнивать по Ткип и энтальпии парообразования 28
Энергия парообразования работа когезии определяется энтальпией парообразования: Энтальпия парообразования твердых тел равна энергии кристаллической решетки В условиях равновесия при p и T = const ∆Gn = 0 и тогда Так как и при кипении р/рат. М = 1 Тогда где L - энтальпия парообразования при Ткип Т. О. , когезию жидкостей (и поверхностное натяжение) можно оценивать и сравнивать по Ткип и энтальпии парообразования 28
 термодинамическое состояния вещества в поверхностных слоях Особенность заключается в избыточной поверхностной энергии на границе раздела фаз из-за нескомпенсированных сил поверхностных молекул и атомов по сравнению с состоянием молекул и атомов в объеме фаз (когезия) Особенность проявляется в ненасыщенности определенных физических сил и химических связей, характерных для конденсированных фаз Свойства поверхности непосредственно отражают природу ионов, атомов и молекул, находящихся на ней Для жидкостей и большинства твердых тел межмолекулярное взаимодействие обусловлено ван-дер-ваальсовыми и водородными связями Разрыв связей Поверхность способная образовывать ван-дер-ваальсовы и водородные связи с молекулами, попадающими на эту поверхность 29
термодинамическое состояния вещества в поверхностных слоях Особенность заключается в избыточной поверхностной энергии на границе раздела фаз из-за нескомпенсированных сил поверхностных молекул и атомов по сравнению с состоянием молекул и атомов в объеме фаз (когезия) Особенность проявляется в ненасыщенности определенных физических сил и химических связей, характерных для конденсированных фаз Свойства поверхности непосредственно отражают природу ионов, атомов и молекул, находящихся на ней Для жидкостей и большинства твердых тел межмолекулярное взаимодействие обусловлено ван-дер-ваальсовыми и водородными связями Разрыв связей Поверхность способная образовывать ван-дер-ваальсовы и водородные связи с молекулами, попадающими на эту поверхность 29
 При разрушении твердых тел, имеющих атомную кристаллическую решетку (кристаллы С, Ge, Si и др. ), разрываются ковалентные связи Реакционная способность атомов на поверхности таких тел чрезвычайно велика В условиях вакуума способны образовывать между собой двойные связи на воздухе реагируют с кислородом, образуя на поверхности оксидные пленки У ионных кристаллов распределение электрического заряда на поверхности значительно отличается от его распределения в объеме реакционная способность поверхности повышена относительно ионов противоположного заряда 30
При разрушении твердых тел, имеющих атомную кристаллическую решетку (кристаллы С, Ge, Si и др. ), разрываются ковалентные связи Реакционная способность атомов на поверхности таких тел чрезвычайно велика В условиях вакуума способны образовывать между собой двойные связи на воздухе реагируют с кислородом, образуя на поверхности оксидные пленки У ионных кристаллов распределение электрического заряда на поверхности значительно отличается от его распределения в объеме реакционная способность поверхности повышена относительно ионов противоположного заряда 30
 Твердые вещества Для большинства твердых веществ химические связи оказываются смешанными В оксидах металлов, из-за разной степени окисления Ме, могут содержаться различные доли ионной и ковалентной связей Неоднозначность реакционной способности поверхности Состав и структура твердых поверхностей зависят от условий их образования и последующей обработки, например • поверхности оксидов в момент образования проявляют более высокую химическую активность, чем после выдерживания на воздухе • предварительное взаимодействие с парами воды - на поверхности алюмосиликатов изменяется количественное соотношение между бренстедовскими и льюисовскими кислотными центрами 31
Твердые вещества Для большинства твердых веществ химические связи оказываются смешанными В оксидах металлов, из-за разной степени окисления Ме, могут содержаться различные доли ионной и ковалентной связей Неоднозначность реакционной способности поверхности Состав и структура твердых поверхностей зависят от условий их образования и последующей обработки, например • поверхности оксидов в момент образования проявляют более высокую химическую активность, чем после выдерживания на воздухе • предварительное взаимодействие с парами воды - на поверхности алюмосиликатов изменяется количественное соотношение между бренстедовскими и льюисовскими кислотными центрами 31
 Описание поверхностного слоя За толщину поверхностного слоя принимают расстояние по обе стороны от границы раздела фаз, за пределами которого свойства слоя перестают отличаться от свойств объемных фаз Существуют два способа (метода) описания поверхностного слоя 1 σs 1. метод избыточных величин Гиббса и 2. метод «слоя конечной толщины» Разделяющая поверхность рассматривается как не имеющая объема или толщины, но характеризуется избыточными ТД-ми параметрами, отражающими проявление пов. энергии Тогда энергия Гиббса системы равна сумме энергий Гиббса G 1 и G 2 объемных фаз 1, 2 и поверхностной энергии Гиббса σs, которая является избыточной: 32
Описание поверхностного слоя За толщину поверхностного слоя принимают расстояние по обе стороны от границы раздела фаз, за пределами которого свойства слоя перестают отличаться от свойств объемных фаз Существуют два способа (метода) описания поверхностного слоя 1 σs 1. метод избыточных величин Гиббса и 2. метод «слоя конечной толщины» Разделяющая поверхность рассматривается как не имеющая объема или толщины, но характеризуется избыточными ТД-ми параметрами, отражающими проявление пов. энергии Тогда энергия Гиббса системы равна сумме энергий Гиббса G 1 и G 2 объемных фаз 1, 2 и поверхностной энергии Гиббса σs, которая является избыточной: 32
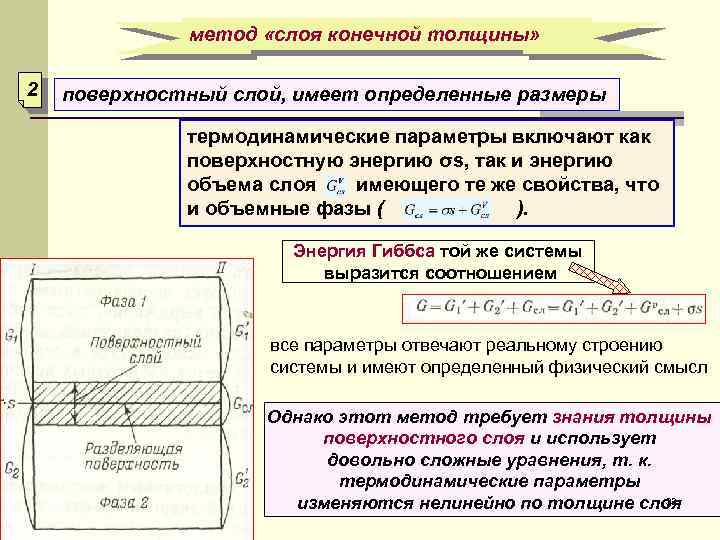 метод «слоя конечной толщины» 2 поверхностный слой, имеет определенные размеры термодинамические параметры включают как поверхностную энергию σs, так и энергию объема слоя , имеющего те же свойства, что и объемные фазы ( ). Энергия Гиббса той же системы выразится соотношением все параметры отвечают реальному строению системы и имеют определенный физический смысл Однако этот метод требует знания толщины поверхностного слоя и использует довольно сложные уравнения, т. к. термодинамические параметры 33 изменяются нелинейно по толщине слоя
метод «слоя конечной толщины» 2 поверхностный слой, имеет определенные размеры термодинамические параметры включают как поверхностную энергию σs, так и энергию объема слоя , имеющего те же свойства, что и объемные фазы ( ). Энергия Гиббса той же системы выразится соотношением все параметры отвечают реальному строению системы и имеют определенный физический смысл Однако этот метод требует знания толщины поверхностного слоя и использует довольно сложные уравнения, т. к. термодинамические параметры 33 изменяются нелинейно по толщине слоя


