Ткач Н,С-слайди.ppt
- Количество слайдов: 9
 ЛИСТ 1 Дніпродзержинський державний технічний університет Хіміко-технологічний факультет кафедра промислової біотехнології та загальної хімії Випускна кваліфікаційна робота бакалавра Аналіз сучасних технологій виробництва незамінних амінокислот з метою вибору оптимальної для умов України
ЛИСТ 1 Дніпродзержинський державний технічний університет Хіміко-технологічний факультет кафедра промислової біотехнології та загальної хімії Випускна кваліфікаційна робота бакалавра Аналіз сучасних технологій виробництва незамінних амінокислот з метою вибору оптимальної для умов України
 ЛИСТ 2 Ø Об’єкт дослідження – лізин, як основна незамінна амінокислота Ø Мета роботи – аналіз існуючих технологій виробництва лізину з метою вибору оптимальної. Ø Задача роботи – охарактеризувати фізико-хімічні властивості лізину, визначити сферу використання амінокислоти, вибрати самий оптимальний спосіб виробництва лізину, охарактеризувати мікробіологічні основи виробництва, розробити процесуальну та технологічну схеми. Потрібно описати заходи по поліпшенню умов з охорони праці в цеху виробництва лізина.
ЛИСТ 2 Ø Об’єкт дослідження – лізин, як основна незамінна амінокислота Ø Мета роботи – аналіз існуючих технологій виробництва лізину з метою вибору оптимальної. Ø Задача роботи – охарактеризувати фізико-хімічні властивості лізину, визначити сферу використання амінокислоти, вибрати самий оптимальний спосіб виробництва лізину, охарактеризувати мікробіологічні основи виробництва, розробити процесуальну та технологічну схеми. Потрібно описати заходи по поліпшенню умов з охорони праці в цеху виробництва лізина.
 ЛИСТ 3 Ø Лізин – незамінна амінокислота, відома у вигляді двох оптично активних L і D форм. Емпірична формула С 6 Н 12 N 2 О 2. Молекулярна маса 146, 19 г/моль. Лізин добре розчинний у воді, кислотах, основах, важко розчинний у спирті і нерозчинний в ефірі. Амінокислота при температурі 224 - 225 ° С розкладається. Кристалізується лізин у вигляді безбарвних голок або гексагональних пластинок. • При титруванні лугом лізин веде себе, як двохосновна кислота, тобто вона може віддавати два протона. Якщо реєструвати зміну р. Н при додаванні лугу, то отримуємо типові криві титрування амінокислоти. Значення рІ основних амінокислот обчисляють як середнє арифметичне значення р. К 2 і р. К 3, наприклад для лізину рІ= (9, 12 + 10, 35) / 2 = 9, 82. Значення р. К характеризує кислотність амінокислот.
ЛИСТ 3 Ø Лізин – незамінна амінокислота, відома у вигляді двох оптично активних L і D форм. Емпірична формула С 6 Н 12 N 2 О 2. Молекулярна маса 146, 19 г/моль. Лізин добре розчинний у воді, кислотах, основах, важко розчинний у спирті і нерозчинний в ефірі. Амінокислота при температурі 224 - 225 ° С розкладається. Кристалізується лізин у вигляді безбарвних голок або гексагональних пластинок. • При титруванні лугом лізин веде себе, як двохосновна кислота, тобто вона може віддавати два протона. Якщо реєструвати зміну р. Н при додаванні лугу, то отримуємо типові криві титрування амінокислоти. Значення рІ основних амінокислот обчисляють як середнє арифметичне значення р. К 2 і р. К 3, наприклад для лізину рІ= (9, 12 + 10, 35) / 2 = 9, 82. Значення р. К характеризує кислотність амінокислот.
 ЛИСТ 4 • • • Лише недавно в світі освоєно виробництво чистого кристалічного L-лізину з концентрацією 98, 5% і вище, що різко підвищило його привабливість для тваринництва і птахівництва, а також, після відповідного очищення, для харчової промисловості. Основні функції, які виконує лізин в організмі людини: 1. Вироблення антитіл імунної системи; 2. Вироблення гормонів ендокринної системи; 3. Вироблення ферментів травної системи; 4. Забезпечення транспорту кисню і поживних речовин; 5. Забезпечення роботи серцевого м'яза; 6. Забезпечення функції жовчного міхура 7. Попереджує карієс. Амінокислота має противірусну дію, особливо відносно вірусів, що викликають герпес і гострі респіраторні інфекції. Рекомендується поєднувати лізин з вітаміном С при вірусних захворюваннях. У Сполучених Штатах Америки і деяких країнах Європи для профілактики часто рецидивуючих форм герпесу застосовуються біологічно активні добавки до їжі на основі лізину. Кілька десятиліть тому було помічено, що у деяких людей, які страждають від герпесу, але дотримували певну дієту, рецидиви бувають рідше
ЛИСТ 4 • • • Лише недавно в світі освоєно виробництво чистого кристалічного L-лізину з концентрацією 98, 5% і вище, що різко підвищило його привабливість для тваринництва і птахівництва, а також, після відповідного очищення, для харчової промисловості. Основні функції, які виконує лізин в організмі людини: 1. Вироблення антитіл імунної системи; 2. Вироблення гормонів ендокринної системи; 3. Вироблення ферментів травної системи; 4. Забезпечення транспорту кисню і поживних речовин; 5. Забезпечення роботи серцевого м'яза; 6. Забезпечення функції жовчного міхура 7. Попереджує карієс. Амінокислота має противірусну дію, особливо відносно вірусів, що викликають герпес і гострі респіраторні інфекції. Рекомендується поєднувати лізин з вітаміном С при вірусних захворюваннях. У Сполучених Штатах Америки і деяких країнах Європи для профілактики часто рецидивуючих форм герпесу застосовуються біологічно активні добавки до їжі на основі лізину. Кілька десятиліть тому було помічено, що у деяких людей, які страждають від герпесу, але дотримували певну дієту, рецидиви бувають рідше
 ЛИСТ 5 • • За допомогою комбінованого способу виробництва лізин отримують з 95% виходом і 99% оптичною чистотою, причому зміст амінокислоти в реакційній суміші може досягати 200 г / л, що практично більш ніж удвічі вище його змісту в культуральній рідині , одержуваної в одну стадію при направленому мікробіологічному синтезі в найкращих виробничих ферментаціях. Технологія процесу включає в себе органічний синтез D, L-а-аміно-εкапролактаму з циклогексану і його ферментативний гідроліз. Дана схема виробництва припускає використання двох ферментів - L-гідролази і рацемази. Перший селективно гідролізує D, L-а-аміно-ε-капролактам, що отримується в процесі органічного синтезу, другий здійснює рацемізацію L-гідролазою D-форми в L-форму. Максимально можлива ефективність такого виробництва буде спостерігатися в тому випадку, коли швидкості обох ферментативних процесів досить високі. Необхідні для здійснення процесу ферменти мають мікробне походження. Відомо, що гідролазу L-а-аміно-εкапролактаму продукують штами дріжджів родів Candida, Cryptococcus, активаторами цього ферменту є двовалентні іони марганцю, магнію і цинку. Фермент рацемазу D-ааміно-ε-капролактаму можливо отримати при культивуванні бактерій родів Achrobacter, Flavobacterium. Спільний вплив обох ферментів на субстрат L, D-а-аміноε-капролактам раціонально проводити в апараті безперервної дії, що містить обидва ферменти в імобілізованому вигляді
ЛИСТ 5 • • За допомогою комбінованого способу виробництва лізин отримують з 95% виходом і 99% оптичною чистотою, причому зміст амінокислоти в реакційній суміші може досягати 200 г / л, що практично більш ніж удвічі вище його змісту в культуральній рідині , одержуваної в одну стадію при направленому мікробіологічному синтезі в найкращих виробничих ферментаціях. Технологія процесу включає в себе органічний синтез D, L-а-аміно-εкапролактаму з циклогексану і його ферментативний гідроліз. Дана схема виробництва припускає використання двох ферментів - L-гідролази і рацемази. Перший селективно гідролізує D, L-а-аміно-ε-капролактам, що отримується в процесі органічного синтезу, другий здійснює рацемізацію L-гідролазою D-форми в L-форму. Максимально можлива ефективність такого виробництва буде спостерігатися в тому випадку, коли швидкості обох ферментативних процесів досить високі. Необхідні для здійснення процесу ферменти мають мікробне походження. Відомо, що гідролазу L-а-аміно-εкапролактаму продукують штами дріжджів родів Candida, Cryptococcus, активаторами цього ферменту є двовалентні іони марганцю, магнію і цинку. Фермент рацемазу D-ааміно-ε-капролактаму можливо отримати при культивуванні бактерій родів Achrobacter, Flavobacterium. Спільний вплив обох ферментів на субстрат L, D-а-аміноε-капролактам раціонально проводити в апараті безперервної дії, що містить обидва ферменти в імобілізованому вигляді
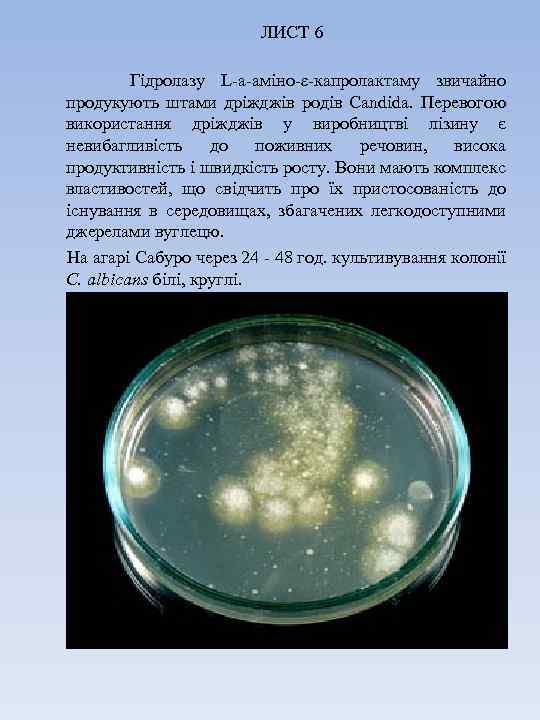 ЛИСТ 6 Гідролазу L-а-аміно-ε-капролактаму звичайно продукують штами дріжджів родів Candida. Перевогою використання дріжджів у виробництві лізину є невибагливість до поживних речовин, висока продуктивність і швидкість росту. Вони мають комплекс властивостей, що свідчить про їх пристосованість до існування в середовищах, збагачених легкодоступними джерелами вуглецю. На агарі Сабуро через 24 - 48 год. культивування колонії C. albicans білі, круглі.
ЛИСТ 6 Гідролазу L-а-аміно-ε-капролактаму звичайно продукують штами дріжджів родів Candida. Перевогою використання дріжджів у виробництві лізину є невибагливість до поживних речовин, висока продуктивність і швидкість росту. Вони мають комплекс властивостей, що свідчить про їх пристосованість до існування в середовищах, збагачених легкодоступними джерелами вуглецю. На агарі Сабуро через 24 - 48 год. культивування колонії C. albicans білі, круглі.
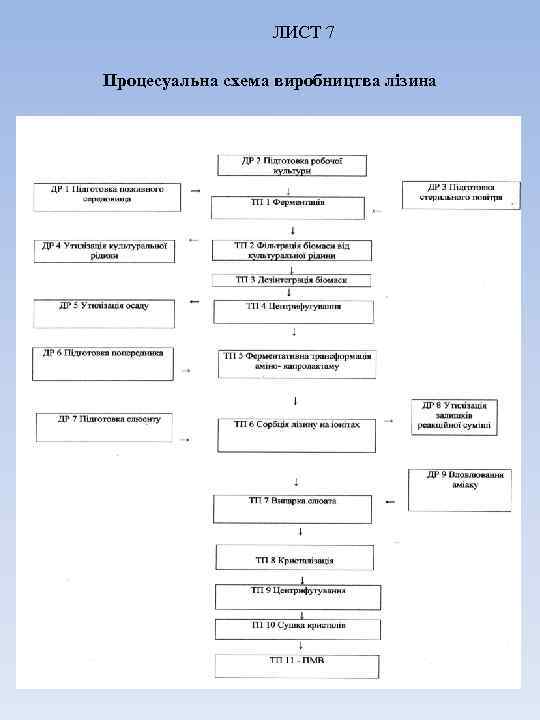 ЛИСТ 7 Процесуальна схема виробництва лізина
ЛИСТ 7 Процесуальна схема виробництва лізина
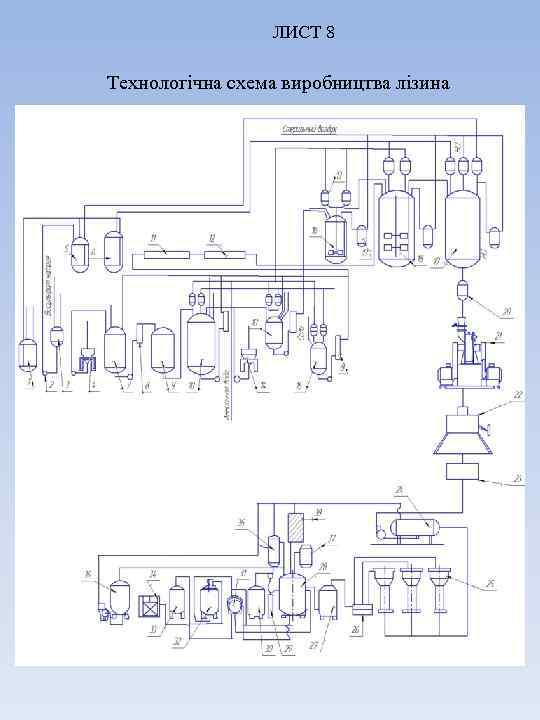 ЛИСТ 8 Технологічна схема виробництва лізина
ЛИСТ 8 Технологічна схема виробництва лізина
 ЛИСТ 9 Висновки • • • Охарактеризували фізико-хімічні властивості лізину; Визначили сферу використання амінокислоти; Виявили, що самим оптимальним способом виробництва лізину є ензиматичний спосіб; Охарактеризували мікробіологічні основи виробництва; Розробили процесуальну та технологічну схеми виробництва лізину; Описали заходи по поліпшенню умов з охорони праці в цеху виробництва лізина.
ЛИСТ 9 Висновки • • • Охарактеризували фізико-хімічні властивості лізину; Визначили сферу використання амінокислоти; Виявили, що самим оптимальним способом виробництва лізину є ензиматичний спосіб; Охарактеризували мікробіологічні основи виробництва; Розробили процесуальну та технологічну схеми виробництва лізину; Описали заходи по поліпшенню умов з охорони праці в цеху виробництва лізина.


