лекция липиды фарм рус.ppt
- Количество слайдов: 33
 Липиды: строение, классификация, функции. Транспорт липидов по крови. Обмен простых липидов
Липиды: строение, классификация, функции. Транспорт липидов по крови. Обмен простых липидов
 Обратный транспорт холестерина печень кишечник ЛПВП 4. ЛПНП 3. ЛПОНП хиломикроны 1. ткани Остатки ХМ и ЛПОНП 1. 2. ЛППП капилляр ЛП-липаза Предшественники ЛПВП из печени и желудка Свободные жирные кислоты
Обратный транспорт холестерина печень кишечник ЛПВП 4. ЛПНП 3. ЛПОНП хиломикроны 1. ткани Остатки ХМ и ЛПОНП 1. 2. ЛППП капилляр ЛП-липаза Предшественники ЛПВП из печени и желудка Свободные жирные кислоты
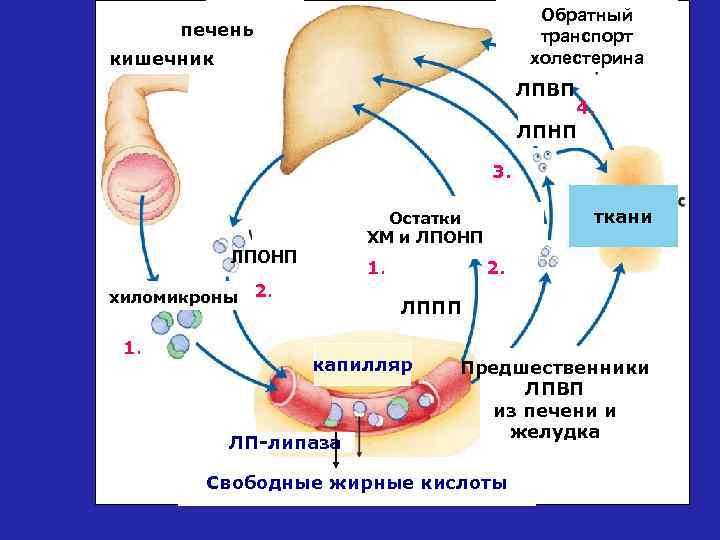
 Транспорт липидов Избыток жирных кислот и углеводов в печени превращаются в триацилглицериды (а также эфиры холестерина и холестерин) и упаковываются в липопротеиды очень низкой плотности (ЛПОНП), после чего поступают в кровь. Они транспортируют липиды в адипоциты и мышцы. При потере триацилглицеридов ЛОНП превращаются в липопротеиды низкой плотности (ЛНП). Они обогащены холестерином и эфирами холестерина. ЛНП переносят холестерин к тканям, взаимодействуя с рецепторами с помощью Аpo-100. Липопротеиды высокой плотности (ЛВП) образуются в печени и поступают в кровь. Они содержат фермент лецитин-холестерол ацилтрансферазу, который обеспечивает образование эфиров холестерина из лецитина и свободного холестерина хиломикронов и ЛПОНП, образуя зрелые частицы, возвращаемые в печень.
Транспорт липидов Избыток жирных кислот и углеводов в печени превращаются в триацилглицериды (а также эфиры холестерина и холестерин) и упаковываются в липопротеиды очень низкой плотности (ЛПОНП), после чего поступают в кровь. Они транспортируют липиды в адипоциты и мышцы. При потере триацилглицеридов ЛОНП превращаются в липопротеиды низкой плотности (ЛНП). Они обогащены холестерином и эфирами холестерина. ЛНП переносят холестерин к тканям, взаимодействуя с рецепторами с помощью Аpo-100. Липопротеиды высокой плотности (ЛВП) образуются в печени и поступают в кровь. Они содержат фермент лецитин-холестерол ацилтрансферазу, который обеспечивает образование эфиров холестерина из лецитина и свободного холестерина хиломикронов и ЛПОНП, образуя зрелые частицы, возвращаемые в печень.
 Функция различных липопротеидов ХМ - транспорт экзогенных триацилглицеридов ЛПОНП – транспорт эндогенных триацилглицеридов ЛППП – предшественник ЛПНП – транспорт холестерина в ткани ЛПВП – обратный транспорт холестерина
Функция различных липопротеидов ХМ - транспорт экзогенных триацилглицеридов ЛПОНП – транспорт эндогенных триацилглицеридов ЛППП – предшественник ЛПНП – транспорт холестерина в ткани ЛПВП – обратный транспорт холестерина
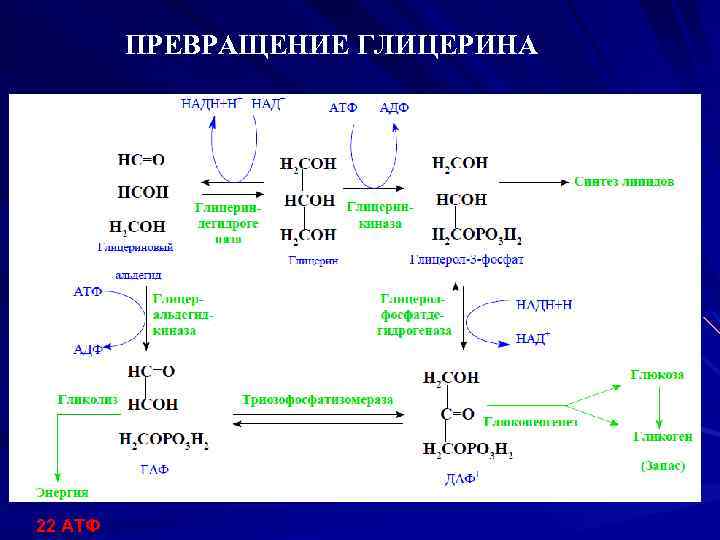 ПРЕВРАЩЕНИЕ ГЛИЦЕРИНА 22 АТФ
ПРЕВРАЩЕНИЕ ГЛИЦЕРИНА 22 АТФ
 ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ Окисление ВЖК протекает в митохондриальном матриксе только в аэробных условиях, так как тесно связано с функционированием цитратного цикла и цепи переноса электронов. Доставка жирных кислот к месту их окисления – к митохондриям – происходит сложным путем: • при участии альбумина осуществляется транспорт жирной кислоты в клетку; • при участии специальных белков (fatty acid binding proteins, FABP) - транспорт в пределах цитозоля до митохондрий; • при участии карнитина – транспорт жирной кислоты из цитозоля в митохондрии.
ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ Окисление ВЖК протекает в митохондриальном матриксе только в аэробных условиях, так как тесно связано с функционированием цитратного цикла и цепи переноса электронов. Доставка жирных кислот к месту их окисления – к митохондриям – происходит сложным путем: • при участии альбумина осуществляется транспорт жирной кислоты в клетку; • при участии специальных белков (fatty acid binding proteins, FABP) - транспорт в пределах цитозоля до митохондрий; • при участии карнитина – транспорт жирной кислоты из цитозоля в митохондрии.
 Активация жирных кислот. Свободная жирная кислота независимо от длины углеводородной цепи является метаболически инертной и не может подвергаться никаким биохимическим превращениям, в том числе окислению, пока не будет активирована. Активация жирной кислоты протекает на наружной поверхности мембраны митохондрий при участии АТФ, коэнзима A (HS-Ko. A) и ионов Mg 2+. Реакция катализируется ферментом ацил-Ко. А-синтетазой: В результате реакции образуется ацил-Ко. А, являющийся активной формой жирной кислоты.
Активация жирных кислот. Свободная жирная кислота независимо от длины углеводородной цепи является метаболически инертной и не может подвергаться никаким биохимическим превращениям, в том числе окислению, пока не будет активирована. Активация жирной кислоты протекает на наружной поверхности мембраны митохондрий при участии АТФ, коэнзима A (HS-Ko. A) и ионов Mg 2+. Реакция катализируется ферментом ацил-Ко. А-синтетазой: В результате реакции образуется ацил-Ко. А, являющийся активной формой жирной кислоты.
 Под действием фермента карнитинацилтрансферазы I (КАТ 1) ацильный остаток с ацил-Ко. А переносится на карнитин с образованием ацилкарнитина. Специфическая транслоказа проводит это вещество через внутреннюю мембрану митохондрий. На внутренней поверхности внутренней мембраны митохондрий карнитинацилтрансфераза II (КАТ П) расщепляет ацилкарнитин с помощью митохондриального HS-Ко. А. Ацил-Ко. А, освобождающийся в матрикс, участвует в реакциях β-окисления, а свободный карнитин той же транслоказой возвращается на наружную мембрану.
Под действием фермента карнитинацилтрансферазы I (КАТ 1) ацильный остаток с ацил-Ко. А переносится на карнитин с образованием ацилкарнитина. Специфическая транслоказа проводит это вещество через внутреннюю мембрану митохондрий. На внутренней поверхности внутренней мембраны митохондрий карнитинацилтрансфераза II (КАТ П) расщепляет ацилкарнитин с помощью митохондриального HS-Ко. А. Ацил-Ко. А, освобождающийся в матрикс, участвует в реакциях β-окисления, а свободный карнитин той же транслоказой возвращается на наружную мембрану.
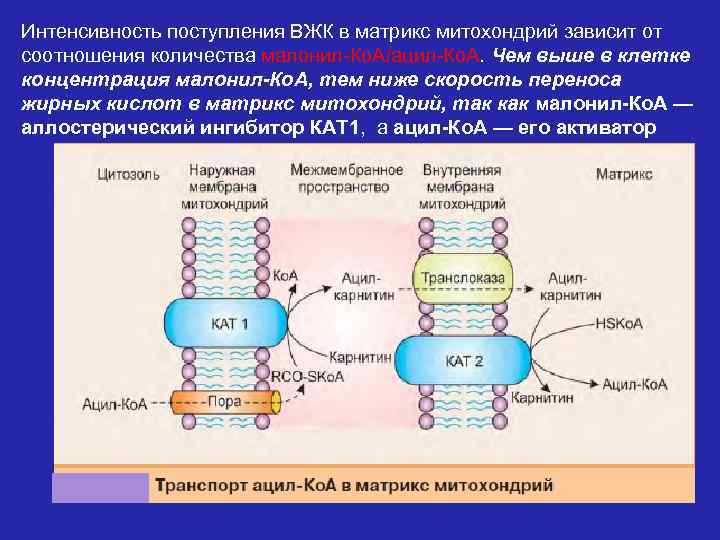 Интенсивность поступления ВЖК в матрикс митохондрий зависит от соотношения количества малонил-Ко. А/ацил-Ко. А. Чем выше в клетке концентрация малонил-Ко. А, тем ниже скорость переноса жирных кислот в матрикс митохондрий, так как малонил-Ко. А — аллостерический ингибитор КАТ 1, а ацил-Ко. А — его активатор
Интенсивность поступления ВЖК в матрикс митохондрий зависит от соотношения количества малонил-Ко. А/ацил-Ко. А. Чем выше в клетке концентрация малонил-Ко. А, тем ниже скорость переноса жирных кислот в матрикс митохондрий, так как малонил-Ко. А — аллостерический ингибитор КАТ 1, а ацил-Ко. А — его активатор
 Попав в матрикс митохондрий, ацильный остаток в циклическом процессе с помощью совокупности ферментов окисляется по βуглеродному атому. Каждый цикл включает четыре последовательные реакции, в результате которых жирная кислота укорачивается на два углеродных атома, которые отщепляются в виде ацетил-Ко. А. Ацетил-Ко. А может вступать в цитратный цикл и окисляться до СО 2 и Н 2 О, а укороченный ацильный остаток будет вовлекаться в следующий цикл β-окисления.
Попав в матрикс митохондрий, ацильный остаток в циклическом процессе с помощью совокупности ферментов окисляется по βуглеродному атому. Каждый цикл включает четыре последовательные реакции, в результате которых жирная кислота укорачивается на два углеродных атома, которые отщепляются в виде ацетил-Ко. А. Ацетил-Ко. А может вступать в цитратный цикл и окисляться до СО 2 и Н 2 О, а укороченный ацильный остаток будет вовлекаться в следующий цикл β-окисления.
 Первая стадия дегидрирования. Ацил-Ко. А в митохондриях прежде всего подвергается ферментативному дегидрированию, при этом ацил-Ко. А теряет 2 атома водорода в α- и β-положениях, превращаясь в Ко. А-эфир ненасыщенной кислоты. Таким образом, первой реакцией в каждом цикле распада ацил-Ко. А является его окисление ФАД-содержащей ацил. Ко. А-дегидрогеназой, приводящее к образованию еноил. Ко. А с двойной связью между С-2 и С-3:
Первая стадия дегидрирования. Ацил-Ко. А в митохондриях прежде всего подвергается ферментативному дегидрированию, при этом ацил-Ко. А теряет 2 атома водорода в α- и β-положениях, превращаясь в Ко. А-эфир ненасыщенной кислоты. Таким образом, первой реакцией в каждом цикле распада ацил-Ко. А является его окисление ФАД-содержащей ацил. Ко. А-дегидрогеназой, приводящее к образованию еноил. Ко. А с двойной связью между С-2 и С-3:
 Стадия гидратации. Ненасыщенный ацил-Ко. А (еноил-Ко. А) при участии фермента еноил-Ко. А-гидратазы присоединяет молекулу воды. В результате образуется β-оксиацил-Ко. А (или 3 -гидроксиацил-Ко. А):
Стадия гидратации. Ненасыщенный ацил-Ко. А (еноил-Ко. А) при участии фермента еноил-Ко. А-гидратазы присоединяет молекулу воды. В результате образуется β-оксиацил-Ко. А (или 3 -гидроксиацил-Ко. А):
 Вторая стадия дегидрирования. Образовавшийся β-оксиацил-Ко. А (3 гидроксиацил-Ко. А) затем дегидрируется. Эту реакцию катализируют НАД+-зависимые дегидрогеназы:
Вторая стадия дегидрирования. Образовавшийся β-оксиацил-Ко. А (3 гидроксиацил-Ко. А) затем дегидрируется. Эту реакцию катализируют НАД+-зависимые дегидрогеназы:
 Тиолазная реакция представляет собой расщепление 3 -оксоацил-Ко. А с помощью тиоловой группы второй молекулы Ко. А. В результате образуется укороченный на два углеродных атома ацил-Ко. А и двууглеродный фрагмент в виде ацетил-Ко. А. Данная реакция катализируется ацетил-Ко. А-ацилтрансферазой (β-кетотиолазой):
Тиолазная реакция представляет собой расщепление 3 -оксоацил-Ко. А с помощью тиоловой группы второй молекулы Ко. А. В результате образуется укороченный на два углеродных атома ацил-Ко. А и двууглеродный фрагмент в виде ацетил-Ко. А. Данная реакция катализируется ацетил-Ко. А-ацилтрансферазой (β-кетотиолазой):
 Энергетический баланс окисления жирных кислот В результате β-окисления ВЖК полностью расщепляются до ацетил-Ко. А, и суммарное уравнение окисления, например пальмитиновой кислоты (С 16) имеет следующий вид: СН 3(СН 2)14 -СО~SКо. А + 7 FAD + 7 NAD+ +7 H 2 O + 7 HSKo. A→ 8 CH 3 CO~SКо. А + 7 FADH 2 + 7(NADH + H+)
Энергетический баланс окисления жирных кислот В результате β-окисления ВЖК полностью расщепляются до ацетил-Ко. А, и суммарное уравнение окисления, например пальмитиновой кислоты (С 16) имеет следующий вид: СН 3(СН 2)14 -СО~SКо. А + 7 FAD + 7 NAD+ +7 H 2 O + 7 HSKo. A→ 8 CH 3 CO~SКо. А + 7 FADH 2 + 7(NADH + H+)
 Окисление ненасыщенных ВЖК идет по пути βокисления до получения жирной кислоты с – НС=СН-связью в положении С 3–С 4. Дополнительные ферменты: еноил-Ко. Аизомераза и трансфераза перемещают двойную связь в положение 2– 3 и цис-изомер превращают в транс-изомер. Далее β-окисление продолжается с участием ферментов, описанных ранее. При расчете выхода АТФ за счет окисления ненасыщенных ВЖК можно пользоваться формулой для расчета выхода энергии при окислении насыщенных ВЖК, вычитая 2 АТФ на каждую двойную связь.
Окисление ненасыщенных ВЖК идет по пути βокисления до получения жирной кислоты с – НС=СН-связью в положении С 3–С 4. Дополнительные ферменты: еноил-Ко. Аизомераза и трансфераза перемещают двойную связь в положение 2– 3 и цис-изомер превращают в транс-изомер. Далее β-окисление продолжается с участием ферментов, описанных ранее. При расчете выхода АТФ за счет окисления ненасыщенных ВЖК можно пользоваться формулой для расчета выхода энергии при окислении насыщенных ВЖК, вычитая 2 АТФ на каждую двойную связь.
 Жирные кислоты с нечетным числом углеродных атомов окисляются таким же образом, как и жирные кислоты с четным числом углеродных атомов, однако, что на последнем этапе расщепления (β-окисления) образуется одна молекула пропионил-Ко. А и одна молекула ацетил-Ко. А, а не 2 молекулы ацетил-Ко. А. Активированный трехуглеродный фрагмент – пропионил-Ко. А – включается в цикл трикарбоновых кислот после превращения в сукцинил-Ко. А.
Жирные кислоты с нечетным числом углеродных атомов окисляются таким же образом, как и жирные кислоты с четным числом углеродных атомов, однако, что на последнем этапе расщепления (β-окисления) образуется одна молекула пропионил-Ко. А и одна молекула ацетил-Ко. А, а не 2 молекулы ацетил-Ко. А. Активированный трехуглеродный фрагмент – пропионил-Ко. А – включается в цикл трикарбоновых кислот после превращения в сукцинил-Ко. А.
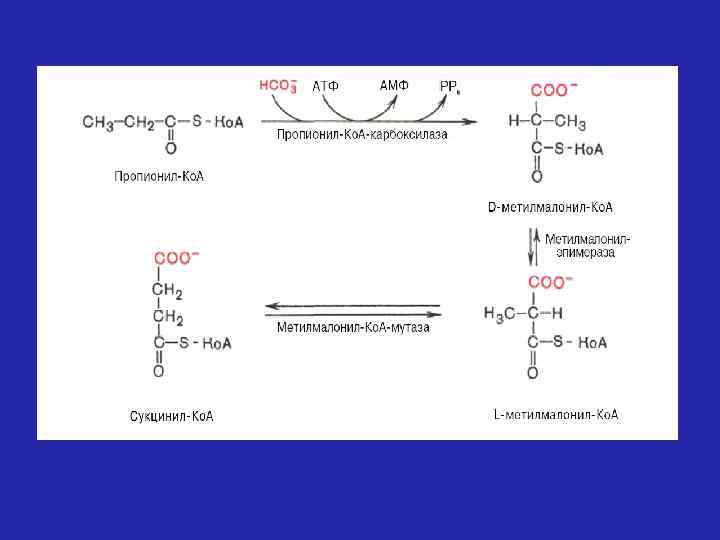
 Нарушения процесса β-окисления. Встречаются патологии, связанные со снижением транспорта ВЖК в матрикс митохондрий. Они могут быть вызваны: – дефицитом карнитина в результате снижения его синтеза, потерями этого вещества при гемодиализе или за счет экскреции с кетоновыми телами; – низкой активностью КАТ 1 фермента, связанной с дефектом в структуре гена этого фермента или его ингибированием некоторыми лекарственными препаратами, например сульфонилмочевиной, которая используется для лечения сахарного диабета. Среди ферментов β-окисления ацил-Ко. А-дегидрогеназа представлена несколькими видами, специфичными к длине углеводородного радикала жирной кислоты. Достаточно часто встречается наследственная болезнь, вызванная дефектами в структуре гена ацил-Ко. А-дегидрогеназы, окисляющей жирные кислоты со средним числом углеродных атомов –С 4 — С 12. Установлено, что смерть каждого десятого новорожденного происходит в результате недостаточности этого фермента. В жирах молока содержится много среднецепочечных жирных кислот, которые не могут окисляться у таких детей. Единственным источником энергии для таких больных становятся углеводы, а при сравнительно продолжительных интервалах между кормлениями развивается тяжелая гипогликемия, сопровождающаяся потерей сознания, а иногда и гибелью ребенка.
Нарушения процесса β-окисления. Встречаются патологии, связанные со снижением транспорта ВЖК в матрикс митохондрий. Они могут быть вызваны: – дефицитом карнитина в результате снижения его синтеза, потерями этого вещества при гемодиализе или за счет экскреции с кетоновыми телами; – низкой активностью КАТ 1 фермента, связанной с дефектом в структуре гена этого фермента или его ингибированием некоторыми лекарственными препаратами, например сульфонилмочевиной, которая используется для лечения сахарного диабета. Среди ферментов β-окисления ацил-Ко. А-дегидрогеназа представлена несколькими видами, специфичными к длине углеводородного радикала жирной кислоты. Достаточно часто встречается наследственная болезнь, вызванная дефектами в структуре гена ацил-Ко. А-дегидрогеназы, окисляющей жирные кислоты со средним числом углеродных атомов –С 4 — С 12. Установлено, что смерть каждого десятого новорожденного происходит в результате недостаточности этого фермента. В жирах молока содержится много среднецепочечных жирных кислот, которые не могут окисляться у таких детей. Единственным источником энергии для таких больных становятся углеводы, а при сравнительно продолжительных интервалах между кормлениями развивается тяжелая гипогликемия, сопровождающаяся потерей сознания, а иногда и гибелью ребенка.
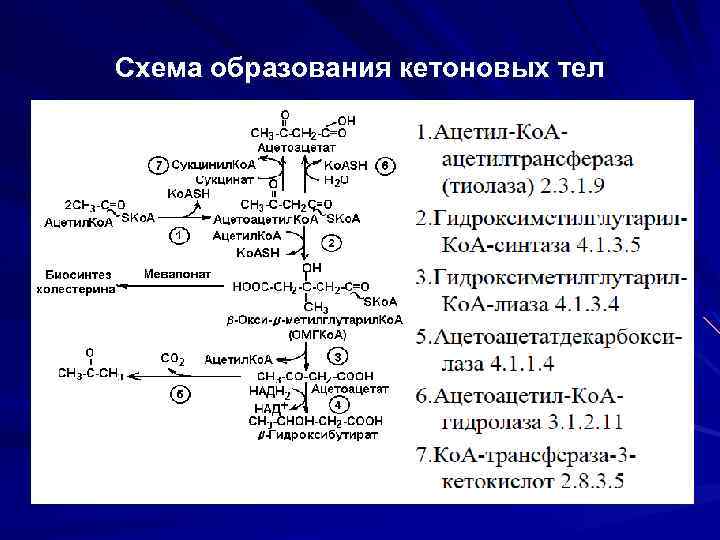 Схема образования кетоновых тел
Схема образования кетоновых тел
 Распад кетоновых тел
Распад кетоновых тел
 Синтез высших жирных кислот Основную регуляторную реакцию синтеза ВЖК катализирует биотинсодержащий фермент — ацетил-Ко. А-карбоксилаза, в ходе которой ацетил-Ко. А превращается в малонил-Ко. А. Реакция протекает в два этапа: I – карбоксилирование биотина с участием АТФ и II – перенос карбоксильной группы на ацетил-Ко. А, в результате чего образуется малонил-Ко. А:
Синтез высших жирных кислот Основную регуляторную реакцию синтеза ВЖК катализирует биотинсодержащий фермент — ацетил-Ко. А-карбоксилаза, в ходе которой ацетил-Ко. А превращается в малонил-Ко. А. Реакция протекает в два этапа: I – карбоксилирование биотина с участием АТФ и II – перенос карбоксильной группы на ацетил-Ко. А, в результате чего образуется малонил-Ко. А:
 Благодаря ключевому положению этой реакции в синтезе ВЖК активность ацетил-Ко. А-карбоксилазы может изменяться в широких пределах путем: – ассоциации и диссоциации протомеров. Цитрат стимулирует ассоциацию и повышает активность фермента, а увеличение концентрации ацил-Ко. А ускоряет диссоциацию протомеров и снижает активность фермента. – фосфорилирования и дефосфорилирования. Инсулин стимулирует дефосфорилирование и повышает активность фермента, а глюкагон и адреналин — фосфорилирование и его инактивацию. – индукции синтеза новых молекул фермента под влиянием инсулина.
Благодаря ключевому положению этой реакции в синтезе ВЖК активность ацетил-Ко. А-карбоксилазы может изменяться в широких пределах путем: – ассоциации и диссоциации протомеров. Цитрат стимулирует ассоциацию и повышает активность фермента, а увеличение концентрации ацил-Ко. А ускоряет диссоциацию протомеров и снижает активность фермента. – фосфорилирования и дефосфорилирования. Инсулин стимулирует дефосфорилирование и повышает активность фермента, а глюкагон и адреналин — фосфорилирование и его инактивацию. – индукции синтеза новых молекул фермента под влиянием инсулина.
 Мультиферментный комплекс, называемый синтетазой (синтазой) жирных кислот, состоит из 6 ферментов, связанных с так называемым ацилпереносящим белком (АПБ). Этот белок относительно термостабилен, имеет две свободные HS-группы и вовлекается в процесс синтеза высших жирных кислот практически на всех его этапах. Последовательность реакций, происходящих при синтезе жирных кислот:
Мультиферментный комплекс, называемый синтетазой (синтазой) жирных кислот, состоит из 6 ферментов, связанных с так называемым ацилпереносящим белком (АПБ). Этот белок относительно термостабилен, имеет две свободные HS-группы и вовлекается в процесс синтеза высших жирных кислот практически на всех его этапах. Последовательность реакций, происходящих при синтезе жирных кислот:
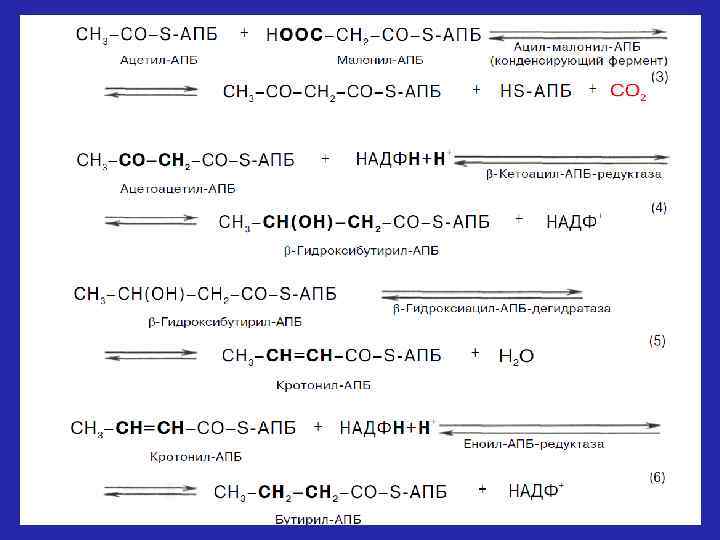
 Далее цикл реакций повторяется. Допустим, что идет синтез пальмитиновой кислоты (С 16). В этом случае образованием бутирил-АПБ завершается лишь первый из 7 циклов, в каждом из которых началом является присоединение молекулы малонил-АПБ к карбоксильному концу растущей цепи жирной кислоты. При этом отщепляется дистальная карбоксильная группа малонил-АПБ в виде СО 2. Например, образовавшийся в первом цикле бутирил-АПБ взаимодействует с малонил-АПБ:
Далее цикл реакций повторяется. Допустим, что идет синтез пальмитиновой кислоты (С 16). В этом случае образованием бутирил-АПБ завершается лишь первый из 7 циклов, в каждом из которых началом является присоединение молекулы малонил-АПБ к карбоксильному концу растущей цепи жирной кислоты. При этом отщепляется дистальная карбоксильная группа малонил-АПБ в виде СО 2. Например, образовавшийся в первом цикле бутирил-АПБ взаимодействует с малонил-АПБ:
 Завершается синтез жирной кислоты отщеплением HS-АПБ от ацил-АПБ под влиянием фермента деацилазы.
Завершается синтез жирной кислоты отщеплением HS-АПБ от ацил-АПБ под влиянием фермента деацилазы.
 По сравнению с β-окислением биосинтез жирных кислот имеет ряд характерных особенностей: • синтез жирных кислот в основном осуществляется в цитозоле клетки, а окисление – в митохондриях; • участие в процессе биосинтеза жирных кислот малонил-Ко. А, который образуется путем связывания СО 2 (в присутствии биотинфермента и АТФ) с ацетил-Ко. А; • на всех этапах синтеза жирных кислот принимает участие ацилпереносящий белок (HS-АПБ); • при биосинтезе образуется D(–)-изомер 3 -гидроксикислоты, а не L(+)-изомер, как это имеет место при β-окислении жирных кислот; • необходимость для синтеза жирных кислот кофермента НАДФН в организме частично (на 50%) образуется в реакциях пентозофосфатного цикла, частично – в других реакциях, в частности в реакциях: Малат + НАДФ+ –> Пируват + СO 2 + НАДФН + Н+ Изоцитрат + НАДФ+ –> α-Кетоглутарат + СO 2 + НАДФН + Н+.
По сравнению с β-окислением биосинтез жирных кислот имеет ряд характерных особенностей: • синтез жирных кислот в основном осуществляется в цитозоле клетки, а окисление – в митохондриях; • участие в процессе биосинтеза жирных кислот малонил-Ко. А, который образуется путем связывания СО 2 (в присутствии биотинфермента и АТФ) с ацетил-Ко. А; • на всех этапах синтеза жирных кислот принимает участие ацилпереносящий белок (HS-АПБ); • при биосинтезе образуется D(–)-изомер 3 -гидроксикислоты, а не L(+)-изомер, как это имеет место при β-окислении жирных кислот; • необходимость для синтеза жирных кислот кофермента НАДФН в организме частично (на 50%) образуется в реакциях пентозофосфатного цикла, частично – в других реакциях, в частности в реакциях: Малат + НАДФ+ –> Пируват + СO 2 + НАДФН + Н+ Изоцитрат + НАДФ+ –> α-Кетоглутарат + СO 2 + НАДФН + Н+.
 Жирные кислоты с числом углеродных атомов больше, чем 16, (элонгация) синтезируются в эндоплазматиче-ском ретикулуме аналогично тому, как это происходит на пальмитилсинтазе. Однако каждую стадию процесса катализируют отдельные ферменты. Удлинение цепи происходит с помощью малонил-Ко. А, а в реакциях восстановления используется NADPH + H+. Образование ненасыщенных жирных кислот (десатурация)— пальмитоолеиновой и олеиновой кислот — происходит на мембране эндоплазматического ретикулума (ЭР), двойные связи между С 9 и С 10 возникают за счет работы оксигеназы жирных кислот, которая требует для своей работы участия О 2 и NADPH.
Жирные кислоты с числом углеродных атомов больше, чем 16, (элонгация) синтезируются в эндоплазматиче-ском ретикулуме аналогично тому, как это происходит на пальмитилсинтазе. Однако каждую стадию процесса катализируют отдельные ферменты. Удлинение цепи происходит с помощью малонил-Ко. А, а в реакциях восстановления используется NADPH + H+. Образование ненасыщенных жирных кислот (десатурация)— пальмитоолеиновой и олеиновой кислот — происходит на мембране эндоплазматического ретикулума (ЭР), двойные связи между С 9 и С 10 возникают за счет работы оксигеназы жирных кислот, которая требует для своей работы участия О 2 и NADPH.
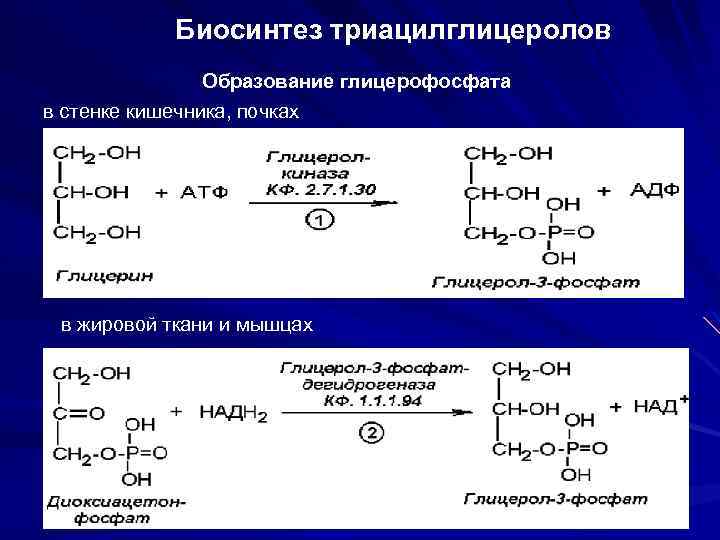 Биосинтез триацилглицеролов Образование глицерофосфата в стенке кишечника, почках в жировой ткани и мышцах
Биосинтез триацилглицеролов Образование глицерофосфата в стенке кишечника, почках в жировой ткани и мышцах
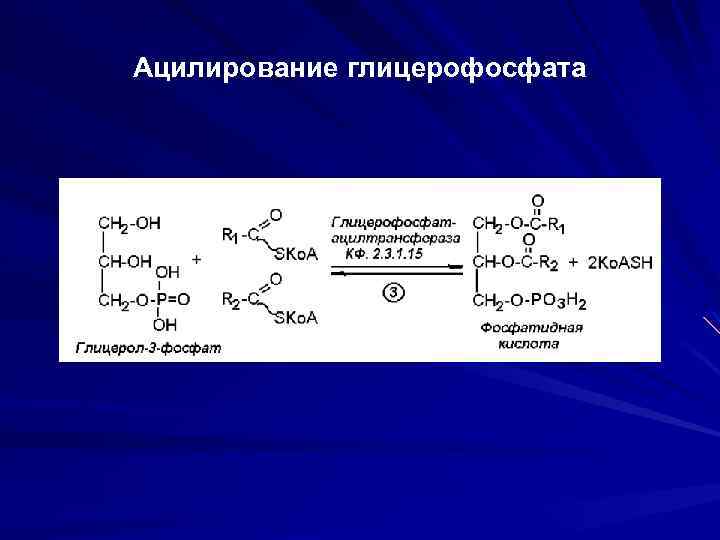 Ацилирование глицерофосфата
Ацилирование глицерофосфата
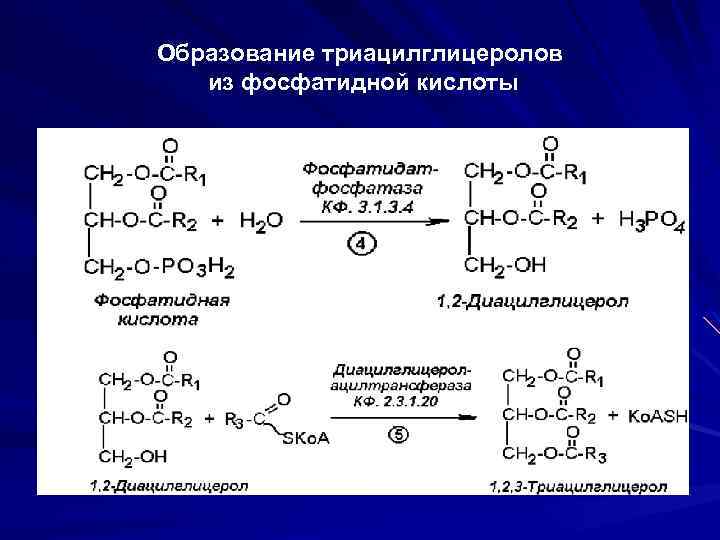 Образование триацилглицеролов из фосфатидной кислоты
Образование триацилглицеролов из фосфатидной кислоты
 БУДЬТЕ ЗДОРОВЫ!
БУДЬТЕ ЗДОРОВЫ!


