Липиды 3.11. 2012.ppt
- Количество слайдов: 68

Липиды 3 Тканевой метаболизм липидов Лекция 14

Содержание: 1. Окисление насыщенных ЖК с нечетным числом атомов С 2. Биосинтез ненасыщенных ЖК 3. Биосинтез кетоновых тел 4. Биосинтез ХС. Пул ХС в клетке 5. Биосинтез ТГ и фосфатидов 6. Биосинтез жирных кислот 7. Механизм регуляции углеводного обмена. Жиро- углеводный цикл Рэндла
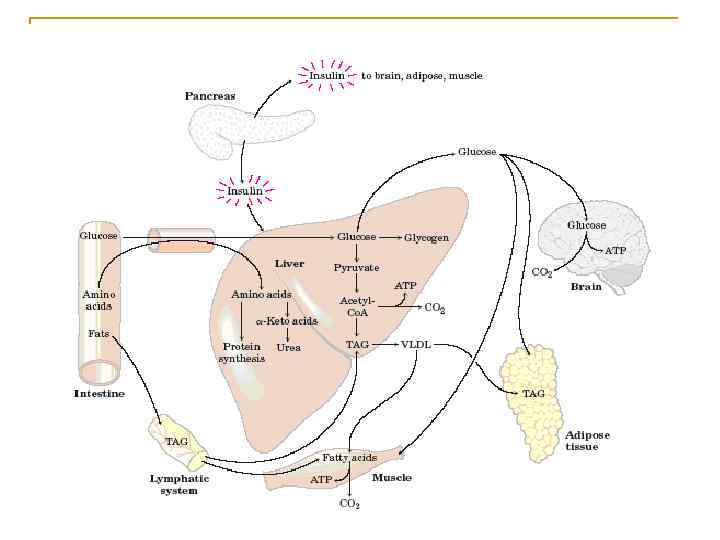

Насыщенные ЖК с нечетным числом атомов С. Для них характерно ß- окисление до момента образования пропионил-S Ко. А, который далее переходит в сукцинил-Ко. А - ЦТК. Ненасыщенный ЖК- обеспечивают жидкое состояние мембран. В клетке образуются из насыщенных ЖК. Яв-ся незаменимым фактором в питании ( линолевая, линоленовая, арахидоновая кислоты).
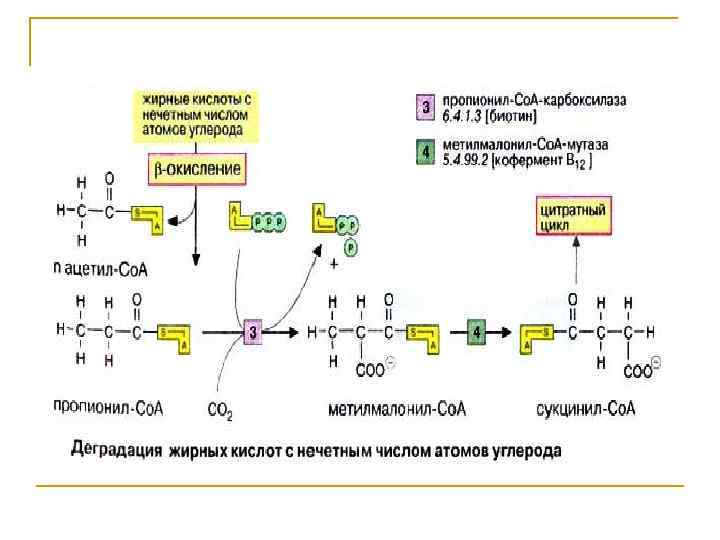
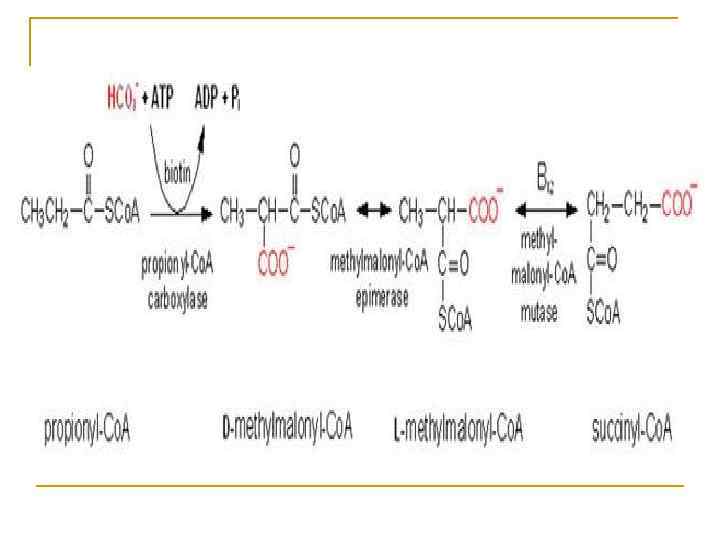

Окисление ненасыщенных ЖК происходит также как и у насыщенных , но с предварительным переносом = связи из положения ▲ 3 -4 в положение ▲ 2 -3. Также изменяется конформация из = связи из цис в транс. Этот фермент- называется ▲ 3, 4 -цис▲ 2, 3 -транс- еноил- Ко. А –изомераза.
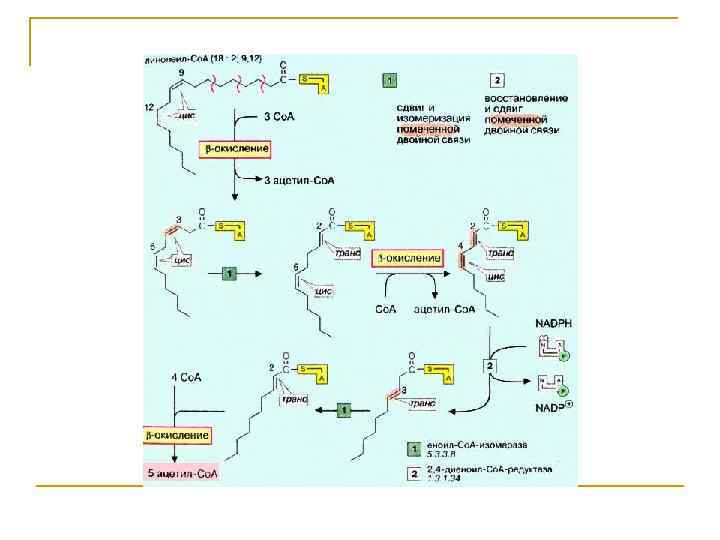
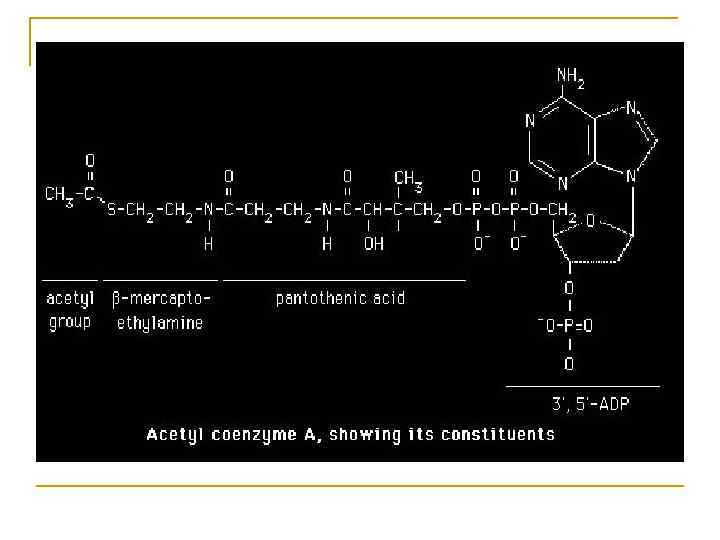


Происхождение ненасыщенных жирных кислот в клетках организма. n n Незаменимые и заменимые. Среди ненасыщенных жирных кислот в организме человека не могут синтезироваться -3 и -6 жирные кислоты в связи с отсутствием ферментной системы, которая могла бы катализировать образование двойной связи в положении -6 или любом другом положении, близко расположенном к -концу.

К таким жирным кислотам относятся линолевая кислота (18: 2, 9, 12), линоленовая кислота (18: 3, 9, 12, 15) и арахидоновая кислота (20: 4, 5, 8, 11, 14). Последняя является незаменимой только при недостатке линолевой кислоты, поскольку в норме она может синтезироваться из линолевой кислоты

Синтез ненасыщенных жирных кислот из насыщенных с параллельным удлинением цепи. Десатурация проходит под действием микросомального комплекса ферментов, состоящего из трех компонентов белковой природы: цитохрома b 5, цитохром b 5 -редуктазы и десатуразы, которые содержат в своем составе негемовое железо. В качестве субстратов используются НАДФН и молекулярный кислород.

Из этих компонентов образуется короткая цепь переноса электронов, с помощью которой на короткий период времени в молекулу жирной кислоты включаются гидроксильные группы. Затем они отщепляются в виде воды, в результате в молекуле жирной кислоты формируется двойная связь. Есть целое семейство субъединиц десатуразы, которые специфичны к определенному месту введения двойной связи.
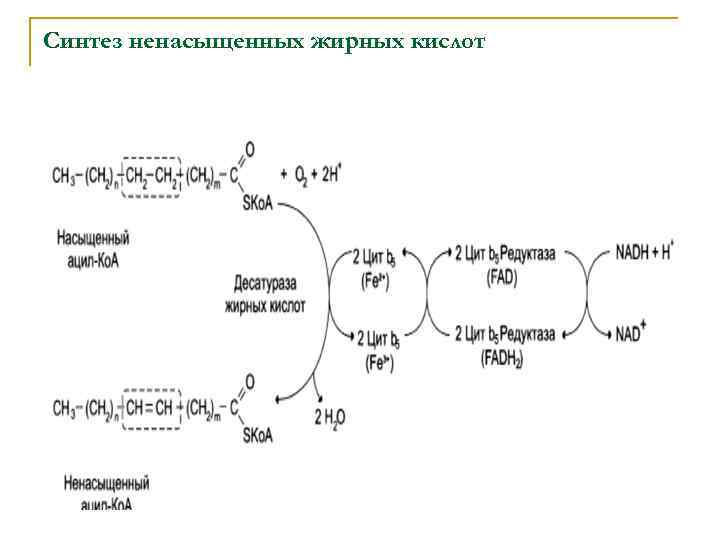
Синтез ненасыщенных жирных кислот
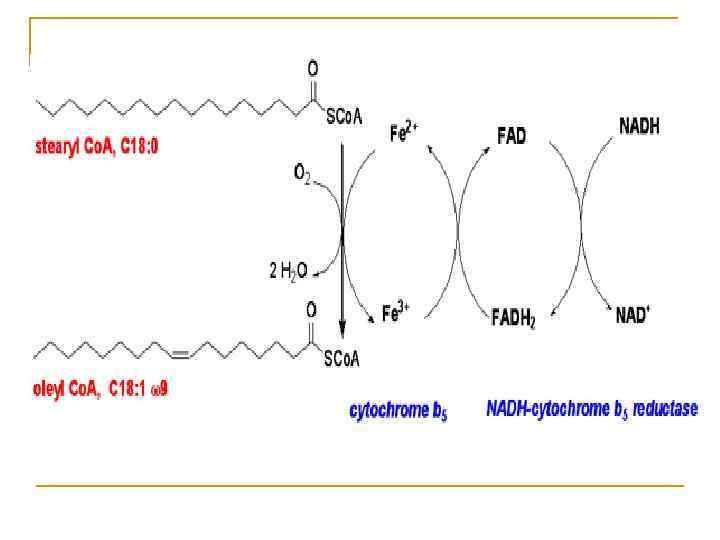

Синтез полиеновых жирных кислот в организме человека
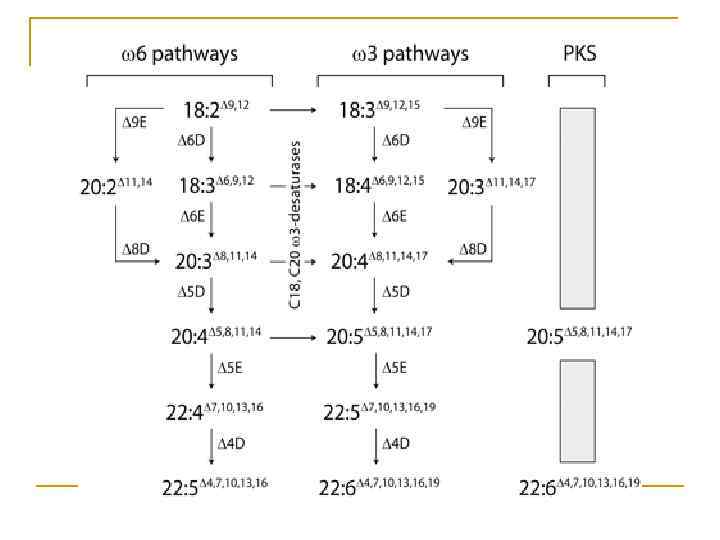
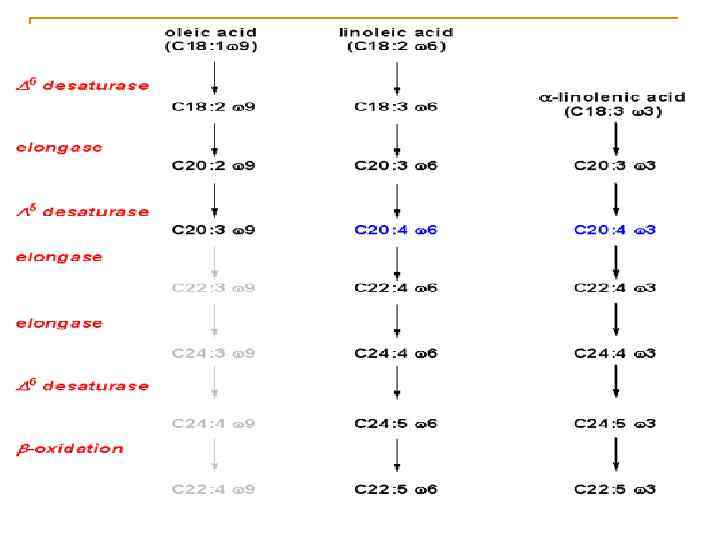

У человека при недостатке в пище незаменимых жирных кислот описаны дерматологические изменения. Обычный рацион взрослых людей содержит достаточное количество незаменимых жирных кислот. Однако у новорожденных, которые получают рацион, обедненный жирами, отмечаются признаки поражения кожи. Они проходят, если в курс лечения включается линолевая кислота.

Случаи подобного дефицита наблюдаются и у пациентов, которые длительное время находятся на парентеральном питании, обедненном незаменимыми жирными кислотами. В качестве профилактики такого состояния достаточно, чтобы в организм поступали незаменимые жирные кислоты в количестве 1 -2% от общей калорической потребности.
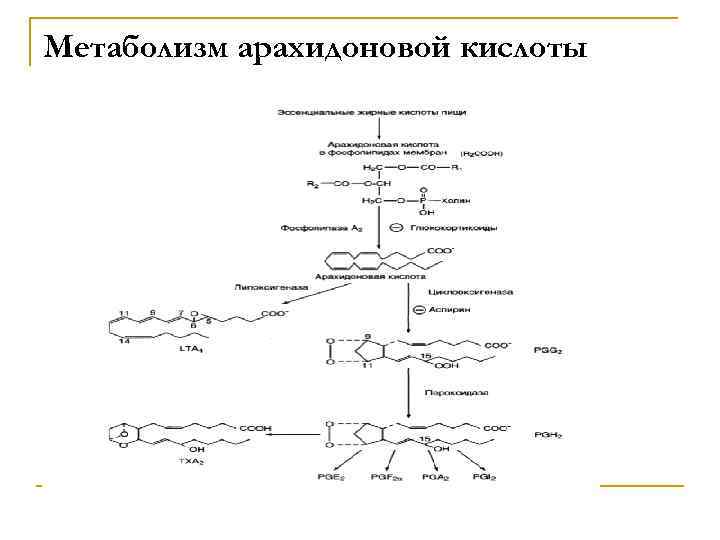
Метаболизм арахидоновой кислоты
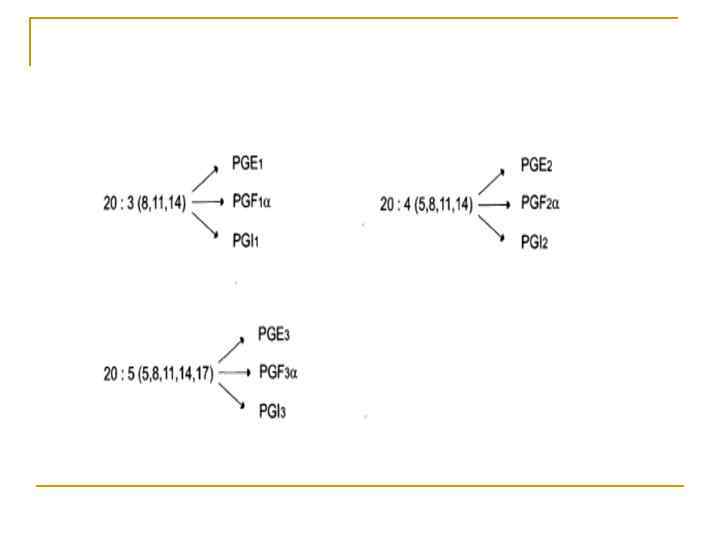

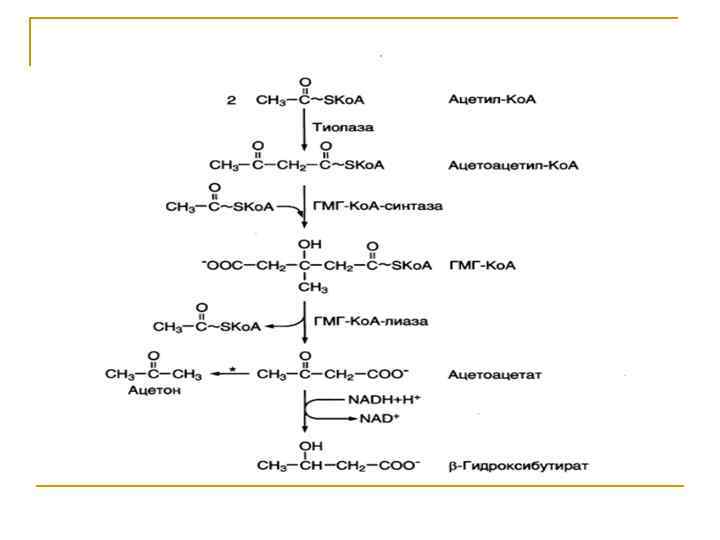
Образование и утилизация кетоновых тел n Двумя основными видами ацетоновых тел являются ацетоацетат и гидроксибутират. -гидроксибутират - это восстановленная форма ацетоацетата. Ацетоацетат образуется в клетках печени из ацетил~Ко. А. Образование происходит в митохондриальном матриксе.
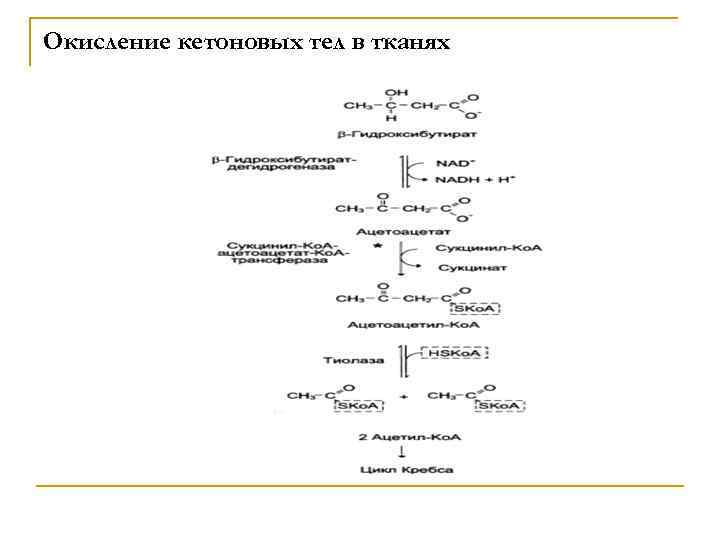
Окисление кетоновых тел в тканях


Первоначальная стадия этого процесса катализируется ферментом - -кетотиолазой. Затем ацетоацетил. Ко. А конденсируется со следующей молекулой ацетил-Ко. А под влиянием фермента ГОМГ-Ко. А синтетазы. В результате образуется -гидрокси -метилглютарил-Ко. А. Затем фермент - ГОМГ-Ко. А лиаза катализирует расщепление ГОМГ-Ко. А на ацетоацетат и ацетил-Ко. А.

В дальнейшем ацетоуксусная кислота восстанавливается под влиянием фермента bгидроксибутиратдегидрогеназы и в результате образуется b-оксимасляная кислота. Затем фермент - ГОМГ-Ко. А лиаза катализирует расщепление ГОМГ-Ко. А на ацетоацетат и ацетил-Ко. А.

В дальнейшем ацетоуксусная кислота восстанавливается под влиянием фермента bгидроксибутиратдегидрогеназы и в результате образуется bоксимасляная кислота.

Количество ацетоацетата, которое восстанавливается в -гидроксибутират, зависит от соотношения НАДН/НАД+. Восстановление это происходит под влиянием фермента гидроксибутиратдегидрогеназы. Печень служит главным местом образования кетоновых тел благодаря высокому содержанию ГОМГ-Ко. А синтетазы в митохондриях гепатоцитов.

Эти реакции происходят в митохондриях. В цитозоле имеются изоферменты - -кетотиолазы и ГОМГ~Ко. А синтетазы, которые также катализируют образование ГОМГ~Ко. А, но в качестве промежуточного продукта в синтезе холестерола. Цитозольный и митохондриальный фонды ГОМГ~Ко. А не смешиваются.

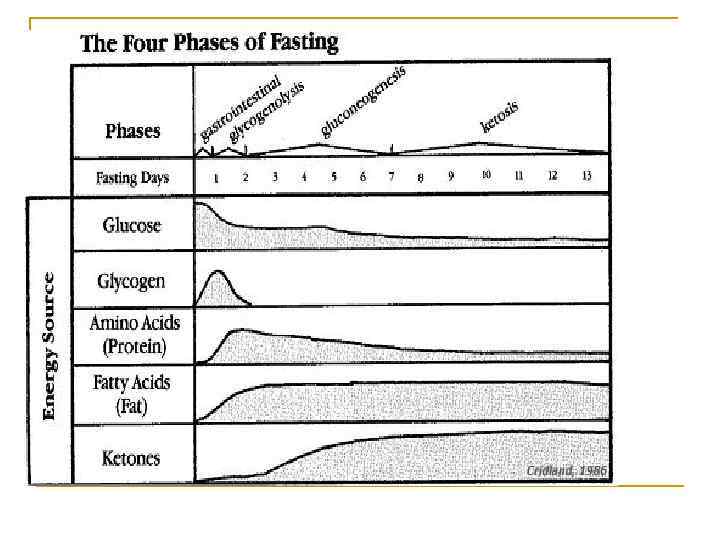
Образование кетоновых тел в печени контролируется состоянием питания. Такое контрольное действие усиливается инсулином и глюкагоном. Принятие пищи и инсулин снижают образование кетоновых тел, в то время как при голодании стимулируется кетогенез вследствие увеличения количества жирных кислот в клетках

Биосинтез ТГ и ФЛ Синтез ТГ происходит из Глицерина (Гн) и ЖК в основном стеариновой , пальмитиновой и олеиновой. Путь биосинтез ТГ в тканях протекает через образование глицерол-3 фосфата, как промежуточного соединения.

В почках, энтероцитах, где активность глицеролкиназы высокая, Глицерин фосфорилируется АТФ до глицеролфосфата. В жировой ткани и мыщцах, вследствие очень низкой активности глицеролкиназы, образование глицеро-3 -фосфата, в основном связано с гликолизом

Известно, что при гликолизе образуется ДАФ (диоксиацетонфосфат), который в присутствии глицеролфосфат-ДГ способен превращаться в Г-3 ф (глицерол-3 фосфат). В печени наблюдаются оба пути образования Г-3 -ф. В тех случаях, когда содержание Глюкозы в ЖК понижено ( при голодании), образуется лишь незначительное количество Г-3 -ф.
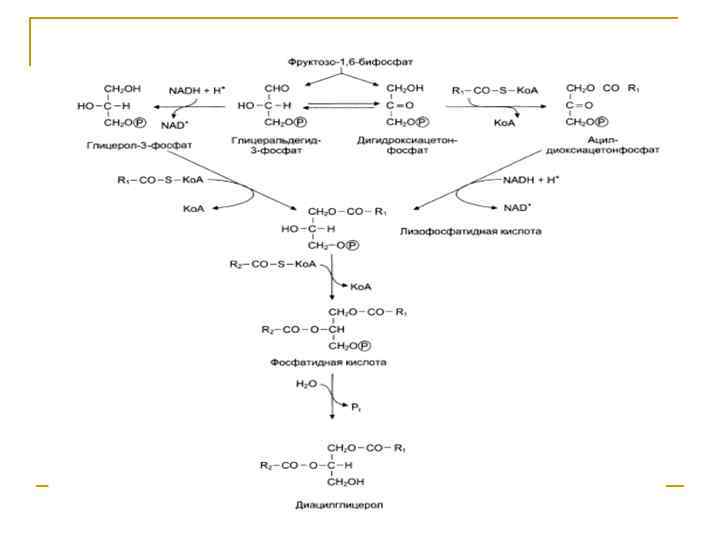

Поэтому, ввиду этого обстоятельства, освободившиеся в результате липолиза, ЖК не могут быть использованы для ресинтеза. Они покидают Жировую ткань, и количество резервного жира снижается.


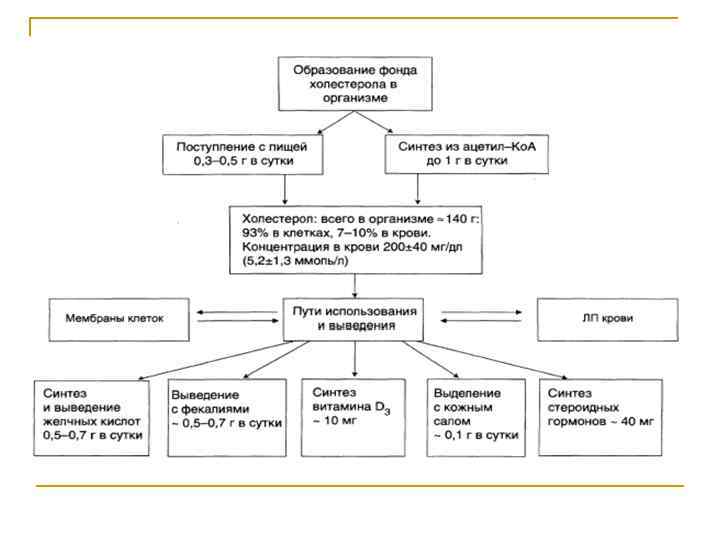
Биосинтез ХС ХС синтезируется гепатоцитами( 80%), энтероцитами (10%) , клетками почек (5%), и кожей. В сутки образуется 0. 3 -1 г ХС (эндогенный пул).

- - - Функции ХС: Непременный участник клеточных мембран Предшественник стероидных гормонов Предшественник желчных кислот и витамина Д

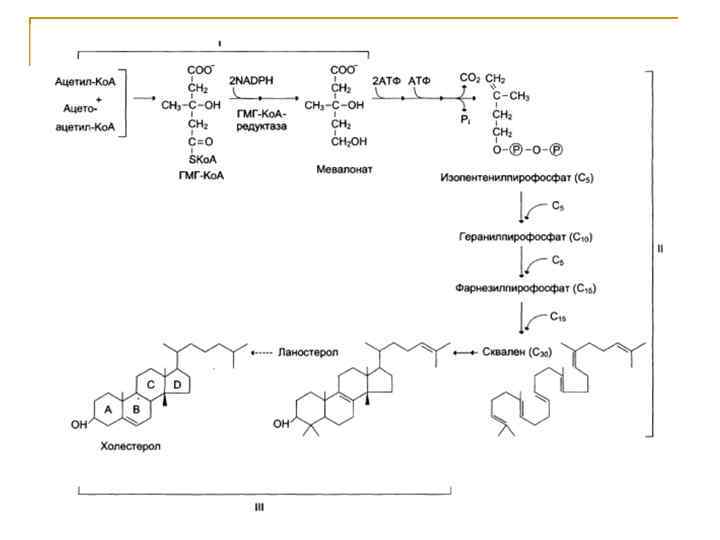
1. 2. 3. Ежесуточно человек потребляет от 2 -3 г ХС. Процесс биосинтеза ХС включает в себя более 35 энзиматических реакций. В них выделяют 3 стадии: Превращение ацетил-Ко. А в мевалоновую кислоту Образование сквалена из мевалоновой кислоты Превращение сквалена в ХС
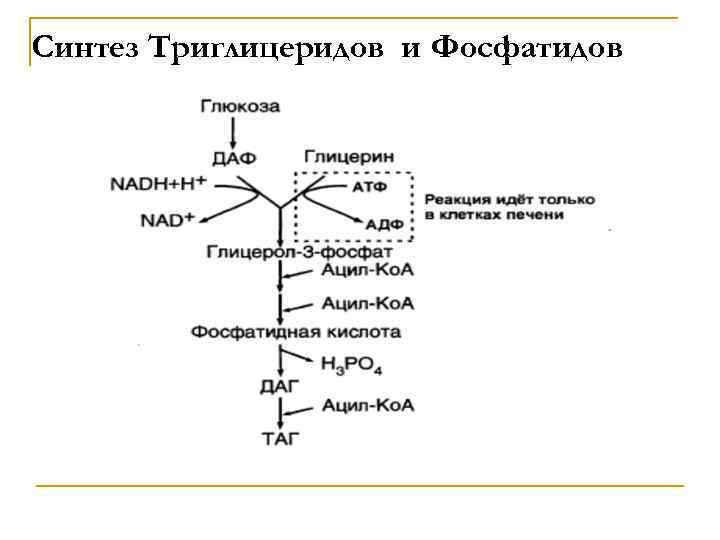
Синтез Триглицеридов и Фосфатидов
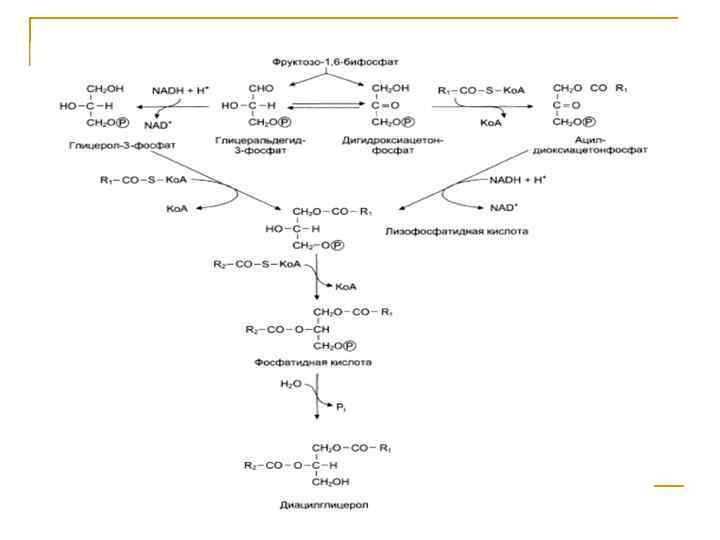
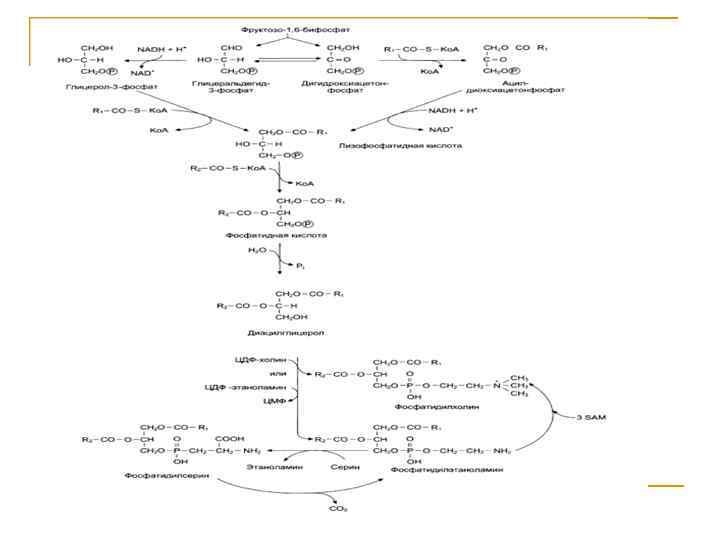

Биосинтез жирных кислот Биосинтез ЖК будет протекать при высоком уровне глюкозы в крови, что связано с интенсивностью гликолиза (поставщика ацетил- SКо. А), ПФП (поставщика NADFH 2 и СО 2).

Но в этих условиях в митохондриях печени имеются запасы СН 3 -СО-SКо. А(продукта ßокисления ЖК). Однако этот ацетил- SКо. А не вступает в реакции синтеза ЖК, т. к. он должен лимитироваться продуктами ПЦ, СО 2 и NADH 2. В данном случае организму выгоднее синтезировать ХС, который требует только лишь NADFH 2 и ацетил-SКо. А, что и происходит при голодании и диабете
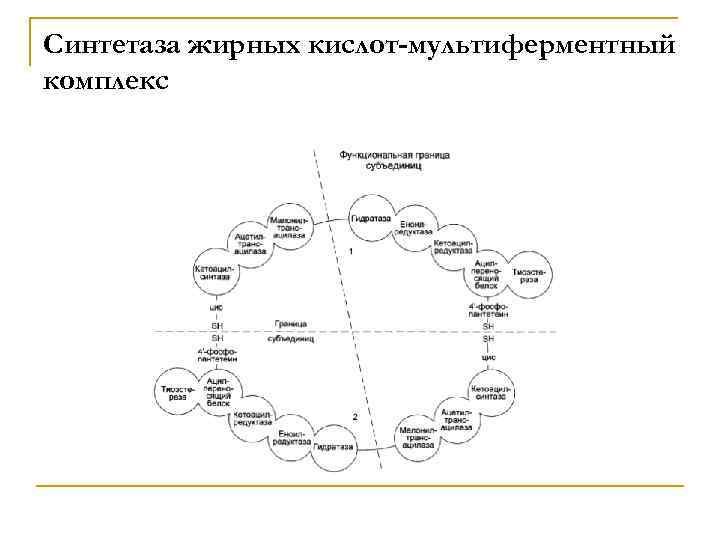
Синтетаза жирных кислот-мультиферментный комплекс
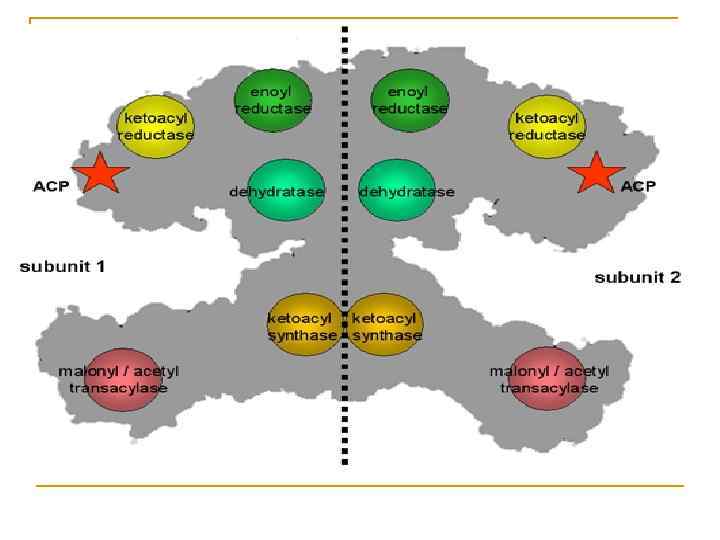
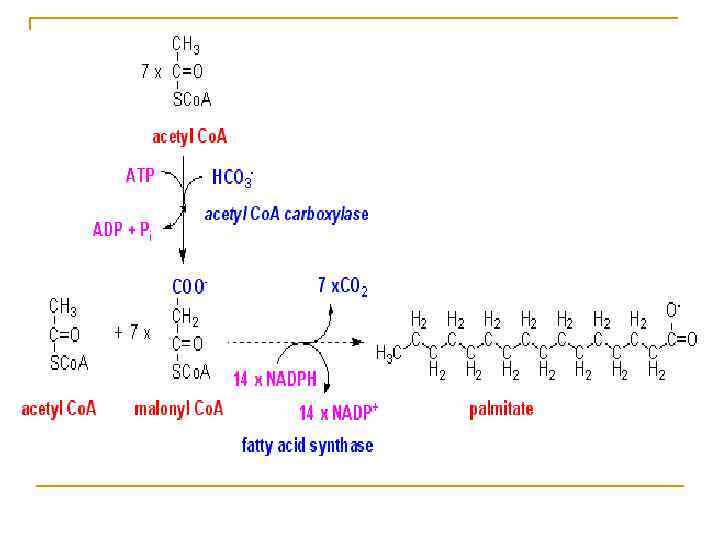
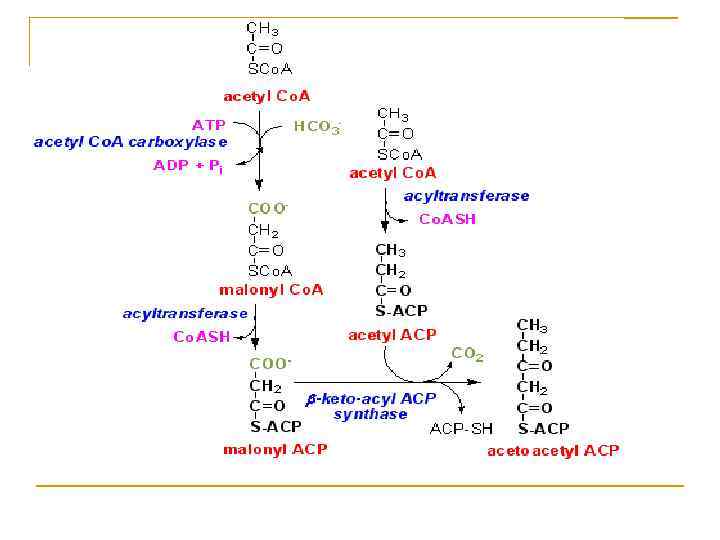
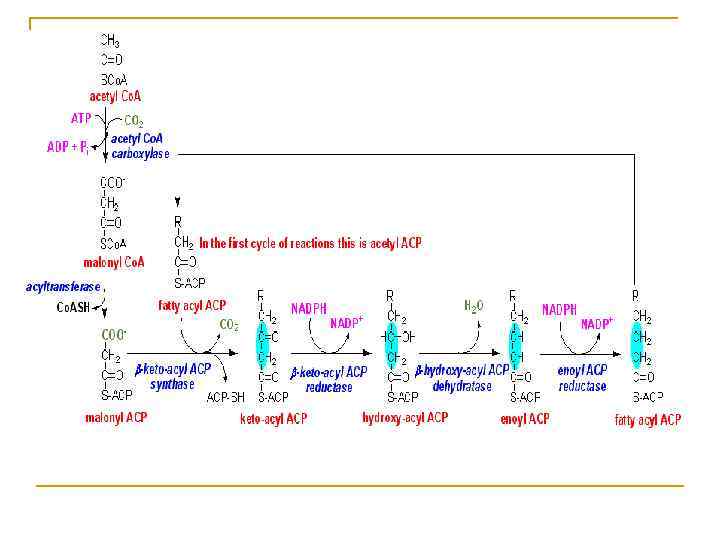
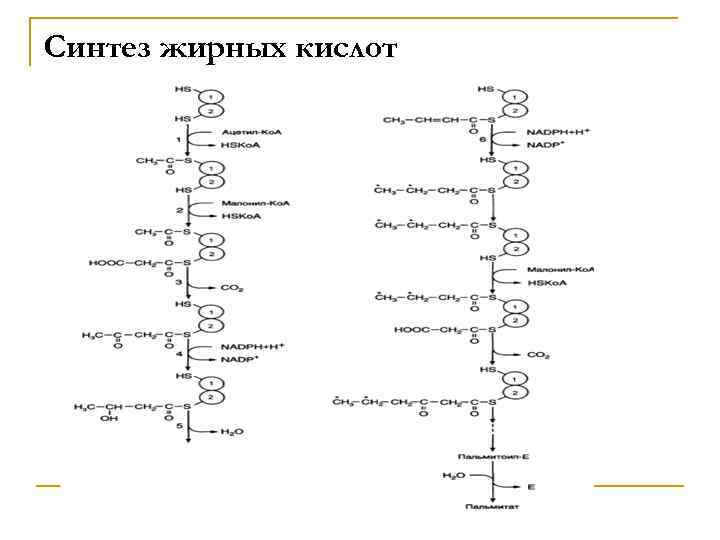
Синтез жирных кислот
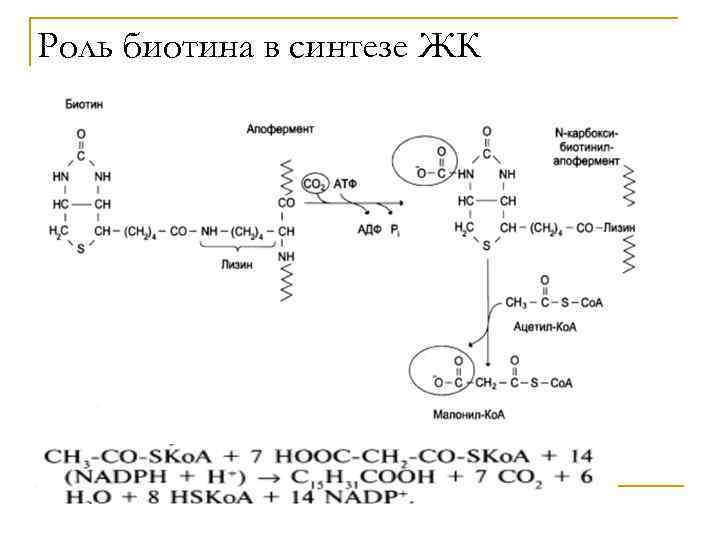
Роль биотина в синтезе ЖК
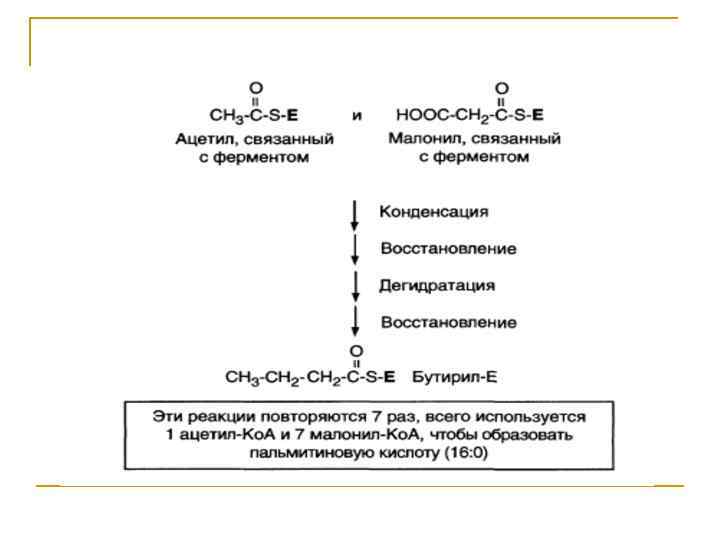
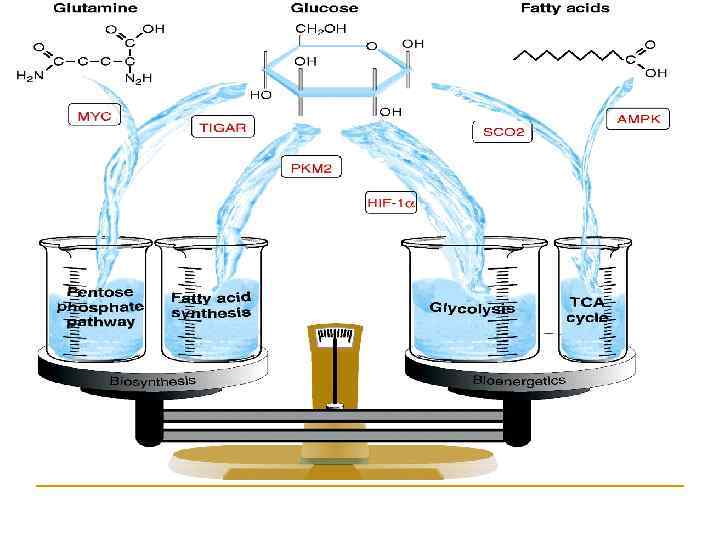

Цикл Рэндела n Конкуренция глюкозы и жирных кислот за использование в качестве субстратов: цикл Рэндэла
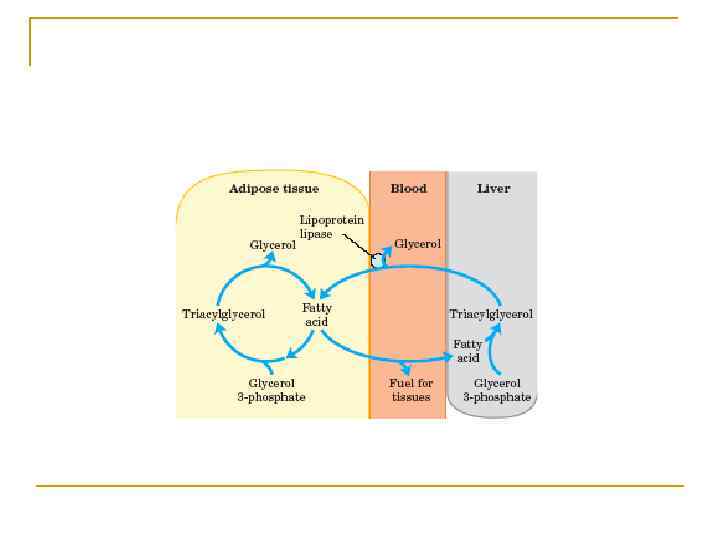

Увеличенное окисление жирных кислот ингибирует окисление глюкозы в клетках скелетных мышц и сердца за счет ингибирования пируватдегидрогеназы (соотношение ацетил~Ко. А/Ко. А-SH). При голодании такое явление призвано уменьшить утилизацию глюкозы периферическими тканями.

Однако у людей с высоким уровнем СЖК это является одной из причин устойчивости к действию инсулина (к примеру, при диабете, беременности). С другой стороны, увеличение окисления глюкозы может ингибировать окисление жирных кислот.

Это обусловлено тем, что регуляция поглощения жирных кислот митохондриями преимущественно осуществляется за счет контроля КПТI со стороны малонил-Ко. А, который выполняет роль аллостерического ингибитора этого фермента.

Липиды 3.11. 2012.ppt