лимфопролиферативные заболевания.ppt
- Количество слайдов: 69
ЛИМФОПРОЛИФЕРАТИВНЫЕ ЗАБОЛЕВАНИЯ

Введение Клетки иммунной системы могут подвергаться злокачественной трансформации, что приводит к их неконтролируемой пролиферации и развитию опухоли. Механизмы пролиферации малигнизированных клеток иммунной системы принципиально отличаются от физиологических механизмов пролиферации иммунокомпетентных клеток. В физиологических условиях пролиферация иммунокомпетентных клеток происходит в результате развития иммунного ответа и направлена на элиминацию антигенов (в том числе опухолевых).

По месту первичного возникновения лимфопролиферативные заболевания классифицируют на: ● лимфомы; ● лейкозы; ● аномалии плазматических клеток (парапротеинемии).

Лейкозы— лимфопролиферативные заболевания, первично возникающие в костном мозге. Лимфомы— опухоли, первично возникающие в кроветворной ткани, расположенной вне костного мозга (чаще в ткани лимфатических узлов). При развитии лимфомы из лимфоидной ткани печени, толстой кишки, головного мозга к термину «лимфома» добавляют указание соответствующего органа (например, лимфома головного мозга). У больных лимфомой нередко со временем происходит колонизация костного мозга опухолевыми клетками из первичного очага, для обозначения таких случаев используют термин «лимфома с лейкемизацией» .

Установлено, что развитие любого злокачественного лимфопролиферативного заболевания происходит в результате опухолевой трансформации клетки, дающей начало опухолевому процессу вследствие ее дальнейшей неконтролируемой пролиферации. Таким образом, злокачественные лимфопролиферативные заболевания имеют моноклональное происхождение, поэтому все клетки опухоли обладают идентичным генотипом и фенотипом (например, экспрессируют одинаковые типы молекул на своей поверхности). Иммунофенотипирование позволяет идентифицировать происхождение опухолевых клеток (например, миелоидное или лимфоидное) и стадию дифференцировки, на которой они подверглись опухолевой трансформации.

Методы выявления опухолевых клеток лимфоидного происхождения Морфологические — внешний вид клеток и ядра при световой или электронной микроскопии. Цитохимические — обнаружение характерных для тех или иных типов клеток ферментов (пероксидаза) или веществ (липидов, гликогена и др. ), определяемых внутриклеточно. Иммунофенотипирование — выявление молекул, экспрессируемых на клеточной поверхности для установления клеточного происхождения (миелоидного или лимфоидного). Осуществляют методом проточной цитометрии. Определение стадии дифференцировки клеток (следовательно, и степени злокачественности). Осуществляют методом проточной цитометрии. Цитогенетический — выявление характерных транслокаций или делеций в хромосомах. Молекулярно-генетический метод исследования рекомбинации генов и подтверждения моноклонального происхождения опухолей, особенно Т клеточных.

Механизмы опухолевой трансформации Большинство злокачественных новообразований развивается в результате спонтанных мутаций, приводящих к нарушению регуляции процессов пролиферации (пролиферация клеток ускоряется), дифференцировки и апоптоза. Существует три группы канцерогенов — факторов, способных вызвать повреждение генетического аппарата клетки и инициировать развитие злокачественного новообразования: ● канцерогены химического происхождения (нитрит натрия, поливинилпирролилон и др. ); ● физические канцерогены (ионизирующее излучение, ультрафиолетовое излучение); ● биологические канцерогены (онкогенные вирусы).

Вирус Эпстайна Барр вызывает развитие лимфомы Бёркитта; ретровирус Т клеточного лейкоза I типа вызывает одноимённое заболевание. несмотря на высокую степень инфицирования данными вирусами, распространённость лимфопролиферативных заболеваний составляет менее 1%. Это свидетельствует о том, что для развития злокачественных новообразований помимо канцерогена необходимы ко факторы. В роли ко факторов могут выступать факторы окружающей среды или генетические поломки, обуславливающие несостоятельность системы репарации ДНК после её повреждения канцерогенами.

Важную роль в развитии злокачественных новообразований (в том числе, лимфопролиферативных) играют клеточные протоонкогены, регулирующие деление, созревание и пролиферацию клеток. Именно клеточные протоонкогены, активированные онкогенами (в результате точечной мутации, транслокации генетического материала или дерепрессии ингибитора протоонкогенов), инициируют неконтролируемое деление клеток, которое приводит к развитию опухоли. Гены онкосупрессоры подавляют пролиферацию клеток, обеспечивают репарацию ДНК или, в случае ее невозможности, запускают программу апоптоза. Примером генов онкосупрессоров, играющих роль в развитии злокачественных лимфолролиферативных заболеваний, являются гены семейства Bc. L. Важную роль в поддержании баланса между уровнем пролиферации и апоптоза В лимфоцитов играет соотношение между проапоптотическими и антиапоптотическими белками данного семейства. Например, контроль над уровнем пролиферации В клеток в фолликулах лимфатических узлов осуществляется благодаря экспрессии белка Bсl 6. Гиперэкспрессия белка Bсl 2 приводит к устойчивости В лимфоцитов к апоптозу и наблюдается у 80% лиц с фолликулярными лимфомами.

Механизмы опухолевой трансформации в результате транслокации генетического материала (ДНК) Активация протоонкогена — при транслокации ДНК в участок промотора гена, регулирующего пролиферацию клетки. Инактивация генов, участвующих в регуляции апоптоза — при транслокации ДНК в участок гена или его промотора, регулирующих процессы апоптоза. Активация генов, кодирующих клеточный цикл — при транслокации ДНК в участки, пограничные с промоторами генов клеточного деления. Инактивация генов, участвующих в репарации ДНК при транслокации ДНК в участки, пограничные с промоторами генов, регулирующих репарацию ДНК. Нарушение функционирования генов, кодирующих дифференцировку клеток— при транслокации ДНК в участки, пограничные с промоторами генов или самими генами, регулирующими созревание клеток. Рекомбинация генетического материала клеточного и вирусного происхождения — активация клеточного деления и пролиферации. Молчащие протоонкогены (С онкогены): ▪ играют роль в процессах внутриклеточной передачи активационного сигнала; ▪ могут быть активированы в результате мутагенеза. Утрата специализированной функций — при инактивации генов онкосупрессоров
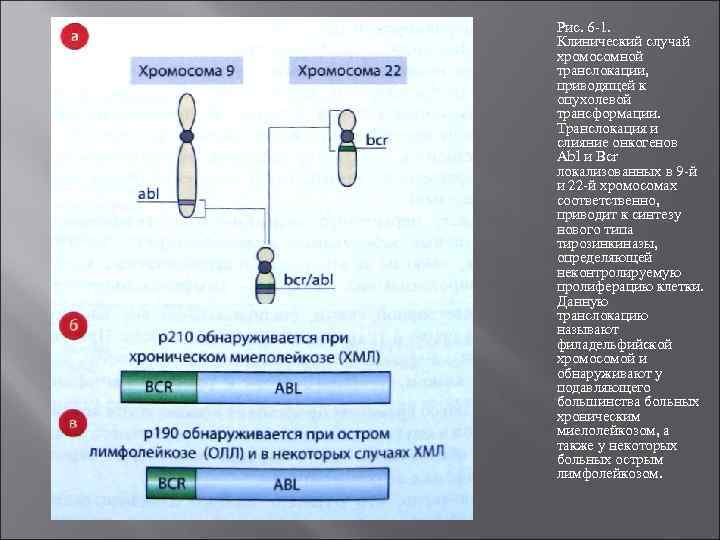
Рис. 6 1. Клинический случай хромосомной транслокации, приводящей к опухолевой трансформации. Транслокация и слияние онкогенов Аbl и Всr локализованных в 9 й и 22 й хромосомах соответственно, приводит к синтезу нового типа тирозинкиназы, определяющей неконтролируемую пролиферацию клетки. Данную транслокацию называют филадельфийской хромосомой и обнаруживают у подавляющего большинства больных хроническим миелолейкозом, а также у некоторых больных острым лимфолейкозом.

Лейкозы Лейкоз (лейкемия) —опухолевое заболевание костного мозга, характеризующееся патологическим разрастанием кроветворной ткани и развитием очагов кроветворения не только в органах кроветворения, но и в любых тканях мезенхимального происхождения. Все лейкозы подразделяют на острые и хронические. В основе такой классификации лежит морфологическая характеристика опухолевых клеток, составляющих субстрат лейкоза. К острым лейкозам относят опухолевые заболевания системы крови, основным субстратом которых являются бластные клетки. Основным субстратом хронических лейкозов являются промежуточные и зрелые формы клеток (палочкоядерные гранулоциты, промиелоциты, метамиелоциты и миелоциты при хроническом миелолейкозе, лимфоциты при хроническом лимфолейкозе и др. ).

Острый лимфолейкоз Острые лейкозы подразделяют на миелобластный, лимфобластный, монобластный, миеломонобластный, промиелоцитарный, недифференцированный и другие. В основе этой классификации лежат фенотипические особенности бластных клеток— цитохимические характеристики (внутриклеточные структуры и ферменты, характерные для данного типа бластных клеток), уровень экспрессии типичных для этого типа бластных клеток молекул.
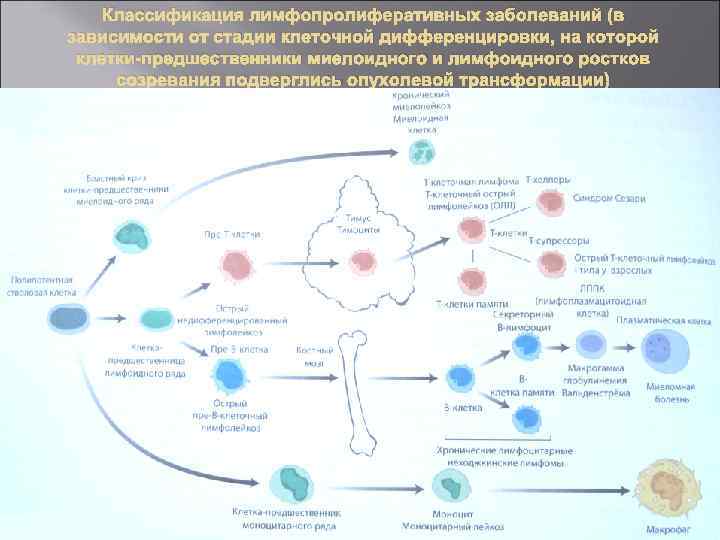
Классификация лимфопролиферативных заболеваний (в зависимости от стадии клеточной дифференцировки, на которой клетки-предшественники миелоидного и лимфоидного ростков созревания подверглись опухолевой трансформации)
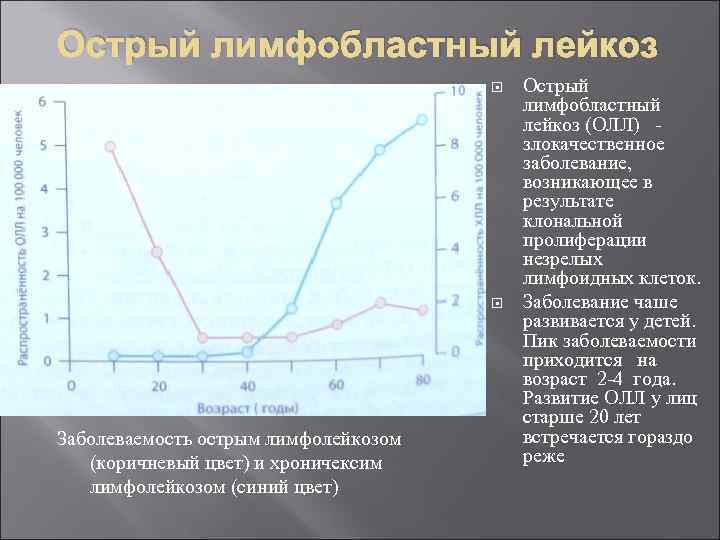
Острый лимфобластный лейкоз Заболеваемость острым лимфолейкозом (коричневый цвет) и хроничексим лимфолейкозом (синий цвет) Острый лимфобластный лейкоз (ОЛЛ) злокачественное заболевание, возникающее в результате клональной пролиферации незрелых лимфоидных клеток. Заболевание чаше развивается у детей. Пик заболеваемости приходится на возраст 2 4 года. Развитие ОЛЛ у лиц старше 20 лет встречается гораздо реже

Клиническая картина ОЛЛ интоксикационный синдром (поднимается температура тела, появляются жалобы на слабость, недомогание, быструю утомляемость, снижение аппетита); анемический синдром (бледность кожных покровов; уровень гемоглобина у лиц с ОЛЛ обычно не превышает 80 г/л); костно суставной синдром (Артралгия, боли в нижних конечностях и по ходу позвоночника, болез ненность при перкуссии трубчатых костей связаны с остеопорозом и поднадкостничной пролиферацией опухолевых клеток); геморрагический синдром (развивается примерно в 50% случаев и проявляется петехиями и экхимозами на коже, кровоточивостью дёсен, внутренними кровотечениями) Характерны увеличение лимфатических узлов, гепатомегалия и спленомегалия.

Диагностика ОЛЛ Диагностика ОЛЛ основана на обнаружении лимфобластов в периферической крови. Окончательный диагноз ОЛЛ ставят на основании данных миелограммы — обнаружение в пунктате костного мозга более 30% лимфобластов позволяет поставить диагноз ОЛЛ Проведение иммунофенотипирования злокачественных клеток является одним из ключевых методов диагностики острых лейкозов, в том числе ОЛЛ, и позволяет определить как степень дифференцировки, так и происхождение малигнизированных клеток. ● Например, о Т клеточном происхождении малигнизированных клеток свидетельствует экспрессия на их поверхност молекул CD 3 и CD 7. ● О В клеточном происхождении лимфобластов свидетельствует экспрессия на их поверхности молекул CD 10 и CD 79 a. ● На поверхности трансформированных клеток миелоидного и моноцитарного ряда обнаруживают молекулы CD 13 и CD 117. Несмотря на то, что в 80 90% случаев острые лейкозы различают по совокупности морфологичес ких и цитохимических характеристик бластных клеток, эти заболевания можно дифференцировать с помощью иммунофенотипирования с точностью 98%.
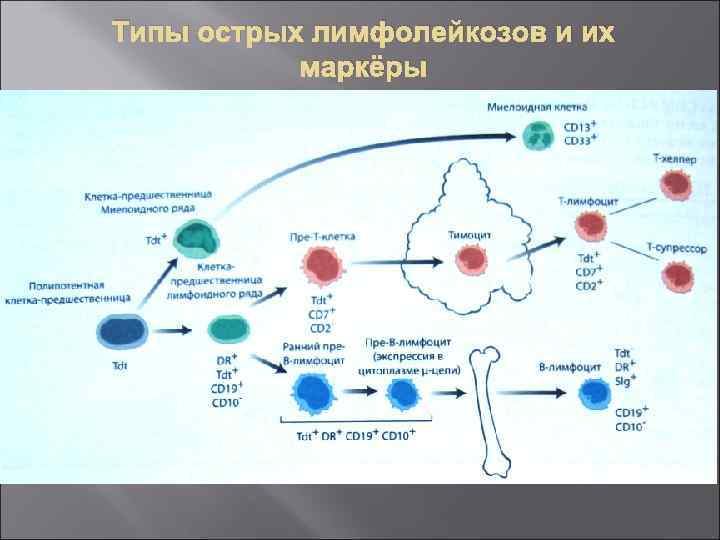
Типы острых лимфолейкозов и их маркёры
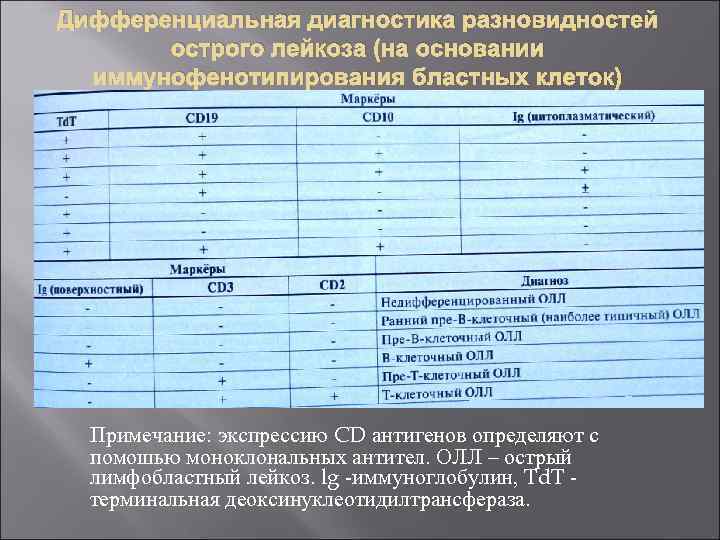
Дифференциальная диагностика разновидностей острого лейкоза (на основании иммунофенотипирования бластных клеток) Примечание: экспрессию CD антигенов определяют с помошью моноклональных антител. ОЛЛ – острый лимфобластный лейкоз. lg иммуноглобулин, Тd. Т терминальная деоксинуклеотидилтрансфераза.
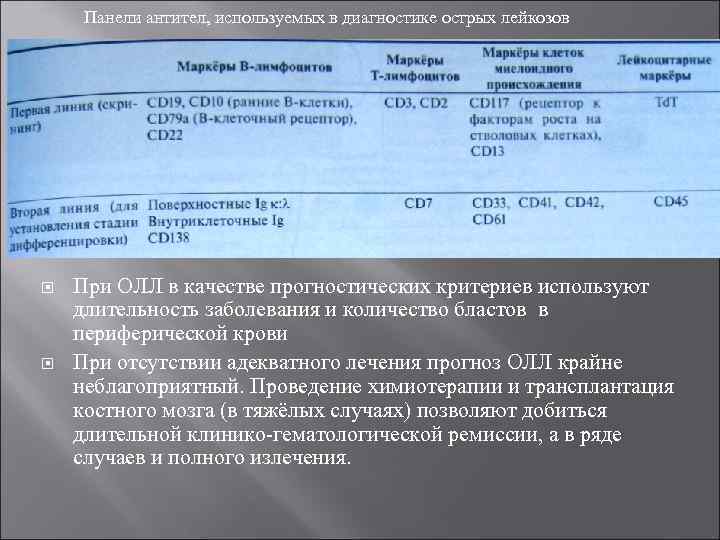
Панели антител, используемых в диагностике острых лейкозов При ОЛЛ в качестве прогностических критериев используют длительность заболевания и количество бластов в периферической крови При отсутствии адекватного лечения прогноз ОЛЛ крайне неблагоприятный. Проведение химиотерапии и трансплантация костного мозга (в тяжёлых случаях) позволяют добиться длительной клинико гематологической ремиссии, а в ряде случаев и полного излечения.

Осложнения острого лимфолейкоза (как результат прогрессировали заболевания или побочных эффектов химиотерапии по поводу проведённой трансплантации костного мозга) Результат побочных эффектов лечения Ранние осложнения Результат опухолевой прогрессии Анемия – подавление кроветворения и гиперспленизм Инфекции – нейтропения вследствие подавления кроветворения Геморрагии – тромбоцитопения вследствие подавления кроветворения Инфекции – нейтропения как результат цитотоксического действия высокодозной химиотерапии Геморрагии – тромбоцитопения как результат цитотоксического действия высокодозной химиотерапии Поздние осложнения Экстрамедуллярные очаги кроветворения Фиброз легких, опухоли щитовидной железы как результат лучевой терапии Сердечная нелостаточность вследствие кардиотоксического эффекта химиопрепаратов

Принципы терапии ОЛЛ Важным принципом терапии ОЛЛ является профилактика развития осложнений. Например, инфузии эритроцитарной и тромбоцитарной масс позволяют предотвратить развитие анемического и геморрагического синдромов. Профилактика инфекционных осложнений ОЛЛ заключается в проведении профилактических курсов антимикотической и антибактериальной терапии с использованием препаратов широкого спектра действия. Принципы терапии острого лимфобластного лейкоза: ● Достижение ремиссии заболевания. ● Элиминация опухолевых клеток и их предшественников. ● Заместительная терапия (аутологичная транс плантация костного мозга, предварительно «очищенного» от опухолевых клеток). ● Предотвращение метастазирования опухоли в менингиальные оболочки и другие ткани.

Хронический лимфолейкоз (ХЛЛ) — опухолевое заболевание лимфоидной ткани с первичной локализацией патологического процесса в костном мозге, субстратом которого являются промежуточные и зрелые формы лимфоцитов. Заболевание встречается преимущественно у лиц пожилого возраста и характеризуется относительно доброкачественным течением, поэтому диагноз часто ставят впервые при случайном исследовании крови.
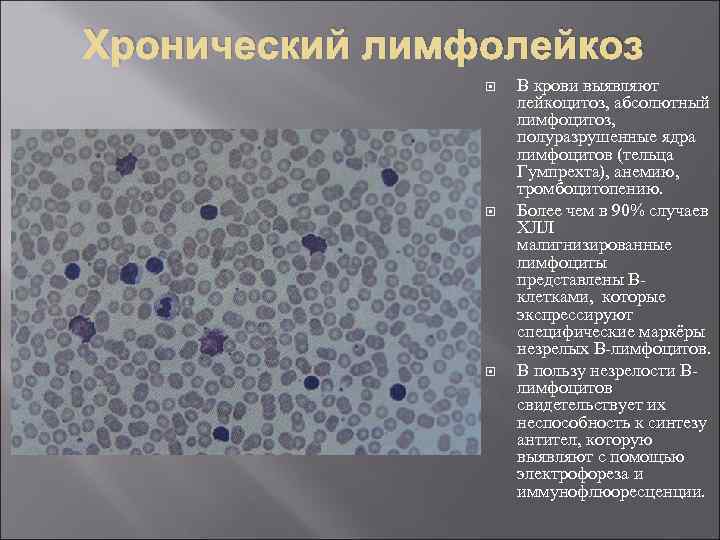
Хронический лимфолейкоз В крови выявляют лейкоцитоз, абсолютный лимфоцитоз, полуразрушенные ядра лимфоцитов (тельца Гумпрехта), анемию, тромбоцитопению. Более чем в 90% случаев ХЛЛ малигнизированные лимфоциты представлены В клетками, которые экспрессируют специфические маркёры незрелых В лимфоцитов. В пользу незрелости В лимфоцитов свидетельствует их неспособность к синтезу антител, которую выявляют с помощью электрофореза и иммунофлюоресценции.
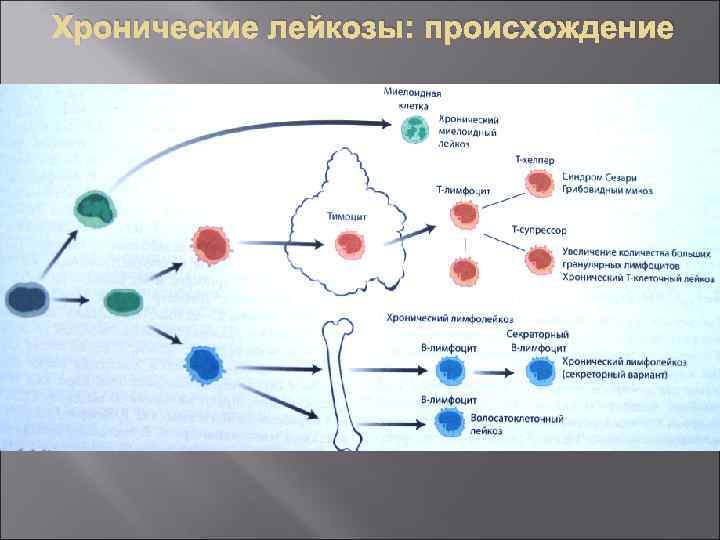
Хронические лейкозы: происхождение
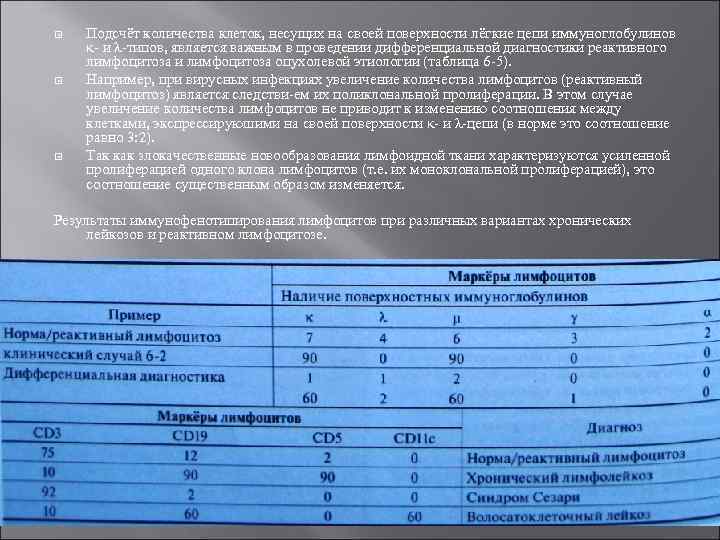
Подсчёт количества клеток, несущих на своей поверхности лёгкие цепи иммуноглобулинов κ и λ типов, является важным в проведении дифференциальной диагностики реактивного лимфоцитоза и лимфоцитоза опухолевой этиологии (таблица 6 5). Например, при вирусных инфекциях увеличение количества лимфоцитов (реактивный лимфоцитоз) является следстви ем их поликлональной пролиферации. В этом случае увеличение количества лимфоцитов не приводит к изменению соотношения между клетками, экспрессируюшими на своей поверхности κ и λ цепи (в норме это соотношение равно 3: 2). Так как злокачественные новообразования лимфоидной ткани характеризуются усиленной пролиферацией одного клона лимфоцитов (т. е. их моноклональной пролиферацией), это соотношение существенным образом изменяется. Результаты иммунофенотипирования лимфоцитов при различных вариантах хронических лейкозов и реактивном лимфоцитозе.

Терапия ХЛЛ Прогноз заболевания вариабелен и зависит от многих факторов. Например, более доброкачественно ХЛЛ протекает у людей старшего возраста. Лечение больных ХЛЛ в основном симптоматическое. При развитии спленомегалии, анемии, тромбоцитопении и нейтропении показано проведение терапии стероидами и умеренными дозами цитостатиков. У некоторых больных ХЛЛ развиваются тяжёлые рецидивирующие бактериальные инфекции, причиной которых является неполноценность гуморального звена иммунной системы. В этих случаях показано проведение заместительной терапии препаратами иммуноглобулинов. Следует отметить, что проведение иммуносупрессивной терапии также способствует повышению восприимчивости больных ХЛЛ к инфекциям. В этом случае преобладают инфекции, обусловленные недостаточностью функционирования Т клеточного звена иммунной системы (инфекции, вызываемые внутриклеточными патогенами). К ним относят, в первую очередь, инфекции, вызываемые вирусами Herpes simplex и Varicella zoster. При неуклонном прогрессировании заболевания для предотвращения развития иммунодефицита применяют ингибиторы аденозиндезаминазы (флударабин) и моноклональные анти СD 20 антитела (ритуксимаб).

Дифференциальная диагностика хронических лимфолейкозов Синдром Сезари пример злокачественного новообразования Т клеточного происхождения. Часто сопровождается поражением кожных покровов. В коже обнаруживают инфильтраты больших мононуклеарных клеток, являющихся специфическим признаком данного заболевания. Результаты иммунофенотипирования трансформированных лимфоцитов периферической крови свидетельствуют о том, что они образуются в результате oпyxoлевой трансформации хелперной популяции CD 4+ лимфоцитов. Частой причиной летального исхода для большинства пациентов с синдромом Сезари является развитие лимфом.

Т-клеточная лейкемия I типа у взрослых другой пример заболевания, возникающего в результате клональной пролиферации Т лимфоцитов. причина инфицирование человека одноимённым вирусом имеет чёткий эндемичный характер и встречается в подавляющем числе случаев в Японии и зоне Карибского бассейна. характерны поражение кожных покровов и неврологическая симптоматика.

Волосатоклеточный лейкоз — редкое заболевание, встречающееся преимущественно у лиц среднего возраста. Характерным признаком заболевания является панцитопения. У большинства пациентов выявляют спленомегалию. В мазке периферической крови присутствуют атипичные лимфоциты. «Волосатые» клетки — В клетки на поздней стадии дифференцировки, которые экспрессируют молекулы интегринов (например, CDllc). Иммуногистохимический и цитохимический методы исследования являются ключевыми в диагностике волосатоклеточного лейкоза. Применение ИФН γ позволяет достичь длительной (более 5 лет) ремиссии у большинства пациентов. Пациентам с выраженной панцитопенией показана спленэктомия.

Маркёры, используемые в дифференциальной диагностике хронических лейкозов.

Лимфомы Лимфома — опухоль, первично развивающаяся из лимфоидной ткани, расположенной вне костного мозга. В отличие от лейкозов, при лимфомах злокачествен ные клетки не циркулируют, а занимают исключительно стационарное положение. Различают два типа лимфом: • болезнь Ходжкина (лимфогранулематоз, лимфома Ходжкина, лимфоматоз хронический злокачественный, болезнь Пальтауфа Штернберга, ретикулёз фибромиелоидныи) и • неходжкинские лимфомы.

Клинические симптомы лимфом: проливной пот, особенно в ночные часы; повышенная утомляемость; снижение массы тела; лимфоаденопатия (болезненность и увеличение лимфатических узлов); немотивированный кожный зуд; присоединение оппортунистических инфекций (например, инфекции, вызванные Herpes simplex или Varicella zoster).
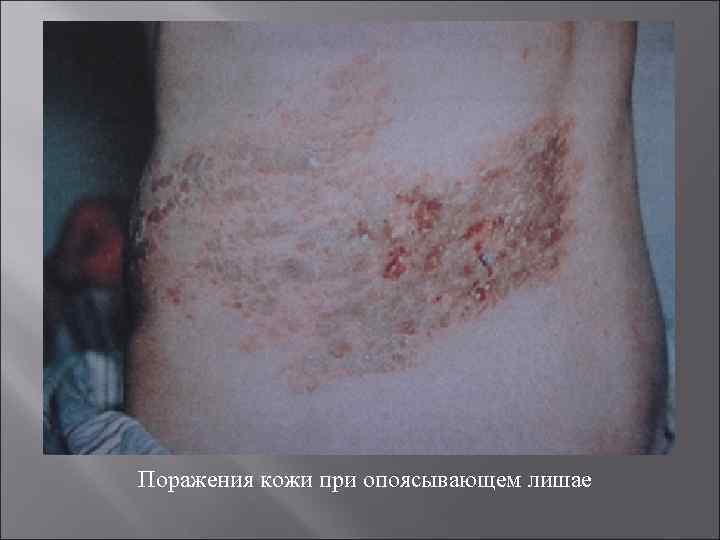
Поражения кожи при опоясывающем лишае
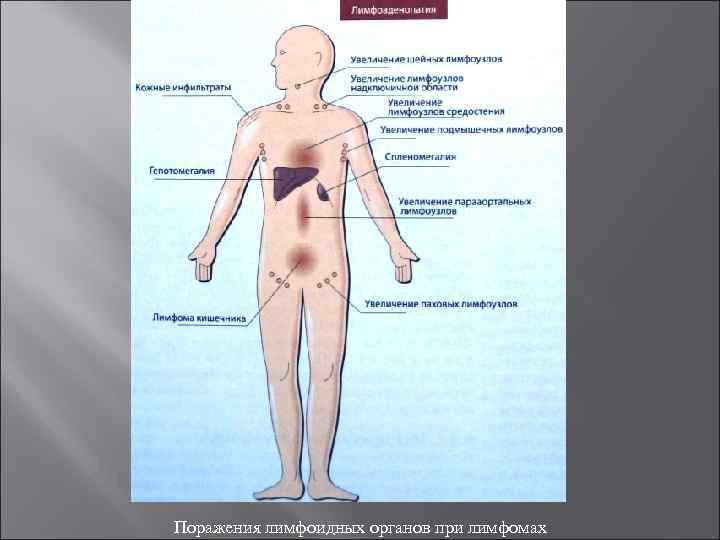
Поражения лимфоидных органов при лимфомах

Болезнь Ходжкина Диагноз лимфогранулематоза устанавливают на основании клинической картины и результатов инструментального и лабораторного исследований Большое значение в диагностике лимфогранулематоза имеет рентгенологическое исследование органов грудной клетки, при котором необходимо обращать внимание на лимфатические узлы средостения. Диагноз лимфогранулематоза требует обязательного морфологического подтверждения (цитологического, а затем и гистологического).

Болезнь Ходжкина Морфологическим субстратом является полиморфноклеточная гранулёма, состоящая из лимфоидных элементов, гистиоцитов, нейтрофилов, эозинофилов, плазматических клеток, фибробластов. Типичной гистологической находкой являются гигантские клетки Березовского Штернберга и их предшественники клетки Ходжкина. Диаметр клеток Березовского Штернберга равен 25 80 мкм, они содержат несколько ядер с нежным равномерно расположенным хроматином. Ядрышко крупное, чёткое, в большинстве случаев эозинофильное. Клетки Ходжкина имеют аналогичное строение, но содержат одно ядро. Оба типа клеток экспрессируют мембранную молекулу СD 30 и ряд маркёров, свойственных как В лимфоцитам, так и клеткам миелоидного ряда. В настояшее время считают, что клетки Березовского Штернберга и клетки Ходжкина — малигнизированные варианты АПК.

Р. Льюкс (R. J. Lukes) выделил 4 гистологических типа лимфогранулематоза: лимфогистиоцитарный тип; нодулярный склероз, ; смешанноклеточный тип; лимфоидное истощение. Гистологические типы лимфогранулематоза одновременно являются морфологическими стадиями заболевания.

Лимфогистиоцитарный тип характеризуется пролиферацией зрелых лимфоцитов и гистиоцитов; склероза почти нет; клетки Березовского Штернберга немногочисленны. При нодулярном склерозе образуются правильные тяжи коллагена, разделяющие опухолевую ткань на участки округлой формы. Смешанноклеточный тип имеет пёструю клеточную картину, отличающуюся присутствием большого числа клеток Березовского Штернберга; встречаются очаги некроза. Для лимфоидного истощения характерно полное отсутствие лимфоцитов на фоне диффузного склероза или большого числа ретикулярных клеток и клеток Березовского Штернберга.

В зависимости от распространённости процесса выделили 4 клинические стадии болезни, в каждой из которых учитывают также отсутствие (А) или наличие (Б) общих симптомов: Для I стадии (локальной) характерно поражение лимфатических узлов одной группы (I) и (или) одного нелимфатического органа. Для II стадии (регионарной) характерно поражение лимфатических узлов двух и более групп и (или) нелимфатического органа, расположенных по одну сторону диафрагмы. Для III стадии (генерализованной) характерно пораже ние лимфатических узлов разных групп по обе стороны диафрагмы, сопровождающееся поражением одного нелимфатического органа и (или) поражение селезенки. На IV стадии (диссеминированной) происходит поражение большого количества групп лимфатических узлов и внутренних органов. Поражение печени и костного мозга всегда свидетельствует о IV стадии болезни. У большинства больных лимфогранулематозом присутствуют выраженные признаки иммуносупрессии Т клеточного звена иммунной системы, что проявляется повышенной частотой возникновения инфекционных заболеваний, вызываемых внутриклеточными бактериями, вирусами и грибами.

Лечение лимфогранулематоза Лечение лимфогранулематоза заключается в проведении лучевой или химиотерапии. Проведение лучевой терапии показано на IA или IIА стадиях заболевания. Если выявляют IБ, III или IV стадию лимфогранулематоза, то необходимо проведение полихимиотерапии. Хирургическое лечение проводят только в комплексе с другими методами. Производят спленэктомию и операции на пищеводе, желудке, трахее и других органах по специальным показаниям (например, при угрозе асфиксии, нарушении пассажа пищи по пищеводу). Проведение полихимиотерапии сопровождается угнетением кроветворения, диспепсическими явлениями, алопецией, которые исчезают после окончания лечения. Поздними осложнениями терапии являются бесплодие, другие злокачественные новообразования (так называемые вторичные опухоли), лейкозы, а также нарушение функции щитовидной железы в результате локального облучения шейной области.

Прогноз зависит от возраста больного, клинической стадии, гистологического типа заболевания, своевременности лечения и др. При остром и подостром течении болезни прогноз неблагоприятный — больные обычно погибают в сроки от I месяца до I года от нача ла заболевания. При своевременно начатом лечении у больных со стадиями IA и IIА прогноз заболевания благоприятный, а 15 летняя выживаемость составляет 70 90%. В случае генерализации процесса (группа Б), а также у лиц с III и IV стадиями заболевания применение полихимиотерапии позволяет достигнуть 5 летнюю ремиссию в 80% случаях.

Неходжкинские лимфомы Неходжкинские лимфомы — гетерогенная группа неопластических заболеваний, развивающихся из клеток иммунной системы (Т или В лимфоцитов, реже гистиоцитов) с первичной локализацией патологического процесса вне костного мозга. Распространенность неходжкинских лимфом составляет 4 5% от общего количества злокачественных новообразований. Клинические проявления неходжкинских лимфом аналогичны таковым при болезни Ходжкина — потеря массы тела, лихорадка, проливной пот, особенно в ночные часы, и лимфоаденопатия. Вследствие подавления ростков кроветворения в костном мозге у данной группы больных появляются анемия и тромбоцмтопения. Присутствуют признаки лимфоидной инфильтрации других органов— печени, селезёнки, кожи, головного мозга или лёгких. Диагностические критерии стадий неходжкинских лимфом те же, что и при лимфогранулематозе.

Среди этиологических факторов рассматривают общие для всех неопластических заболеваний факторы — ионизирующее излучение, химические канцерогены, вирусы и др. Неходжкинские лимфомы часто развиваются у пациентов: получавших в течение длительного времени терапию алкилируюшими соединениями; получавших терапию циклоспорином или моноклональными анти СDЗ антителами 4 перенёсших трансплантацию органа. Снижение доз иммунодепрессантов или их отмена приводят к регрессии опухолевого процесса, что в очередной раз подтверждает ключевую роль Т лимфоцитов в осуществлении контроля над скоростью пролиферации малигнизированных клеток.

Лимфома Бёркитта развитие эндемической африканской лимфомы Бёркитта у детей в 95% случаев связано с инфицированием вирусом Эпстайна Барр. Вирус связывается с рецептором на мембране В л (гликопротеином CD 21), что приводит к поликлональной митогенной стимуляции В л. Поликлональная пролиферация лимфоцитов является первой стадией опухолевой трансформации. Эта стадия обратима. В дальнейшем происходит транслокация гена МYС, расположенного на длинном плече 8 й хромосомы в локусе 24 (8 q 24). Возможно несколько вариантов транслокации: t (8; 14), t (2: 8). t(8; 22). При этих транслокациях онкоген МYС, расположенный на 8 й хромосоме, сливается соответственно с геном тяжёлой цепи иммуноглобулинов на 14 й хромосоме, геном лёгкой κ цепи на 2 й хромосоме или геном лёгкой λ цели на 22 й хромосоме.
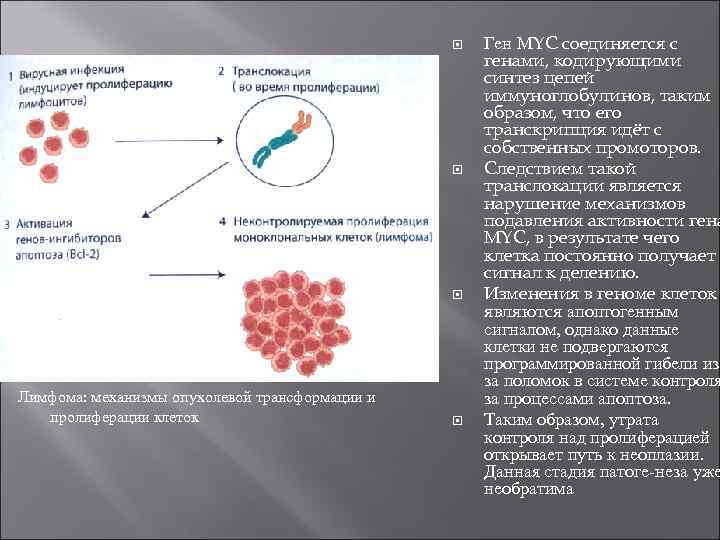
Лимфома: механизмы опухолевой трансформации и пролиферации клеток Ген МYС соединяется с генами, кодирующими синтез цепей иммуноглобулинов, таким образом, что его транскрипция идёт с собственных промоторов. Следствием такой транслокации является нарушение механизмов подавления активности гена МYС, в результате чего клетка постоянно получает сигнал к делению. Изменения в геноме клеток являются апоптогенным сигналом, однако данные клетки не подвергаются программированной гибели из за поломок в системе контроля за процессами апоптоза. Таким образом, утрата контроля над пролиферацией открывает путь к неоплазии. Данная стадия патоге неза уже необратима

Классификация неходжкинских лимфом 1. В клеточные лимфомы Неходжкинские лимфомы В клеточного происхождения. Хронический лимфобластный лейкоз и мелкоклеточные лимфомы: злокачественные новообразования, происходящие из незрелых В лимфоцитов. Фолликулярные и крупноклеточные лимфомы: источник — антигенстимулированные В клетки. 2. Т клеточная лимфома Лимфоцитарная, представлена малыми лимфоцитами Лимфоцитарная, представлена клетками с выпуклым ядром Грибовидный микоз Иммунобластная Т клеточная саркома Лимфоэпителиоидная 3. Гистиоцитарная лимфома 4. Неклассифицированная лимфома

Методы диагностики Гистологическое исследование биопсийного материала и иммунофенотипирование позволяют не только подтвердить диагноз лимфомы, но и установить степень её злокачественности, т. к. опухолевые клетки несут маркёры лимфоцитов, типичные для той стадии, на которой прекратилось созревание. молекулярно-генетический метод выявление рекомбинации генов, кодирующих синтез иммуноглобулинов, позволяет достоверно установить принадлежность опухолевых клеток к В клеткам и разграничить различные варианты В клеточных неоплазий. Рекомбинация генов, кодирующих синтез TCR, специфична для Т лимфоцитов и свидетельствует о Т клеточном происхождении лимфопролиферативных опухолей. компьютерная томография и УЗИ органов брюшной полости для оценки диссеминации процесса, эффективности проводимой терапии и прогноза лимфопролиферативных заболеваний Трепанобиопсия костного мозга (вовлечение костного мозга в патологический процесс свидетельствует о плохом прогнозе).

Осложнения неходжкинских лимфом: аутоиммунная гемолитическая анемия тромбоцитопения снижение титра сывороточных иммуноглобулинов способствует повышению восприимчивости к бактериальным инфекциям (наблюдается у 50% больных с неходжкинскими лимфомами).

Лечение Лечение лимфом основано на использовании полихимиотерапии и лучевой терапии. В последнее время в комбинации с высокодозной полихимиотерапией используют ритуксимаб (моноклональные анти СD 20 антитела). Использование комбинированной терапии подразумевает проведение профилактических мероприятий, направленных, на предотвращение развития грибковых и вирусных инфекций, являющихся следствием транзиторного иммунодефицита, развивающегося в результате применения моноклональных анти СD 20 антител. При отсутствии лейкемизации возможно проведение интенсивной химиотерапии с последующей трансплантацией аутологичного костного мозга, заготовленного до начала химиотерапии. Следует отметить, что в настоящее время возможна «очистка» костного мозга — извлечение опухолевых клеток из трансплантата. Это позволяет проводить процедуру трансплантации аутологичного костного мозга даже больным с признаками лейкемизации. Перед проведением трансплантации аутологичного костного мозга, необходимо осуществлять контроль «чистоты» препарата, основанный на определении методом полимеразной цепной реакции онкогена Bc. L 2, служащего критерием наличия малигнизированных клеток в материале. Кроме аутотрансплантации для лечения лимфом применяют аллогенную трансплантацию костного мозга. Трансплантация костного мозга позволяет существенным образом продлить жизнь пациентов с неходжкинскими лимфомами.

Аномалии плазматических клеток Множественная миелома Доброкачественная парапротеинемия (моноклональная гаммапатия неясной этиологии) Макроглобулинемия Вальденстрёма Другие аномалии плазматических клеток

Множественная миелома Множественная миелома (миеломная болезнь, генерализованная плазмоцитома, болезнь Рустицкого Калера) — системное гиперпластически опухолевое заболевание кроветворных органов, характеризующееся диффузным или узловым разрастанием плазматических клеток, продуцирующих патологические белки (парапротеины). В основе развития лежит опухолевая трансформация плазматических клеток, происходящая под влиянием избыточной продукции ИЛ 6. Результатом опухолевой трансформации плазмоцитов является гиперпродукция моноклональных антител, обнаруживаемых в повышенном количестве в сыворотке крови и моче. Наибольшая распространённость миеломной болезни приходится на лиц пожилого возраста (3 случая на 100000 населения), в то время как у лиц моложе 40 лет данное заболевание практически не встречается.
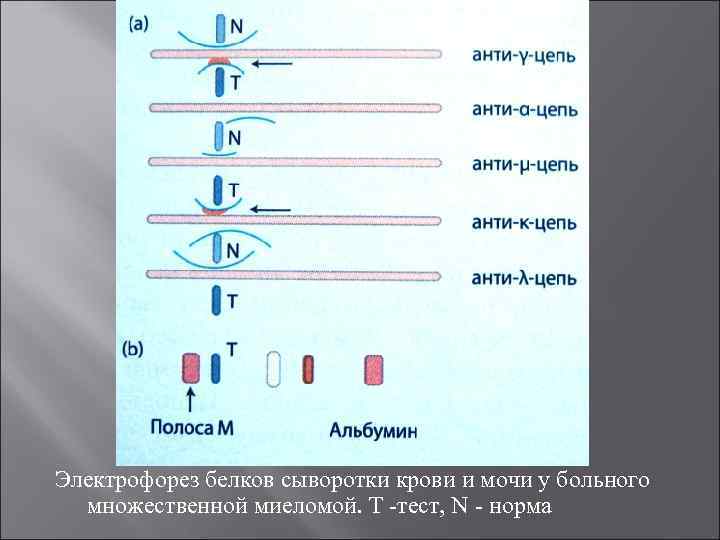
Электрофорез белков сыворотки крови и мочи у больного множественной миеломой. Т тест, N норма

Клинические проявления миеломной болезни частые бактериальные инфекции (вследствие иммуносупрессивного действия опухолевого процесса, способность к продукции антител в ответ на обычную антигенную стимуляцию снижена) почечную недостаточность (из за гиперкальциемии и действия парапротеинов на почечные канальцы) боли в костях и патологические перломы костей (из за действия факторов активации остеокластов и развития остеопороза, поскольку клетки множественной миеломы синтезируют цитокины (ИЛ 1, ИЛ 6, ФНО а, ИФН β), стимулируюшие деятельность остеокластов) анемию (из за подавления эритропоэза опухолью и гемолиза эритроцитов вследствие выработки опухолевыми клетками аутоантител) В более редких случаях миеломная болезнь может стать причиной нейропатии, дисфункции поджелудочной железы и синдрома повышенной вязкости крови
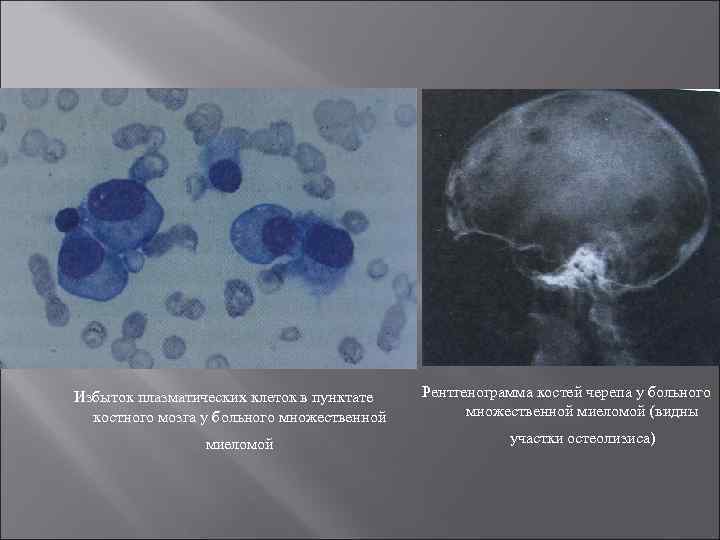
Избыток плазматических клеток в пунктате костного мозга у больного множественной миеломой Рентгенограмма костей черепа у больного множественной миеломой (видны участки остеолизиса)

Характерные признаки множественной миеломы Присутствие парапротеинов в сыворотке и моче Увеличение количества плазматических клеток в костном мозге (более 20%) и их моноклональный характер (более 12% клеток с одним типом лёгких цепей иммуноглобулина) Признаки остеолизиса Наличие как минимум 2 вышеуказанных признаков является достаточным для постановки диагноза множественной миеломы

У больных множественной миеломой плазматические клетки синтезируют избыток лёгких цепей иммуноглобулинов (по сравнению с тяжёлыми цепями), поэтому лёгкие цепи иммуноглобулинов довольно часто обнаруживают в моче. Данные белки, известные как белки Бенс Джонса, имеют малый размер и молекулярную массу около 22 к. Да. Именно это делает возможным их проникновение через базальную мембрану клубочков почек и попадание в мочу. в физиологических условиях синтез антител плазматическими клетками тоже сопровождается избыточной продукцией лёгких цепей иммуноглобулинов, которые у здоровых лиц также экскретируются почками. Однако у здоровых лиц лёгкие цепи иммуноглобулинов продуцируются всеми типами плазматических клеток, т. е. являются поликлональными, а не моноклональными, как у больных множественной миеломой. Свободные лёгкие цепи иммуноглобулинов обнаруживают в моче с помошью метода иммунофиксации или соответствующих антисывороток. У больных на стадии прогрессирования часто выявляют протеинурию, являющуюся следствием повреждения почечных канальцев. При исследовании пунктата костного мозга часто выявляют плазмоклеточную инфильтрацию костного мозга
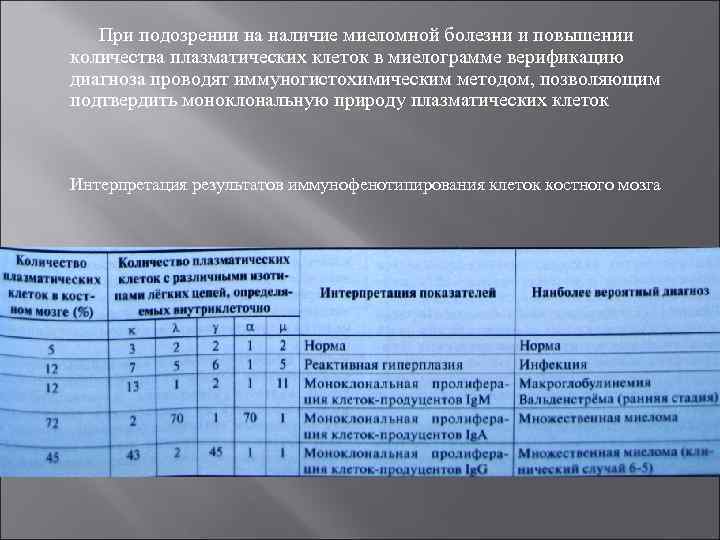
При подозрении на наличие миеломной болезни и повышении количества плазматических клеток в миелограмме верификацию диагноза проводят иммуногистохимическим методом, позволяющим подтвердить моноклональную природу плазматических клеток Интерпретация результатов иммунофенотипирования клеток костного мозга

Лечение миеломной болезни При отсутствии адекватной терапии болезнь стремительно прогрессирует и заканчивается летальным исходом в течение 1 года Для лечения миеломной болезни используют цитостатики и глюкокортикостероиды Трансплантация костного мозга (как аллотрансплантаиия, так и аутотрансплантация) также позволяет улучшить прогноз (пятилетняя выживаемость больных миеломной болезнью составляет 5 40%) На завершающей стадии клинических испытаний находятся исследования по оценке эффективности применения эритропоэтина для лечения анемии, бифосфонатов для предотвращения остеопороза и метастазирования в костный мозг, моноклональных антител к рецептору ИЛ 6. Перспективно использование цитокинов (в частности, ГМ КСФ) для стимуляции гемопоэза перед забором костномозговых клеток с последующей аутотрансплантацией костного мозга, стимуляция цитотоксического иммунного ответа по отношению к специфическим опухолевым антигенам (например, муцину 1 типа), применение ИФН а для стимуляции противоопухолевого иммунного ответа.

Доброкачественная парапротеинемия (моноклональная гаммапатия неясной этиологии) Доброкачественная парапротеинемия — состояние, сопровождающееся селективным увеличением уровня моноклональных белков в сыворотке без клинических, лабораторных или инструментальных признаков злокачественного процесса. Доброкачественные гаммапатии составляют около 25% всех парапротеинемий и в подавляющем числе случаев встречаются в пожилом и старческом возрасте.
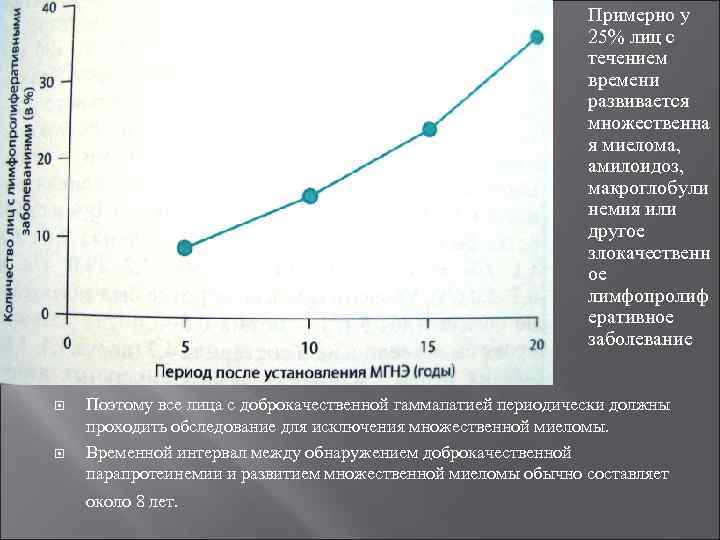
Примерно у 25% лиц с течением времени развивается множественна я миелома, амилоидоз, макроглобули немия или другое злокачественн ое лимфопролиф еративное заболевание Поэтому все лица с доброкачественной гаммапатией периодически должны проходить обследование для исключения множественной миеломы. Временной интервал между обнаружением доброкачественной парапротеинемии и развитием множественной миеломы обычно составляет около 8 лет.

Сравнительная характеристика моноклональной гаммапатии неясной этиологии (МГНЭ), солитарной и множественной миеломы

Макроглобулинемия Вальденстрёма разновидность парапротеинемий. развивающаяся преимущественно у лиц пожилого и старческого возраста на фоне уже имевшейся доброкачественной парапротеинемий. В отличие от множественной миеломы, большинство клинических симптомов данного заболевания обусловлено повышением титра сывороточного Ig. M В основе патогенеза лежит злокачественная экспансия предшественников плазматических клеток, секретируюших Ig. M.

Опухолевые клетки могут размножаться в костном мозге, печени, селезёнке и лимфатических узлах. Молекула Ig. M — пентамер, имеюший большой размер и молекулярную массу 800 к. Да. Повышение уровня Ig. M в сыворотке более 40 г/л → увеличение вязкости крови → замедление скорости кровотока и развитие стазов в мелких сосудах → нарушение микроциркуляции → разрывы сосудов микроциркуляторного русла, функциональная неполноценность тромбоцитов, окутанных макроглобулинами, и угнетение макроглобулинами коагуляционного гемостаза → повышение кровоточивости. Типичными проявлениями макроглобулинемии Вальденстрёма являются кровотечения из дёсен и слизистой носа. Очень часто развивается макромобулинемическая ретинопатия и происходят кровоизлияния в сетчатку.

Определение содержания общего белка в сыворотке крови выявляет значительное увеличение. На протеинограмме определяют гомогенный М пик, расположенный между β и γ глобулинами. Реакция Манчини выявляет увеличение Ig. M. Экскрецию лёгких цепей иммуноглобулинов, проявляющуюся их появлением в моче, выявляют лишь у небольшого числа больных.

Лечение Плазмаферез, позволяющий быс тро снизить содержание Ig. M в сыворотке и понизить вязкость крови; контроль над уровнем пролиферации малигнизированного клона предшественников плазматических клеток с помощью курсов химиотерапии. Средняя продолжительность жизни больных с макроглобулинемией Вальденстрёма составляет 4 5 лет. Проведение адекватной и своевременной терапии поз воляет увеличить продолжительность жизни до 10 лет и более. Наиболее типичные осложнения связаны с повышением вязкости крови или развитием криоглобулинемии. Развитие инфекционных осложнений при данном заболевании нетипично.

Другие аномалии плазматических клеток Злокачественные плазматические клетки способны вырабатывать моноклональные лёгкие Ig в большом количестве, поэтому частым признаком аномалий плазматических клеток является амилоидоз. Некоторые paзновидности малигнизированных плазматических клеток вырабатывают избыточное количество не лёгких, а тяжёлых цепей иммуноглобулинов. Болезни тяжёлых цепей иммуноглобулинов относят к группе парапротеинемических гемобластозов, вызванных нарушением синтеза lg и появлением в крови и моче парапротеина, представленного фрагментами тяжёлых цепей lg α , γ , или μ классов.

Болезнь а-тяжёлых цепей в большинстве случаев проявляется болями в животе, потерей массы тела, синдромом мальабсорбции, диареей. Этиологический фактор не установлен. Не исключена роль энтеропатогенов и алиментарного фактора Основным патогенетическим механизмом является развитие устойчивой воспалительной реакции в слизистой оболочке кишечника в ответ на её инфильтрацию а тяжёлыми цепями иммуноглобулинов. поэтому болезнь а тяжёлых цепей расценивают как иммунопролиферативное заболевание тонкой кишки.

Болезнь а-тяжёлых цепей В развитии данного заболевания выделяют 2 стадии: 1 ст. инфильтрация слизистой оболочки тонкой кишки а тяжёлыми цепями; 2 ст. постепенное озлокачествление процесса, сопровождающееся усилением пролиферации плазматических клеток и возможным развитием острого лимфолейкоза. Принципы лечения данного заболевания основаны на сочетании химиотерапии и антибиотикотерапии.
лимфопролиферативные заболевания.ppt