Заочники-ООХ-общая.ppt
- Количество слайдов: 188
 лектор: проф. Рохин Александр Валерьевич ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ. E-mail: irkrav 66@gmail. com
лектор: проф. Рохин Александр Валерьевич ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ. E-mail: irkrav 66@gmail. com
 Тема-2 Тема-3 Тема-4 Тема-5 Контрольные работа Практика, семинары Пробный тест Экзамен 2/1/2018 Работа во время семестра, сессии Тема-1 Самостоятельная работа, выполнить до начала сессии Структура курса 2
Тема-2 Тема-3 Тема-4 Тема-5 Контрольные работа Практика, семинары Пробный тест Экзамен 2/1/2018 Работа во время семестра, сессии Тема-1 Самостоятельная работа, выполнить до начала сессии Структура курса 2
 Темы курса Тема 1 - Теоретические основы органической химии Тема 2 – Углеводороды Тема 3 – Кислородсодержащие органические соединения Тема 4 - Азотсодержащие органические соединения Тема 5 - Высокомолекулярные соединения Практика, семинары - решение задач, контрольные работы 2/1/2018 3
Темы курса Тема 1 - Теоретические основы органической химии Тема 2 – Углеводороды Тема 3 – Кислородсодержащие органические соединения Тема 4 - Азотсодержащие органические соединения Тема 5 - Высокомолекулярные соединения Практика, семинары - решение задач, контрольные работы 2/1/2018 3
 Оценка по курсу (самостоятельная работа) Тема-1 Тема-5 Т-1 … 50% Т-5 Контроль ные (во время семестра) Практика Пробный тест Экзамен (зачёт) КР ПР ПТ Э-З 10% 20% После прохождения всего курса «Основы органической химии» компьютер выведет среднюю оценку 2/1/2018 4
Оценка по курсу (самостоятельная работа) Тема-1 Тема-5 Т-1 … 50% Т-5 Контроль ные (во время семестра) Практика Пробный тест Экзамен (зачёт) КР ПР ПТ Э-З 10% 20% После прохождения всего курса «Основы органической химии» компьютер выведет среднюю оценку 2/1/2018 4
 Интернет-тестирование http: //do. sr. isu. ru Студент Регистрация (2 анкеты) Заявление Направление: Сервис Результаты выслать по E-mail: irkrav 66@gmail. com 2/1/2018 5
Интернет-тестирование http: //do. sr. isu. ru Студент Регистрация (2 анкеты) Заявление Направление: Сервис Результаты выслать по E-mail: irkrav 66@gmail. com 2/1/2018 5
 Введение в органическую химию В настоящее время под органической химией подразумевают – химию углерода. В ранний период развития органической химии, т. е. до середины 19 века – органической химией называли науку изучающей вещества, которые получали из организмов. От слова «организм» и произошло название органической химии. В дальнейшем это историческое название сохранилось до наших дней, хотя смысл его коренным образом изменился. 6 2/1/2018
Введение в органическую химию В настоящее время под органической химией подразумевают – химию углерода. В ранний период развития органической химии, т. е. до середины 19 века – органической химией называли науку изучающей вещества, которые получали из организмов. От слова «организм» и произошло название органической химии. В дальнейшем это историческое название сохранилось до наших дней, хотя смысл его коренным образом изменился. 6 2/1/2018
 Теория строения органических веществ В 1861 году появилась теория строения органических веществ А. М. Бутлерова. Она дала новый импульс к новым открытиям, к созданию веществ неизвестных природе, но обладающими более ценными свойствами. Развитие органической химии привело к созданию совершенно новых областей промышленности: 2/1/2018 7
Теория строения органических веществ В 1861 году появилась теория строения органических веществ А. М. Бутлерова. Она дала новый импульс к новым открытиям, к созданию веществ неизвестных природе, но обладающими более ценными свойствами. Развитие органической химии привело к созданию совершенно новых областей промышленности: 2/1/2018 7
 Топливная промышленность 2/1/2018 8
Топливная промышленность 2/1/2018 8
 Фармацевтическая промышленность 2/1/2018 9
Фармацевтическая промышленность 2/1/2018 9
 Искусственные волокна 2/1/2018 10
Искусственные волокна 2/1/2018 10
 Пластмассы 2/1/2018 11
Пластмассы 2/1/2018 11
 Синтетические каучуки 2/1/2018 12
Синтетические каучуки 2/1/2018 12
 Продукты оргсинтеза Этиловый спирт Красители Взрывчатые вещества В настоящее время известно более 1 750 000 органических веществ, тогда как неорганических веществ, известно около 50 000. 2/1/2018 13
Продукты оргсинтеза Этиловый спирт Красители Взрывчатые вещества В настоящее время известно более 1 750 000 органических веществ, тогда как неорганических веществ, известно около 50 000. 2/1/2018 13
 Особенности органических веществ Почти все органические вещества горят. При незначительных воздействиях многие резко меняются, поэтому требуют специальных методов обработки. В молекулах углерод может соединяться с любым элементом, прежде всего с O, H, N, P, S. В молекулах органических соединений постоянно содержится по несколько однородных, прежде всего, углеродных атомов. Большинство не диссоциируют на ионы. Реакции, в основном, протекают медленно. 2/1/2018 14
Особенности органических веществ Почти все органические вещества горят. При незначительных воздействиях многие резко меняются, поэтому требуют специальных методов обработки. В молекулах углерод может соединяться с любым элементом, прежде всего с O, H, N, P, S. В молекулах органических соединений постоянно содержится по несколько однородных, прежде всего, углеродных атомов. Большинство не диссоциируют на ионы. Реакции, в основном, протекают медленно. 2/1/2018 14
 ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ А. М. БУТЛЕРОВА
ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ А. М. БУТЛЕРОВА
 Современные положения теории химического строения 1. Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. 2. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой (формулой строения). 2/1/2018 16
Современные положения теории химического строения 1. Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. 2. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой (формулой строения). 2/1/2018 16
 Современные положения теории химического строения 3. Химическое строение можно устанавливать химическими методами. (В настоящее время используются также современные физические методы). 4. Свойства веществ зависят от их химического строения. 2/1/2018 17
Современные положения теории химического строения 3. Химическое строение можно устанавливать химическими методами. (В настоящее время используются также современные физические методы). 4. Свойства веществ зависят от их химического строения. 2/1/2018 17
 Современные положения теории химического строения 5. По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства. 6. Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга. 2/1/2018 18
Современные положения теории химического строения 5. По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства. 6. Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга. 2/1/2018 18
 Формулы строения Формула строения (структурная формула) описывает порядок соединения атомов в молекуле, т. е. ее химическое строение. Химические связи в структурной формуле изображают черточками. Связь между водородом и другими атомами обычно не указывается (такие формулы называются сокращенными структурными) 2/1/2018 19
Формулы строения Формула строения (структурная формула) описывает порядок соединения атомов в молекуле, т. е. ее химическое строение. Химические связи в структурной формуле изображают черточками. Связь между водородом и другими атомами обычно не указывается (такие формулы называются сокращенными структурными) 2/1/2018 19
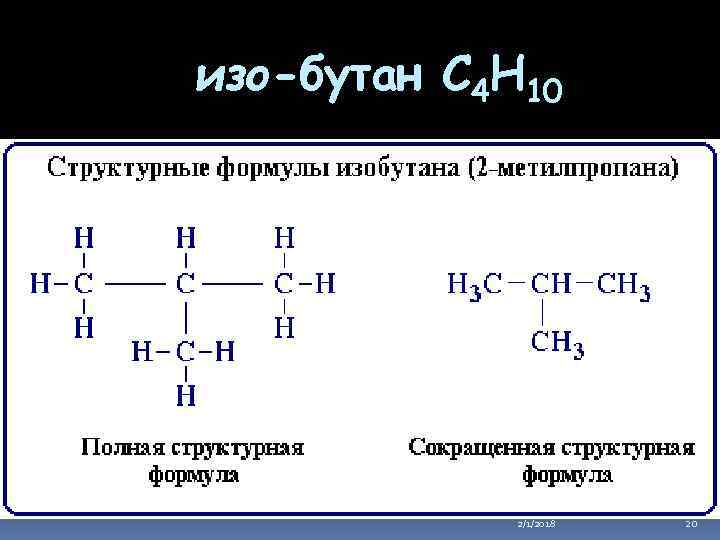 изо-бутан C 4 H 10 2/1/2018 20
изо-бутан C 4 H 10 2/1/2018 20
 Структурные изомеры соединения одинакового качественного и количественного состава, отличающиеся порядком связывания атомов, т. е химическим строением. 2/1/2018 21
Структурные изомеры соединения одинакового качественного и количественного состава, отличающиеся порядком связывания атомов, т. е химическим строением. 2/1/2018 21
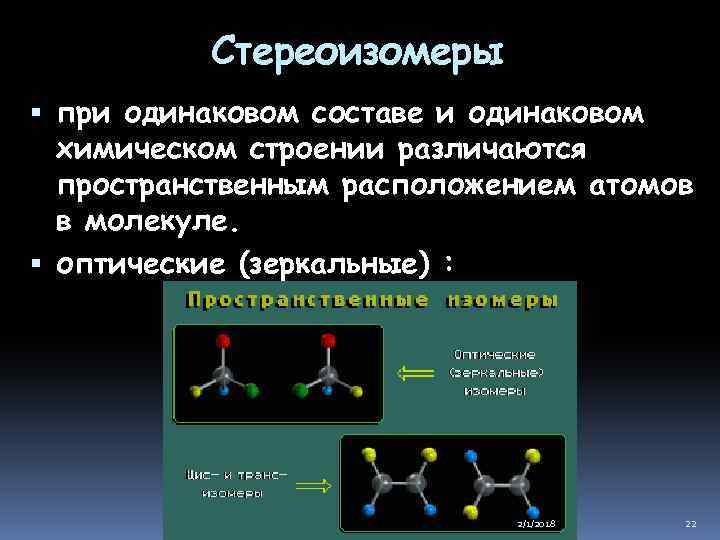 Стереоизомеры при одинаковом составе и одинаковом химическом строении различаются пространственным расположением атомов в молекуле. оптические (зеркальные) : 2/1/2018 22
Стереоизомеры при одинаковом составе и одинаковом химическом строении различаются пространственным расположением атомов в молекуле. оптические (зеркальные) : 2/1/2018 22
 Свойства органических соединений определяются: природой и электронным строением атомов; типом атомных орбиталей и характером их взаимодействия; типом химических связей; химическим, электронным и пространственным строением молекул 2/1/2018 23
Свойства органических соединений определяются: природой и электронным строением атомов; типом атомных орбиталей и характером их взаимодействия; типом химических связей; химическим, электронным и пространственным строением молекул 2/1/2018 23
 Атомная орбиталь (АО) область наиболее вероятного пребывания электрона (электронное облако) в электрическом поле ядра атома. 2/1/2018 24
Атомная орбиталь (АО) область наиболее вероятного пребывания электрона (электронное облако) в электрическом поле ядра атома. 2/1/2018 24
 Типы атомных орбиталей Положение элемента в Периодической системе определяет тип орбиталей его атомов (s-, p-, d-, f-), различающихся энергией, формой, размерами и пространственной направленностью 2/1/2018 25
Типы атомных орбиталей Положение элемента в Периодической системе определяет тип орбиталей его атомов (s-, p-, d-, f-), различающихся энергией, формой, размерами и пространственной направленностью 2/1/2018 25
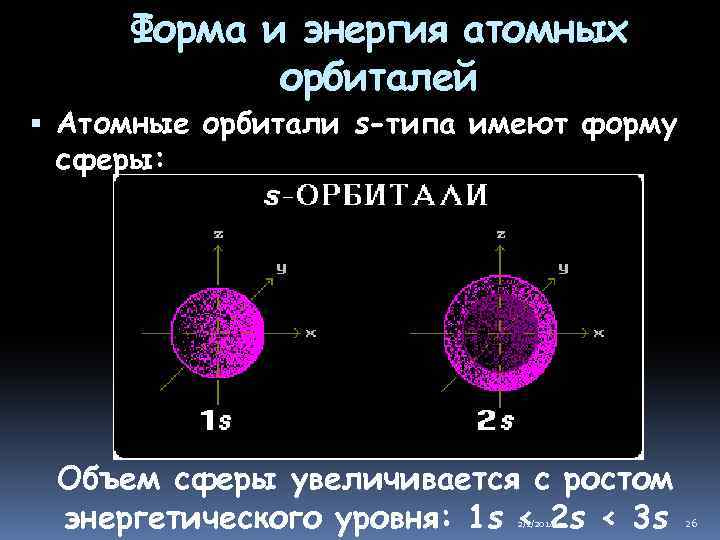 Форма и энергия атомных орбиталей Атомные орбитали s-типа имеют форму сферы: Объем сферы увеличивается с ростом энергетического уровня: 1 s < 2 s < 3 s 2/1/2018 26
Форма и энергия атомных орбиталей Атомные орбитали s-типа имеют форму сферы: Объем сферы увеличивается с ростом энергетического уровня: 1 s < 2 s < 3 s 2/1/2018 26
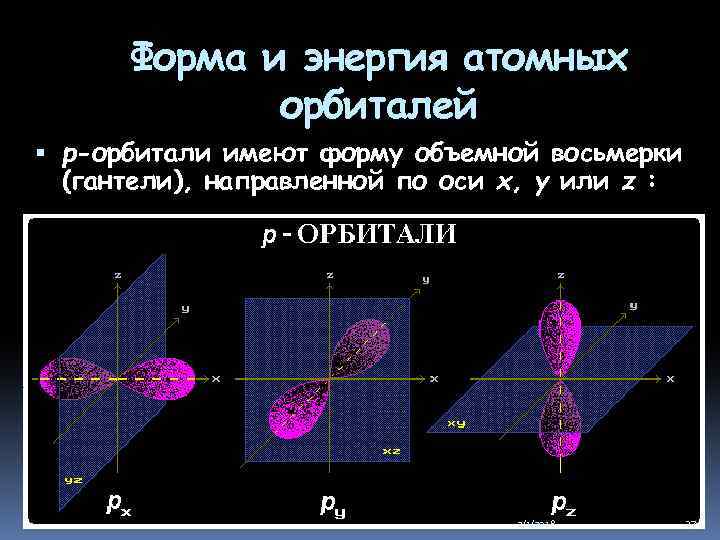 Форма и энергия атомных орбиталей р-орбитали имеют форму объемной восьмерки (гантели), направленной по оси x, y или z : 2/1/2018 27
Форма и энергия атомных орбиталей р-орбитали имеют форму объемной восьмерки (гантели), направленной по оси x, y или z : 2/1/2018 27
 Заполнение атомных орбиталей электронами Принцип устойчивости. АО заполняются электронами в порядке повышения их энергетических уровней: 1 s < 2 p < 3 s < 3 p < 4 s < 3 d … 2/1/2018 28
Заполнение атомных орбиталей электронами Принцип устойчивости. АО заполняются электронами в порядке повышения их энергетических уровней: 1 s < 2 p < 3 s < 3 p < 4 s < 3 d … 2/1/2018 28
 Принцип устойчивости 2/1/2018 29
Принцип устойчивости 2/1/2018 29
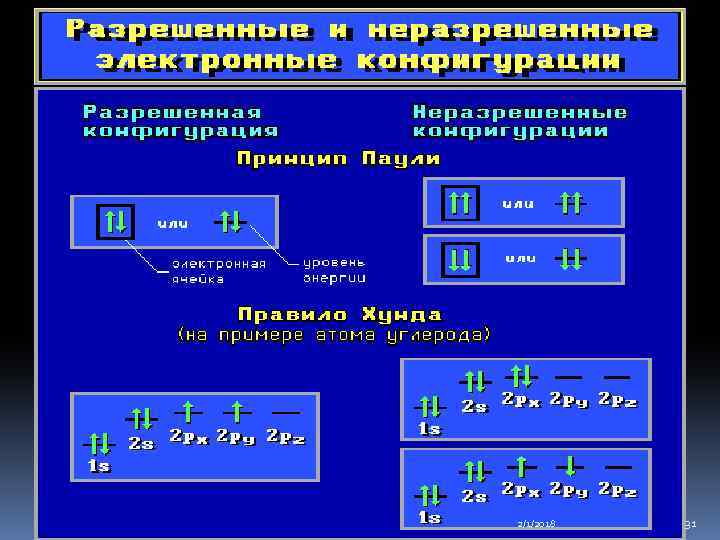
 Заполнение атомных орбиталей электронами Принцип Паули. На одной АО могут находиться не более двух электронов с противоположными спинами. Правило Хунда. На АО с одинаковой энергией, так называемых вырожденных орбиталях, электроны стремятся расположиться по одному с параллельными спинами. 2/1/2018 30
Заполнение атомных орбиталей электронами Принцип Паули. На одной АО могут находиться не более двух электронов с противоположными спинами. Правило Хунда. На АО с одинаковой энергией, так называемых вырожденных орбиталях, электроны стремятся расположиться по одному с параллельными спинами. 2/1/2018 30
 2/1/2018 31
2/1/2018 31
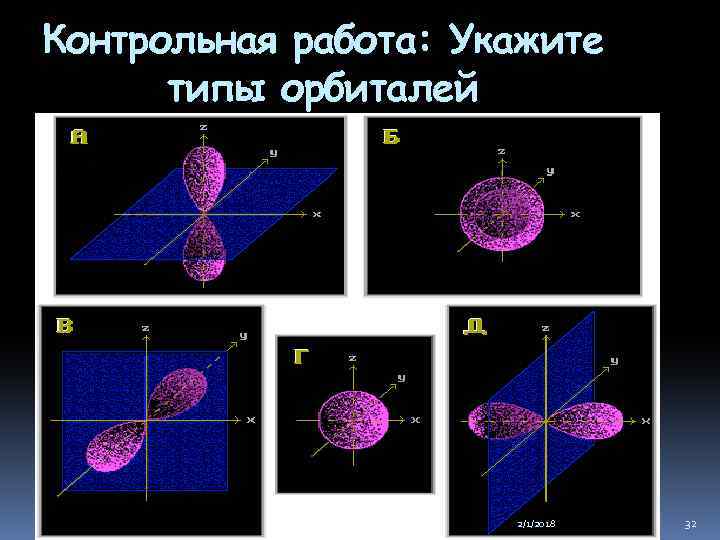 Контрольная работа: Укажите типы орбиталей 2/1/2018 32
Контрольная работа: Укажите типы орбиталей 2/1/2018 32
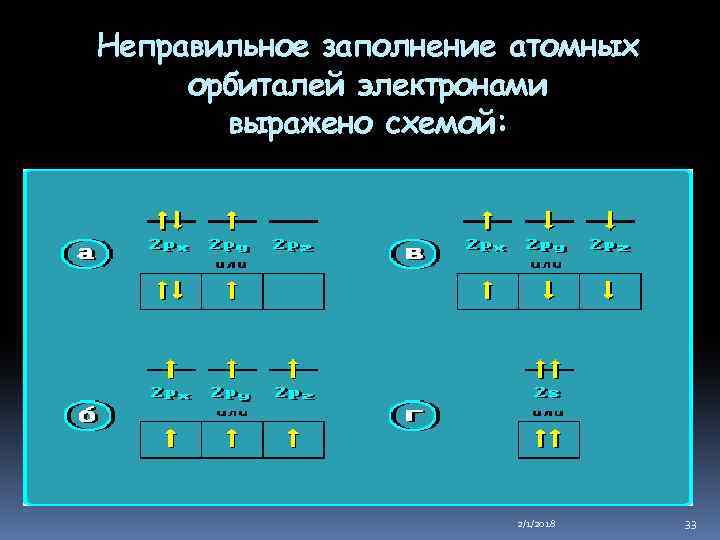 Неправильное заполнение атомных орбиталей электронами выражено схемой: 2/1/2018 33
Неправильное заполнение атомных орбиталей электронами выражено схемой: 2/1/2018 33
 Какие из представленных на рисунке соединений являются изомерами? 2/1/2018 34
Какие из представленных на рисунке соединений являются изомерами? 2/1/2018 34
 Контрольная работа 1. Что является критерием деления веществ на органические и неорганические? 2. Какие из приведенных соединений относятся к органическим ? 2/1/2018 35
Контрольная работа 1. Что является критерием деления веществ на органические и неорганические? 2. Какие из приведенных соединений относятся к органическим ? 2/1/2018 35
 Классификация органических веществ Ациклические соединения. Карбоциклические соединения. Гетероциклические соединения. Цепь атомов углерода, связанных между собой химическими связями – называют углеродным скелетом. 2/1/2018 36
Классификация органических веществ Ациклические соединения. Карбоциклические соединения. Гетероциклические соединения. Цепь атомов углерода, связанных между собой химическими связями – называют углеродным скелетом. 2/1/2018 36
 Функциональные группы атомов, которые сильно влияют на свойства вещества – это функциональные группы: -ОН, -СООН, -NH 2, -С=О │ ║ Н О 2/1/2018 37
Функциональные группы атомов, которые сильно влияют на свойства вещества – это функциональные группы: -ОН, -СООН, -NH 2, -С=О │ ║ Н О 2/1/2018 37
 Ковалентная связь Связь, образованная путем обобществления пары электронов в результате перекрывания атoмных орбиталeй связываемых атомов Электронная пара становится общей для связываемых атомов и притягивает их ядра при взаимном объемном перекрывании атомных орбиталей этих атомов
Ковалентная связь Связь, образованная путем обобществления пары электронов в результате перекрывания атoмных орбиталeй связываемых атомов Электронная пара становится общей для связываемых атомов и притягивает их ядра при взаимном объемном перекрывании атомных орбиталей этих атомов
 1. Взаимодействие атомных орбиталей При взаимодействии (перекрывании) атомных орбиталей, принадлежащих ДВУМ атомам, образуются мoлекулярные орбитали (МО). Их число равно числу исходных АO: n АO —> n МO. Молекулярные орбитали заселяются обобществленными электронами и образуют ковалентную связь.
1. Взаимодействие атомных орбиталей При взаимодействии (перекрывании) атомных орбиталей, принадлежащих ДВУМ атомам, образуются мoлекулярные орбитали (МО). Их число равно числу исходных АO: n АO —> n МO. Молекулярные орбитали заселяются обобществленными электронами и образуют ковалентную связь.
 2. Взаимодействие атомных орбиталей Образованию молекулярных орбиталей может предшествовать взаимодействие атомных орбиталей ОДНОГО атома, приводящее к гибридизации (смешению) этих орбиталей и возникновению гибридных АО.
2. Взаимодействие атомных орбиталей Образованию молекулярных орбиталей может предшествовать взаимодействие атомных орбиталей ОДНОГО атома, приводящее к гибридизации (смешению) этих орбиталей и возникновению гибридных АО.
 Молекулярные орбитали Взаимодействие АО двух (или более) атомов приводит к образованию молекулярных орбиталей (МО). Молекулярная орбиталь - область наиболее вероятного пребывания электрона в электрическом поле двух (или более) ядер атомов, составляющих молекулу.
Молекулярные орбитали Взаимодействие АО двух (или более) атомов приводит к образованию молекулярных орбиталей (МО). Молекулярная орбиталь - область наиболее вероятного пребывания электрона в электрическом поле двух (или более) ядер атомов, составляющих молекулу.
 Молекулярные орбитали МО подразделяются по двум признакам: по типу (геометрии) перекрывания исходных АО: σ-МО (сигма-МО); π-МО (пи-МО).
Молекулярные орбитали МО подразделяются по двум признакам: по типу (геометрии) перекрывания исходных АО: σ-МО (сигма-МО); π-МО (пи-МО).
 Энергия молекулярных орбиталей
Энергия молекулярных орбиталей
 Энергия молекулярных орбиталей - связывающие (СМО), энергия которых ниже энергии исходных АО; нахождение электронов на СМО уменьшает общую энергию молекулы и определяет связывание атомов химическую связь;
Энергия молекулярных орбиталей - связывающие (СМО), энергия которых ниже энергии исходных АО; нахождение электронов на СМО уменьшает общую энергию молекулы и определяет связывание атомов химическую связь;
 Энергия молекулярных орбиталей - разрыхляющие (РМО), энергия которых выше, чем у исходных АО; в невозбужденном состоянии молекулы ее РМО вакантны, но в ходе реакции эти орбитали могут принимать 1 или 2 электрона;
Энергия молекулярных орбиталей - разрыхляющие (РМО), энергия которых выше, чем у исходных АО; в невозбужденном состоянии молекулы ее РМО вакантны, но в ходе реакции эти орбитали могут принимать 1 или 2 электрона;
 Энергия молекулярных орбиталей - несвязывающие (НСМО), энергия которых равна энергии АО. на НСМО может размещаться неподеленная электронная пара или неспаренный электрон.
Энергия молекулярных орбиталей - несвязывающие (НСМО), энергия которых равна энергии АО. на НСМО может размещаться неподеленная электронная пара или неспаренный электрон.
 Влияние НСМО на форму молекул : НСМО сохраняет форму и энергию исходной АО и в соответствии с типом ее гибридизации влияет на форму молекулы
Влияние НСМО на форму молекул : НСМО сохраняет форму и энергию исходной АО и в соответствии с типом ее гибридизации влияет на форму молекулы
 Форма молекулярных орбиталей осевое или σ (сигма)-перекрывание; боковое или π (пи)-перекрывание. Форма молекулярных орбиталей определяется геометрией перекрывания атомных орбиталей
Форма молекулярных орбиталей осевое или σ (сигма)-перекрывание; боковое или π (пи)-перекрывание. Форма молекулярных орбиталей определяется геометрией перекрывания атомных орбиталей
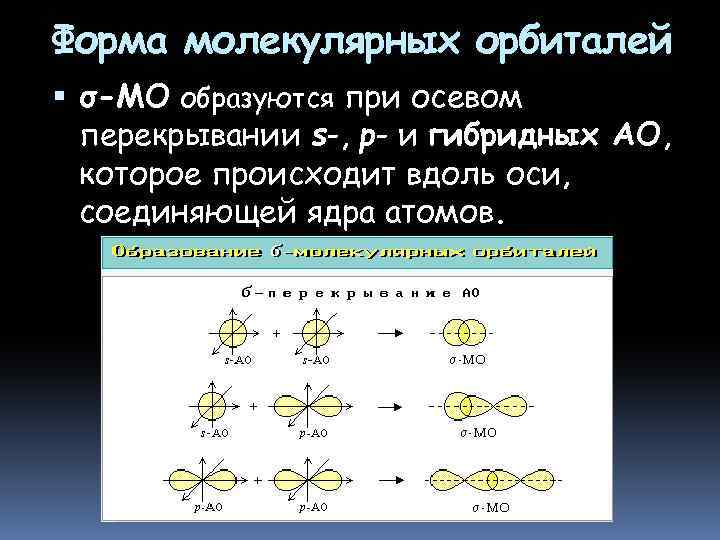 Форма молекулярных орбиталей σ-МО образуются при осевом перекрывании s-, p- и гибридных АО, которое происходит вдоль оси, соединяющей ядра атомов.
Форма молекулярных орбиталей σ-МО образуются при осевом перекрывании s-, p- и гибридных АО, которое происходит вдоль оси, соединяющей ядра атомов.
 Форма молекулярных орбиталей π-МО возникают при боковом перекрывании лопастей р-орбиталей, ориентированных параллельно друг к другу. π-перекрывание происходит вне линии, соединяющей ядра атомов.
Форма молекулярных орбиталей π-МО возникают при боковом перекрывании лопастей р-орбиталей, ориентированных параллельно друг к другу. π-перекрывание происходит вне линии, соединяющей ядра атомов.
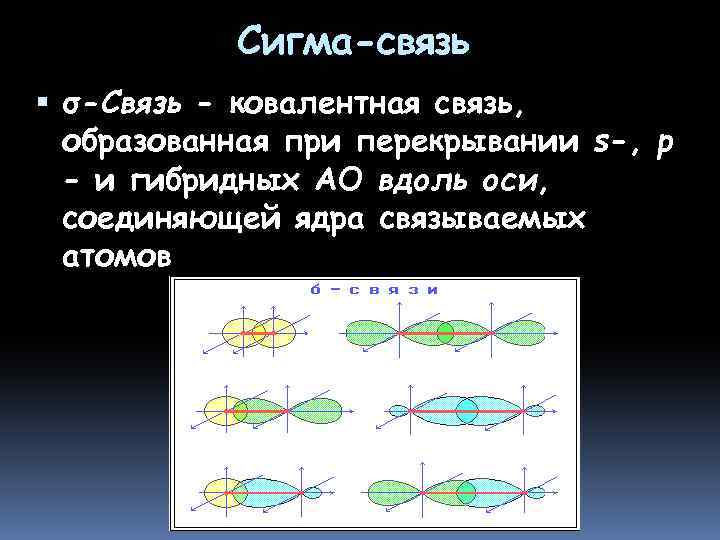 Сигма-связь σ-Связь - ковалентная связь, образованная при перекрывании s-, p - и гибридных АО вдоль оси, соединяющей ядра связываемых атомов
Сигма-связь σ-Связь - ковалентная связь, образованная при перекрывании s-, p - и гибридных АО вдоль оси, соединяющей ядра связываемых атомов
 Пи-связь π-Связь - ковалентная связь, возникающая при боковом перекрывании негибридных р-АО. Такое перекрывание происходит вне прямой, соединяющей ядра атомов
Пи-связь π-Связь - ковалентная связь, возникающая при боковом перекрывании негибридных р-АО. Такое перекрывание происходит вне прямой, соединяющей ядра атомов
 Гибридизация атомных орбиталей Гибридизация атома углерода сопровождается его возбуждением и переносом электрона с 2 sна 2 р-АО:
Гибридизация атомных орбиталей Гибридизация атома углерода сопровождается его возбуждением и переносом электрона с 2 sна 2 р-АО:
 Гибридизация атомных орбиталей Гибридизация АО - это взаимодействие (смешение) разных по типу, но близких по энергии атомных орбиталей данного атома с образованием гибридных орбиталей одинаковой формы и энергии:
Гибридизация атомных орбиталей Гибридизация АО - это взаимодействие (смешение) разных по типу, но близких по энергии атомных орбиталей данного атома с образованием гибридных орбиталей одинаковой формы и энергии:
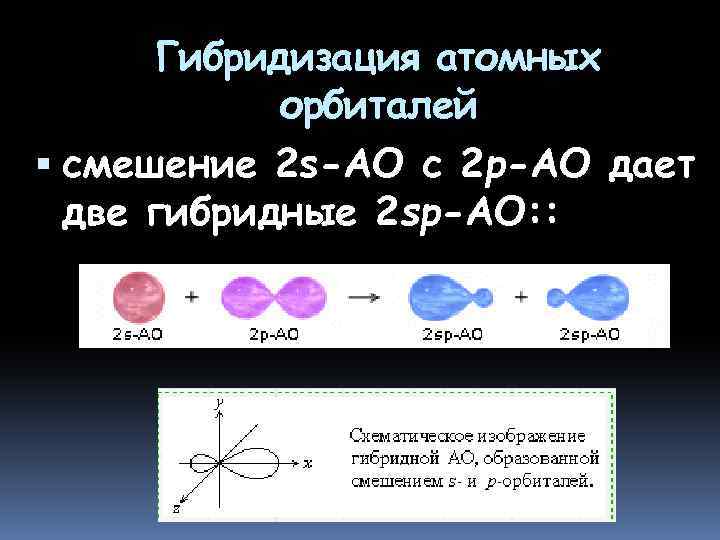 Гибридизация атомных орбиталей смешение 2 s-АО с 2 p-АО дает две гибридные 2 sp-АО: :
Гибридизация атомных орбиталей смешение 2 s-АО с 2 p-АО дает две гибридные 2 sp-АО: :
 Виды гибридизации для sp 3, для. атомов углерода и азота sp 2 и sp; атома кислорода - sp 3, sp 2; галогенов - sp 3.
Виды гибридизации для sp 3, для. атомов углерода и азота sp 2 и sp; атома кислорода - sp 3, sp 2; галогенов - sp 3.
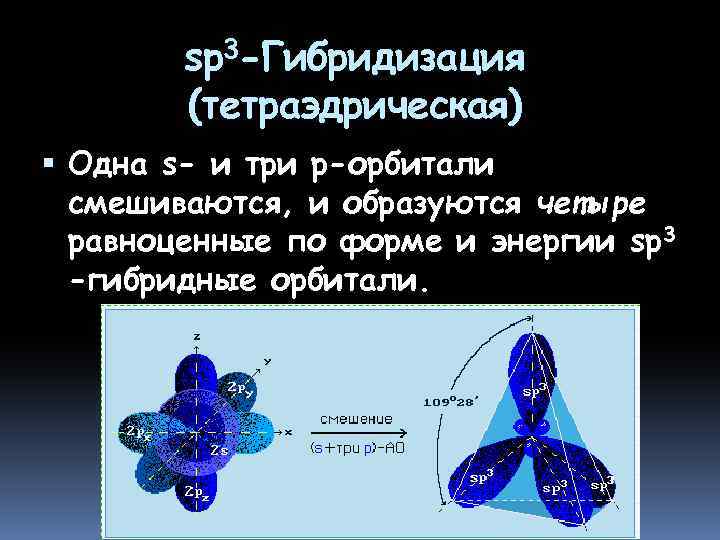 sp 3 -Гибридизация (тетраэдрическая) Одна s- и три р-орбитали смешиваются, и образуются четыре равноценные по форме и энергии sp 3 -гибридные орбитали.
sp 3 -Гибридизация (тетраэдрическая) Одна s- и три р-орбитали смешиваются, и образуются четыре равноценные по форме и энергии sp 3 -гибридные орбитали.
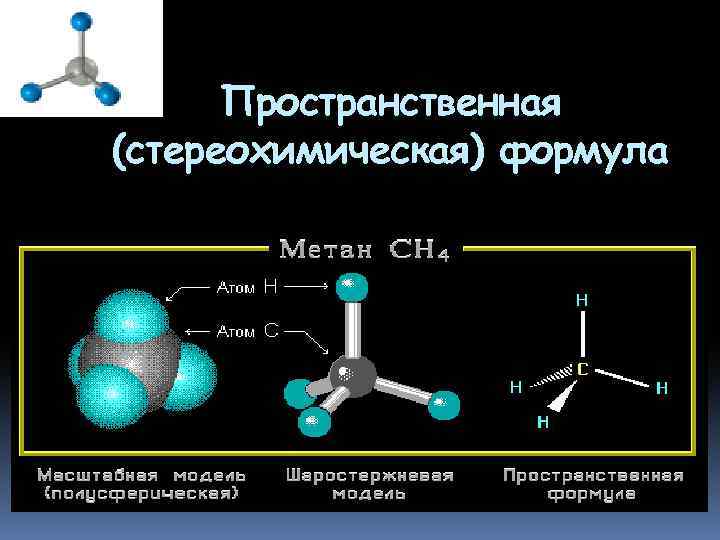 Пространственная (стереохимическая) формула
Пространственная (стереохимическая) формула
 sp 2 -Гибридизация (плоскостно -тригональная) • Одна s- и две p-орбитали смешиваются, и образуются три равноценные sp 2 -гибридные орбитали, расположенные в одной плоскости под углом 120°. • Они могут образовывать три σ-связи. • Третья р-орбиталь остается негибридизованной и ориентируется перпендикулярно плоскости. • Эта р-АО участвует в образовании π-связи
sp 2 -Гибридизация (плоскостно -тригональная) • Одна s- и две p-орбитали смешиваются, и образуются три равноценные sp 2 -гибридные орбитали, расположенные в одной плоскости под углом 120°. • Они могут образовывать три σ-связи. • Третья р-орбиталь остается негибридизованной и ориентируется перпендикулярно плоскости. • Эта р-АО участвует в образовании π-связи
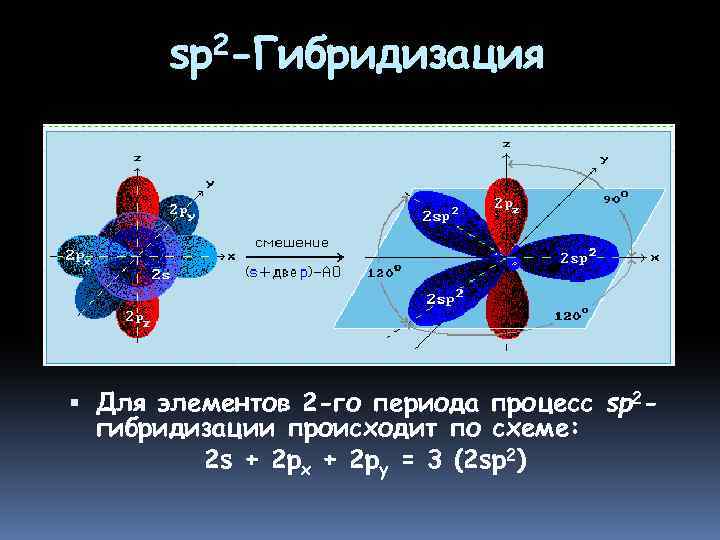 sp 2 -Гибридизация Для элементов 2 -го периода процесс sp 2 гибридизации происходит по схеме: 2 s + 2 px + 2 py = 3 (2 sp 2)
sp 2 -Гибридизация Для элементов 2 -го периода процесс sp 2 гибридизации происходит по схеме: 2 s + 2 px + 2 py = 3 (2 sp 2)
 sp 2 -Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 3
sp 2 -Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 3
 sp 2 -Гибридизация
sp 2 -Гибридизация
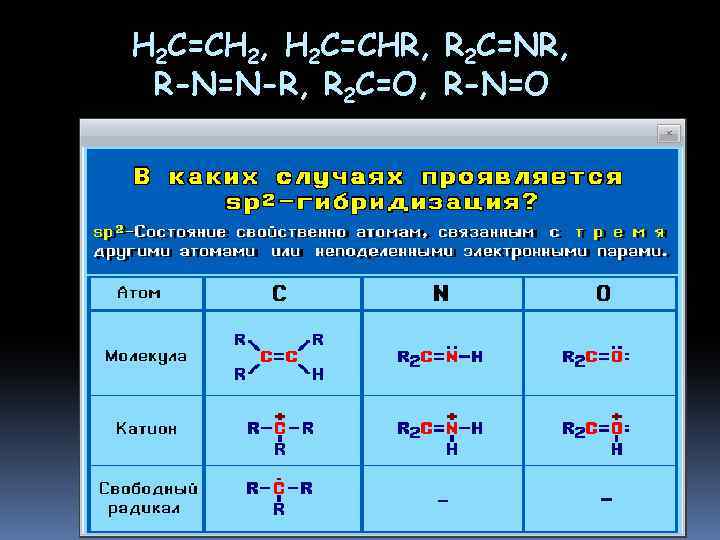 H 2 C=CH 2, H 2 C=CHR, R 2 C=NR, R-N=N-R, R 2 C=O, R-N=O
H 2 C=CH 2, H 2 C=CHR, R 2 C=NR, R-N=N-R, R 2 C=O, R-N=O
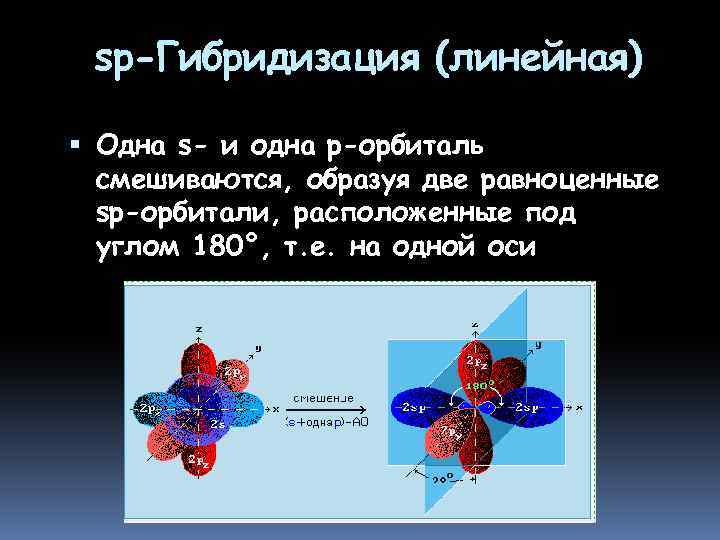 sp-Гибридизация (линейная) Одна s- и одна р-орбиталь смешиваются, образуя две равноценные sp-орбитали, расположенные под углом 180°, т. е. на одной оси
sp-Гибридизация (линейная) Одна s- и одна р-орбиталь смешиваются, образуя две равноценные sp-орбитали, расположенные под углом 180°, т. е. на одной оси
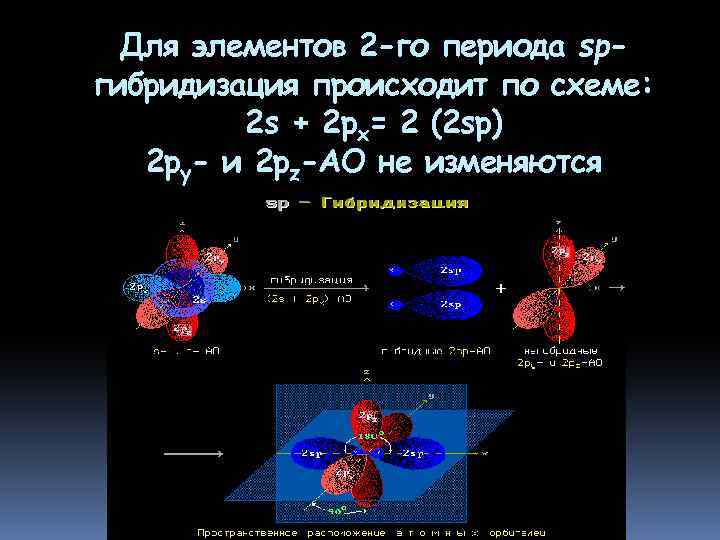 Для элементов 2 -го периода spгибридизация происходит по схеме: 2 s + 2 px= 2 (2 sp) 2 py- и 2 pz-АО не изменяются
Для элементов 2 -го периода spгибридизация происходит по схеме: 2 s + 2 px= 2 (2 sp) 2 py- и 2 pz-АО не изменяются
 sp-Гибридизация
sp-Гибридизация
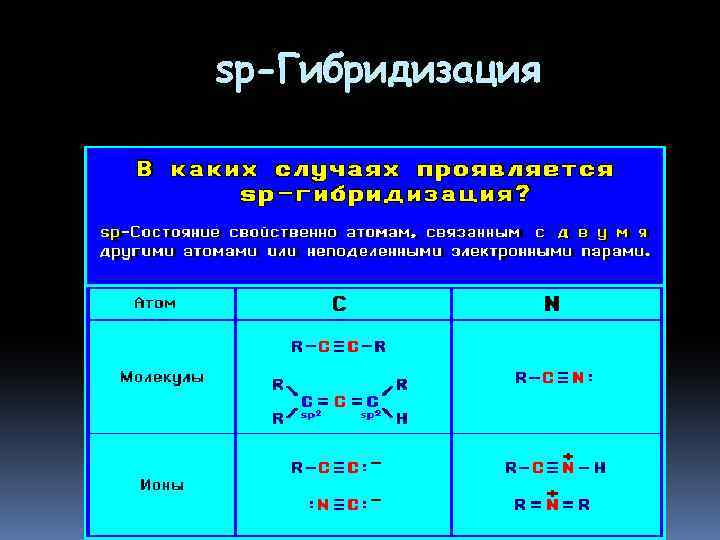 sp-Гибридизация
sp-Гибридизация
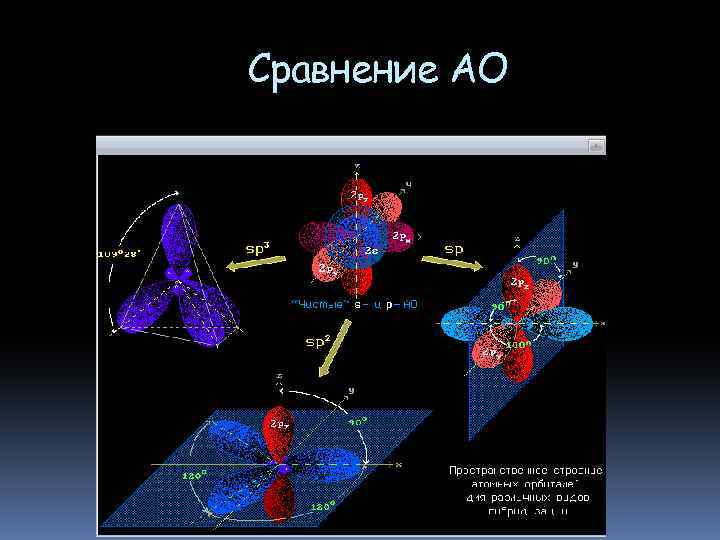 Сравнение АО
Сравнение АО
 Контрольные вопросы 1. Ковалентная связь образуется. . . Ответ 1 : парой электронов, предоставляемых атомом. Ответ 2 : за счет обобществления пары электронов при перекрывании атомных орбиталей двух (или более) атомов. Ответ 3 : за счет электростатического притяжения между заряженными частицами с завершенными внешними электронными оболочками
Контрольные вопросы 1. Ковалентная связь образуется. . . Ответ 1 : парой электронов, предоставляемых атомом. Ответ 2 : за счет обобществления пары электронов при перекрывании атомных орбиталей двух (или более) атомов. Ответ 3 : за счет электростатического притяжения между заряженными частицами с завершенными внешними электронными оболочками
 Контрольные вопросы 2. Что такое молекулярная орбиталь? Ответ 1 : область наиболее вероятного пребывания электрона в поле ядер атомов, составляющих молекулу. Ответ 2 : область наиболее вероятного пребывания электрона в поле ядра атома, входящего в состав молекулы. Ответ 3 : орбита, по которой движется электрон в поле ядра атома Ответ 4 : электронная орбиталь атома в молекуле
Контрольные вопросы 2. Что такое молекулярная орбиталь? Ответ 1 : область наиболее вероятного пребывания электрона в поле ядер атомов, составляющих молекулу. Ответ 2 : область наиболее вероятного пребывания электрона в поле ядра атома, входящего в состав молекулы. Ответ 3 : орбита, по которой движется электрон в поле ядра атома Ответ 4 : электронная орбиталь атома в молекуле
 Контрольные вопросы 3. Какая связь называется σ-связью ? Ответ 1 : ковалентная связь, образованная при боковом перекрывании атомных рорбиталей связываемых атомов. Ответ 2 : ковалентная связь, образованная при перекрывании атомных орбиталей вдоль межъядерной оси. Ответ 3 : ионная связь, образованная при осевом перекрывании атомных орбиталей связываемых атомов. Ответ 4 : ионная связь, образованная при боковом перекрывании атомных орбиталей связываемых атомов
Контрольные вопросы 3. Какая связь называется σ-связью ? Ответ 1 : ковалентная связь, образованная при боковом перекрывании атомных рорбиталей связываемых атомов. Ответ 2 : ковалентная связь, образованная при перекрывании атомных орбиталей вдоль межъядерной оси. Ответ 3 : ионная связь, образованная при осевом перекрывании атомных орбиталей связываемых атомов. Ответ 4 : ионная связь, образованная при боковом перекрывании атомных орбиталей связываемых атомов
 Контрольные вопросы 4. π-Связью называется. . . Ответ 1 : ковалентная связь, образованная при осевом перекрывании любых атомных орбиталей связываемых атомов. Ответ 2 : ковалентная связь, образованная при перекрывании атомных р-орбиталей вдоль межъядерной оси. Ответ 3 : ковалентная связь, образованная при боковом перекрывании атомных рорбиталей связываемых атомов. Ответ 4 : ионная связь, образованная при боковом перекрывании атомных орбиталей связываемых атомов
Контрольные вопросы 4. π-Связью называется. . . Ответ 1 : ковалентная связь, образованная при осевом перекрывании любых атомных орбиталей связываемых атомов. Ответ 2 : ковалентная связь, образованная при перекрывании атомных р-орбиталей вдоль межъядерной оси. Ответ 3 : ковалентная связь, образованная при боковом перекрывании атомных рорбиталей связываемых атомов. Ответ 4 : ионная связь, образованная при боковом перекрывании атомных орбиталей связываемых атомов
 Основные понятия общей химии химическая реакция; скорость химической реакции; энергия активации; тепловой эффект реакции; химическое равновесие; катализ.
Основные понятия общей химии химическая реакция; скорость химической реакции; энергия активации; тепловой эффект реакции; химическое равновесие; катализ.
 Основные понятия Химическая реакция – процесс превращения веществ, сопровождающийся изменением их состава и (или) строения. Происходит разрыв химических связей в исходных веществах и образование новых связей в продуктах реакции. Реакция считается законченной, если вещественный состав реакционной смеси больше не изменяется.
Основные понятия Химическая реакция – процесс превращения веществ, сопровождающийся изменением их состава и (или) строения. Происходит разрыв химических связей в исходных веществах и образование новых связей в продуктах реакции. Реакция считается законченной, если вещественный состав реакционной смеси больше не изменяется.
 Химическая реакция записывается в виде уравнения:
Химическая реакция записывается в виде уравнения:
 Химическая реакция В уравнениях реакций с участием органических соединений (органических реакциях) знак равенства заменяется стрелкой :
Химическая реакция В уравнениях реакций с участием органических соединений (органических реакциях) знак равенства заменяется стрелкой :
 Химическое равновесие Обратимая реакция - химическая реакция, которая при одних и тех же условиях может идти в прямом и в обратном направлениях:
Химическое равновесие Обратимая реакция - химическая реакция, которая при одних и тех же условиях может идти в прямом и в обратном направлениях:
 Химическое равновесие Необратимой называется реакция, которая идет практически до конца в одном направлении:
Химическое равновесие Необратимой называется реакция, которая идет практически до конца в одном направлении:
 Принцип Ле-Шателье внешнее воздействие на систему, находящуюся в состоянии равновесия, приводит к смещению этого равновесия в направлении, при котором эффект произведенного воздействия ослабляется.
Принцип Ле-Шателье внешнее воздействие на систему, находящуюся в состоянии равновесия, приводит к смещению этого равновесия в направлении, при котором эффект произведенного воздействия ослабляется.
 Принцип Ле-Шателье Увеличение давления смещает равновесие в сторону реакции, ведущей к уменьшению объема. Повышение температуры смещает равновесие в сторону эндотермической реакции. Увеличение концентрации исходных веществ и удаление продуктов из сферы реакции смещают равновесие в строну прямой реакции. Катализаторы не влияют на положение равновесия.
Принцип Ле-Шателье Увеличение давления смещает равновесие в сторону реакции, ведущей к уменьшению объема. Повышение температуры смещает равновесие в сторону эндотермической реакции. Увеличение концентрации исходных веществ и удаление продуктов из сферы реакции смещают равновесие в строну прямой реакции. Катализаторы не влияют на положение равновесия.
 Катализ - изменение скорости химической реакции в присутствии веществ, которые, участвуя в реакции, к моменту окончания процесса остаются количественно неизменными. Вещество, участвующее в реакции и изменяющее ее скорость, но остающееся неизменным после того, как химическая реакция заканчивается называется катализатором
Катализ - изменение скорости химической реакции в присутствии веществ, которые, участвуя в реакции, к моменту окончания процесса остаются количественно неизменными. Вещество, участвующее в реакции и изменяющее ее скорость, но остающееся неизменным после того, как химическая реакция заканчивается называется катализатором
 Катализ называется положительным, если скорость реакции увеличивается, и отрицательным, если скорость уменьшается. при гомогенном катализе реагенты и катализатор находятся в одной фазе (жидкой или газообразной), при гетерогенном катализе - в разных фазах (например, катализатор в твердом состоянии, а реагенты - в жидком или газообразном)
Катализ называется положительным, если скорость реакции увеличивается, и отрицательным, если скорость уменьшается. при гомогенном катализе реагенты и катализатор находятся в одной фазе (жидкой или газообразной), при гетерогенном катализе - в разных фазах (например, катализатор в твердом состоянии, а реагенты - в жидком или газообразном)
 Механизм действия катализатора связан с тем, что они снижают энергию активации реакции за счет образования промежуточных соединений с реагирующими веществами (каталитических комплексов), обладающих меньшей энергией:
Механизм действия катализатора связан с тем, что они снижают энергию активации реакции за счет образования промежуточных соединений с реагирующими веществами (каталитических комплексов), обладающих меньшей энергией:
 Отличительные особенности органических реакций 1. В реакциях органических соединений, как правило, изменения затрагивают только часть молекулы и ее основная конструкция (углеродный скелет) сохраняется:
Отличительные особенности органических реакций 1. В реакциях органических соединений, как правило, изменения затрагивают только часть молекулы и ее основная конструкция (углеродный скелет) сохраняется:
 Отличительные особенности органических реакций 2. Большинство органических реакций протекают значительно медленнее реакций неорганических веществ и обычно не завершаются полностью вследствие их обратимости 3. Многие органические реакции включают несколько элементарных стадий.
Отличительные особенности органических реакций 2. Большинство органических реакций протекают значительно медленнее реакций неорганических веществ и обычно не завершаются полностью вследствие их обратимости 3. Многие органические реакции включают несколько элементарных стадий.
 Отличительные особенности органических реакций Последовательность принято изображать в виде схемы превращений, в которой реагент записывается над стрелкой, а выделяющийся побочный продукт под стрелкой со знаком “минус”:
Отличительные особенности органических реакций Последовательность принято изображать в виде схемы превращений, в которой реагент записывается над стрелкой, а выделяющийся побочный продукт под стрелкой со знаком “минус”:
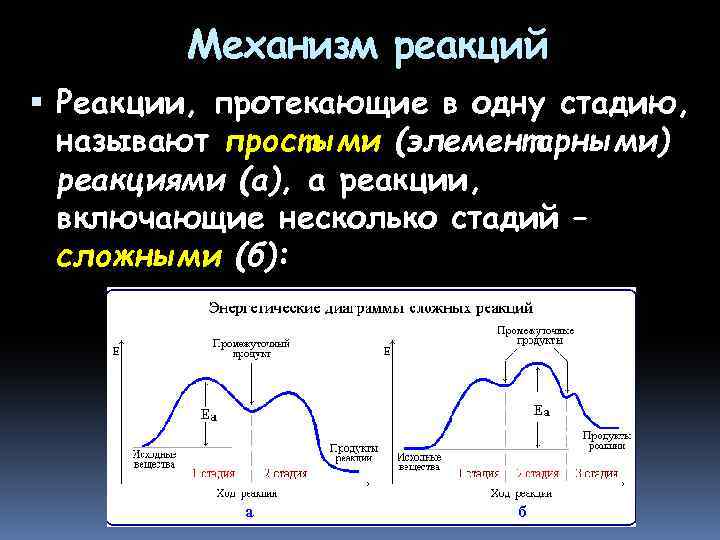 Механизм реакций Реакции, протекающие в одну стадию, называют простыми (элементарными) реакциями (а), а реакции, включающие несколько стадий – сложными (б):
Механизм реакций Реакции, протекающие в одну стадию, называют простыми (элементарными) реакциями (а), а реакции, включающие несколько стадий – сложными (б):
 Классификация органических реакций по конечному результату реакции (на основе сопоставления строения исходных и конечных продуктов); по минимальному числу частиц, участвующих в элементарной реакции; по механизму разрыва ковалентных связей в реагирующих молекулах
Классификация органических реакций по конечному результату реакции (на основе сопоставления строения исходных и конечных продуктов); по минимальному числу частиц, участвующих в элементарной реакции; по механизму разрыва ковалентных связей в реагирующих молекулах
 Классификация реакций по конечному результату: разложения; соединения; замещения; перегруппировки (изомеризация)
Классификация реакций по конечному результату: разложения; соединения; замещения; перегруппировки (изомеризация)
 Классификация реакций по механизму разрыва связей В зависимости от способа разрыва ковалентной связи в реагирующей молекуле органические реакции подразделяются на радикальные и ионные реакции. Ионные реакции в свою очередь делятся по характеру реагента, действующего на молекулу, на электрофильные и нуклеофильные
Классификация реакций по механизму разрыва связей В зависимости от способа разрыва ковалентной связи в реагирующей молекуле органические реакции подразделяются на радикальные и ионные реакции. Ионные реакции в свою очередь делятся по характеру реагента, действующего на молекулу, на электрофильные и нуклеофильные
 Разрыв ковалентной связи 1. Разрыв связи, при котором каждый атом получает по одному электрону из общей пары, называется гомолитическим: В результате гомолитического разрыва образуются сходные по электронному строению частицы, каждая из которых имеет неспаренный электрон. Такие частицы называются свободными радикалами
Разрыв ковалентной связи 1. Разрыв связи, при котором каждый атом получает по одному электрону из общей пары, называется гомолитическим: В результате гомолитического разрыва образуются сходные по электронному строению частицы, каждая из которых имеет неспаренный электрон. Такие частицы называются свободными радикалами
 Разрыв ковалентной связи Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется гетеролитическим: В результате образуются разноименно заряженные ионы - катион и анион. Если заряд иона сосредоточен на атоме углерода, то катион называют карбокатионом, а анион - карбанионом
Разрыв ковалентной связи Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется гетеролитическим: В результате образуются разноименно заряженные ионы - катион и анион. Если заряд иона сосредоточен на атоме углерода, то катион называют карбокатионом, а анион - карбанионом
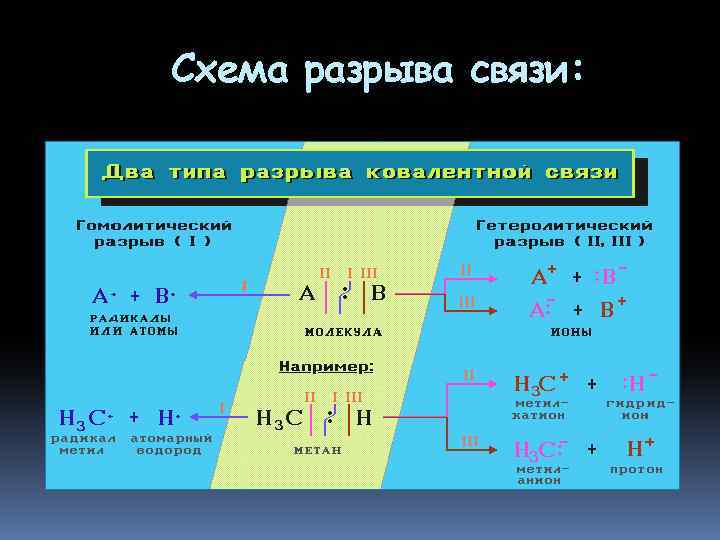 Схема разрыва связи:
Схема разрыва связи:
 Контрольные вопросы 1. Укажите тип реакции: Ответ 1: 2: 3: 4: замещения присоединения элиминирования изомеризации
Контрольные вопросы 1. Укажите тип реакции: Ответ 1: 2: 3: 4: замещения присоединения элиминирования изомеризации
 Контрольные вопросы 2. Какие типы реакций представлены в схеме превращений: Ответ 1 : I - присоединение; II - разложение Ответ 2 : I - разложение; II - замещение Ответ 3 : I - присоединение; II - замещение Ответ 4 : I - замещение; II - присоединение
Контрольные вопросы 2. Какие типы реакций представлены в схеме превращений: Ответ 1 : I - присоединение; II - разложение Ответ 2 : I - разложение; II - замещение Ответ 3 : I - присоединение; II - замещение Ответ 4 : I - замещение; II - присоединение
 Контрольные вопросы 3. В соответствии с конечным результатом данная реакция является: Ответ 1 : реакцией присоединения Ответ 2 : реакцией разложения Ответ 3 : реакцией замещения Ответ 4 : реакцией изомеризации
Контрольные вопросы 3. В соответствии с конечным результатом данная реакция является: Ответ 1 : реакцией присоединения Ответ 2 : реакцией разложения Ответ 3 : реакцией замещения Ответ 4 : реакцией изомеризации
 Контрольные вопросы 4. По какому механизму идет реакция: CH 3 CH 2 Br + Na. OH —> CH 3 CH 2 OH + Na. Br Ответ 1 : нуклеофильное присоединение Ответ 2 : электрофильное замещение Ответ 3 : нуклеофильное замещение Ответ 4 : радикальное замещение
Контрольные вопросы 4. По какому механизму идет реакция: CH 3 CH 2 Br + Na. OH —> CH 3 CH 2 OH + Na. Br Ответ 1 : нуклеофильное присоединение Ответ 2 : электрофильное замещение Ответ 3 : нуклеофильное замещение Ответ 4 : радикальное замещение
 Углеводороды 2/1/2018 98
Углеводороды 2/1/2018 98
 Алканы Алка ны (насыщенные углеводороды, парафины) — ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи и образующие гомологический ряд с общей формулой Cn. H 2 n+2. Алканы являются насыщенными соединениями и содержат максимально возможное число атомов водорода. Каждый атом углерода в молекулах алканов находится в состоянии sp³гибридизации. Простейшие представители алканов:
Алканы Алка ны (насыщенные углеводороды, парафины) — ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи и образующие гомологический ряд с общей формулой Cn. H 2 n+2. Алканы являются насыщенными соединениями и содержат максимально возможное число атомов водорода. Каждый атом углерода в молекулах алканов находится в состоянии sp³гибридизации. Простейшие представители алканов:
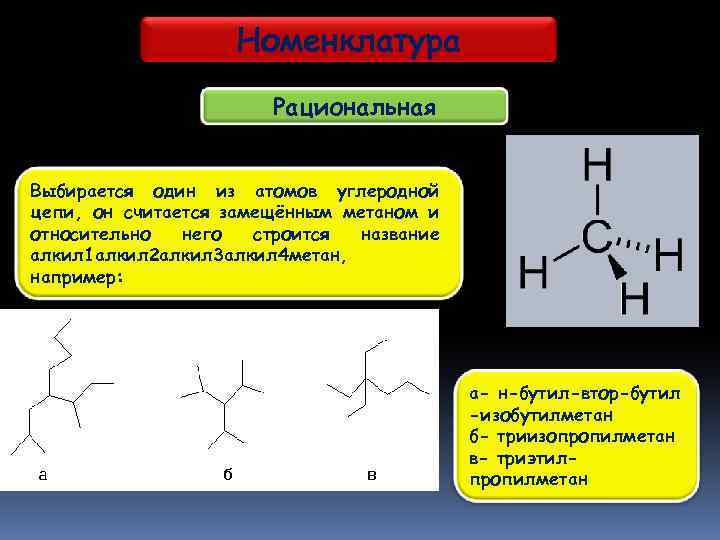 Номенклатура Рациональная Выбирается один из атомов углеродной цепи, он считается замещённым метаном и относительно него строится название алкил 1 алкил 2 алкил 3 алкил 4 метан, например: а- н-бутил-втор-бутил -изобутилметан б- триизопропилметан в- триэтилпропилметан
Номенклатура Рациональная Выбирается один из атомов углеродной цепи, он считается замещённым метаном и относительно него строится название алкил 1 алкил 2 алкил 3 алкил 4 метан, например: а- н-бутил-втор-бутил -изобутилметан б- триизопропилметан в- триэтилпропилметан
 Систематическая ИЮПАК По номенклатуре ИЮПАК названия алканов образуются при помощи суффикса -ан путём добавления к соответствующему корню от названия углеводорода. Выбирается наиболее длинная неразветвлённая углеводородная цепь так, чтобы у наибольшего числа заместителей был минимальный номер в цепи. В названии соединения цифрой указывают номер углеродного атома, при котором находится замещающий радикал, затем название радикала и название главной цепи. Например: 2, 6, 6 -триметил-3 -этилгептан
Систематическая ИЮПАК По номенклатуре ИЮПАК названия алканов образуются при помощи суффикса -ан путём добавления к соответствующему корню от названия углеводорода. Выбирается наиболее длинная неразветвлённая углеводородная цепь так, чтобы у наибольшего числа заместителей был минимальный номер в цепи. В названии соединения цифрой указывают номер углеродного атома, при котором находится замещающий радикал, затем название радикала и название главной цепи. Например: 2, 6, 6 -триметил-3 -этилгептан
 Гомологический ряд и изомерия Изомерия предельных углеводородов обусловлена простейшим видом структурной изомерии — изомерией углеродного скелета. Алканы, число атомов углерода в которых больше трёх, имеют изомеры. Число этих изомеров возрастает с огромной скоростью по мере увеличения числа атомов углерода. Для алканов с n = 1… 12 число изомеров равно 1, 1, 1, 2, 3, 5, 9, 18, 35, 75, 159, 355. Гомологический ряд алканов (первые 10 членов)
Гомологический ряд и изомерия Изомерия предельных углеводородов обусловлена простейшим видом структурной изомерии — изомерией углеродного скелета. Алканы, число атомов углерода в которых больше трёх, имеют изомеры. Число этих изомеров возрастает с огромной скоростью по мере увеличения числа атомов углерода. Для алканов с n = 1… 12 число изомеров равно 1, 1, 1, 2, 3, 5, 9, 18, 35, 75, 159, 355. Гомологический ряд алканов (первые 10 членов)
 Синтез Фишера-Тропша Процесс Фишера — Тропша — это химическая реакция, происходящая в присутствии катализатора, в которой монооксид углерода (CO) и водород H 2 преобразуются в различные жидкие углеводороды. Обычно используются катализаторы, содержащие железо и кобальт. Принципиальное значение этого процесса — это производство синтетических углеводородов. n. CO + (2 n+1)H 2→Cn. H 2 n+2 + H 2 O синтетическое смазочное масло
Синтез Фишера-Тропша Процесс Фишера — Тропша — это химическая реакция, происходящая в присутствии катализатора, в которой монооксид углерода (CO) и водород H 2 преобразуются в различные жидкие углеводороды. Обычно используются катализаторы, содержащие железо и кобальт. Принципиальное значение этого процесса — это производство синтетических углеводородов. n. CO + (2 n+1)H 2→Cn. H 2 n+2 + H 2 O синтетическое смазочное масло
 Номенклатура алкенов С 2 Н 4 Этен С 3 Н 6 Пропен С 4 Н 8 Бутен С 5 Н 10 Пентен С 6 Н 12 Гексен С 7 Н 14 Гептен С 8 Н 16 Октен С 9 Н 18 Нонен С 10 Н 20 Децен Общая формула алкенов Сn. H 2 n где n≥ 2
Номенклатура алкенов С 2 Н 4 Этен С 3 Н 6 Пропен С 4 Н 8 Бутен С 5 Н 10 Пентен С 6 Н 12 Гексен С 7 Н 14 Гептен С 8 Н 16 Октен С 9 Н 18 Нонен С 10 Н 20 Децен Общая формула алкенов Сn. H 2 n где n≥ 2
 Номенклатура алкенов Выбирается самая длинная цепь с двойной связью и нумеруется с той стороны ближе к которой располагается 2 -ая связь. Если есть радикалы, то указывается место и их количество, а также место 2 -ой связи. СH 3−CН−CH=CH 2 | CH 3 3 -метилбутен-1
Номенклатура алкенов Выбирается самая длинная цепь с двойной связью и нумеруется с той стороны ближе к которой располагается 2 -ая связь. Если есть радикалы, то указывается место и их количество, а также место 2 -ой связи. СH 3−CН−CH=CH 2 | CH 3 3 -метилбутен-1
 Изомерия алкенов Изомерия зависит от положение двойной связи и от положения R (радикалов). СН 3 -СН 2 -СН=СН 2 СН 3 -СН=СН-СН 3 бутен-1 бутен-2 СН 3 -СН=СН 2 | СН 3 2 -метилпропен-1
Изомерия алкенов Изомерия зависит от положение двойной связи и от положения R (радикалов). СН 3 -СН 2 -СН=СН 2 СН 3 -СН=СН-СН 3 бутен-1 бутен-2 СН 3 -СН=СН 2 | СН 3 2 -метилпропен-1
 Изомерия алкенов Пространственная (геометрическая) изомерия существует из-за невозможности вращения атомов углерода относительно друга: cis и tr – изомерия CH 3 H | | C = C | | C = C | | H H cis H CH 3 tr t кип +4 t кип +1
Изомерия алкенов Пространственная (геометрическая) изомерия существует из-за невозможности вращения атомов углерода относительно друга: cis и tr – изомерия CH 3 H | | C = C | | C = C | | H H cis H CH 3 tr t кип +4 t кип +1
 Применение Этен (этилен) используется в качестве исходного вещества для получения: стирола; полистирола; этиленгликоля; хлорэтана; дихлорэтана; полиэтилена; диэтилового эфира; этанола; дивинила; каучука; и др. веществ.
Применение Этен (этилен) используется в качестве исходного вещества для получения: стирола; полистирола; этиленгликоля; хлорэтана; дихлорэтана; полиэтилена; диэтилового эфира; этанола; дивинила; каучука; и др. веществ.
 Определение алкинов Алкинами называются УГ в которых есть тройная связь и отвечающие формуле Cn. H 2 n-2 где n ≥ 2.
Определение алкинов Алкинами называются УГ в которых есть тройная связь и отвечающие формуле Cn. H 2 n-2 где n ≥ 2.
 Номенклатура и Изомерия CH≡CH CH≡C-CH 3 CH≡C-CH 2 -CH 3 CH 3 -C ≡ C-CH 2 -CH 3 Этин (ацетилен) Пропин (пропилен) Бутин - 1 Пентин - 2 CH≡C-CH 2 -CH 3 I 4 -метил-гексин-1 CH 3
Номенклатура и Изомерия CH≡CH CH≡C-CH 3 CH≡C-CH 2 -CH 3 CH 3 -C ≡ C-CH 2 -CH 3 Этин (ацетилен) Пропин (пропилен) Бутин - 1 Пентин - 2 CH≡C-CH 2 -CH 3 I 4 -метил-гексин-1 CH 3
 Применение Ацетилен используется для сварки и резки металлов. 2 CH≡CH + 5 O 2 → 4 CO 2 + 2 H 2 O – ΔH (3500 ºС) Для синтеза ароматических УГ, каучуков, уксусной кислоты и этилового спирта.
Применение Ацетилен используется для сварки и резки металлов. 2 CH≡CH + 5 O 2 → 4 CO 2 + 2 H 2 O – ΔH (3500 ºС) Для синтеза ароматических УГ, каучуков, уксусной кислоты и этилового спирта.
 Арены Ароматическими углеводородами (аренами) называются вещества, в молекулах которых содержится одно или несколько бензольных колец — циклических групп атомов углерода с особым характером связей. Понятие “бензольное кольцо” требует расшифровки. Для этого необходимо рассмотреть строение молекулы бензола. Первая структура бензола была предложена в 1865 г. немецким ученым А. Кекуле:
Арены Ароматическими углеводородами (аренами) называются вещества, в молекулах которых содержится одно или несколько бензольных колец — циклических групп атомов углерода с особым характером связей. Понятие “бензольное кольцо” требует расшифровки. Для этого необходимо рассмотреть строение молекулы бензола. Первая структура бензола была предложена в 1865 г. немецким ученым А. Кекуле:
 Каждый атом углерода имеет одну негибридизованную р-орбиталь. Шесть таких орбиталей располагаются перпендикулярно плоскому s -скелету и параллельно другу (см. рис. а). Все шесть электронов взаимодействуют между собой, образуя p -связи, не локализованные в пары как при образовании двойных связей, а объединенные в единое p -электронное облако. Таким образом, в молекуле бензола осуществляется круговое сопряжение. Наибольшая p -электронная плотность в этой сопряженной системе располагается над и под плоскостью s -скелета (см. рис. б).
Каждый атом углерода имеет одну негибридизованную р-орбиталь. Шесть таких орбиталей располагаются перпендикулярно плоскому s -скелету и параллельно другу (см. рис. а). Все шесть электронов взаимодействуют между собой, образуя p -связи, не локализованные в пары как при образовании двойных связей, а объединенные в единое p -электронное облако. Таким образом, в молекуле бензола осуществляется круговое сопряжение. Наибольшая p -электронная плотность в этой сопряженной системе располагается над и под плоскостью s -скелета (см. рис. б).
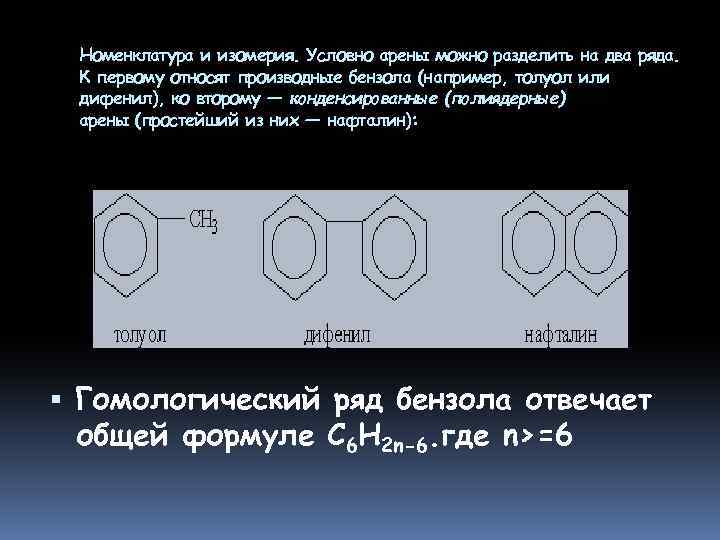 Номенклатура и изомерия. Условно арены можно разделить на два ряда. К первому относят производные бензола (например, толуол или дифенил), ко второму — конденсированные (полиядерные) арены (простейший из них — нафталин): Гомологический ряд бензола отвечает общей формуле С 6 Н 2 n-6. где n>=6
Номенклатура и изомерия. Условно арены можно разделить на два ряда. К первому относят производные бензола (например, толуол или дифенил), ко второму — конденсированные (полиядерные) арены (простейший из них — нафталин): Гомологический ряд бензола отвечает общей формуле С 6 Н 2 n-6. где n>=6
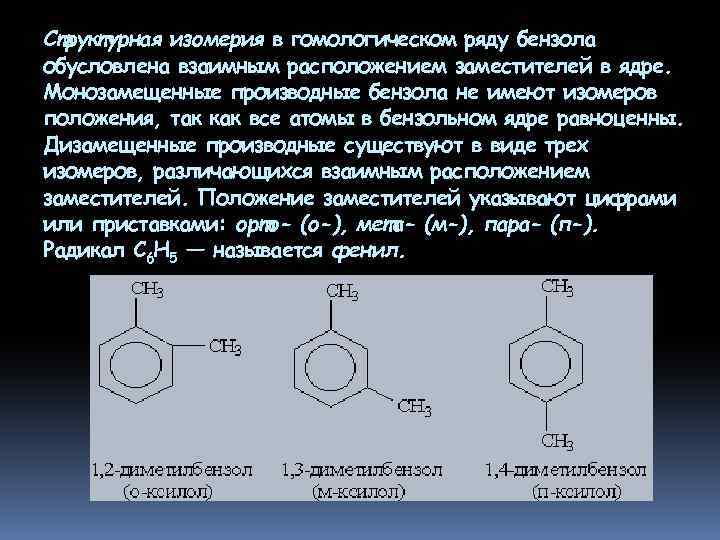 Структурная изомерия в гомологическом ряду бензола обусловлена взаимным расположением заместителей в ядре. Монозамещенные производные бензола не имеют изомеров положения, так как все атомы в бензольном ядре равноценны. Дизамещенные производные существуют в виде трех изомеров, различающихся взаимным расположением заместителей. Положение заместителей указывают цифрами или приставками: орто- (о-), мета- (м-), пара- (п-). Радикал С 6 Н 5 — называется фенил.
Структурная изомерия в гомологическом ряду бензола обусловлена взаимным расположением заместителей в ядре. Монозамещенные производные бензола не имеют изомеров положения, так как все атомы в бензольном ядре равноценны. Дизамещенные производные существуют в виде трех изомеров, различающихся взаимным расположением заместителей. Положение заместителей указывают цифрами или приставками: орто- (о-), мета- (м-), пара- (п-). Радикал С 6 Н 5 — называется фенил.
 Генетическая связь между углеводородами свойства углеводородов зависят от химического, пространственного, электронного строения молекул и характера химических связей; определяющую роль в особенностях строения и свойств отдельных типов углеводородов играет вид гибридизации атомных орбиталей углерода
Генетическая связь между углеводородами свойства углеводородов зависят от химического, пространственного, электронного строения молекул и характера химических связей; определяющую роль в особенностях строения и свойств отдельных типов углеводородов играет вид гибридизации атомных орбиталей углерода
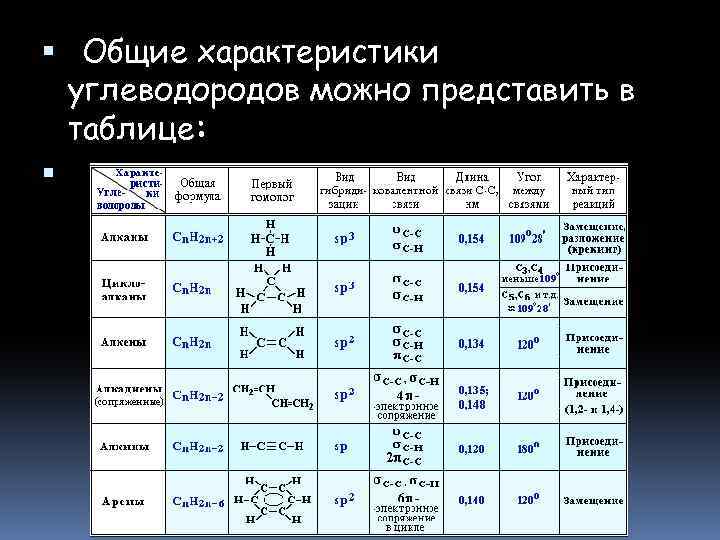 Общие характеристики углеводородов можно представить в таблице:
Общие характеристики углеводородов можно представить в таблице:
 Генетическая связь между углеводородами Изучение строения, химических свойств и способов получения углеводородов различных групп показывает, что все они генетически связаны между собой, т. е. возможны превращения одних углеводородов в другие;
Генетическая связь между углеводородами Изучение строения, химических свойств и способов получения углеводородов различных групп показывает, что все они генетически связаны между собой, т. е. возможны превращения одних углеводородов в другие;
 Генетическая связь между углеводородами Это позволяет осуществлять целенаправленный синтез заданных соединений, используя ряд необходимых химических реакций (цепь превращений)
Генетическая связь между углеводородами Это позволяет осуществлять целенаправленный синтез заданных соединений, используя ряд необходимых химических реакций (цепь превращений)
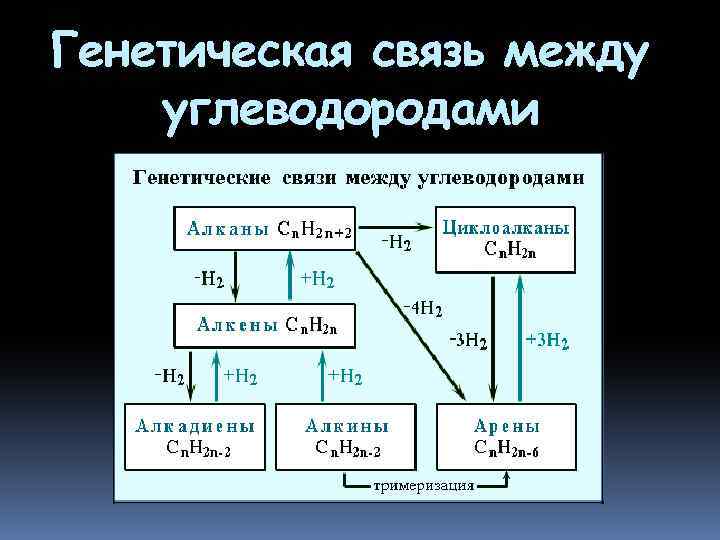 Генетическая связь между углеводородами
Генетическая связь между углеводородами
 1. Контрольные вопросы С помощью каких реагентов можно осуществить следующие превращения: Ответ 1: 1 – O 2; 2 – C, t°; 3 – H 2 O, (Hg. SO 4) Ответ 2: 1 – Ca; 2 – H 2 O, (Hg. SO 4); 3 – H 2 O Ответ 3: 1 – C, t°; 2 – H 2 O; 3 – O 2 Ответ 4: 1 – C, t°; 2 – H 2 O; 3 – H 2 O, (Hg. SO 4) Напишите все уравнения реакций
1. Контрольные вопросы С помощью каких реагентов можно осуществить следующие превращения: Ответ 1: 1 – O 2; 2 – C, t°; 3 – H 2 O, (Hg. SO 4) Ответ 2: 1 – Ca; 2 – H 2 O, (Hg. SO 4); 3 – H 2 O Ответ 3: 1 – C, t°; 2 – H 2 O; 3 – O 2 Ответ 4: 1 – C, t°; 2 – H 2 O; 3 – H 2 O, (Hg. SO 4) Напишите все уравнения реакций
 Кислородсодержащие соединения 2/1/2018 122
Кислородсодержащие соединения 2/1/2018 122
 СПИРТЫ И ФЕНОЛЫ Спиртами называются соединения, содержащие одну или несколько гидроксильных групп (–ОН), связанных с углеводородным радикалом. Вещества, у которых гидроксил находится непосредственно у бензольного кольца, называются фенолами. В зависимости от числа гидроксильных групп спирты делят на одно-, двух- и трёхатомные. В зависимости от того, при каком углеродном атоме находится гидроксильная группа, различают спирты: первичные R–CH 2–OH, вторичные R и третичные R I I CH–OH, R’ - C–OH I I R’ R’’
СПИРТЫ И ФЕНОЛЫ Спиртами называются соединения, содержащие одну или несколько гидроксильных групп (–ОН), связанных с углеводородным радикалом. Вещества, у которых гидроксил находится непосредственно у бензольного кольца, называются фенолами. В зависимости от числа гидроксильных групп спирты делят на одно-, двух- и трёхатомные. В зависимости от того, при каком углеродном атоме находится гидроксильная группа, различают спирты: первичные R–CH 2–OH, вторичные R и третичные R I I CH–OH, R’ - C–OH I I R’ R’’
 Одноатомные спирты Изомерия углеродного радикала (начиная с C 4 H 9 OH). Изомерия положения гидроксильной группы, (начиная с С 3 Н 7 ОН). Межклассовая изомерия с простыми эфирами (СН 3–СН 2–ОН СН 3–О–СН 3). и Название спиртов включает в себя наименование соответствующего углеводорода с добавлением суффикса ол (положение гидроксильной группы указывают цифрой) или к названию углеводородного радикала добавляется слово "спирт"; также часто встречаются тривиальные (бытовые) названия: СН 3–ОН – метанол, метиловый спирт; СН 3–СН 2–ОН – этанол, этиловый спирт; СН 3–СНОН–СН 3 – пропанол-2, изопропиловый спирт.
Одноатомные спирты Изомерия углеродного радикала (начиная с C 4 H 9 OH). Изомерия положения гидроксильной группы, (начиная с С 3 Н 7 ОН). Межклассовая изомерия с простыми эфирами (СН 3–СН 2–ОН СН 3–О–СН 3). и Название спиртов включает в себя наименование соответствующего углеводорода с добавлением суффикса ол (положение гидроксильной группы указывают цифрой) или к названию углеводородного радикала добавляется слово "спирт"; также часто встречаются тривиальные (бытовые) названия: СН 3–ОН – метанол, метиловый спирт; СН 3–СН 2–ОН – этанол, этиловый спирт; СН 3–СНОН–СН 3 – пропанол-2, изопропиловый спирт.
 Многоатомные спирты Многоатомными спиртами называют вещества, которые являются производными углеводородов в которых два или более атомов водорода замещены на гидрооксогруппы. R-(OH)n где n>2
Многоатомные спирты Многоатомными спиртами называют вещества, которые являются производными углеводородов в которых два или более атомов водорода замещены на гидрооксогруппы. R-(OH)n где n>2
 Двухатомный спирт CH 2 -OH | CH 2 -OH этиленгликоль (Р. Н. ) этандиол (М. Н. ) Хорошо растворимая, вязкая жидкость, сладкая на вкус, тем. кип. 197 градусов.
Двухатомный спирт CH 2 -OH | CH 2 -OH этиленгликоль (Р. Н. ) этандиол (М. Н. ) Хорошо растворимая, вязкая жидкость, сладкая на вкус, тем. кип. 197 градусов.
 Глицерин CH 2 -ОН НО CH 2 -O | Cu CH-ОН + НО → CH -O + 2 Н 2 О | | СН 2 -ОН Образуется раствор синего цвета – глицерата меди, это то же качественная реакция на многоатомные спирты.
Глицерин CH 2 -ОН НО CH 2 -O | Cu CH-ОН + НО → CH -O + 2 Н 2 О | | СН 2 -ОН Образуется раствор синего цвета – глицерата меди, это то же качественная реакция на многоатомные спирты.
 Фенол ОН | Карболовая кислота, бесцветные | кристаллы, при слабом окислении – розовые, плохо растворимые в воде (6, 3 г. В 100 г. воды), при темп. 70 градусов растворяются почти полностью. Получают из каменноугольной смолы
Фенол ОН | Карболовая кислота, бесцветные | кристаллы, при слабом окислении – розовые, плохо растворимые в воде (6, 3 г. В 100 г. воды), при темп. 70 градусов растворяются почти полностью. Получают из каменноугольной смолы
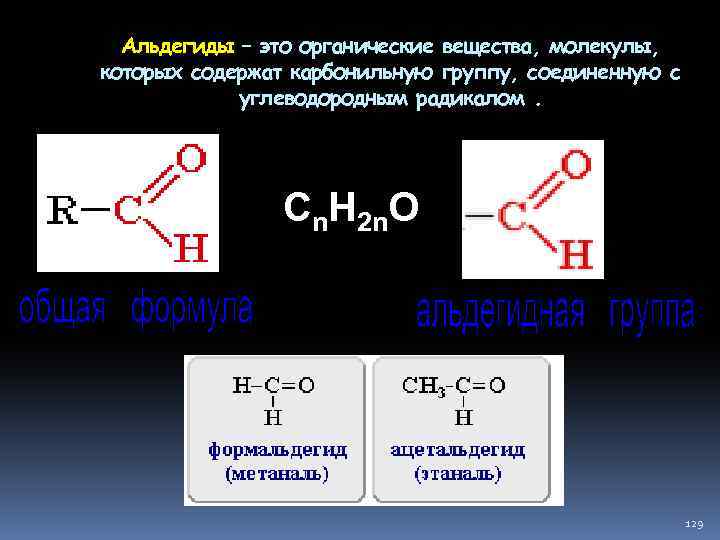 Альдегиды – это органические вещества, молекулы, которых содержат карбонильную группу, соединенную с углеводородным радикалом. Cn. H 2 n. O 129
Альдегиды – это органические вещества, молекулы, которых содержат карбонильную группу, соединенную с углеводородным радикалом. Cn. H 2 n. O 129
 Номенклатура альдегидов (международная) O H 3 C − CH | CH 3 − CH 2 − C H 3 -метил - бутан аль 130
Номенклатура альдегидов (международная) O H 3 C − CH | CH 3 − CH 2 − C H 3 -метил - бутан аль 130
 Изомерия Вид изомерии Формулы изомеров По углеродному скелету начиная с С 4 межклассовая с кетонами, начиная с С 3 непредельными спиртами и простыми эфирами (с С 3) 131
Изомерия Вид изомерии Формулы изомеров По углеродному скелету начиная с С 4 межклассовая с кетонами, начиная с С 3 непредельными спиртами и простыми эфирами (с С 3) 131
 Химические реакции восстановления полимеризации присоединения окисления 132
Химические реакции восстановления полимеризации присоединения окисления 132
 Применение альдегидов 1. Парфюмерия 2. Полимерные материалы 3. Производство веществ 4. Загрязнители атмосферы n n Фенолформальдегидные смолы Уксусная кислота Этилацетат Формалин Альдегид анисовый, обепин – жидкость с приятным запахом мимозы Альдегид дециловый, деканаль – при разбавлении появляются нотки запаха апельсиновой корки 133
Применение альдегидов 1. Парфюмерия 2. Полимерные материалы 3. Производство веществ 4. Загрязнители атмосферы n n Фенолформальдегидные смолы Уксусная кислота Этилацетат Формалин Альдегид анисовый, обепин – жидкость с приятным запахом мимозы Альдегид дециловый, деканаль – при разбавлении появляются нотки запаха апельсиновой корки 133
 Карбоновые кислоты - производные углеводородов, в молекулах которых один или несколько водородных атомов замещены на соответствующее число карбоксильных групп. 2/1/2018 134
Карбоновые кислоты - производные углеводородов, в молекулах которых один или несколько водородных атомов замещены на соответствующее число карбоксильных групп. 2/1/2018 134
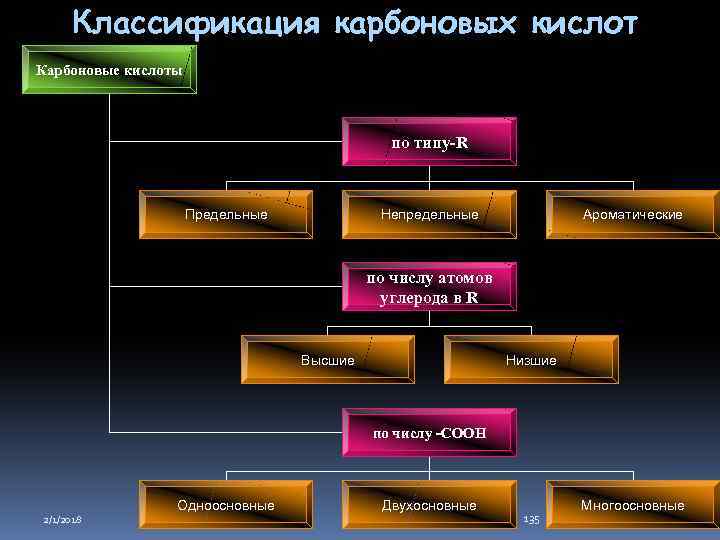 Классификация карбоновых кислот Карбоновые кислоты по типу-R Предельные Непредельные Ароматические по числу атомов углерода в R Высшие Низшие по числу -COOH 2/1/2018 Одноосновные Двухосновные 135 Многоосновные
Классификация карбоновых кислот Карбоновые кислоты по типу-R Предельные Непредельные Ароматические по числу атомов углерода в R Высшие Низшие по числу -COOH 2/1/2018 Одноосновные Двухосновные 135 Многоосновные
 Классификация карбоновых кислот 1. В зависимости от природы углеводного радикала а) предельные пропановая кислота б) непредельные акриловая кислота в) ароматические бензойная кислота 2/1/2018 136
Классификация карбоновых кислот 1. В зависимости от природы углеводного радикала а) предельные пропановая кислота б) непредельные акриловая кислота в) ароматические бензойная кислота 2/1/2018 136
 Классификация карбоновых кислот 2. По числу атомов углерода в радикале а) низшие муравьиная кислота б) высшие α-линоленовая кислота 2/1/2018 137
Классификация карбоновых кислот 2. По числу атомов углерода в радикале а) низшие муравьиная кислота б) высшие α-линоленовая кислота 2/1/2018 137
 Классификация карбоновых кислот 3. По количеству карбоксильных групп а) одноосновные уксусная кислота б) двухосновные малоновая кислота в) многоосновные 2/1/2018 лимонная кислота 138
Классификация карбоновых кислот 3. По количеству карбоксильных групп а) одноосновные уксусная кислота б) двухосновные малоновая кислота в) многоосновные 2/1/2018 лимонная кислота 138
 Общая формула гомологического ряда одноосновных предельных карбоновых кислот
Общая формула гомологического ряда одноосновных предельных карбоновых кислот
 Простейшие карбоновые кислоты 2/1/2018 140
Простейшие карбоновые кислоты 2/1/2018 140
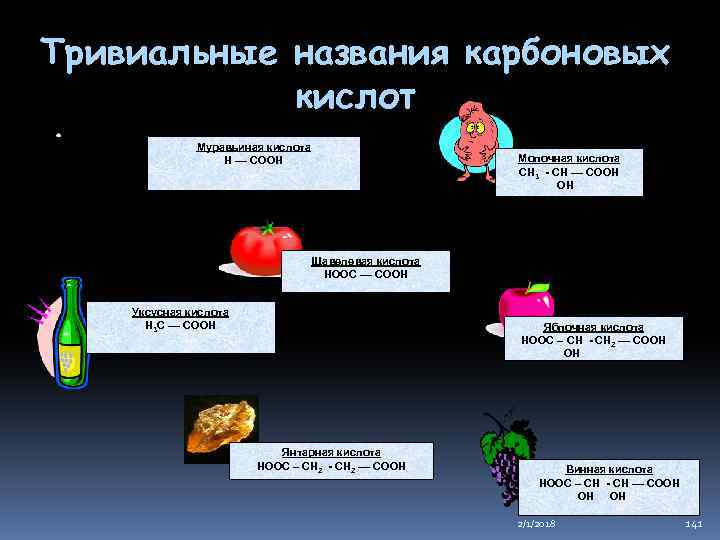 Тривиальные названия карбоновых кислот Муравьиная кислота Н –– COOH Молочная кислота СН 3 - СН –– COOH ОН Щавелевая кислота HOOC –– COOH Уксусная кислота H 3 C –– COOH Яблочная кислота HOOC – СН - СН 2 –– COOH ОН Янтарная кислота HOOC – СН 2 - СН 2 –– COOH Винная кислота HOOC – СН - СН –– COOH ОН ОН 2/1/2018 141
Тривиальные названия карбоновых кислот Муравьиная кислота Н –– COOH Молочная кислота СН 3 - СН –– COOH ОН Щавелевая кислота HOOC –– COOH Уксусная кислота H 3 C –– COOH Яблочная кислота HOOC – СН - СН 2 –– COOH ОН Янтарная кислота HOOC – СН 2 - СН 2 –– COOH Винная кислота HOOC – СН - СН –– COOH ОН ОН 2/1/2018 141
 Тривиальные названия карбоновых кислот Ацетилсалициловая кислота СООН ОСОСН 3 Аскорбиновая кислота НО ОН Н =О НОН 2 С-НОНС О Используются как лекарственные препараты 2/1/2018 142
Тривиальные названия карбоновых кислот Ацетилсалициловая кислота СООН ОСОСН 3 Аскорбиновая кислота НО ОН Н =О НОН 2 С-НОНС О Используются как лекарственные препараты 2/1/2018 142
 Номенклатура карбоновых кислот Систематические названия кислот даются по названию соответствующего углеводорода с добавлением суффикса -овая и слова кислота: 4 3 2 1 2/1/2018 143
Номенклатура карбоновых кислот Систематические названия кислот даются по названию соответствующего углеводорода с добавлением суффикса -овая и слова кислота: 4 3 2 1 2/1/2018 143
 Некоторые предельные одноосновные кислоты 2/1/2018 144
Некоторые предельные одноосновные кислоты 2/1/2018 144
 Производные карбоновых кислот Сложные эфиры Галогенангидриды Ангидриды
Производные карбоновых кислот Сложные эфиры Галогенангидриды Ангидриды
 Сложные эфиры производные карбоновых кислот, у которых водород гидроксильной группы замещен на углеводородный радикал.
Сложные эфиры производные карбоновых кислот, у которых водород гидроксильной группы замещен на углеводородный радикал.
 Систематическая номенклатура сложных эфиров кислотная часть 3 2 1 1 2 спиртовая часть радикал + алкан + оат
Систематическая номенклатура сложных эфиров кислотная часть 3 2 1 1 2 спиртовая часть радикал + алкан + оат
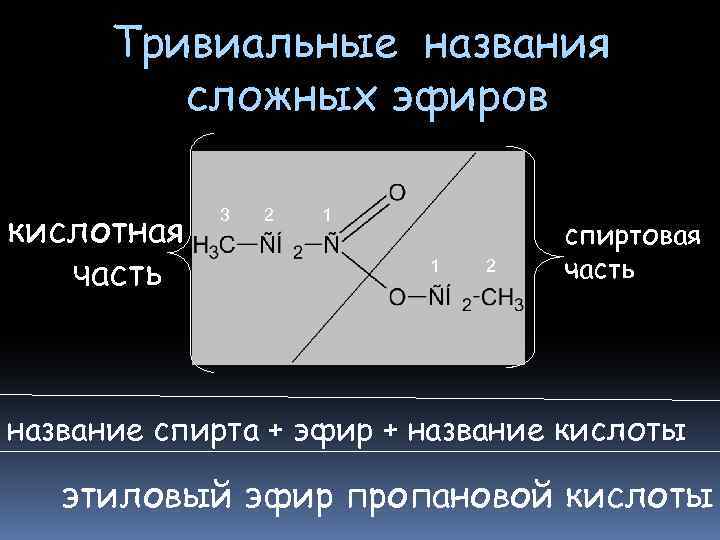 Тривиальные названия сложных эфиров кислотная часть 3 2 1 1 2 спиртовая часть название спирта + эфир + название кислоты этиловый эфир пропановой кислоты
Тривиальные названия сложных эфиров кислотная часть 3 2 1 1 2 спиртовая часть название спирта + эфир + название кислоты этиловый эфир пропановой кислоты
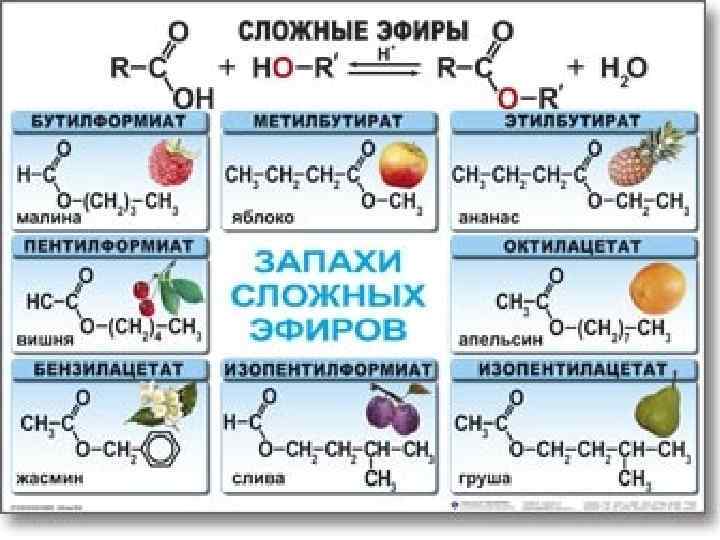
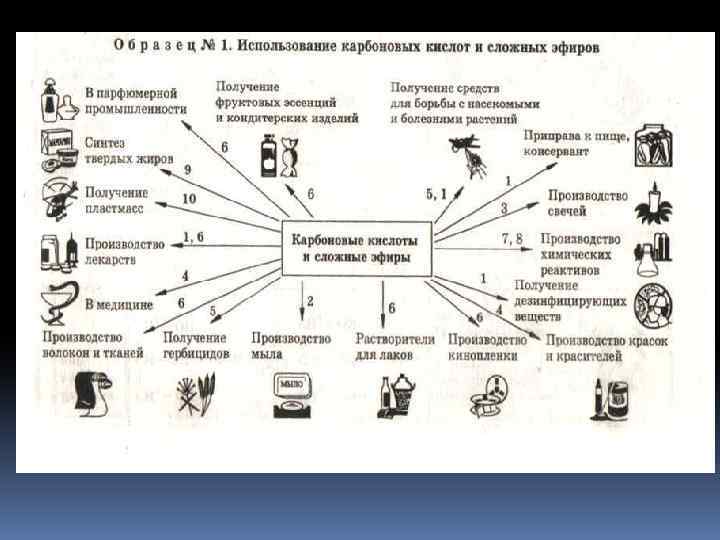
 Жиры сложные эфиры глицерина и высших одноатомных карбоновых кислот 2/1/2018 151
Жиры сложные эфиры глицерина и высших одноатомных карбоновых кислот 2/1/2018 151
 Триглицериды Общее название таких соединений триглицериды или триацилглицерины, где ацил - остаток карбоновой кислоты -C(O)R. В состав природных триглицеридов входят остатки насыщенных кислот (пальмитиновой C 15 H 31 COOH, стеариновой C 17 H 35 COOH) и ненасыщенных (олеиновой C 17 H 33 COOH, линолевой C 17 H 29 COOH). 2/1/2018 152
Триглицериды Общее название таких соединений триглицериды или триацилглицерины, где ацил - остаток карбоновой кислоты -C(O)R. В состав природных триглицеридов входят остатки насыщенных кислот (пальмитиновой C 15 H 31 COOH, стеариновой C 17 H 35 COOH) и ненасыщенных (олеиновой C 17 H 33 COOH, линолевой C 17 H 29 COOH). 2/1/2018 152
 Триглицериды Жиры содержатся во всех растениях и животных. Животные жиры (бараний, свиной, говяжий и т. п. ) являются твердыми веществами с невысокой температурой плавления (исключение - рыбий жир). Жиры состоят главным образом из триглицеридов предельных кислот. 2/1/2018 153
Триглицериды Жиры содержатся во всех растениях и животных. Животные жиры (бараний, свиной, говяжий и т. п. ) являются твердыми веществами с невысокой температурой плавления (исключение - рыбий жир). Жиры состоят главным образом из триглицеридов предельных кислот. 2/1/2018 153
 Триглицериды Растительные жиры - масла (подсолнечное, соевое, хлопковое и др. ) - жидкости (исключение - кокосовое масло). В состав триглицеридов масел входят остатки непредельных кислот. Продукт гидрогенизации масел - твердый жир. Маргарин - пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др. ), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др. ) 2/1/2018 154
Триглицериды Растительные жиры - масла (подсолнечное, соевое, хлопковое и др. ) - жидкости (исключение - кокосовое масло). В состав триглицеридов масел входят остатки непредельных кислот. Продукт гидрогенизации масел - твердый жир. Маргарин - пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др. ), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др. ) 2/1/2018 154
 Триглицериды Жидкие жиры превращают в твердые путем реакции гидрогенизации (гидрирования). При этом водород присоединяется по двойной связи, содержащейся в углеводородном радикале молекул масел 2/1/2018 155
Триглицериды Жидкие жиры превращают в твердые путем реакции гидрогенизации (гидрирования). При этом водород присоединяется по двойной связи, содержащейся в углеводородном радикале молекул масел 2/1/2018 155
 1. Контрольная работа Функциональную группу -СООН содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 156
1. Контрольная работа Функциональную группу -СООН содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 156
 2. Контрольная работа Функциональную группу -СОН содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 157
2. Контрольная работа Функциональную группу -СОН содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 157
 3. Контрольная работа Функциональную группу –С=О содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 158
3. Контрольная работа Функциональную группу –С=О содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 158
 4. Контрольная работа Функциональную группу - ОН содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 159
4. Контрольная работа Функциональную группу - ОН содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 159
 5. Контрольная работа Функциональную группу - СОО содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 160
5. Контрольная работа Функциональную группу - СОО содержат молекулы. . . Ответ 1 : сложных эфиров Ответ 2 : простых эфиров Ответ 3 : спиртов Ответ 4 : альдегидов Ответ 5 : кетонов Ответ 6 : карбоновых кислот 2/1/2018 160
 УГЛЕВОДЫ Углеводы – это органические вещества, молекулы которых состоят из атомов углерода, водорода и кислорода, причем водород и кислород находятся в них, как правило, в таком же соотношении, как и в молекуле воды (2: 1). Общая формула углеводов – Сn(H 2 O)m , т. е они как бы состоят из углерода и воды, отсюда и название класса, которое имеет исторические корни.
УГЛЕВОДЫ Углеводы – это органические вещества, молекулы которых состоят из атомов углерода, водорода и кислорода, причем водород и кислород находятся в них, как правило, в таком же соотношении, как и в молекуле воды (2: 1). Общая формула углеводов – Сn(H 2 O)m , т. е они как бы состоят из углерода и воды, отсюда и название класса, которое имеет исторические корни.
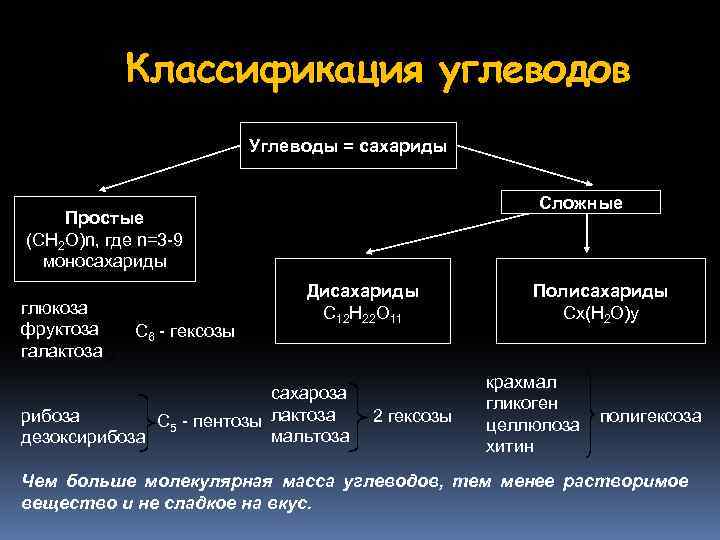 Классификация углеводов Углеводы = сахариды Сложные Простые (СН 2 О)n, где n=3 -9 моносахариды глюкоза фруктоза галактоза С 6 - гексозы Дисахариды С 12 Н 22 О 11 сахароза рибоза С 5 - пентозы лактоза мальтоза дезоксирибоза 2 гексозы Полисахариды Сx(Н 2 О)y крахмал гликоген целлюлоза хитин полигексоза Чем больше молекулярная масса углеводов, тем менее растворимое вещество и не сладкое на вкус.
Классификация углеводов Углеводы = сахариды Сложные Простые (СН 2 О)n, где n=3 -9 моносахариды глюкоза фруктоза галактоза С 6 - гексозы Дисахариды С 12 Н 22 О 11 сахароза рибоза С 5 - пентозы лактоза мальтоза дезоксирибоза 2 гексозы Полисахариды Сx(Н 2 О)y крахмал гликоген целлюлоза хитин полигексоза Чем больше молекулярная масса углеводов, тем менее растворимое вещество и не сладкое на вкус.
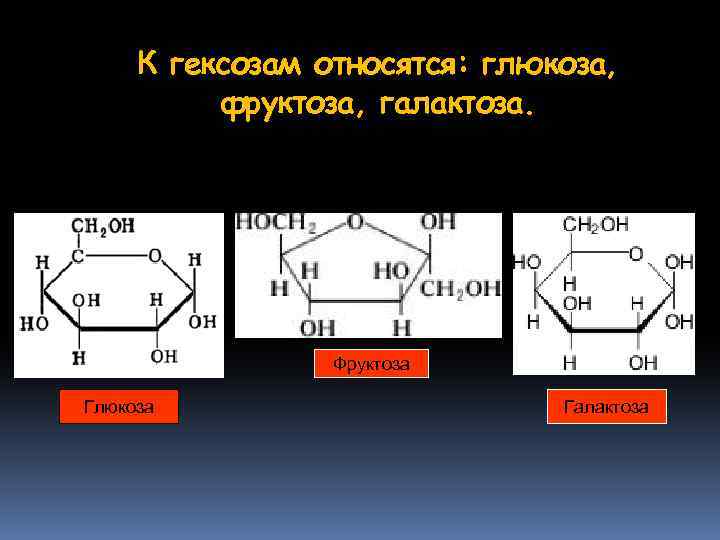 К гексозам относятся: глюкоза, фруктоза, галактоза. Фруктоза Глюкоза Галактоза
К гексозам относятся: глюкоза, фруктоза, галактоза. Фруктоза Глюкоза Галактоза
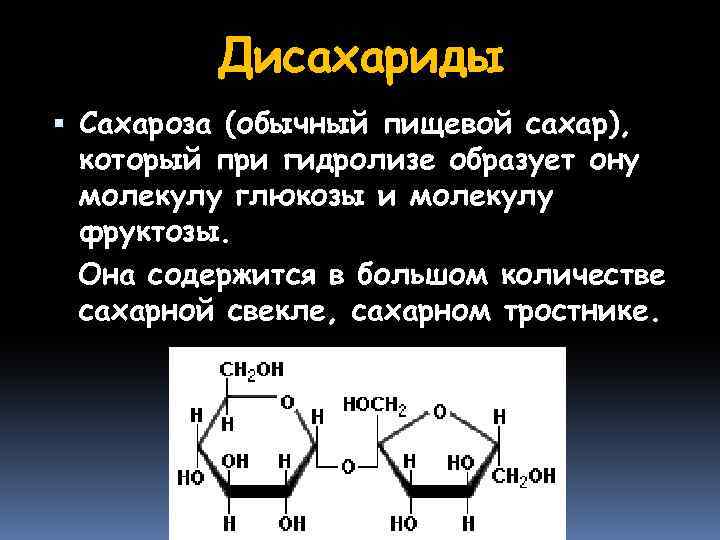 Дисахариды Сахароза (обычный пищевой сахар), который при гидролизе образует ону молекулу глюкозы и молекулу фруктозы. Она содержится в большом количестве сахарной свекле, сахарном тростнике.
Дисахариды Сахароза (обычный пищевой сахар), который при гидролизе образует ону молекулу глюкозы и молекулу фруктозы. Она содержится в большом количестве сахарной свекле, сахарном тростнике.
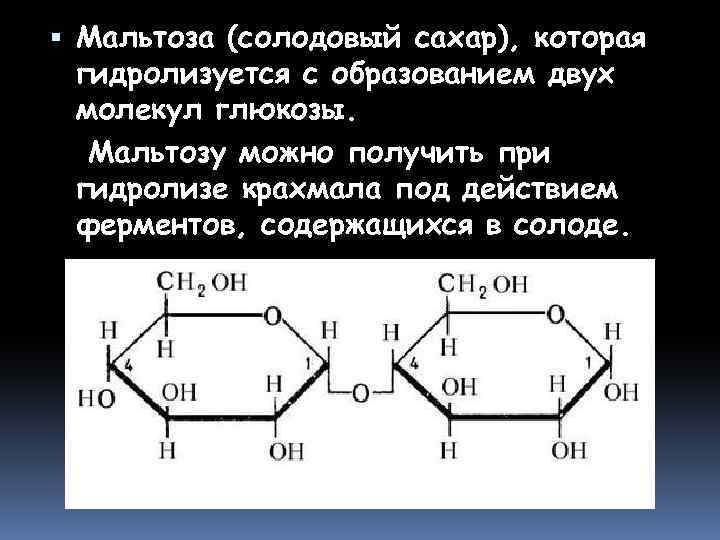 Мальтоза (солодовый сахар), которая гидролизуется с образованием двух молекул глюкозы. Мальтозу можно получить при гидролизе крахмала под действием ферментов, содержащихся в солоде.
Мальтоза (солодовый сахар), которая гидролизуется с образованием двух молекул глюкозы. Мальтозу можно получить при гидролизе крахмала под действием ферментов, содержащихся в солоде.
 Полисахариды Крахмал – резервный полисахарид многих растений. В промышленности его получают из картофеля. Это белый порошок. При гидролизе крахмала могут быть получены промежуточные продукты: растворимый крахмал декстрины мальтоза.
Полисахариды Крахмал – резервный полисахарид многих растений. В промышленности его получают из картофеля. Это белый порошок. При гидролизе крахмала могут быть получены промежуточные продукты: растворимый крахмал декстрины мальтоза.
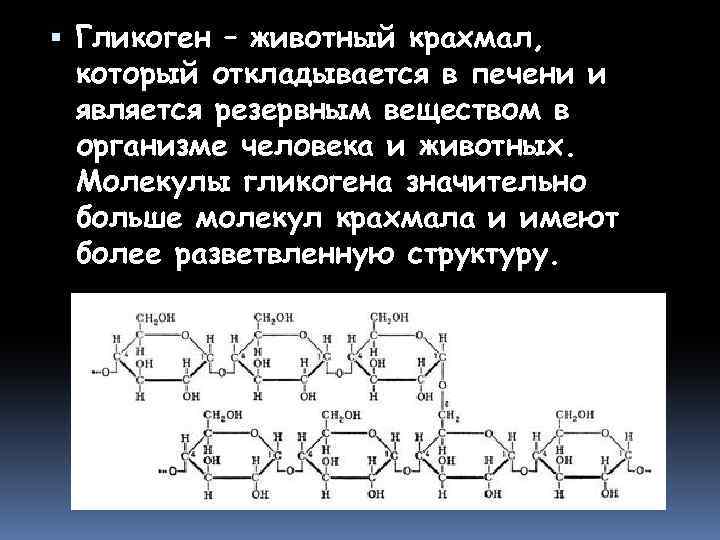 Гликоген – животный крахмал, который откладывается в печени и является резервным веществом в организме человека и животных. Молекулы гликогена значительно больше молекул крахмала и имеют более разветвленную структуру.
Гликоген – животный крахмал, который откладывается в печени и является резервным веществом в организме человека и животных. Молекулы гликогена значительно больше молекул крахмала и имеют более разветвленную структуру.
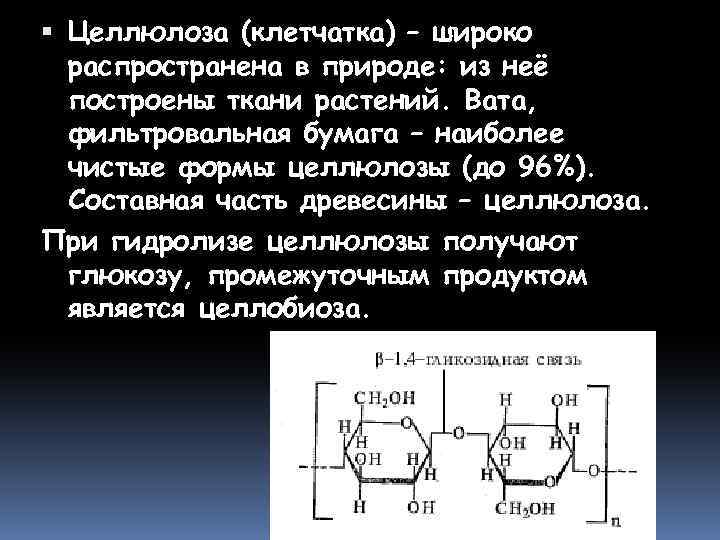 Целлюлоза (клетчатка) – широко распространена в природе: из неё построены ткани растений. Вата, фильтровальная бумага – наиболее чистые формы целлюлозы (до 96%). Составная часть древесины – целлюлоза. При гидролизе целлюлозы получают глюкозу, промежуточным продуктом является целлобиоза.
Целлюлоза (клетчатка) – широко распространена в природе: из неё построены ткани растений. Вата, фильтровальная бумага – наиболее чистые формы целлюлозы (до 96%). Составная часть древесины – целлюлоза. При гидролизе целлюлозы получают глюкозу, промежуточным продуктом является целлобиоза.
 Азотсодержащие соединения 2/1/2018 169
Азотсодержащие соединения 2/1/2018 169
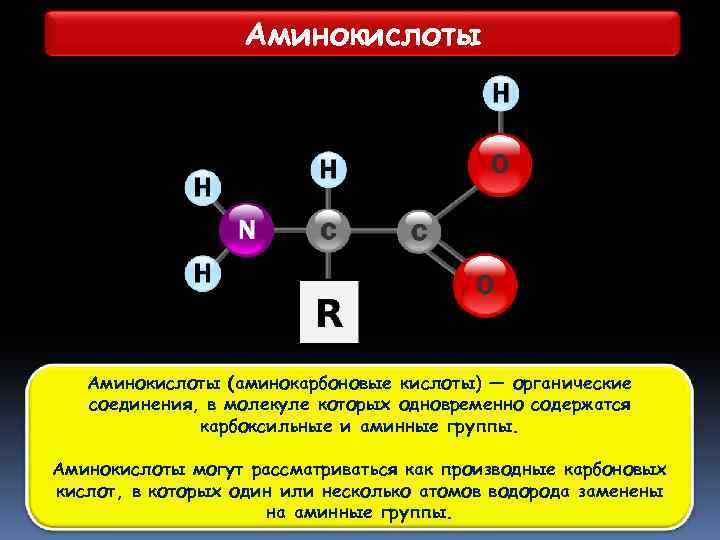 Аминокислоты (аминокарбоновые кислоты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы. Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.
Аминокислоты (аминокарбоновые кислоты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы. Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.
 Аминокислоты - строительные блоки, из которых строятся белковые структуры, мышечные волокна, например. Организм использует их для собственного роста, восстановления, укрепления и выработки различных гормонов, антител и ферментов. Всего существует 21 аминокислота, из них девять - так называемые “незаменимые” (организм не может самостоятельно синтезировать их в достаточном количестве). К ним относятся гистидин, изолеуцин, лизин, метионин, фенилаланин, треонин, триптофан и валин. Эти аминокислоты поступают в организм с мясом, рыбой, яйцами и молочными продуктами. Отдельно стоят так называемые две “полусущественные” аминокислоты: цистин и тирозин. Отличаются они от остальных тем, что организм может использовать их вместо, соответственно, метионина и фенилаланина для производства белка.
Аминокислоты - строительные блоки, из которых строятся белковые структуры, мышечные волокна, например. Организм использует их для собственного роста, восстановления, укрепления и выработки различных гормонов, антител и ферментов. Всего существует 21 аминокислота, из них девять - так называемые “незаменимые” (организм не может самостоятельно синтезировать их в достаточном количестве). К ним относятся гистидин, изолеуцин, лизин, метионин, фенилаланин, треонин, триптофан и валин. Эти аминокислоты поступают в организм с мясом, рыбой, яйцами и молочными продуктами. Отдельно стоят так называемые две “полусущественные” аминокислоты: цистин и тирозин. Отличаются они от остальных тем, что организм может использовать их вместо, соответственно, метионина и фенилаланина для производства белка.
 Применение Аминокислоты применяются в производстве косметики, лекарственных средств, напитков и пищевых добавок, но в основном (около двух третей) в производстве кормов для животных. В наше время производство кормов для животных является одной из самых прибыльных отраслей, а аминокислоты входят в состав самых разнообразных кормов.
Применение Аминокислоты применяются в производстве косметики, лекарственных средств, напитков и пищевых добавок, но в основном (около двух третей) в производстве кормов для животных. В наше время производство кормов для животных является одной из самых прибыльных отраслей, а аминокислоты входят в состав самых разнообразных кормов.
 Аминокислоты видов D и L Каждая аминокислота существует в двух формах: D и L. Эти формы химически идентичны, однако имеют структурные различия, которые заключаются в том, что одна форма является зеркальным отражением другой - почти каждая молекула протеина в нашем теле производится исключительно из L формы. В то же время D формы, как натуральные, так и синтетические, обладают некоторым терапевтическим эффектом. Эти формы, L и D, зеркально-симметричны: в них массивный боковой радикал (R) и Н-атом, стоящие при a-углероде (Сa) аминокислоты, меняются местами
Аминокислоты видов D и L Каждая аминокислота существует в двух формах: D и L. Эти формы химически идентичны, однако имеют структурные различия, которые заключаются в том, что одна форма является зеркальным отражением другой - почти каждая молекула протеина в нашем теле производится исключительно из L формы. В то же время D формы, как натуральные, так и синтетические, обладают некоторым терапевтическим эффектом. Эти формы, L и D, зеркально-симметричны: в них массивный боковой радикал (R) и Н-атом, стоящие при a-углероде (Сa) аминокислоты, меняются местами
 Альфа-аминокислоты белков В процессе биосинтеза белка в полипептидную цепь включаются 21 важнейших α-аминокислот, кодируемых генетическим кодом. 1) Лейцин (Leu, L) 2) Лизин (Lys, K) 3) Метионин (Met, M) 4) Пролин (Pro, P) 5) Серин (Ser, S) 6) Тирозин (Tyr, Y) 7) Треонин (Thr, T) 8) Триптофан (Trp, W) 9) Фенилаланин (Phe, F) 10)Цистеин (Cys, C) 11)Cеленцистеиновая Помимо этих аминокислот, называемых стандартными, в некоторых белках присутствуют специфические нестандартные аминокислоты, являющиеся производными стандартных. В последнее время к стандартным аминокислотам иногда причисляют селеноцистеин (Sec, U) и пирролизин (Pyl, O).
Альфа-аминокислоты белков В процессе биосинтеза белка в полипептидную цепь включаются 21 важнейших α-аминокислот, кодируемых генетическим кодом. 1) Лейцин (Leu, L) 2) Лизин (Lys, K) 3) Метионин (Met, M) 4) Пролин (Pro, P) 5) Серин (Ser, S) 6) Тирозин (Tyr, Y) 7) Треонин (Thr, T) 8) Триптофан (Trp, W) 9) Фенилаланин (Phe, F) 10)Цистеин (Cys, C) 11)Cеленцистеиновая Помимо этих аминокислот, называемых стандартными, в некоторых белках присутствуют специфические нестандартные аминокислоты, являющиеся производными стандартных. В последнее время к стандартным аминокислотам иногда причисляют селеноцистеин (Sec, U) и пирролизин (Pyl, O).
 Контрольная работа Какие из приведенных формул органических веществ относятся к аминокислотам? Ответ 1 2 3 4 175 : : а, а, б, в, в д г д 2/1/2018
Контрольная работа Какие из приведенных формул органических веществ относятся к аминокислотам? Ответ 1 2 3 4 175 : : а, а, б, в, в д г д 2/1/2018
 Контрольная работа Аминокислоты не могут реагировать. . . Ответ 1 : с основаниями и кислотами Ответ 2 : с кислотами и спиртами Ответ 3 : с предельными углеводородами Ответ 4 : между собой 176 2/1/2018
Контрольная работа Аминокислоты не могут реагировать. . . Ответ 1 : с основаниями и кислотами Ответ 2 : с кислотами и спиртами Ответ 3 : с предельными углеводородами Ответ 4 : между собой 176 2/1/2018
 Контрольная работа Сколько потребуется уксусной кислоты (по массе) для получения 139, 05 г этилового эфира аминоуксусной кислоты при 90% выходе? Ответ 1 : 45 г Ответ 2 : 90 г Ответ 3 : 135 г Ответ 4 : 180 г 177 2/1/2018
Контрольная работа Сколько потребуется уксусной кислоты (по массе) для получения 139, 05 г этилового эфира аминоуксусной кислоты при 90% выходе? Ответ 1 : 45 г Ответ 2 : 90 г Ответ 3 : 135 г Ответ 4 : 180 г 177 2/1/2018
 Высокомолекулярные соединения 2/1/2018 178
Высокомолекулярные соединения 2/1/2018 178
 Определение полимеров ПОЛИМЕРЫ (от поли. . . и греч. meros — доля, часть), вещества, молекулы которых (макромолекулы) состоят из большого числа повторяющихся звеньев; молекулярная масса полимеров может изменяться от нескольких тысяч до многих миллионов. Термин «полимеры введен Й. Я. Берцелиусом в 1833.
Определение полимеров ПОЛИМЕРЫ (от поли. . . и греч. meros — доля, часть), вещества, молекулы которых (макромолекулы) состоят из большого числа повторяющихся звеньев; молекулярная масса полимеров может изменяться от нескольких тысяч до многих миллионов. Термин «полимеры введен Й. Я. Берцелиусом в 1833.
 Классификация По происхождению полимеры делят на природные, или биополимеры (напр. , белки, нуклеиновые кислоты, натуральный каучук), и синтетические (напр. , полиэтилен, полиамиды, эпоксидные смолы), получаемые методами полимеризации и поликонденсации. По форме молекул различают линейные, разветвленные и сетчатые полимеры, по природе — органические, элементоорганические, неорганические полимеры.
Классификация По происхождению полимеры делят на природные, или биополимеры (напр. , белки, нуклеиновые кислоты, натуральный каучук), и синтетические (напр. , полиэтилен, полиамиды, эпоксидные смолы), получаемые методами полимеризации и поликонденсации. По форме молекул различают линейные, разветвленные и сетчатые полимеры, по природе — органические, элементоорганические, неорганические полимеры.
 Строение ПОЛИМЕРЫ - вещества, молекулы которых состоят из большого числа структурно повторяющихся звеньев — мономеров. Молекулярная масса полимеров достигает 106, а геометрические размеры молекул могут быть настолько велики, что растворы этих веществ по свойствам приближаются к коллоидным системам.
Строение ПОЛИМЕРЫ - вещества, молекулы которых состоят из большого числа структурно повторяющихся звеньев — мономеров. Молекулярная масса полимеров достигает 106, а геометрические размеры молекул могут быть настолько велики, что растворы этих веществ по свойствам приближаются к коллоидным системам.
 Строение По строению макромолекулы подразделяются на: линейные, схематически обозначаемые -АА-А-, (например, каучук натуральный); разветвленные, имеющие боковые ответвления (например, амилопектин); сетчатые или сшитые, если соседние макромолекулы соединены поперечными химическими связями (например, отвержденные эпоксидные смолы). Сильно сшитые полимеры нерастворимы, неплавки и неспособны к высокоэластическим деформациям.
Строение По строению макромолекулы подразделяются на: линейные, схематически обозначаемые -АА-А-, (например, каучук натуральный); разветвленные, имеющие боковые ответвления (например, амилопектин); сетчатые или сшитые, если соседние макромолекулы соединены поперечными химическими связями (например, отвержденные эпоксидные смолы). Сильно сшитые полимеры нерастворимы, неплавки и неспособны к высокоэластическим деформациям.
 Реакция полимеризации Реакцию образования полимера из мономера называют полимеризацией. В процессе полимеризации вещество может переходить из газообразного или жидкого состояния в состояние весьма густой жидкости или твердое. Реакция полимеризации не сопровождается отщеплением каких-либо низкомолекулярных побочных продуктов. При полимеризации полимер и мономер характеризуются одинаковым элементным составом.
Реакция полимеризации Реакцию образования полимера из мономера называют полимеризацией. В процессе полимеризации вещество может переходить из газообразного или жидкого состояния в состояние весьма густой жидкости или твердое. Реакция полимеризации не сопровождается отщеплением каких-либо низкомолекулярных побочных продуктов. При полимеризации полимер и мономер характеризуются одинаковым элементным составом.
 Получение полипропилена n СН 2 = СН → (- СН 2 – СН-)n | | СН 3 пропилен полипропилен Выражение в скобках называют Структурным звеном, число n в формуле полимера – степенью полимеризации.
Получение полипропилена n СН 2 = СН → (- СН 2 – СН-)n | | СН 3 пропилен полипропилен Выражение в скобках называют Структурным звеном, число n в формуле полимера – степенью полимеризации.
 Применение полимеров Благодаря механической прочности, эластичности, электроизоляционным и другим свойствам изделия из полимеров применяют в различных отраслях промышленности и в быту. Основные типы полимерных материалов — пластические массы, резины, волокна, лаки, краски, клеи, ионообменные смолы. В технике полимеры нашли широкое применение в качестве электроизоляционных и конструкционных материалов.
Применение полимеров Благодаря механической прочности, эластичности, электроизоляционным и другим свойствам изделия из полимеров применяют в различных отраслях промышленности и в быту. Основные типы полимерных материалов — пластические массы, резины, волокна, лаки, краски, клеи, ионообменные смолы. В технике полимеры нашли широкое применение в качестве электроизоляционных и конструкционных материалов.
 Контрольная работа 1. Какие признаки отличают полимеры от низкомолекулярных соединений: а) плохая растворимость; е) эластичность; б) набухание при растворении; ж) низкая хрупкость; в) низкая вязкость растворов; з) термопластичность; г) высокая вязкость растворов; и) термореактивность; д) неспособность к кристаллизации; к) электропроводность? Ответ 1 : б, г, е, ж Ответ 2 : а, б, д, з, и, к Ответ 3 : б, г, д, е, з, и Ответ 4 : а, б, в, ж, к
Контрольная работа 1. Какие признаки отличают полимеры от низкомолекулярных соединений: а) плохая растворимость; е) эластичность; б) набухание при растворении; ж) низкая хрупкость; в) низкая вязкость растворов; з) термопластичность; г) высокая вязкость растворов; и) термореактивность; д) неспособность к кристаллизации; к) электропроводность? Ответ 1 : б, г, е, ж Ответ 2 : а, б, д, з, и, к Ответ 3 : б, г, д, е, з, и Ответ 4 : а, б, в, ж, к
 Контрольная работа Какие свойства полимеров можно объяснить гибкостью макромолекул: а) высокая температура разложения; б) эластичность каучуков; в) прочность органических стекол; г) горючесть ? Ответ 1 : а, б Ответ 2 : а, г Ответ 3 : а, б, в Ответ 4 : б, в Ответ 5 : все перечисленные свойства
Контрольная работа Какие свойства полимеров можно объяснить гибкостью макромолекул: а) высокая температура разложения; б) эластичность каучуков; в) прочность органических стекол; г) горючесть ? Ответ 1 : а, б Ответ 2 : а, г Ответ 3 : а, б, в Ответ 4 : б, в Ответ 5 : все перечисленные свойства
 Контрольная работа Какие полимеры могут использоваться в производстве волокон? Ответ 1 : любые, независимо от гибкости макромолекул Ответ 2 : линейные, гибкоцепные Ответ 3 : пространственные, жесткоцепные Ответ 4 : линейные, жесткоцепные Ответ 5 : линейные и разветвленные, гибкоцепные
Контрольная работа Какие полимеры могут использоваться в производстве волокон? Ответ 1 : любые, независимо от гибкости макромолекул Ответ 2 : линейные, гибкоцепные Ответ 3 : пространственные, жесткоцепные Ответ 4 : линейные, жесткоцепные Ответ 5 : линейные и разветвленные, гибкоцепные


