Лектор: Малышева Жанна Николаевна Кандидат химических































1 закон термодинамики.ppt
- Количество слайдов: 34
 Лектор: Малышева Жанна Николаевна Кандидат химических наук , доцент кафедры ФАХП, профессор РАЕ. Дисциплина: Физическая химия 1
Лектор: Малышева Жанна Николаевна Кандидат химических наук , доцент кафедры ФАХП, профессор РАЕ. Дисциплина: Физическая химия 1
 Литература: 1. Стромберг А. Г. , Семченко Д. М. Физическая химия. Учебник для студентов химико-технологичеких специальностей ВУЗов. –М. : Высшая школа, 1988. – 495 с. 2. Кудряшов И. В. , Каретников Г. С. Сборник примеров и задач по физической химии. – М. : Высшая школа, 1991 (1983). – 527 с. 3. Краткий справочник физико- химических величин/ под ред. А. А. Равделя и А. М. Пономаревой. – Л. : Химия, 1983 г.
Литература: 1. Стромберг А. Г. , Семченко Д. М. Физическая химия. Учебник для студентов химико-технологичеких специальностей ВУЗов. –М. : Высшая школа, 1988. – 495 с. 2. Кудряшов И. В. , Каретников Г. С. Сборник примеров и задач по физической химии. – М. : Высшая школа, 1991 (1983). – 527 с. 3. Краткий справочник физико- химических величин/ под ред. А. А. Равделя и А. М. Пономаревой. – Л. : Химия, 1983 г.
 Организация обучения и итоги: 1. Лекции – 36 ч. 2. Лабораторно-практические занятия – 36 ч. допуски на ЭВМ + 7 лаб. работ беседа с преподавателем коллоквиумы(отчеты) 3. Семестровые задания-2 4. Теоретический зачет
Организация обучения и итоги: 1. Лекции – 36 ч. 2. Лабораторно-практические занятия – 36 ч. допуски на ЭВМ + 7 лаб. работ беседа с преподавателем коллоквиумы(отчеты) 3. Семестровые задания-2 4. Теоретический зачет
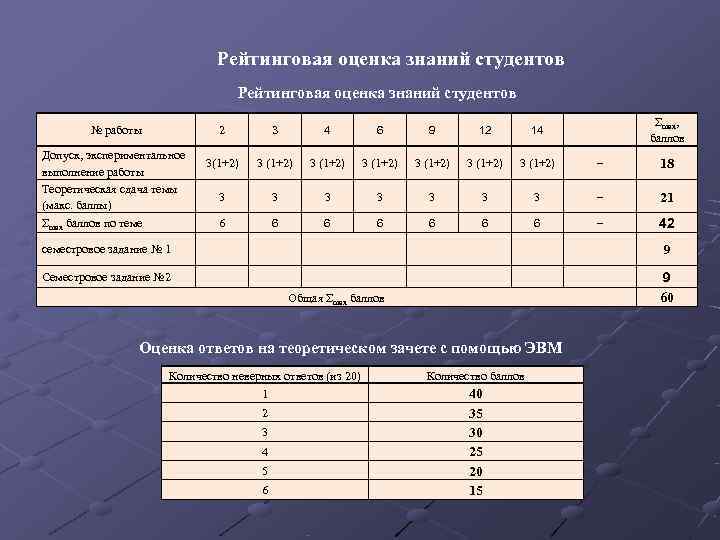
 Рейтинговая оценка знаний студентов Σmaх, № работы 2 3 4 6 9 12 14 баллов Допуск, экспериментальное 3(1+2) 3 (1+2) 3 (1+2) – 18 выполнение работы Теоретическая сдача темы 3 3 – 21 (макс. баллы) Σmax баллов по теме 6 6 – 42 семестровое задание № 1 9 Семестровое задание № 2 9 Общая Σmax баллов 60 Оценка ответов на теоретическом зачете с помощью ЭВМ Количество неверных ответов (из 20) Количество баллов 1 40 2 35 3 30 4 25 20 6 15
Рейтинговая оценка знаний студентов Σmaх, № работы 2 3 4 6 9 12 14 баллов Допуск, экспериментальное 3(1+2) 3 (1+2) 3 (1+2) – 18 выполнение работы Теоретическая сдача темы 3 3 – 21 (макс. баллы) Σmax баллов по теме 6 6 – 42 семестровое задание № 1 9 Семестровое задание № 2 9 Общая Σmax баллов 60 Оценка ответов на теоретическом зачете с помощью ЭВМ Количество неверных ответов (из 20) Количество баллов 1 40 2 35 3 30 4 25 20 6 15
 Физическая химия – есть наука, объясняющая на основании положений и опытов физики о том, что происходит в смешанных телах при химических операциях. 1752 г. - первая формулировка физической химии «Живая биологическая клетка похожа на физико-химическую Лабораторию и от нее надо ждать всех тех же явлений, кото- рые бывают при физико-химических процессах. » И. П. Павлов 5
Физическая химия – есть наука, объясняющая на основании положений и опытов физики о том, что происходит в смешанных телах при химических операциях. 1752 г. - первая формулировка физической химии «Живая биологическая клетка похожа на физико-химическую Лабораторию и от нее надо ждать всех тех же явлений, кото- рые бывают при физико-химических процессах. » И. П. Павлов 5
 Современное определение – наука, объясняющая химические явления на основе общих принципов физики. Относится к фундаментальным наукам. Она обобщает реальные явления и представляет их в виде закономерностей, которые характеризуют условия протекания процессов в различных отраслях промышленного и сельскохозяйственного производства, природных явлениях и жизнедеятельности живых организмов. Физическую химию живых биосистем изучает биофизика. 6
Современное определение – наука, объясняющая химические явления на основе общих принципов физики. Относится к фундаментальным наукам. Она обобщает реальные явления и представляет их в виде закономерностей, которые характеризуют условия протекания процессов в различных отраслях промышленного и сельскохозяйственного производства, природных явлениях и жизнедеятельности живых организмов. Физическую химию живых биосистем изучает биофизика. 6
 Основная задача – предсказание возможности, направления и конечного результата протекания химических реакций. Это дает возможность управлять химическими процессами, обеспечивая их полное и быстрое протекание 7
Основная задача – предсказание возможности, направления и конечного результата протекания химических реакций. Это дает возможность управлять химическими процессами, обеспечивая их полное и быстрое протекание 7
 Основные разделы курса 1) Строение вещества 2) Химическая термодинамика Применяет законы общей термодинамики к изучению химических реакций +Термохимия – учение о теплотах химических Строение атомов, реакций молекул, агрегатные состояния веществ При изучении биосистем термодинамика (не изучается, рассматривается Позволяет оценить вероятность протекания в курсе физики) Процессов по тому или иному механизму, что способствует лучшему пониманию биопроцессов. 8
Основные разделы курса 1) Строение вещества 2) Химическая термодинамика Применяет законы общей термодинамики к изучению химических реакций +Термохимия – учение о теплотах химических Строение атомов, реакций молекул, агрегатные состояния веществ При изучении биосистем термодинамика (не изучается, рассматривается Позволяет оценить вероятность протекания в курсе физики) Процессов по тому или иному механизму, что способствует лучшему пониманию биопроцессов. 8
 Основные разделы курса 3) Учение о растворах 4) Электрохимия Структура и свойства растворов Растворы электролитов неэлектролитов +Электродные процессы Определение окислительно- восстановительных потенциалов в биологических объектах. 9
Основные разделы курса 3) Учение о растворах 4) Электрохимия Структура и свойства растворов Растворы электролитов неэлектролитов +Электродные процессы Определение окислительно- восстановительных потенциалов в биологических объектах. 9
 Основные разделы курса 5) Химическая кинетика + катализ (в том числе ферментативный) Скорость химических реакций(C, P, T, катализатор), а так же скорости биологических процессов 10
Основные разделы курса 5) Химическая кинетика + катализ (в том числе ферментативный) Скорость химических реакций(C, P, T, катализатор), а так же скорости биологических процессов 10
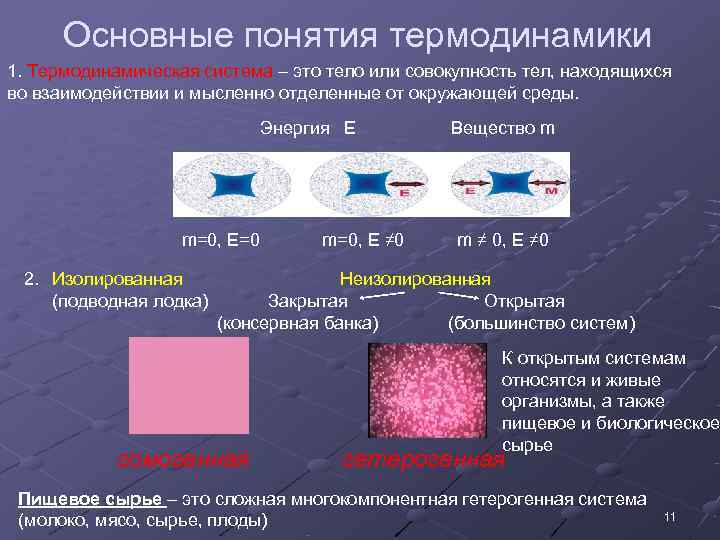
 Основные понятия термодинамики 1. Термодинамическая система – это тело или совокупность тел, находящихся во взаимодействии и мысленно отделенные от окружающей среды. Энергия Е Вещество m m=0, Е=0 m=0, Е ≠ 0 m ≠ 0, Е ≠ 0 2. Изолированная Неизолированная (подводная лодка) Закрытая Открытая (консервная банка) (большинство систем) К открытым системам относятся и живые организмы, а также пищевое и биологическое сырье гомогенная гетерогенная Пищевое сырье – это сложная многокомпонентная гетерогенная система (молоко, мясо, сырье, плоды) 11
Основные понятия термодинамики 1. Термодинамическая система – это тело или совокупность тел, находящихся во взаимодействии и мысленно отделенные от окружающей среды. Энергия Е Вещество m m=0, Е=0 m=0, Е ≠ 0 m ≠ 0, Е ≠ 0 2. Изолированная Неизолированная (подводная лодка) Закрытая Открытая (консервная банка) (большинство систем) К открытым системам относятся и живые организмы, а также пищевое и биологическое сырье гомогенная гетерогенная Пищевое сырье – это сложная многокомпонентная гетерогенная система (молоко, мясо, сырье, плоды) 11
 3. Термодинамические параметры – совокупность свойств, определяющих состояние системы. ЭКСТЕНСИВНЫЕ Зависят от массы вещества, количества частиц ИНТЕНСИВНЫЕ Не зависят от массы вещества 12
3. Термодинамические параметры – совокупность свойств, определяющих состояние системы. ЭКСТЕНСИВНЫЕ Зависят от массы вещества, количества частиц ИНТЕНСИВНЫЕ Не зависят от массы вещества 12
 4. Термодинамический процесс – это изменение в системе, вызванное изменением термодинамических параметров. 5. Круговой процесс (цикл) – процесс, при котором система возвращается в исходное состояние 6. Внутренняя энергия – совокупность всех видов энергий, которыми обладает система(экстенсивная величина) - изменение внутренней энергии. Абсолютное значение u не известно, но для химической реакции достаточно знать ∆u Важное свойство -функция состояния (вводится для удобства изучения идеальных и реальных процессов). 7. Функция состояния – это термодинамический параметр, изменение которого не зависит от пути перехода из начального в конечное состояние, а зависит только от начального и конечного состояния системы. Функция перехода – это параметр, зависящий от пути перехода из начального в конечное состояние. 8. Q – теплота, A – работа. Формы передачи энергии. - в общем случае теплота и работа являются функциями перехода, а при определенных условиях функция приобретают свойства функции состояния. . 13
4. Термодинамический процесс – это изменение в системе, вызванное изменением термодинамических параметров. 5. Круговой процесс (цикл) – процесс, при котором система возвращается в исходное состояние 6. Внутренняя энергия – совокупность всех видов энергий, которыми обладает система(экстенсивная величина) - изменение внутренней энергии. Абсолютное значение u не известно, но для химической реакции достаточно знать ∆u Важное свойство -функция состояния (вводится для удобства изучения идеальных и реальных процессов). 7. Функция состояния – это термодинамический параметр, изменение которого не зависит от пути перехода из начального в конечное состояние, а зависит только от начального и конечного состояния системы. Функция перехода – это параметр, зависящий от пути перехода из начального в конечное состояние. 8. Q – теплота, A – работа. Формы передачи энергии. - в общем случае теплота и работа являются функциями перехода, а при определенных условиях функция приобретают свойства функции состояния. . 13
 Свойства функции состояния: 1. - изменение зависит от состояния 2. изменение является полным дифференциалом 3. при циклическом процессе функция не изменяется (если интеграл по замкнутому контуру равен 0, то подинтегральное выражение является полным дифференциалом функции состояния) 14
Свойства функции состояния: 1. - изменение зависит от состояния 2. изменение является полным дифференциалом 3. при циклическом процессе функция не изменяется (если интеграл по замкнутому контуру равен 0, то подинтегральное выражение является полным дифференциалом функции состояния) 14
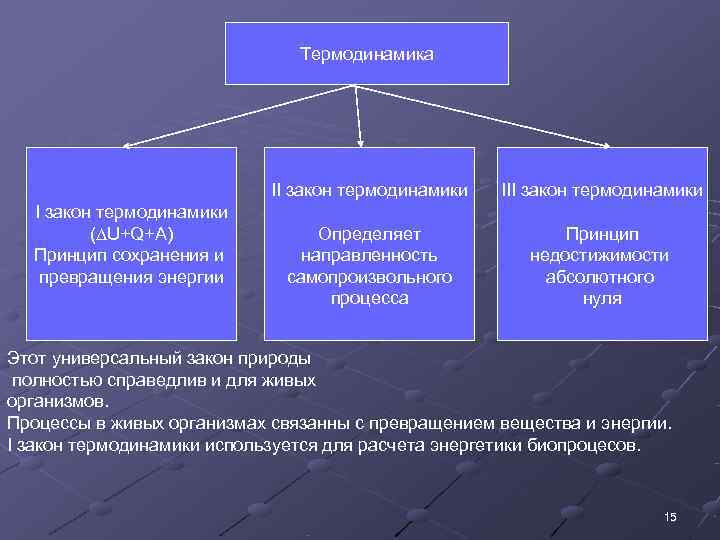
 Термодинамика II закон термодинамики (∆U+Q+A) Определяет Принцип сохранения и направленность недостижимости превращения энергии самопроизвольного абсолютного процесса нуля Этот универсальный закон природы полностью справедлив и для живых организмов. Процессы в живых организмах связанны с превращением вещества и энергии. I закон термодинамики используется для расчета энергетики биопроцесов. 15
Термодинамика II закон термодинамики (∆U+Q+A) Определяет Принцип сохранения и направленность недостижимости превращения энергии самопроизвольного абсолютного процесса нуля Этот универсальный закон природы полностью справедлив и для живых организмов. Процессы в живых организмах связанны с превращением вещества и энергии. I закон термодинамики используется для расчета энергетики биопроцесов. 15
 I закон термодинамики Формулировки: 1. Энергия не возникает из ничего и не исчезает бесследно. Если исчезает один вид энергии, то взамен появляется другой. 2. Различные виды энергии переходят друг в друга в строго эквивалентных количествах 3. В изолированной системе общий запас энергии остается постоянным 16
I закон термодинамики Формулировки: 1. Энергия не возникает из ничего и не исчезает бесследно. Если исчезает один вид энергии, то взамен появляется другой. 2. Различные виды энергии переходят друг в друга в строго эквивалентных количествах 3. В изолированной системе общий запас энергии остается постоянным 16
 Математическая трактовка I закона термодинамики Интегральная Дифференц. форма форма ∂A, ∂Q - бесконечно малые величины Q и A, т. к. это функции перехода, d. U- полный дифференциал U, т. к. она функция состояния. 17
Математическая трактовка I закона термодинамики Интегральная Дифференц. форма форма ∂A, ∂Q - бесконечно малые величины Q и A, т. к. это функции перехода, d. U- полный дифференциал U, т. к. она функция состояния. 17
 - сумма всех элементарных работ, совершаемых системой. Если отсутствуют все виды работ, кроме работы расширения. то имеем уравнение (6) когда , тогда . Выражения для работы в различных процессах. 1. Изобарный Совершается наибольшая работа. 18
- сумма всех элементарных работ, совершаемых системой. Если отсутствуют все виды работ, кроме работы расширения. то имеем уравнение (6) когда , тогда . Выражения для работы в различных процессах. 1. Изобарный Совершается наибольшая работа. 18
 2. Изохорный (v=const) Работа отсутствует. 3. Изотермический (T=const) 19
2. Изохорный (v=const) Работа отсутствует. 3. Изотермический (T=const) 19
 4. Адиабатический (Q=0, δQ=0) 1 изобара (А – max) P 3 изотерма 4 адиабата 2 изохора V Работа Отсутствует Аизоб > Аизот > Аидиаб 20
4. Адиабатический (Q=0, δQ=0) 1 изобара (А – max) P 3 изотерма 4 адиабата 2 изохора V Работа Отсутствует Аизоб > Аизот > Аидиаб 20
 Следствие из I закона термодинамики (для практически важных процессов) Из (7) и (9) => теплота становится функцией состояния для двух частных случаев (v, p=const) Он является следствием I закона термодинамики. (7) и (9) – математические выражения закона Гесса – основного закона термохимии. Тепловой эффект не зависит от пути протекания, а зависит только от исходного и конечного состояния системы. (P и V=const) 21
Следствие из I закона термодинамики (для практически важных процессов) Из (7) и (9) => теплота становится функцией состояния для двух частных случаев (v, p=const) Он является следствием I закона термодинамики. (7) и (9) – математические выражения закона Гесса – основного закона термохимии. Тепловой эффект не зависит от пути протекания, а зависит только от исходного и конечного состояния системы. (P и V=const) 21
 Закон Г. И. Гесса (открыт в 1840 г) При постоянном давлении и объеме тепловой эффект химической реакции зависит только от вида и состояния исходных веществ и продуктов реакции, но не зависит от промежуточных состояний. Герман Иванович Гесс – российский химик, Формулировка Гесса академик Петербуржской Академии наук. 22
Закон Г. И. Гесса (открыт в 1840 г) При постоянном давлении и объеме тепловой эффект химической реакции зависит только от вида и состояния исходных веществ и продуктов реакции, но не зависит от промежуточных состояний. Герман Иванович Гесс – российский химик, Формулировка Гесса академик Петербуржской Академии наук. 22
 +Q -Q 23
+Q -Q 23
 Применение закона Гесса для расчета тепловых эффектов химических реакций Путь расчетов: 1. Необходимо определить какие алгебраические действия надо провести с уравнениями. 2. Совершая аналогичные алгебраические действия с тепловыми эффектами получаем искомую величину 24
Применение закона Гесса для расчета тепловых эффектов химических реакций Путь расчетов: 1. Необходимо определить какие алгебраические действия надо провести с уравнениями. 2. Совершая аналогичные алгебраические действия с тепловыми эффектами получаем искомую величину 24
 Стандартные условия: 2. P=1 атм (1 бар) или 105 Па. при заданной температуре T, если Т=298, то это – справочные данные 1. Расчеты по теплотам образования. Теплота образования – это тепловой эффект образования 1 моля соединение из соответствующих простых веществ (С, N 2, , H 2, O 2 ) обозначается Реакция образования: Для простых веществ f- «formation» Для расчета тепловых эффектов химической реакции пользуются правилом, которое является следствием закона Гесса. Тепловой эффект химической реакции равен разности тепловых эффектов образования продуктов и исходных веществ с учетом стехиометрических коэффициентов. 25
Стандартные условия: 2. P=1 атм (1 бар) или 105 Па. при заданной температуре T, если Т=298, то это – справочные данные 1. Расчеты по теплотам образования. Теплота образования – это тепловой эффект образования 1 моля соединение из соответствующих простых веществ (С, N 2, , H 2, O 2 ) обозначается Реакция образования: Для простых веществ f- «formation» Для расчета тепловых эффектов химической реакции пользуются правилом, которое является следствием закона Гесса. Тепловой эффект химической реакции равен разности тепловых эффектов образования продуктов и исходных веществ с учетом стехиометрических коэффициентов. 25
 2. Расчет по теплотам сгорания Теплота сгорания – это тепловой эффект сгорания (окисления) 1 моля вещества до продуктов полного окисления (CO 2, H 20, Cl 2, N 2, SO 2). Обозначается: или Реакция горения: Расчетное уравнение для реакции Тепловой эффект химической реакции равен разности тепловых эффектов сгорания исходных веществ и продуктов реакции с учетом стехиометрических коэффициентов. 26
2. Расчет по теплотам сгорания Теплота сгорания – это тепловой эффект сгорания (окисления) 1 моля вещества до продуктов полного окисления (CO 2, H 20, Cl 2, N 2, SO 2). Обозначается: или Реакция горения: Расчетное уравнение для реакции Тепловой эффект химической реакции равен разности тепловых эффектов сгорания исходных веществ и продуктов реакции с учетом стехиометрических коэффициентов. 26
 3. Расчеты по теплотам растворения Интегральная теплота растворения – это тепловой эффект растворения 1 моля соединения в чистом растворителе (∆Нm). Расчет теплот разбавления: 4. Расчеты по энергиям связи Энергией связи (A-B) называется энергия необходимая для разрыва связи и разведения частиц на бесконечное состояние AB(Г)->A(Г)+B(Г) Тепловой эффект химической реакции равен разности энергии разрываемых связей (исх) и образующихся(прод) с учетами стехиометрических коэффициентов 27
3. Расчеты по теплотам растворения Интегральная теплота растворения – это тепловой эффект растворения 1 моля соединения в чистом растворителе (∆Нm). Расчет теплот разбавления: 4. Расчеты по энергиям связи Энергией связи (A-B) называется энергия необходимая для разрыва связи и разведения частиц на бесконечное состояние AB(Г)->A(Г)+B(Г) Тепловой эффект химической реакции равен разности энергии разрываемых связей (исх) и образующихся(прод) с учетами стехиометрических коэффициентов 27
 Теплоёмкость. Из I закона термодинамики - 28
Теплоёмкость. Из I закона термодинамики - 28
 Для простых твердых веществ атомная теплоемкость постоянна (закон Дюлонга и Пти). Для соединений молярная теплоемкость равна сумме теплоемкостей атомов n , входящих в молекулы (закон Коппа-Неймана). Ср = n 25 Дж/моль К При больших разностях T нужно учитывать c=f(t). 29
Для простых твердых веществ атомная теплоемкость постоянна (закон Дюлонга и Пти). Для соединений молярная теплоемкость равна сумме теплоемкостей атомов n , входящих в молекулы (закон Коппа-Неймана). Ср = n 25 Дж/моль К При больших разностях T нужно учитывать c=f(t). 29
 Зависимость теплового эффекта от температуры. Закон Кирхгофа. Из закона Гесса: ∆Ср>0 ∆Н ∆Ср=0 ∆Ср<0 Температурный коэффициент теплового эффекта равен изменению теплоемкости системы (7) И (9) – дифференциальные формы Кирхгофа при протекании реакции (при V, P=const) 30
Зависимость теплового эффекта от температуры. Закон Кирхгофа. Из закона Гесса: ∆Ср>0 ∆Н ∆Ср=0 ∆Ср<0 Температурный коэффициент теплового эффекта равен изменению теплоемкости системы (7) И (9) – дифференциальные формы Кирхгофа при протекании реакции (при V, P=const) 30
 31
31
 Расчетное уравнение для определения тепловых эффектов реакции при температуре T. глюкоза Термохимия Такая же теплота образуется не только при сжигании позволяет вне организма, но и при биохимическом превращении составлять баланс её в самом организме – «глюкозе» (через 12 промежуточных стадий). энергии Это означает, что организм не является источником в живом организме новой энергии, а подчиняется I закону термодинамики. 32
Расчетное уравнение для определения тепловых эффектов реакции при температуре T. глюкоза Термохимия Такая же теплота образуется не только при сжигании позволяет вне организма, но и при биохимическом превращении составлять баланс её в самом организме – «глюкозе» (через 12 промежуточных стадий). энергии Это означает, что организм не является источником в живом организме новой энергии, а подчиняется I закону термодинамики. 32
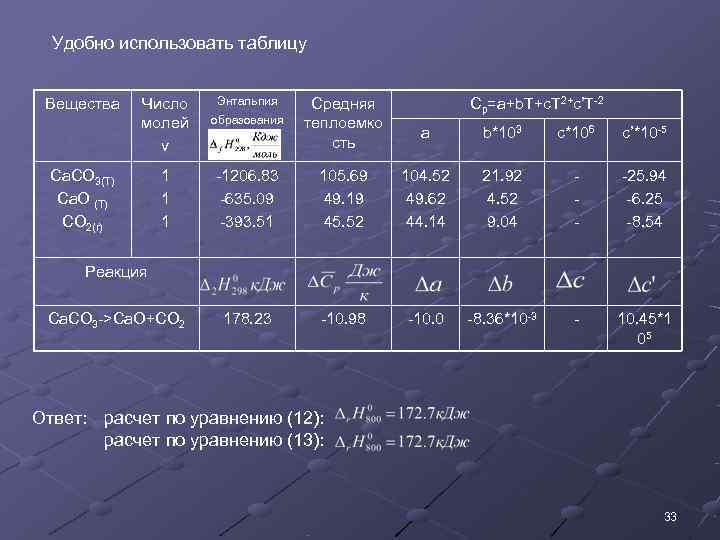
 Удобно использовать таблицу Вещества Число Энтальпия Средняя Cp=a+b. T+c. T 2+c’T-2 молей образования теплоемко a b*103 c*106 c’*10 -5 v сть Ca. CO 3(T) 1 -1206. 83 105. 69 104. 52 21. 92 - -25. 94 Ca. O (T) 1 -635. 09 49. 19 49. 62 4. 52 - -6. 25 CO 2(r) 1 -393. 51 45. 52 44. 14 9. 04 - -8. 54 Реакция Ca. CO 3 ->Ca. O+CO 2 178. 23 -10. 98 -10. 0 -8. 36*10 -3 - 10. 45*1 05 Ответ: расчет по уравнению (12): расчет по уравнению (13): 33
Удобно использовать таблицу Вещества Число Энтальпия Средняя Cp=a+b. T+c. T 2+c’T-2 молей образования теплоемко a b*103 c*106 c’*10 -5 v сть Ca. CO 3(T) 1 -1206. 83 105. 69 104. 52 21. 92 - -25. 94 Ca. O (T) 1 -635. 09 49. 19 49. 62 4. 52 - -6. 25 CO 2(r) 1 -393. 51 45. 52 44. 14 9. 04 - -8. 54 Реакция Ca. CO 3 ->Ca. O+CO 2 178. 23 -10. 98 -10. 0 -8. 36*10 -3 - 10. 45*1 05 Ответ: расчет по уравнению (12): расчет по уравнению (13): 33
 Термодинамика дает ответ о возможности протекания процесса, но часто в реальных условиях такой процесс не идет. Например: С + О 2 → СО 2 ∆G = -393, 06 к. Дж/моль (процесс протекает самопроизвольно) Однако в реальных условиях этот процесс не идет. Чтобы он пошел нужно создать условия для увеличения скорости, т. е. кинетики. Часто и многие биологические реакции термодинамически возможны, но чтобы обеспечить достаточную скорость необходим биокатализатор (ферменты). Вопросы, решаемые химической кинетикой исключительно важные для биосистем. С ее помощью можно установить основные параметры таких процессов, как брожение пива, созревание сыров, прогоркание жиров и т. д. , а так же влиять на них, совершенствовать и развивать новые технологии. Развитие жизни на Земле связано с реакциями, которые являются эндотермическими и для них , но под действием света течение таких реакции становится возможным кинетически (фотосинтез).
Термодинамика дает ответ о возможности протекания процесса, но часто в реальных условиях такой процесс не идет. Например: С + О 2 → СО 2 ∆G = -393, 06 к. Дж/моль (процесс протекает самопроизвольно) Однако в реальных условиях этот процесс не идет. Чтобы он пошел нужно создать условия для увеличения скорости, т. е. кинетики. Часто и многие биологические реакции термодинамически возможны, но чтобы обеспечить достаточную скорость необходим биокатализатор (ферменты). Вопросы, решаемые химической кинетикой исключительно важные для биосистем. С ее помощью можно установить основные параметры таких процессов, как брожение пива, созревание сыров, прогоркание жиров и т. д. , а так же влиять на них, совершенствовать и развивать новые технологии. Развитие жизни на Земле связано с реакциями, которые являются эндотермическими и для них , но под действием света течение таких реакции становится возможным кинетически (фотосинтез).

