Лекция 1 Газовые законы.ppt
- Количество слайдов: 20
 Лектор и автор курса: Журавлева Людмила Анатольевна Кандидат химических наук, доцент Кафедра химии Института естественных и технических наук Сур. ГУ
Лектор и автор курса: Журавлева Людмила Анатольевна Кандидат химических наук, доцент Кафедра химии Института естественных и технических наук Сур. ГУ
 литература: 1. ЭБС издательства «Лань» : Кругляков, П. М. Физическая и коллоидная химия. Практикум / П. М. Кругляков, А. В. Нуштаева, Н. Г. Вилкова, Н. В. Кошева. - СПб. : Лань, 2013. — 288 с. — ISBN 978 -5 -8114 -1376 -8 2. Шершавина, Алла Александровна. Физическая и коллоидная химия : методы физико-химического анализа : учебное пособие / А. А. Шершавина. — М. : Новое знание, 2005. — 799 с. 3. Физическая и коллоидная химия : учебник / А. П. Беляев и др. ; под ред. А. П. Беляева. — М. : ГЭОТАР-Медиа, 2008. — 700 с. 4. Журавлева, Людмила Анатольевна. Физическая и коллоидная химия : учебно- методическое пособие / Л. А. Журавлева, Е. Б. Чернов. — Сургут : Издательский центр Сур. ГУ, 2010 - Ч. 1. — Сургут : Издательский центр Сур. ГУ, 2010. — 110 с. 5. Беляев, Алексей Петрович. Физическая и коллоидная химия : учебник / А. П. Беляев, В. И. Кучук ; под ред. А. П. Беляева ; Министерство образования и науки РФ. — 2 -е изд. , перераб. и доп. — Москва : ГЭОТАР-Медиа, 2014. -751 с.
литература: 1. ЭБС издательства «Лань» : Кругляков, П. М. Физическая и коллоидная химия. Практикум / П. М. Кругляков, А. В. Нуштаева, Н. Г. Вилкова, Н. В. Кошева. - СПб. : Лань, 2013. — 288 с. — ISBN 978 -5 -8114 -1376 -8 2. Шершавина, Алла Александровна. Физическая и коллоидная химия : методы физико-химического анализа : учебное пособие / А. А. Шершавина. — М. : Новое знание, 2005. — 799 с. 3. Физическая и коллоидная химия : учебник / А. П. Беляев и др. ; под ред. А. П. Беляева. — М. : ГЭОТАР-Медиа, 2008. — 700 с. 4. Журавлева, Людмила Анатольевна. Физическая и коллоидная химия : учебно- методическое пособие / Л. А. Журавлева, Е. Б. Чернов. — Сургут : Издательский центр Сур. ГУ, 2010 - Ч. 1. — Сургут : Издательский центр Сур. ГУ, 2010. — 110 с. 5. Беляев, Алексей Петрович. Физическая и коллоидная химия : учебник / А. П. Беляев, В. И. Кучук ; под ред. А. П. Беляева ; Министерство образования и науки РФ. — 2 -е изд. , перераб. и доп. — Москва : ГЭОТАР-Медиа, 2014. -751 с.
 6. Ипполитов, Евгений Георгиевич. Физическая химия : учебник для студентов высших учебных заведений / Е. Г. Ипполитов, А. В. Артемов, В. В. Батраков ; под ред. Е. Г. Ипполитова. — М. : Academia, 2005. — 447 с. 7. Тиноко, И. Физическая химия. Принципы и применение в биологических науках / И. Тиноко, К. Зауэр, Дж. Вэнг, Дж. Паглиси ; пер. с англ. Е. Р. Разумовой ; под ред. В. И. Горшкова. — М. : Техносфера, 2005. — 743 с. 8. Беляев, Алексей Петрович. Физическая и коллоидная химия : учебник для студентов / А. П. Беляев, В. И. Кучук ; под ред. А. П. Беляева ; Министерство образования и науки РФ . — 2 -е изд. , перераб. и доп. — Москва : ГЭОТАР-Медиа, 2014. — 751 с. 9. Воронцова, Нина Васильевна. Коллоидная химия : учебно-методическое пособие / Н. Воронцова, Л. А. Журавлева ; Департамент образования и науки Ханты-Мансийского автономного округа - Югры, ГОУ ВПО "Сургутский государственный университет Ханты-Мансийского автономного округа - Югры", Кафедра химии. — Сургут : Издательский центр Сур. ГУ, 2010. — 115 с. 10. Журавлева, Людмила Анатольевна, Практикум по коллоидной химии : учебное пособие / Л. А. Журавлева, Н. Воронцова. — Сургут : Издательский центр Сур. ГУ, 2011. — 161 с.
6. Ипполитов, Евгений Георгиевич. Физическая химия : учебник для студентов высших учебных заведений / Е. Г. Ипполитов, А. В. Артемов, В. В. Батраков ; под ред. Е. Г. Ипполитова. — М. : Academia, 2005. — 447 с. 7. Тиноко, И. Физическая химия. Принципы и применение в биологических науках / И. Тиноко, К. Зауэр, Дж. Вэнг, Дж. Паглиси ; пер. с англ. Е. Р. Разумовой ; под ред. В. И. Горшкова. — М. : Техносфера, 2005. — 743 с. 8. Беляев, Алексей Петрович. Физическая и коллоидная химия : учебник для студентов / А. П. Беляев, В. И. Кучук ; под ред. А. П. Беляева ; Министерство образования и науки РФ . — 2 -е изд. , перераб. и доп. — Москва : ГЭОТАР-Медиа, 2014. — 751 с. 9. Воронцова, Нина Васильевна. Коллоидная химия : учебно-методическое пособие / Н. Воронцова, Л. А. Журавлева ; Департамент образования и науки Ханты-Мансийского автономного округа - Югры, ГОУ ВПО "Сургутский государственный университет Ханты-Мансийского автономного округа - Югры", Кафедра химии. — Сургут : Издательский центр Сур. ГУ, 2010. — 115 с. 10. Журавлева, Людмила Анатольевна, Практикум по коллоидной химии : учебное пособие / Л. А. Журавлева, Н. Воронцова. — Сургут : Издательский центр Сур. ГУ, 2011. — 161 с.
 Лекция 1 Важнейшие понятия химии. Агрегатные состояния веществ. Газовые законы для идеальных и реальных газов
Лекция 1 Важнейшие понятия химии. Агрегатные состояния веществ. Газовые законы для идеальных и реальных газов
 Физическая химия – это наука о применении физических законов к физическим явлениям и химическим процессам. Объектом изучения физической химии являются системы. Система – это любая выбранная совокупность веществ, отделенная от внешней среды поверхностью раздела, часто воображаемой. Системы делятся : - изолированные - нет обмена с окружающей средой ни энергией, ни веществом (термос, сосуд Дьюара); - закрытые – это системы, которые обмениваются с окружающей средой энергией (Е), но не обменивается веществом (чайник, система отопления); - открытая - это система, которая обменивается с окружающей средой и энергией и веществом (живой организм). Наука развивается путем идеализации , что позволяет сформулировать законы и эмпирические формулы , которые хорошо описывают явления и процессы, протекающие в данных системах.
Физическая химия – это наука о применении физических законов к физическим явлениям и химическим процессам. Объектом изучения физической химии являются системы. Система – это любая выбранная совокупность веществ, отделенная от внешней среды поверхностью раздела, часто воображаемой. Системы делятся : - изолированные - нет обмена с окружающей средой ни энергией, ни веществом (термос, сосуд Дьюара); - закрытые – это системы, которые обмениваются с окружающей средой энергией (Е), но не обменивается веществом (чайник, система отопления); - открытая - это система, которая обменивается с окружающей средой и энергией и веществом (живой организм). Наука развивается путем идеализации , что позволяет сформулировать законы и эмпирические формулы , которые хорошо описывают явления и процессы, протекающие в данных системах.
 Характеристика систем: Равновесные - это системы, в которых важнейшие параметры не меняются во времени. Это равновесие динамическое, т. е. параметры меняются в противоположных направлениях; Неравновесные – это системы, важнейшие параметры которых меняются в одном направлении; Гомогенные - это однородные системы, состоящие из одной фазы, т. е. системы, в которых дисперсная фаза и дисперсионная среда не имеют поверхности раздела; Гетерогенные - это системы, состоящие из нескольких фаз, т. е. системы, в которых дисперсная фаза и дисперсионная среда имеют поверхность раздела.
Характеристика систем: Равновесные - это системы, в которых важнейшие параметры не меняются во времени. Это равновесие динамическое, т. е. параметры меняются в противоположных направлениях; Неравновесные – это системы, важнейшие параметры которых меняются в одном направлении; Гомогенные - это однородные системы, состоящие из одной фазы, т. е. системы, в которых дисперсная фаза и дисперсионная среда не имеют поверхности раздела; Гетерогенные - это системы, состоящие из нескольких фаз, т. е. системы, в которых дисперсная фаза и дисперсионная среда имеют поверхность раздела.

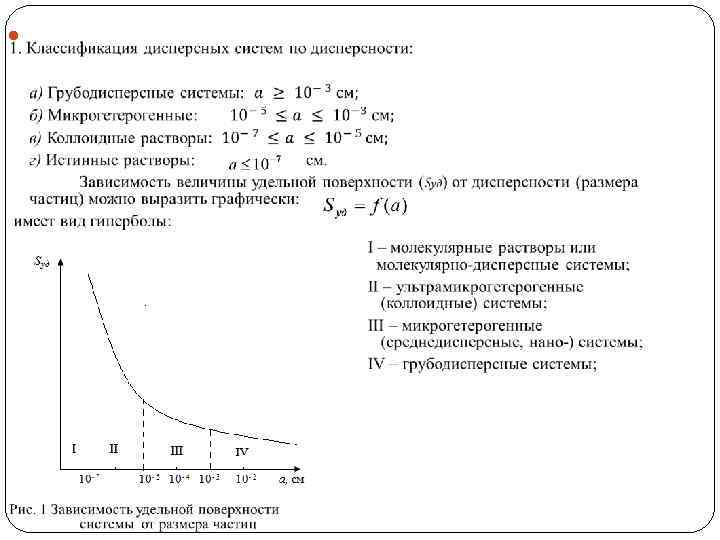
 Агрегатные состояния веществ Для большинства веществ агрегатных состояний три: -газообразное состояние - отсутствие ближнего и дальнего порядка, т. е. хаотическое движение молекул, отсутствие объема и формы; -жидкое состояние - отсутствие дальнего и наличие ближнего порядка. Характерны текучесть и отсутствие формы; - твердое состояние - наличие ближнего и дальнего порядка, Характерны объем и форма.
Агрегатные состояния веществ Для большинства веществ агрегатных состояний три: -газообразное состояние - отсутствие ближнего и дальнего порядка, т. е. хаотическое движение молекул, отсутствие объема и формы; -жидкое состояние - отсутствие дальнего и наличие ближнего порядка. Характерны текучесть и отсутствие формы; - твердое состояние - наличие ближнего и дальнего порядка, Характерны объем и форма.
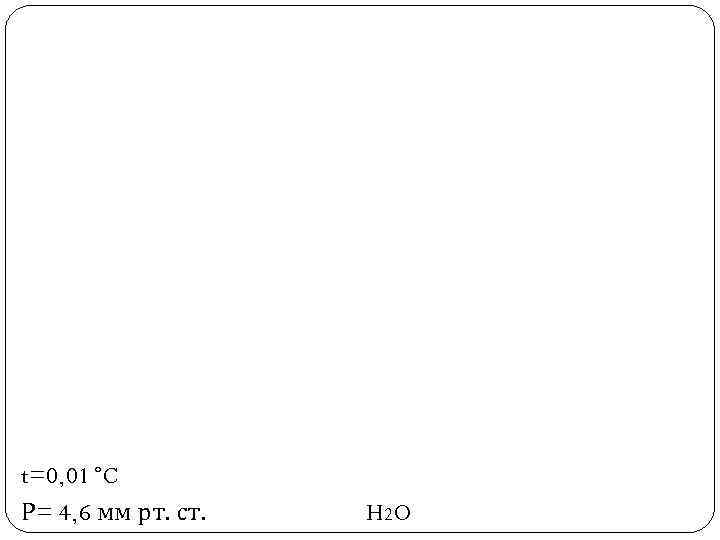 t=0, 01 ◦C Р= 4, 6 мм рт. ст. H 2 O
t=0, 01 ◦C Р= 4, 6 мм рт. ст. H 2 O
 ГАЗЫ Газы могут существовать индивидуально и как смеси, которые смешиваются в неограниченных пропорциях. Газы характеризуются определенными параметрами: давлением, температурой, плотностью и объемом.
ГАЗЫ Газы могут существовать индивидуально и как смеси, которые смешиваются в неограниченных пропорциях. Газы характеризуются определенными параметрами: давлением, температурой, плотностью и объемом.
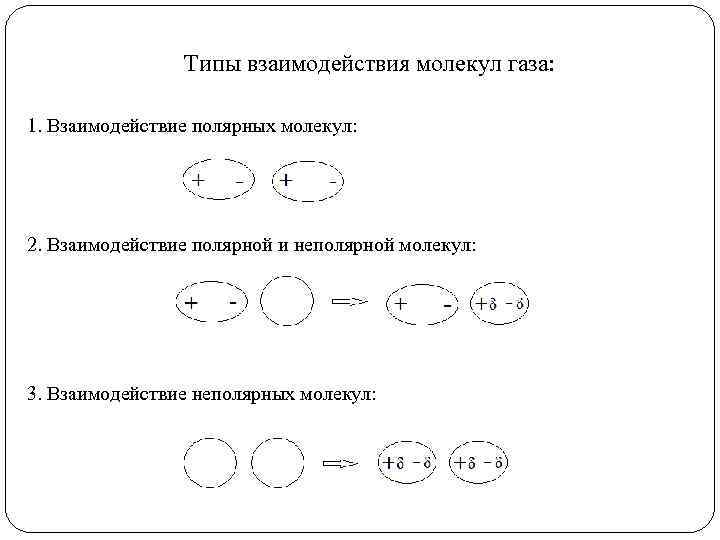 Типы взаимодействия молекул газа: 1. Взаимодействие полярных молекул: 2. Взаимодействие полярной и неполярной молекул: 3. Взаимодействие неполярных молекул:
Типы взаимодействия молекул газа: 1. Взаимодействие полярных молекул: 2. Взаимодействие полярной и неполярной молекул: 3. Взаимодействие неполярных молекул:






 Vр. у. (H 2) = 22, 43 л Vр. у. (N 2) = 22, 40 л Vр. у. (Ne) = 22, 42 л Vр. у. (O 2) = 22, 39 л
Vр. у. (H 2) = 22, 43 л Vр. у. (N 2) = 22, 40 л Vр. у. (Ne) = 22, 42 л Vр. у. (O 2) = 22, 39 л
 Спасибо за внимание! Вопросы?
Спасибо за внимание! Вопросы?


