Лекция 08 - Защита от коррозии.ppt
- Количество слайдов: 19

Лекция Защита металлов от коррозии

Способы защиты от коррозии 1. Нанесение покрытий 2. Легирование металлов 3. Электрохимическая защита 4. Изменение свойств коррозионной среды 5. Рациональное конструирование изделий
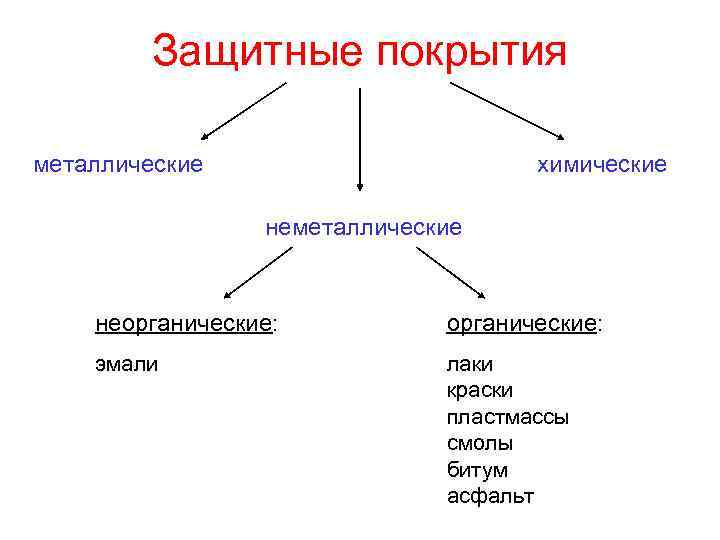
Защитные покрытия металлические химические неметаллические неорганические: эмали лаки краски пластмассы смолы битум асфальт

Химические покрытия Химическая обработка поверхности металла с целью получения пленки, устойчивой к коррозии Оксидирование – получение оксидных пленок Воронение сталей: 3 Fe + 4 Na. NO 3 → Fe 3 O 4 + 4 Na. NO 2 Анодирование алюминия (электролиз) А(+) 2 Al + H 2 O – 6 e– → Al 2 O 3 + 6 H+ K(–) 2 H+ + 2 e– → H 2 Фосфатирование (Mn 3(PO 4)2, Fe 3(PO 4)2) Азотирование (Cr 2 N, Al. N)

Металлические покрытия Анодное покрытие – покрытие металлом, с более отрицательным потенциалом Оцинкованное железо А(–) Zn – 2 e– → Zn 2+ K(+) (Fe) 2 H+ + 2 e– → H 2 Катодное покрытие – покрытие металлом, с более положительным потенциалом Луженое железо А(–) Fe – 2 e– → Fe 2+ K(+) (Sn) 2 H+ + 2 e– → H 2

Методы нанесения металлических покрытий 1) Термодиффузионный метод 2) Горячий метод – погружение в расплавленный металл 3) Распыление металла 4) Механотермический или плакирование

Термодиффузионный метод Поверхностное насыщение основного металла атомами легирующего компонента в результате его диффузии при высоких температурах. Покрытие: алюминием (Al) –термоалитирование хромом (Cr) – термохромирование кремнием (Si) – термосилицирование
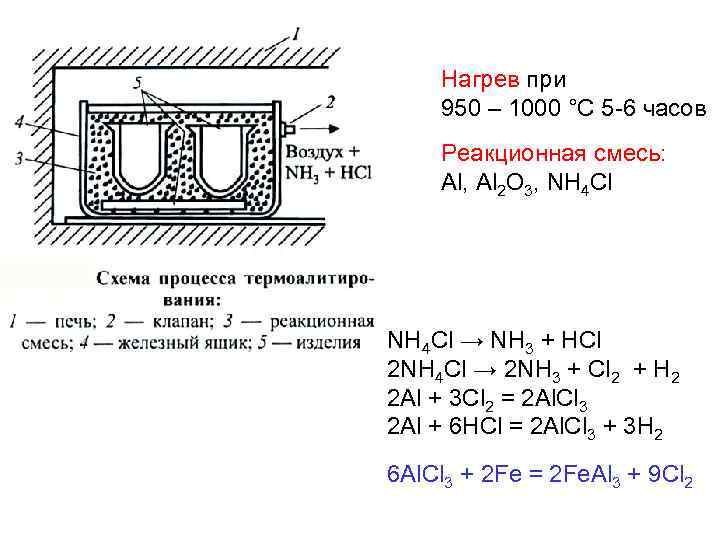
Нагрев при 950 – 1000 °С 5 -6 часов Реакционная смесь: Al, Al 2 O 3, NH 4 Cl → NH 3 + HCl 2 NH 4 Cl → 2 NH 3 + Cl 2 + H 2 2 Al + 3 Cl 2 = 2 Al. Cl 3 2 Al + 6 HCl = 2 Al. Cl 3 + 3 H 2 6 Al. Cl 3 + 2 Fe = 2 Fe. Al 3 + 9 Cl 2
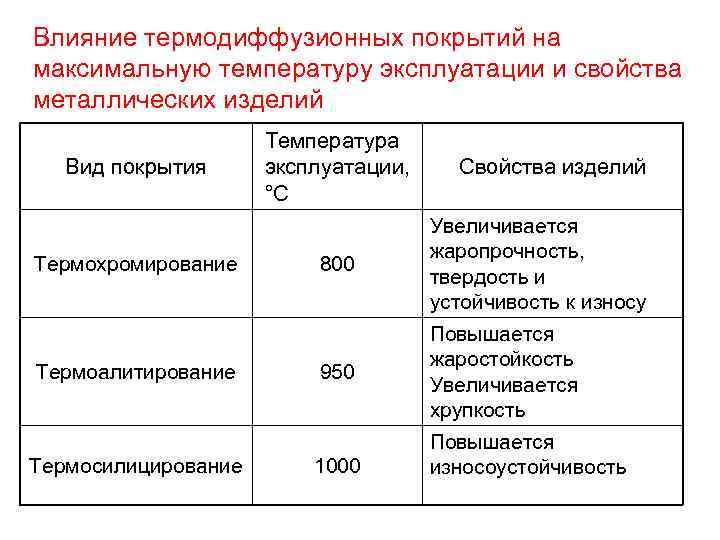
Влияние термодиффузионных покрытий на максимальную температуру эксплуатации и свойства металлических изделий Вид покрытия Термохромирование Термоалитирование Термосилицирование Температура эксплуатации, °С Свойства изделий 800 Увеличивается жаропрочность, твердость и устойчивость к износу 950 Повышается жаростойкость Увеличивается хрупкость 1000 Повышается износоустойчивость

Горячий метод Погружение защищаемого металла в расплав металла, используемого для покрытия. Применяют: Zn (Т пл. = 419 °С) Sn (Т пл. = 232 °С) Pb (Т пл. = 327 °С) Al (Т пл. = 658 °С)

Металлизация напылением Нанесение расплавленного металла на поверхность с помощью струи сжатого воздуха или инертного газа. Плакирование На матрицу основного металла накладывают с обеих сторон листы другого металла, затем весь пакет подвергают горячей прокатке.

Легирование металлов Введение в сплав компонентов (Cr, Ni, Al, Pb, Mo, Mn, W), повышающих коррозионную стойкость Состав стали (Fe) Cr (4 -9%) Свойства устойчивость в атмосфере, растворах кислот, солей (кроме хлоридов) Применение нефтеперерабатывающая промышленность Cr (25%), Si (1%) жаростойкость до 900 – 950ºС Cr (30%), Al (5%), Si (0, 5%) жаростойкость до 1300ºС спирали электронагреватель ных приборов горелки, элементы печей
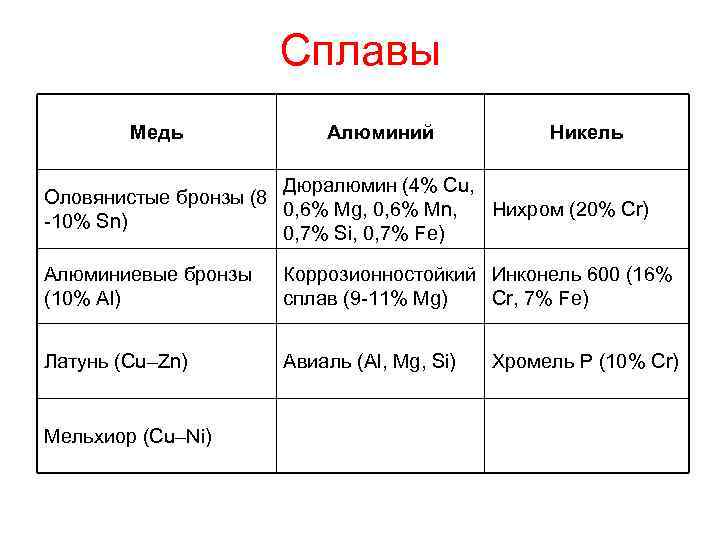
Сплавы Медь Алюминий Никель Дюралюмин (4% Cu, Оловянистые бронзы (8 0, 6% Mg, 0, 6% Mn, Нихром (20% Cr) -10% Sn) 0, 7% Si, 0, 7% Fe) Алюминиевые бронзы (10% Al) Коррозионностойкий Инконель 600 (16% сплав (9 -11% Mg) Cr, 7% Fe) Латунь (Cu–Zn) Авиаль (Al, Mg, Si) Мельхиор (Cu–Ni) Хромель Р (10% Cr)
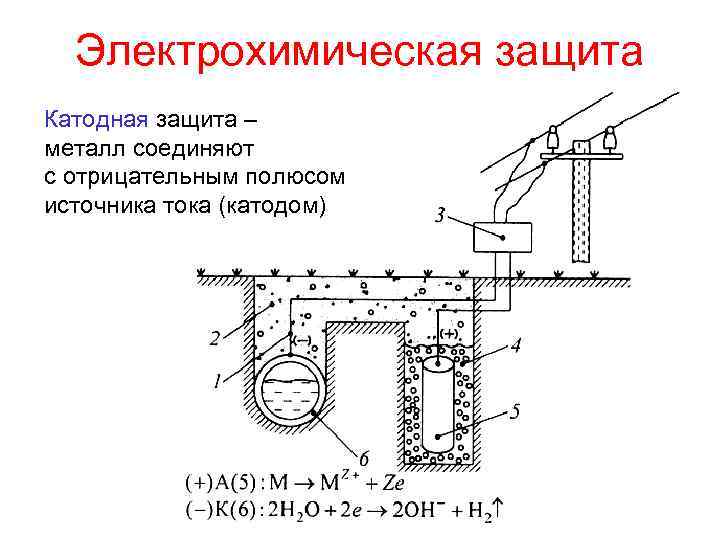
Электрохимическая защита Катодная защита – металл соединяют с отрицательным полюсом источника тока (катодом)

Электрохимическая защита Протекторная защита – к изделию присоединяют металл с более отрицательным потенциалом (Zn, Mg, Al) Анодная защита – металл соединяют с положительным полюсом источника тока (анодом) (для легко пассивирующихся металлов (Ni, Cr, Ti, Al))

Изменение свойств коррозионной среды Введение ингибиторов коррозии Адсорбционные ингибиторы (диэтиламин, уротропин, меркаптаны) Пассивационные ингибиторы (Na 2 Cr 2 O 7, Na. NO 2, Na 2 Si. O 3) 2 Fe + 2 Na 2 Cr. O 4 +2 H 2 O = Cr 2 O 3 + Fe 2 O 3 + 4 Na. OH 2 Fe + Na. NO 2 + 2 H 2 O = Fe 2 O 3 + Na. OH + NH 3

Изменение свойств коррозионной среды Удаление агрессивных компонентов из среды Деаэрация (кипячение, барботаж инертного газа) Применение восстановителей (сульфиты, гидразин) O 2 + N 2 H 4 = N 2 + 2 H 2 O Подщелачивание (Ca(OH)2, Na. OH) Удаление солей (ионный обмен)

Коррозия под действием блуждающих токов "Вход" тока – катодный участок, "выход" тока – анодный участок (корродирует) Защита Дренаж – соединение проводником анодной зоны трубы и катодной зоны рельса Дополнительный анод, соединенный с катодным участком рельса

Тест 1) Предложите катодное покрытие для никеля. Напишите уравнение коррозии при нарушении этого покрытия в кислой среде. 2) В латуни (сплав цинка и меди) избирательной коррозии подвергается: а) цинк; б) медь 3) Перечислите методы нанесения металлических покрытий 4) Дайте определение следующим терминам: а) легирование б) ингибитор коррозии в) протектор 5) Выберите металлы, которые можно использовать в качестве анодного покрытия для никеля: а) медь б) железо в) кадмий г) хром д) серебро е) кобальт
Лекция 08 - Защита от коррозии.ppt