Лекция Химия неметаллов Свойства химических






































Лекция неметаллы (2012).ppt
- Количество слайдов: 49
 Лекция Химия неметаллов Свойства химических элементов и простых веществ. Химические элементы в периодической системе. Классификация элементов по химической природе. Классификация простых веществ. Аллотропия, полиморфизм. Физические свойства простых веществ. Химические свойства простых веществ
Лекция Химия неметаллов Свойства химических элементов и простых веществ. Химические элементы в периодической системе. Классификация элементов по химической природе. Классификация простых веществ. Аллотропия, полиморфизм. Физические свойства простых веществ. Химические свойства простых веществ
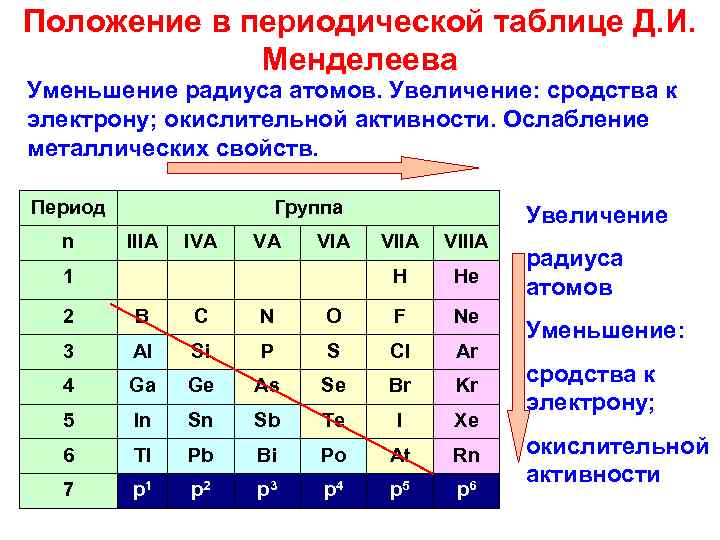
 Положение в периодической таблице Д. И. Менделеева Уменьшение радиуса атомов. Увеличение: сродства к Уменьшение радиуса атомов. электрону; окислительной активности. Ослабление Увеличение: сродства к электрону; окислительной активности. металлических свойств. Ослабление металлических Период Группа Увеличение n IIIA IVA VIA VIIIA радиуса 1 H He атомов 2 B C N O F Ne Уменьшение: 3 Al Si P S Cl Ar 4 Ga Ge As Se Br Kr сродства к электрону; 5 In Sb Te I Xe 6 Tl Pb Bi Po At Rn окислительной активности 7 p 1 p 2 p 3 p 4 p 5 p 6
Положение в периодической таблице Д. И. Менделеева Уменьшение радиуса атомов. Увеличение: сродства к Уменьшение радиуса атомов. электрону; окислительной активности. Ослабление Увеличение: сродства к электрону; окислительной активности. металлических свойств. Ослабление металлических Период Группа Увеличение n IIIA IVA VIA VIIIA радиуса 1 H He атомов 2 B C N O F Ne Уменьшение: 3 Al Si P S Cl Ar 4 Ga Ge As Se Br Kr сродства к электрону; 5 In Sb Te I Xe 6 Tl Pb Bi Po At Rn окислительной активности 7 p 1 p 2 p 3 p 4 p 5 p 6
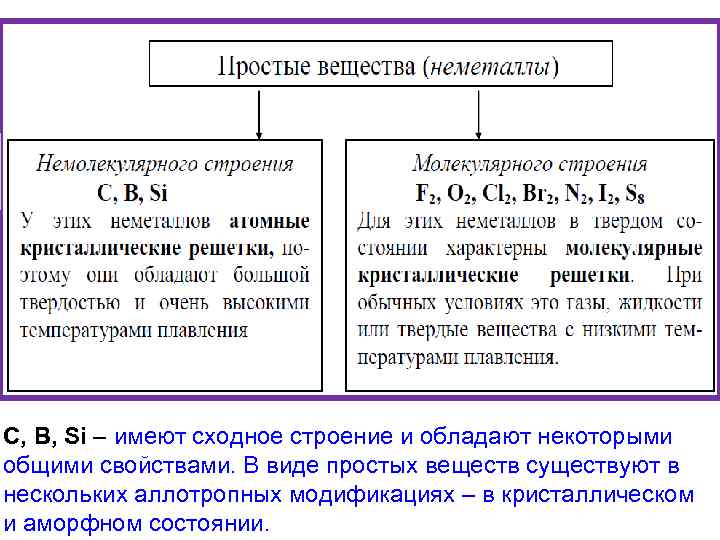
 С, В, Si – имеют сходное строение и обладают некоторыми общими свойствами. В виде простых веществ существуют в нескольких аллотропных модификациях – в кристаллическом и аморфном состоянии.
С, В, Si – имеют сходное строение и обладают некоторыми общими свойствами. В виде простых веществ существуют в нескольких аллотропных модификациях – в кристаллическом и аморфном состоянии.
 Простое вещество – химическое соединение, образованное из атомов одного химического элемента. Простые вещества являются формами существования элементов в свободном состоянии, например, сера, железо, озон, алмаз, азот. Аллотропия (от греч. allo - другой) – способность химического элемента к существованию в виде различных простых веществ - аллотропных модификаций. Эти вещества могут отличаться кристаллической структурой, как, например, графит и алмаз, фуллерены. Кислород существует в двух формах (обе молекулярные), обычного двухатомного кислорода O 2 и озона O 3. Аллотропные модификации присущи многим элементам: сере, фосфору, олову, мышьяку и др. Полиморфизм (отгреч. polymorphos-многообразный), пособность твердых в-в существовать в двух или неск. формах с разл. кристаллич. структурой и св-вами при одном и том же хим. составе. Такие формы наз. полиморфными модификациями. Взаимные превращения полиморфных модификаций наз. полиморфными переходами. П. простых в-в принято называть аллотропией.
Простое вещество – химическое соединение, образованное из атомов одного химического элемента. Простые вещества являются формами существования элементов в свободном состоянии, например, сера, железо, озон, алмаз, азот. Аллотропия (от греч. allo - другой) – способность химического элемента к существованию в виде различных простых веществ - аллотропных модификаций. Эти вещества могут отличаться кристаллической структурой, как, например, графит и алмаз, фуллерены. Кислород существует в двух формах (обе молекулярные), обычного двухатомного кислорода O 2 и озона O 3. Аллотропные модификации присущи многим элементам: сере, фосфору, олову, мышьяку и др. Полиморфизм (отгреч. polymorphos-многообразный), пособность твердых в-в существовать в двух или неск. формах с разл. кристаллич. структурой и св-вами при одном и том же хим. составе. Такие формы наз. полиморфными модификациями. Взаимные превращения полиморфных модификаций наз. полиморфными переходами. П. простых в-в принято называть аллотропией.
 Получение неметаллов • Если в соединении неметалл находится в отрицательной степени окисления, то получить его в виде простого вещества можно действием окислителя: 4 N– 3 H 3 + 3 O 2 → 2 N 2 + 6 H 2 O, 2 H 2 S– 2 + O 2 → 2 S + 2 H 2 O, 2 KI– 1 + 2 Fe. Cl 3 → I 2 + 2 KCl + 2 Fe. Cl 2, 16 HCl– 1+ 2 KMn. O 4 → 5 Cl 2+2 KCl+2 Mn. Cl 2+ 8 H 2 O, 2 KBr– 1+Mn. O 2+2 H 2 SO 4→ Br 2+Mn. SO 4+K 2 SO 4+2 H 2 O.
Получение неметаллов • Если в соединении неметалл находится в отрицательной степени окисления, то получить его в виде простого вещества можно действием окислителя: 4 N– 3 H 3 + 3 O 2 → 2 N 2 + 6 H 2 O, 2 H 2 S– 2 + O 2 → 2 S + 2 H 2 O, 2 KI– 1 + 2 Fe. Cl 3 → I 2 + 2 KCl + 2 Fe. Cl 2, 16 HCl– 1+ 2 KMn. O 4 → 5 Cl 2+2 KCl+2 Mn. Cl 2+ 8 H 2 O, 2 KBr– 1+Mn. O 2+2 H 2 SO 4→ Br 2+Mn. SO 4+K 2 SO 4+2 H 2 O.
 • Если в соединении неметалл находится в положительной степени окисления, то получить его в виде простого вещества можно действием восстановителя: • Si+4 O 2 + 2 Mg → Si + 2 Mg. O, Na 2 S+4 O 3+2 H 2 S+H 2 SO 4→ 2 S↓+Na 2 SO 4+3 H 2 O • 2 KCl+5 O 3 + I 2 → Cl 2 + 2 KIO 3.
• Если в соединении неметалл находится в положительной степени окисления, то получить его в виде простого вещества можно действием восстановителя: • Si+4 O 2 + 2 Mg → Si + 2 Mg. O, Na 2 S+4 O 3+2 H 2 S+H 2 SO 4→ 2 S↓+Na 2 SO 4+3 H 2 O • 2 KCl+5 O 3 + I 2 → Cl 2 + 2 KIO 3.
 • 1) анодное окисление (A+, анод): • 2 H 2 O– 2 – e– → O 2↑ + 4 H+ (раствор), • 2 Cl– – 2 e– → Cl 2↑ (раствор или расплав), • 2 F– – 2 e–→ F 2↑ (расплав); • 2) катодное восстановление (K–, катод): • 2 H+12 O + 2 e–→ H 2↑ + 2 OH–. • термическим разложением сложных веществ: • (катализатор Mn. O 2) • KCl. O 3 O 2↑ + KCl, • NH 4 NO 2 → N 2 + H 2 O.
• 1) анодное окисление (A+, анод): • 2 H 2 O– 2 – e– → O 2↑ + 4 H+ (раствор), • 2 Cl– – 2 e– → Cl 2↑ (раствор или расплав), • 2 F– – 2 e–→ F 2↑ (расплав); • 2) катодное восстановление (K–, катод): • 2 H+12 O + 2 e–→ H 2↑ + 2 OH–. • термическим разложением сложных веществ: • (катализатор Mn. O 2) • KCl. O 3 O 2↑ + KCl, • NH 4 NO 2 → N 2 + H 2 O.
 Химические свойства неметаллов • Неметаллы могут выступать окислителями. При этом восстановителями могут быть: • а) металлы: O 20 + Mg → Mg. O– 2 (оксид магния), N 20 + Li → Li 3 N– 3 (нитрид лития), S 0 + Zn → Zn. S– 2 (сульфид цинка); • б) менее активные неметаллы: O 20 + C→ CO 2– 2, O 20 + P → P 2 O 5– 2, O 20 + S → SO 2– 2, в) сложные вещества: O 20 + C 2 H 5 OH→CO 2– 2 + H 2 O– 2, Br 20 + Ni(OH) 2 + KOH → KBr– 1 + Ni 2 O 3⋅x. H 2 O.
Химические свойства неметаллов • Неметаллы могут выступать окислителями. При этом восстановителями могут быть: • а) металлы: O 20 + Mg → Mg. O– 2 (оксид магния), N 20 + Li → Li 3 N– 3 (нитрид лития), S 0 + Zn → Zn. S– 2 (сульфид цинка); • б) менее активные неметаллы: O 20 + C→ CO 2– 2, O 20 + P → P 2 O 5– 2, O 20 + S → SO 2– 2, в) сложные вещества: O 20 + C 2 H 5 OH→CO 2– 2 + H 2 O– 2, Br 20 + Ni(OH) 2 + KOH → KBr– 1 + Ni 2 O 3⋅x. H 2 O.
 • Неметаллы бывают восстановителями только в реакциях с более активными неметаллами: H 20 + N 2 → NH 3+1, S 0 + F 2 → S+6 F 6, • а также с сильными окислителями: P 0 + KCl. O 3 (при ударе) → P 2+5 O 5 + KCl, S 0 + KNO 3 (при нагревании) → KNO 2 +S+4 O 2 • Углерод при высоких температурах способен восстанавливать оксиды металлов : 3 С 0 + Fe 2 O 3 = 3 C+2 O + Fe
• Неметаллы бывают восстановителями только в реакциях с более активными неметаллами: H 20 + N 2 → NH 3+1, S 0 + F 2 → S+6 F 6, • а также с сильными окислителями: P 0 + KCl. O 3 (при ударе) → P 2+5 O 5 + KCl, S 0 + KNO 3 (при нагревании) → KNO 2 +S+4 O 2 • Углерод при высоких температурах способен восстанавливать оксиды металлов : 3 С 0 + Fe 2 O 3 = 3 C+2 O + Fe
 • При взаимодействии с водой ряда наиболее активных неметаллов происходит их диспропорционирование: Cl 20 + H 2 O ↔ HCl– 1 + HOCl+1, I 20 + H 2 O ↔ HI– 1 + HIO 3+5 Cl 20 + 2 Na. OH ↔ Na. Cl– 1 + Na. OCl+1 + H 2 O • При нагревании раствора устойчивее более высокие степени окисления галогенов: t Cl 20 + KOH (р-р) → KCl– 1 + KCl. O 3+5 (бертолетова соль)
• При взаимодействии с водой ряда наиболее активных неметаллов происходит их диспропорционирование: Cl 20 + H 2 O ↔ HCl– 1 + HOCl+1, I 20 + H 2 O ↔ HI– 1 + HIO 3+5 Cl 20 + 2 Na. OH ↔ Na. Cl– 1 + Na. OCl+1 + H 2 O • При нагревании раствора устойчивее более высокие степени окисления галогенов: t Cl 20 + KOH (р-р) → KCl– 1 + KCl. O 3+5 (бертолетова соль)
 • при нагревании в щелочах растворяются и некоторые менее активные неметаллы: 3 S + 3 Na. OH = 2 Na 2 S+ Na 2 SO 3, 2 P + 2 Na. OH + H 2 O = PH 3+ Na 2(PO 3 H). • Неметаллы с минимальной электроотрицательностью растворяются в щелочах с выделением водорода: Si + 2 Na. OH + 2 H 2 O = Na 2[H 2 Si. O 4] + 2 H 2↑.
• при нагревании в щелочах растворяются и некоторые менее активные неметаллы: 3 S + 3 Na. OH = 2 Na 2 S+ Na 2 SO 3, 2 P + 2 Na. OH + H 2 O = PH 3+ Na 2(PO 3 H). • Неметаллы с минимальной электроотрицательностью растворяются в щелочах с выделением водорода: Si + 2 Na. OH + 2 H 2 O = Na 2[H 2 Si. O 4] + 2 H 2↑.
 • Углерод реагирует с водяным паром только выше 900 °С: C + H 2 O = CO + H 2 • Во фторе вода горит с выделением кислорода: F 2 + H 2 O = HF + O 2
• Углерод реагирует с водяным паром только выше 900 °С: C + H 2 O = CO + H 2 • Во фторе вода горит с выделением кислорода: F 2 + H 2 O = HF + O 2
 Соединения неметаллов с водородом H 2 + F 2 → 2 HF (фтороводород) при tком При нагревании : H 2 + Cl 2 → HCl; 2 H 2 + O 2 → 2 H 2 O. H 2 +Br 2 → 2 HBr В остальных случаях реакция идёт с трудом или вообще не идёт: N 2 + 3 H 2 → 2 NH 3 (катализатор, t=500 °С и P=300 атм)
Соединения неметаллов с водородом H 2 + F 2 → 2 HF (фтороводород) при tком При нагревании : H 2 + Cl 2 → HCl; 2 H 2 + O 2 → 2 H 2 O. H 2 +Br 2 → 2 HBr В остальных случаях реакция идёт с трудом или вообще не идёт: N 2 + 3 H 2 → 2 NH 3 (катализатор, t=500 °С и P=300 атм)
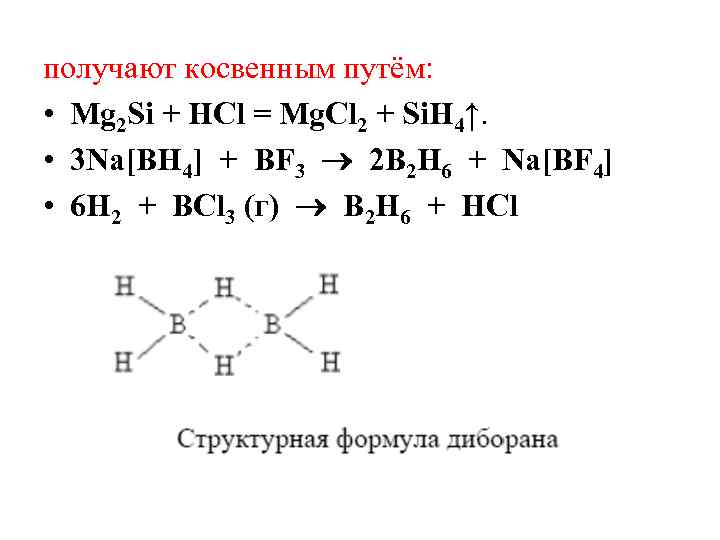
 получают косвенным путём: • Mg 2 Si + HCl = Mg. Cl 2 + Si. H 4↑. • 3 Na[BH 4] + BF 3 2 B 2 H 6 + Na[BF 4] • 6 H 2 + BCl 3 (г) B 2 H 6 + HCl
получают косвенным путём: • Mg 2 Si + HCl = Mg. Cl 2 + Si. H 4↑. • 3 Na[BH 4] + BF 3 2 B 2 H 6 + Na[BF 4] • 6 H 2 + BCl 3 (г) B 2 H 6 + HCl
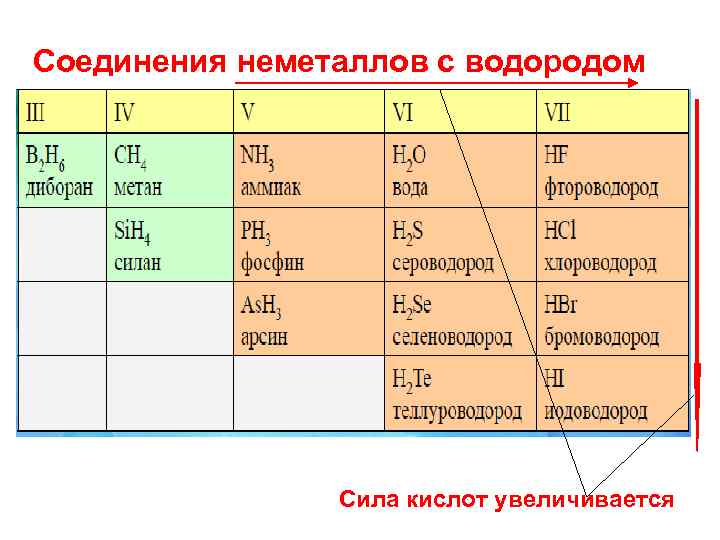
 Соединения неметаллов с водородом Сила кислот увеличивается
Соединения неметаллов с водородом Сила кислот увеличивается
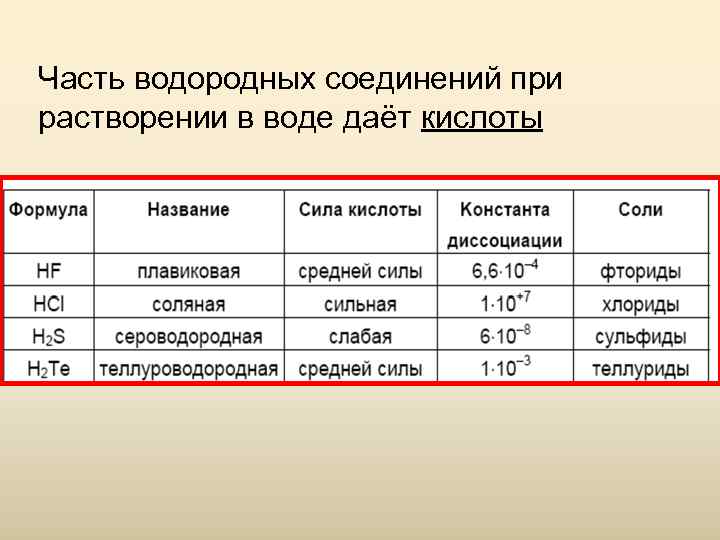
 Часть водородных соединений при растворении в воде даёт кислоты
Часть водородных соединений при растворении в воде даёт кислоты
 • При взаимодействии кислотных водородных соединений со щелочами получаются соли: • H 2 S + 2 Na. OH → Na 2 S + 2 H 2 O Из водородных соединений основную природу имеет только аммиак. В его растворе устанавливаются равновесия: • NH 3 + H 2 O ↔H 2 O∙NH 3⋅↔ NH 4+ + OH–. • При взаимодействии аммиака с кислотами получаются соли, содержащие ион NH 4+ (ион аммония): • NH 3 + HCl ( р) → NH 4 Cl.
• При взаимодействии кислотных водородных соединений со щелочами получаются соли: • H 2 S + 2 Na. OH → Na 2 S + 2 H 2 O Из водородных соединений основную природу имеет только аммиак. В его растворе устанавливаются равновесия: • NH 3 + H 2 O ↔H 2 O∙NH 3⋅↔ NH 4+ + OH–. • При взаимодействии аммиака с кислотами получаются соли, содержащие ион NH 4+ (ион аммония): • NH 3 + HCl ( р) → NH 4 Cl.
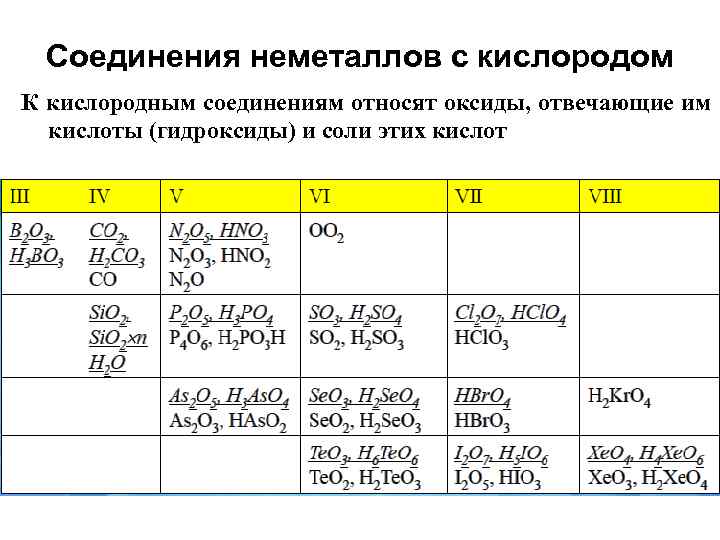
 Соединения неметаллов с кислородом К кислородным соединениям относят оксиды, отвечающие им кислоты (гидроксиды) и соли этих кислот
Соединения неметаллов с кислородом К кислородным соединениям относят оксиды, отвечающие им кислоты (гидроксиды) и соли этих кислот
 Получение и химические свойства оксидов 1) взаимодействием неметаллов с кислородом: S + O 2 → SO 2, 2) удалением воды из кислот: 2 H 3 BO 3 → B 2 O 3 + 3 H 2 O (при нагревании) 3) окислением оксидов в низших степенях окисления: 2 C+2 O + O 2 → 2 C+4 O 2, (t) 2 S+4 O 2+O 2 → 2 S+6 O 3; (катализатор; t) 4) окислением других сложных веществ при нагревании: 2 H 2 S + 3 O 2 → 3 SO 2 + 2 H 2 O, CH 4 + 2 O 2 → CO 2 + 2 H 2 O,
Получение и химические свойства оксидов 1) взаимодействием неметаллов с кислородом: S + O 2 → SO 2, 2) удалением воды из кислот: 2 H 3 BO 3 → B 2 O 3 + 3 H 2 O (при нагревании) 3) окислением оксидов в низших степенях окисления: 2 C+2 O + O 2 → 2 C+4 O 2, (t) 2 S+4 O 2+O 2 → 2 S+6 O 3; (катализатор; t) 4) окислением других сложных веществ при нагревании: 2 H 2 S + 3 O 2 → 3 SO 2 + 2 H 2 O, CH 4 + 2 O 2 → CO 2 + 2 H 2 O,
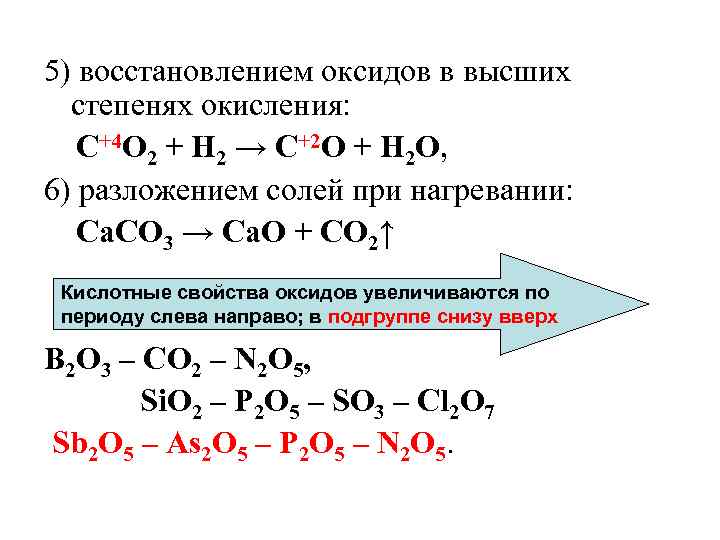
 5) восстановлением оксидов в высших степенях окисления: C+4 O 2 + H 2 → C+2 O + H 2 O, 6) разложением солей при нагревании: Ca. CO 3 → Ca. O + CO 2↑ Кислотные свойства оксидов увеличиваются по периоду слева направо; в подгруппе снизу вверх B 2 O 3 – CO 2 – N 2 O 5, Si. O 2 – P 2 O 5 – SO 3 – Cl 2 O 7 Sb 2 O 5 – As 2 O 5 – P 2 O 5 – N 2 O 5.
5) восстановлением оксидов в высших степенях окисления: C+4 O 2 + H 2 → C+2 O + H 2 O, 6) разложением солей при нагревании: Ca. CO 3 → Ca. O + CO 2↑ Кислотные свойства оксидов увеличиваются по периоду слева направо; в подгруппе снизу вверх B 2 O 3 – CO 2 – N 2 O 5, Si. O 2 – P 2 O 5 – SO 3 – Cl 2 O 7 Sb 2 O 5 – As 2 O 5 – P 2 O 5 – N 2 O 5.
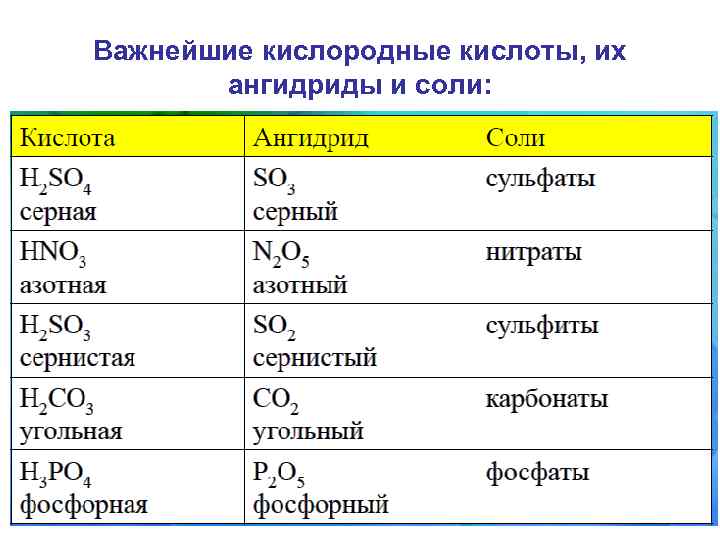
 Важнейшие кислородные кислоты, их ангидриды и соли:
Важнейшие кислородные кислоты, их ангидриды и соли:
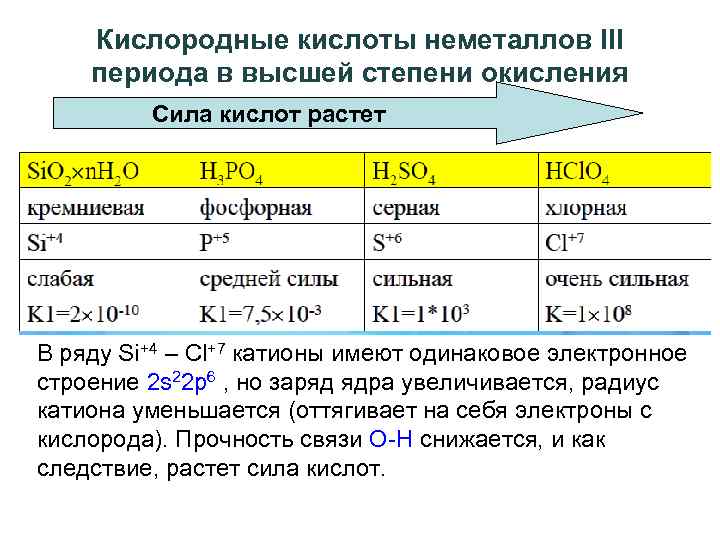
 Кислородные кислоты неметаллов III периода в высшей степени окисления Сила кислот растет В ряду Si+4 – Cl+7 катионы имеют одинаковое электронное строение 2 s 22 p 6 , но заряд ядра увеличивается, радиус катиона уменьшается (оттягивает на себя электроны с кислорода). Прочность связи O-H снижается, и как следствие, растет сила кислот.
Кислородные кислоты неметаллов III периода в высшей степени окисления Сила кислот растет В ряду Si+4 – Cl+7 катионы имеют одинаковое электронное строение 2 s 22 p 6 , но заряд ядра увеличивается, радиус катиона уменьшается (оттягивает на себя электроны с кислорода). Прочность связи O-H снижается, и как следствие, растет сила кислот.
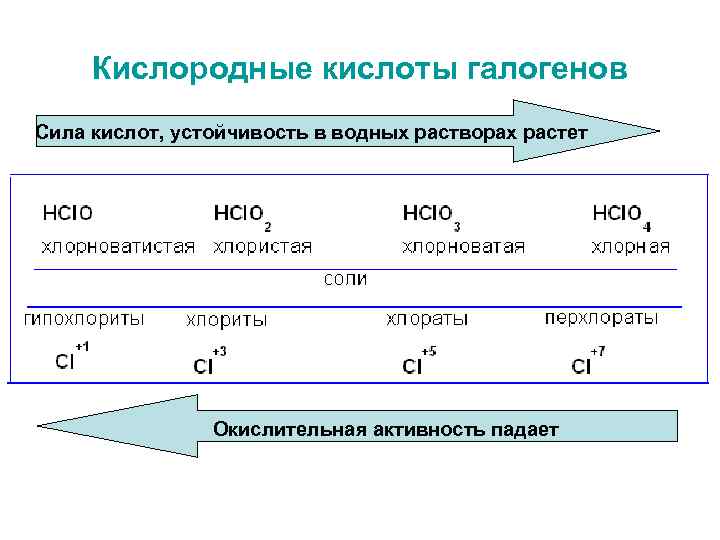
 Кислородные кислоты галогенов Сила кислот, устойчивость в водных растворах растет Окислительная активность падает
Кислородные кислоты галогенов Сила кислот, устойчивость в водных растворах растет Окислительная активность падает
 Кислоты-окислители при взаимодействии с металлами или другими восстановителями восстанавливается не водород, а центральный катион неметалла • Cu + 2 H 2 S+6 O 4 (конц. ) → Cu. SO 4 + S+4 O 2 + 2 H 2 O. • 3 Cu + 8 HN+5 O 3 (33%) → 3 Cu(NO 3)2 + 2 N+2 O + 4 H 2 O, • Cu + 4 HN+5 O 3 (70%) → Cu(NO 3)2 + 2 N+4 O 2 + 2 H 2 O, • 3 Zn + 8 HN+5 O 3 (конц. ) → 3 Zn(NO 3)2 + 2 N+2 O + 4 H 2 O, • 4 Zn + 6 HN+5 O 3 (разб. ) → 4 Zn(NO 3)2 + N+12 O + 3 H 2 O.
Кислоты-окислители при взаимодействии с металлами или другими восстановителями восстанавливается не водород, а центральный катион неметалла • Cu + 2 H 2 S+6 O 4 (конц. ) → Cu. SO 4 + S+4 O 2 + 2 H 2 O. • 3 Cu + 8 HN+5 O 3 (33%) → 3 Cu(NO 3)2 + 2 N+2 O + 4 H 2 O, • Cu + 4 HN+5 O 3 (70%) → Cu(NO 3)2 + 2 N+4 O 2 + 2 H 2 O, • 3 Zn + 8 HN+5 O 3 (конц. ) → 3 Zn(NO 3)2 + 2 N+2 O + 4 H 2 O, • 4 Zn + 6 HN+5 O 3 (разб. ) → 4 Zn(NO 3)2 + N+12 O + 3 H 2 O.
 СОЛИ КИСЛОРОДНЫХ КИСЛОТ • Соли могут быть получены взаимодействием кислотных оксидов или кислот - с основаниями: • CO 2 + 2 Na. OH → Na 2 CO 3 + H 2 O, • H 2 SO 4 + 2 Na. OH → Na 2 SO 4 + 2 H 2 O, - с основными оксидами: • Ba. O + CO 2 → Ba. CO 3, • Ca. O + H 2 SO 4 → Ca. SO 4 + H 2 O, - с солями более слабых кислот: • Na 2 Si. O 3 + H 2 O + CO 2 → Na 2 CO 3 + “H 2 Si. O 3“↓
СОЛИ КИСЛОРОДНЫХ КИСЛОТ • Соли могут быть получены взаимодействием кислотных оксидов или кислот - с основаниями: • CO 2 + 2 Na. OH → Na 2 CO 3 + H 2 O, • H 2 SO 4 + 2 Na. OH → Na 2 SO 4 + 2 H 2 O, - с основными оксидами: • Ba. O + CO 2 → Ba. CO 3, • Ca. O + H 2 SO 4 → Ca. SO 4 + H 2 O, - с солями более слабых кислот: • Na 2 Si. O 3 + H 2 O + CO 2 → Na 2 CO 3 + “H 2 Si. O 3“↓
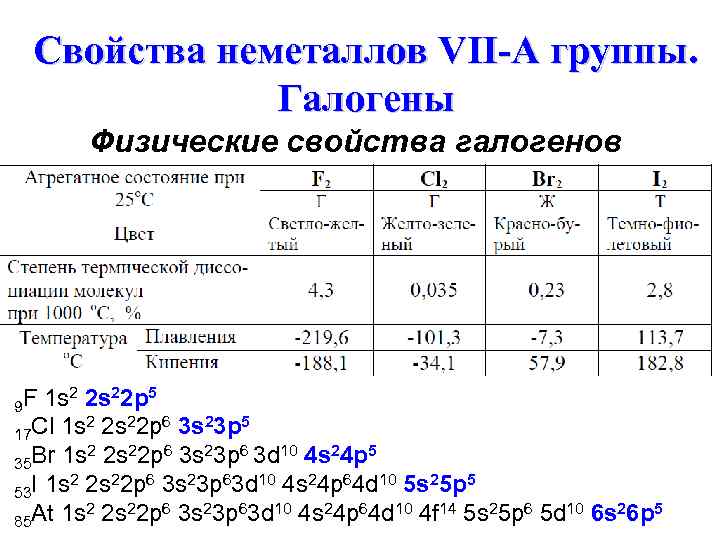
 Свойства неметаллов VII-A группы. Галогены Физические свойства галогенов 9 F 1 s 2 2 s 22 p 5 17 Cl 1 s 2 2 s 22 p 6 3 s 23 p 5 35 Br 1 s 2 s 2 p 3 s 3 p 3 d 2 2 6 10 4 s 24 p 5 53 I 1 s 2 s 2 p 3 s 3 p 3 d 2 2 6 10 4 s 24 p 64 d 10 5 s 25 p 5 85 Аt 1 s 2 s 2 p 3 s 3 p 3 d 2 2 6 10 4 s 24 p 64 d 10 4 f 14 5 s 25 p 6 5 d 10 6 s 26 p 5
Свойства неметаллов VII-A группы. Галогены Физические свойства галогенов 9 F 1 s 2 2 s 22 p 5 17 Cl 1 s 2 2 s 22 p 6 3 s 23 p 5 35 Br 1 s 2 s 2 p 3 s 3 p 3 d 2 2 6 10 4 s 24 p 5 53 I 1 s 2 s 2 p 3 s 3 p 3 d 2 2 6 10 4 s 24 p 64 d 10 5 s 25 p 5 85 Аt 1 s 2 s 2 p 3 s 3 p 3 d 2 2 6 10 4 s 24 p 64 d 10 4 f 14 5 s 25 p 6 5 d 10 6 s 26 p 5
 Галогены обладают большим сродством к электрону и являются сильными окислителями. Окислительные свойства их возрастают от йода к фтору. Они активно взаимодействуют почти со всеми элементами периодической системы. 1. с металлами, образуя соли: 2 Na + F 2 = 2 Na. F ( на холоду) 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 (при нагревании) Аl + 3 I 2 = 2 Аl 2 I 3 (Н 2 О – катализатор) 2. с водородом, образуя соединения НГ: Н 2 + Г 2 = 2 НГ 3. со многими неметаллами: С + 2 Сl 2 = ССl 4; Si + 2 Br 2 = Si. Br 4; 2 P + 3 Cl 2 = 2 PCl 3 S + 3 F 2 = SF 6 ; PCl 3 + Cl 2 = PCl 5 Хе + 3 F 2 = Хе. F 6 (при нагревании) 2 P + 3 Br 2 = 2 PBr 3 СН 4 + Сl 2 = СН 3 Сl + НСl 2 P + 3 I 2 = 2 PI 3 (при нагревании)
Галогены обладают большим сродством к электрону и являются сильными окислителями. Окислительные свойства их возрастают от йода к фтору. Они активно взаимодействуют почти со всеми элементами периодической системы. 1. с металлами, образуя соли: 2 Na + F 2 = 2 Na. F ( на холоду) 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 (при нагревании) Аl + 3 I 2 = 2 Аl 2 I 3 (Н 2 О – катализатор) 2. с водородом, образуя соединения НГ: Н 2 + Г 2 = 2 НГ 3. со многими неметаллами: С + 2 Сl 2 = ССl 4; Si + 2 Br 2 = Si. Br 4; 2 P + 3 Cl 2 = 2 PCl 3 S + 3 F 2 = SF 6 ; PCl 3 + Cl 2 = PCl 5 Хе + 3 F 2 = Хе. F 6 (при нагревании) 2 P + 3 Br 2 = 2 PBr 3 СН 4 + Сl 2 = СН 3 Сl + НСl 2 P + 3 I 2 = 2 PI 3 (при нагревании)
 4. С водой Фтор энергично разлагает воду, продукты реакции зависят от температуры: Н 2 О(к) + F 2(г) = НF(ж) + НОF(г) (ниже 0 о. С) 2 Н 2 О(ж) + 2 F 2(г) = 4 НF + ОF 2↑ (при 0 – 90 о. С) 2 Н 2 О(г) + 2 F 2 = 4 НF↑ + О 2↑ (> 90 о. С со взрывом) Хлор Сl 2 + Н 2 О <=> НСl + НСl. О Бром и Йод Г 2 + Н 2 О <=> НГ + НГО
4. С водой Фтор энергично разлагает воду, продукты реакции зависят от температуры: Н 2 О(к) + F 2(г) = НF(ж) + НОF(г) (ниже 0 о. С) 2 Н 2 О(ж) + 2 F 2(г) = 4 НF + ОF 2↑ (при 0 – 90 о. С) 2 Н 2 О(г) + 2 F 2 = 4 НF↑ + О 2↑ (> 90 о. С со взрывом) Хлор Сl 2 + Н 2 О <=> НСl + НСl. О Бром и Йод Г 2 + Н 2 О <=> НГ + НГО
 При взаимодействии фтора со щелочами продукты реакции зависят от концентрации щелочи: 2 КОН + 2 F 2 = 2 КF + ОF 2↑ + Н 2 О (2 -5 % водный раствор) 4 КОН + 2 F 2 = 4 КF + О 2↑ + 2 Н 2 О (конц. раствор) Продукты взаимодействия хлора со щелочами зависят от температуры. При комнатной температуре Сl 2 + 2 КОН = КСl + КСl. О + Н 2 О А при пропускании хлора в горячий раствор щелочи происходят следующие процессы (аналогичным образом ведут себя бром и йод): 3 Сl 2 + 6 КОН = 5 КСl + КСl. О 3 + 3 Н 2 О
При взаимодействии фтора со щелочами продукты реакции зависят от концентрации щелочи: 2 КОН + 2 F 2 = 2 КF + ОF 2↑ + Н 2 О (2 -5 % водный раствор) 4 КОН + 2 F 2 = 4 КF + О 2↑ + 2 Н 2 О (конц. раствор) Продукты взаимодействия хлора со щелочами зависят от температуры. При комнатной температуре Сl 2 + 2 КОН = КСl + КСl. О + Н 2 О А при пропускании хлора в горячий раствор щелочи происходят следующие процессы (аналогичным образом ведут себя бром и йод): 3 Сl 2 + 6 КОН = 5 КСl + КСl. О 3 + 3 Н 2 О
 ПОЛУЧЕНИЕ ГАЛОГЕНОВ Фтор получают только электролизом В лаборатории Сl 2 получают взаимодействием конц. соляной кислоты с сильными окислителями (Mn. O 2 , K 2 Cr 2 O 7, KMn. O 4, KCl. O 3 и др. ): Mn. O 2 + 4 HCl = Mn. Cl 2 + 2 H 2 O K 2 Cr 2 O 7 + 14 HCl = 2 Cr. Cl 3 + 2 KCl + 3 Cl 2 + 7 H 2 O
ПОЛУЧЕНИЕ ГАЛОГЕНОВ Фтор получают только электролизом В лаборатории Сl 2 получают взаимодействием конц. соляной кислоты с сильными окислителями (Mn. O 2 , K 2 Cr 2 O 7, KMn. O 4, KCl. O 3 и др. ): Mn. O 2 + 4 HCl = Mn. Cl 2 + 2 H 2 O K 2 Cr 2 O 7 + 14 HCl = 2 Cr. Cl 3 + 2 KCl + 3 Cl 2 + 7 H 2 O
 В промышленности хлор получают электролизом электролиз 2 H 2 O + 2 Na. Cl ===== Н 2 + Cl 2 + 2 Na. OH K 2 Cr 2 O 7 + 6 KBr + 7 H 2 SO 4 = 2 Cr 2(SO 4)3 + 4 K 2 SO 4 + 3 Br 2 + 7 H 2 O 8 Na. I + 5 H 2 SO 4 (конц. ) = Na 2 SO 4 + 4 I 2 + H 2 S + 4 H 2 O 4 КI + 2 Сu. SO 4 = 2 Сu. I + I 2 + 2 К 2 SO 4 электролиз 2 H 2 O + 2 Na. I ===== Н 2 + I 2 + 2 Na. OH 2 Na. Br + Cl 2 = 2 Na. Cl + Br 2
В промышленности хлор получают электролизом электролиз 2 H 2 O + 2 Na. Cl ===== Н 2 + Cl 2 + 2 Na. OH K 2 Cr 2 O 7 + 6 KBr + 7 H 2 SO 4 = 2 Cr 2(SO 4)3 + 4 K 2 SO 4 + 3 Br 2 + 7 H 2 O 8 Na. I + 5 H 2 SO 4 (конц. ) = Na 2 SO 4 + 4 I 2 + H 2 S + 4 H 2 O 4 КI + 2 Сu. SO 4 = 2 Сu. I + I 2 + 2 К 2 SO 4 электролиз 2 H 2 O + 2 Na. I ===== Н 2 + I 2 + 2 Na. OH 2 Na. Br + Cl 2 = 2 Na. Cl + Br 2
 Углерод, кремний
Углерод, кремний
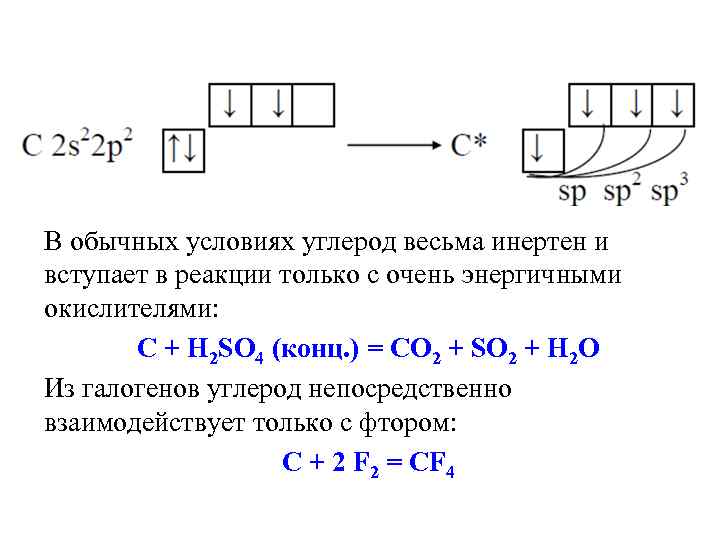
 В обычных условиях углерод весьма инертен и вступает в реакции только с очень энергичными окислителями: С + Н 2 SО 4 (конц. ) = СО 2 + SО 2 + Н 2 О Из галогенов углерод непосредственно взаимодействует только с фтором: С + 2 F 2 = СF 4
В обычных условиях углерод весьма инертен и вступает в реакции только с очень энергичными окислителями: С + Н 2 SО 4 (конц. ) = СО 2 + SО 2 + Н 2 О Из галогенов углерод непосредственно взаимодействует только с фтором: С + 2 F 2 = СF 4
 С + О 2 = СО 2 (избыток кислорода) 2 С + О 2 = 2 СО (недостаток кислорода) При высокой температуре ( t=800 -1000 о С ) углерод соединяется с серой С + 2 S = СS 2 При более высоких температурах углерод соединяется с азотом, образуя дициан (N≡ С–С ≡ N) или (СN)2: 2 С + N 2 = С 2 N 2 Дициан медленно гидролизуется : (СN)2 + 4 Н 2 О = (NН 4)2 С 2 О 4 (СN)2 + Н 2 = 2 НСN
С + О 2 = СО 2 (избыток кислорода) 2 С + О 2 = 2 СО (недостаток кислорода) При высокой температуре ( t=800 -1000 о С ) углерод соединяется с серой С + 2 S = СS 2 При более высоких температурах углерод соединяется с азотом, образуя дициан (N≡ С–С ≡ N) или (СN)2: 2 С + N 2 = С 2 N 2 Дициан медленно гидролизуется : (СN)2 + 4 Н 2 О = (NН 4)2 С 2 О 4 (СN)2 + Н 2 = 2 НСN
 КСN + Н 2 О ↔ КОН + НСN На воздухе КСN разлагается, так как Н 2 СО 3 сильнее синильной кислоты КСN + Н 2 О + СО 2 = КНСО 3 + НСN 4 Аu +8 Na. CN +2 Н 2 О + О 2 = 4 Na[Au(CN)2]+ Nа. ОН При сплавлении цианидов с серой образуются тиоцианаты (роданиды) – соли тиоциановой кислоты или роданистоводородной кислоты: КСN + S = КSСN
КСN + Н 2 О ↔ КОН + НСN На воздухе КСN разлагается, так как Н 2 СО 3 сильнее синильной кислоты КСN + Н 2 О + СО 2 = КНСО 3 + НСN 4 Аu +8 Na. CN +2 Н 2 О + О 2 = 4 Na[Au(CN)2]+ Nа. ОН При сплавлении цианидов с серой образуются тиоцианаты (роданиды) – соли тиоциановой кислоты или роданистоводородной кислоты: КСN + S = КSСN
 Kарбиды В зависимости от электроотрицательности элемента делятся на три группы: а) Солеподобные – это соединения углерода с активными металлами: Ве 2 С, Са. С 2 , Аl 4 С 3. в этих соединениях связь промежуточная между ионной и ковалентной. • 3 С + Са. О = Са. С 2 + СО • Са. С 2 + 2 Н 2 О = Са(ОН)2 + С 2 Н 2 • Аl 4 С 3 + 12 Н 2 О = 4 Аl(ОН)3 + 3 СН 4
Kарбиды В зависимости от электроотрицательности элемента делятся на три группы: а) Солеподобные – это соединения углерода с активными металлами: Ве 2 С, Са. С 2 , Аl 4 С 3. в этих соединениях связь промежуточная между ионной и ковалентной. • 3 С + Са. О = Са. С 2 + СО • Са. С 2 + 2 Н 2 О = Са(ОН)2 + С 2 Н 2 • Аl 4 С 3 + 12 Н 2 О = 4 Аl(ОН)3 + 3 СН 4
 • б) Карбиды внедрения – в них атомы углерода занимают пустоты в кристаллических решетках металлов, имеют, как правило, переменный состав W 2 С. Соединения обладают большой твердостью и высокими температурами плавления, химической стойкостью • в) Ковалентные карбиды – образуются с элементами близкими по электроотрица- тельности (соседями по периодической системе), например, карбиды кремния и бора (Si. C, B 4 C 3).
• б) Карбиды внедрения – в них атомы углерода занимают пустоты в кристаллических решетках металлов, имеют, как правило, переменный состав W 2 С. Соединения обладают большой твердостью и высокими температурами плавления, химической стойкостью • в) Ковалентные карбиды – образуются с элементами близкими по электроотрица- тельности (соседями по периодической системе), например, карбиды кремния и бора (Si. C, B 4 C 3).
 Кислородсодержащие соединения углерода Оксид углерода(II) - CO В СО кратность связи равна трем С == О: Две связи углерод – кислород образуются по обменному механизму, а третья – по донорно- акцепторному механизму за счет свободной орбитали атома углерода и двух электронов атома кислорода. СО - несолеобразующий оксид. В промышленности оксид углерода(II) получают, пропуская воздух через слой раскаленного угля: С + О 2 = СО 2; С + СО 2 <=> 2 СО, ΔΗ° = 172 к. Дж
Кислородсодержащие соединения углерода Оксид углерода(II) - CO В СО кратность связи равна трем С == О: Две связи углерод – кислород образуются по обменному механизму, а третья – по донорно- акцепторному механизму за счет свободной орбитали атома углерода и двух электронов атома кислорода. СО - несолеобразующий оксид. В промышленности оксид углерода(II) получают, пропуская воздух через слой раскаленного угля: С + О 2 = СО 2; С + СО 2 <=> 2 СО, ΔΗ° = 172 к. Дж
 смесь СО с азотом воздуха, называется генераторным газом или воздушный газом: 2 С + О 2 + 4 N 2 = 2 СО + 4 N 2 (воздушный газ) • СО + Сl 2 = СОСl 2 ( t, катализатор) Фосген – бесцветный газ, очень ядовит. Медленно гидролизуется : • СОСl 2 + 2 Н 2 О = Н 2 СО 3 + 2 НСl При нагревании реагирует с серой с образовани-ем бесцветного газа оксида-сульфида углерода: СО + S = СОS При нагревании и под давлением CO с водоро-дом образует метанол: • СО + 2 Н 2 <=> СН 3 ОН
смесь СО с азотом воздуха, называется генераторным газом или воздушный газом: 2 С + О 2 + 4 N 2 = 2 СО + 4 N 2 (воздушный газ) • СО + Сl 2 = СОСl 2 ( t, катализатор) Фосген – бесцветный газ, очень ядовит. Медленно гидролизуется : • СОСl 2 + 2 Н 2 О = Н 2 СО 3 + 2 НСl При нагревании реагирует с серой с образовани-ем бесцветного газа оксида-сульфида углерода: СО + S = СОS При нагревании и под давлением CO с водоро-дом образует метанол: • СО + 2 Н 2 <=> СН 3 ОН
 Оксид углерода(II) проявляет восстановительные свойства: • Fе 2 О 3 + 3 СО = 2 Fе + 3 СО 2 • При обычных условиях СО восстанавливает Рd и Ag из их солей: • Рd. Сl 2 + СО + Н 2 О = Рd + СО 2 + 2 НСl • При повышенной t и под давлением СО может соединяться с некоторыми металлами, образуя карбонилы: • Fе + 5 СО = Fе(СО)5 ; Cr + 6 СО = Сr(СО)6
Оксид углерода(II) проявляет восстановительные свойства: • Fе 2 О 3 + 3 СО = 2 Fе + 3 СО 2 • При обычных условиях СО восстанавливает Рd и Ag из их солей: • Рd. Сl 2 + СО + Н 2 О = Рd + СО 2 + 2 НСl • При повышенной t и под давлением СО может соединяться с некоторыми металлами, образуя карбонилы: • Fе + 5 СО = Fе(СО)5 ; Cr + 6 СО = Сr(СО)6
 Оксид углерода(IV) – СО 2 В молекуле СО 2 атом углерода находится в состоянии sp-гибридизации и молекула имеет линейное строение О = С = О Са. СО 3 + 2 НСl = Са. Сl 2 + СО 2↑ + Н 2 О СО 2 + Н 2 О <=> Н 2 СО 3 <=> Н+ + НСО 3¯ <=> Н+ + СО 32¯ Буферная система Н 2 СО 3 – НСО 3¯ служит главной буферной системой плазмы крови, поддерживает постоянное значение р. Н крови порядка 7, 4
Оксид углерода(IV) – СО 2 В молекуле СО 2 атом углерода находится в состоянии sp-гибридизации и молекула имеет линейное строение О = С = О Са. СО 3 + 2 НСl = Са. Сl 2 + СО 2↑ + Н 2 О СО 2 + Н 2 О <=> Н 2 СО 3 <=> Н+ + НСО 3¯ <=> Н+ + СО 32¯ Буферная система Н 2 СО 3 – НСО 3¯ служит главной буферной системой плазмы крови, поддерживает постоянное значение р. Н крови порядка 7, 4
 СО 2 легко реагирует со щелочами, образуя средние (карбонаты) или кислые соли (гидрокарбонаты): • СО 2 + Са(ОН)2 = Са. СО 3 + Н 2 О • Са. СО 3 + СО 2 + Н 2 О = Са(НСО 3)2 При действии Nа 2 СО 3 на растворы сильно гидролизующихся солей (Аl 3+, Сr 3+, Fе 3+ и др. ) образуются гидроксиды металлов: 2 Мg. Сl 2+2 Nа 2 СО 3+Н 2 О =(Мg. ОН)2 СО 3 +СО 2↑+4 Nа. Сl 2 Аl. Сl 3 +3 Nа 2 СО 3+3 Н 2 О = 2 Аl(ОН)3↓ +3 СО 2↑+6 Nа. Сl
СО 2 легко реагирует со щелочами, образуя средние (карбонаты) или кислые соли (гидрокарбонаты): • СО 2 + Са(ОН)2 = Са. СО 3 + Н 2 О • Са. СО 3 + СО 2 + Н 2 О = Са(НСО 3)2 При действии Nа 2 СО 3 на растворы сильно гидролизующихся солей (Аl 3+, Сr 3+, Fе 3+ и др. ) образуются гидроксиды металлов: 2 Мg. Сl 2+2 Nа 2 СО 3+Н 2 О =(Мg. ОН)2 СО 3 +СО 2↑+4 Nа. Сl 2 Аl. Сl 3 +3 Nа 2 СО 3+3 Н 2 О = 2 Аl(ОН)3↓ +3 СО 2↑+6 Nа. Сl
 При нагревании: • Са. СО 3 = Са. О + СО 2↑ • Са(НСО 3)2 = Са. СО 3 + СО 2↑ + Н 2 О • (Сu. ОН)2 СО 3 = Сu. О + СО 2↑ + Н 2 О карбонаты натрия и калия плавятся без разложения Сильные кислоты вытесняют из карбонатов и гидрокарбонатов угольную кислоту: • К 2 СО 3 + 2 НСl = 2 КСl + СО 2↑ + Н 2 О • КНСО 3 + НСl = КСl + СО 2↑ + Н 2 О
При нагревании: • Са. СО 3 = Са. О + СО 2↑ • Са(НСО 3)2 = Са. СО 3 + СО 2↑ + Н 2 О • (Сu. ОН)2 СО 3 = Сu. О + СО 2↑ + Н 2 О карбонаты натрия и калия плавятся без разложения Сильные кислоты вытесняют из карбонатов и гидрокарбонатов угольную кислоту: • К 2 СО 3 + 2 НСl = 2 КСl + СО 2↑ + Н 2 О • КНСО 3 + НСl = КСl + СО 2↑ + Н 2 О
 Свойства кремния и его соединений Кристаллический кремний получают из кремнезема Si. О 2 • Si. О 2 + 2 С = Si + 2 СО • Si. О 2 + Мg = Si + 2 Мg. О Химически чистый Si термическим разложением Si. Н 4: Si. Н 4 = Si + 2 Н 2 кремний взаимодействует со многими неметаллами: • Si + 2 Сl 2 = Si. Сl 4 ( 400 о. С) • Si + О 2 = Si. О 2 ( 600 о. С) • Si + С = Si. С ( 2000 о. С)
Свойства кремния и его соединений Кристаллический кремний получают из кремнезема Si. О 2 • Si. О 2 + 2 С = Si + 2 СО • Si. О 2 + Мg = Si + 2 Мg. О Химически чистый Si термическим разложением Si. Н 4: Si. Н 4 = Si + 2 Н 2 кремний взаимодействует со многими неметаллами: • Si + 2 Сl 2 = Si. Сl 4 ( 400 о. С) • Si + О 2 = Si. О 2 ( 600 о. С) • Si + С = Si. С ( 2000 о. С)
 некоторыми расплавленными металлами кремний (Мg, Сu, Fе), образует силициды : • Si + 2 Мg = Мg 2 Si Кислоты на кремний не действуют, за исключением плавиковой кислоты или смеси азотной и плавиковой кислот: • Si + 6 НF + 4 НNО 3 = Н 2[Si. F 6] + 4 NО 2 + 4 Н 2 О хорошо растворяется в водных растворах щелочей: • Si + 2 Nа. ОН + Н 2 О = Nа 2 Si. О 3 + 2 Н 2↑ легко реагирует с галогенами, образуя галогениды Si. Г 4: Si + 2 F 2 = Si. F 4
некоторыми расплавленными металлами кремний (Мg, Сu, Fе), образует силициды : • Si + 2 Мg = Мg 2 Si Кислоты на кремний не действуют, за исключением плавиковой кислоты или смеси азотной и плавиковой кислот: • Si + 6 НF + 4 НNО 3 = Н 2[Si. F 6] + 4 NО 2 + 4 Н 2 О хорошо растворяется в водных растворах щелочей: • Si + 2 Nа. ОН + Н 2 О = Nа 2 Si. О 3 + 2 Н 2↑ легко реагирует с галогенами, образуя галогениды Si. Г 4: Si + 2 F 2 = Si. F 4
 Соединения кремния Получить галогениды кремния можно по реакциям: • Si. О 2 + 2 Сl 2 = Si. С 14 + 2 СО • Si. О 2 + 2 Са. F 2 + 2 Н 2 SО 4 = Si. F 4 + 2 Са. SО 4+2 Н 2 О Соединения кремния с водородом (Si. Н 4, Si 2 Н 6, Si 3 Н 8 и т. д. ) получают: Мg 2 Si + 4 НС 1 = Мg. С 12 + Si. Н 4 • Si. Н 4 + О 2 = Si. О 2 + Н 2 О • Si. Н 4 + 2 Н 2 О = Si. О 2 + 4 Н 2 • Si. Н 4 + 2 Nа. ОН + Н 2 О = Nа 2 Si. О 3 + 4 Н 2
Соединения кремния Получить галогениды кремния можно по реакциям: • Si. О 2 + 2 Сl 2 = Si. С 14 + 2 СО • Si. О 2 + 2 Са. F 2 + 2 Н 2 SО 4 = Si. F 4 + 2 Са. SО 4+2 Н 2 О Соединения кремния с водородом (Si. Н 4, Si 2 Н 6, Si 3 Н 8 и т. д. ) получают: Мg 2 Si + 4 НС 1 = Мg. С 12 + Si. Н 4 • Si. Н 4 + О 2 = Si. О 2 + Н 2 О • Si. Н 4 + 2 Н 2 О = Si. О 2 + 4 Н 2 • Si. Н 4 + 2 Nа. ОН + Н 2 О = Nа 2 Si. О 3 + 4 Н 2
 • Известны два оксида кремния Si. О и Si. О 2. Оксид кремния(II) в природе не встречается, получается при восстановлении кремнезема: • Si. О 2 + Si = Si. О • Si. О 2 + С = Si. О + СО медленно окисляется на воздухе: Si. О + О 2 = Si. О 2 легко растворяется в водных растворах щелочей: • Si. О + 2 Nа. ОН = Nа 2 Si. О 3 + Н 2 • Оксид кремния(IV) – кислотный оксид. Si. О 2 – бесцветное твердое вещество, нерастворимое в воде и кислотах (кроме НF). • Si. О 2 + 4 НF = Si. F 4 + 2 Н 2 О • Si. F 4 + 2 НF = Н 2[Si. F 6]
• Известны два оксида кремния Si. О и Si. О 2. Оксид кремния(II) в природе не встречается, получается при восстановлении кремнезема: • Si. О 2 + Si = Si. О • Si. О 2 + С = Si. О + СО медленно окисляется на воздухе: Si. О + О 2 = Si. О 2 легко растворяется в водных растворах щелочей: • Si. О + 2 Nа. ОН = Nа 2 Si. О 3 + Н 2 • Оксид кремния(IV) – кислотный оксид. Si. О 2 – бесцветное твердое вещество, нерастворимое в воде и кислотах (кроме НF). • Si. О 2 + 4 НF = Si. F 4 + 2 Н 2 О • Si. F 4 + 2 НF = Н 2[Si. F 6]
 Si. О 2 легко растворяется в кипящих водных растворах щелочей: Si. О 2 + 2 Nа. ОН = Nа 2 Si. О 3 + Н 2 О Кремневую кислоту Н 2 Si. О 3 получают косвенным путем, так как Si. О 2 нерастворим в воде: • Nа 2 Si. О 3 + 2 НС 1 = Н 2 Si. О 3 + 2 Nа. С 1 • Соли кремневой кислоты подвергаются гидролизу и растворы солей имеют щелочную реакцию: Nа 2 Si. О 3 + Н 2 О <=> Nа 2 Si 2 О 5 + 2 Nа. ОН Si. О 32 - + Н 2 О <=> НSi. О 3 -+ ОН- 2 НSi. О 3 -<=> Si 2 О 52 - + Н 2 О Обыкновенное стекло получают путем сплавления кремнезема с известняком и содой: Nа 2 СО 3+Са. СО 3+ 6 Si. О 2 = Nа 2 О · Са. О · 6 Si. О 2 + 2 СО 2↑
Si. О 2 легко растворяется в кипящих водных растворах щелочей: Si. О 2 + 2 Nа. ОН = Nа 2 Si. О 3 + Н 2 О Кремневую кислоту Н 2 Si. О 3 получают косвенным путем, так как Si. О 2 нерастворим в воде: • Nа 2 Si. О 3 + 2 НС 1 = Н 2 Si. О 3 + 2 Nа. С 1 • Соли кремневой кислоты подвергаются гидролизу и растворы солей имеют щелочную реакцию: Nа 2 Si. О 3 + Н 2 О <=> Nа 2 Si 2 О 5 + 2 Nа. ОН Si. О 32 - + Н 2 О <=> НSi. О 3 -+ ОН- 2 НSi. О 3 -<=> Si 2 О 52 - + Н 2 О Обыкновенное стекло получают путем сплавления кремнезема с известняком и содой: Nа 2 СО 3+Са. СО 3+ 6 Si. О 2 = Nа 2 О · Са. О · 6 Si. О 2 + 2 СО 2↑
 Применение
Применение

