Растворы ВМВ мед-проф.pptx
- Количество слайдов: 59
 Лекция Высокомолекулярные вещества (ВМВ) 1. Основные понятия. Классификация. 2. Свойства растворов. 3. Набухание. 4. Вязкость. 5. Осмотическое давление. 6. Агрегативная устойчивость белков. Высаливание. Денатурация. Коацервация. Лектор: Ганзина Ирина Викторовна доцент кафедры химии кандидат биологических наук
Лекция Высокомолекулярные вещества (ВМВ) 1. Основные понятия. Классификация. 2. Свойства растворов. 3. Набухание. 4. Вязкость. 5. Осмотическое давление. 6. Агрегативная устойчивость белков. Высаливание. Денатурация. Коацервация. Лектор: Ганзина Ирина Викторовна доцент кафедры химии кандидат биологических наук
 Высокомолекулярные вещества (полимеры) – это вещества с молекулярной массой от десяти тысяч до нескольких миллионов единиц. Размеры молекул ВМВ в вытянутом состоянии могут достигать 1000 нм. Температура кипения ВМВ значительно выше температуры разложения, поэтому они существуют, как правило, в жидком, аморфном или твердом состоянии.
Высокомолекулярные вещества (полимеры) – это вещества с молекулярной массой от десяти тысяч до нескольких миллионов единиц. Размеры молекул ВМВ в вытянутом состоянии могут достигать 1000 нм. Температура кипения ВМВ значительно выше температуры разложения, поэтому они существуют, как правило, в жидком, аморфном или твердом состоянии.
 По происхождению ВМВ делятся на природные, искусственные и синтетические. Природные ВМВ или биополимеры (белки, нуклеиновые кислоты, полисахариды, а также биополимеры смешанного типа – гликопротеины, нуклеопротеины и др. ) являются структурной основой всех живых организмов.
По происхождению ВМВ делятся на природные, искусственные и синтетические. Природные ВМВ или биополимеры (белки, нуклеиновые кислоты, полисахариды, а также биополимеры смешанного типа – гликопротеины, нуклеопротеины и др. ) являются структурной основой всех живых организмов.
 Природный каучук выделяют из Hevea brasilensis
Природный каучук выделяют из Hevea brasilensis
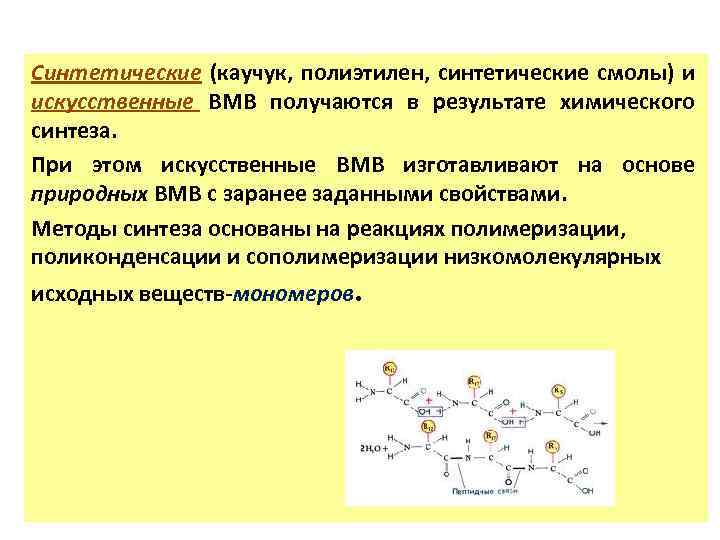 Синтетические (каучук, полиэтилен, синтетические смолы) и искусственные ВМВ получаются в результате химического синтеза. При этом искусственные ВМВ изготавливают на основе природных ВМВ с заранее заданными свойствами. Методы синтеза основаны на реакциях полимеризации, поликонденсации и сополимеризации низкомолекулярных исходных веществ-мономеров.
Синтетические (каучук, полиэтилен, синтетические смолы) и искусственные ВМВ получаются в результате химического синтеза. При этом искусственные ВМВ изготавливают на основе природных ВМВ с заранее заданными свойствами. Методы синтеза основаны на реакциях полимеризации, поликонденсации и сополимеризации низкомолекулярных исходных веществ-мономеров.
 • Степенью полимеризации n называется повторяющихся звеньев в макромолекуле. число Любой синтетический полимер состоит из макромолекул разной степени полимеризации и характеризуется полидисперсностью
• Степенью полимеризации n называется повторяющихся звеньев в макромолекуле. число Любой синтетический полимер состоит из макромолекул разной степени полимеризации и характеризуется полидисперсностью
 По строению полимерной цепи ВМВ бывают линейными, разветвленными и пространственными. Например, • целлюлоза (растительный полисахарид) - имеет линейную структуру, • гликоген (животный полисахарид) – имеет разветвленную структуру, • фенопласты – имеет пространственную сетчатую структуру.
По строению полимерной цепи ВМВ бывают линейными, разветвленными и пространственными. Например, • целлюлоза (растительный полисахарид) - имеет линейную структуру, • гликоген (животный полисахарид) – имеет разветвленную структуру, • фенопласты – имеет пространственную сетчатую структуру.
 Конфигурация синтетических полимеров линейные разветвленные сшитые сверхразветвленные дендримеры
Конфигурация синтетических полимеров линейные разветвленные сшитые сверхразветвленные дендримеры
 В животном организме присутствуют в основном плохорастворимые полимеры разветвленной и пространственной структур.
В животном организме присутствуют в основном плохорастворимые полимеры разветвленной и пространственной структур.
 Для молекул белков известно 4 уровня структурной организации. Первичная структура – это последовательность аминокислотных остатков в полипептидной цепи. NH 2 -Tyr-Pro-Lys-Gly-Phe-Tyr-Lys-COOH.
Для молекул белков известно 4 уровня структурной организации. Первичная структура – это последовательность аминокислотных остатков в полипептидной цепи. NH 2 -Tyr-Pro-Lys-Gly-Phe-Tyr-Lys-COOH.
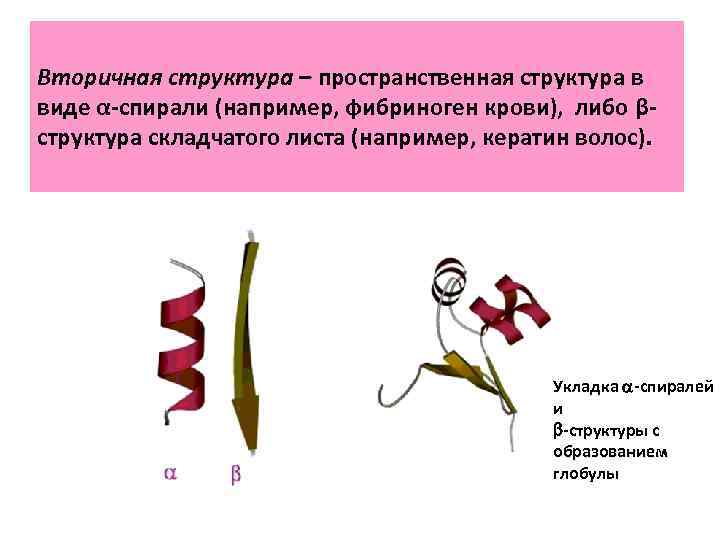 Вторичная структура – пространственная структура в виде α-спирали (например, фибриноген крови), либо βструктура складчатого листа (например, кератин волос). Укладка a-спиралей и b-структуры с образованием глобулы
Вторичная структура – пространственная структура в виде α-спирали (например, фибриноген крови), либо βструктура складчатого листа (например, кератин волос). Укладка a-спиралей и b-структуры с образованием глобулы
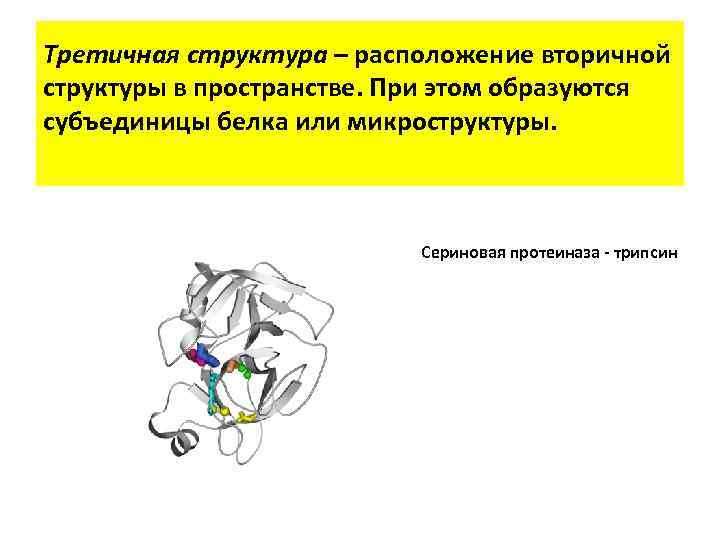 Третичная структура – расположение вторичной структуры в пространстве. При этом образуются субъединицы белка или микроструктуры. Сериновая протеиназа - трипсин
Третичная структура – расположение вторичной структуры в пространстве. При этом образуются субъединицы белка или микроструктуры. Сериновая протеиназа - трипсин
 Третичная структура ацилтрансфераза пиктатлиаза С
Третичная структура ацилтрансфераза пиктатлиаза С
 Четвертичная структура – объединение субъединиц в макроструктуры (например, гемоглобин крови).
Четвертичная структура – объединение субъединиц в макроструктуры (например, гемоглобин крови).

 По способности к электролитической диссоциации ВМВ делятся на • Неэлектролиты (каучуки); • Полиэлектролиты (белки). Полиэлектролиты подразделяются на: • поликислоты, • полиоснования, • полиамфолиты.
По способности к электролитической диссоциации ВМВ делятся на • Неэлектролиты (каучуки); • Полиэлектролиты (белки). Полиэлектролиты подразделяются на: • поликислоты, • полиоснования, • полиамфолиты.
 Полимеры имеют две особенности строения молекул: 1. Существование двух типов связи: - химические связи (энергия связи порядка десятков и сотен к. Дж / моль); - межмолекулярные силы Ван-дер-Ваальса (энергия связи порядка единиц и десятков к. Дж / моль). 2. Гибкость цепей, обусловленная внутренним вращением звеньев. Благодаря этому макромолекула ВМВ может принимать различные конформации- пространственные формы макромолекул. Конформация представляет собой пространственную форму макромолекулы, соответствующую максимуму энтропии.
Полимеры имеют две особенности строения молекул: 1. Существование двух типов связи: - химические связи (энергия связи порядка десятков и сотен к. Дж / моль); - межмолекулярные силы Ван-дер-Ваальса (энергия связи порядка единиц и десятков к. Дж / моль). 2. Гибкость цепей, обусловленная внутренним вращением звеньев. Благодаря этому макромолекула ВМВ может принимать различные конформации- пространственные формы макромолекул. Конформация представляет собой пространственную форму макромолекулы, соответствующую максимуму энтропии.
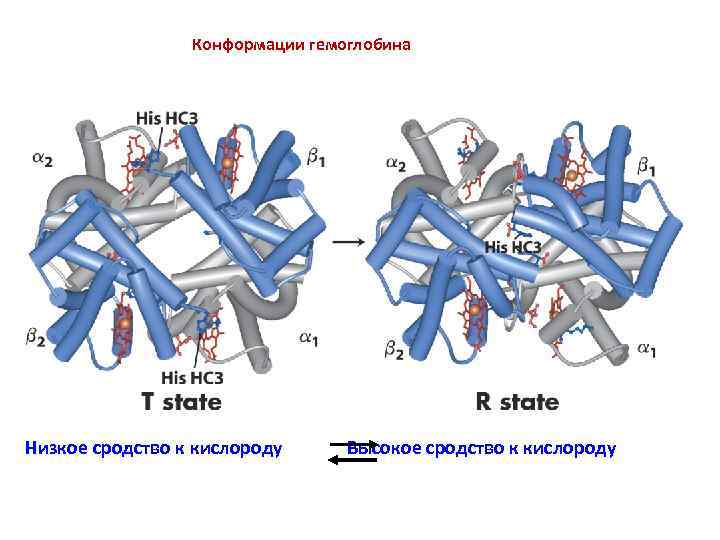 Конформации гемоглобина Низкое сродство к кислороду Высокое сродство к кислороду
Конформации гемоглобина Низкое сродство к кислороду Высокое сродство к кислороду
 Конформационными переходами можно объяснить многие процессы, происходящие в организме, например, регуляцию активности ферментов. Гибкость как свойство молекулы обусловливает эластичность как свойство материала (например, эластичность волос, кожи и т. п. ).
Конформационными переходами можно объяснить многие процессы, происходящие в организме, например, регуляцию активности ферментов. Гибкость как свойство молекулы обусловливает эластичность как свойство материала (например, эластичность волос, кожи и т. п. ).
 Свойства растворов ВМВ Растворы ВМВ являются лиофильными коллоидными системами. Для них характерны свойства как общие с растворами низкомолекулярных веществ и коллоидными системами, так и специфические. Растворы ВМВ с истинными растворами имеют ряд общих свойств: 1. Образуются самопроизвольно. 2. Являются термодинамически устойчивыми и не требуют присутствия стабилизаторов.
Свойства растворов ВМВ Растворы ВМВ являются лиофильными коллоидными системами. Для них характерны свойства как общие с растворами низкомолекулярных веществ и коллоидными системами, так и специфические. Растворы ВМВ с истинными растворами имеют ряд общих свойств: 1. Образуются самопроизвольно. 2. Являются термодинамически устойчивыми и не требуют присутствия стабилизаторов.
 3. В растворах ВМВ взвешенными частицами являются не мицеллы, а гигантских размеров макромолекулы, способные диссоциировать на ионы. 4. В растворах ВМВ отсутствует четко выраженная поверхность раздела фаз, их можно разбавлять и концентрировать.
3. В растворах ВМВ взвешенными частицами являются не мицеллы, а гигантских размеров макромолекулы, способные диссоциировать на ионы. 4. В растворах ВМВ отсутствует четко выраженная поверхность раздела фаз, их можно разбавлять и концентрировать.
 С коллоидными гидрофобными системами растворы ВМВ объединяют : 1. Близкие размеры частиц (d = 10 -5 -10 -7 см) 2. Растворы ВМВ рассеивают падающий свет и при боковом освещении можно наблюдать размытый конус Тиндаля. 3. В МВ не проходят через полупроницаемую мембрану, поэтому способы очистки растворов ВМВ от электролитов сходны со способами очистки коллоидных растворов.
С коллоидными гидрофобными системами растворы ВМВ объединяют : 1. Близкие размеры частиц (d = 10 -5 -10 -7 см) 2. Растворы ВМВ рассеивают падающий свет и при боковом освещении можно наблюдать размытый конус Тиндаля. 3. В МВ не проходят через полупроницаемую мембрану, поэтому способы очистки растворов ВМВ от электролитов сходны со способами очистки коллоидных растворов.
 К специфическим свойствам растворов ВМВ относят: • набухание, • вязкость, • осмотическое давление.
К специфическим свойствам растворов ВМВ относят: • набухание, • вязкость, • осмотическое давление.
 • Набухание – это увеличение объема и массы полимера в результате избирательного поглощения низкомолекулярного вещества из жидкой или газообразной среды. При набухании молекулы растворителя заполняют пространство между макромолекулами, проникая в петли структур.
• Набухание – это увеличение объема и массы полимера в результате избирательного поглощения низкомолекулярного вещества из жидкой или газообразной среды. При набухании молекулы растворителя заполняют пространство между макромолекулами, проникая в петли структур.
 Различают набухание: • неограниченное; • ограниченное. Неограниченное набухание заканчивается растворением полимера. Например, растворение белка в воде.
Различают набухание: • неограниченное; • ограниченное. Неограниченное набухание заканчивается растворением полимера. Например, растворение белка в воде.
 Ограниченное набухание сопровождается увеличением объема и массы полимера без его растворения.
Ограниченное набухание сопровождается увеличением объема и массы полимера без его растворения.
 Количественной характеристикой процесса ограниченного набухания служит степень набухания (α), которая показывает отношение приращения объема или массы набухшего полимера к первоначальному объему или массе.
Количественной характеристикой процесса ограниченного набухания служит степень набухания (α), которая показывает отношение приращения объема или массы набухшего полимера к первоначальному объему или массе.
 • Набухание
• Набухание
 На степень набухания влияют: 1)Природа полимера и растворителя. Полярные ВМВ лучше набухают в полярных растворителях (например, белки в воде), неполярные в неполярных (например, каучук в бензоле).
На степень набухания влияют: 1)Природа полимера и растворителя. Полярные ВМВ лучше набухают в полярных растворителях (например, белки в воде), неполярные в неполярных (например, каучук в бензоле).
 2) Температура. Процесс набухания осуществляется в 2 стадии: I. Сольватация молекул полимера. Это экзотермический процесс, ∆H < 0. Поэтому на этой стадии при повышении температуры степень набухания понижается. II. Основная стадия набухания-увеличение объема и массы полимера- как правило, идет без теплового эффекта, иногда это эндотермический процесс. • Увеличение температуры на данной стадии приводит к повышению степени набухания полимера.
2) Температура. Процесс набухания осуществляется в 2 стадии: I. Сольватация молекул полимера. Это экзотермический процесс, ∆H < 0. Поэтому на этой стадии при повышении температуры степень набухания понижается. II. Основная стадия набухания-увеличение объема и массы полимера- как правило, идет без теплового эффекта, иногда это эндотермический процесс. • Увеличение температуры на данной стадии приводит к повышению степени набухания полимера.
 3) Присутствие электролитов. Анионы способствуют набуханию в большей степени, чем катионы. По способности увеличивать степень набухания составлены лиотропные ряды: SCN- > I- > Br- > Cl- > SO 42 -. Из катионов: K+ и Na+ способствуют набуханию, Ca 2+ - препятствуют. 4) p. H среды. Наименьшая степень набухания полимера, в частности белков, наблюдается в их изоэлектрической точке.
3) Присутствие электролитов. Анионы способствуют набуханию в большей степени, чем катионы. По способности увеличивать степень набухания составлены лиотропные ряды: SCN- > I- > Br- > Cl- > SO 42 -. Из катионов: K+ и Na+ способствуют набуханию, Ca 2+ - препятствуют. 4) p. H среды. Наименьшая степень набухания полимера, в частности белков, наблюдается в их изоэлектрической точке.
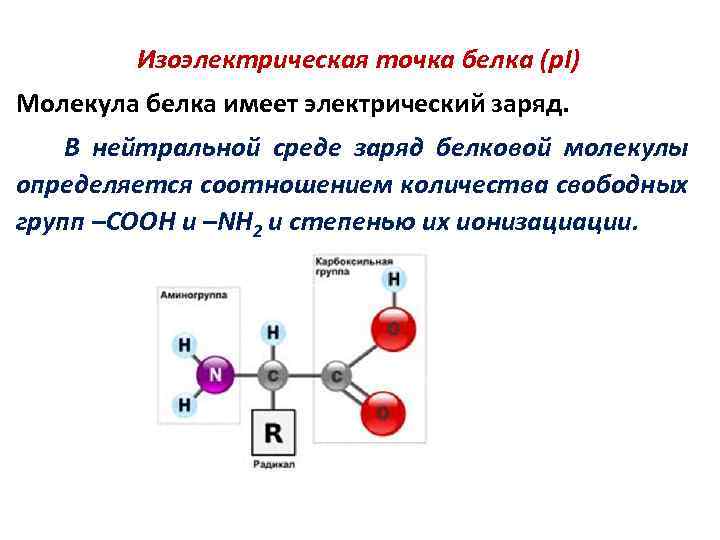 Изоэлектрическая точка белка (p. I) Молекула белка имеет электрический заряд. В нейтральной среде заряд белковой молекулы определяется соотношением количества свободных групп –COOH и –NH 2 и степенью их ионизациации.
Изоэлектрическая точка белка (p. I) Молекула белка имеет электрический заряд. В нейтральной среде заряд белковой молекулы определяется соотношением количества свободных групп –COOH и –NH 2 и степенью их ионизациации.
 • Чем больше карбоксильных групп –COOH, тем выше отрицательный заряд, и белок будет проявлять свойства слабой кислоты. • Преобладание амино-групп –NH 2 сообщает белку основные свойства и положительный заряд. В кислой среде белок заряжается положительно, в щелочной отрицательно.
• Чем больше карбоксильных групп –COOH, тем выше отрицательный заряд, и белок будет проявлять свойства слабой кислоты. • Преобладание амино-групп –NH 2 сообщает белку основные свойства и положительный заряд. В кислой среде белок заряжается положительно, в щелочной отрицательно.
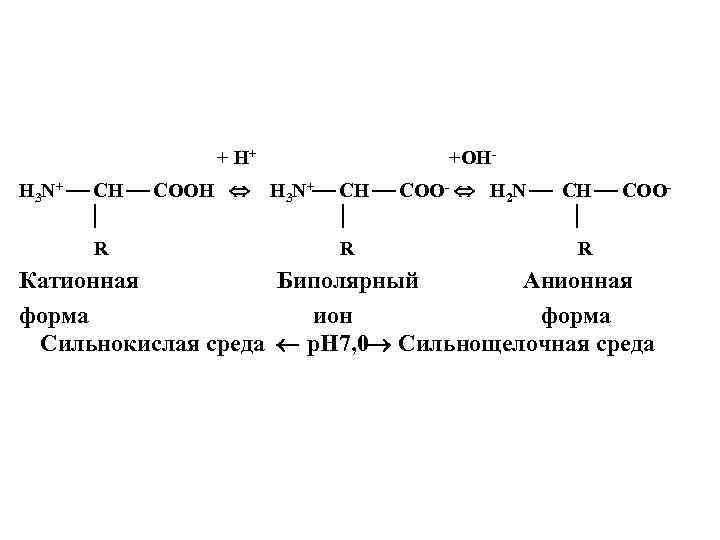 + H+ H 3 N+ CH COOH R +ОHH 3 N+ CH COO- H 2 N CH COO R R Катионная Биполярный Анионная форма ион форма Сильнокислая среда p. H 7, 0 Сильнощелочная среда
+ H+ H 3 N+ CH COOH R +ОHH 3 N+ CH COO- H 2 N CH COO R R Катионная Биполярный Анионная форма ион форма Сильнокислая среда p. H 7, 0 Сильнощелочная среда
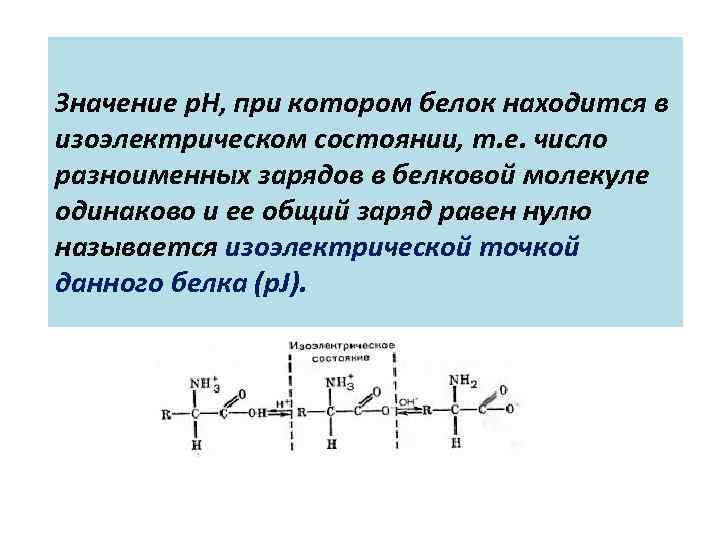 Значение p. H, при котором белок находится в изоэлектрическом состоянии, т. е. число разноименных зарядов в белковой молекуле одинаково и ее общий заряд равен нулю называется изоэлектрической точкой данного белка (p. J).
Значение p. H, при котором белок находится в изоэлектрическом состоянии, т. е. число разноименных зарядов в белковой молекуле одинаково и ее общий заряд равен нулю называется изоэлектрической точкой данного белка (p. J).
 Методы определения PJ: 1) По скорости коагуляции (max); 2) По скорости желатинирования (max); 3) По степени набухания (min); 4) По электрофоретической подвижности (в изоэлектрическом состоянии белок неподвижен в электрическом поле). Из-за электрического заряда белки разделяются на фракции при электрофорезе.
Методы определения PJ: 1) По скорости коагуляции (max); 2) По скорости желатинирования (max); 3) По степени набухания (min); 4) По электрофоретической подвижности (в изоэлектрическом состоянии белок неподвижен в электрическом поле). Из-за электрического заряда белки разделяются на фракции при электрофорезе.
 ВЯЗКОСТЬ РАСТВОРОВ ВМВ Растворы ВМВ отличаются аномальновысокой вязкостью. Это обусловлено следующими причинами: 1) Силами сцепления гидрофильных макромолекул ВМВ (белков или полисахаридов) с молекулами растворителя.
ВЯЗКОСТЬ РАСТВОРОВ ВМВ Растворы ВМВ отличаются аномальновысокой вязкостью. Это обусловлено следующими причинами: 1) Силами сцепления гидрофильных макромолекул ВМВ (белков или полисахаридов) с молекулами растворителя.
 2) Образованием ассоциатов при взаимодействии макромолекул между собой. При этом, чем выше концентрация раствора, тем больше макромолекул взаимодействуют между собой, образуя различные структуры, что приводит к увеличению вязкости.
2) Образованием ассоциатов при взаимодействии макромолекул между собой. При этом, чем выше концентрация раствора, тем больше макромолекул взаимодействуют между собой, образуя различные структуры, что приводит к увеличению вязкости.
 3) На аномально-высокую вязкость оказывает влияние форма и гибкость макромолекул полимера. Линейные частицы, особенно если они расположены поперек потока, оказывают большее сопротивление течению жидкости, чем сферические, поэтому вязкость раствора ВМВ с линейными частицами выше.
3) На аномально-высокую вязкость оказывает влияние форма и гибкость макромолекул полимера. Линейные частицы, особенно если они расположены поперек потока, оказывают большее сопротивление течению жидкости, чем сферические, поэтому вязкость раствора ВМВ с линейными частицами выше.
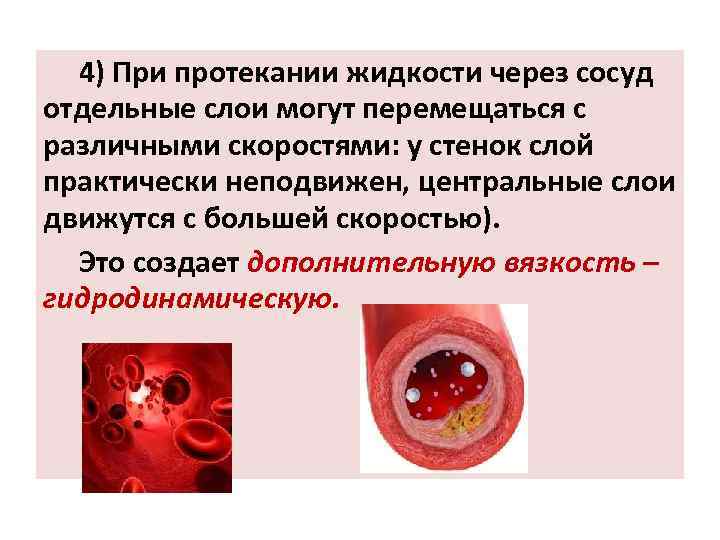 4) При протекании жидкости через сосуд отдельные слои могут перемещаться с различными скоростями: у стенок слой практически неподвижен, центральные слои движутся с большей скоростью). Это создает дополнительную вязкость – гидродинамическую.
4) При протекании жидкости через сосуд отдельные слои могут перемещаться с различными скоростями: у стенок слой практически неподвижен, центральные слои движутся с большей скоростью). Это создает дополнительную вязкость – гидродинамическую.
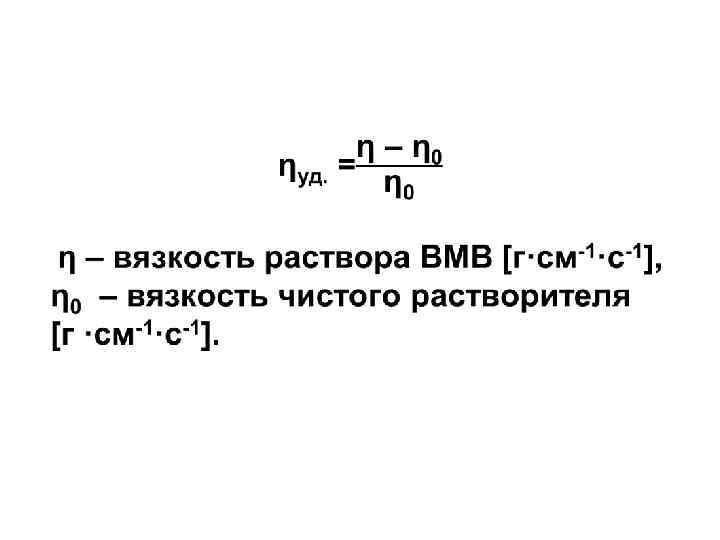
 5. Увеличение вязкости, связанное с изменением концентрации при растворении полимера принято характеризовать удельной вязкостью, которая показывает на какую величину повышается вязкость раствора ВМВ на единицу вязкости дисперсионной среды:
5. Увеличение вязкости, связанное с изменением концентрации при растворении полимера принято характеризовать удельной вязкостью, которая показывает на какую величину повышается вязкость раствора ВМВ на единицу вязкости дисперсионной среды:
 •
•
 Для линейной (вытянутой) формы макромолекул удельную вязкость рассчитывают по уравнению Штаудингера: ηуд. = К· Мr(X) · C(X) Мr –относительная молекулярная масса полимера; C (X) – весовая концентрация полимера [г · м-3]; К – константа, характеризующая особенности гомологического ряда полимера.
Для линейной (вытянутой) формы макромолекул удельную вязкость рассчитывают по уравнению Штаудингера: ηуд. = К· Мr(X) · C(X) Мr –относительная молекулярная масса полимера; C (X) – весовая концентрация полимера [г · м-3]; К – константа, характеризующая особенности гомологического ряда полимера.
 •
•
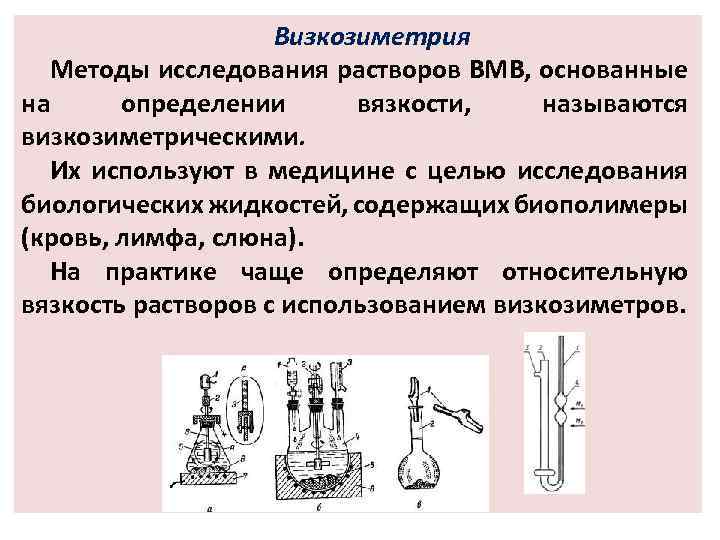 Визкозиметрия Методы исследования растворов ВМВ, основанные на определении вязкости, называются визкозиметрическими. Их используют в медицине с целью исследования биологических жидкостей, содержащих биополимеры (кровь, лимфа, слюна). На практике чаще определяют относительную вязкость растворов с использованием визкозиметров.
Визкозиметрия Методы исследования растворов ВМВ, основанные на определении вязкости, называются визкозиметрическими. Их используют в медицине с целью исследования биологических жидкостей, содержащих биополимеры (кровь, лимфа, слюна). На практике чаще определяют относительную вязкость растворов с использованием визкозиметров.
 Осмотическое давление растворов ВМВ В растворах ВМВ осмотическое давление имеет ряд особенностей. Это связано с тем, что макромолекула ВМВ может рассматриваться как совокупность молекул меньшего размера.
Осмотическое давление растворов ВМВ В растворах ВМВ осмотическое давление имеет ряд особенностей. Это связано с тем, что макромолекула ВМВ может рассматриваться как совокупность молекул меньшего размера.
 •
•
 Факторы, влияющие на осмотическое давление ВМВ: 1) Концентрация -с повышением концентрации ВМВ осмотическое давление возрастает. 2) Температура- при повышении температуры осмотическое давление возрастает. 3) p. H- в изоэлектрической точке осмотическое давление будет минимальным.
Факторы, влияющие на осмотическое давление ВМВ: 1) Концентрация -с повышением концентрации ВМВ осмотическое давление возрастает. 2) Температура- при повышении температуры осмотическое давление возрастает. 3) p. H- в изоэлектрической точке осмотическое давление будет минимальным.
 Агрегативная устойчивость белков. Высаливание. Денатурация. Коацервация. Агрегативная устойчивость – это способность системы сохранять определенную степень дисперсности, не объединяясь в более крупные агрегаты. Агрегативная устойчивость определяется: - наличием дзета-потенциала; - плотностью гидратной оболочки.
Агрегативная устойчивость белков. Высаливание. Денатурация. Коацервация. Агрегативная устойчивость – это способность системы сохранять определенную степень дисперсности, не объединяясь в более крупные агрегаты. Агрегативная устойчивость определяется: - наличием дзета-потенциала; - плотностью гидратной оболочки.
 Нарушить агрегативную устойчивость можно: 1. нейтрализацией заряда, т. е. снижением величины ζ-потенциала; 2. добавлением водоотнимающего средства, т. е. нарушением гидратной оболочки.
Нарушить агрегативную устойчивость можно: 1. нейтрализацией заряда, т. е. снижением величины ζ-потенциала; 2. добавлением водоотнимающего средства, т. е. нарушением гидратной оболочки.
 • Процесс осаждения белков с помощью концентрированных растворов солей называется высаливанием. При этом используют растворы Na 2 SO 4, (NH 4)2 SO 4, соли магния, фосфаты. • Наиболее эффективно высаливание проходит в изоэлектрической точке белка.
• Процесс осаждения белков с помощью концентрированных растворов солей называется высаливанием. При этом используют растворы Na 2 SO 4, (NH 4)2 SO 4, соли магния, фосфаты. • Наиболее эффективно высаливание проходит в изоэлектрической точке белка.

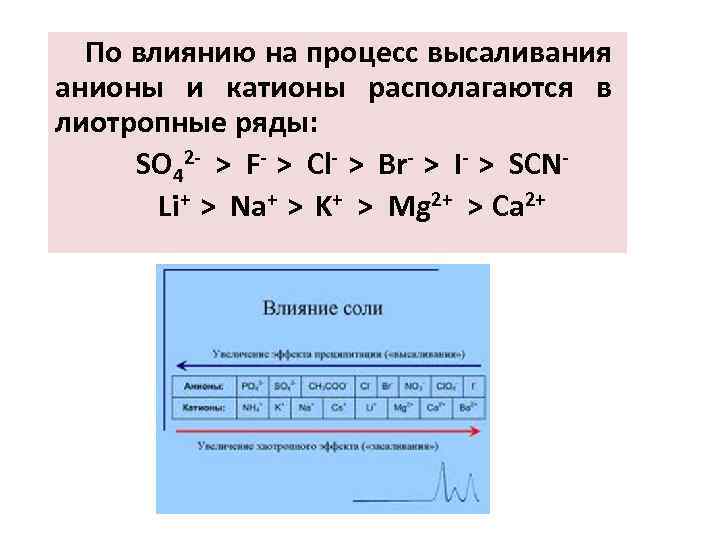 По влиянию на процесс высаливания анионы и катионы располагаются в лиотропные ряды: SO 42 - > F- > Cl- > Br- > I- > SCNLi+ > Na+ > K+ > Mg 2+ > Ca 2+
По влиянию на процесс высаливания анионы и катионы располагаются в лиотропные ряды: SO 42 - > F- > Cl- > Br- > I- > SCNLi+ > Na+ > K+ > Mg 2+ > Ca 2+
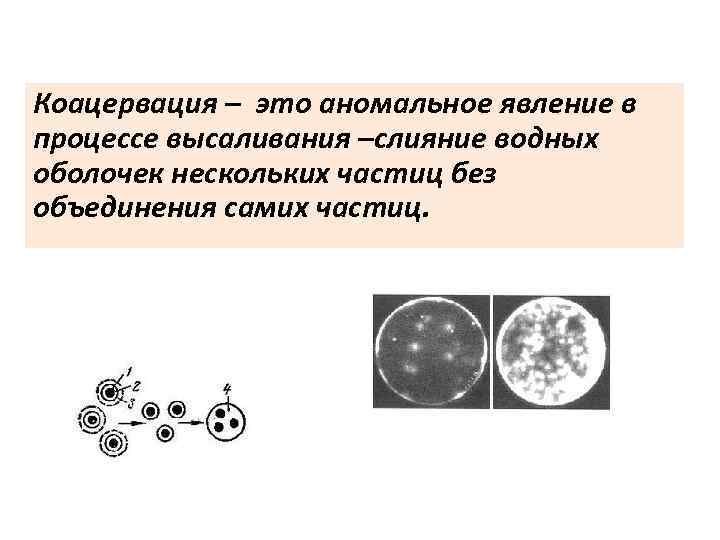 Коацервация – это аномальное явление в процессе высаливания –слияние водных оболочек нескольких частиц без объединения самих частиц.
Коацервация – это аномальное явление в процессе высаливания –слияние водных оболочек нескольких частиц без объединения самих частиц.
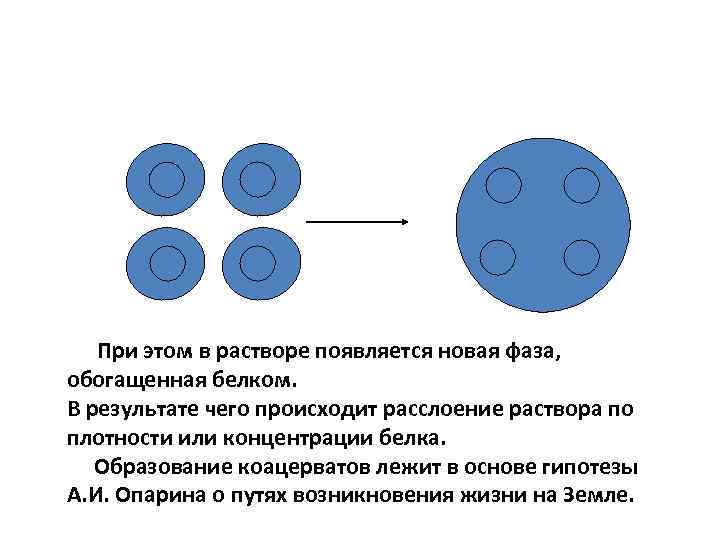 При этом в растворе появляется новая фаза, обогащенная белком. В результате чего происходит расслоение раствора по плотности или концентрации белка. Образование коацерватов лежит в основе гипотезы А. И. Опарина о путях возникновения жизни на Земле.
При этом в растворе появляется новая фаза, обогащенная белком. В результате чего происходит расслоение раствора по плотности или концентрации белка. Образование коацерватов лежит в основе гипотезы А. И. Опарина о путях возникновения жизни на Земле.
 Денатурация белка – это нарушение первоначальных свойств белка, вызванное изменением пространственной структуры его макромолекулы и сопровождающееся изменением физико-химических и биологических свойств белка Белки в процессе денатурации: • теряют гидрофильные свойства, • нарушаются форма и размеры макромолекул, • увеличивается вязкость растворов,
Денатурация белка – это нарушение первоначальных свойств белка, вызванное изменением пространственной структуры его макромолекулы и сопровождающееся изменением физико-химических и биологических свойств белка Белки в процессе денатурации: • теряют гидрофильные свойства, • нарушаются форма и размеры макромолекул, • увеличивается вязкость растворов,
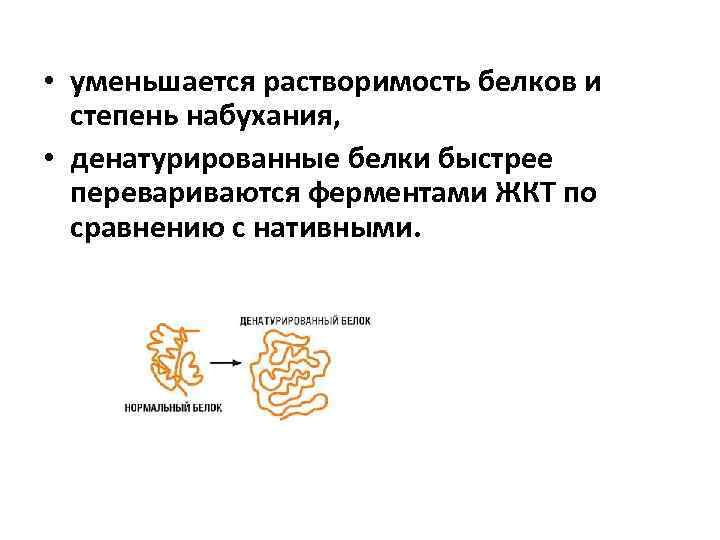 • уменьшается растворимость белков и степень набухания, • денатурированные белки быстрее перевариваются ферментами ЖКТ по сравнению с нативными.
• уменьшается растворимость белков и степень набухания, • денатурированные белки быстрее перевариваются ферментами ЖКТ по сравнению с нативными.
 Денатурация белков происходит под влиянием различных факторов: 1. Колебания температуры 2. Изменение р. Н раствора 3. Воздействие излучения 4. Добавление электролитов и др.
Денатурация белков происходит под влиянием различных факторов: 1. Колебания температуры 2. Изменение р. Н раствора 3. Воздействие излучения 4. Добавление электролитов и др.
 Благодарю за внимание!
Благодарю за внимание!


