Лекция 3 Электролиты.pptx
- Количество слайдов: 33

ЛЕКЦИЯ: Теория сильных и слабых электролитов

Электролитами называются вещества, которые в растворе или в расплаве частично или полностью распадаются на ионы и проводят электрический ток за счет движения ионов.

Сванте Аррениус В 1887 г. шведский учёный С. Аррениус для объяснения особенностей водных растворов веществ предложил теорию электролитической диссоциации.

1. Молекулы электролитов при растворении или расплавлении распадаются на ионы (+) и (-) заряженные. Процесс распада молекул электролитов на ионы называется электролитической диссоциацией или ионизацией.

2. Ионы движутся хаотически, а при пропускании электролитического тока (+) заряженные частицы (Kat) двигаются к (-) заряженному электроду - катоду (Cu. OH+; Fe. OH²+; NH 4+), а (-) заряженные частицы(An) - к (+) заряженному электроду аноду (Cl-; SO 3²-; Cr 2 O 7²-; H 2 PO 4 -; HCO 3 -).

3. Диссоциация - процесс обратимый. Наряду с ионизацией распадом молекул на ионы идет процесс ассоциации или молизации (соединение ионов) Na 2 SO 4 ↔ 2 Na+ + SO 4²- 4. Общая сумма зарядов (Kat) равна общей сумме зарядов (An) и противоположна по знаку.
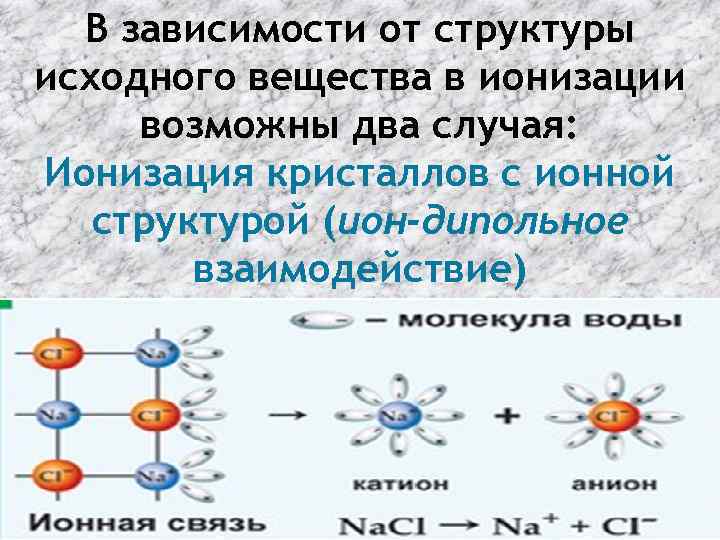
В зависимости от структуры исходного вещества в ионизации возможны два случая: Ионизация кристаллов с ионной структурой (ион-дипольное взаимодействие)
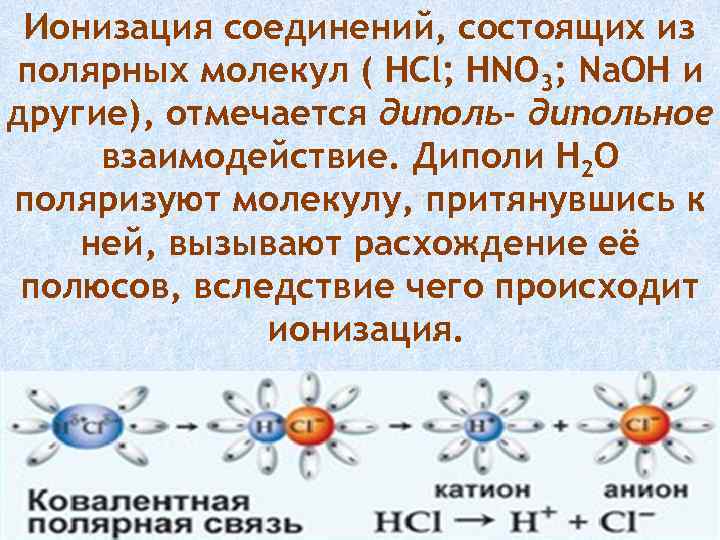
Ионизация соединений, состоящих из полярных молекул ( HCl; HNO 3; Na. OH и другие), отмечается диполь- дипольное взаимодействие. Диполи H 2 O поляризуют молекулу, притянувшись к ней, вызывают расхождение её полюсов, вследствие чего происходит ионизация.

Теория Аррениуса не учитывала влияние растворителя на процесс ионизации. Д. И. Менделеев и И. А. Каблуков дополнили теорию электролитической диссоциации: роль растворителя заключается не только в поляризации и разделении ионов противоположного знака, а также и в молизации, т. к. в результате диссоциации образуются не свободные ионы, а гидратированные (H 2 O) или сальватированные (с другим растворителем).

Образование гидратных (сальватных) оболочек способствует уменьшению электростатического взаимодействия ионов. Ослабление этого процесса происходит тем сильнее, чем больше величина диэлектрической проницаемости (ε) растворителя. Ионизация возможна в полярных растворителях (ε > 30): H 2 O-81; HCN-95; H 2 SO 4 -84. Малополярные растворители (ε=10 -30): пиридин-12, 5; этанол-25; не полярные растворители (ε<10): сероуглерод-2, 7; бензол-2, 3; гексан -1, 9 не обладают диссоциирующей способностью.

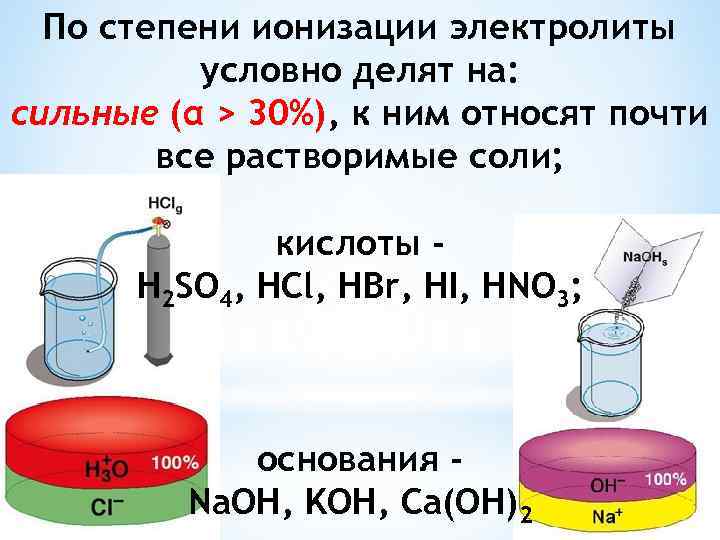
По степени ионизации электролиты условно делят на: сильные (α > 30%), к ним относят почти все растворимые соли; кислоты H 2 SO 4, HCl, HBr, HI, HNO 3; основания Na. OH, KOH, Ca(OH)2

cлабые (α < 3%), это большинство органических кислот, а также H 2 S, HCN, H 2 CO 3, H 2 SO 3, HCl. O, H 2 O, H 3 BO 3, Hg 2 Cl 2, Fe(SCN)3, Fe(OH)2, NH 4 OH, Pb(OH)2

электролиты средней силы (α=3 -30%)


На степень электролитической диссоциации влияют: ТЕМПЕРАТУРА: для эндотермических процессов (∆H > 0) увеличение t°C способствует > α; для экзотермических процессов (∆H < 0) уменьшение t°C способствует > α. КОНЦЕНТРАЦИЯ РАСТВОРА: при разбавлении растворов α значительно возрастает.

ДОБАВЛЕНИЕ ОДНОИМЕННОГО ИОНА: CH 3 COOH ↔ CH 3 OO¯ + H+ Например, введение сильного электролита CH 3 COONa ↔ CH 3 COO¯ + Na+ способствует увеличению концентрации CH 3 COO¯- иона, приводящему к сдвигу равновесия в лево, уменьшению α.



Суммарное уравнение: H 2 CO 3 + 2 H 2 O ↔ 2 H 3 O+ + CO 32 К общ. = К 1·К 2 Распад электролита по каждой последующей ступени происходит в меньшей степени, чем по предыдущей К 1>К 2>К 3 (для трехосновной Н 3 РО 4). Зная константу ионизации электролита, можно рассчитать степень ионизации.
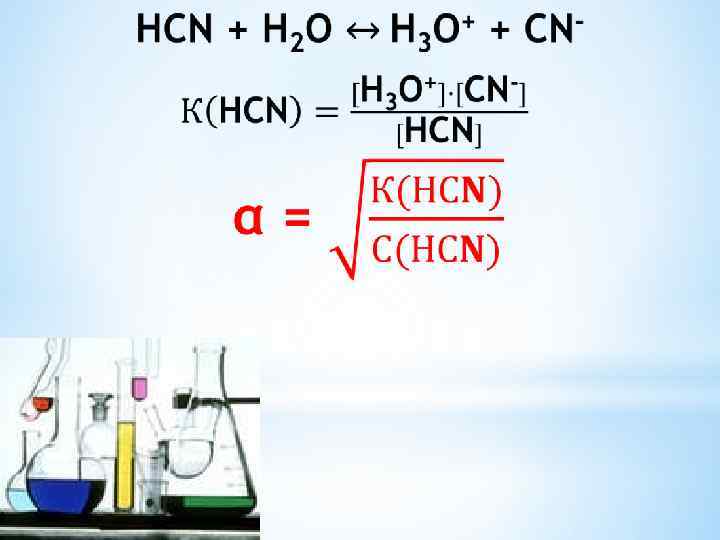

Эта формула отражает закон Оствальда: степень диссоциации слабого электролита возрастает с разбавлением раствора. Сильные электролиты не подчиняются этому закону.

ТЕОРИЯ ВОДНЫХ РАСТВОРОВ СИЛЬНЫХ ЭЛЕКТРОЛИТОВ сформулирована в 1923 году Дебаем и Хюккелем: 1. Сильные электролиты в растворе полярных растворителей ионизированы практически нацело (α≈ 100%).

2. В мало разбавленных растворах сильных электролитов среднее расстояние между ионами мало, а силы межионного взаимодействия велики. 3. В растворах сильных электролитов ионы не совсем свободны: движение их стеснено взаимным притяжением друг к другу.

Каждый ион электролита окружен противоположно заряженными ионами, получившими название «ИОННОЙ АТМОСФЕРЫ» , которая тормозит движение ионов и влияет на степень ионизации. α является кажущейся, т. к. она не соответствует действительной степени распада электролита на ионы из-за образования ионной атмосферы , ионных пар (дуплетов), триплетов.

Вследствие этого снижается эффективность ионов в таких явлениях, как перенос заряда (электрический ток) в растворах, понижение температуры замерзания, повышение температуры кипения, увеличение осмотического давления.

Таким образом, можно считать, что во всех процессах участвуют лишь «активные ионы» , т. е. ионы, не принимающие участия в данный момент в меж ионных взаимодействиях. Поэтому для оценки влияния ионной атмосферы пользуются активностью (а).

Активность – эффективная концентрация электролита, в соответствии с которой он участвует в химических процессах. а(х) = f(х) ∙ C(x) (моль/л) f (x) – коэффициент активности, который показывает отклонение свойств реальных растворов от идеальных.

В идеальных растворах а = С, а в реальных С > a. Экспериментально (f) и (а) можно определить криометрическим, осмометрическим, электрохимическим методом, а также можно рассчитать.


Количественной характеристикой меж ионных электростатических взаимодействий является ионная сила раствора - величина измеряемая полу суммой произведений концентраций всех ионов в растворе на квадрат их заряда: µ=1/2[C(x 1 2(x )∙Z 1)+ C(x 2 2(x )∙Z 2)+…]

Таким образом, при большой концентрации раствора силы меж ионного взаимодействия увеличиваются, µ растет, что приводит к уменьшению а и f. У слабых электролитов отсутствует «ионная атмосфера» и меж ионные электростатические взаимодействия, поэтому они в расчет не берутся.

Лекция 3 Электролиты.pptx