31 Регуляция водно-электролитного баланса.ppt
- Количество слайдов: 88

ЛЕКЦИЯ РЕГУЛЯЦИЯ ВОДНОЭЛЕКТРОЛИТНОГО БАЛАНСА А. Т. Марьянович, проф.

ПЛАН ЛЕКЦИИ ЗНАЧЕНИЕ ВОДНО-ЭЛЕКТРОЛИТНОГО ГОМЕОСТАЗА 1. ПРИНЦИПЫ ПОДДЕРЖАНИЯ ВОДНОЭЛЕКТРОЛИТНОГО ГОМЕОСТАЗА 2. ПОДДЕРЖАНИЕ ИЗОВОЛЮМИИ 3. ПОДДЕРЖАНИЕ ИЗОИОНИИ 4. ПОДДЕРЖАНИЕ ИЗООСМИИ 5. ПОДДЕРЖАНИЕ КИСЛОТНООСНОВНОГО РАВНОВЕСИЯ RÉSUMÉ

ВВЕДЕНИЕ ЗНАЧЕНИЕ ВОДНОЭЛЕКТРОЛИТНОГО ГОМЕОСТАЗА

В самом общем виде живой организм можно описать как водный раствор, заключенный в оболочку – поверхность тела. Knut Schmidt-Nielsen 1915 -2007 Animal Physiology: Adaptation and Environment

I ОСНОВНЫЕ ПРИНЦИПЫ

1/3 ВНЕ КЛЕТОЧНАЯ ВНУТРИ КЛЕТОЧНАЯ 2/3
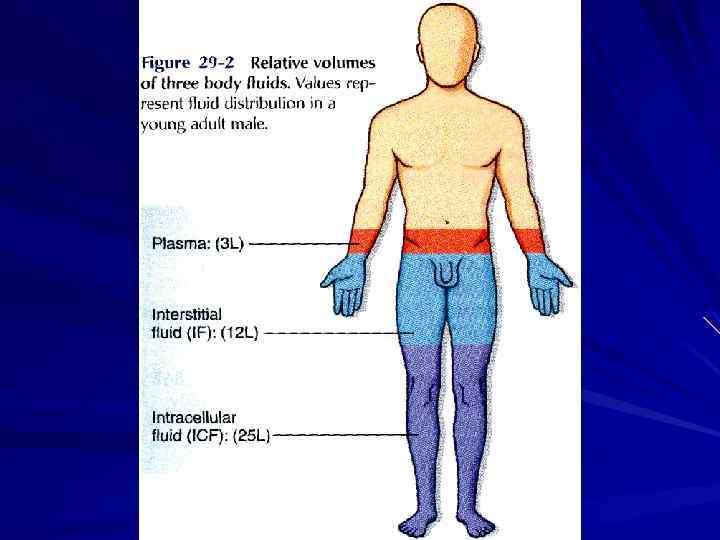

ТРИ КОМПАРТМЕНТА 1. ГДЕ ИМЕННО ПОДДЕРЖИВАЕТСЯ ПОСТОЯНСТВО СРЕДЫ? 2. ЧТО ЕГО НАРУШАЕТ? 3. ГДЕ ИЗМЕРЯЕМ ПАРАМЕТРЫ И ЧЕРЕЗ ЧТО ВОЗДЕЙСТВУЕМ НА ОРГАНИЗМ?

ПЛАЗМА КРОВИ 3 ИНТЕРСТИЦИЙ 12 ВНУТРИКЛЕТОЧНАЯ 25

ВОДНО-СОЛЕВОЙ БАЛАНС ИЗОВОЛЮМИЯ: объем крови ИЗОИОНИЯ: K+ Ca 2+ H 2 PO 4 ИЗООСМИЯ: осмолярность, Na+ КИСЛОТНО-ОСНОВНОЕ РАВНОВЕСИЕ: p. H
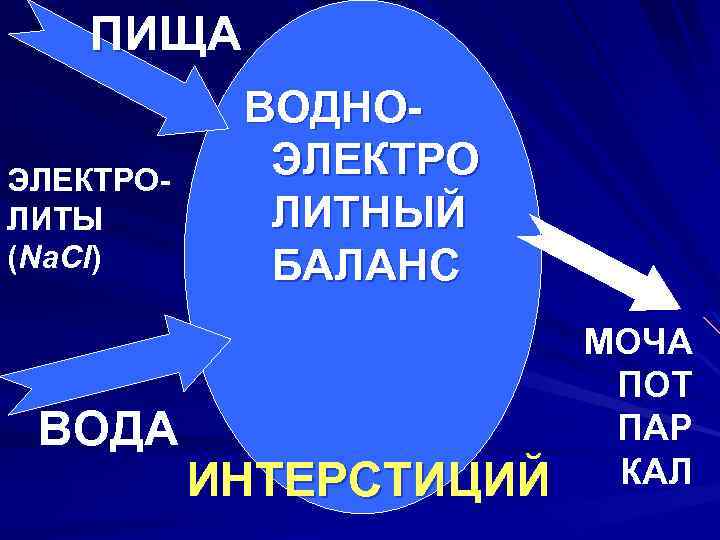
ПИЩА ЭЛЕКТРОЛИТЫ (Na. Cl) ВОДА ВОДНОЭЛЕКТРО ЛИТНЫЙ БАЛАНС ИНТЕРСТИЦИЙ МОЧА ПОТ ПАР КАЛ

ВОЗМУЩАЮЩИЕ ФАКТОРЫ

СОЛЕНАЯ ПИЩА

William Adolphe Bouguereau 1886


ЖАРА

ХОЛОД

II ИЗОВОЛЮМИЯ

НОРМА (л) ОБЪЕМ ЦИРКУЛИРУЮЩЕЙ КРОВИ – ОЦК ОБЪЕМ ЦИРКУЛИРУЮЩЕЙ ПЛАЗМЫ – ОЦП 5 3
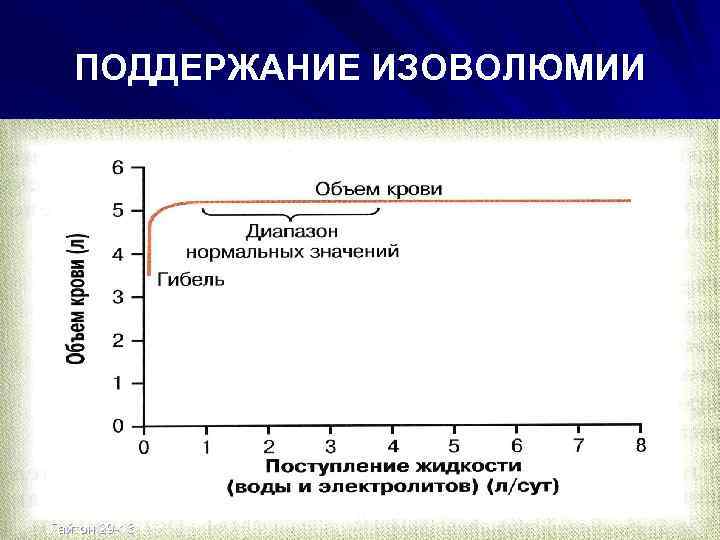
ПОДДЕРЖАНИЕ ИЗОВОЛЮМИИ Гайтон 29 -13
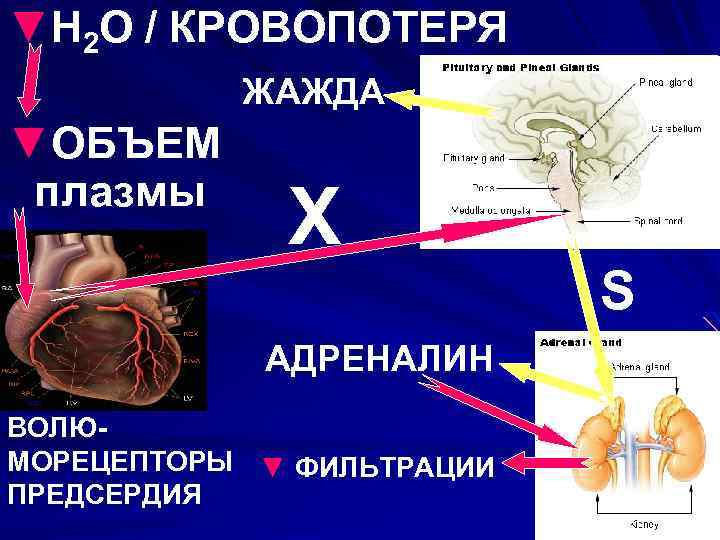
▼H 2 O / КРОВОПОТЕРЯ ЖАЖДА ▼ОБЪЕМ плазмы Х АДРЕНАЛИН ВОЛЮМОРЕЦЕПТОРЫ ▼ ФИЛЬТРАЦИИ ПРЕДСЕРДИЯ S

ГИПОВОЛЮМИЯ и ГИПОТОНИЯ СИЛЬНАЯ ГИПОВОЛЮМИЯ ВСЕГДА СОПРОВОЖДАЕТСЯ СНИЖЕНИЕМ АД: RAAS – РЕНИН-АНГИОТЕНЗИН АЛЬДОСТЕРОНОВАЯ СИСТЕМА ADH АДРЕНАЛИН

III ИЗОИОНИЯ
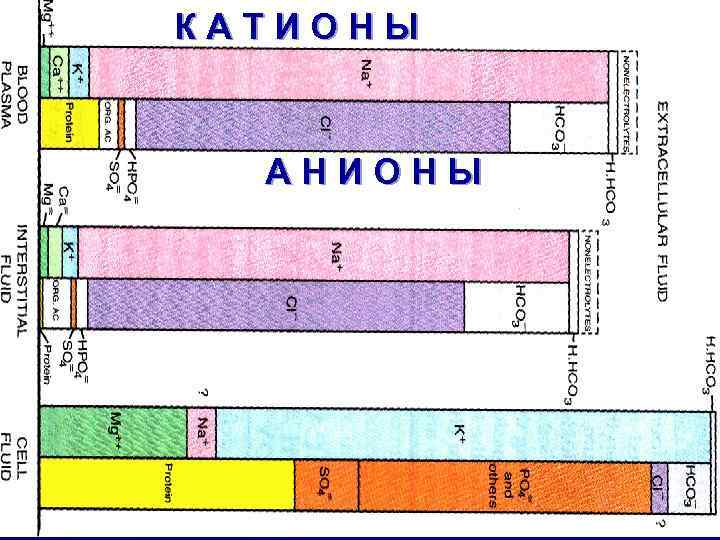
КАТИОНЫ АНИОНЫ

+ K

НОРМА КАЛИЯ во внеклеточной жидкости 4. 2 м. М
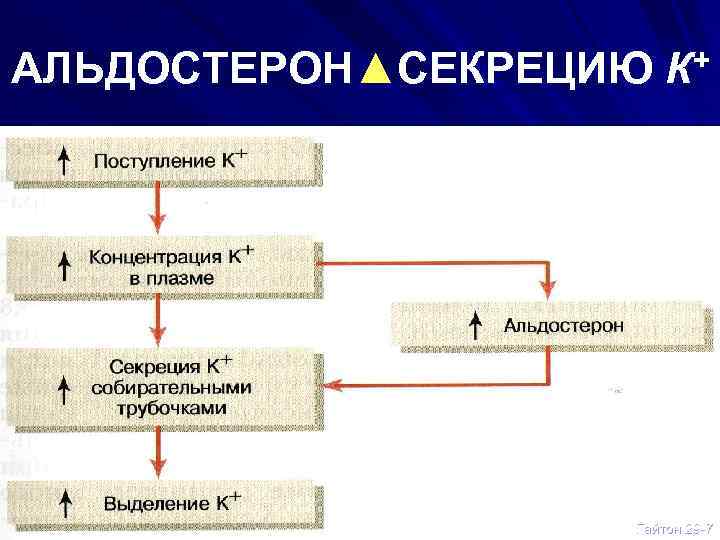
АЛЬДОСТЕРОН▲СЕКРЕЦИЮ К+ Гайтон 29 -7
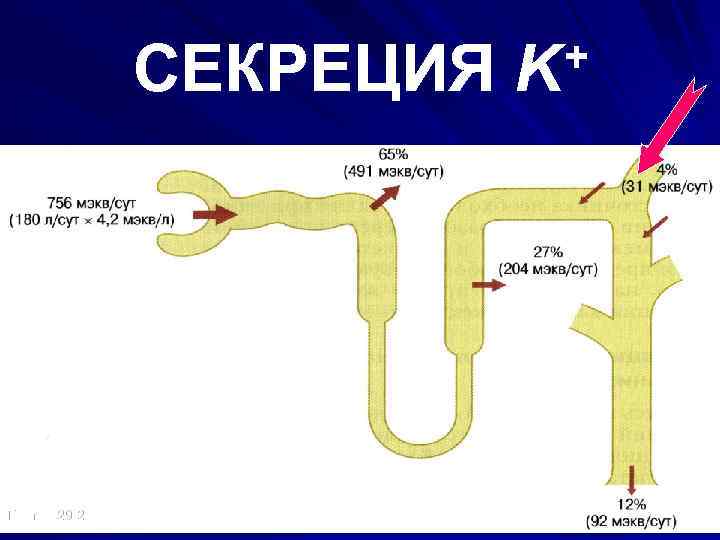
СЕКРЕЦИЯ Гайтон 29 -2 + K
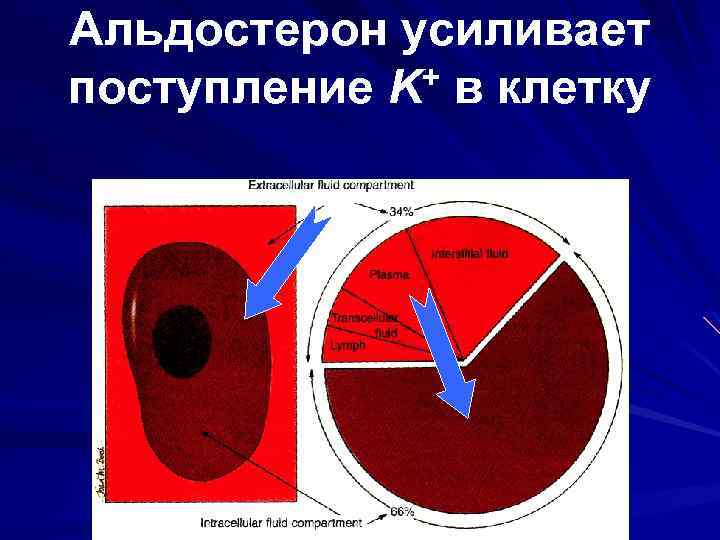
Альдостерон усиливает поступление K+ в клетку

АЛЬДОСТЕРОН и K+ АЛЬДОСТЕРОН УВЕЛИЧИВАЕТ: ПОГЛОЩЕНИЕ КЛЕТКОЙ СЕКРЕЦИЮ В ПОЧКЕ ВЫДЕЛЕНИЕ С ПОТОМ

2+ Ca
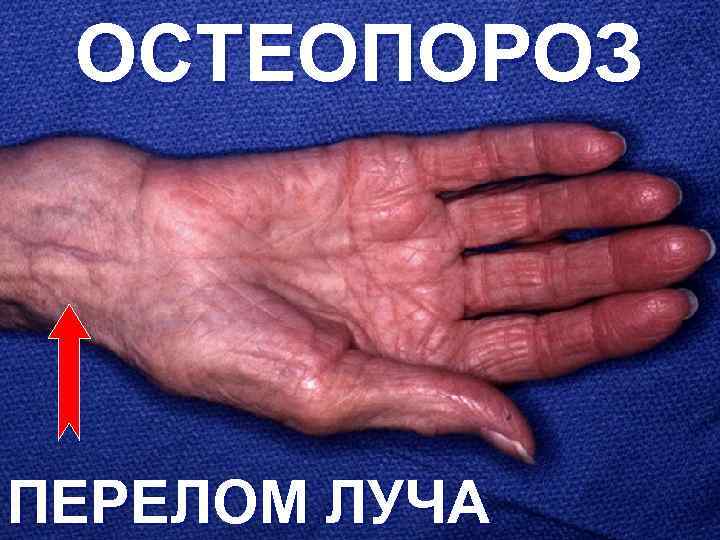
ОСТЕОПОРОЗ ПЕРЕЛОМ ЛУЧА

НОРМА Ca во внеклеточной жидкости 1. 2 м. М 9. 4 мг/100 мл
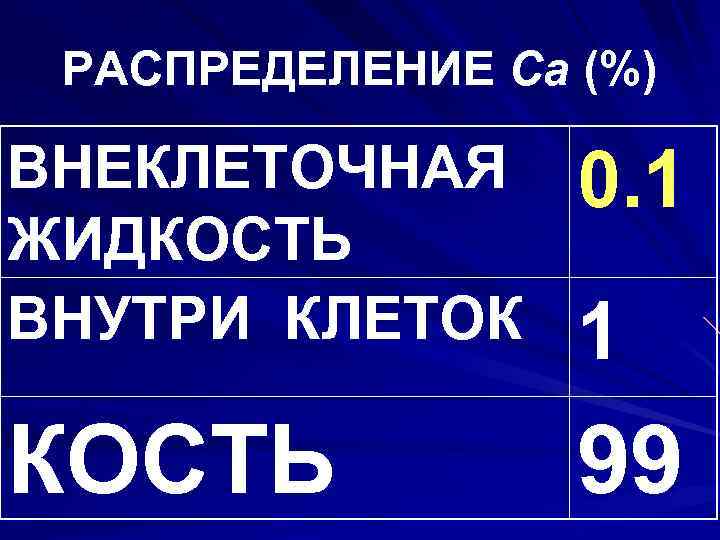
РАСПРЕДЕЛЕНИЕ Ca (%) ВНЕКЛЕТОЧНАЯ ЖИДКОСТЬ ВНУТРИ КЛЕТОК 0. 1 КОСТЬ 99 1
![▼[Ca 2+] плазмы ПЩЖ n = 84 PTH (паратирин) АКТИВИРУЕТ ОСТЕОКЛАСТЫ Ca 2+ ВСАСЫВАНИЕ ▼[Ca 2+] плазмы ПЩЖ n = 84 PTH (паратирин) АКТИВИРУЕТ ОСТЕОКЛАСТЫ Ca 2+ ВСАСЫВАНИЕ](https://present5.com/presentation/220064782_305865704/image-35.jpg)
▼[Ca 2+] плазмы ПЩЖ n = 84 PTH (паратирин) АКТИВИРУЕТ ОСТЕОКЛАСТЫ Ca 2+ ВСАСЫВАНИЕ РЕАБСОРБЦИЮ Ca 2+ В ПЛАЗМУ

C-КЛЕТКИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ n = 32 CT (кальцитонин) ▲ОСТЕОБЛАСТОВ ▲ЭКСКРЕЦИИ Са 2+ Ca УХОДИТ ИЗ ПЛАЗМЫ

IV ИЗООСМИЯ
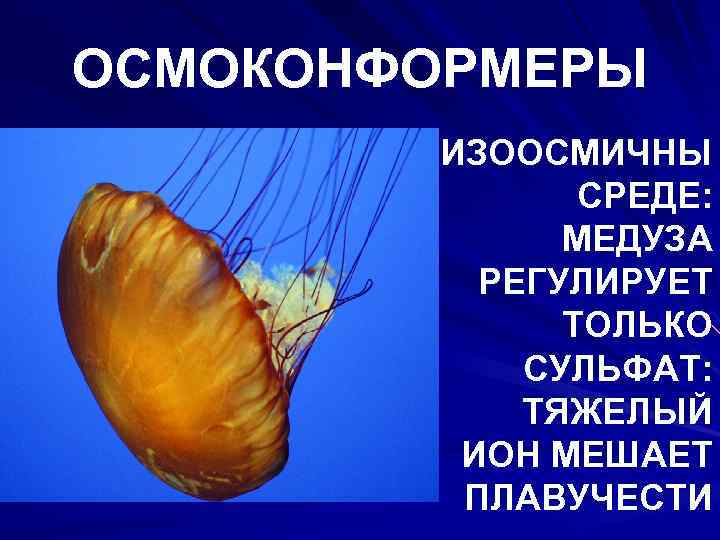
ОСМОКОНФОРМЕРЫ ИЗООСМИЧНЫ СРЕДЕ: МЕДУЗА РЕГУЛИРУЕТ ТОЛЬКО СУЛЬФАТ: ТЯЖЕЛЫЙ ИОН МЕШАЕТ ПЛАВУЧЕСТИ

ОСМОРЕГУЛЯТОРЫ Росм. ≈ const. КРАБ В СОЛОНОВАТОЙ ВОДЕ СОХРАНЯЕТ ВЫСОКОЕ Росм.

НОРМА ОСМОЛЯРНОСТИ 300 мосм/л 5500 мм рт. ст. 7. 2 атм.
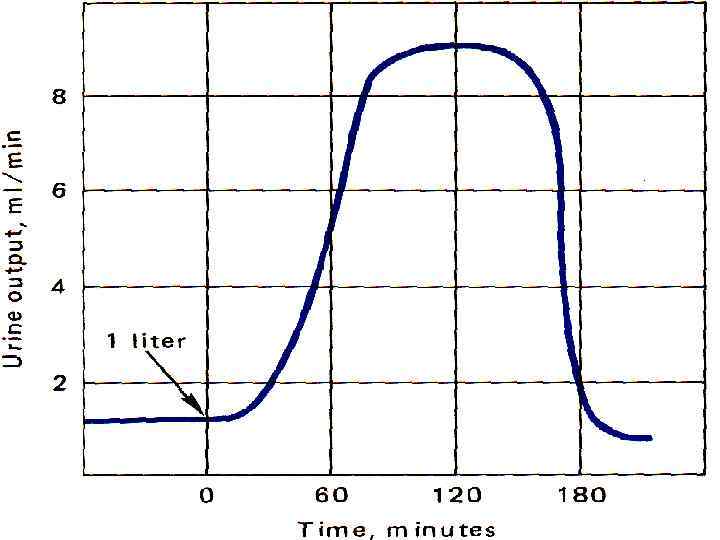
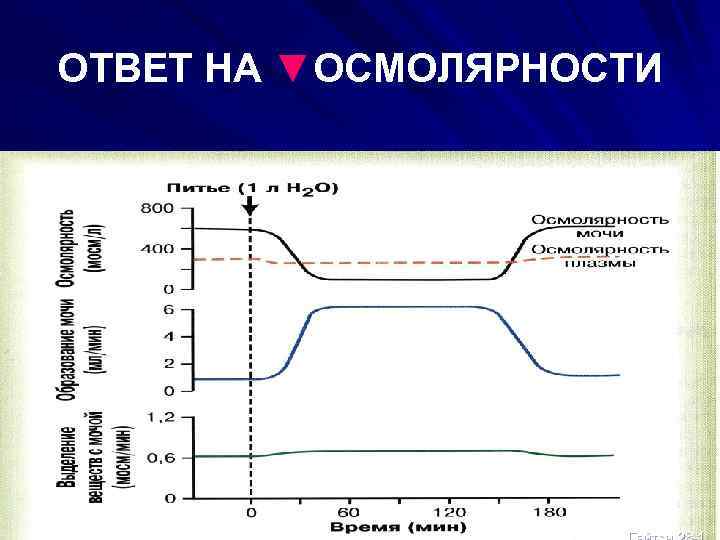
ОТВЕТ НА ▼ОСМОЛЯРНОСТИ

ОТВЕТ НА ▲ ОСМОЛЯРНОСТИ ▲ ЖАЖДА ADH (VP) ▲ ANP (атриальный натрийуретический пептид) ▼ АЛЬДОСТЕРОН ▲

Самое большое физиологическое преимущество жизни на суше состоит в доступности кислорода; наибольшей угрозой для наземной жизни является опасность высыхания. Knut Schmidt-Nielsen 1915 -2007 Animal Physiology: Adaptation and Environment

ВЛАГОПОТЕРИ ▼ массы тела (%) 1. 5 ЖАЖДА 4 8 ОГРАНИЧЕНИЕ ПОДВИЖНОСТИ НЕРАЗБОРЧИВОСТЬ РЕЧИ 20 СМЕРТЬ
![▼H 2 O ▲[Na+] ▲P осм. ПИТЬЕ ОСМОРЕЦЕПТОРЫ МОЗГА ЖАЖДА ▼H 2 O ▲[Na+] ▲P осм. ПИТЬЕ ОСМОРЕЦЕПТОРЫ МОЗГА ЖАЖДА](https://present5.com/presentation/220064782_305865704/image-46.jpg)
▼H 2 O ▲[Na+] ▲P осм. ПИТЬЕ ОСМОРЕЦЕПТОРЫ МОЗГА ЖАЖДА
![ЖАЖДА ▲ ВЛАГОПОТЕРЬ / ИЗБЫТОК Na. Cl ▲ [Na+] и ОСМОЛЯРНОСТИ ▲ ОСМОРЕЦЕПТОРОВ МОЗГА ЖАЖДА ▲ ВЛАГОПОТЕРЬ / ИЗБЫТОК Na. Cl ▲ [Na+] и ОСМОЛЯРНОСТИ ▲ ОСМОРЕЦЕПТОРОВ МОЗГА](https://present5.com/presentation/220064782_305865704/image-47.jpg)
ЖАЖДА ▲ ВЛАГОПОТЕРЬ / ИЗБЫТОК Na. Cl ▲ [Na+] и ОСМОЛЯРНОСТИ ▲ ОСМОРЕЦЕПТОРОВ МОЗГА ▲ ЖАЖДЫ ▲ ПИТЬЯ НОРМАЛИЗАЦИЯ [Na+] и ОСМОЛЯРНОСТИ
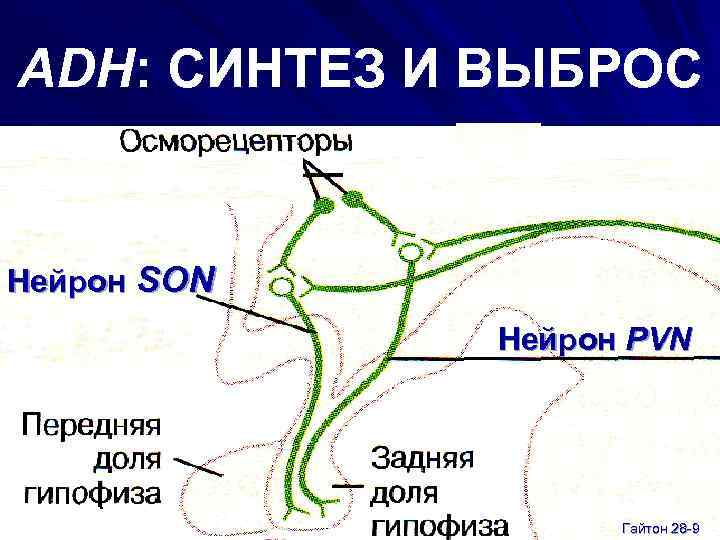
ADH: СИНТЕЗ И ВЫБРОС Нейрон SON Нейрон PVN Гайтон 28 -9
![▼ H 2 O ▲[Na+] ОСМОРЕЦЕПТОРЫ ▲Pосм. ГИПОТАЛ АМУС НЕЙРОГИПОФИЗ ▲ADH ▲РЕАБСОРБЦИЯ ВОДЫ ▼ H 2 O ▲[Na+] ОСМОРЕЦЕПТОРЫ ▲Pосм. ГИПОТАЛ АМУС НЕЙРОГИПОФИЗ ▲ADH ▲РЕАБСОРБЦИЯ ВОДЫ](https://present5.com/presentation/220064782_305865704/image-49.jpg)
▼ H 2 O ▲[Na+] ОСМОРЕЦЕПТОРЫ ▲Pосм. ГИПОТАЛ АМУС НЕЙРОГИПОФИЗ ▲ADH ▲РЕАБСОРБЦИЯ ВОДЫ

ОЦП и RAAS ▼ОЦП → ▼ АД → ▲РЕНИН → ▲АТ II → ▲АЛЬДОСТЕРОН → ▲РЕАБСОРБЦИЯ Na+ В ПОЧКЕ И ПОТОВЫХ ЖЕЛЕЗАХ → ▲РЕАБСОРБЦИЯ ВОДЫ В ПОЧКЕ → ▲АТ II → МОЗГ →▲ЖАЖДА →▲ПИТЬЕ
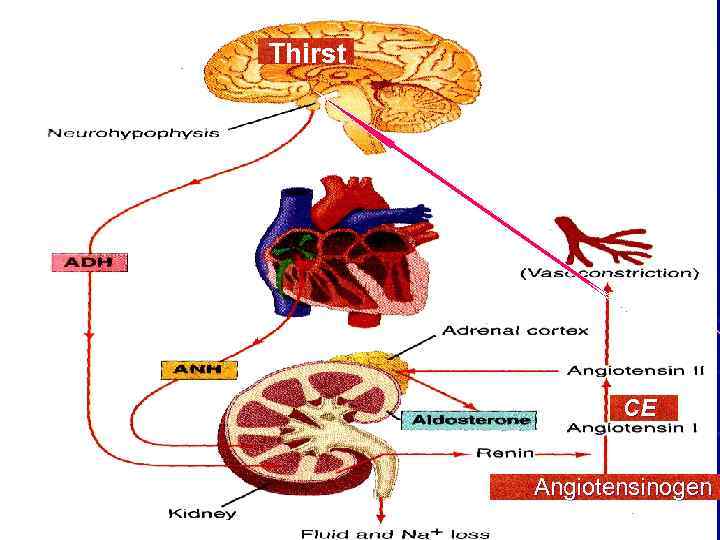
Thirst CE Angiotensinogen
![ADH ▲ ВЛАГОПОТЕРЬ / ИЗБЫТОК Na. Cl ▲ [Na+] и ОСМОЛЯРНОСТИ ▲ ОСМОРЕЦЕПТОРОВ ▲ ADH ▲ ВЛАГОПОТЕРЬ / ИЗБЫТОК Na. Cl ▲ [Na+] и ОСМОЛЯРНОСТИ ▲ ОСМОРЕЦЕПТОРОВ ▲](https://present5.com/presentation/220064782_305865704/image-52.jpg)
ADH ▲ ВЛАГОПОТЕРЬ / ИЗБЫТОК Na. Cl ▲ [Na+] и ОСМОЛЯРНОСТИ ▲ ОСМОРЕЦЕПТОРОВ ▲ ADH В ГИПОТАЛАМУСЕ ▲ВЫБРОСА ADH из НЕЙРОГИПОФИЗА ▲РЕАБСОРБЦИИ ВОДЫ НОРМАЛИЗАЦИЯ [Na+] и ОСМОЛЯРНОСТИ
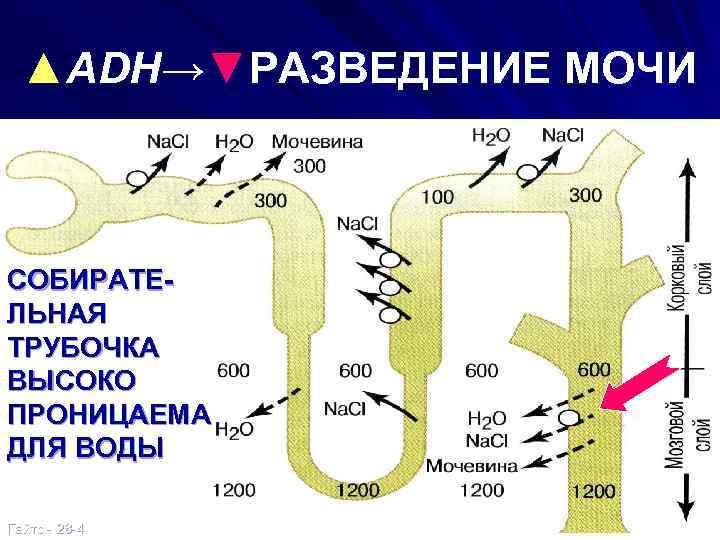
▲ADH→▼РАЗВЕДЕНИЕ МОЧИ СОБИРАТЕЛЬНАЯ ТРУБОЧКА ВЫСОКО ПРОНИЦАЕМА ДЛЯ ВОДЫ Гайтон 28 -4
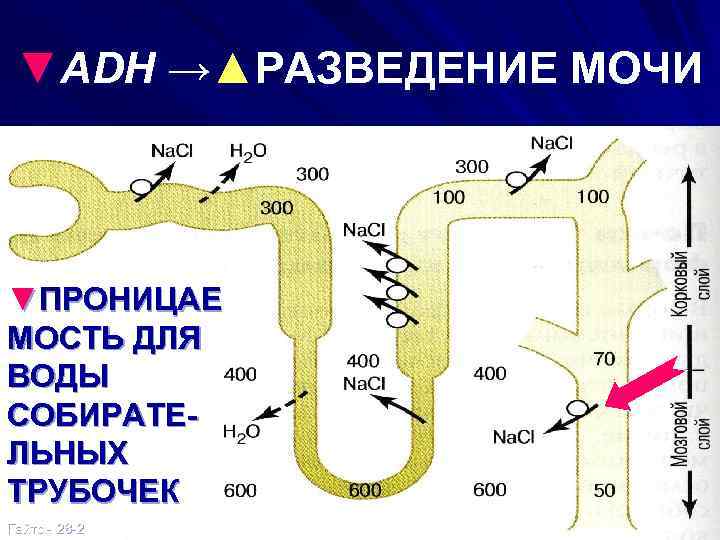
▼ADH →▲РАЗВЕДЕНИЕ МОЧИ ▼ПРОНИЦАЕ МОСТЬ ДЛЯ ВОДЫ СОБИРАТЕЛЬНЫХ ТРУБОЧЕК Гайтон 28 -2
![▼ H 2 O ▲[Na+] в МОЧЕ ▼АЛЬДО- СТЕРОНА ▼ РЕАБСОРБЦИЯ Na ▼ H 2 O ▲[Na+] в МОЧЕ ▼АЛЬДО- СТЕРОНА ▼ РЕАБСОРБЦИЯ Na](https://present5.com/presentation/220064782_305865704/image-55.jpg)
▼ H 2 O ▲[Na+] в МОЧЕ ▼АЛЬДО- СТЕРОНА ▼ РЕАБСОРБЦИЯ Na
![АЛЬДОСТЕРОН ▲ВЛАГОПОТЕРЬ / ИЗБЫТОК Na. Cl ▲ [Na+] ▲ КОРЫ НАДПОЧЕЧНИКОВ ▼ АЛЬДОСТЕРОНА ▼ АЛЬДОСТЕРОН ▲ВЛАГОПОТЕРЬ / ИЗБЫТОК Na. Cl ▲ [Na+] ▲ КОРЫ НАДПОЧЕЧНИКОВ ▼ АЛЬДОСТЕРОНА ▼](https://present5.com/presentation/220064782_305865704/image-56.jpg)
АЛЬДОСТЕРОН ▲ВЛАГОПОТЕРЬ / ИЗБЫТОК Na. Cl ▲ [Na+] ▲ КОРЫ НАДПОЧЕЧНИКОВ ▼ АЛЬДОСТЕРОНА ▼ РЕАБСОРЦИИ Na+ ▲ ВЫВЕДЕНИЯ Na+ НОРМАЛИЗАЦИЯ [Na+]
![▼ H 2 O ▲[Na+] в МОЧЕ ▲ANP ▼ РЕАБСОРБЦИЯ Na ▼ H 2 O ▲[Na+] в МОЧЕ ▲ANP ▼ РЕАБСОРБЦИЯ Na](https://present5.com/presentation/220064782_305865704/image-57.jpg)
▼ H 2 O ▲[Na+] в МОЧЕ ▲ANP ▼ РЕАБСОРБЦИЯ Na
![ANP ▲ ВЛАГОПОТЕРЬ, ИЗБЫТОК Na. Cl ▲ [Na+] ▲ Na-РЕЦЕПТОРОВ ПРЕДСЕРДИЯ ▲ ANP ▼ ANP ▲ ВЛАГОПОТЕРЬ, ИЗБЫТОК Na. Cl ▲ [Na+] ▲ Na-РЕЦЕПТОРОВ ПРЕДСЕРДИЯ ▲ ANP ▼](https://present5.com/presentation/220064782_305865704/image-58.jpg)
ANP ▲ ВЛАГОПОТЕРЬ, ИЗБЫТОК Na. Cl ▲ [Na+] ▲ Na-РЕЦЕПТОРОВ ПРЕДСЕРДИЯ ▲ ANP ▼ РЕАБСОРЦИИ Na+ ▲ ВЫВЕДЕНИЯ Na+ НОРМАЛИЗАЦИЯ +] [Na

V КИСЛОТНООСНОВНОЕ РАВНОВЕСИЕ

СИНОНИМЫ КИСЛОТНО-ОСНОВНОЕ РАВНОВЕСИЕ КИСЛОТНО-ЩЕЛОЧНОЕ РАВНОВЕСИЕ КИСЛОТНО-ОСНОВНОЙ БАЛАНС КИСЛОТНО-ЩЕЛОЧНОЙ БАЛАНС
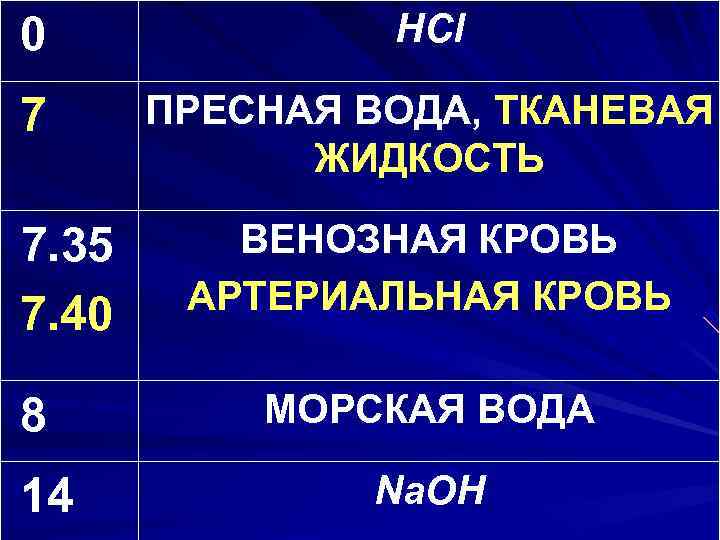
0 HCl 7 ПРЕСНАЯ ВОДА, ТКАНЕВАЯ ЖИДКОСТЬ 7. 35 7. 40 8 14 ВЕНОЗНАЯ КРОВЬ АРТЕРИАЛЬНАЯ КРОВЬ МОРСКАЯ ВОДА Na. OH
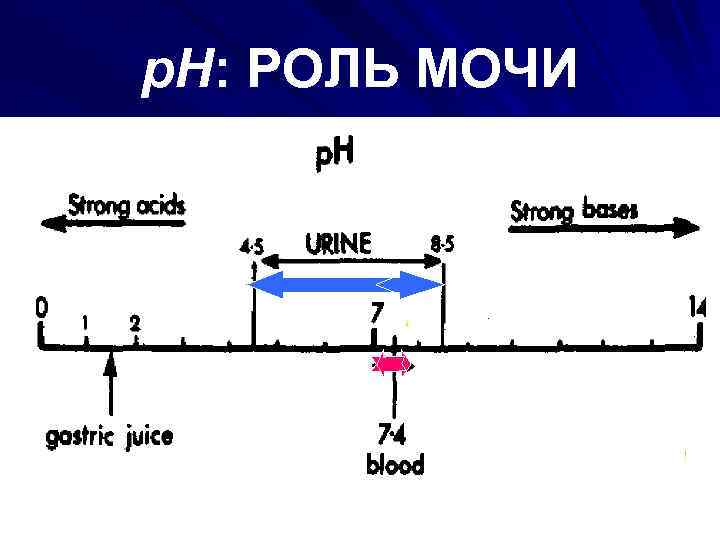
p. H: РОЛЬ МОЧИ

БУФЕР ЭТО – ЛЮБОЕ ВЕЩЕСТВО, СПОСОБНОЕ ОБРАТИМО СВЯЗЫВАТЬСЯ С ПРОТОНАМИ: БУФЕР + + H = H-БУФЕР

БУФЕРНЫЕ СИСТЕМЫ БИКАРБОНАТНАЯ ФОСФАТНАЯ БЕЛКОВ ПЛАЗМЫ КРОВИ ГЕМОГЛОБИНА
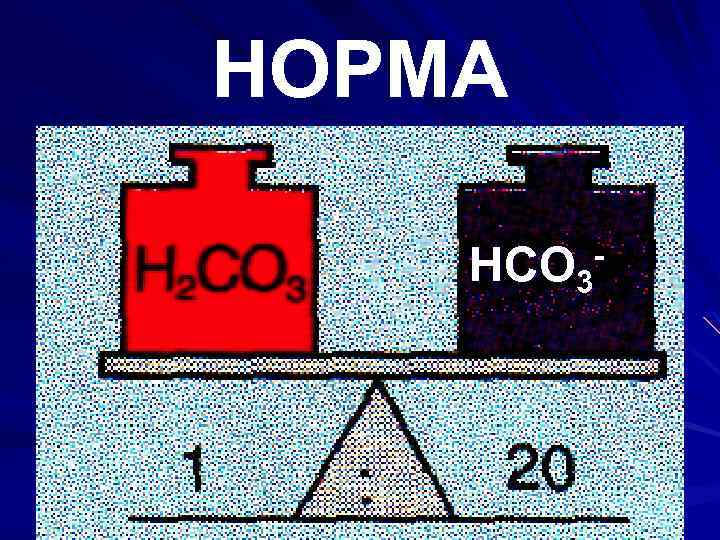
НОРМА HCO 3

АЦИДОЗ и АЛКАЛОЗ МЕТАБОЛИЧЕСКИЕ ▼▲ HCO 3 РЕСПИРАТОРНЫЕ ▲▼ H 2 CO 3

МЕТАБОЛИЧЕСКИЙ АЦИДОЗ НАКАПЛИВАЮТСЯ: КЕТОНЫ ХЛОРИДЫ ИОНЫ ОРГАНИЧЕСКИХ КИСЛОТ

ТИПЫ АЦИДОЗА МЕТАБОЛИЧЕСКИЙ - (САХАРНЫЙ ▼HCO 3 ДИАБЕТ, ГОЛОДАНИЕ) РЕСПИРАТОРНЫЙ ▲H 2 CO 3 (ПНЕВМОНИЯ, ЭМФИЗЕМА)
МЕТАБОЛИЧЕСКИЙ АЦИДОЗ O 3 C H

ОТВЕТ на АЦИДОЗ на ПРИМЕРЕ ФОСФАТНОГО БУФЕРА

В ПЛАЗМЕ БОЛЕЕ КИСЛЫЙ ФОСФАТ → В МЕНЕЕ КИСЛЫЙ (И ОСТАЛСЯ В ПЛАЗМЕ), ОТДАВ H+ НА ОБРАЗОВАНИЕ H 2 CO 3 В ПОЧКЕ ОБРАТНЫЙ ПРОЦЕСС: МЕНЕЕ КИСЛЫЙ ФОСФАТ → БОЛЕЕ КИСЛЫЙ И ВЫШЕЛ С МОЧОЙ, УНОСЯ H+

В ПЛАЗМЕ Na. H 2 PO 4 + Na. HCO 3 → → Na 2 HPO 4 + H 2 CO 3
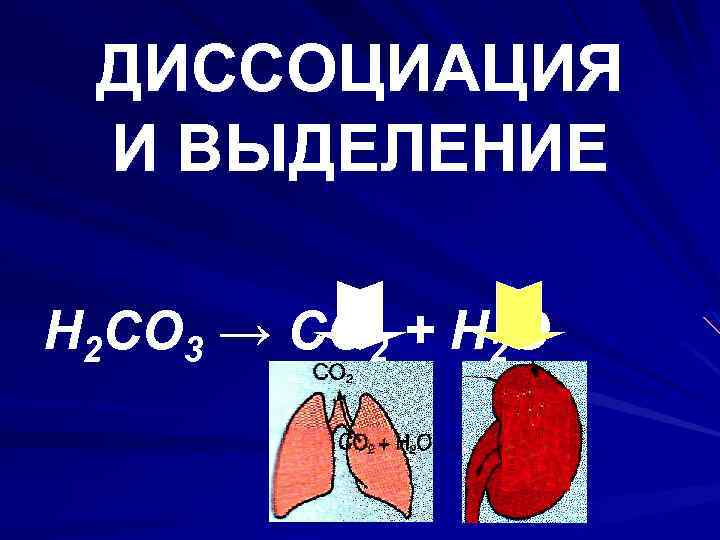
ДИССОЦИАЦИЯ И ВЫДЕЛЕНИЕ H 2 CO 3 → CO 2 + H 2 O
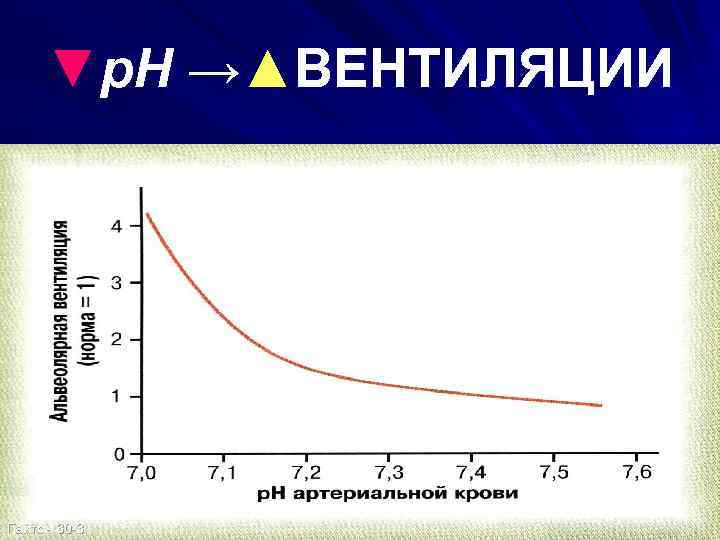
▼p. H →▲ВЕНТИЛЯЦИИ Гайтон 30 -3
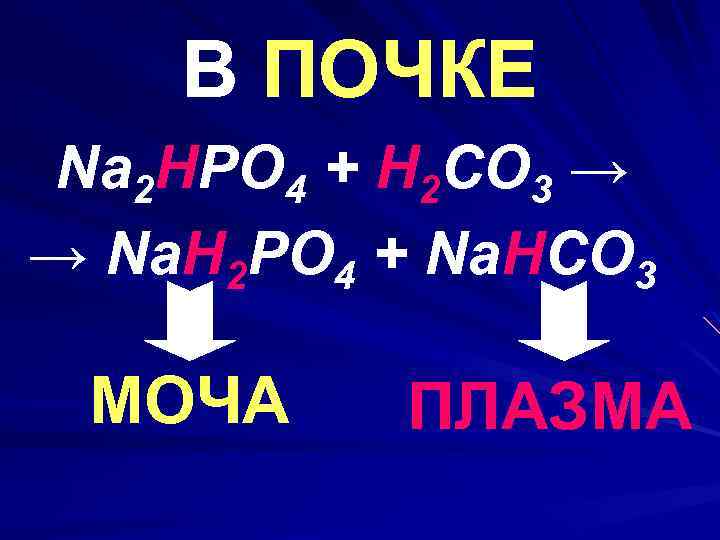
В ПОЧКЕ Na 2 HPO 4 + H 2 CO 3 → → Na. H 2 PO 4 + Na. HCO 3 МОЧА ПЛАЗМА
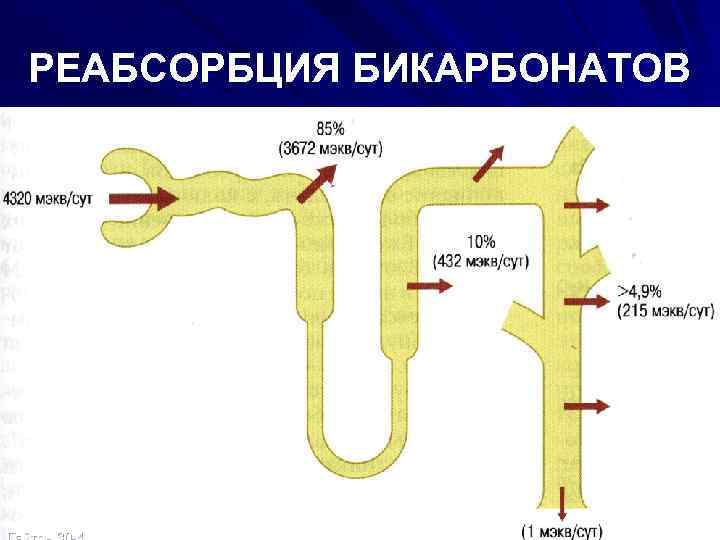
РЕАБСОРБЦИЯ БИКАРБОНАТОВ

ОТВЕТ НА АЦИДОЗ СЕКРЕЦИЯ АММИАКА В ПОЧЕЧНОМ ЭПИТЕЛИИ: Gln → Glu + NH 3 глутамин глут-я к-та аммиак
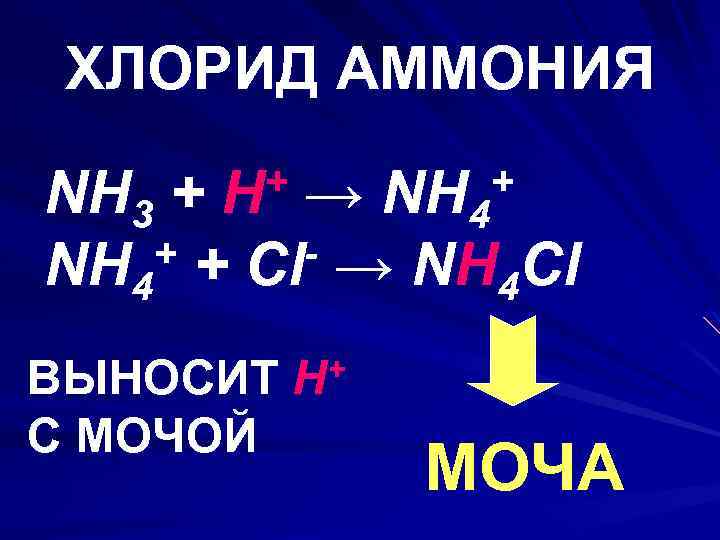
ХЛОРИД АММОНИЯ + H NH 3 + → + + Cl- → NH Cl NH 4 4 ВЫНОСИТ С МОЧОЙ + NH 4 + H МОЧА

АЛКАЛОЗ ПИЩА→ НАКОПЛЕНИЕ ОСНОВНЫХ ИОНОВ В ПЛАЗМЕ

ТИПЫ АЛКАЛОЗА МЕТАБОЛИЧЕСКИЙ - (УПОТРЕБЛЕНИЕ ▲HCO 3 ПИТЬЕВОЙ СОДЫ) РЕСПИРАТОРНЫЙ ▼H 2 CO 3 (ЛИХОРАДКА)
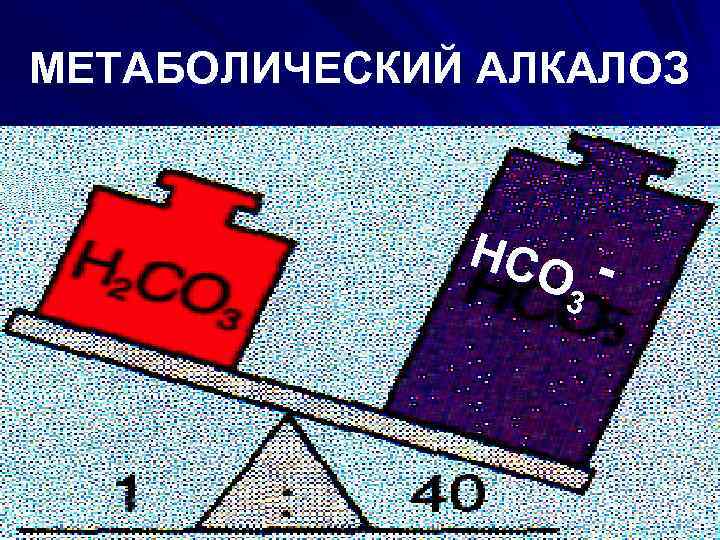
МЕТАБОЛИЧЕСКИЙ АЛКАЛОЗ HCO 3

ОТВЕТ НА АЛКАЛОЗ ПОЧКА ЗАДЕРЖИВАЕТ ВЫВЕДЕНИЕ H+ И УВЕЛИЧИВАЕТ – HCO 3(▼РЕАБСОРБЦИЮ) ЛЕГКИЕ ВЫВОДЯТ МЕНЬШЕ CO 2, СПОСОБСТВУЯ НАКОПЛЕНИЮ В ПЛАЗМЕ H 2 CO 3
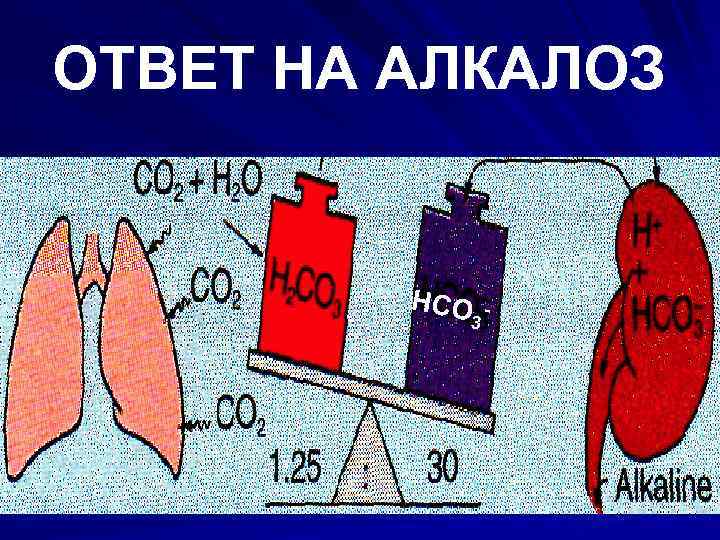
ОТВЕТ НА АЛКАЛОЗ HCO 3
![RÉSUMÉ 1. Постояноство ОЦП, [Na+], [K+], [Ca 2+], Pосм. и p. H тканевой жидкости RÉSUMÉ 1. Постояноство ОЦП, [Na+], [K+], [Ca 2+], Pосм. и p. H тканевой жидкости](https://present5.com/presentation/220064782_305865704/image-84.jpg)
RÉSUMÉ 1. Постояноство ОЦП, [Na+], [K+], [Ca 2+], Pосм. и p. H тканевой жидкости поддерживается нервными и гуморальными механизмами 2. Главные эффекторы – почки и легкие

ЛЕКЦИЯ ОКОНЧЕНА Milton Glaser, 1964

РЕЗЕРВ
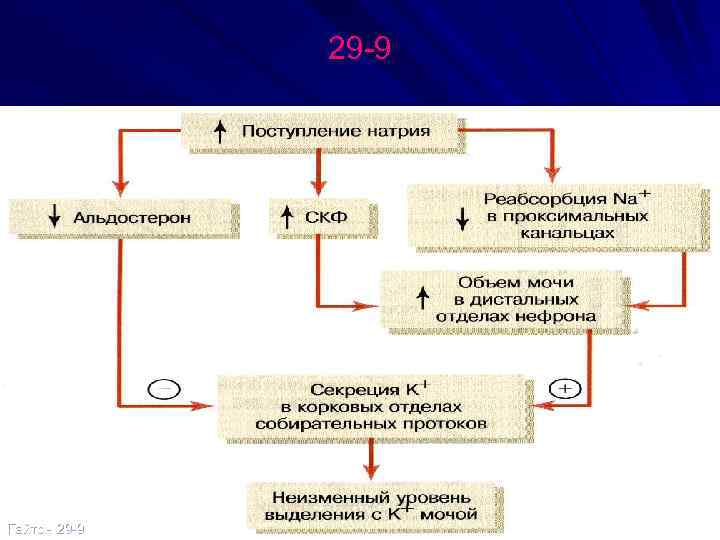
29 -9 Гайтон 29 -9
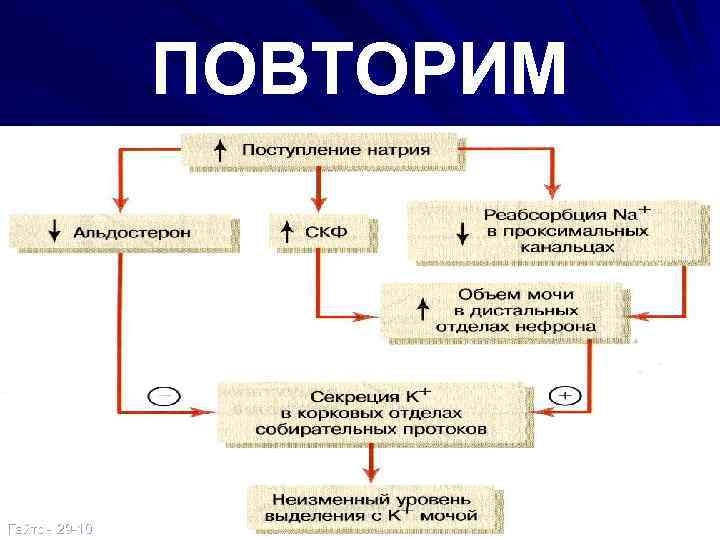
ПОВТОРИМ Гайтон 29 -10
31 Регуляция водно-электролитного баланса.ppt