Lektsia_4_Protolit_teoria_Protoliticheskie_r.pptx
- Количество слайдов: 36
 ЛЕКЦИЯ: ПРОТОЛИТИЧЕСКОЕ РАВНОВЕСИЕ В ВОДНЫХ И НЕВОДНЫХ РАСТВОРАХ.
ЛЕКЦИЯ: ПРОТОЛИТИЧЕСКОЕ РАВНОВЕСИЕ В ВОДНЫХ И НЕВОДНЫХ РАСТВОРАХ.
 В 1923 г датский ученый Бренстед и английский ученый Лоури разработали протонную (протолитическую) теорию кислот и оснований, согласно которой кислота – это атом, молекула или ион, способные отдавать протон водорода (Н+), донор протонов, а основание - это атом, молекула или ион, способные принимать протон водорода, акцептор (Н+) протонов.
В 1923 г датский ученый Бренстед и английский ученый Лоури разработали протонную (протолитическую) теорию кислот и оснований, согласно которой кислота – это атом, молекула или ион, способные отдавать протон водорода (Н+), донор протонов, а основание - это атом, молекула или ион, способные принимать протон водорода, акцептор (Н+) протонов.
 Кислотные свойства соединений проявляются лишь в присутствии оснований, а основные свойства лишь в присутствии кислот. От кислоты к основанию переходит Н+ такие реакции называются протолитическими, а равновесия в системе с переносом Н+ называются протолитические равновесия.
Кислотные свойства соединений проявляются лишь в присутствии оснований, а основные свойства лишь в присутствии кислот. От кислоты к основанию переходит Н+ такие реакции называются протолитическими, а равновесия в системе с переносом Н+ называются протолитические равновесия.
 Кислота, отдавая Н+, превращается в основание, которое называется сопряженным. + Н СН 3 СООН + Н 2 О ↔ СН 3 СОО- + Н 3 О+ кислота основание с. о с. к
Кислота, отдавая Н+, превращается в основание, которое называется сопряженным. + Н СН 3 СООН + Н 2 О ↔ СН 3 СОО- + Н 3 О+ кислота основание с. о с. к
 Три типа кислот и оснований: Нейтральные: кислоты (HCl, H 2 SO 4, H 3 PO 4) основания (NH 3, H 2 O, C 2 H 5 OH) Катионные: кислоты (NH 4+, H 3 O+, ) основания(-NH 3+, NH 2+) Анионные: кислоты (HSO 4 -, H 2 PO 4 -) основания (Cl-, СН 3 СОО-, ОН-)
Три типа кислот и оснований: Нейтральные: кислоты (HCl, H 2 SO 4, H 3 PO 4) основания (NH 3, H 2 O, C 2 H 5 OH) Катионные: кислоты (NH 4+, H 3 O+, ) основания(-NH 3+, NH 2+) Анионные: кислоты (HSO 4 -, H 2 PO 4 -) основания (Cl-, СН 3 СОО-, ОН-)
 Типы протолитических реакций: Автопротолиз, сольволиз (самоионизация) Н 2 О + Н 2 О ↔ ОН- + к о с. о. Н 3 О+ с. к. СН 3 СООН+СН 3 СООН↔СН 3 СОО-+СН 3 СООН 2+ к о с. к ацетат ион ацетония
Типы протолитических реакций: Автопротолиз, сольволиз (самоионизация) Н 2 О + Н 2 О ↔ ОН- + к о с. о. Н 3 О+ с. к. СН 3 СООН+СН 3 СООН↔СН 3 СОО-+СН 3 СООН 2+ к о с. к ацетат ион ацетония
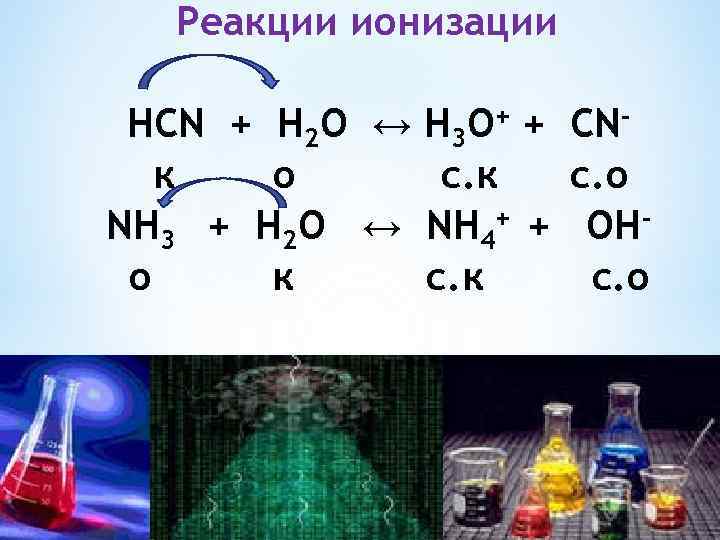 Реакции ионизации НСN + Н 2 О ↔ Н 3 О+ + СNк о с. к с. о NH 3 + Н 2 О ↔ NH 4+ + ОНо к с. о
Реакции ионизации НСN + Н 2 О ↔ Н 3 О+ + СNк о с. к с. о NH 3 + Н 2 О ↔ NH 4+ + ОНо к с. о
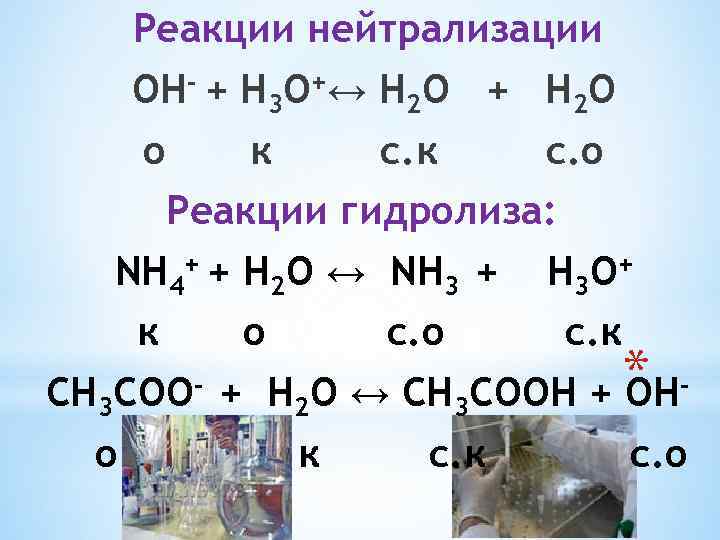 Реакции нейтрализации ОН- + Н 3 О+↔ Н 2 O + Н 2 O о к с. о Реакции гидролиза: NH 4+ + Н 2 O ↔ NH 3 + к о с. о Н 3 О+ с. к СН 3 СОО- + Н 2 O ↔ СН 3 СООН + * ОН о к с. о
Реакции нейтрализации ОН- + Н 3 О+↔ Н 2 O + Н 2 O о к с. о Реакции гидролиза: NH 4+ + Н 2 O ↔ NH 3 + к о с. о Н 3 О+ с. к СН 3 СОО- + Н 2 O ↔ СН 3 СООН + * ОН о к с. о
 Протолитические кислотно-основные равновесия могут иметь место не только в Н 2 O, но и в других растворителях, например в жидком аммиаке: СН 3 СООН + NH 3 ↔ СН 3 СОО- + NH 4+ к о с. к в безводном НF: С 2 Н 5 ОН + НF ↔ С 2 Н 5 ОН 2+ + Fо к с. о Недостаток теории Брендстеда-Лоури: не применима к веществам, не содержащим Н+(галогенидам бора, алюминия, кремния, олова).
Протолитические кислотно-основные равновесия могут иметь место не только в Н 2 O, но и в других растворителях, например в жидком аммиаке: СН 3 СООН + NH 3 ↔ СН 3 СОО- + NH 4+ к о с. к в безводном НF: С 2 Н 5 ОН + НF ↔ С 2 Н 5 ОН 2+ + Fо к с. о Недостаток теории Брендстеда-Лоури: не применима к веществам, не содержащим Н+(галогенидам бора, алюминия, кремния, олова).
 Поэтому более общей является электронная теория кислот и оснований Льюиса, согласно которой: Кислота - вещество, принимающее электронные пары - акцептор электронов; Основание - вещество, поставляющее электроны для образования химической связи - донор электронов. Взаимодействие между ними заключается в образовании химической донорно-акцепторной связи. А↑↓ + В ↔ А↑↓В основ кисл ОН-↑↓ + Н+ ↔ НО↑↓Н
Поэтому более общей является электронная теория кислот и оснований Льюиса, согласно которой: Кислота - вещество, принимающее электронные пары - акцептор электронов; Основание - вещество, поставляющее электроны для образования химической связи - донор электронов. Взаимодействие между ними заключается в образовании химической донорно-акцепторной связи. А↑↓ + В ↔ А↑↓В основ кисл ОН-↑↓ + Н+ ↔ НО↑↓Н
 Н Н Н - N: + НCI → Н - N : НCI Н/ Н/ основ. кислота Н 3 С Н 3 С - N : + BCI 3 → (Н 3 С)3 N: BCI 3 Н 3 С / основ. кислота Теория Льюиса рассматривает разные химические процессы: реакцию нейтрализации, взаимодействия аминов с галогенами бора, комплексообразование.
Н Н Н - N: + НCI → Н - N : НCI Н/ Н/ основ. кислота Н 3 С Н 3 С - N : + BCI 3 → (Н 3 С)3 N: BCI 3 Н 3 С / основ. кислота Теория Льюиса рассматривает разные химические процессы: реакцию нейтрализации, взаимодействия аминов с галогенами бора, комплексообразование.
 К основанием Льюиса относятся CI-; NH 3; амины, кислородсодержащие органические соединения R 2 CO. К кислотам Льюиса: галогениды бора, алюминия, кремния, олова. Рассмотренные теории ионизации кислот и оснований не противоречат, а дополняют друга и имеют глубокую внутреннюю связь.
К основанием Льюиса относятся CI-; NH 3; амины, кислородсодержащие органические соединения R 2 CO. К кислотам Льюиса: галогениды бора, алюминия, кремния, олова. Рассмотренные теории ионизации кислот и оснований не противоречат, а дополняют друга и имеют глубокую внутреннюю связь.
 Ионизация воды. Водородный и гидроксильный показатели. Константа автопротолиза. Вода ведет себя как амфолит, согласно теории Бренстера-Лоури Н 2 O+Н 2 O↔Н 3 О++ОН- + 56, 5 КДж/моль Кравн= [Н 3 О+] [ОН-] / [Н 2 O]2 = 1, 8 10 -16 моль/л Н 2 O-слабый электролит, поэтому [Н 2 O] = const Кравн[Н 2 O]= [Н 3 О+] [ОН-] – закон действующих масс Ионное произведение: К(Н 2 O) = Кw= [Н 3 О+] [ОН-] где К(Н 2 O) - const (константа автопротолиза) К(Н 2 O) = 1· 10 -14
Ионизация воды. Водородный и гидроксильный показатели. Константа автопротолиза. Вода ведет себя как амфолит, согласно теории Бренстера-Лоури Н 2 O+Н 2 O↔Н 3 О++ОН- + 56, 5 КДж/моль Кравн= [Н 3 О+] [ОН-] / [Н 2 O]2 = 1, 8 10 -16 моль/л Н 2 O-слабый электролит, поэтому [Н 2 O] = const Кравн[Н 2 O]= [Н 3 О+] [ОН-] – закон действующих масс Ионное произведение: К(Н 2 O) = Кw= [Н 3 О+] [ОН-] где К(Н 2 O) - const (константа автопротолиза) К(Н 2 O) = 1· 10 -14
![Возьмем 1 кг (л) воды [Н 2 O]=1000 г/18 г/моль=55, 5 моль/л К(Н 2 Возьмем 1 кг (л) воды [Н 2 O]=1000 г/18 г/моль=55, 5 моль/л К(Н 2](https://present5.com/presentation/198569245_449820736/image-14.jpg) Возьмем 1 кг (л) воды [Н 2 O]=1000 г/18 г/моль=55, 5 моль/л К(Н 2 O) = 1, 86 10 -16 55, 5=1· 10 -14 В чистой воде [Н 3 О+] = [ОН-] = 1· 10 -7 - раствор нейтральный В присутствии посторонних электролитов это равенство не соблюдается, а [Н 3 О+] и [ОН-] можно рассчитать: [Н 3 О+] = К(Н 2 O)/[ОН-]; [ОН-] = К(Н 2 O) /[Н 3 О+] Если [Н 3 О+] > [ОН-], то реакция среды в растворе кислая [Н 3 О+] >1 10 -7, а для случая, когда[Н 3 О+] < [ОН-] щелочная [Н 3 О+] < 1 10 -7
Возьмем 1 кг (л) воды [Н 2 O]=1000 г/18 г/моль=55, 5 моль/л К(Н 2 O) = 1, 86 10 -16 55, 5=1· 10 -14 В чистой воде [Н 3 О+] = [ОН-] = 1· 10 -7 - раствор нейтральный В присутствии посторонних электролитов это равенство не соблюдается, а [Н 3 О+] и [ОН-] можно рассчитать: [Н 3 О+] = К(Н 2 O)/[ОН-]; [ОН-] = К(Н 2 O) /[Н 3 О+] Если [Н 3 О+] > [ОН-], то реакция среды в растворе кислая [Н 3 О+] >1 10 -7, а для случая, когда[Н 3 О+] < [ОН-] щелочная [Н 3 О+] < 1 10 -7
![Для удобства расчетов используют значение: р. Н = - lg[Н 3 О+] - водородный Для удобства расчетов используют значение: р. Н = - lg[Н 3 О+] - водородный](https://present5.com/presentation/198569245_449820736/image-15.jpg) Для удобства расчетов используют значение: р. Н = - lg[Н 3 О+] - водородный показатель р. ОН= - lg[ОН-]-гидроксильный показатель т. к. К(Н 2 O) = 1∙ 10 -14 Прологарифмируем и умножим на -1: - lg К(Н 2 O) = - lg[Н 3 О+] – lg[ОН-] - lg 1 10 -14 = - lg[Н 3 О+] - lg[ОН-] 14 = p. H + p. OH р. Н определяют с помощью индикаторов, более точное определение с помощью потенциометров. р. Н < 7 (среда кислая), р. Н > 7 (среда щелочная), р. Н = 7 (среда нейтральная)
Для удобства расчетов используют значение: р. Н = - lg[Н 3 О+] - водородный показатель р. ОН= - lg[ОН-]-гидроксильный показатель т. к. К(Н 2 O) = 1∙ 10 -14 Прологарифмируем и умножим на -1: - lg К(Н 2 O) = - lg[Н 3 О+] – lg[ОН-] - lg 1 10 -14 = - lg[Н 3 О+] - lg[ОН-] 14 = p. H + p. OH р. Н определяют с помощью индикаторов, более точное определение с помощью потенциометров. р. Н < 7 (среда кислая), р. Н > 7 (среда щелочная), р. Н = 7 (среда нейтральная)
 Расчет р. Н сильных электролитов. В растворах сильных электролитов р. Н кислот и оснований зависит от концентрации кислоты и основания: [Н+] = C(1/z кислоты) [ОН-] = C(1/z основания) Например, рассчитать р. Н 0, 1 моль/л р-ра НСl: [Н+] = C(НСl) = 0, 1 моль/л р. Н = - lg 0, 1 = 1 р. ОН = 14 – р. Н = 14 – 1 = 13 Рассчитать р. Н 0, 01 моль/л р-ра Nа. ОН: [ОН-] = C(Nа. ОН) = 0, 01 моль/л р. ОН = - lg 0, 01 = 2 р. Н = 14 – р. ОН = 14 – 2 = 12
Расчет р. Н сильных электролитов. В растворах сильных электролитов р. Н кислот и оснований зависит от концентрации кислоты и основания: [Н+] = C(1/z кислоты) [ОН-] = C(1/z основания) Например, рассчитать р. Н 0, 1 моль/л р-ра НСl: [Н+] = C(НСl) = 0, 1 моль/л р. Н = - lg 0, 1 = 1 р. ОН = 14 – р. Н = 14 – 1 = 13 Рассчитать р. Н 0, 01 моль/л р-ра Nа. ОН: [ОН-] = C(Nа. ОН) = 0, 01 моль/л р. ОН = - lg 0, 01 = 2 р. Н = 14 – р. ОН = 14 – 2 = 12
 В растворах слабых кислот: НА ↔ Н+ + А- или НА + Н 2 О ↔ А- + Н 3 О+ -lg[Н 3 О+]= -1/2·lg. К(НА)- 1/2·lg. C(1/z. НА) р. Н = 1/2·р. К(НА) - 1/2·lg. C(НА) Например, чему равен водородный показатель 0, 1 моль/л р-ра НСN? р. Н = 1/2·р. К(НСN) - 1/2·lg. C(НСN) р. Н = 1/2· 9, 3 - 1/2·lg 0, 1 = 4, 65 + 0, 5 = 5, 15
В растворах слабых кислот: НА ↔ Н+ + А- или НА + Н 2 О ↔ А- + Н 3 О+ -lg[Н 3 О+]= -1/2·lg. К(НА)- 1/2·lg. C(1/z. НА) р. Н = 1/2·р. К(НА) - 1/2·lg. C(НА) Например, чему равен водородный показатель 0, 1 моль/л р-ра НСN? р. Н = 1/2·р. К(НСN) - 1/2·lg. C(НСN) р. Н = 1/2· 9, 3 - 1/2·lg 0, 1 = 4, 65 + 0, 5 = 5, 15
 Расчет р. Н слабых оснований: В + Н 2 О ↔ ВН+ + ОНр. ОН = 1/2 р. К(В)- 1/2 lg. C(1/z В) р. Н = 14 - р. ОН р. Н = 14 - 1/2 р. К(В) + 1/2 lg. C(1/z В) Например, чему равен водородный показатель 0, 01 моль/л р-ра гидроксида аммония? NН 3 + Н 2 О ↔ NН 4 ОН + ОНр. Н = 14 - 1/2 р. К(NН 3) + 1/2 lg C(NН 3) р. Н = 14 - 1/2· 4, 76 + 1/2 lg 0, 01 = 14 – 2, 38 – 1 = 10, 62
Расчет р. Н слабых оснований: В + Н 2 О ↔ ВН+ + ОНр. ОН = 1/2 р. К(В)- 1/2 lg. C(1/z В) р. Н = 14 - р. ОН р. Н = 14 - 1/2 р. К(В) + 1/2 lg. C(1/z В) Например, чему равен водородный показатель 0, 01 моль/л р-ра гидроксида аммония? NН 3 + Н 2 О ↔ NН 4 ОН + ОНр. Н = 14 - 1/2 р. К(NН 3) + 1/2 lg C(NН 3) р. Н = 14 - 1/2· 4, 76 + 1/2 lg 0, 01 = 14 – 2, 38 – 1 = 10, 62
 БУФЕРНЫЕ СИСТЕМЫ Буферные системы - это равновесные системы, способные сохранять постоянное значение р. Н при добавлении к ним небольших количеств сильных кислот и оснований, а также при разбавлении. Свойство растворов сохранять определенное значение р. Н называется буферным действием. К буферам 1 типа относятся протолитические системы растворов слабых кислот и их солей с сильными основаниями или, смеси растворов солей многоосновных кислот различной степени замещения.
БУФЕРНЫЕ СИСТЕМЫ Буферные системы - это равновесные системы, способные сохранять постоянное значение р. Н при добавлении к ним небольших количеств сильных кислот и оснований, а также при разбавлении. Свойство растворов сохранять определенное значение р. Н называется буферным действием. К буферам 1 типа относятся протолитические системы растворов слабых кислот и их солей с сильными основаниями или, смеси растворов солей многоосновных кислот различной степени замещения.
 Например, буферные смеси при молярном соотношении 1: 1. НСООН + НСООNa формиатная, р. Н=3, 8 СН 3 СООН + СН 3 СООNa ацетатная, р. Н=4, 7 Na 2 НРО 4 + Na. Н 2 РО 4 фосфатная, р. Н=6, 6 Н 2 СО 3 + Na. НСО 3 карбонатная, р. Н=6, 4
Например, буферные смеси при молярном соотношении 1: 1. НСООН + НСООNa формиатная, р. Н=3, 8 СН 3 СООН + СН 3 СООNa ацетатная, р. Н=4, 7 Na 2 НРО 4 + Na. Н 2 РО 4 фосфатная, р. Н=6, 6 Н 2 СО 3 + Na. НСО 3 карбонатная, р. Н=6, 4
 К буферам 2 типа относятся протолитические системы слабых оснований и их солей с сильными кислотами. Например, NН 4 ОН + NН 4 Cl аммиачная, р. Н=9, 25 (при молярном соотношении 1: 1) Буферным действием могут обладать растворы, состоящие из анионов разных слабых кислот, например, фосфатцитратный буфер Na 2 НРО 4 - С 6 Н 8 О 7
К буферам 2 типа относятся протолитические системы слабых оснований и их солей с сильными кислотами. Например, NН 4 ОН + NН 4 Cl аммиачная, р. Н=9, 25 (при молярном соотношении 1: 1) Буферным действием могут обладать растворы, состоящие из анионов разных слабых кислот, например, фосфатцитратный буфер Na 2 НРО 4 - С 6 Н 8 О 7
 Способность буферных систем поддерживать постоянство р. Н при добавлении к ним небольших количеств сильной кислоты или сильного основания основана на том, что одна составная часть буферной системы может взаимодействовать с ионами (Н 3 О+) добавляемой кислоты, а другая с ионами (ОН-) прибавляемого основания. Вследствие этого буферная система способна сохранить постоянство величины р. Н.
Способность буферных систем поддерживать постоянство р. Н при добавлении к ним небольших количеств сильной кислоты или сильного основания основана на том, что одна составная часть буферной системы может взаимодействовать с ионами (Н 3 О+) добавляемой кислоты, а другая с ионами (ОН-) прибавляемого основания. Вследствие этого буферная система способна сохранить постоянство величины р. Н.
 МЕХАНИЗМ ДЕЙСТВИЯ БУФЕРНЫХ СИСТЕМ Например: если к ацетатной буферной системе прилить сильную кислоту (НCl; Н 2 SО 4), то произойдет реакция между ацетат ионами и ионом гидроксония кислоты, что можно выразить уравнением: СН 3 СООNa + НСl → СН 3 СООН + Na. Cl СН 3 СОО- + Н 3 О+ → СН 3 СООН + Н 2 О Сильная хлороводородная кислота замещается слабой уксусной кислотой, посылающей в раствор ничтожно малое количество ионов гидроксония.
МЕХАНИЗМ ДЕЙСТВИЯ БУФЕРНЫХ СИСТЕМ Например: если к ацетатной буферной системе прилить сильную кислоту (НCl; Н 2 SО 4), то произойдет реакция между ацетат ионами и ионом гидроксония кислоты, что можно выразить уравнением: СН 3 СООNa + НСl → СН 3 СООН + Na. Cl СН 3 СОО- + Н 3 О+ → СН 3 СООН + Н 2 О Сильная хлороводородная кислота замещается слабой уксусной кислотой, посылающей в раствор ничтожно малое количество ионов гидроксония.
 При добавлении к ацетатной буферной смеси сильной щелочи (Na. ОН; КОН) пойдет реакция нейтрализации уксусной кислоты сильным основанием: СН 3 СООН+Na. ОН→СН 3 СООNa+Н 2 О СН 3 СООН+ОН- → СН 3 СОО-+ Н 2 О В аммиачной буферной системе протекают следующие реакции: NН 4 ОН + НСl → NН 4 Сl + Н 2 О NН 4 Сl + KОН → NН 4 ОН + КCl
При добавлении к ацетатной буферной смеси сильной щелочи (Na. ОН; КОН) пойдет реакция нейтрализации уксусной кислоты сильным основанием: СН 3 СООН+Na. ОН→СН 3 СООNa+Н 2 О СН 3 СООН+ОН- → СН 3 СОО-+ Н 2 О В аммиачной буферной системе протекают следующие реакции: NН 4 ОН + НСl → NН 4 Сl + Н 2 О NН 4 Сl + KОН → NН 4 ОН + КCl







 БУФЕРНЫЕ СИСТЕМЫ ОРГАНИЗМА Основная функция буферных систем - предотвращение значительных сдвигов р. Н путём взаимодействия буфера как с кислотой, так и с основанием. Действие буферных систем в организме направлено преимущественно на нейтрализацию образующихся кислот. Н+ + буфер- <==> Н-буфер В организме одновременно существует несколько различных буферных систем. В функциональном плане их можно разделить на бикарбонатную и небикарбонатную. Небикарбонатная буферная система включает гемоглобин, различные белки и фосфаты. Она наиболее активно действует в крови и внутри клеток.
БУФЕРНЫЕ СИСТЕМЫ ОРГАНИЗМА Основная функция буферных систем - предотвращение значительных сдвигов р. Н путём взаимодействия буфера как с кислотой, так и с основанием. Действие буферных систем в организме направлено преимущественно на нейтрализацию образующихся кислот. Н+ + буфер- <==> Н-буфер В организме одновременно существует несколько различных буферных систем. В функциональном плане их можно разделить на бикарбонатную и небикарбонатную. Небикарбонатная буферная система включает гемоглобин, различные белки и фосфаты. Она наиболее активно действует в крови и внутри клеток.
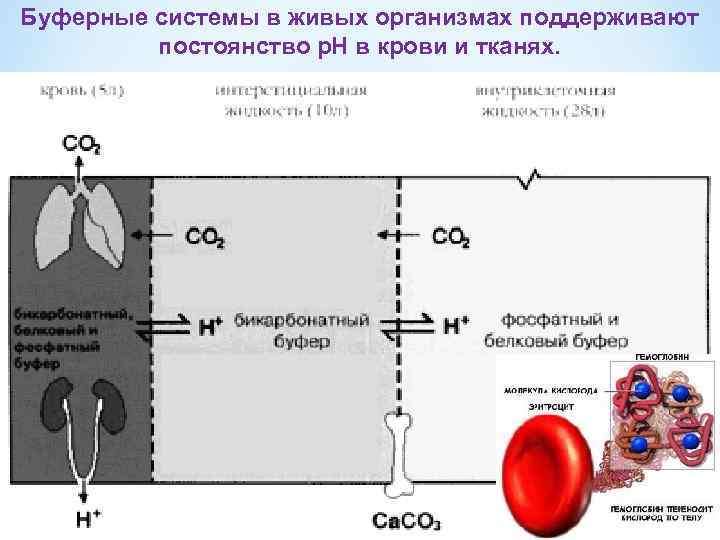 Буферные системы в живых организмах поддерживают постоянство р. Н в крови и тканях.
Буферные системы в живых организмах поддерживают постоянство р. Н в крови и тканях.
 В организме человека за сутки образуется такое количество различных кислот, которое эквивалентно 2, 0 - 3, 0 литрам концентрированной хлороводородной кислоты. Тем не менее, благодаря наличию буферных систем организма неравномерно распределенных между эритроцитами и плазмой крови, р. Н крови остается постоянным (7, 4 0, 04). При смещении р. Н крови в кислую сторону от нормы, возникает – АЦИДОЗ, а в щелочную – АЛКАЛОЗ. Ацидоз возникает вследствие: голодания, сахарного диабета, при шоке при почечной недостаточности, при заболеваниях легких (пневмония, отек легких), при отравлении наркотиками и транквилизаторами.
В организме человека за сутки образуется такое количество различных кислот, которое эквивалентно 2, 0 - 3, 0 литрам концентрированной хлороводородной кислоты. Тем не менее, благодаря наличию буферных систем организма неравномерно распределенных между эритроцитами и плазмой крови, р. Н крови остается постоянным (7, 4 0, 04). При смещении р. Н крови в кислую сторону от нормы, возникает – АЦИДОЗ, а в щелочную – АЛКАЛОЗ. Ацидоз возникает вследствие: голодания, сахарного диабета, при шоке при почечной недостаточности, при заболеваниях легких (пневмония, отек легких), при отравлении наркотиками и транквилизаторами.
 Алкалоз - при кишечной непроходимости, рвоте, лихорадке. Для коррекции кислотноосновного равновесия при ацидозах назначают 4 % раствор гидрокарбоната натрия внутривенно. При алкалозе 5% раствор аскорбиновой кислоты. Сохранение постоянства р. Н обеспечивается наличием мощных буферных систем. Наиболее мощными буферными системами крови являются: гемоглобиновая буферная система, составляющая 75% всей буферной емкости крови, также фосфатная, карбонатная, белковая.
Алкалоз - при кишечной непроходимости, рвоте, лихорадке. Для коррекции кислотноосновного равновесия при ацидозах назначают 4 % раствор гидрокарбоната натрия внутривенно. При алкалозе 5% раствор аскорбиновой кислоты. Сохранение постоянства р. Н обеспечивается наличием мощных буферных систем. Наиболее мощными буферными системами крови являются: гемоглобиновая буферная система, составляющая 75% всей буферной емкости крови, также фосфатная, карбонатная, белковая.



