Биогенные элементы. Углерод.ppt
- Количество слайдов: 25
 Лекция по дисциплине «Основы токсикологии» Материал подготовлен Кузьминой И. В. , доцентом кафедры ООС и РИПР, НПИ
Лекция по дисциплине «Основы токсикологии» Материал подготовлен Кузьминой И. В. , доцентом кафедры ООС и РИПР, НПИ
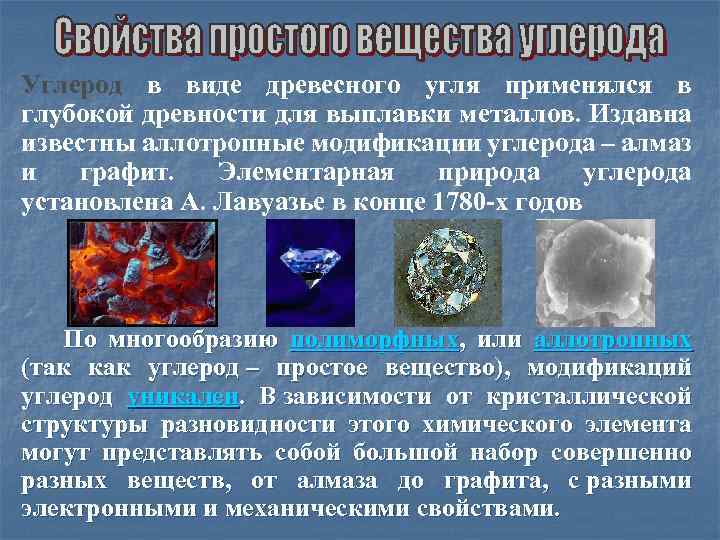 Углерод в виде древесного угля применялся в глубокой древности для выплавки металлов. Издавна известны аллотропные модификации углерода – алмаз и графит. Элементарная природа углерода установлена А. Лавуазье в конце 1780 х годов По многообразию полиморфных, или аллотропных (так как углерод – простое вещество), модификаций углерод уникален. В зависимости от кристаллической структуры разновидности этого химического элемента могут представлять собой большой набор совершенно разных веществ, от алмаза до графита, с разными электронными и механическими свойствами.
Углерод в виде древесного угля применялся в глубокой древности для выплавки металлов. Издавна известны аллотропные модификации углерода – алмаз и графит. Элементарная природа углерода установлена А. Лавуазье в конце 1780 х годов По многообразию полиморфных, или аллотропных (так как углерод – простое вещество), модификаций углерод уникален. В зависимости от кристаллической структуры разновидности этого химического элемента могут представлять собой большой набор совершенно разных веществ, от алмаза до графита, с разными электронными и механическими свойствами.
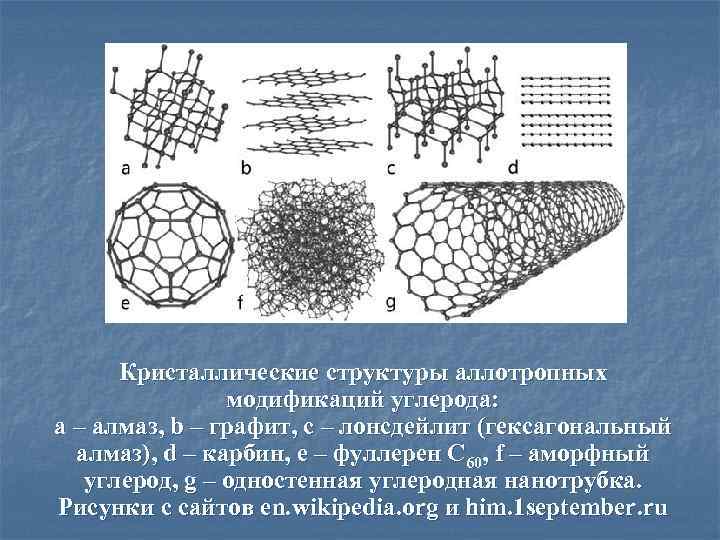 Кристаллические структуры аллотропных модификаций углерода: a – алмаз, b – графит, c – лонсдейлит (гексагональный алмаз), d – карбин, e – фуллерен C 60, f – аморфный углерод, g – одностенная углеродная нанотрубка. Рисунки с сайтов en. wikipedia. org и him. 1 september. ru
Кристаллические структуры аллотропных модификаций углерода: a – алмаз, b – графит, c – лонсдейлит (гексагональный алмаз), d – карбин, e – фуллерен C 60, f – аморфный углерод, g – одностенная углеродная нанотрубка. Рисунки с сайтов en. wikipedia. org и him. 1 september. ru
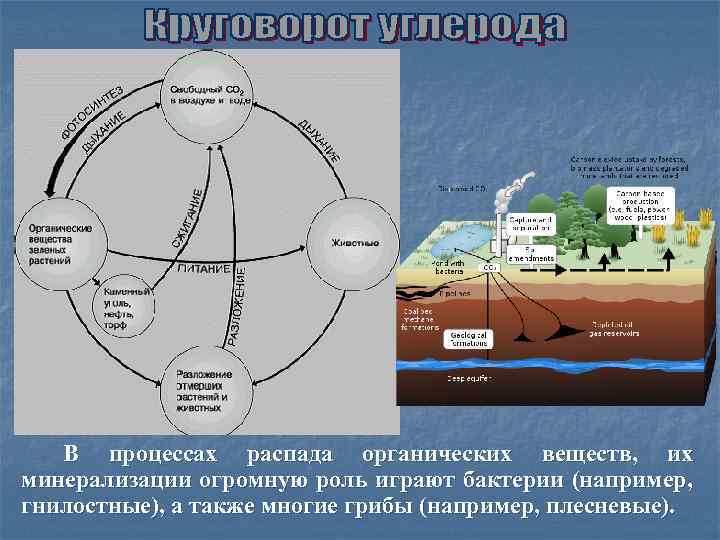 В процессах распада органических веществ, их минерализации огромную роль играют бактерии (например, гнилостные), а также многие грибы (например, плесневые).
В процессах распада органических веществ, их минерализации огромную роль играют бактерии (например, гнилостные), а также многие грибы (например, плесневые).
 В активном круговороте углерода участвует очень небольшая часть всей его массы. Огромное количество угольной кислоты законсервировано в виде ископаемых известняков и других пород. Между углекислым газом атмосферы и водой океана, в свою очередь, существует подвижное равновесие. Многие водные организмы поглощают углекислый кальций, создают свои скелеты, а затем из них образуются пласты известняков. Из атмосферы было извлечено и захоронено в десятки тысяч раз больше углекислого газа, чем в ней находится в данный момент. Атмосфера пополняется углекислым газом благодаря процессам разложения органического вещества, карбонатов и др. , а также, всё в большей мере, в результате индустриальной деятельности человека.
В активном круговороте углерода участвует очень небольшая часть всей его массы. Огромное количество угольной кислоты законсервировано в виде ископаемых известняков и других пород. Между углекислым газом атмосферы и водой океана, в свою очередь, существует подвижное равновесие. Многие водные организмы поглощают углекислый кальций, создают свои скелеты, а затем из них образуются пласты известняков. Из атмосферы было извлечено и захоронено в десятки тысяч раз больше углекислого газа, чем в ней находится в данный момент. Атмосфера пополняется углекислым газом благодаря процессам разложения органического вещества, карбонатов и др. , а также, всё в большей мере, в результате индустриальной деятельности человека.
 Особенно мощным источником являются вулканы, газы которых состоят главным образом из углекислого газа и паров воды. Некоторая часть углекислого газа и воды, извергаемых вулканами, возрождается из осадочных пород, в частности известняков, при контакте магмы с ними и их ассимиляции магмой. В процессе круговорота углерода происходит неоднократное фракционирование его по изотопному составу (12 C – 16 C), особенно в магматогенном процессе (образование CO 2, алмазов, карбонатов), при биогенном образовании органического вещества (угля, нефти, тканей организмов и др. ).
Особенно мощным источником являются вулканы, газы которых состоят главным образом из углекислого газа и паров воды. Некоторая часть углекислого газа и воды, извергаемых вулканами, возрождается из осадочных пород, в частности известняков, при контакте магмы с ними и их ассимиляции магмой. В процессе круговорота углерода происходит неоднократное фракционирование его по изотопному составу (12 C – 16 C), особенно в магматогенном процессе (образование CO 2, алмазов, карбонатов), при биогенном образовании органического вещества (угля, нефти, тканей организмов и др. ).
 Содержание углерода, масс. доля, % (по А. П. Виноградову) Земная кора Почвы Морская вода 0, 15 2, 0 0, 002 Растения Животные 18 21 В земной коре большая часть его углерода входит в состав карбонатов (Са. СО 3, Mg. CО 3), нефти, каменного и бурого угля, сланцев, при родного газа. Хотя содержание СО 2 в атмосфере невелико (~0, 03 %), но его общая масса составляет около 600 млн. т. Встречается углерод и в свободном состоянии в виде графита и алмаза.
Содержание углерода, масс. доля, % (по А. П. Виноградову) Земная кора Почвы Морская вода 0, 15 2, 0 0, 002 Растения Животные 18 21 В земной коре большая часть его углерода входит в состав карбонатов (Са. СО 3, Mg. CО 3), нефти, каменного и бурого угля, сланцев, при родного газа. Хотя содержание СО 2 в атмосфере невелико (~0, 03 %), но его общая масса составляет около 600 млн. т. Встречается углерод и в свободном состоянии в виде графита и алмаза.
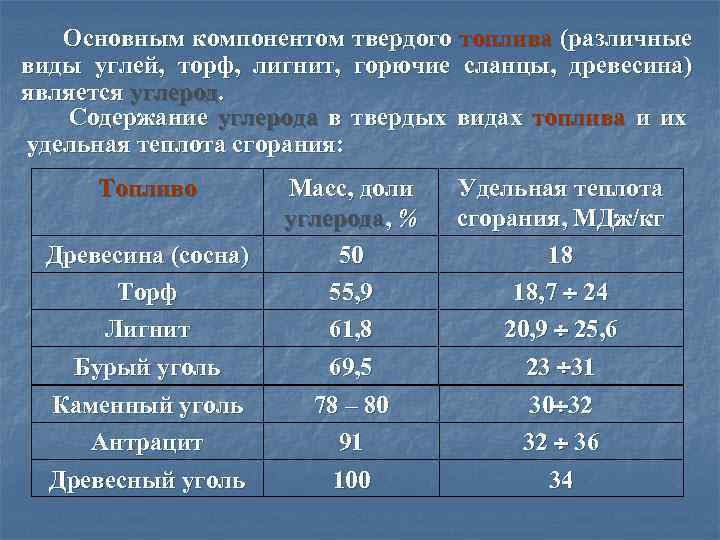 Основным компонентом твердого топлива (различные виды углей, торф, лигнит, горючие сланцы, древесина) является углерод. Содержание углерода в твердых видах топлива и их удельная теплота сгорания: Топливо Древесина (сосна) Торф Лигнит Бурый уголь Масс, доли углерода, % 50 55, 9 61, 8 69, 5 Удельная теплота сгорания, МДж/кг 18 18, 7 24 20, 9 25, 6 23 31 Каменный уголь Антрацит Древесный уголь 78 – 80 91 100 30 32 32 36 34
Основным компонентом твердого топлива (различные виды углей, торф, лигнит, горючие сланцы, древесина) является углерод. Содержание углерода в твердых видах топлива и их удельная теплота сгорания: Топливо Древесина (сосна) Торф Лигнит Бурый уголь Масс, доли углерода, % 50 55, 9 61, 8 69, 5 Удельная теплота сгорания, МДж/кг 18 18, 7 24 20, 9 25, 6 23 31 Каменный уголь Антрацит Древесный уголь 78 – 80 91 100 30 32 32 36 34
 Обычно топливо классифицируют по его агрегатному состоянию: твердое (уголь, торф, древесина, сланцы), жидкое (нефть и нефтепродукты) и газообразное (природный газ). Также можно разделить виды топлива и по его происхождению: растительное, минеральное и продукты промышленной переработки.
Обычно топливо классифицируют по его агрегатному состоянию: твердое (уголь, торф, древесина, сланцы), жидкое (нефть и нефтепродукты) и газообразное (природный газ). Также можно разделить виды топлива и по его происхождению: растительное, минеральное и продукты промышленной переработки.
 Среднее содержание углерода в живом веществе 21 % – по В. И. Вернадскому углерод относится к углерод макроэлементам. В результате естественного отбора основу живых систем составляют только шесть элементов: углерод, водород, кислород, азот, фосфор, сера, получивших название органогенов. Эти элементы составляют в организме 97, 4 %. Органогеном номер 1, несомненно, является углерод. Он способен образовывать прочные ковалентные связи.
Среднее содержание углерода в живом веществе 21 % – по В. И. Вернадскому углерод относится к углерод макроэлементам. В результате естественного отбора основу живых систем составляют только шесть элементов: углерод, водород, кислород, азот, фосфор, сера, получивших название органогенов. Эти элементы составляют в организме 97, 4 %. Органогеном номер 1, несомненно, является углерод. Он способен образовывать прочные ковалентные связи.
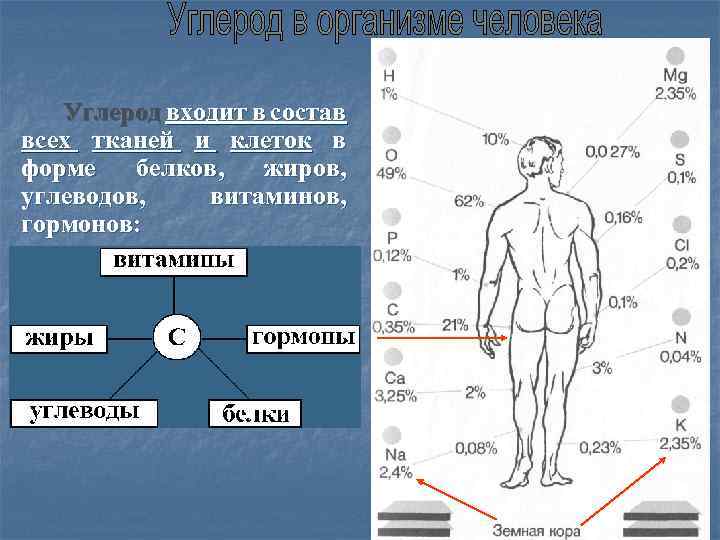 Углерод входит в состав всех тканей и клеток в форме белков, жиров, углеводов, витаминов, гормонов:
Углерод входит в состав всех тканей и клеток в форме белков, жиров, углеводов, витаминов, гормонов:
 Углерод располагается во II периоде, 4 группе, главной подгруппе. электронная формула С: 1 s 2 2 p 2 валентные электроны Электронно графическая формула С: В н. с. (нормальное состояние), степень окисления +2 У углерода на внешнем энергетическом уровне есть свободные 2 р орбитали, поэтому при возбуждении один электрон 2 s орбитали перейдет на свободную 2 р орбиталь:
Углерод располагается во II периоде, 4 группе, главной подгруппе. электронная формула С: 1 s 2 2 p 2 валентные электроны Электронно графическая формула С: В н. с. (нормальное состояние), степень окисления +2 У углерода на внешнем энергетическом уровне есть свободные 2 р орбитали, поэтому при возбуждении один электрон 2 s орбитали перейдет на свободную 2 р орбиталь:
 В в. с. (возбужденном состоянии), степень окисления +4 В большинстве неорганических соединений углерод имеет степень окисления +4, в оксиде углерода СО и карбонилах металлов степень окисления углерода равна +2, в дициане C 2 N 2 и галогенцианах +3 (по ряду химических свойств галогенцианы напоминают молекулы галогенов, поэтому степень окисления галогенов в галогенцианах целесообразно считать равной 0). Важнейшие неорганические соединения углерода: монооксид углерода СО и карбонилы металлов; диоксид углерода СО 2 и соли Н 2 СО 3 – карбонаты; синильная кислота HCN и ее соли – циани ды, омплексы, содержащие комплексы, к CN–; соли HNCS – роданиды; серо углерод CS 2; фосген СОСl 2; четыреххлористый углерод ССl 4; карбиды Са. С 2, Fe 3 C, WC, Мо. С и некоторые др. В живом организме углерод находится и степени окисления +4
В в. с. (возбужденном состоянии), степень окисления +4 В большинстве неорганических соединений углерод имеет степень окисления +4, в оксиде углерода СО и карбонилах металлов степень окисления углерода равна +2, в дициане C 2 N 2 и галогенцианах +3 (по ряду химических свойств галогенцианы напоминают молекулы галогенов, поэтому степень окисления галогенов в галогенцианах целесообразно считать равной 0). Важнейшие неорганические соединения углерода: монооксид углерода СО и карбонилы металлов; диоксид углерода СО 2 и соли Н 2 СО 3 – карбонаты; синильная кислота HCN и ее соли – циани ды, омплексы, содержащие комплексы, к CN–; соли HNCS – роданиды; серо углерод CS 2; фосген СОСl 2; четыреххлористый углерод ССl 4; карбиды Са. С 2, Fe 3 C, WC, Мо. С и некоторые др. В живом организме углерод находится и степени окисления +4
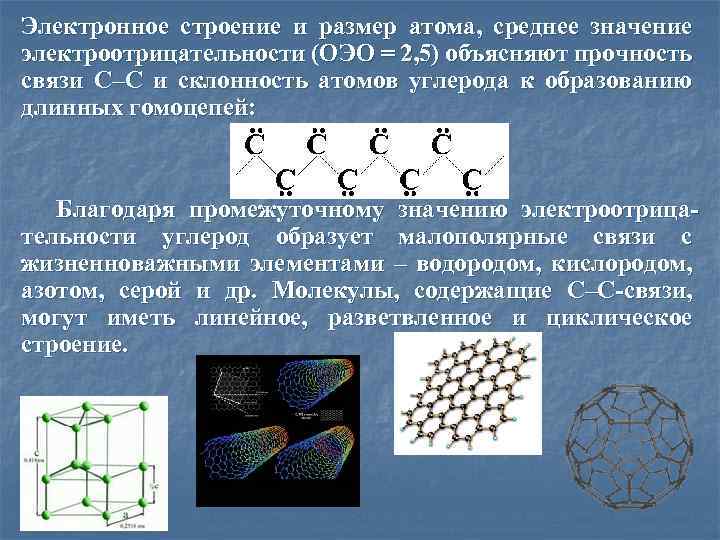 Электронное строение и размер атома, среднее значение электроотрицательности (ОЭО = 2, 5) объясняют прочность связи С–С и склонность атомов углерода к образованию длинных гомоцепей: Благодаря промежуточному значению электроотрица тельности углерод образует малополярные связи с жизненноважными элементами – водородом, кислородом, азотом, серой и др. Молекулы, содержащие С–С связи, могут иметь линейное, разветвленное и циклическое строение.
Электронное строение и размер атома, среднее значение электроотрицательности (ОЭО = 2, 5) объясняют прочность связи С–С и склонность атомов углерода к образованию длинных гомоцепей: Благодаря промежуточному значению электроотрица тельности углерод образует малополярные связи с жизненноважными элементами – водородом, кислородом, азотом, серой и др. Молекулы, содержащие С–С связи, могут иметь линейное, разветвленное и циклическое строение.
 Различные органические молекулы, содержащие связанные между собой атомы углерода с разнообразными заместителями, образуют громадное число биомолекул.
Различные органические молекулы, содержащие связанные между собой атомы углерода с разнообразными заместителями, образуют громадное число биомолекул.
 Оксид углерода (IV) СО 2 являются кислотным, и соответствующий ему гидроксид Н 2 СО 3 – слабой кислотой. Диоксид углерода СО 2 постоянно образуется в тканях организма в процессе обмена веществ и играет важную роль в регуляции дыхания и кровообращения. Диоксид углерода является физиологическим стимулятором дыхательного центра. Большие концентрации СО 2 (свыше 10 %) вызывают сильный ацидоз – снижение р. Н крови, бурную одышку и паралич дыхательного центра.
Оксид углерода (IV) СО 2 являются кислотным, и соответствующий ему гидроксид Н 2 СО 3 – слабой кислотой. Диоксид углерода СО 2 постоянно образуется в тканях организма в процессе обмена веществ и играет важную роль в регуляции дыхания и кровообращения. Диоксид углерода является физиологическим стимулятором дыхательного центра. Большие концентрации СО 2 (свыше 10 %) вызывают сильный ацидоз – снижение р. Н крови, бурную одышку и паралич дыхательного центра.
 Углерод диоксид растворяется в воде (0, 03 моль/л при 298 К). При этом в растворе образуется угольная кислота: Н 2 O + СO 2 Н 2 СО 3 Равновесие смещено влево, поэтому большая часть углерода диоксида находится в виде гидрата СО 2. Н 2 О, а не Н 2 СО 3. Угольная кислота Н 2 СО 3 существует только в растворе. Относится к слабым кислотам: K 1 = 4, 2. 10– 7, K 2 = 4, 8. 10– 11 моль/л.
Углерод диоксид растворяется в воде (0, 03 моль/л при 298 К). При этом в растворе образуется угольная кислота: Н 2 O + СO 2 Н 2 СО 3 Равновесие смещено влево, поэтому большая часть углерода диоксида находится в виде гидрата СО 2. Н 2 О, а не Н 2 СО 3. Угольная кислота Н 2 СО 3 существует только в растворе. Относится к слабым кислотам: K 1 = 4, 2. 10– 7, K 2 = 4, 8. 10– 11 моль/л.
 Растворы солей угольной кислоты вследствие гидролиза имеют щелочную реакцию (р. Н>7), например: Na 2 CO 3 + НОН Na. HCO 3 + Na. OH CO 32– + НОН НCO 3– + ОН– Водородкарбонатная буферная система (Н 2 СО 3 – НCO 3–) служит главной буферной системой плазмы крови, обеспечивающей поддержание кислотно основного гомеостаза, постоянного значения р. Н крови порядка 7, 4. Так как при гидролизе карбонатов и водородкарбонатов и получается щелочная среда, эти соединения применяют в медицинской практике в качестве антацидных (нейтрализующих кислоты) средств при повышенной кислотности желудочного сока. К ним относятся натрий водородкарбонат Na. HCO 3 и кальций карбонат Са. СО 3: Na. HCO 3 + НСl Na. Cl + Н 2 О + СО 2 Са. СО 3 + 2 НСl Са. Сl 2 + Н 2 О + СО 2
Растворы солей угольной кислоты вследствие гидролиза имеют щелочную реакцию (р. Н>7), например: Na 2 CO 3 + НОН Na. HCO 3 + Na. OH CO 32– + НОН НCO 3– + ОН– Водородкарбонатная буферная система (Н 2 СО 3 – НCO 3–) служит главной буферной системой плазмы крови, обеспечивающей поддержание кислотно основного гомеостаза, постоянного значения р. Н крови порядка 7, 4. Так как при гидролизе карбонатов и водородкарбонатов и получается щелочная среда, эти соединения применяют в медицинской практике в качестве антацидных (нейтрализующих кислоты) средств при повышенной кислотности желудочного сока. К ним относятся натрий водородкарбонат Na. HCO 3 и кальций карбонат Са. СО 3: Na. HCO 3 + НСl Na. Cl + Н 2 О + СО 2 Са. СО 3 + 2 НСl Са. Сl 2 + Н 2 О + СО 2
 Из соединений элементов IVA группы, в которых они проявляют степень окисления +2, интерес для медиков и биологов представляет углерод (II) оксид СО. Это соединение ядовито и чрезвычайно опасно, потому что не имеет запаха. Углерод (II) оксид – угарный газ – продукт неполного окисления углерода. Как это ни парадоксально, одним из источников СО является сам человек, организм которого производит и выделяет во внешнюю среду (с выдыхаемым воздухом) за сутки около 10 мл СО. Это так называемый эндогенный углерод (II) оксид, который образуется в процессах кроветворения.
Из соединений элементов IVA группы, в которых они проявляют степень окисления +2, интерес для медиков и биологов представляет углерод (II) оксид СО. Это соединение ядовито и чрезвычайно опасно, потому что не имеет запаха. Углерод (II) оксид – угарный газ – продукт неполного окисления углерода. Как это ни парадоксально, одним из источников СО является сам человек, организм которого производит и выделяет во внешнюю среду (с выдыхаемым воздухом) за сутки около 10 мл СО. Это так называемый эндогенный углерод (II) оксид, который образуется в процессах кроветворения.
 Проникая с воздухом в легкие, углерод (II) оксид быстро проходит через альвеолярно капиллярную мембрану, растворяется в плазме крови, диффундирует в эритроциты и вступает в обратимое химическое взаимодействие как с окисленным Hb. О 2, так и с восстановленным гемоглобином Нb: Нb. О 2 + СО Нb. СО + О 2 Нb + СО Нb. СО Образующийся карбонилгемоглобин Нb. СО не способен присоединять к себе кислород. Вследствие этого становится невозможным перенос кислорода от легких к тканям.
Проникая с воздухом в легкие, углерод (II) оксид быстро проходит через альвеолярно капиллярную мембрану, растворяется в плазме крови, диффундирует в эритроциты и вступает в обратимое химическое взаимодействие как с окисленным Hb. О 2, так и с восстановленным гемоглобином Нb: Нb. О 2 + СО Нb. СО + О 2 Нb + СО Нb. СО Образующийся карбонилгемоглобин Нb. СО не способен присоединять к себе кислород. Вследствие этого становится невозможным перенос кислорода от легких к тканям.
 Высокое химическое сродство углерода (II) оксида СО к двухвалентному железу является основной причиной взаимодействия СО с гемоглобином. Можно полагать, что и другие бионеорганические соединения, содержащие ионы Fe 2+, должны реагировать с этим ядом. Так как реакция взаимодействия оксигемоглобина с угарным газом обратима, то повышение в дыхательной среде парциального давления О 2 будет ускорять диссоциацию карбонилгемоглобина и выделение СО из организма (равновесие смещается влево по принципу Ле Шателье): Нb. О 2 + СО Нb. СО + О 2 В настоящее время имеются лечебные препараты, которые используют в качестве антидотов при отравлении организма углеродом (II) оксидом. Например, введение восстановленного железа резко ускоряет удаление СО из организма в виде, очевидно, карбонила железа. Действие этого препарата основано на способности СО выступать в качестве лиганда в различных комплексах.
Высокое химическое сродство углерода (II) оксида СО к двухвалентному железу является основной причиной взаимодействия СО с гемоглобином. Можно полагать, что и другие бионеорганические соединения, содержащие ионы Fe 2+, должны реагировать с этим ядом. Так как реакция взаимодействия оксигемоглобина с угарным газом обратима, то повышение в дыхательной среде парциального давления О 2 будет ускорять диссоциацию карбонилгемоглобина и выделение СО из организма (равновесие смещается влево по принципу Ле Шателье): Нb. О 2 + СО Нb. СО + О 2 В настоящее время имеются лечебные препараты, которые используют в качестве антидотов при отравлении организма углеродом (II) оксидом. Например, введение восстановленного железа резко ускоряет удаление СО из организма в виде, очевидно, карбонила железа. Действие этого препарата основано на способности СО выступать в качестве лиганда в различных комплексах.
 Некоторое количество СО содержится в автомобильных выхлопных газах, что сильно загрязняет атмосферу в больших городах. Актуальной проблемой является создание «чистого автомобиля» . В настоящее время преобладают два направления решения данной задачи – создание электрического автомобиля с химическими источниками тока и оборудование обычных автомобилей каталитическими приставками, «дожигающими» СО в выхлопных газах. Такие приставки разработаны (Д. В Сокольским с сотрудниками) и используются, но пока несколько дороги, так как в состав контактной массы входит палладий.
Некоторое количество СО содержится в автомобильных выхлопных газах, что сильно загрязняет атмосферу в больших городах. Актуальной проблемой является создание «чистого автомобиля» . В настоящее время преобладают два направления решения данной задачи – создание электрического автомобиля с химическими источниками тока и оборудование обычных автомобилей каталитическими приставками, «дожигающими» СО в выхлопных газах. Такие приставки разработаны (Д. В Сокольским с сотрудниками) и используются, но пока несколько дороги, так как в состав контактной массы входит палладий.
 Высокодисперсный углерод обладает значительной адсорбционной способностью. Одним из широко применяемых адсорбентов является активный уголь. Ею получают обработкой древесного угля перегретым водяным паром, который удаляет смолистые ве щества, заполняющие поры угля, повторяющие капиллярное стро ение древесины. В качестве адсорбентов применяют также угли, получаемые из других животных и растительных тканей – кости, крови, фруктовых косточек. Явление адсорбции было открыто и изучено именно на древесном угле. Поглощение газов углем было замечено в 1773 г Шееле (Швеция) и в 1777 г. Фонтана (Франция) В 1785 г. академик Т. Е. Ловиц (Россия) открыл адсорбцию углем растворенных веществ, обстоятельно исследовал это явление и предложил применять его для очистки органических веществ Академик Н Д Зелинский в 1915 г разработал противогаз, действие которого основано на адсорбции отравляющих веществ активным углем.
Высокодисперсный углерод обладает значительной адсорбционной способностью. Одним из широко применяемых адсорбентов является активный уголь. Ею получают обработкой древесного угля перегретым водяным паром, который удаляет смолистые ве щества, заполняющие поры угля, повторяющие капиллярное стро ение древесины. В качестве адсорбентов применяют также угли, получаемые из других животных и растительных тканей – кости, крови, фруктовых косточек. Явление адсорбции было открыто и изучено именно на древесном угле. Поглощение газов углем было замечено в 1773 г Шееле (Швеция) и в 1777 г. Фонтана (Франция) В 1785 г. академик Т. Е. Ловиц (Россия) открыл адсорбцию углем растворенных веществ, обстоятельно исследовал это явление и предложил применять его для очистки органических веществ Академик Н Д Зелинский в 1915 г разработал противогаз, действие которого основано на адсорбции отравляющих веществ активным углем.
 Древесный уголь (кожа ящерицы)
Древесный уголь (кожа ящерицы)
 Водородные соединения углерода – углеводороды являются объектом изучения в органической химии. Поэтому кратко отметим лишь некоторые свойства простейшего из них – метана СН 4. Метан образуется при взаимодействии углерода с водородом: С + 2 Н 2 СН 4 При низких температурах данная реакция идет медленно, а при высоких ее равновесие смещено влево. В лабораторных условиях СН 4 получают нагреванием безводного ацетата натрия со ще лочью: CH 3 COONa + Na. OH СН 4 + Na 2 CО 3 Основным промышленным источником метана является природный газ, содержащий ~94 % СН 4. Метан – горючий газ без цвета, вкуса и запаха, т. кип. – 161 о. С, т. пл. – 184 °С, малорастворим в воде и не реагирует с ней при комнатной температуре.
Водородные соединения углерода – углеводороды являются объектом изучения в органической химии. Поэтому кратко отметим лишь некоторые свойства простейшего из них – метана СН 4. Метан образуется при взаимодействии углерода с водородом: С + 2 Н 2 СН 4 При низких температурах данная реакция идет медленно, а при высоких ее равновесие смещено влево. В лабораторных условиях СН 4 получают нагреванием безводного ацетата натрия со ще лочью: CH 3 COONa + Na. OH СН 4 + Na 2 CО 3 Основным промышленным источником метана является природный газ, содержащий ~94 % СН 4. Метан – горючий газ без цвета, вкуса и запаха, т. кип. – 161 о. С, т. пл. – 184 °С, малорастворим в воде и не реагирует с ней при комнатной температуре.


