Лекция 10 платиновые металлы.ppt
- Количество слайдов: 73
 Лекция Платиновые металлы
Лекция Платиновые металлы

 К платиновым металлам относятся: Ru (4 d 75 s 1) 44 Rh (4 d 85 s 1) 45 Pd (4 d 95 s 1) 46 Os (5 d 66 s 2) 76 Ir (5 d 76 s 2) 77 Pt (5 d 96 s 1) 78
К платиновым металлам относятся: Ru (4 d 75 s 1) 44 Rh (4 d 85 s 1) 45 Pd (4 d 95 s 1) 46 Os (5 d 66 s 2) 76 Ir (5 d 76 s 2) 77 Pt (5 d 96 s 1) 78
 Все платиновые металлы относятся к числу мало распространенных элементов. Содержание их в рудах не превышает «граммов» на тонну.
Все платиновые металлы относятся к числу мало распространенных элементов. Содержание их в рудах не превышает «граммов» на тонну.
 Платина • В записях А. де Ульолоа упоминается благородный металл platina (испанское platina, уменьшительное от plata — серебро), найденный в колумбийских золотых рудниках (1736). • В 1741 южноамериканские образцы металла были доставлены в Европу, где сначала платину рассматривали как «белое золото» . В середине 18 века (1752) была установлена элементарная природа платины. В настоящее время «белым золотом» называют сплавы золота и платины.
Платина • В записях А. де Ульолоа упоминается благородный металл platina (испанское platina, уменьшительное от plata — серебро), найденный в колумбийских золотых рудниках (1736). • В 1741 южноамериканские образцы металла были доставлены в Европу, где сначала платину рассматривали как «белое золото» . В середине 18 века (1752) была установлена элементарная природа платины. В настоящее время «белым золотом» называют сплавы золота и платины.
 РУТЕНИЙ • РУТЕНИЙ (от латинского названия России - Ruthenia). • В 1844 в Казанском университете К. К. Клаус выделил из уральской самородной платины 6 г неизвестного ранее металла. Он определил его атомную массу, исследовал химические свойства и дал название.
РУТЕНИЙ • РУТЕНИЙ (от латинского названия России - Ruthenia). • В 1844 в Казанском университете К. К. Клаус выделил из уральской самородной платины 6 г неизвестного ранее металла. Он определил его атомную массу, исследовал химические свойства и дал название.
 Родий • В 1803 английский ученый У. Х. Волластон исследовал фильтрат, полученный после растворения самородной южноамериканской платины в царской водке. • В 1804 он выделил из этого фильтрата розовато-красный порошок, последующее прокаливание которого в атмосфере водорода привело к получению порошка нового металла — родия. Название происходит от греческого rhodon — роза, по розовато-красному цвету его солей.
Родий • В 1803 английский ученый У. Х. Волластон исследовал фильтрат, полученный после растворения самородной южноамериканской платины в царской водке. • В 1804 он выделил из этого фильтрата розовато-красный порошок, последующее прокаливание которого в атмосфере водорода привело к получению порошка нового металла — родия. Название происходит от греческого rhodon — роза, по розовато-красному цвету его солей.
 Палладий • Палладий открыт в 1803 У. Х. Волластоном при изучении самородной платины. ПАЛЛАДИЙ - по названию одного из крупнейших астероидов Паллада.
Палладий • Палладий открыт в 1803 У. Х. Волластоном при изучении самородной платины. ПАЛЛАДИЙ - по названию одного из крупнейших астероидов Паллада.
 Осмий • Открыт в 1804 английским химиком С. Теннантом в черном порошке, остающемся после растворения платины в царской водке. • Для осмия характерно образование тетраоксида Os. O 4 с резким запахом. Отсюда и название элемента, происходящее от греческого «осме» — запах.
Осмий • Открыт в 1804 английским химиком С. Теннантом в черном порошке, остающемся после растворения платины в царской водке. • Для осмия характерно образование тетраоксида Os. O 4 с резким запахом. Отсюда и название элемента, происходящее от греческого «осме» — запах.
 Иридий • Открыт в 1804 английским химиком С. Теннантом, который изучал состав платиновых минералов. • ИРИДИЙ - от греческого «ирис» — радуга.
Иридий • Открыт в 1804 английским химиком С. Теннантом, который изучал состав платиновых минералов. • ИРИДИЙ - от греческого «ирис» — радуга.
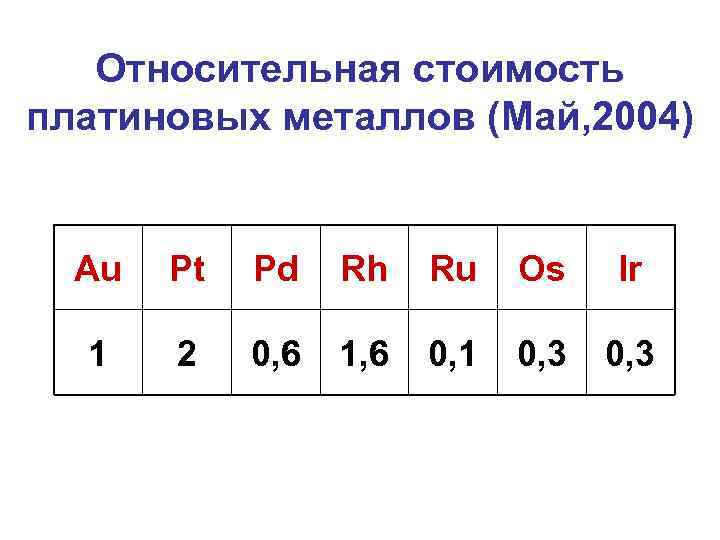 Относительная стоимость платиновых металлов (Май, 2004) Au Pt Pd Rh Ru Os Ir 1 2 0, 6 1, 6 0, 1 0, 3
Относительная стоимость платиновых металлов (Май, 2004) Au Pt Pd Rh Ru Os Ir 1 2 0, 6 1, 6 0, 1 0, 3
 • В свободном состоянии платиновые металлы очень тугоплавки и труднолетучи. По плотности иногда делят на • Легкие: Ru, Rh, Pd • Тяжелые: Os, Ir, Pt
• В свободном состоянии платиновые металлы очень тугоплавки и труднолетучи. По плотности иногда делят на • Легкие: Ru, Rh, Pd • Тяжелые: Os, Ir, Pt
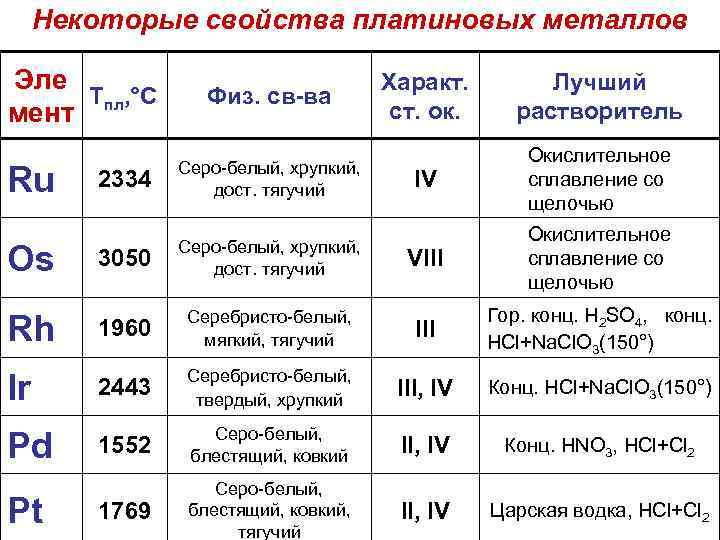 Некоторые свойства платиновых металлов Эле Тпл, °С мент Физ. св-ва Характ. ст. ок. Лучший растворитель IV Окислительное сплавление со щелочью VIII Окислительное сплавление со щелочью 2334 Серо-белый, хрупкий, дост. тягучий 3050 Серо-белый, хрупкий, дост. тягучий Rh 1960 Серебристо-белый, мягкий, тягучий III Гор. конц. H 2 SO 4, конц. HCl+Na. Cl. O 3(150°) Ir 2443 Серебристо-белый, твердый, хрупкий III, IV Конц. HCl+Na. Cl. O 3(150°) Pd 1552 Серо-белый, блестящий, ковкий II, IV Конц. HNO 3, HCl+Cl 2 1769 Серо-белый, блестящий, ковкий, тягучий II, IV Царская водка, HCl+Cl 2 Ru Os Pt
Некоторые свойства платиновых металлов Эле Тпл, °С мент Физ. св-ва Характ. ст. ок. Лучший растворитель IV Окислительное сплавление со щелочью VIII Окислительное сплавление со щелочью 2334 Серо-белый, хрупкий, дост. тягучий 3050 Серо-белый, хрупкий, дост. тягучий Rh 1960 Серебристо-белый, мягкий, тягучий III Гор. конц. H 2 SO 4, конц. HCl+Na. Cl. O 3(150°) Ir 2443 Серебристо-белый, твердый, хрупкий III, IV Конц. HCl+Na. Cl. O 3(150°) Pd 1552 Серо-белый, блестящий, ковкий II, IV Конц. HNO 3, HCl+Cl 2 1769 Серо-белый, блестящий, ковкий, тягучий II, IV Царская водка, HCl+Cl 2 Ru Os Pt
 Химические свойства • Платиновые металлы довольно устойчивы к химическому воздействию. • Наиболее активными являются Pt и Pd.
Химические свойства • Платиновые металлы довольно устойчивы к химическому воздействию. • Наиболее активными являются Pt и Pd.
 Растворение платиновых металлов • Сплавление со щелочью в присутствии окислителей: Ru + 3 KNO 3 + 2 KOH = K 2 Ru. O 4 + 3 KNO 2 + H 2 O
Растворение платиновых металлов • Сплавление со щелочью в присутствии окислителей: Ru + 3 KNO 3 + 2 KOH = K 2 Ru. O 4 + 3 KNO 2 + H 2 O
 • Растворение в царской водке: 3 Pt + 4 HNO 3 + 18 HCl = 3 H 2[Pt. Cl 6] + 4 NO + 8 H 2 O
• Растворение в царской водке: 3 Pt + 4 HNO 3 + 18 HCl = 3 H 2[Pt. Cl 6] + 4 NO + 8 H 2 O
 • Растворение в конц. HCl, насыщенной Cl 2: Pt + 2 Cl 2 + 2 HCl = H 2[Pt. Cl 6]
• Растворение в конц. HCl, насыщенной Cl 2: Pt + 2 Cl 2 + 2 HCl = H 2[Pt. Cl 6]
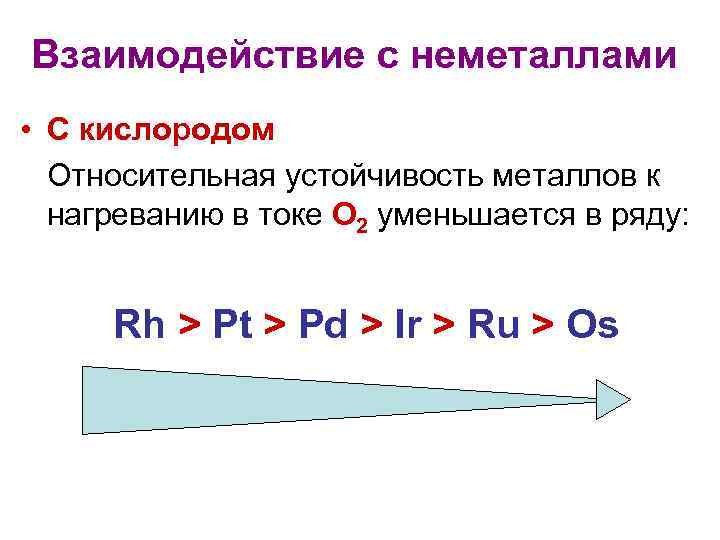 Взаимодействие с неметаллами • С кислородом Относительная устойчивость металлов к нагреванию в токе О 2 уменьшается в ряду: Rh > Pt > Pd > Ir > Ru > Os
Взаимодействие с неметаллами • С кислородом Относительная устойчивость металлов к нагреванию в токе О 2 уменьшается в ряду: Rh > Pt > Pd > Ir > Ru > Os
 • Тонкий порошок осмия медленно окисляется до Os. O 4 уже при комнатной температуре : Os + 2 O 2 → Os. O 4 • Для осмия наиболее характерно образование оксидов Os. O 4 и Os. O 2. • В газовой фазе существуют оксиды Os. O и Os. O 3.
• Тонкий порошок осмия медленно окисляется до Os. O 4 уже при комнатной температуре : Os + 2 O 2 → Os. O 4 • Для осмия наиболее характерно образование оксидов Os. O 4 и Os. O 2. • В газовой фазе существуют оксиды Os. O и Os. O 3.
 • Тетраоксид осмия Os. O 4 проявляет кислотные свойства и является сильным окислителем: Os. O 4 + Na. OH = Na 2[Os. O 4(OH)2].
• Тетраоксид осмия Os. O 4 проявляет кислотные свойства и является сильным окислителем: Os. O 4 + Na. OH = Na 2[Os. O 4(OH)2].
 • Компактный рутений не окисляется кислородом воздуха при нагревании до 930°C. • Порошкообразный рутений при нагревании реагирует с кислородом с образованием диоксида рутения Ru. O 2. • Известно несколько оксидов рутения.
• Компактный рутений не окисляется кислородом воздуха при нагревании до 930°C. • Порошкообразный рутений при нагревании реагирует с кислородом с образованием диоксида рутения Ru. O 2. • Известно несколько оксидов рутения.
 • Взаимодействие Ir с кислородом происходит только при температуре выше 1000°C: Ir + O 2 = Ir. O 2.
• Взаимодействие Ir с кислородом происходит только при температуре выше 1000°C: Ir + O 2 = Ir. O 2.
 • При 350 -800°C Pd окисляется с образованием оксида Pd. O: 2 Pd + O 2 = 2 Pd. O Выше 850°C оксид палладия Pd. O разлагается на металл и кислород, и при этих температурах Pd устойчив к окислению.
• При 350 -800°C Pd окисляется с образованием оксида Pd. O: 2 Pd + O 2 = 2 Pd. O Выше 850°C оксид палладия Pd. O разлагается на металл и кислород, и при этих температурах Pd устойчив к окислению.
 • Оксиды палладия (III) и (IV) при нагревании теряют кислород и переходят в Pd. O: 2 Pd 2 O 3 = 4 Pd. O + O 2, 2 Pd. O 2 = 2 Pd. O + O 2.
• Оксиды палладия (III) и (IV) при нагревании теряют кислород и переходят в Pd. O: 2 Pd 2 O 3 = 4 Pd. O + O 2, 2 Pd. O 2 = 2 Pd. O + O 2.
 • При нагревании платина реагирует с кислородом с образованием оксидов. • Выделены следующие оксиды платины: Pt. O, коричневый Pt. O 2, красновато-коричневый Pt. O 3, а черный также Pt 2 O 3 и Pt 3 O 4.
• При нагревании платина реагирует с кислородом с образованием оксидов. • Выделены следующие оксиды платины: Pt. O, коричневый Pt. O 2, красновато-коричневый Pt. O 3, а черный также Pt 2 O 3 и Pt 3 O 4.
 • Родий характеризуется высокой химической устойчивостью. С неметаллами он взаимодействует только при температуре красного каления. • Мелкоизмельченный родий медленно окисляется только при температуре выше 600°C: 4 Rh + 3 O 2 = 2 Rh 2 O 3.
• Родий характеризуется высокой химической устойчивостью. С неметаллами он взаимодействует только при температуре красного каления. • Мелкоизмельченный родий медленно окисляется только при температуре выше 600°C: 4 Rh + 3 O 2 = 2 Rh 2 O 3.
 • Взаимодействие с другими неметаллами • При нагревании осмий реагирует со фтором, хлором, кислородом, серой, другими халькогенами и неметаллами. Os + 3 F 2 = Os. F 6 (при 250– 300°C), Os + Cl 2 = Os. Cl 4 (при 650– 700°C).
• Взаимодействие с другими неметаллами • При нагревании осмий реагирует со фтором, хлором, кислородом, серой, другими халькогенами и неметаллами. Os + 3 F 2 = Os. F 6 (при 250– 300°C), Os + Cl 2 = Os. Cl 4 (при 650– 700°C).
 • Иридий отличается высокой химической стойкостью. С неметаллами взаимодействует только в мелкораздробленном состоянии при температуре красного каления.
• Иридий отличается высокой химической стойкостью. С неметаллами взаимодействует только в мелкораздробленном состоянии при температуре красного каления.
 • При комнатной температуре палладий реагирует с влажными Cl 2 и Br 2: Pd + Cl 2 = Pd. Cl 2 • При нагревании Pd реагирует с фтором, серой, селеном, теллуром, мышьяком и кремнием.
• При комнатной температуре палладий реагирует с влажными Cl 2 и Br 2: Pd + Cl 2 = Pd. Cl 2 • При нагревании Pd реагирует с фтором, серой, селеном, теллуром, мышьяком и кремнием.
 • Pd oбладает уникальной способностью растворять водород: в 1 объеме Pd при нормальных условиях растворяется 800 объемов H 2. Если Pd, поглотивший H 2, вынести на воздух, то он потеряет весь H 2.
• Pd oбладает уникальной способностью растворять водород: в 1 объеме Pd при нормальных условиях растворяется 800 объемов H 2. Если Pd, поглотивший H 2, вынести на воздух, то он потеряет весь H 2.
 • При нагревании платина реагирует с серой, селеном, теллуром, углеродом и кремнием. Pt + S → Pt. S
• При нагревании платина реагирует с серой, селеном, теллуром, углеродом и кремнием. Pt + S → Pt. S
 • При нагревании реагирует с галогенами в присутствии галогенидов щелочных металлов: Pt + 2 Cl 2 + 2 Na. Cl = Na 2[Pt. Cl 6]. cинтезированы такие галогениды платины как Pt. Br 4, Pt. Cl 2· 2 Pt. Cl 3, Pt. Br 2 и Pt. I 2
• При нагревании реагирует с галогенами в присутствии галогенидов щелочных металлов: Pt + 2 Cl 2 + 2 Na. Cl = Na 2[Pt. Cl 6]. cинтезированы такие галогениды платины как Pt. Br 4, Pt. Cl 2· 2 Pt. Cl 3, Pt. Br 2 и Pt. I 2
 • Как и палладий, платина может растворять молекулярный водород, но объем поглощаемого водорода меньше и способность его отдавать при нагревании у платины меньше.
• Как и палладий, платина может растворять молекулярный водород, но объем поглощаемого водорода меньше и способность его отдавать при нагревании у платины меньше.
 Соединения платиновых металлов Бинарные соединения Комплексные соединения Сульфиды, Оксиды, Галогениды, Фосфиды и др. Много!!!
Соединения платиновых металлов Бинарные соединения Комплексные соединения Сульфиды, Оксиды, Галогениды, Фосфиды и др. Много!!!
 Бинарные соединения • Наибольшее значение имеют оксиды и галогениды, которые используются для синтеза других соединений платиновой группы.
Бинарные соединения • Наибольшее значение имеют оксиды и галогениды, которые используются для синтеза других соединений платиновой группы.
 • Гексафторид Pt. F 6 — один из сильнейших окислителей, способный окислить молекулы кислорода, ксенона или NO: O 2 + Pt. F 6 = O 2+[Pt. F 6]–. (C обнаруженного Н. Бартлеттом взаимодействия между Хе и Pt. F 6, приводящего к образованию Xe. Pt. F 6, началась химия инертных газов. )
• Гексафторид Pt. F 6 — один из сильнейших окислителей, способный окислить молекулы кислорода, ксенона или NO: O 2 + Pt. F 6 = O 2+[Pt. F 6]–. (C обнаруженного Н. Бартлеттом взаимодействия между Хе и Pt. F 6, приводящего к образованию Xe. Pt. F 6, началась химия инертных газов. )
 • Образование комплексных соединений с участием тетрахлорида платины : Pt. Cl 4 + 2 Na. Cl = Na 2[Pt. Cl 6].
• Образование комплексных соединений с участием тетрахлорида платины : Pt. Cl 4 + 2 Na. Cl = Na 2[Pt. Cl 6].
 • В присутствии хлоридов палладия образуются комплексы: Pd. Cl 4 + 2 Na. Cl = Na 2 Pd. Cl 6 • Гидроксиды палладия также участвуют в образовании комплексов Pd(OH)4 + 2 KOH = K 2 Pd(OH)6
• В присутствии хлоридов палладия образуются комплексы: Pd. Cl 4 + 2 Na. Cl = Na 2 Pd. Cl 6 • Гидроксиды палладия также участвуют в образовании комплексов Pd(OH)4 + 2 KOH = K 2 Pd(OH)6
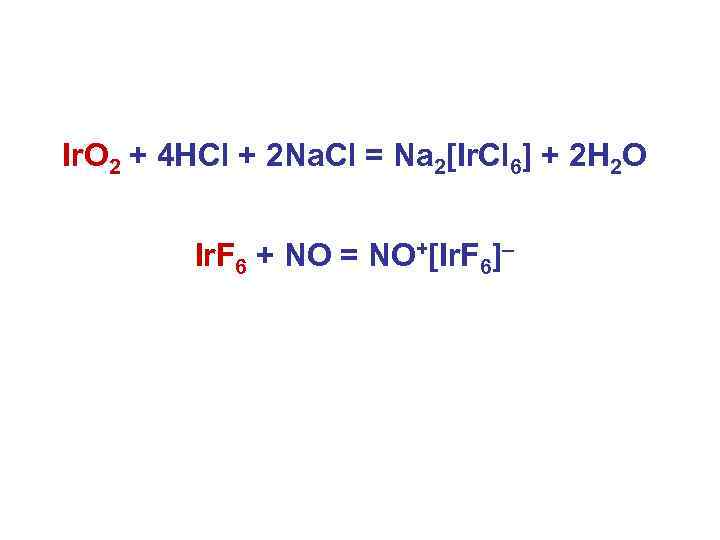 Ir. O 2 + 4 HCl + 2 Na. Cl = Na 2[Ir. Cl 6] + 2 H 2 O Ir. F 6 + NO = NO+[Ir. F 6]–
Ir. O 2 + 4 HCl + 2 Na. Cl = Na 2[Ir. Cl 6] + 2 H 2 O Ir. F 6 + NO = NO+[Ir. F 6]–
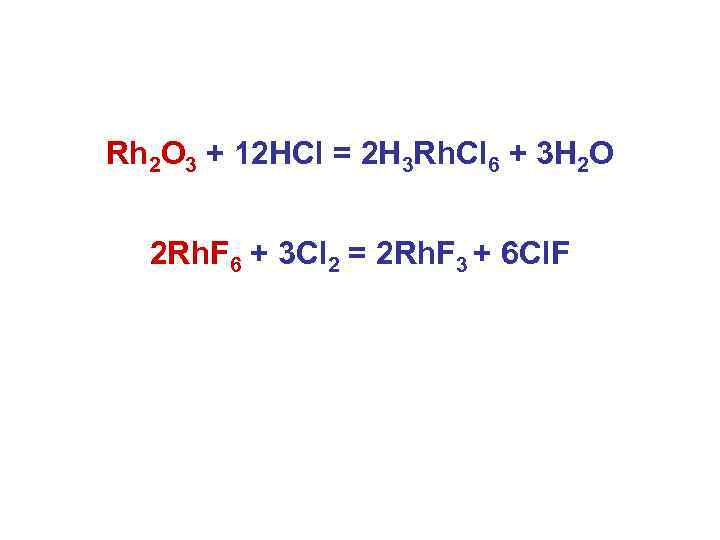 Rh 2 O 3 + 12 HCl = 2 H 3 Rh. Cl 6 + 3 H 2 O 2 Rh. F 6 + 3 Cl 2 = 2 Rh. F 3 + 6 Cl. F
Rh 2 O 3 + 12 HCl = 2 H 3 Rh. Cl 6 + 3 H 2 O 2 Rh. F 6 + 3 Cl 2 = 2 Rh. F 3 + 6 Cl. F
 Комплексные соединения платиновых металлов §Очевидно, что координация лигандов к § § металлу меняет все свойства и лигандов, и металла. Участвуют в таких же реакциях, что и любые другие соединения, также проявляют специфическую реакционноспособность. Специфический для комплексных соединений тип реакций – реакции замещения лигандов.
Комплексные соединения платиновых металлов §Очевидно, что координация лигандов к § § металлу меняет все свойства и лигандов, и металла. Участвуют в таких же реакциях, что и любые другие соединения, также проявляют специфическую реакционноспособность. Специфический для комплексных соединений тип реакций – реакции замещения лигандов.
![Реакции замещения лигандов MXn +Y = MXn-1 Y +X • Пример: [Pt(NH 3)4]2+ + Реакции замещения лигандов MXn +Y = MXn-1 Y +X • Пример: [Pt(NH 3)4]2+ +](https://present5.com/presentation/126659746_100833605/image-42.jpg) Реакции замещения лигандов MXn +Y = MXn-1 Y +X • Пример: [Pt(NH 3)4]2+ + Cl- = [Pt(NH 3)3 Cl]+ + NH 3
Реакции замещения лигандов MXn +Y = MXn-1 Y +X • Пример: [Pt(NH 3)4]2+ + Cl- = [Pt(NH 3)3 Cl]+ + NH 3
 Академик Черняев Илья Ильич (1893 -1966) Возглавлял кафедру с 1934 по 1941 г. Действительный член АН СССР, четырежды лауреат Государственной премии СССР (1946, 1949, 1951, 1952 гг. ), ученик Л. А. Чугаева, Черняев И. И. - выдающийся учёный и талантливый исследователь в области химии платиновых металлов и актиноидов, один из создаталей аффинажной промышленности платиновых металлов в нашей стране. Он внёс большой вклад в разработку технологии веществ для оборонной промышленности.
Академик Черняев Илья Ильич (1893 -1966) Возглавлял кафедру с 1934 по 1941 г. Действительный член АН СССР, четырежды лауреат Государственной премии СССР (1946, 1949, 1951, 1952 гг. ), ученик Л. А. Чугаева, Черняев И. И. - выдающийся учёный и талантливый исследователь в области химии платиновых металлов и актиноидов, один из создаталей аффинажной промышленности платиновых металлов в нашей стране. Он внёс большой вклад в разработку технологии веществ для оборонной промышленности.
 Транс-влияние • В 1926 г. И. И. Черняевым было открыто явление транс-влияния: природа лиганда, находящегося в трансположении(напротив) к замещаемому лиганду, оказывает решающее влияние на скорость замещения. • Это позволяет направленно синтезировать пространственные изомеры.
Транс-влияние • В 1926 г. И. И. Черняевым было открыто явление транс-влияния: природа лиганда, находящегося в трансположении(напротив) к замещаемому лиганду, оказывает решающее влияние на скорость замещения. • Это позволяет направленно синтезировать пространственные изомеры.
![• При действии NH 3 на [Pt(Сl)4]2 - всегда получается цис-изомер: Сl Сl • При действии NH 3 на [Pt(Сl)4]2 - всегда получается цис-изомер: Сl Сl](https://present5.com/presentation/126659746_100833605/image-45.jpg) • При действии NH 3 на [Pt(Сl)4]2 - всегда получается цис-изомер: Сl Сl Сl Pt 2 - Сl NH 3 Сl Сl Pt NH 3 Сl _ Сl NH 3 Сl Pt NH 3
• При действии NH 3 на [Pt(Сl)4]2 - всегда получается цис-изомер: Сl Сl Сl Pt 2 - Сl NH 3 Сl Сl Pt NH 3 Сl _ Сl NH 3 Сl Pt NH 3
![• При действии Сl- на [Pt(NH 3)4]2+ всегда получается транс-изомер: NH 3 Pt • При действии Сl- на [Pt(NH 3)4]2+ всегда получается транс-изомер: NH 3 Pt](https://present5.com/presentation/126659746_100833605/image-46.jpg) • При действии Сl- на [Pt(NH 3)4]2+ всегда получается транс-изомер: NH 3 Pt NH 3 2+ Сl- + NH 3 Сl Pt NH 3 Сl- NH 3 Сl Pt Сl NH 3
• При действии Сl- на [Pt(NH 3)4]2+ всегда получается транс-изомер: NH 3 Pt NH 3 2+ Сl- + NH 3 Сl Pt NH 3 Сl- NH 3 Сl Pt Сl NH 3
 Ряд транс-влияния лигандов - ~ CO ~ C CN 2 H 4 > NO 2 - > Cl- > NH Br 3 - > > J - > H > OH 2 O
Ряд транс-влияния лигандов - ~ CO ~ C CN 2 H 4 > NO 2 - > Cl- > NH Br 3 - > > J - > H > OH 2 O
 Механизмы замещения лигандов Ln. MX +Y = Ln. MY +X • Возможны два предельных(идеальных) механизма: 1. Диссоциативный 2. Ассоциативный
Механизмы замещения лигандов Ln. MX +Y = Ln. MY +X • Возможны два предельных(идеальных) механизма: 1. Диссоциативный 2. Ассоциативный
 Диссоциативный механизм • Лимитирующей стадией реакции замещения является мономолекулярная стадия разрыва связи замещаемого лиганда с центральным ионом: 1. Ln. MX = [Ln. M] +X медленная стадия 2. [Ln. M] +Y = Ln. MY быстрая стадия SN 1 -механизм
Диссоциативный механизм • Лимитирующей стадией реакции замещения является мономолекулярная стадия разрыва связи замещаемого лиганда с центральным ионом: 1. Ln. MX = [Ln. M] +X медленная стадия 2. [Ln. M] +Y = Ln. MY быстрая стадия SN 1 -механизм
 Ассоциативный механизм • Лимитирующей стадией реакции замещения является бимолекулярная стадия образования переходного комплекса с координационным числом на единицу больше, чем в исходном: X Ln. MX +Y = [Ln. M ] медленная стадия SN 2 -механизм Y
Ассоциативный механизм • Лимитирующей стадией реакции замещения является бимолекулярная стадия образования переходного комплекса с координационным числом на единицу больше, чем в исходном: X Ln. MX +Y = [Ln. M ] медленная стадия SN 2 -механизм Y
 Реакции нуклеофильного замещения (SN). -мономолекуляpное (SN 1), -бимолекуляpного нуклеофильного замещения (SN 2).
Реакции нуклеофильного замещения (SN). -мономолекуляpное (SN 1), -бимолекуляpного нуклеофильного замещения (SN 2).
 Какова природа трансвлияния Черняева? • В терминологии органической химии - определяющими являются индуктивный (через ϭ – связь) и мезомерный (через π – связь) эффекты лигандов.
Какова природа трансвлияния Черняева? • В терминологии органической химии - определяющими являются индуктивный (через ϭ – связь) и мезомерный (через π – связь) эффекты лигандов.
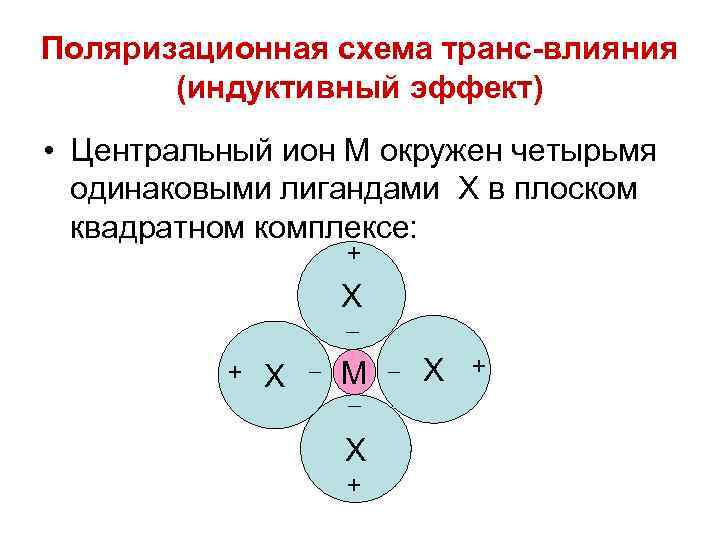 Поляризационная схема транс-влияния (индуктивный эффект) • Центральный ион М окружен четырьмя одинаковыми лигандами Х в плоском квадратном комплексе: Х Х М Х Х
Поляризационная схема транс-влияния (индуктивный эффект) • Центральный ион М окружен четырьмя одинаковыми лигандами Х в плоском квадратном комплексе: Х Х М Х Х
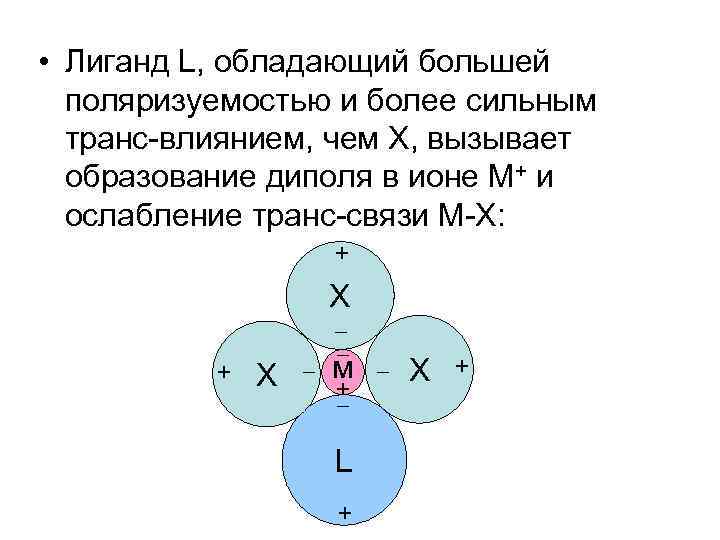 • Лиганд L, обладающий большей поляризуемостью и более сильным транс-влиянием, чем Х, вызывает образование диполя в ионе М+ и ослабление транс-связи М-Х: Х Х м L Х
• Лиганд L, обладающий большей поляризуемостью и более сильным транс-влиянием, чем Х, вызывает образование диполя в ионе М+ и ослабление транс-связи М-Х: Х Х м L Х
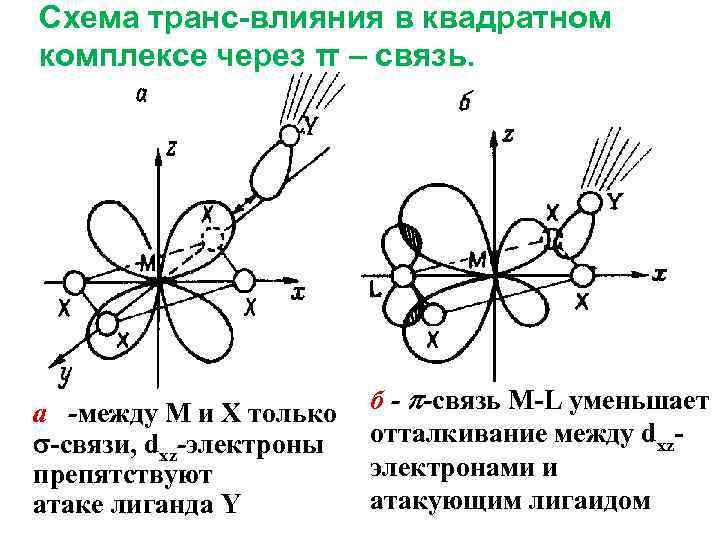 Схема транс-влияния в квадратном комплексе через π – связь. a -между М и Х только -связи, dxz-электроны препятствуют атаке лиганда Y б - -связь М-L уменьшает отталкивание между dxzэлектронами и атакующим лигаидом
Схема транс-влияния в квадратном комплексе через π – связь. a -между М и Х только -связи, dxz-электроны препятствуют атаке лиганда Y б - -связь М-L уменьшает отталкивание между dxzэлектронами и атакующим лигаидом
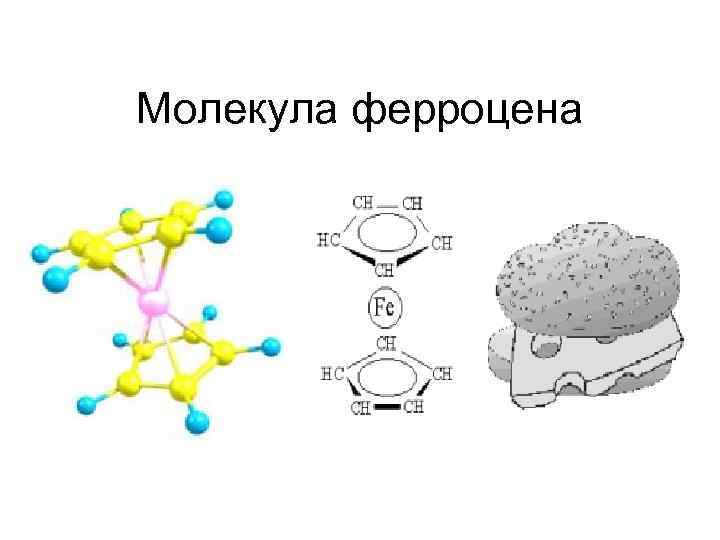 Молекула ферроцена
Молекула ферроцена
 Наиболее «знаменитые» комплексы • Рутеноцен (C 5 H 5)2 Ru 2+
Наиболее «знаменитые» комплексы • Рутеноцен (C 5 H 5)2 Ru 2+
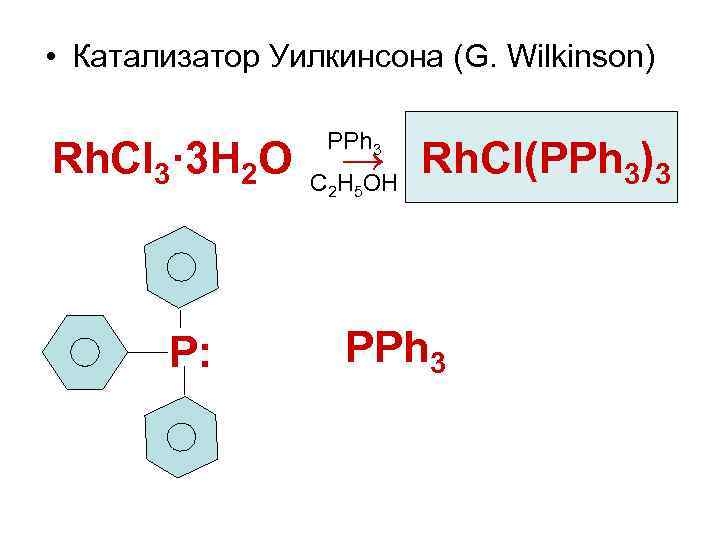 • Катализатор Уилкинсона (G. Wilkinson) PPh 3 Rh. Cl 3· 3 H 2 O → Rh. Cl(PPh 3)3 C H OH 2 P: 5 PPh 3
• Катализатор Уилкинсона (G. Wilkinson) PPh 3 Rh. Cl 3· 3 H 2 O → Rh. Cl(PPh 3)3 C H OH 2 P: 5 PPh 3
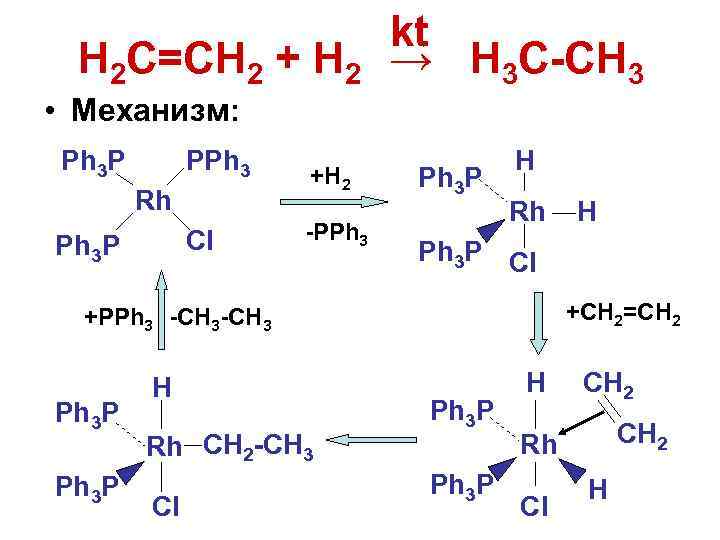 kt H 2 C=CH 2 + H 2 → H 3 C-CH 3 • Механизм: Ph 3 P PPh 3 Rh Cl Ph 3 P +H 2 -PPh 3 P H Rh Ph 3 P Cl +CH 2=CH 2 +PPh 3 -CH 3 Ph 3 P H Rh CH 2 -CH 3 Cl H Ph 3 P H CH 2 Rh Cl H
kt H 2 C=CH 2 + H 2 → H 3 C-CH 3 • Механизм: Ph 3 P PPh 3 Rh Cl Ph 3 P +H 2 -PPh 3 P H Rh Ph 3 P Cl +CH 2=CH 2 +PPh 3 -CH 3 Ph 3 P H Rh CH 2 -CH 3 Cl H Ph 3 P H CH 2 Rh Cl H
 Кластеры • Кластеры – группы из двух или более атомов металла, в которых эти атомы соединены непосредственно химической связью. • Могут быть образованы не только металлами.
Кластеры • Кластеры – группы из двух или более атомов металла, в которых эти атомы соединены непосредственно химической связью. • Могут быть образованы не только металлами.
![• Комплексы со связью металл-металл Cl Cl [Pt. Cl 4]2 - + CO • Комплексы со связью металл-металл Cl Cl [Pt. Cl 4]2 - + CO](https://present5.com/presentation/126659746_100833605/image-61.jpg) • Комплексы со связью металл-металл Cl Cl [Pt. Cl 4]2 - + CO → [ Cl – Pt – Cl ]2 CO CO
• Комплексы со связью металл-металл Cl Cl [Pt. Cl 4]2 - + CO → [ Cl – Pt – Cl ]2 CO CO
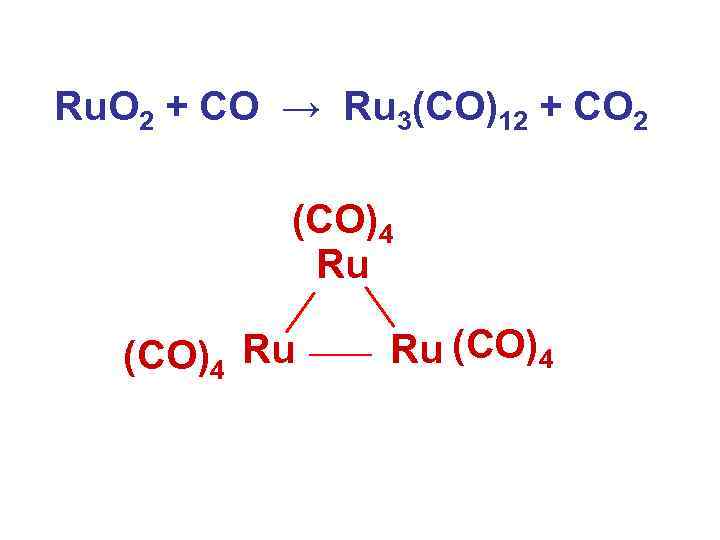 Ru. O 2 + CO → Ru 3(CO)12 + CO 2 (CO)4 Ru Ru (CO)4
Ru. O 2 + CO → Ru 3(CO)12 + CO 2 (CO)4 Ru Ru (CO)4
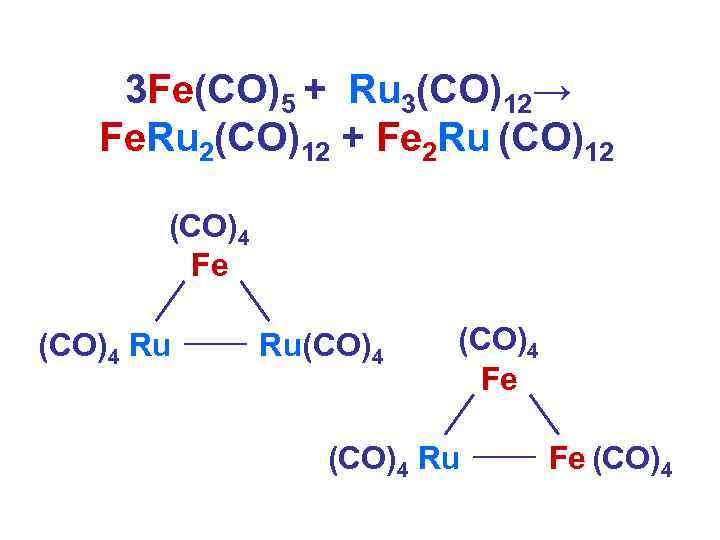 3 Fe(CO)5 + Ru 3(CO)12→ Fe. Ru 2(CO)12 + Fe 2 Ru (CO)12 (CO)4 Fe (CO)4 Ru Ru(CO)4 Fe (CO)4 Ru Fe (CO)4
3 Fe(CO)5 + Ru 3(CO)12→ Fe. Ru 2(CO)12 + Fe 2 Ru (CO)12 (CO)4 Fe (CO)4 Ru Ru(CO)4 Fe (CO)4 Ru Fe (CO)4
 Кластер акад. И. И. Моисеева Pd-561 1. Атомы Pd, активные в катализе 2. Атомы Pd 3. Фенантролин
Кластер акад. И. И. Моисеева Pd-561 1. Атомы Pd, активные в катализе 2. Атомы Pd 3. Фенантролин
 Илья Иосифович МОИСЕЕВ Академик РАН; действительный член Academia Europea и Academia Scientiarum et Artium Eurupea; Награжден орденом Трудового Красного Знамени; орденом Почета; Лауреат Государственной премии РФ; , премия «Триумф» , международной премии А. П. Карпинского. РЕАКЦИЯ СН 2=СН 2 + НОАс + ½ О 2 МОИСЕЕВА Pd-561 СН 2=СНОАс + Н 2 О
Илья Иосифович МОИСЕЕВ Академик РАН; действительный член Academia Europea и Academia Scientiarum et Artium Eurupea; Награжден орденом Трудового Красного Знамени; орденом Почета; Лауреат Государственной премии РФ; , премия «Триумф» , международной премии А. П. Карпинского. РЕАКЦИЯ СН 2=СН 2 + НОАс + ½ О 2 МОИСЕЕВА Pd-561 СН 2=СНОАс + Н 2 О
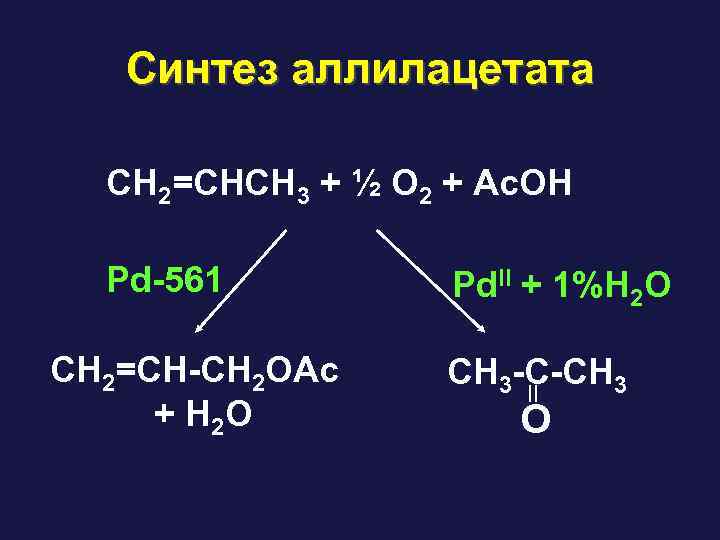 Синтез аллилацетата CH 2=CHCH 3 + ½ O 2 + Ac. OH Pd-561 CH 2=CH-CH 2 OAc + H 2 O Pd. II + 1%H 2 O CH 3 -C-CH 3 O
Синтез аллилацетата CH 2=CHCH 3 + ½ O 2 + Ac. OH Pd-561 CH 2=CH-CH 2 OAc + H 2 O Pd. II + 1%H 2 O CH 3 -C-CH 3 O
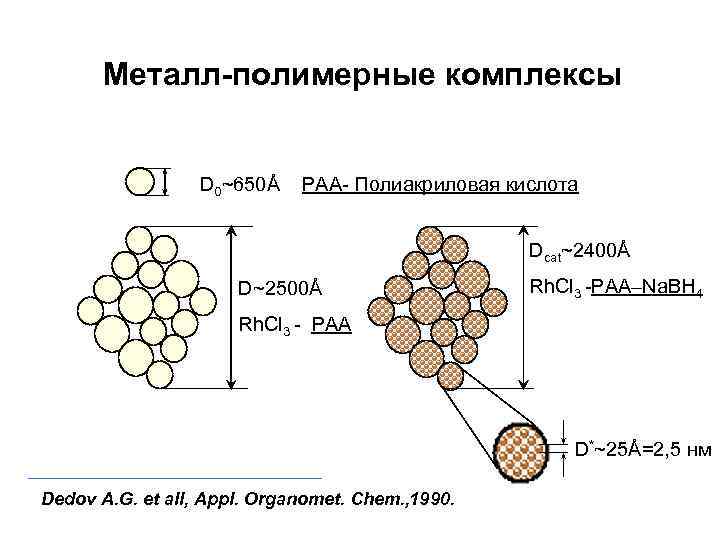 Металл-полимерные комплексы D 0~650Å PAA- Полиакриловая кислота Dcat~2400Å D~2500Å Rh. Cl 3 -PAA–Na. BH 4 Rh. Cl 3 - PAA D*~25Å=2, 5 нм Dedov A. G. et all, Appl. Organomet. Chem. , 1990.
Металл-полимерные комплексы D 0~650Å PAA- Полиакриловая кислота Dcat~2400Å D~2500Å Rh. Cl 3 -PAA–Na. BH 4 Rh. Cl 3 - PAA D*~25Å=2, 5 нм Dedov A. G. et all, Appl. Organomet. Chem. , 1990.
 1. Растворимые металл-полимерные катализаторы более активны и имеют минимальные диффузионные ограничения 2. Полимер в растворе должен обладать способностью взаимодействовать как лиганд с изменяемой дентантностью. Он мог бы легко превращаться из монодентатного в бидентатный и в полидентатную систему Он мог бы облегчать протекание реакции. 3. Глобула полимера может являться «шлюзом» для реагентов: Транспортировать реагенты между фазами и давать локальные концентрации реагента и субстрата
1. Растворимые металл-полимерные катализаторы более активны и имеют минимальные диффузионные ограничения 2. Полимер в растворе должен обладать способностью взаимодействовать как лиганд с изменяемой дентантностью. Он мог бы легко превращаться из монодентатного в бидентатный и в полидентатную систему Он мог бы облегчать протекание реакции. 3. Глобула полимера может являться «шлюзом» для реагентов: Транспортировать реагенты между фазами и давать локальные концентрации реагента и субстрата
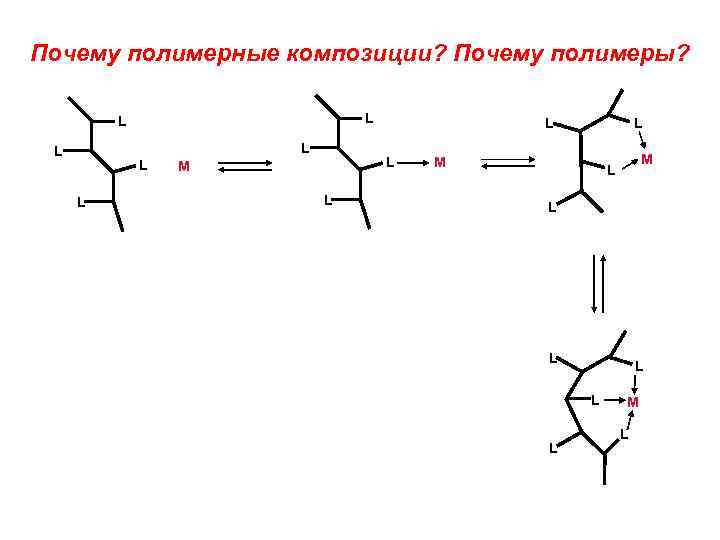 Почему полимерные композиции? Почему полимеры? L L L L M M L L L M L
Почему полимерные композиции? Почему полимеры? L L L L M M L L L M L
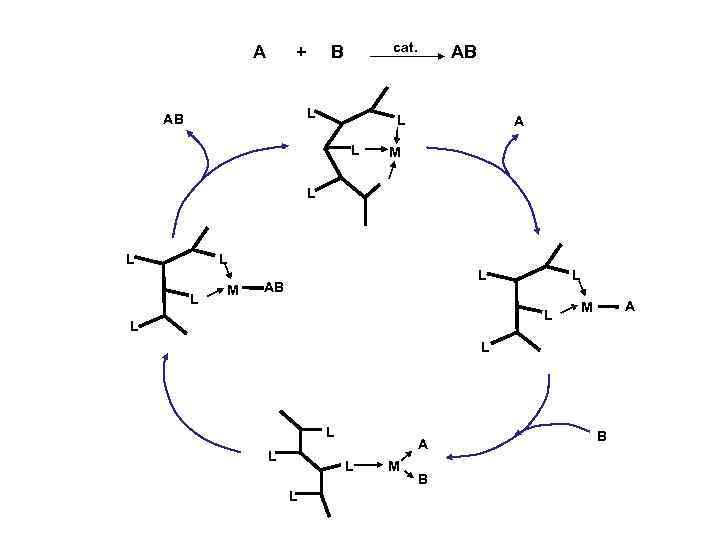 cat. A + B L AB AB L L A M L L M L AB L L L A M L L L A L L M B B
cat. A + B L AB AB L L A M L L M L AB L L L A M L L L A L L M B B
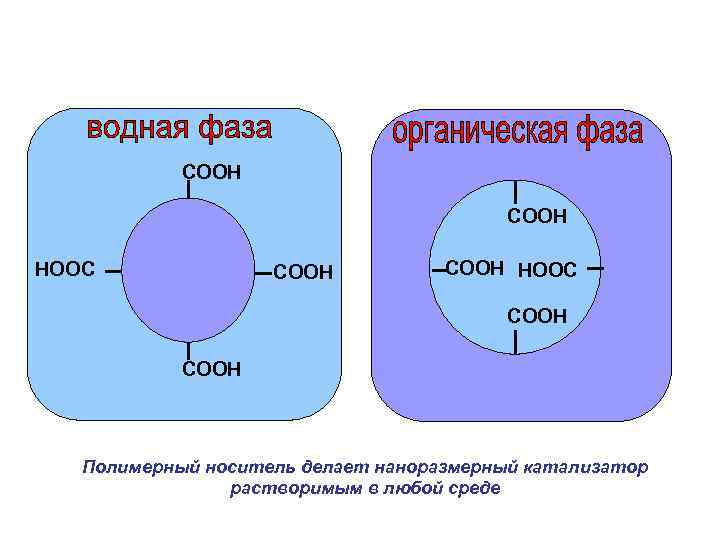 СООН HООС СООН НООC СООН Полимерный носитель делает наноразмерный катализатор растворимым в любой среде
СООН HООС СООН НООC СООН Полимерный носитель делает наноразмерный катализатор растворимым в любой среде
 100 A
100 A
 220 A
220 A


