Лекция 8 d-элементы.ppt
- Количество слайдов: 58
 Лекция Переходные элементы d-элементы
Лекция Переходные элементы d-элементы
 Перехо дные мета ллы (перехо дные элеме нты) — элементы побочных подгрупп Периодической системы химических элементов Д. И. Менделеева, в атомах которых появляются электроны на d- и f-орбиталях. В общем виде электронное строение переходных элементов можно представить следующим образом: . На ns-орбитали содержится один или два электрона, остальные валентные электроны находятся на -орбитали. Поскольку число валентных электронов заметно меньше числа орбиталей, то простые вещества, образованные переходными элементами, являются металлами.
Перехо дные мета ллы (перехо дные элеме нты) — элементы побочных подгрупп Периодической системы химических элементов Д. И. Менделеева, в атомах которых появляются электроны на d- и f-орбиталях. В общем виде электронное строение переходных элементов можно представить следующим образом: . На ns-орбитали содержится один или два электрона, остальные валентные электроны находятся на -орбитали. Поскольку число валентных электронов заметно меньше числа орбиталей, то простые вещества, образованные переходными элементами, являются металлами.
 Общий обзор переходных элементов • d-элемент – элемент с частично заполненным d-подуровнем в атомах или ионах, • f-элемент – элемент с частично заполненным f-подуровнем в атомах или ионах,
Общий обзор переходных элементов • d-элемент – элемент с частично заполненным d-подуровнем в атомах или ионах, • f-элемент – элемент с частично заполненным f-подуровнем в атомах или ионах,
 Все d- и f-элементы – металлы. • d-металлы – переходные металлы, • 4 f-металлы – редкоземельные металлы или редкие земли.
Все d- и f-элементы – металлы. • d-металлы – переходные металлы, • 4 f-металлы – редкоземельные металлы или редкие земли.
 d-элементы К ним относятся элементы между IIA и IIIA группами периодической системы, которые характеризуются постепенным заполнением внутренних d-орбиталей.
d-элементы К ним относятся элементы между IIA и IIIA группами периодической системы, которые характеризуются постепенным заполнением внутренних d-орбиталей.
 Исключения: Zn, Cd, Hg и их катионы - d 10, близки по свойствам с dэлементами, однако их нельзя рассматривать как истинные dэлементы.
Исключения: Zn, Cd, Hg и их катионы - d 10, близки по свойствам с dэлементами, однако их нельзя рассматривать как истинные dэлементы.
 d-элементы с подоболочкой d 10, в их катионах d-подуровень незавершен: Cu Pd Ag Au 3 d 104 s 1 4 d 105 s 1 4 f 145 d 106 s 1 Cu 2+ Pd 2+ Ag 3+ Au 3+ 3 d 9 4 d 8 5 d 8 Cu. O Pd. O K[Ag. F 4] Au. F 3
d-элементы с подоболочкой d 10, в их катионах d-подуровень незавершен: Cu Pd Ag Au 3 d 104 s 1 4 d 105 s 1 4 f 145 d 106 s 1 Cu 2+ Pd 2+ Ag 3+ Au 3+ 3 d 9 4 d 8 5 d 8 Cu. O Pd. O K[Ag. F 4] Au. F 3
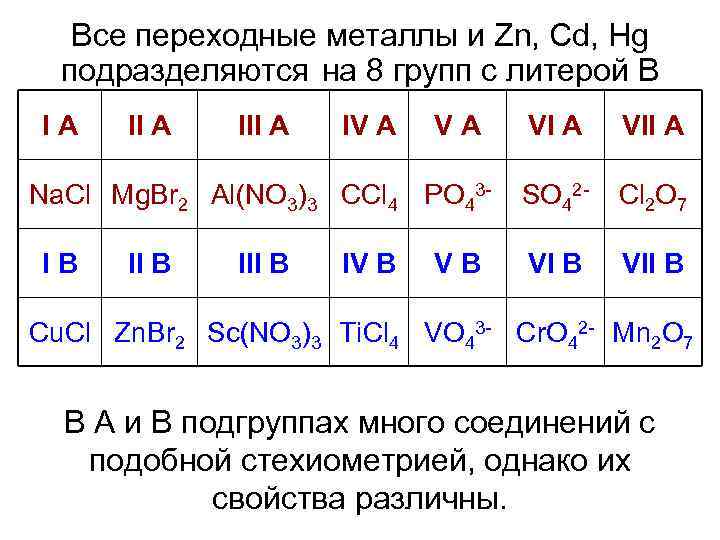 Все переходные металлы и Zn, Cd, Hg подразделяются на 8 групп с литерой В I A III A IV A Na. Cl Mg. Br 2 Al(NO 3)3 CCl 4 PO 43 I B III B IV B VI A VII A SO 42 - Cl 2 O 7 VI B VII B Cu. Cl Zn. Br 2 Sc(NO 3)3 Ti. Cl 4 VO 43 - Cr. O 42 - Mn 2 O 7 В А и В подгруппах много соединений с подобной стехиометрией, однако их свойства различны.
Все переходные металлы и Zn, Cd, Hg подразделяются на 8 групп с литерой В I A III A IV A Na. Cl Mg. Br 2 Al(NO 3)3 CCl 4 PO 43 I B III B IV B VI A VII A SO 42 - Cl 2 O 7 VI B VII B Cu. Cl Zn. Br 2 Sc(NO 3)3 Ti. Cl 4 VO 43 - Cr. O 42 - Mn 2 O 7 В А и В подгруппах много соединений с подобной стехиометрией, однако их свойства различны.
 Группа VIII B Fe Ru Os Co Rh Ir Ni Pd Pt Триада Fe Триада Pd Триада Pt
Группа VIII B Fe Ru Os Co Rh Ir Ni Pd Pt Триада Fe Триада Pd Триада Pt
 Тенденции в изменении свойств (подобие между элементами А и В подгрупп) • Изменения в ст. ок. по периоду. • Увеличивается ионный радиус (вниз по подгруппе). • Увеличивается Тпл, Ткип (вниз по подгруппе). • Изменения в ст. ок. одного элемента: Ti. Cl 2 - Ti. Cl 3 - Ti. Cl 4 Ионное тв. в-во - молекулярная жид. • Оксиды и гидроксиды в низких степенях окисления имеют осн. характер (Cr 2+), а в высоких – кислотный(Cr 2 O 7 -).
Тенденции в изменении свойств (подобие между элементами А и В подгрупп) • Изменения в ст. ок. по периоду. • Увеличивается ионный радиус (вниз по подгруппе). • Увеличивается Тпл, Ткип (вниз по подгруппе). • Изменения в ст. ок. одного элемента: Ti. Cl 2 - Ti. Cl 3 - Ti. Cl 4 Ионное тв. в-во - молекулярная жид. • Оксиды и гидроксиды в низких степенях окисления имеют осн. характер (Cr 2+), а в высоких – кислотный(Cr 2 O 7 -).
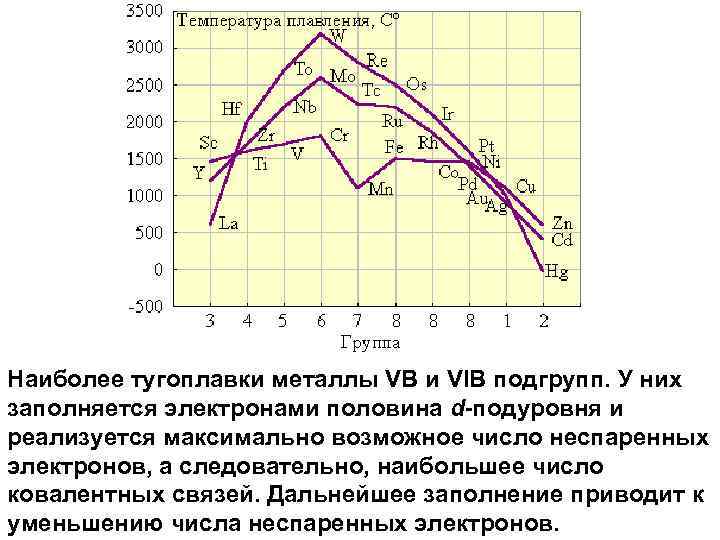 Наиболее тугоплавки металлы VВ и VIВ подгрупп. У них заполняется электронами половина d-подуровня и реализуется максимально возможное число неспаренных электронов, а следовательно, наибольшее число ковалентных связей. Дальнейшее заполнение приводит к уменьшению числа неспаренных электронов.
Наиболее тугоплавки металлы VВ и VIВ подгрупп. У них заполняется электронами половина d-подуровня и реализуется максимально возможное число неспаренных электронов, а следовательно, наибольшее число ковалентных связей. Дальнейшее заполнение приводит к уменьшению числа неспаренных электронов.
 Свойства переходных металлов • Ковкие, тягучие, высокий предел прочности на разрыв, имеют более высокие Тпл, Тк по сравнению с непереходными металлами
Свойства переходных металлов • Ковкие, тягучие, высокий предел прочности на разрыв, имеют более высокие Тпл, Тк по сравнению с непереходными металлами
 • Ионы и соединения обычно окрашены • Образуют различные комплексные ионы
• Ионы и соединения обычно окрашены • Образуют различные комплексные ионы
 • За небольшим исключением, проявляют многочисленные степени окисления • Многие парамагнитны • Проявляют каталитические свойства • Хорошие проводники электрического тока
• За небольшим исключением, проявляют многочисленные степени окисления • Многие парамагнитны • Проявляют каталитические свойства • Хорошие проводники электрического тока
 Каталитические свойства d-элементов • Процесс Габера для получения NH 3 Fe, Fe O N 2 + 3 H 2 2 NH 3 T, P • Получение SO 3 VO 2 SO 2 + O 2 = 2 SO 3 400° • Каталитическое гидрирование Pt R-CH=CH 2 + H 2 R-CH 2 -CH 3 • Энзиматическое окисление Fe. E RH + H 2 O 2 ROH + H 2 O 2 3 2 5
Каталитические свойства d-элементов • Процесс Габера для получения NH 3 Fe, Fe O N 2 + 3 H 2 2 NH 3 T, P • Получение SO 3 VO 2 SO 2 + O 2 = 2 SO 3 400° • Каталитическое гидрирование Pt R-CH=CH 2 + H 2 R-CH 2 -CH 3 • Энзиматическое окисление Fe. E RH + H 2 O 2 ROH + H 2 O 2 3 2 5
 З серии d-металлов, имеющих незавершенную d-орбиталь 3 d 21 Sc – 30 Zn 4 d 39 Y – 48 Cd 57 La – 80 Hg Свойства этих металлов могут быть скорректированы с общим количеством d-электронов, либо с числом неспаренных электронов.
З серии d-металлов, имеющих незавершенную d-орбиталь 3 d 21 Sc – 30 Zn 4 d 39 Y – 48 Cd 57 La – 80 Hg Свойства этих металлов могут быть скорректированы с общим количеством d-электронов, либо с числом неспаренных электронов.
 Электроотрицательность (Е), энергия ионизации (I), окислительно-восстановительный потенциал (Р°) E I, к. Дж/м P°, B Sc 1. 2 637 -2. 08 Zn 1. 6 912 -0. 176 +0. 34(Cu)
Электроотрицательность (Е), энергия ионизации (I), окислительно-восстановительный потенциал (Р°) E I, к. Дж/м P°, B Sc 1. 2 637 -2. 08 Zn 1. 6 912 -0. 176 +0. 34(Cu)
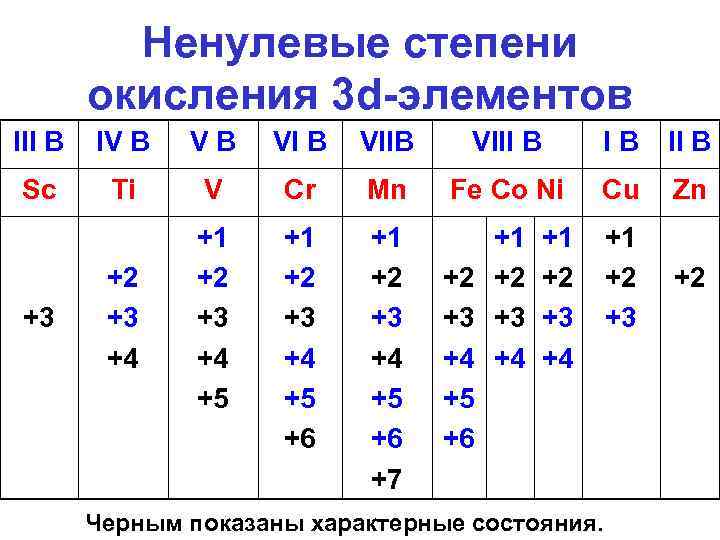 Ненулевые степени окисления 3 d-элементов III B IV B VIII B Sc Ti V Cr Mn Fe Co Ni Cu Zn +2 +3 +4 +1 +2 +3 +4 +5 +6 +7 +1 +2 +2 +3 +3 +4 +4 +5 +6 +1 +2 +3 +4 Черным показаны характерные состояния.
Ненулевые степени окисления 3 d-элементов III B IV B VIII B Sc Ti V Cr Mn Fe Co Ni Cu Zn +2 +3 +4 +1 +2 +3 +4 +5 +6 +7 +1 +2 +2 +3 +3 +4 +4 +5 +6 +1 +2 +3 +4 Черным показаны характерные состояния.
 Марганец • Составляет 0, 03% от общего числа атомов земной коры. • Главным образом встречается в виде серо-черного минерала – пиролюзита Mn. O 2·х. H 2 O
Марганец • Составляет 0, 03% от общего числа атомов земной коры. • Главным образом встречается в виде серо-черного минерала – пиролюзита Mn. O 2·х. H 2 O
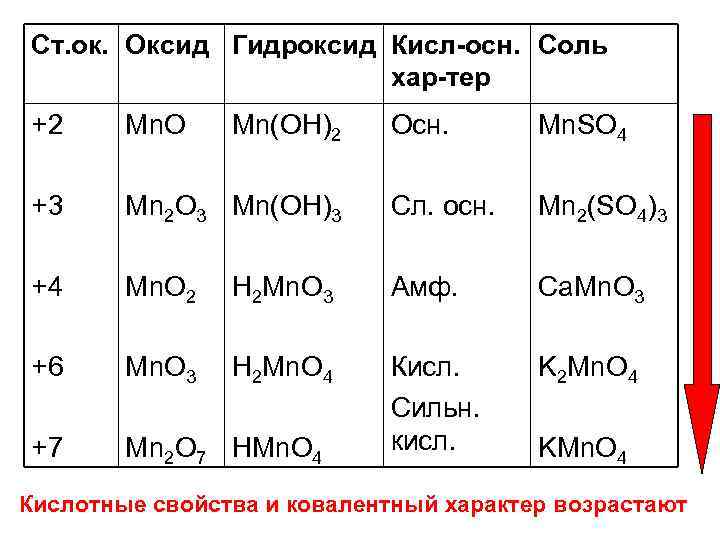 Ст. ок. Оксид Гидроксид Кисл-осн. Соль хар-тер +2 Mn. O +3 Mn(OH)2 Осн. Mn. SO 4 Mn 2 O 3 Mn(OH)3 Сл. осн. Mn 2(SO 4)3 +4 Mn. O 2 H 2 Mn. O 3 Амф. Ca. Mn. O 3 +6 Mn. O 3 H 2 Mn. O 4 K 2 Mn. O 4 +7 Mn 2 O 7 HMn. O 4 Кисл. Сильн. кисл. KMn. O 4 Кислотные свойства и ковалентный характер возрастают
Ст. ок. Оксид Гидроксид Кисл-осн. Соль хар-тер +2 Mn. O +3 Mn(OH)2 Осн. Mn. SO 4 Mn 2 O 3 Mn(OH)3 Сл. осн. Mn 2(SO 4)3 +4 Mn. O 2 H 2 Mn. O 3 Амф. Ca. Mn. O 3 +6 Mn. O 3 H 2 Mn. O 4 K 2 Mn. O 4 +7 Mn 2 O 7 HMn. O 4 Кисл. Сильн. кисл. KMn. O 4 Кислотные свойства и ковалентный характер возрастают
 Получение Марганца • 90% всего добываемого марганца используется для изготовления легированных сталей. Поэтому из руд выплавляют не чистый марганец, а сплав Mn(70%) с железом и углеродом – ферромарганец. Mn. O 2 + 2 C = 2 CO +Mn • Чистый марганец получают электролизом растворов его солей.
Получение Марганца • 90% всего добываемого марганца используется для изготовления легированных сталей. Поэтому из руд выплавляют не чистый марганец, а сплав Mn(70%) с железом и углеродом – ферромарганец. Mn. O 2 + 2 C = 2 CO +Mn • Чистый марганец получают электролизом растворов его солей.
 Свойства марганца • Металл средней активности. На воздухе покрывается тонкой плёнкой оксидов. При прокаливании на воздухе выше 800°C марганец покрывается окалиной, состоящей из внешнего слоя Mn 3 O 4 и внутреннего слоя состава Mn. O.
Свойства марганца • Металл средней активности. На воздухе покрывается тонкой плёнкой оксидов. При прокаливании на воздухе выше 800°C марганец покрывается окалиной, состоящей из внешнего слоя Mn 3 O 4 и внутреннего слоя состава Mn. O.
 • Реагирует с неметаллами, например, с серой: Mn + S = Mn. S • Растворяется в кислотах с образованием Mn+2: Mn + 2 HCl = Mn. Cl 2 + H 2 3 Mn +7 HNO 3 = 3 HMn. O 4 +7 NO +H 2 O
• Реагирует с неметаллами, например, с серой: Mn + S = Mn. S • Растворяется в кислотах с образованием Mn+2: Mn + 2 HCl = Mn. Cl 2 + H 2 3 Mn +7 HNO 3 = 3 HMn. O 4 +7 NO +H 2 O
 Свойства марганца Mn+2 Оксид марганца (II) Mn. O получается восстановлением природного пиролюзита Mn. O 2 водородом: Mn. O 2 + H 2 = Mn. O + H 2 O Mn. O также образуется при разложении солей двухвалентного марганца (карбоната и других) при температуре около 300°C в инертной атмосфере: Mn. CO 3 = Mn. O + CO 2 Этот оксид обладает полупроводниковыми свойствами.
Свойства марганца Mn+2 Оксид марганца (II) Mn. O получается восстановлением природного пиролюзита Mn. O 2 водородом: Mn. O 2 + H 2 = Mn. O + H 2 O Mn. O также образуется при разложении солей двухвалентного марганца (карбоната и других) при температуре около 300°C в инертной атмосфере: Mn. CO 3 = Mn. O + CO 2 Этот оксид обладает полупроводниковыми свойствами.
 Гидроксид марганца (II) Mn(OH)2 - светло -розовое нерастворимое в воде основание: Mn. SO 4 + 2 Na. OH = Mn(OH)2 + Na 2 SO 4 • Легко растворимо в кислотах: Mn(OH)2 + 2 HCl = Mn. Cl 2 + 2 H 2 O • На воздухе Mn(OH)2 быстро темнеет в результате окисления: 2 Mn(OH)2 + O 2 + 2 H 2 O = 2[Mn. O 2 • 2 H 2 O]
Гидроксид марганца (II) Mn(OH)2 - светло -розовое нерастворимое в воде основание: Mn. SO 4 + 2 Na. OH = Mn(OH)2 + Na 2 SO 4 • Легко растворимо в кислотах: Mn(OH)2 + 2 HCl = Mn. Cl 2 + 2 H 2 O • На воздухе Mn(OH)2 быстро темнеет в результате окисления: 2 Mn(OH)2 + O 2 + 2 H 2 O = 2[Mn. O 2 • 2 H 2 O]
 • При действии сильных окислителей наблюдается переход Mn 2+ в Mn. O 4 - : кат. Cu. SO 4 2 Mn(OH)2 + 5 Br 2 + 12 Na. OH = 2 Na. Mn. O 4 + 10 Na. Br + 8 H 2 O 2 Mn(NO 3)2 + 5 Pb. O 2 + 6 HNO 3 = 2 HMn. O 4 + 5 Pb(NO 3)2 + 2 H 2 O 2 Mn(NO 3)2 + 5 Na. Bi. O 3 + 16 HNO 3 = 2 HMn. O 4 + 5 Na. NO 2 + 5 Bi(NO 3)3 + 7 H 2 O
• При действии сильных окислителей наблюдается переход Mn 2+ в Mn. O 4 - : кат. Cu. SO 4 2 Mn(OH)2 + 5 Br 2 + 12 Na. OH = 2 Na. Mn. O 4 + 10 Na. Br + 8 H 2 O 2 Mn(NO 3)2 + 5 Pb. O 2 + 6 HNO 3 = 2 HMn. O 4 + 5 Pb(NO 3)2 + 2 H 2 O 2 Mn(NO 3)2 + 5 Na. Bi. O 3 + 16 HNO 3 = 2 HMn. O 4 + 5 Na. NO 2 + 5 Bi(NO 3)3 + 7 H 2 O
 Свойства марганца Mn+4 • Оксид марганца (IV) Mn. O 2 - тёмнокоричневый порошок, нерастворимый в воде. Образуется при термическом разложении нитрата марганца (II): t° Mn(NO 3)2 ® Mn. O 2 + 2 NO 2 • При сильном нагревании теряет кислород, превращаясь в Mn 2 O 3 (при 600°C) или Mn 3 O 4 (при 1000°C).
Свойства марганца Mn+4 • Оксид марганца (IV) Mn. O 2 - тёмнокоричневый порошок, нерастворимый в воде. Образуется при термическом разложении нитрата марганца (II): t° Mn(NO 3)2 ® Mn. O 2 + 2 NO 2 • При сильном нагревании теряет кислород, превращаясь в Mn 2 O 3 (при 600°C) или Mn 3 O 4 (при 1000°C).
 • Взаимодействует с кислотами с образованием Mn+2 : Mn. O 2 + 4 HCl ® Mn. Cl 2 + 2 H 2 O Mn. O 2 + 2 H 2 SO 4 ® Mn. SO 4 + O 2 2 O +2 H • При сплавлении с содой и селитрой образует манганат натрия тёмно - зелёного цвета: t° Mn. O 2 + Na 2 CO 3 + Na. NO 3 ® Na 2 Mn. O 4 + Na. NO 2 + CO 2
• Взаимодействует с кислотами с образованием Mn+2 : Mn. O 2 + 4 HCl ® Mn. Cl 2 + 2 H 2 O Mn. O 2 + 2 H 2 SO 4 ® Mn. SO 4 + O 2 2 O +2 H • При сплавлении с содой и селитрой образует манганат натрия тёмно - зелёного цвета: t° Mn. O 2 + Na 2 CO 3 + Na. NO 3 ® Na 2 Mn. O 4 + Na. NO 2 + CO 2
 H 2 Mn. O 4 – марганцовистая кислота (манганаты) HMn. O 4– марганцовая кислота (перманганаты)
H 2 Mn. O 4 – марганцовистая кислота (манганаты) HMn. O 4– марганцовая кислота (перманганаты)
 Свойства марганца Mn+6 , Mn+7 Оксид марганца (VII) Mn 2 O 7 - тёмно-зелёная жидкость, кислотный оксид. Получают действием концентрированной серной кислоты на кристаллический KMn. O 4 (марганцевая кислота HMn. O 4 нестабильна): 2 KMn. O 4 + H 2 SO 4 = Mn 2 O 7 + K 2 SO 4 + H 2 O При растворении в щелочах образует перманганаты: Mn 2 O 7 + 2 KOH = 2 KMn. O 4 + H 2 O
Свойства марганца Mn+6 , Mn+7 Оксид марганца (VII) Mn 2 O 7 - тёмно-зелёная жидкость, кислотный оксид. Получают действием концентрированной серной кислоты на кристаллический KMn. O 4 (марганцевая кислота HMn. O 4 нестабильна): 2 KMn. O 4 + H 2 SO 4 = Mn 2 O 7 + K 2 SO 4 + H 2 O При растворении в щелочах образует перманганаты: Mn 2 O 7 + 2 KOH = 2 KMn. O 4 + H 2 O
 • Сплавлением Mn. O 2 со щелочами в присутствие окислителей получают соли марганцовистой кислоты 2 Mn. O 2 + 4 KOH + O 2= 2 K 2 Mn. O 4 + 2 H 2 O • Свободная марганцовистая кислота неустойчива + H 3 H 2 Mn. O 4 = Mn. O 2+2 Н 2 О + 2 HMn. O 4 • Подобный самопроизвольный распад солей протекает значительно медленнее 2 K 2 Mn. O 4 + 2 Н 2 О = 2 KMn. O 4 + Mn. O 2 + 4 КОН
• Сплавлением Mn. O 2 со щелочами в присутствие окислителей получают соли марганцовистой кислоты 2 Mn. O 2 + 4 KOH + O 2= 2 K 2 Mn. O 4 + 2 H 2 O • Свободная марганцовистая кислота неустойчива + H 3 H 2 Mn. O 4 = Mn. O 2+2 Н 2 О + 2 HMn. O 4 • Подобный самопроизвольный распад солей протекает значительно медленнее 2 K 2 Mn. O 4 + 2 Н 2 О = 2 KMn. O 4 + Mn. O 2 + 4 КОН
 • Перманганат калия KMn+7 O 4 -тёмнофиолетовое кристаллическое вещество, растворимое в воде. При нагревании разлагается с выделением кислорода: 2 KMn. O 4 ® K 2 Mn. O 4 + Mn. O 2 + O 2 t°
• Перманганат калия KMn+7 O 4 -тёмнофиолетовое кристаллическое вещество, растворимое в воде. При нагревании разлагается с выделением кислорода: 2 KMn. O 4 ® K 2 Mn. O 4 + Mn. O 2 + O 2 t°
![OH- • K 2 Mn. O 4+ [восст] Mn. O 2 H+ Mn+2 OH- OH- • K 2 Mn. O 4+ [восст] Mn. O 2 H+ Mn+2 OH-](https://present5.com/presentation/126659746_100832902/image-33.jpg) OH- • K 2 Mn. O 4+ [восст] Mn. O 2 H+ Mn+2 OH- K 2 Mn. O 4 H 2 O • KMn. O 4+ [восст] Mn. O 2 H+ Mn+2
OH- • K 2 Mn. O 4+ [восст] Mn. O 2 H+ Mn+2 OH- K 2 Mn. O 4 H 2 O • KMn. O 4+ [восст] Mn. O 2 H+ Mn+2
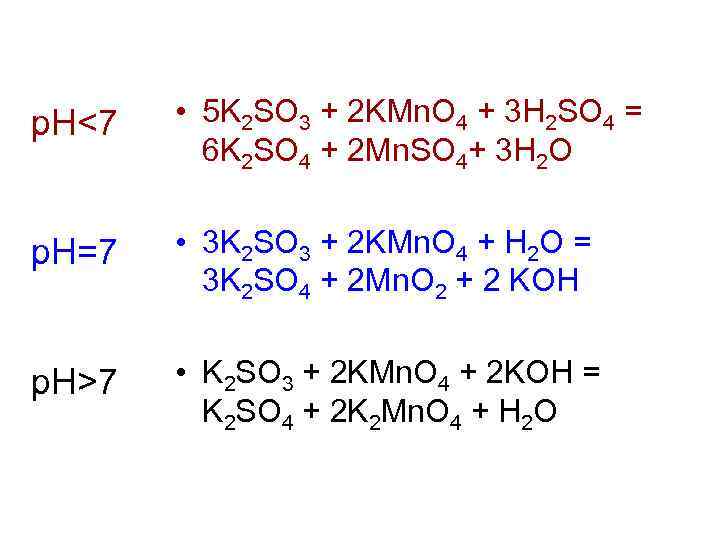 p. H<7 • 5 K 2 SO 3 + 2 KMn. O 4 + 3 H 2 SO 4 = 6 K 2 SO 4 + 2 Mn. SO 4+ 3 H 2 O p. H=7 • 3 K 2 SO 3 + 2 KMn. O 4 + H 2 O = 3 K 2 SO 4 + 2 Mn. O 2 + 2 KOH p. H>7 • K 2 SO 3 + 2 KMn. O 4 + 2 KOH = K 2 SO 4 + 2 K 2 Mn. O 4 + H 2 O
p. H<7 • 5 K 2 SO 3 + 2 KMn. O 4 + 3 H 2 SO 4 = 6 K 2 SO 4 + 2 Mn. SO 4+ 3 H 2 O p. H=7 • 3 K 2 SO 3 + 2 KMn. O 4 + H 2 O = 3 K 2 SO 4 + 2 Mn. O 2 + 2 KOH p. H>7 • K 2 SO 3 + 2 KMn. O 4 + 2 KOH = K 2 SO 4 + 2 K 2 Mn. O 4 + H 2 O
 Применение марганца • Марганец используют как добавку к сталям для их раскисления, десульфурации (при этом происходит удаление из стали нежелательных примесей — кислорода, серы и других), а также для легирования сталей. • Марганец применяется также в медных, алюминиевых и магниевых сплавах. • Покрытия из марганца на металлических поверхностях обеспечивают их антикоррозионную защиту. • Соединения марганца служат катализаторами многих хим. реакций, • Входят в состав микроудобрений.
Применение марганца • Марганец используют как добавку к сталям для их раскисления, десульфурации (при этом происходит удаление из стали нежелательных примесей — кислорода, серы и других), а также для легирования сталей. • Марганец применяется также в медных, алюминиевых и магниевых сплавах. • Покрытия из марганца на металлических поверхностях обеспечивают их антикоррозионную защиту. • Соединения марганца служат катализаторами многих хим. реакций, • Входят в состав микроудобрений.
 Хром Основная руда – хромистый железняк Fe. O·Cr 2 O 3.
Хром Основная руда – хромистый железняк Fe. O·Cr 2 O 3.
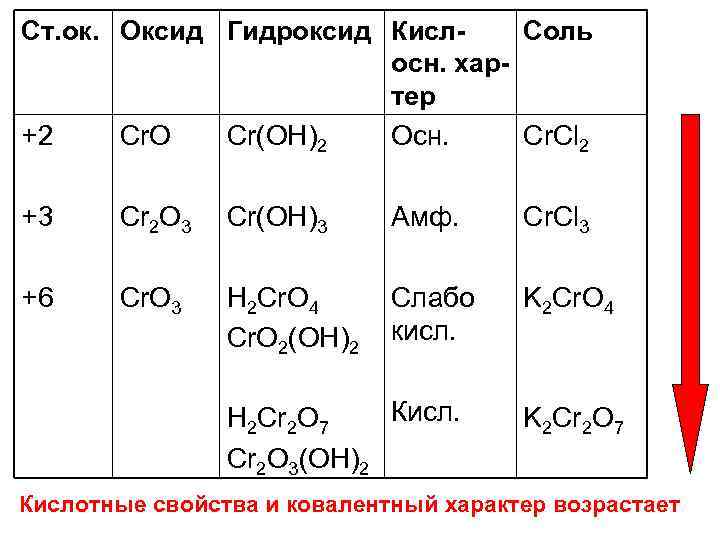 Ст. ок. Оксид Гидроксид Кисл. Соль осн. хартер +2 Cr. O Cr(OH)2 Осн. Cr. Cl 2 +3 Cr 2 O 3 Cr(OH)3 Амф. Cr. Cl 3 +6 Cr. O 3 H 2 Cr. O 4 Cr. O 2(OH)2 Слабо кисл. K 2 Cr. O 4 Кисл. H 2 Cr 2 O 7 Cr 2 O 3(OH)2 K 2 Cr 2 O 7 Кислотные свойства и ковалентный характер возрастает
Ст. ок. Оксид Гидроксид Кисл. Соль осн. хартер +2 Cr. O Cr(OH)2 Осн. Cr. Cl 2 +3 Cr 2 O 3 Cr(OH)3 Амф. Cr. Cl 3 +6 Cr. O 3 H 2 Cr. O 4 Cr. O 2(OH)2 Слабо кисл. K 2 Cr. O 4 Кисл. H 2 Cr 2 O 7 Cr 2 O 3(OH)2 K 2 Cr 2 O 7 Кислотные свойства и ковалентный характер возрастает
 Получение хрома • Cr 2 O 3 подвергают алюминотермии: Cr 2 O 3 + 2 Al = Al 2 O 3 + 2 Cr. • Также используют кремний: 2 Cr 2 O 3 + 3 Si = 3 Si. O 2 + 4 Cr
Получение хрома • Cr 2 O 3 подвергают алюминотермии: Cr 2 O 3 + 2 Al = Al 2 O 3 + 2 Cr. • Также используют кремний: 2 Cr 2 O 3 + 3 Si = 3 Si. O 2 + 4 Cr
 Свойства хрома • При обычных условиях хром реагирует только со фтором. При высоких температурах (выше 600°C) взаимодействует с кислородом, галогенами, азотом, кремнием, бором, серой, фосфором. 4 Cr + 3 O 2 ® 2 Cr 2 O 3 2 Cr + 3 Cl 2 ® 2 Cr. Cl 3 2 Cr + N 2 ® 2 Cr. N 2 Cr + 3 S ® Cr 2 S 3
Свойства хрома • При обычных условиях хром реагирует только со фтором. При высоких температурах (выше 600°C) взаимодействует с кислородом, галогенами, азотом, кремнием, бором, серой, фосфором. 4 Cr + 3 O 2 ® 2 Cr 2 O 3 2 Cr + 3 Cl 2 ® 2 Cr. Cl 3 2 Cr + N 2 ® 2 Cr. N 2 Cr + 3 S ® Cr 2 S 3
 • В раскалённом состоянии реагирует с парами воды: 2 Cr + 3 H 2 O « Cr 2 O 3 + 3 H 2 • Хром растворяется в разбавленных сильных кислотах (HCl, H 2 SO 4). В отсутствии воздуха образуются соли Cr 2+, а на воздухе – соли Cr 3+. Cr + 2 HCl ® Cr. Cl 2 + H 2 2 Cr + 6 HCl + O 2 ® 2 Cr. Cl 3 + 2 H 2 O + H 2
• В раскалённом состоянии реагирует с парами воды: 2 Cr + 3 H 2 O « Cr 2 O 3 + 3 H 2 • Хром растворяется в разбавленных сильных кислотах (HCl, H 2 SO 4). В отсутствии воздуха образуются соли Cr 2+, а на воздухе – соли Cr 3+. Cr + 2 HCl ® Cr. Cl 2 + H 2 2 Cr + 6 HCl + O 2 ® 2 Cr. Cl 3 + 2 H 2 O + H 2
 • Наличие защитной окисной плёнки на поверхности металла объясняет его пассивность по отношению к концентрированным растворам кислот – окислителей.
• Наличие защитной окисной плёнки на поверхности металла объясняет его пассивность по отношению к концентрированным растворам кислот – окислителей.
 Свойства хрома+2 • Оксид хрома (II) и гидроксид хрома (II) имеют основной характер. Cr(OH)2 + 2 HCl ® Cr. Cl 2 + 2 H 2 O • Соединения хрома (II) - сильные восстановители; переходят в соединения хрома (III) под действием кислорода воздуха. 2 Cr. Cl 2 + 2 HCl ® 2 Cr. Cl 3 + H 2 4 Cr(OH)2 + O 2 + 2 H 2 O ® 4 Cr(OH)3
Свойства хрома+2 • Оксид хрома (II) и гидроксид хрома (II) имеют основной характер. Cr(OH)2 + 2 HCl ® Cr. Cl 2 + 2 H 2 O • Соединения хрома (II) - сильные восстановители; переходят в соединения хрома (III) под действием кислорода воздуха. 2 Cr. Cl 2 + 2 HCl ® 2 Cr. Cl 3 + H 2 4 Cr(OH)2 + O 2 + 2 H 2 O ® 4 Cr(OH)3
 600° • Сr. Cl 3 + H 2 Cr. Cl 2 + HCl Хлористый хром (Cr. Cl 2) – бесцветное кристаллическое вещество, водный раствор имеет голубую окраску, используется для поглощения кислорода воздуха: 4 Cr. Cl 2 + O 2 + 4 HCl = 4 Cr. Cl 3 + 2 H 2 O
600° • Сr. Cl 3 + H 2 Cr. Cl 2 + HCl Хлористый хром (Cr. Cl 2) – бесцветное кристаллическое вещество, водный раствор имеет голубую окраску, используется для поглощения кислорода воздуха: 4 Cr. Cl 2 + O 2 + 4 HCl = 4 Cr. Cl 3 + 2 H 2 O
 Свойства хрома +3 • Оксид хрома (III) Cr 2 O 3 – зелёный, нерастворимый в воде порошок. Может быть получен при прокаливании гидроксида хрома (III) или дихроматов калия и аммония: 2 Cr(OH)3 ® Cr 2 O 3 + 3 H 2 O 4 K 2 Cr 2 O 7 ® 2 Cr 2 O 3 + 4 K 2 Cr. O 4 + 3 O 2 (NH 4)2 Cr 2 O 7 ® Cr 2 O 3 + N 2 4 H 2 O +
Свойства хрома +3 • Оксид хрома (III) Cr 2 O 3 – зелёный, нерастворимый в воде порошок. Может быть получен при прокаливании гидроксида хрома (III) или дихроматов калия и аммония: 2 Cr(OH)3 ® Cr 2 O 3 + 3 H 2 O 4 K 2 Cr 2 O 7 ® 2 Cr 2 O 3 + 4 K 2 Cr. O 4 + 3 O 2 (NH 4)2 Cr 2 O 7 ® Cr 2 O 3 + N 2 4 H 2 O +
 • Амфотерный оксид. При сплавлении Cr 2 O 3 со щелочами, содой и кислыми солями получаются соединения хрома со степенью окисления (+3): Cr 2 O 3 + 2 Na. OH ® 2 Na. Cr. O 2 + H 2 O Cr 2 O 3 + Na 2 CO 3 ® 2 Na. Cr. O 2 + CO 2 Cr 2 O 3 + 6 KHSO 4 ® Cr 2(SO 4)3 + 3 K 2 SO 4 + 3 H 2 O
• Амфотерный оксид. При сплавлении Cr 2 O 3 со щелочами, содой и кислыми солями получаются соединения хрома со степенью окисления (+3): Cr 2 O 3 + 2 Na. OH ® 2 Na. Cr. O 2 + H 2 O Cr 2 O 3 + Na 2 CO 3 ® 2 Na. Cr. O 2 + CO 2 Cr 2 O 3 + 6 KHSO 4 ® Cr 2(SO 4)3 + 3 K 2 SO 4 + 3 H 2 O
 • При сплавлении со смесью щёлочи и окислителя получают соединения хрома в степени окисления (+6): 2 Cr 2 O 3+4 KOH +KCl. O 3 ® 2 K 2 Cr 2 O 7+ KCl +2 H 2 O (дихромат калия)
• При сплавлении со смесью щёлочи и окислителя получают соединения хрома в степени окисления (+6): 2 Cr 2 O 3+4 KOH +KCl. O 3 ® 2 K 2 Cr 2 O 7+ KCl +2 H 2 O (дихромат калия)
 • Гидроксид хрома (III) Cr(OH)3 - нерастворимое в воде вещество зелёного цвета. Cr 2(SO 4)3 + 6 Na. OH ® 2 Cr(OH)3¯ + 3 Na 2 SO 4 • Обладает амфотерными свойствами - растворяется как в кислотах, так и в щелочах: 2 Cr(OH)3 + 3 H 2 SO 4 ® Cr 2(SO 4)3 + 6 H 2 O Cr(OH)3 + KOH ® K[Cr(OH)4]
• Гидроксид хрома (III) Cr(OH)3 - нерастворимое в воде вещество зелёного цвета. Cr 2(SO 4)3 + 6 Na. OH ® 2 Cr(OH)3¯ + 3 Na 2 SO 4 • Обладает амфотерными свойствами - растворяется как в кислотах, так и в щелочах: 2 Cr(OH)3 + 3 H 2 SO 4 ® Cr 2(SO 4)3 + 6 H 2 O Cr(OH)3 + KOH ® K[Cr(OH)4]
 • Соли хрома (III) имеют фиолетовую или тёмно-зелёную окраску. По химическим свойствам напоминают бесцветные соли алюминия. • Соединения Cr (III) могут проявлять и окислительные, и восстановительные свойства: Zn + 2 Cr. Cl 3 ® 2 Cr. Cl 2 + Zn. Cl 2 2 Cr. Cl 3 + 16 Na. OH + 3 Br 2 ® 6 Na. Br + 6 Na. Cl + 8 H 2 O + 2 Na 2 Cr. O 4
• Соли хрома (III) имеют фиолетовую или тёмно-зелёную окраску. По химическим свойствам напоминают бесцветные соли алюминия. • Соединения Cr (III) могут проявлять и окислительные, и восстановительные свойства: Zn + 2 Cr. Cl 3 ® 2 Cr. Cl 2 + Zn. Cl 2 2 Cr. Cl 3 + 16 Na. OH + 3 Br 2 ® 6 Na. Br + 6 Na. Cl + 8 H 2 O + 2 Na 2 Cr. O 4
 • В щелочной среде производные Cr+3 легко окисляются до хроматов 2 KCr. O 2 +3 Br 2 +8 KOH = 6 KBr + 4 H 2 O + 2 K 2 Cr. O 4 Cr 2(SO 4)3 + 3 H 2 O 2 + 10 Na. OH = 2 Na 2 Cr. O 4 + 3 Na 2 SO 4 + 8 H 2 O
• В щелочной среде производные Cr+3 легко окисляются до хроматов 2 KCr. O 2 +3 Br 2 +8 KOH = 6 KBr + 4 H 2 O + 2 K 2 Cr. O 4 Cr 2(SO 4)3 + 3 H 2 O 2 + 10 Na. OH = 2 Na 2 Cr. O 4 + 3 Na 2 SO 4 + 8 H 2 O
 Соединения хрома +6 • Оксид хрома (VI) Cr. O 3 - ярко-красные кристаллы, растворимые в воде. • Получают из хромата (или дихромата) калия и H 2 SO 4(конц. ). K 2 Cr. O 4 + H 2 SO 4 ® Cr. O 3 + K 2 SO 4 + H 2 O K 2 Cr 2 O 7 + H 2 SO 4 ® 2 Cr. O 3 + K 2 SO 4 + H 2 O
Соединения хрома +6 • Оксид хрома (VI) Cr. O 3 - ярко-красные кристаллы, растворимые в воде. • Получают из хромата (или дихромата) калия и H 2 SO 4(конц. ). K 2 Cr. O 4 + H 2 SO 4 ® Cr. O 3 + K 2 SO 4 + H 2 O K 2 Cr 2 O 7 + H 2 SO 4 ® 2 Cr. O 3 + K 2 SO 4 + H 2 O
 • Cr. O 3 – ядовит, сильный окислитель, разлагается при 200° по реакции: 4 Cr. O 3 = 2 Cr 2 O 3 + 3 O 2 • Cr. O 3 + H 2 O = H 2 Cr. O 4 хромовая кислота
• Cr. O 3 – ядовит, сильный окислитель, разлагается при 200° по реакции: 4 Cr. O 3 = 2 Cr 2 O 3 + 3 O 2 • Cr. O 3 + H 2 O = H 2 Cr. O 4 хромовая кислота
 • Cr. O 3 - кислотный оксид, со щелочами образует жёлтые хроматы Cr. O 42 -: Cr. O 3 + 2 KOH ® K 2 Cr. O 4 + H 2 O • В кислой среде хроматы превращаются в оранжевые дихроматы Cr 2 O 72 -: 2 K 2 Cr. O 4 + H 2 SO 4 ® K 2 Cr 2 O 7 + K 2 SO 4 + H 2 O • В щелочной среде эта реакция протекает в обратном направлении: K 2 Cr 2 O 7 + 2 KOH ® 2 K 2 Cr. O 4 + H 2 O
• Cr. O 3 - кислотный оксид, со щелочами образует жёлтые хроматы Cr. O 42 -: Cr. O 3 + 2 KOH ® K 2 Cr. O 4 + H 2 O • В кислой среде хроматы превращаются в оранжевые дихроматы Cr 2 O 72 -: 2 K 2 Cr. O 4 + H 2 SO 4 ® K 2 Cr 2 O 7 + K 2 SO 4 + H 2 O • В щелочной среде эта реакция протекает в обратном направлении: K 2 Cr 2 O 7 + 2 KOH ® 2 K 2 Cr. O 4 + H 2 O
 Растворы бихроматов показывают кислую реакцию Cr 2 O 72 - + Н 2 О 2 HCr. O 4 - 2 Cr. O 42 - +2 H+ • Получение хроматов и бихроматов: K 2 Cr 2 O 7 + 2 КОН = 2 K 2 Cr. O 4 + Н 2 О 2 K 2 Cr. O 4 + H 2 SO 4 = K 2 Cr 2 O 7 +K 2 SO 4+ Н 2 О
Растворы бихроматов показывают кислую реакцию Cr 2 O 72 - + Н 2 О 2 HCr. O 4 - 2 Cr. O 42 - +2 H+ • Получение хроматов и бихроматов: K 2 Cr 2 O 7 + 2 КОН = 2 K 2 Cr. O 4 + Н 2 О 2 K 2 Cr. O 4 + H 2 SO 4 = K 2 Cr 2 O 7 +K 2 SO 4+ Н 2 О
 • Соли хромовых кислот в кислой среде – сильные окислители K 2 Cr 2 O 7 +14 HГ =2 KГ +2 Сr. Г 3 +3 Г 2+7 Н 2 О (Г= Cl, Br, J) • Смесь равных объемов насыщенного на холоду раствора K 2 Cr 2 O 7 и концентрированной H 2 SO 4 применяется для мытья химической посуды и называется «хромовая смесь» .
• Соли хромовых кислот в кислой среде – сильные окислители K 2 Cr 2 O 7 +14 HГ =2 KГ +2 Сr. Г 3 +3 Г 2+7 Н 2 О (Г= Cl, Br, J) • Смесь равных объемов насыщенного на холоду раствора K 2 Cr 2 O 7 и концентрированной H 2 SO 4 применяется для мытья химической посуды и называется «хромовая смесь» .
 • Cr. O 3 + 2 HCl(газ) = Cr. O 2 Cl 2 + H 2 O хлористый хромил красно-бурая жидкость • Cr. O 2 Cl 2 + H 2 O Cr. O 2(OH)2 + 2 HCl • Все соединения хрома (VI) - сильные окислители: 4 Cr. O 3 + 3 S ® 3 SO 2 + 2 Cr 2 O 3
• Cr. O 3 + 2 HCl(газ) = Cr. O 2 Cl 2 + H 2 O хлористый хромил красно-бурая жидкость • Cr. O 2 Cl 2 + H 2 O Cr. O 2(OH)2 + 2 HCl • Все соединения хрома (VI) - сильные окислители: 4 Cr. O 3 + 3 S ® 3 SO 2 + 2 Cr 2 O 3
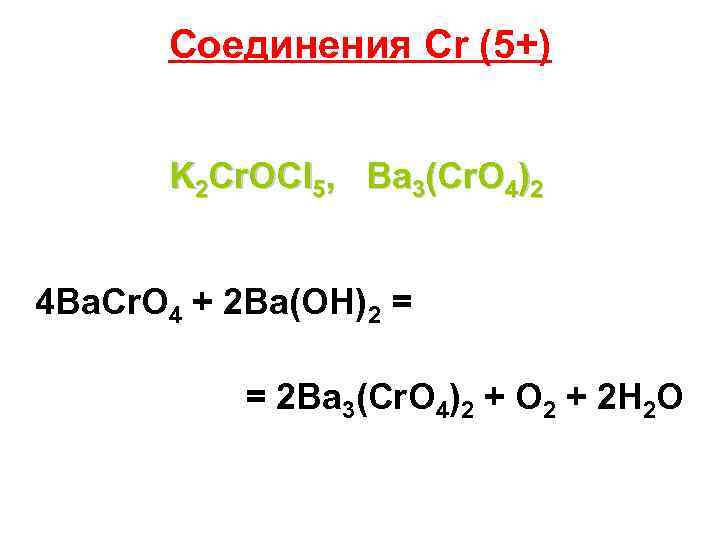 Соединения Cr (5+) K 2 Cr. OCl 5, Ba 3(Cr. O 4)2 4 Ba. Cr. O 4 + 2 Ba(OH)2 = = 2 Ba 3(Cr. O 4)2 + O 2 + 2 H 2 O
Соединения Cr (5+) K 2 Cr. OCl 5, Ba 3(Cr. O 4)2 4 Ba. Cr. O 4 + 2 Ba(OH)2 = = 2 Ba 3(Cr. O 4)2 + O 2 + 2 H 2 O
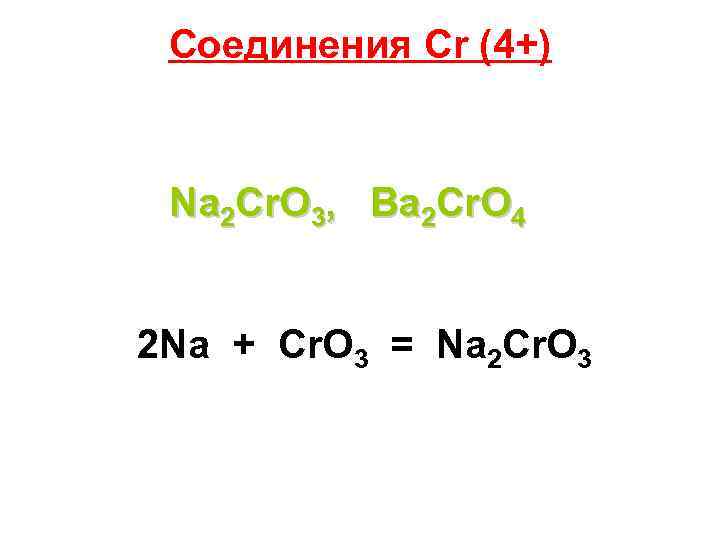 Соединения Cr (4+) Na 2 Cr. O 3, Ba 2 Cr. O 4 2 Na + Cr. O 3 = Na 2 Cr. O 3
Соединения Cr (4+) Na 2 Cr. O 3, Ba 2 Cr. O 4 2 Na + Cr. O 3 = Na 2 Cr. O 3
 Применение хрома • Для получения сплавов: нержавеющей стали, нихрома и др. • Декоративные коррозионно-стойкие покрытия. • Соединения хрома — огнеупорные материалы. • Оксид хрома (III) — пигмент зеленой краски, также входит в состав абразивных материалов (паст ГОИ). • Изменение окраски при восстановлении соединений хрома(VI) применяют для проведения экспресс-анализа на содержание алкоголя в выдыхаемом воздухе.
Применение хрома • Для получения сплавов: нержавеющей стали, нихрома и др. • Декоративные коррозионно-стойкие покрытия. • Соединения хрома — огнеупорные материалы. • Оксид хрома (III) — пигмент зеленой краски, также входит в состав абразивных материалов (паст ГОИ). • Изменение окраски при восстановлении соединений хрома(VI) применяют для проведения экспресс-анализа на содержание алкоголя в выдыхаемом воздухе.


