Lektsia_N_16_Vzaimodeystvie_metallov.ppt
- Количество слайдов: 13
 Лекция N Взаимодействие металлов с водой, растворами солей, щелочей и кислот. Профессор Рыбальченко В. С.
Лекция N Взаимодействие металлов с водой, растворами солей, щелочей и кислот. Профессор Рыбальченко В. С.
 Характер взаимодействия металлов с водой. ¡ При обычной температуре с водой взаимодействуют только наиболее активные металлы, стоящие в ряду активностей до магния. РЯД АКТИВНОСТЕЙ МЕТАЛЛОВ: Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H , Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au Реакция протекает по схеме: Мe 0 + H 2 O → Me+n(OH)n + H 2↑
Характер взаимодействия металлов с водой. ¡ При обычной температуре с водой взаимодействуют только наиболее активные металлы, стоящие в ряду активностей до магния. РЯД АКТИВНОСТЕЙ МЕТАЛЛОВ: Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H , Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au Реакция протекает по схеме: Мe 0 + H 2 O → Me+n(OH)n + H 2↑
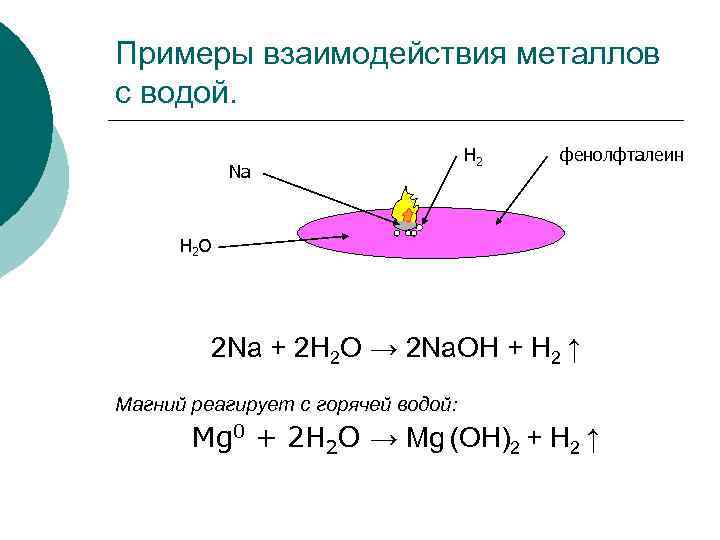 Примеры взаимодействия металлов с водой. Na H 2 фенолфталеин H 2 O 2 Na + 2 H 2 O → 2 Na. OH + H 2 ↑ Магний реагирует с горячей водой: Мg 0 + 2 H 2 O → Mg (OH)2 + H 2 ↑
Примеры взаимодействия металлов с водой. Na H 2 фенолфталеин H 2 O 2 Na + 2 H 2 O → 2 Na. OH + H 2 ↑ Магний реагирует с горячей водой: Мg 0 + 2 H 2 O → Mg (OH)2 + H 2 ↑
 В раскаленном состоянии железо реагирует с перегретым водяным паром. ¡ Железо-паровой способ получения водорода: 2 Fe + 3 H 2 O = Fe 2 O 3 + 3 H 2 Раскаленное Нагретый пар
В раскаленном состоянии железо реагирует с перегретым водяным паром. ¡ Железо-паровой способ получения водорода: 2 Fe + 3 H 2 O = Fe 2 O 3 + 3 H 2 Раскаленное Нагретый пар
 С растворами щелочей реагируют металлы, оксиды и гидроксиды которых обладают амфотерными свойствами. ¡ В щелочных средах неустойчивы Al, Zn и их сплавы. 2 Al + 2 Na. OH + 6 H 2 O → 2 Na[Al(OH)4] + 3 H 2↑ Zn + 2 Na. OH + 2 H 2 O → Na 2[Zn(OH)4] + H 2↑
С растворами щелочей реагируют металлы, оксиды и гидроксиды которых обладают амфотерными свойствами. ¡ В щелочных средах неустойчивы Al, Zn и их сплавы. 2 Al + 2 Na. OH + 6 H 2 O → 2 Na[Al(OH)4] + 3 H 2↑ Zn + 2 Na. OH + 2 H 2 O → Na 2[Zn(OH)4] + H 2↑
 Характер взаимодействия металлов с растворами солей • Каждый более активный металл (не взаимодействующий с водой) способен вытеснить стоящий за ним металл из растворов его солей. Например: Cu Cu(NO 3)2 Ag Cu + Ag. NO 3 = Cu(NO 3)2 + Ag Cu + Hg(NO 3)2 = Cu(NO 3)2 + Hg Ag. NO 3
Характер взаимодействия металлов с растворами солей • Каждый более активный металл (не взаимодействующий с водой) способен вытеснить стоящий за ним металл из растворов его солей. Например: Cu Cu(NO 3)2 Ag Cu + Ag. NO 3 = Cu(NO 3)2 + Ag Cu + Hg(NO 3)2 = Cu(NO 3)2 + Hg Ag. NO 3
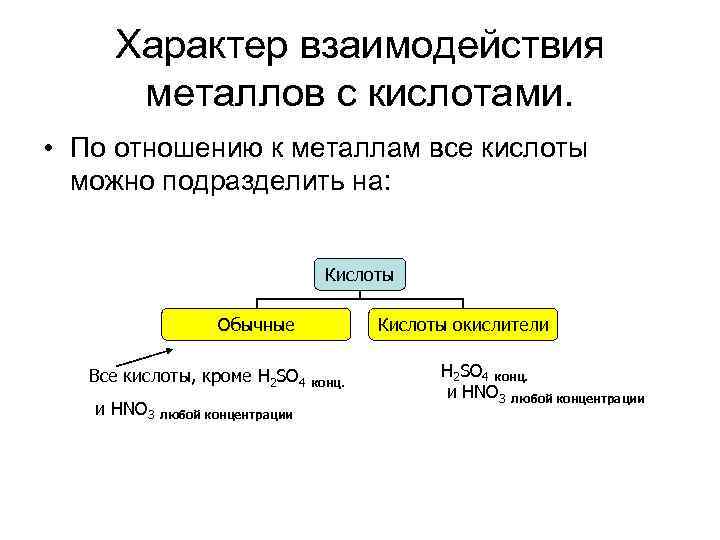 Характер взаимодействия металлов с кислотами. • По отношению к металлам все кислоты можно подразделить на: Кислоты Обычные Все кислоты, кроме H 2 SO 4 и HNO 3 любой концентрации Кислоты окислители конц. H 2 SO 4 конц. и HNO 3 любой концентрации
Характер взаимодействия металлов с кислотами. • По отношению к металлам все кислоты можно подразделить на: Кислоты Обычные Все кислоты, кроме H 2 SO 4 и HNO 3 любой концентрации Кислоты окислители конц. H 2 SO 4 конц. и HNO 3 любой концентрации
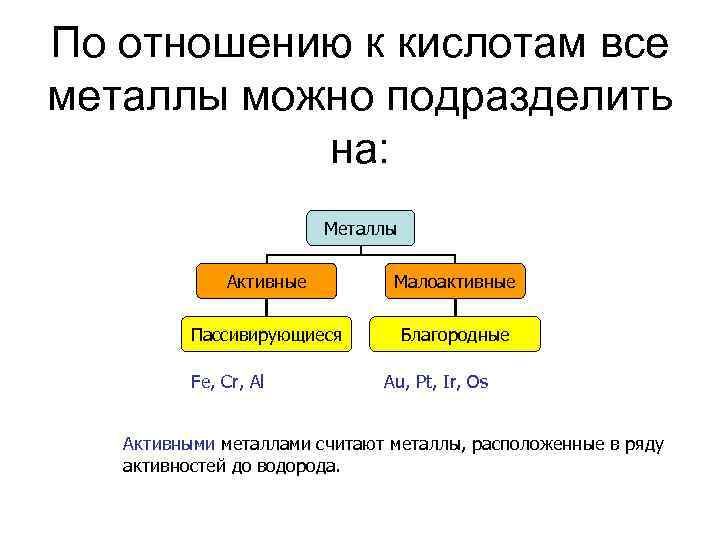 По отношению к кислотам все металлы можно подразделить на: Металлы Активные Малоактивные Пассивирующиеся Благородные Fe, Cr, Al Au, Pt, Ir, Os Активными металлами считают металлы, расположенные в ряду активностей до водорода.
По отношению к кислотам все металлы можно подразделить на: Металлы Активные Малоактивные Пассивирующиеся Благородные Fe, Cr, Al Au, Pt, Ir, Os Активными металлами считают металлы, расположенные в ряду активностей до водорода.
 Взаимодействие металлов с обычными кислотами l С обычными кислотами взаимодействуют только активные металлы. Реакция протекает по схеме: Me 0+ H+1 An → Me+n. An + H 20 металл + кислота → соль + водород
Взаимодействие металлов с обычными кислотами l С обычными кислотами взаимодействуют только активные металлы. Реакция протекает по схеме: Me 0+ H+1 An → Me+n. An + H 20 металл + кислота → соль + водород
 НАПРИМЕР : Zn + H 2 SO 4 разб. → Zn. SO 4 + H 2↑ Выделяющиеся пузырьки газообразного водорода
НАПРИМЕР : Zn + H 2 SO 4 разб. → Zn. SO 4 + H 2↑ Выделяющиеся пузырьки газообразного водорода
 Характер взаимодействия концентрированной H 2 SO 4 с металлами. не взаимодействует с благородными металлами; ¡ в концентрированном состоянии без нагревания пассивирует Fe, Cr и Al; ¡ с остальными металлами реакция протекает по схеме: +4 SO 2 0 +6 +n Me + H 2 SO 4 = Me. SO 4 + S 0 + H 2 O H 2 S-2 ¡ Глубина восстановления S+6 определяется активностью металла: чем активнее металл, тем больше меняется степень окисления.
Характер взаимодействия концентрированной H 2 SO 4 с металлами. не взаимодействует с благородными металлами; ¡ в концентрированном состоянии без нагревания пассивирует Fe, Cr и Al; ¡ с остальными металлами реакция протекает по схеме: +4 SO 2 0 +6 +n Me + H 2 SO 4 = Me. SO 4 + S 0 + H 2 O H 2 S-2 ¡ Глубина восстановления S+6 определяется активностью металла: чем активнее металл, тем больше меняется степень окисления.
 Характер взаимодействия HNO 3 с металлами. ¡ ¡ ¡ не взаимодействует с благородными металлами; в концентрированном состоянии без нагревания пассивирует Fe, Cr и Al; с остальными металлами реакция протекает по схеме: I Me 0 + HN+5 O 3 = Me+n. NO 3 + II N+4 O 2 N+2 O N 2+1 O N-3 H 4 NO 3 + H 2 O Глубина восстановления N+5 зависит : I) от активности металла: чем активнее металл, тем глубже происходит изменение степени окисления. II) от концентрации кислоты: чем более разбавлена кислота, тем глубже происходит изменение степени окисления.
Характер взаимодействия HNO 3 с металлами. ¡ ¡ ¡ не взаимодействует с благородными металлами; в концентрированном состоянии без нагревания пассивирует Fe, Cr и Al; с остальными металлами реакция протекает по схеме: I Me 0 + HN+5 O 3 = Me+n. NO 3 + II N+4 O 2 N+2 O N 2+1 O N-3 H 4 NO 3 + H 2 O Глубина восстановления N+5 зависит : I) от активности металла: чем активнее металл, тем глубже происходит изменение степени окисления. II) от концентрации кислоты: чем более разбавлена кислота, тем глубже происходит изменение степени окисления.
 Примеры реакций. ¡ ¡ ¡ 4 HNO 3 (конц. )+ Cu = Cu(NO 3)2 + 2 NO 2 + 2 H 2 O 8 HNO 3 (разб. ) + 3 Cu = 3 Cu(NO 3)2 + 2 NO +4 H 2 O 10 HNO 3 (с. разб. ) + 4 Са = 4 Ca(NO 3)2 + NН 4 NO 3 + 3 H 2 O
Примеры реакций. ¡ ¡ ¡ 4 HNO 3 (конц. )+ Cu = Cu(NO 3)2 + 2 NO 2 + 2 H 2 O 8 HNO 3 (разб. ) + 3 Cu = 3 Cu(NO 3)2 + 2 NO +4 H 2 O 10 HNO 3 (с. разб. ) + 4 Са = 4 Ca(NO 3)2 + NН 4 NO 3 + 3 H 2 O


