Lektsia_-kons_dlya_OS.ppt
- Количество слайдов: 146
 Лекция-консультация Химия Подготовка к тестированию
Лекция-консультация Химия Подготовка к тестированию
 Дидактические единицы l l l ДЕ 1. Номенклатура. Сопряжение. Электронные эффекты заместителей. Карбоновые кислоты. Липиды. (6 вопросов). ДЕ 2. Аминокислоты. Белки. Нуклеиновые кислоты. Углеводы. (7 вопросов). ДЕ 3. Школьный курс органической химии (4 вопроса). ДЕ 4. Школьный курс неорганической химии (4 вопроса). ДЕ 5. Химическая термодинамика, кинетика, равновесие. (6 вопросов). l l ДЕ 6. Растворы. Концентрация. Физико-химические свойства (осмос, закон Ф. Рауля, следствия). Растворы электролитов. (6 вопроса) ДЕ 7. Окислительно-восстановительные реакции. Коррозия. Диаграммы состояния. (5 вопросов).
Дидактические единицы l l l ДЕ 1. Номенклатура. Сопряжение. Электронные эффекты заместителей. Карбоновые кислоты. Липиды. (6 вопросов). ДЕ 2. Аминокислоты. Белки. Нуклеиновые кислоты. Углеводы. (7 вопросов). ДЕ 3. Школьный курс органической химии (4 вопроса). ДЕ 4. Школьный курс неорганической химии (4 вопроса). ДЕ 5. Химическая термодинамика, кинетика, равновесие. (6 вопросов). l l ДЕ 6. Растворы. Концентрация. Физико-химические свойства (осмос, закон Ф. Рауля, следствия). Растворы электролитов. (6 вопроса) ДЕ 7. Окислительно-восстановительные реакции. Коррозия. Диаграммы состояния. (5 вопросов).
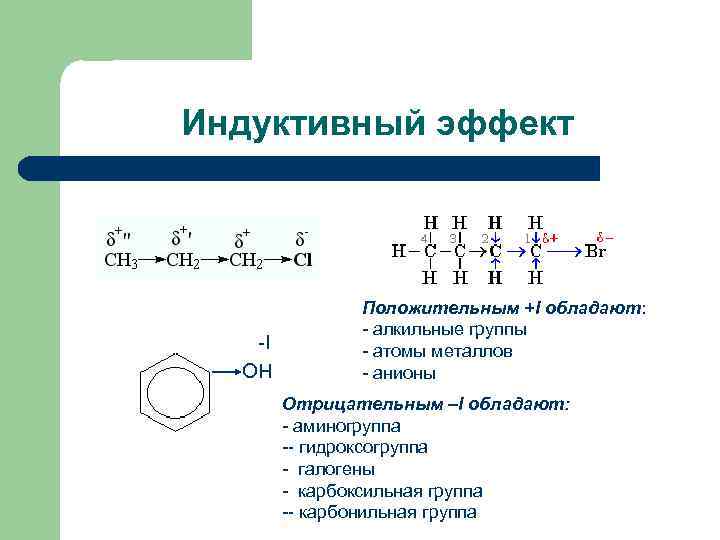 Индуктивный эффект -I ОН Положительным +I обладают: - алкильные группы - атомы металлов - анионы Отрицательным –I обладают: - аминогруппа -- гидроксогруппа - галогены - карбоксильная группа -- карбонильная группа
Индуктивный эффект -I ОН Положительным +I обладают: - алкильные группы - атомы металлов - анионы Отрицательным –I обладают: - аминогруппа -- гидроксогруппа - галогены - карбоксильная группа -- карбонильная группа
 Мезомерный эффект Группы атомов, смещающих электронную плотность на себя, обладают - М: - СОН; - СООН - содержат более электроотрицательные атомы, находящиеся в sp 2. Заместители, повышающие электронную плотность в сопряженной системе, проявляют + М: -ОН; -ОR; -SH; -NH 2 – содержат атомы в sp 3 гибридном состоянии Мезомерный эффект – это передача электронного влияния заместителя по системе π - связей
Мезомерный эффект Группы атомов, смещающих электронную плотность на себя, обладают - М: - СОН; - СООН - содержат более электроотрицательные атомы, находящиеся в sp 2. Заместители, повышающие электронную плотность в сопряженной системе, проявляют + М: -ОН; -ОR; -SH; -NH 2 – содержат атомы в sp 3 гибридном состоянии Мезомерный эффект – это передача электронного влияния заместителя по системе π - связей
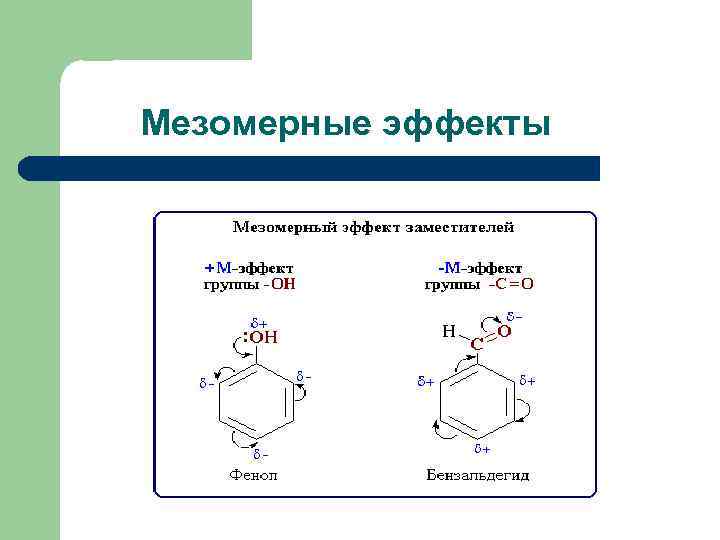 Мезомерные эффекты
Мезомерные эффекты
 Признаки ароматичности соединений Плоский замкнутый цикл. sp 2 гибридизация атомов l Сопряженная электронная система (4 n+2) π-электронов, охватывающая все атомы цикла - правило нем. физика Э. Хюккеля, где: n – целое число n =1 число е 6 n =2 число е 10 n = 3 число е 14 l
Признаки ароматичности соединений Плоский замкнутый цикл. sp 2 гибридизация атомов l Сопряженная электронная система (4 n+2) π-электронов, охватывающая все атомы цикла - правило нем. физика Э. Хюккеля, где: n – целое число n =1 число е 6 n =2 число е 10 n = 3 число е 14 l
 Факторы, от которых зависит сила протолитической кислоты l l Электроотрицательность атома, с которым связан протон Размер атома Возможность делокализации отрицательного заряда по другим атомам Способность растворителя сольватировать образующиеся ионы
Факторы, от которых зависит сила протолитической кислоты l l Электроотрицательность атома, с которым связан протон Размер атома Возможность делокализации отрицательного заряда по другим атомам Способность растворителя сольватировать образующиеся ионы
 Типы бренстедовских кислот l - О - Н – кислоты : карбоновые кислоты, фенолы, спирты l - S - H - кислоты: тиолы l - N - Н - кислоты: амиды, амины, имиды l - С - Н - кислоты: углеводороды и их производные
Типы бренстедовских кислот l - О - Н – кислоты : карбоновые кислоты, фенолы, спирты l - S - H - кислоты: тиолы l - N - Н - кислоты: амиды, амины, имиды l - С - Н - кислоты: углеводороды и их производные
 Изменение кислотных свойств органических веществ СН – кислоты < NH - кислоты < OH - кислоты < SH - кислоты Увеличивается сила кислоты, т. к. повышается стабильность аниона Увеличение длины углеводородного радикала и его разветвление приводит к уменьшению силы кислоты СН 3 ОН р. Ка = 16; С 2 Н 5 ОН р. Ка = 18 Введение заместителей в углеводородный радикал способствует изменению кислотности Н 3 СН р. Ка = 40. 0 Сl 3 CH р. Ка =15, 7
Изменение кислотных свойств органических веществ СН – кислоты < NH - кислоты < OH - кислоты < SH - кислоты Увеличивается сила кислоты, т. к. повышается стабильность аниона Увеличение длины углеводородного радикала и его разветвление приводит к уменьшению силы кислоты СН 3 ОН р. Ка = 16; С 2 Н 5 ОН р. Ка = 18 Введение заместителей в углеводородный радикал способствует изменению кислотности Н 3 СН р. Ка = 40. 0 Сl 3 CH р. Ка =15, 7
 Классификация оснований – акцепторов протона Π- основания: l l l арены алкадиены n- основания (ониевые основания): . . l аммониевые l оксониевые . . -О. . сульфониевые . . -S. . l N . . = N. . =О. . = N (аммиак, его производные, гетероциклы) (спирты, альдегиды, кетоны, простые эфиры) (тиоспирты, тиоэфиры, сульфиды)
Классификация оснований – акцепторов протона Π- основания: l l l арены алкадиены n- основания (ониевые основания): . . l аммониевые l оксониевые . . -О. . сульфониевые . . -S. . l N . . = N. . =О. . = N (аммиак, его производные, гетероциклы) (спирты, альдегиды, кетоны, простые эфиры) (тиоспирты, тиоэфиры, сульфиды)
 Сила ониевых оснований зависит l l l от электроотрицательности гетероатома; от размеров гетероатома; от электронных эффектов заместителей. NH 3 + HOH ↔ р. Кb =9. 25 NH 4+ + OHp. Kа = 4. 75 (CH 3)2 NH + HOH ↔ (CH 3)2 NH 2+ + OHp. Kb = 2. 97 p. Kа = 11. 03
Сила ониевых оснований зависит l l l от электроотрицательности гетероатома; от размеров гетероатома; от электронных эффектов заместителей. NH 3 + HOH ↔ р. Кb =9. 25 NH 4+ + OHp. Kа = 4. 75 (CH 3)2 NH + HOH ↔ (CH 3)2 NH 2+ + OHp. Kb = 2. 97 p. Kа = 11. 03
 Классификация карбоновых кислот l По числу карбоксильных групп: - монокарбоновые - дикарбоновые - трикарбоновые l По строению и природе радикала: - предельные (ациклические и циклические) - непредельные - ароматические (карбо- и гетеро-) l По наличию других функциональных групп в радикале: - гидроксикислоты ( -ОН ) - оксикислоты - аминокислоты (=О) ( - NН 2 )
Классификация карбоновых кислот l По числу карбоксильных групп: - монокарбоновые - дикарбоновые - трикарбоновые l По строению и природе радикала: - предельные (ациклические и циклические) - непредельные - ароматические (карбо- и гетеро-) l По наличию других функциональных групп в радикале: - гидроксикислоты ( -ОН ) - оксикислоты - аминокислоты (=О) ( - NН 2 )
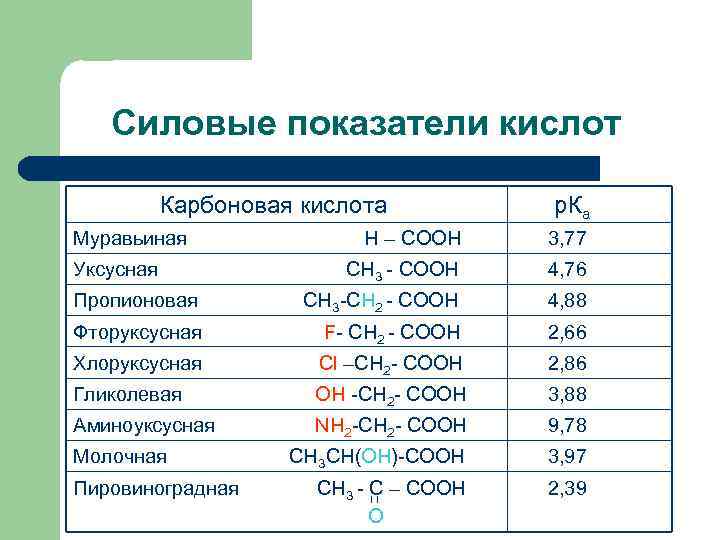 Силовые показатели кислот Карбоновая кислота Муравьиная р. Ка Н – СООН 3, 77 СН 3 - СООН 4, 76 Пропионовая СН 3 -СН 2 - СООН 4, 88 Фторуксусная F- СН 2 - СООН 2, 66 Хлоруксусная Сl –СН 2 - СООН 2, 86 Гликолевая ОН -СН 2 - СООН 3, 88 Аминоуксусная NН 2 -СН 2 - СООН 9, 78 СН 3 СН(ОН)-СООН 3, 97 СН 3 - С – СООН О 2, 39 Уксусная Молочная Пировиноградная
Силовые показатели кислот Карбоновая кислота Муравьиная р. Ка Н – СООН 3, 77 СН 3 - СООН 4, 76 Пропионовая СН 3 -СН 2 - СООН 4, 88 Фторуксусная F- СН 2 - СООН 2, 66 Хлоруксусная Сl –СН 2 - СООН 2, 86 Гликолевая ОН -СН 2 - СООН 3, 88 Аминоуксусная NН 2 -СН 2 - СООН 9, 78 СН 3 СН(ОН)-СООН 3, 97 СН 3 - С – СООН О 2, 39 Уксусная Молочная Пировиноградная
 Химические свойства карбоновых кислот l Реакции с участием карбоксильной группы а) замещение атомов водорода б) замещение гидроксильной группы (нуклеофильное замещение) Это: - образование солей - образование сложных эфиров - образование тиоэфиров - образование амидов l Реакции с участием радикала: - дегидрирование - карбоксилирование
Химические свойства карбоновых кислот l Реакции с участием карбоксильной группы а) замещение атомов водорода б) замещение гидроксильной группы (нуклеофильное замещение) Это: - образование солей - образование сложных эфиров - образование тиоэфиров - образование амидов l Реакции с участием радикала: - дегидрирование - карбоксилирование
 Дикарбоновые кислоты Общая формула Сn. H 2 n-2 O 4 Щавелевая (этандиовая) НООС-СООН Малоновая (пропандиовая) НООС-СН 2 -СООН Янтарная (бутандиовая) НООС-(СН 2)2 СООН Глутаровая (пентандиовая) НООС-(СН 2)3 -СООН
Дикарбоновые кислоты Общая формула Сn. H 2 n-2 O 4 Щавелевая (этандиовая) НООС-СООН Малоновая (пропандиовая) НООС-СН 2 -СООН Янтарная (бутандиовая) НООС-(СН 2)2 СООН Глутаровая (пентандиовая) НООС-(СН 2)3 -СООН
 Заменимые аминокислоты l l l l l Аланин Аргинин Аспарагиновая кислота Глицин Глутаминовая кислота Гистидин Пролин Серин Тирозин Цистеин
Заменимые аминокислоты l l l l l Аланин Аргинин Аспарагиновая кислота Глицин Глутаминовая кислота Гистидин Пролин Серин Тирозин Цистеин
 Незаменимые аминокислоты Валин Лейцин Изолейцин Лизин Треонин Метионин Фенилаланин Триптофан
Незаменимые аминокислоты Валин Лейцин Изолейцин Лизин Треонин Метионин Фенилаланин Триптофан
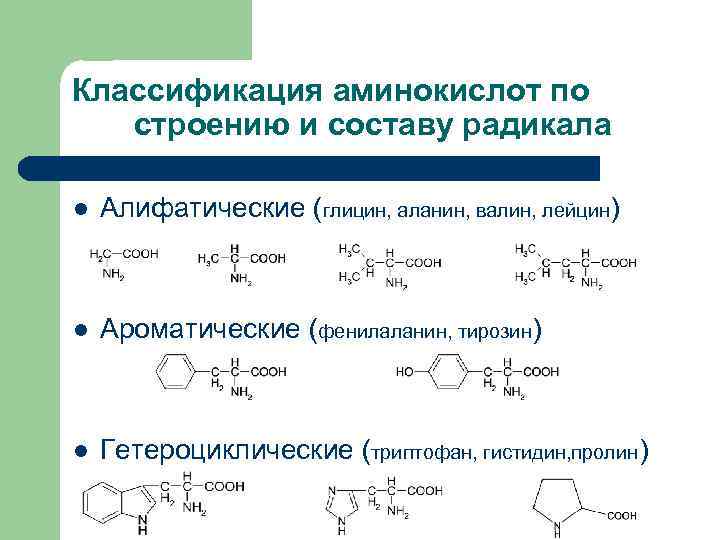 Классификация аминокислот по строению и составу радикала l Алифатические (глицин, аланин, валин, лейцин) l Ароматические (фенилаланин, тирозин) l Гетероциклические (триптофан, гистидин, пролин)
Классификация аминокислот по строению и составу радикала l Алифатические (глицин, аланин, валин, лейцин) l Ароматические (фенилаланин, тирозин) l Гетероциклические (триптофан, гистидин, пролин)
 Классификация аминокислот по кислотно-основным свойствам l Нейтральные (моноаминомонокарбоновые) Валин l Основные (диаминомонокарбоновые) Лизин l Кислые (моноаминодикарбоновые) Аспарагиновая кислота
Классификация аминокислот по кислотно-основным свойствам l Нейтральные (моноаминомонокарбоновые) Валин l Основные (диаминомонокарбоновые) Лизин l Кислые (моноаминодикарбоновые) Аспарагиновая кислота
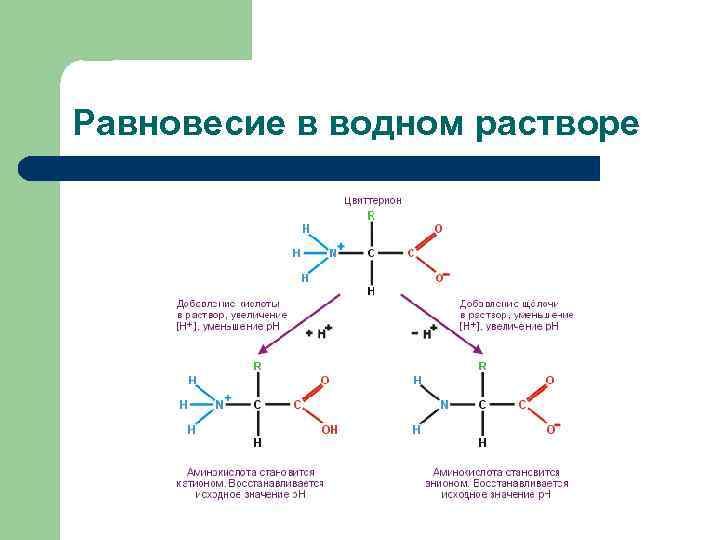 Равновесие в водном растворе
Равновесие в водном растворе
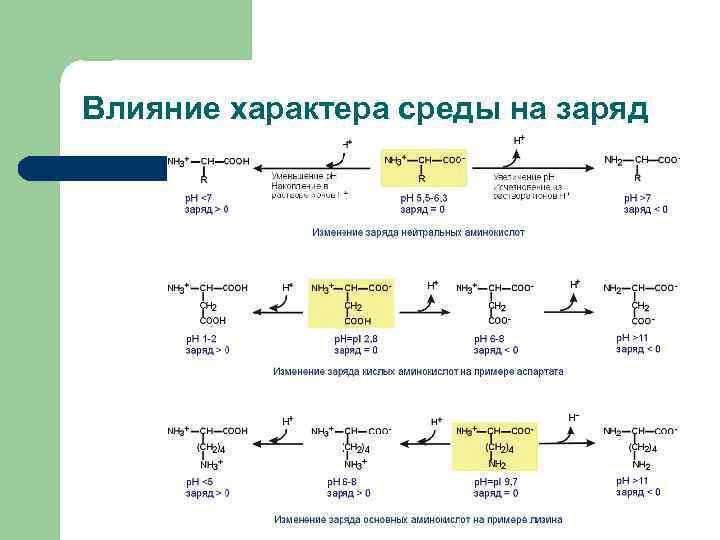 Влияние характера среды на заряд
Влияние характера среды на заряд
 Химические свойства In vitro: l l l по карбоксильной группе: Образование солей при взаимодействии с кислотами и основаниями, в т. ч. внутрикомплексных солей при взаимодействии с ионами тяжелых металлов Образование сложных эфиров Образование амидов Декарбоксилирование в присутствии Ва(ОН)2 по аминогруппе: Образование солей при взаимодействии с кислотами Ацилирование взаимодействие друг с другом
Химические свойства In vitro: l l l по карбоксильной группе: Образование солей при взаимодействии с кислотами и основаниями, в т. ч. внутрикомплексных солей при взаимодействии с ионами тяжелых металлов Образование сложных эфиров Образование амидов Декарбоксилирование в присутствии Ва(ОН)2 по аминогруппе: Образование солей при взаимодействии с кислотами Ацилирование взаимодействие друг с другом
 Химические свойства l l In vivo: Декарбоксилирование Дезаминирование: - неокислительное - окислительное Трансаминирование (переаминирование) Поликонденсация с образованием полипептидов
Химические свойства l l In vivo: Декарбоксилирование Дезаминирование: - неокислительное - окислительное Трансаминирование (переаминирование) Поликонденсация с образованием полипептидов
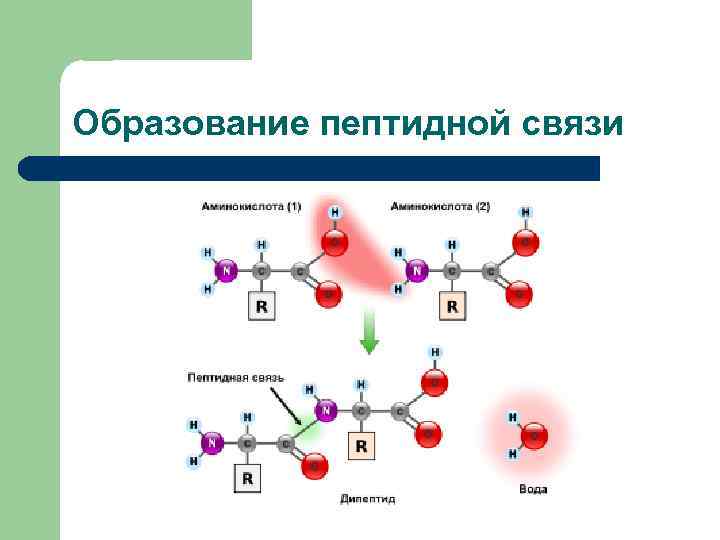 Образование пептидной связи
Образование пептидной связи
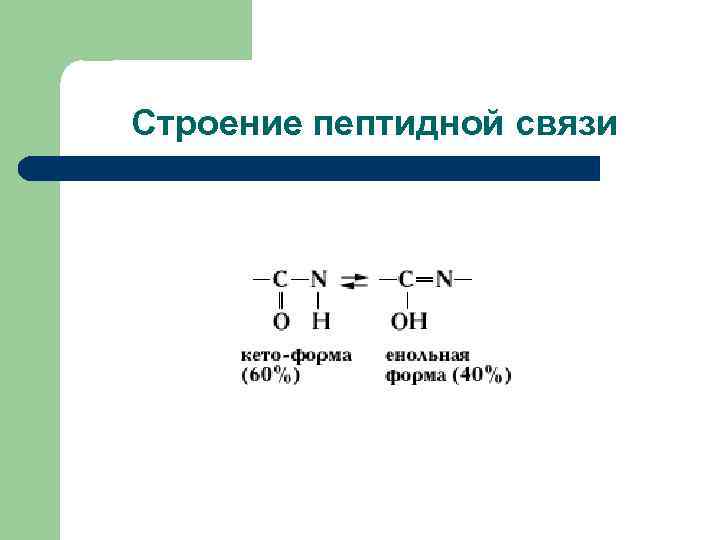 Строение пептидной связи
Строение пептидной связи
 Биуретовая реакция для обнаружения пептидных связей
Биуретовая реакция для обнаружения пептидных связей
 Ксантопротеиновая реакция Для обнаружения а-аминокислот, содержащих в радикале циклы ароматического характера
Ксантопротеиновая реакция Для обнаружения а-аминокислот, содержащих в радикале циклы ароматического характера
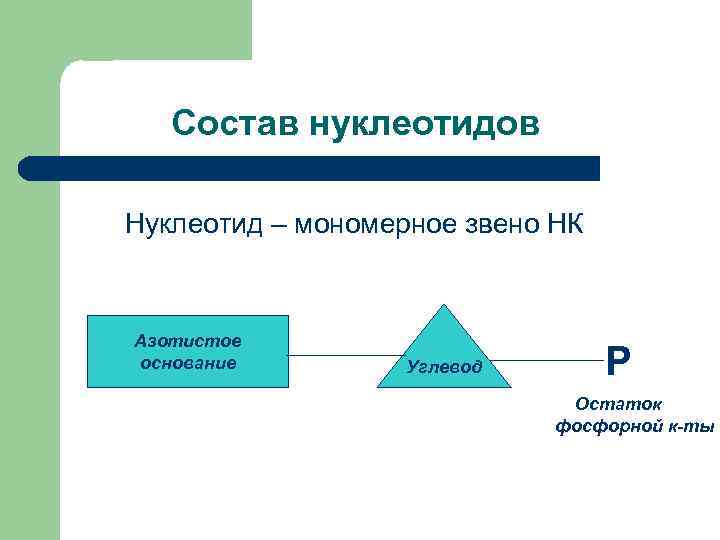 Состав нуклеотидов Нуклеотид – мономерное звено НК Азотистое основание Углевод Р Остаток фосфорной к-ты
Состав нуклеотидов Нуклеотид – мономерное звено НК Азотистое основание Углевод Р Остаток фосфорной к-ты
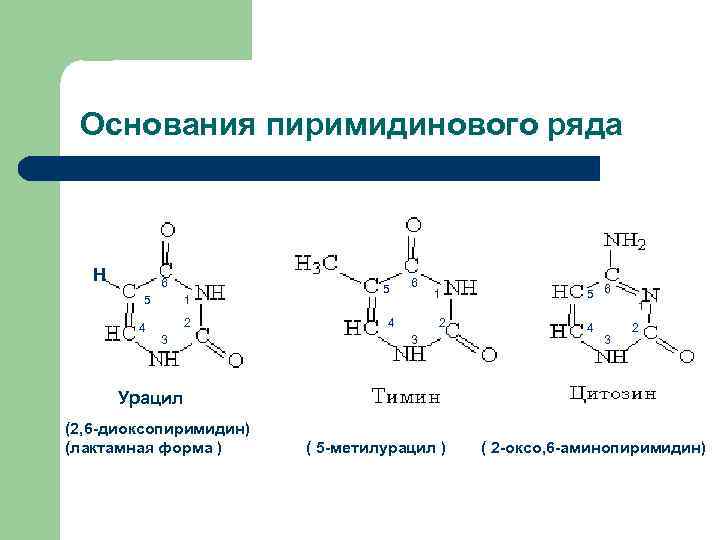 Основания пиримидинового ряда Н 6 5 4 1 2 3 5 6 4 3 1 2 Урацил (2, 6 -диоксопиримидин) (лактамная форма ) ( 5 -метилурацил ) ( 2 -оксо, 6 -аминопиримидин)
Основания пиримидинового ряда Н 6 5 4 1 2 3 5 6 4 3 1 2 Урацил (2, 6 -диоксопиримидин) (лактамная форма ) ( 5 -метилурацил ) ( 2 -оксо, 6 -аминопиримидин)
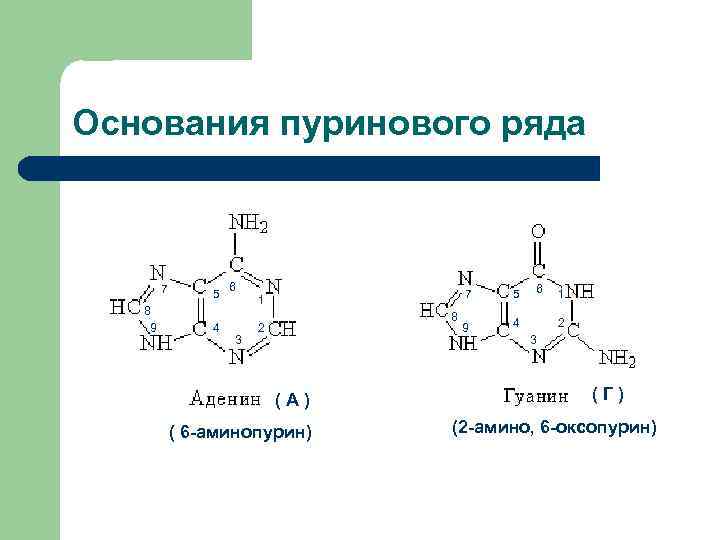 Основания пуринового ряда 7 8 9 5 4 6 3 7 1 8 2 (А) ( 6 -аминопурин) 5 9 6 4 1 2 3 (Г) (2 -амино, 6 -оксопурин)
Основания пуринового ряда 7 8 9 5 4 6 3 7 1 8 2 (А) ( 6 -аминопурин) 5 9 6 4 1 2 3 (Г) (2 -амино, 6 -оксопурин)
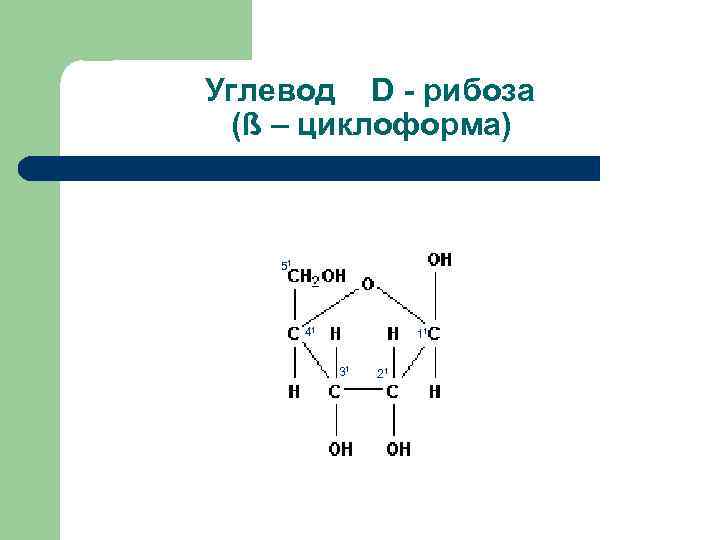 Углевод D - рибоза (ß – циклоформа) 51 41 11 31 21
Углевод D - рибоза (ß – циклоформа) 51 41 11 31 21
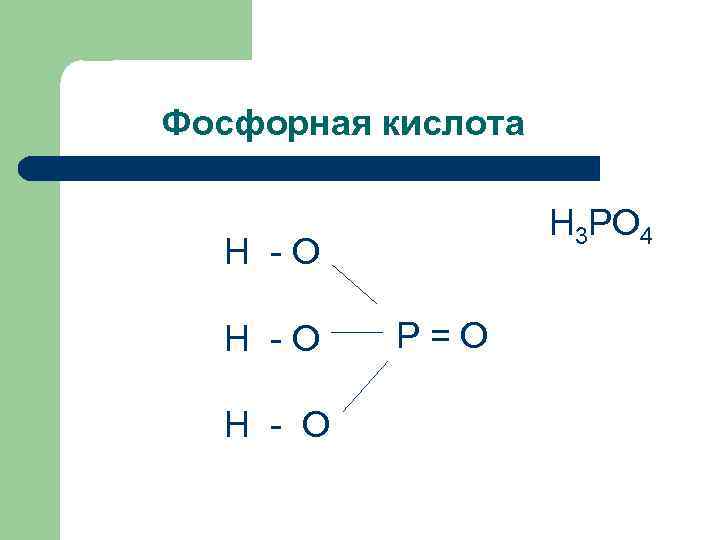 Фосфорная кислота Н 3 РО 4 Н -О Н - О Р=О
Фосфорная кислота Н 3 РО 4 Н -О Н - О Р=О
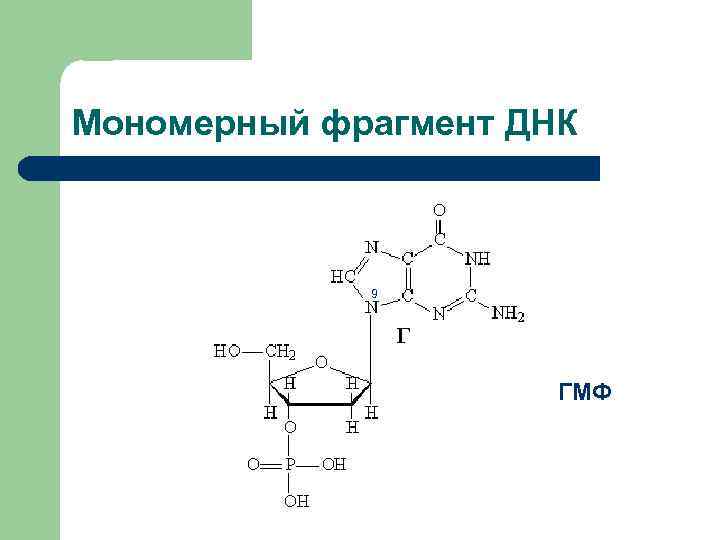 Мономерный фрагмент ДНК 9 ГМФ
Мономерный фрагмент ДНК 9 ГМФ
 Номенклатура нуклеотидов Основание l l l Урацил(У) Тимин (Т) Цитозин (Ц) Аденин (А) Гуанин (Г) Нуклеозид Нуклеотид Уридинмонофосфорная к-та УМФ Тимидинмонофосфорная к-та ТМФ Цитидинмонофосфорная к-та ЦМФ Аденозинмонофосфорная к-та АМФ Гуанозинмонофосфорная к-та ГМФ
Номенклатура нуклеотидов Основание l l l Урацил(У) Тимин (Т) Цитозин (Ц) Аденин (А) Гуанин (Г) Нуклеозид Нуклеотид Уридинмонофосфорная к-та УМФ Тимидинмонофосфорная к-та ТМФ Цитидинмонофосфорная к-та ЦМФ Аденозинмонофосфорная к-та АМФ Гуанозинмонофосфорная к-та ГМФ
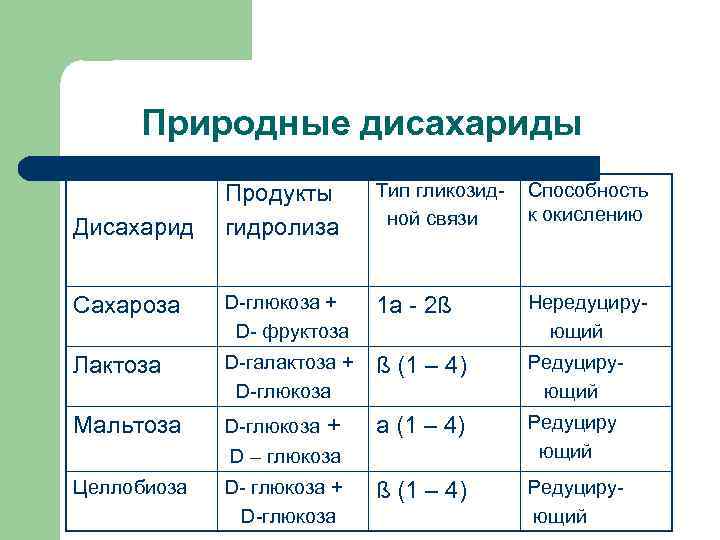 Природные дисахариды Продукты гидролиза Тип гликозидной связи Способность к окислению Сахароза D-глюкоза + D- фруктоза 1 a - 2ß Нередуцирующий Лактоза D-галактоза + D-глюкоза ß (1 – 4) Редуцирующий Мальтоза D-глюкоза + D – глюкоза a (1 – 4) Редуциру ющий Целлобиоза D- глюкоза + D-глюкоза ß (1 – 4) Редуцирующий Дисахарид
Природные дисахариды Продукты гидролиза Тип гликозидной связи Способность к окислению Сахароза D-глюкоза + D- фруктоза 1 a - 2ß Нередуцирующий Лактоза D-галактоза + D-глюкоза ß (1 – 4) Редуцирующий Мальтоза D-глюкоза + D – глюкоза a (1 – 4) Редуциру ющий Целлобиоза D- глюкоза + D-глюкоза ß (1 – 4) Редуцирующий Дисахарид
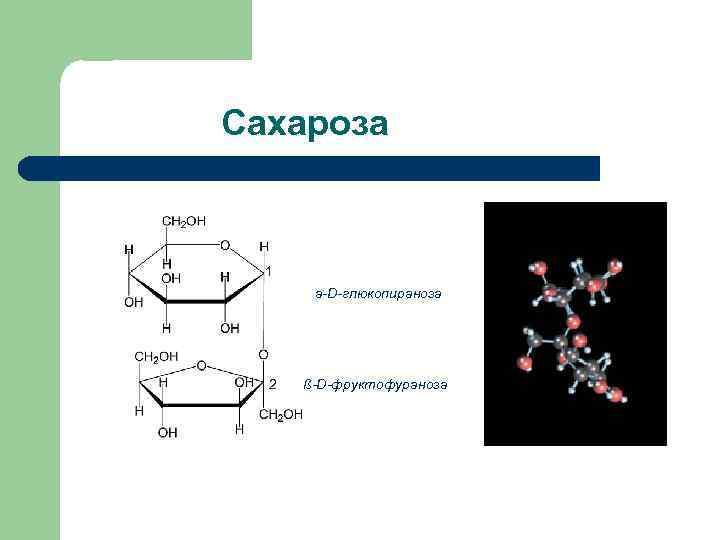 Сахароза 1 а-D-глюкопираноза 2 ß-D-фруктофураноза
Сахароза 1 а-D-глюкопираноза 2 ß-D-фруктофураноза
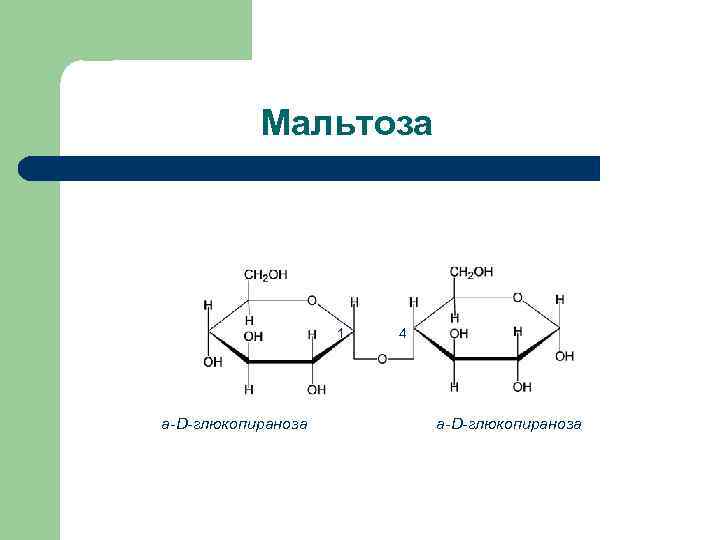 Мальтоза 1 a-D-глюкопираноза 4 a-D-глюкопираноза
Мальтоза 1 a-D-глюкопираноза 4 a-D-глюкопираноза
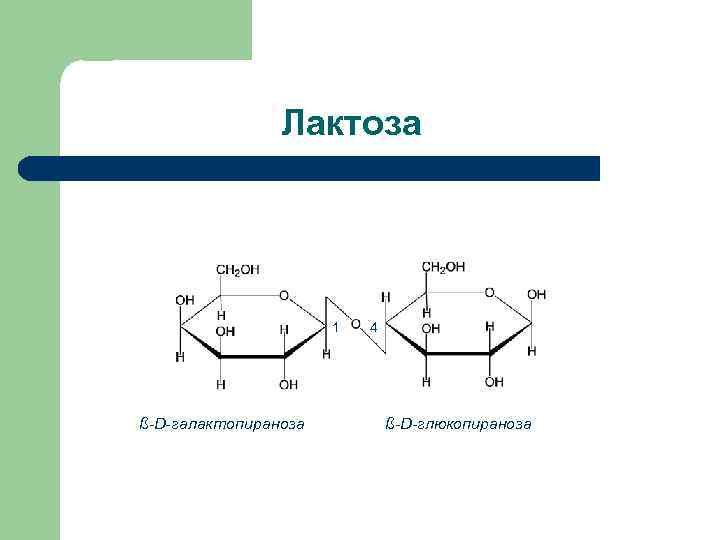 Лактоза 1 ß-D-галактопираноза 4 ß-D-глюкопираноза
Лактоза 1 ß-D-галактопираноза 4 ß-D-глюкопираноза
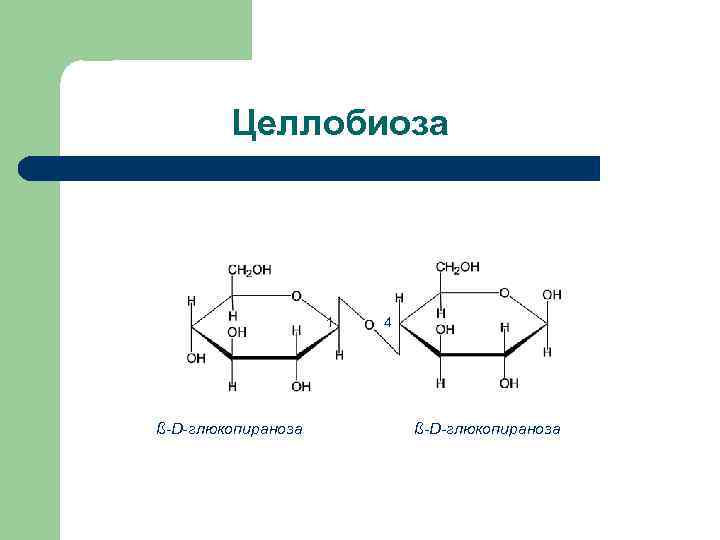 Целлобиоза 1 ß-D-глюкопираноза 4 ß-D-глюкопираноза
Целлобиоза 1 ß-D-глюкопираноза 4 ß-D-глюкопираноза
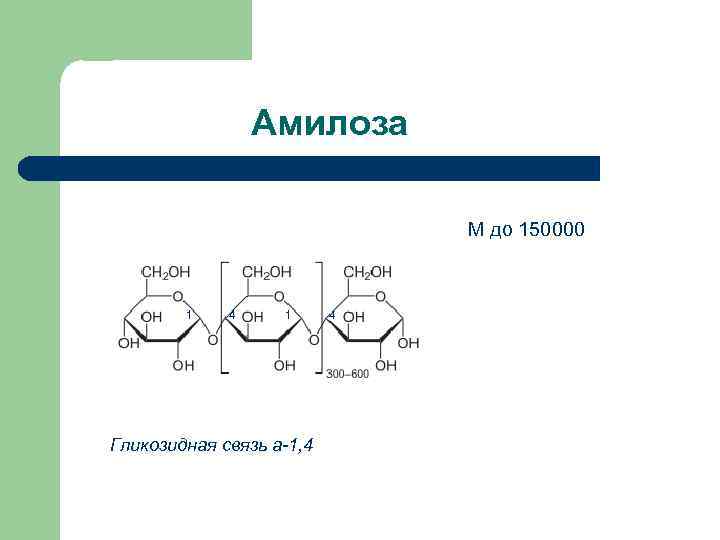 Амилоза М до 150000 1 4 1 Гликозидная связь а-1, 4 4
Амилоза М до 150000 1 4 1 Гликозидная связь а-1, 4 4
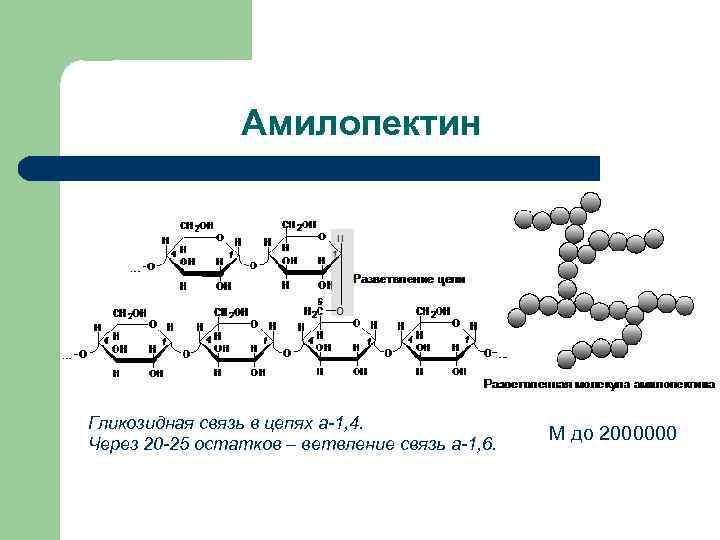 Амилопектин Гликозидная связь в цепях а-1, 4. Через 20 -25 остатков – ветвление связь а-1, 6. М до 2000000
Амилопектин Гликозидная связь в цепях а-1, 4. Через 20 -25 остатков – ветвление связь а-1, 6. М до 2000000
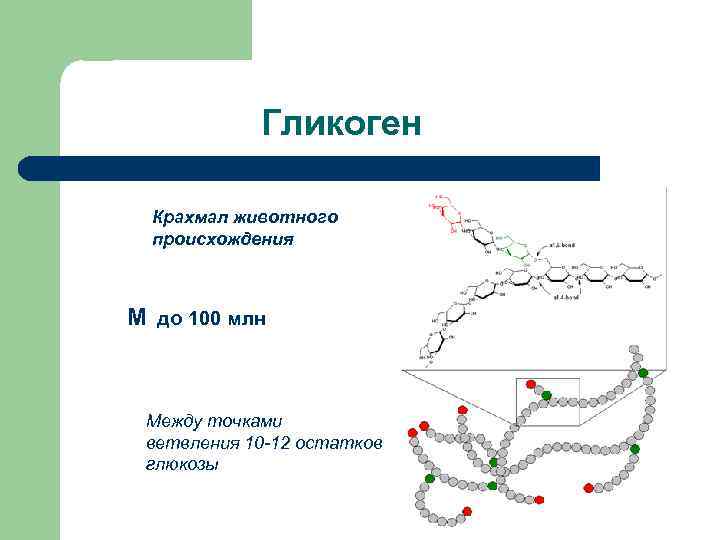 Гликоген Крахмал животного происхождения М до 100 млн Между точками ветвления 10 -12 остатков глюкозы
Гликоген Крахмал животного происхождения М до 100 млн Между точками ветвления 10 -12 остатков глюкозы
 Декстраны Природные полисахариды бактериального происхождения 1, 6 -гликозидные связи « Клинические декстраны» : - Полиглюкин 6 % раствор - Реополиглюкин 10 % раствор
Декстраны Природные полисахариды бактериального происхождения 1, 6 -гликозидные связи « Клинические декстраны» : - Полиглюкин 6 % раствор - Реополиглюкин 10 % раствор
 Гиалуроновая кислота 1 3 D-глюкуроновая кислота N- ацетил-D-глюкозамин
Гиалуроновая кислота 1 3 D-глюкуроновая кислота N- ацетил-D-глюкозамин
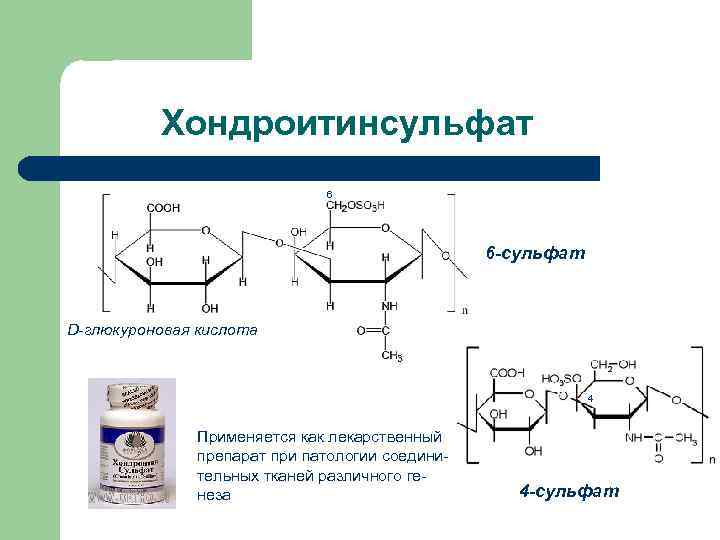 Хондроитинсульфат 6 6 -сульфат D-глюкуроновая кислота 4 Применяется как лекарственный препарат при патологии соединительных тканей различного генеза 4 -сульфат
Хондроитинсульфат 6 6 -сульфат D-глюкуроновая кислота 4 Применяется как лекарственный препарат при патологии соединительных тканей различного генеза 4 -сульфат
 Гепарин препятствует свертыванию крови. Растворим в физиологическом растворе. р. Н 1 -% раствора 6 -7, 5
Гепарин препятствует свертыванию крови. Растворим в физиологическом растворе. р. Н 1 -% раствора 6 -7, 5
 ДЕ 3. Школьный курс органической химии l l Модуль 1. Теория строения органических соединений. Модуль 2. Углеводороды. Модуль 3. Спирты и карбонильные соединения. Модуль 4. Азотсодержащие производные углеводородов (амины, аминокислоты, химические свойства).
ДЕ 3. Школьный курс органической химии l l Модуль 1. Теория строения органических соединений. Модуль 2. Углеводороды. Модуль 3. Спирты и карбонильные соединения. Модуль 4. Азотсодержащие производные углеводородов (амины, аминокислоты, химические свойства).
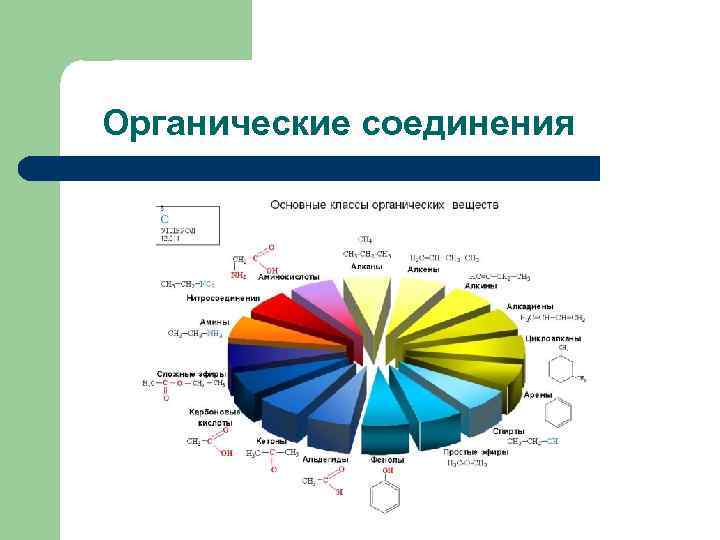 Органические соединения
Органические соединения
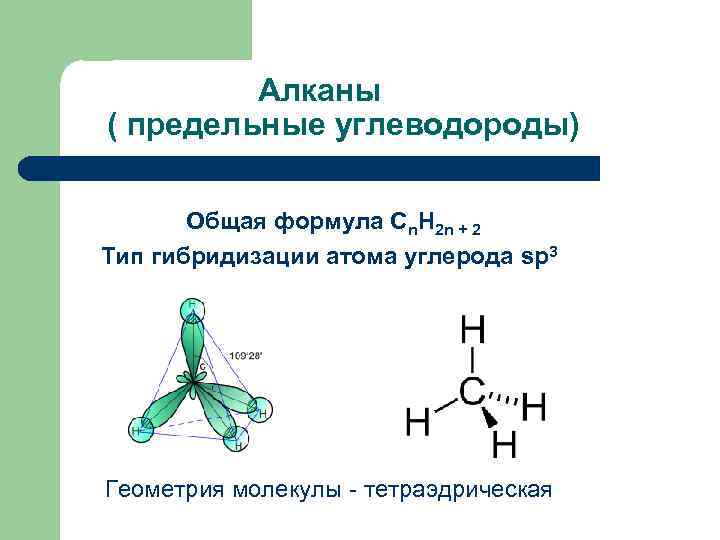 Алканы ( предельные углеводороды) Общая формула Сn. H 2 n + 2 Тип гибридизации атома углерода sp 3 Геометрия молекулы - тетраэдрическая
Алканы ( предельные углеводороды) Общая формула Сn. H 2 n + 2 Тип гибридизации атома углерода sp 3 Геометрия молекулы - тетраэдрическая
 Химические свойства алканов l l l l Большая химическая инертность. Устойчивость к действию кислот, щелочей и окислителей (бромная вода, перманганат калия) Горение на воздухе и в атмосфере кислорода Крекинг (термическое разложение при высокой температуре) Способность к реакциям замещения (радикальный м-зм) Изомеризация (начиная с бутана) Нитрование (реакция Коновалова) Дегидрирование
Химические свойства алканов l l l l Большая химическая инертность. Устойчивость к действию кислот, щелочей и окислителей (бромная вода, перманганат калия) Горение на воздухе и в атмосфере кислорода Крекинг (термическое разложение при высокой температуре) Способность к реакциям замещения (радикальный м-зм) Изомеризация (начиная с бутана) Нитрование (реакция Коновалова) Дегидрирование
 Реакция замещения Радикальный механизм: Обрыв цепи:
Реакция замещения Радикальный механизм: Обрыв цепи:
 Условия гомолитического разрыва связи (гомолиза) 1. Облучение 2. Высокая температура 3. Проведение реакции в газовой фазе Далее радикальные реагенты вызывают гомолитический разрыв связи в субстрате:
Условия гомолитического разрыва связи (гомолиза) 1. Облучение 2. Высокая температура 3. Проведение реакции в газовой фазе Далее радикальные реагенты вызывают гомолитический разрыв связи в субстрате:
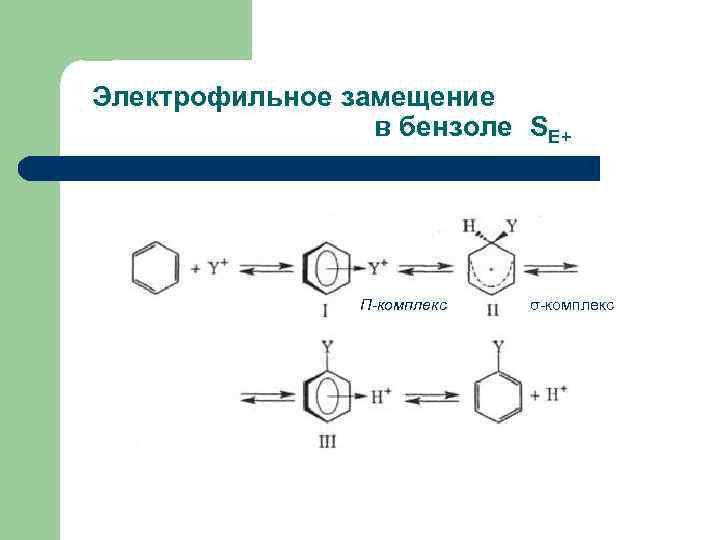 Электрофильное замещение в бензоле SE+ Π-комплекс σ-комплекс
Электрофильное замещение в бензоле SE+ Π-комплекс σ-комплекс
 Электрофильное присоединение в алкенах АЕ+ Присоединение галогенов: Присоединение галогеноводородов: Ионный механизм
Электрофильное присоединение в алкенах АЕ+ Присоединение галогенов: Присоединение галогеноводородов: Ионный механизм
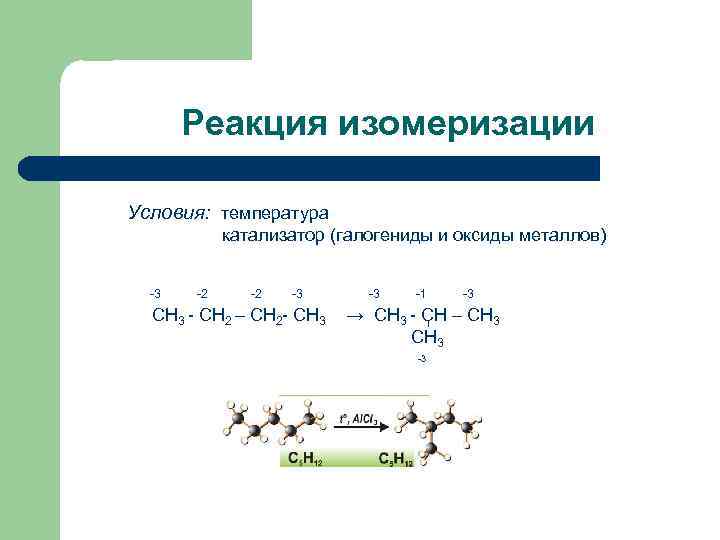 Реакция изомеризации Условия: температура катализатор (галогениды и оксиды металлов) -3 -2 -2 -3 СН 3 - СН 2 – СН 2 - СН 3 -3 -1 -3 → СН 3 - СН – СН 3 -3
Реакция изомеризации Условия: температура катализатор (галогениды и оксиды металлов) -3 -2 -2 -3 СН 3 - СН 2 – СН 2 - СН 3 -3 -1 -3 → СН 3 - СН – СН 3 -3
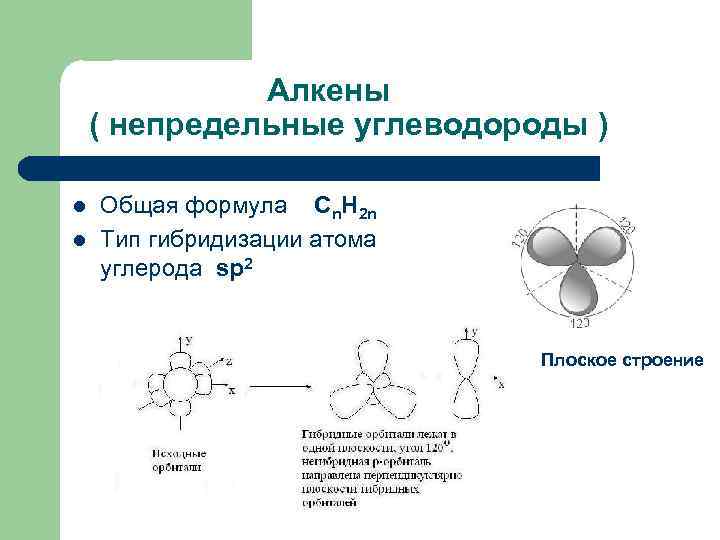 Алкены ( непредельные углеводороды ) l l Общая формула Сn. H 2 n Тип гибридизации атома углерода sр2 Плоское строение
Алкены ( непредельные углеводороды ) l l Общая формула Сn. H 2 n Тип гибридизации атома углерода sр2 Плоское строение
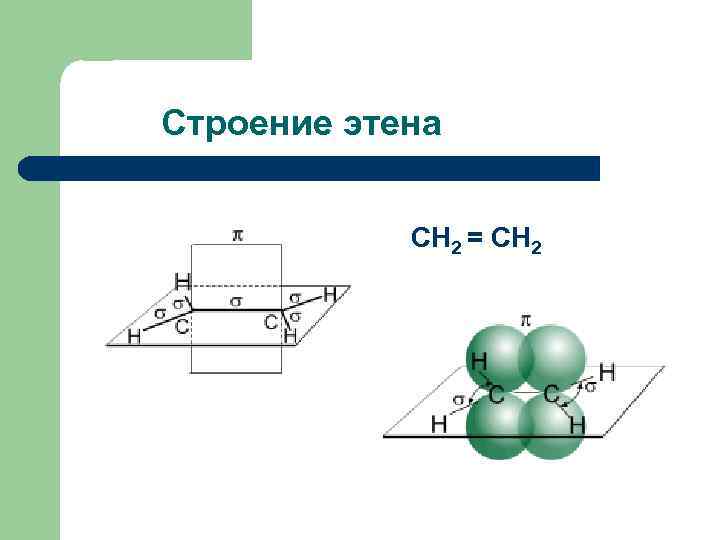 Строение этена СН 2 = СН 2
Строение этена СН 2 = СН 2
 Химические свойства алкенов 1. Присоединение водорода при повышенной t : 2. Присоединение галогенов: 3. Присоединение галогеноводородов: Ионный механизм АЕ
Химические свойства алкенов 1. Присоединение водорода при повышенной t : 2. Присоединение галогенов: 3. Присоединение галогеноводородов: Ионный механизм АЕ
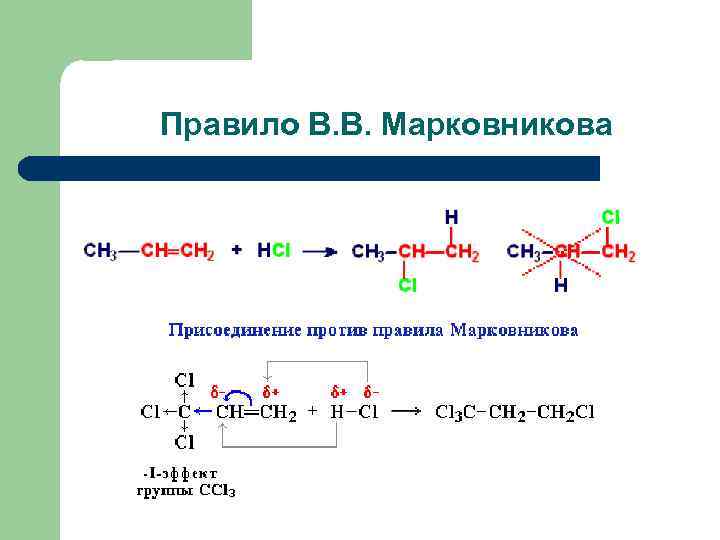 Правило В. В. Марковникова
Правило В. В. Марковникова
 Химические свойства алкенов 4. Присоединение воды (гидратация) 5. Окисление: 6. Горение: С 2 Н 4 + 3 О 2 = 2 СО 2 + 2 Н 2 О 7. Полимеризация:
Химические свойства алкенов 4. Присоединение воды (гидратация) 5. Окисление: 6. Горение: С 2 Н 4 + 3 О 2 = 2 СО 2 + 2 Н 2 О 7. Полимеризация:
 Диеновые углеводороды Общая формула Сn. H 2 n-2
Диеновые углеводороды Общая формула Сn. H 2 n-2
 Получение бутадиена Реакция С. В. Лебедева: 4500 С Al 2 O 3+ Zn. O
Получение бутадиена Реакция С. В. Лебедева: 4500 С Al 2 O 3+ Zn. O
 Алкины ( ацетиленовые углеводороды) l l Общая формула Сn. H 2 n-2 Тип гибридизации атома углерода sp Линейная молекула
Алкины ( ацетиленовые углеводороды) l l Общая формула Сn. H 2 n-2 Тип гибридизации атома углерода sp Линейная молекула
 Химические свойства алкинов 1. Гидрирование: Пропин Пропен Пропан 2. Галогенирование: Этин 1, 2 дибромэтен 3. Гидрогалогенирование: Этин Хлорэтен 1, 1, 2, 2 тетрабромэтан
Химические свойства алкинов 1. Гидрирование: Пропин Пропен Пропан 2. Галогенирование: Этин 1, 2 дибромэтен 3. Гидрогалогенирование: Этин Хлорэтен 1, 1, 2, 2 тетрабромэтан
 Химические свойства алкинов 4. Гидратация (реакция М. Г. Кучерова): Этин Виниловый спирт Этаналь 5. Окисление: Карбоновые кислоты Этандиовая кислота
Химические свойства алкинов 4. Гидратация (реакция М. Г. Кучерова): Этин Виниловый спирт Этаналь 5. Окисление: Карбоновые кислоты Этандиовая кислота
 Химические свойства алкинов 8. Реакции полимеризации: Винилацетилен 9. Реакции замещения с образованием ацетиленидов:
Химические свойства алкинов 8. Реакции полимеризации: Винилацетилен 9. Реакции замещения с образованием ацетиленидов:
 Реакции замещения в бензольном кольце l Заместители первого рода (ЭД): - NH 2 -OH l -CH 3 -Cl -Br -I Заместители второго рода (ЭА): — -NO 2 -C=N -SO 3 H - COOH
Реакции замещения в бензольном кольце l Заместители первого рода (ЭД): - NH 2 -OH l -CH 3 -Cl -Br -I Заместители второго рода (ЭА): — -NO 2 -C=N -SO 3 H - COOH
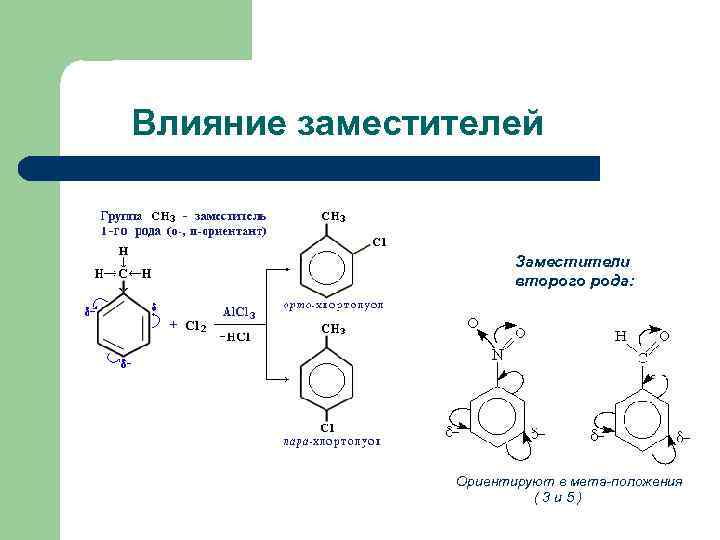 Влияние заместителей Заместители второго рода: Ориентируют в мета-положения (3 и 5)
Влияние заместителей Заместители второго рода: Ориентируют в мета-положения (3 и 5)
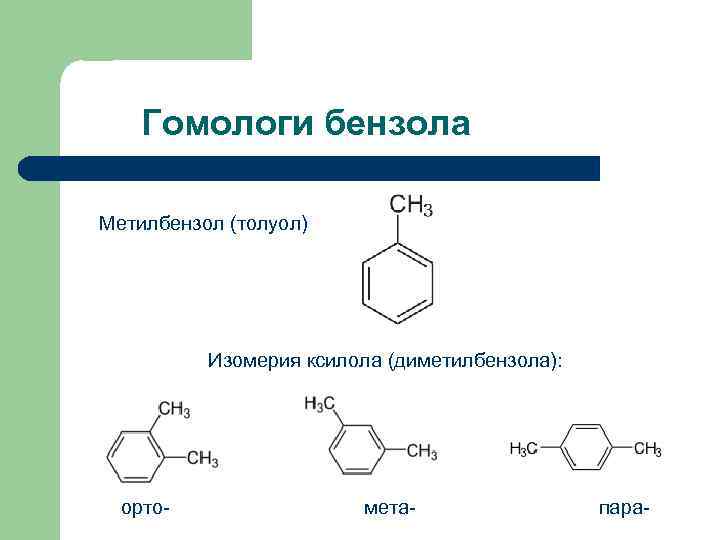 Гомологи бензола Метилбензол (толуол) Изомерия ксилола (диметилбензола): орто- мета- пара-
Гомологи бензола Метилбензол (толуол) Изомерия ксилола (диметилбензола): орто- мета- пара-
 Кислородсодержащие органические соединения Степень окисления углерода -2 0 +2
Кислородсодержащие органические соединения Степень окисления углерода -2 0 +2
 Спирты l Функциональная группа - ОН l Классификация спиртов: - одноатомные - двухатомные - трехатомные и многоатомные l Общая формула предельных одноатомных спиртов Сn. H 2 n+1 OH
Спирты l Функциональная группа - ОН l Классификация спиртов: - одноатомные - двухатомные - трехатомные и многоатомные l Общая формула предельных одноатомных спиртов Сn. H 2 n+1 OH
 Физические свойства спиртов l l Низшие спирты (до С 12) жидкости с характерным запахом спирта, высшие – твердые вещества без запаха. Плотность жидких спиртов меньше воды, т. е. меньше 1 г/мл Низшие спирты (до С 3) хорошо смешиваются с водой , что объясняется возникновением водородных связей, далее – растворимость падает. Молекулы спирта также ассоциированы за счет водородных связей
Физические свойства спиртов l l Низшие спирты (до С 12) жидкости с характерным запахом спирта, высшие – твердые вещества без запаха. Плотность жидких спиртов меньше воды, т. е. меньше 1 г/мл Низшие спирты (до С 3) хорошо смешиваются с водой , что объясняется возникновением водородных связей, далее – растворимость падает. Молекулы спирта также ассоциированы за счет водородных связей
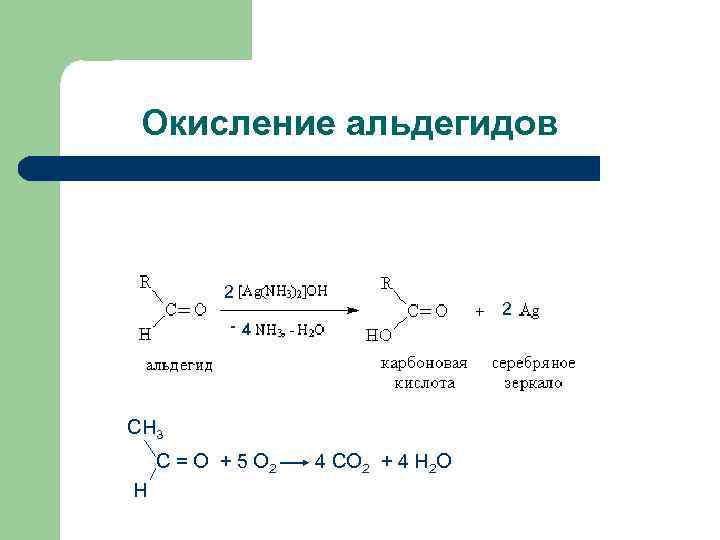 Окисление альдегидов 2 2 -4 СН 3 С = О + 5 О 2 Н 4 СО 2 + 4 Н 2 О
Окисление альдегидов 2 2 -4 СН 3 С = О + 5 О 2 Н 4 СО 2 + 4 Н 2 О
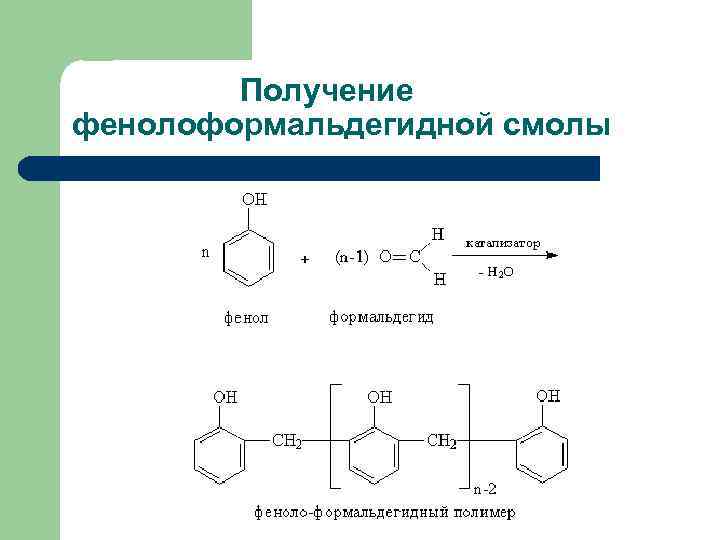 Получение фенолоформальдегидной смолы
Получение фенолоформальдегидной смолы
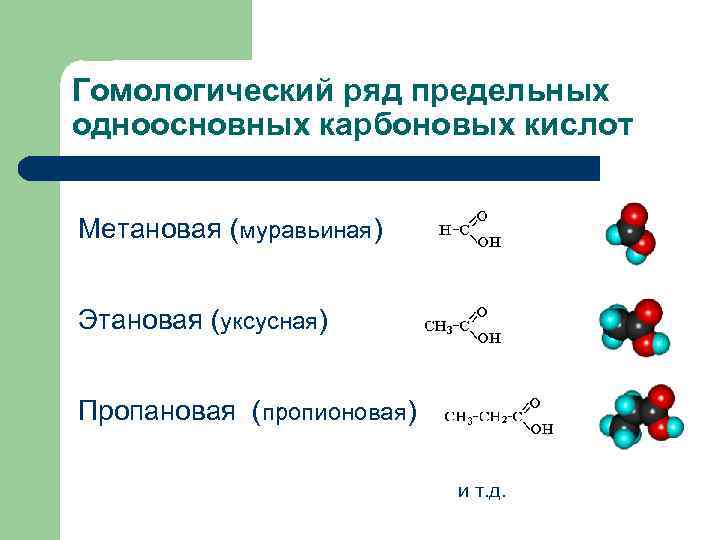 Гомологический ряд предельных одноосновных карбоновых кислот Метановая (муравьиная) Этановая (уксусная) Пропановая (пропионовая) и т. д.
Гомологический ряд предельных одноосновных карбоновых кислот Метановая (муравьиная) Этановая (уксусная) Пропановая (пропионовая) и т. д.
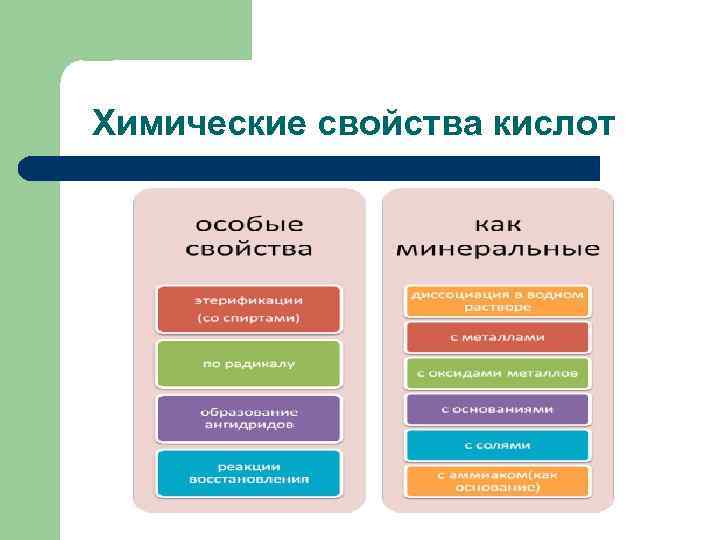 Химические свойства кислот
Химические свойства кислот
 ДЕ 4. Школьный курс неорганической химии l l l Модуль 1. Строение атома Модуль 2. Химическая связь. Модуль 3. Классы неорганических соединений. Гидролиз солей.
ДЕ 4. Школьный курс неорганической химии l l l Модуль 1. Строение атома Модуль 2. Химическая связь. Модуль 3. Классы неорганических соединений. Гидролиз солей.
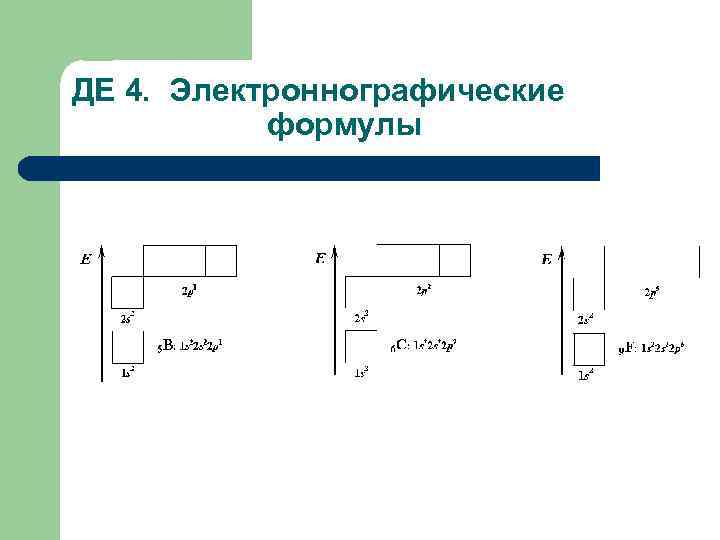 ДЕ 4. Электроннографические формулы
ДЕ 4. Электроннографические формулы
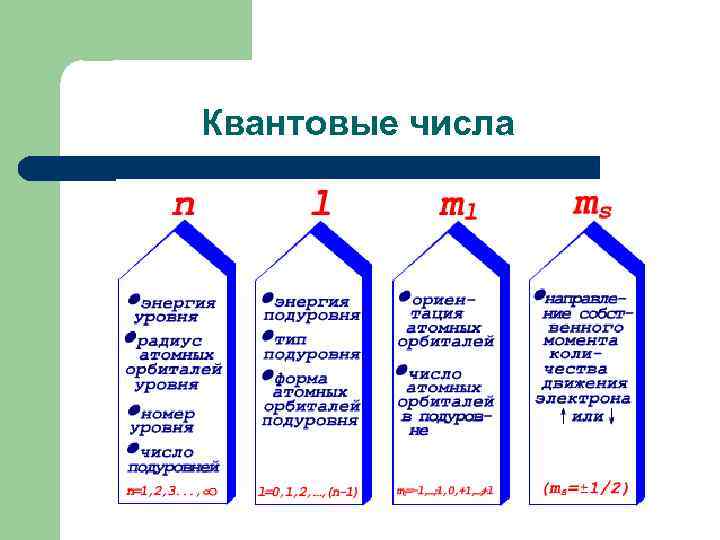 Квантовые числа
Квантовые числа
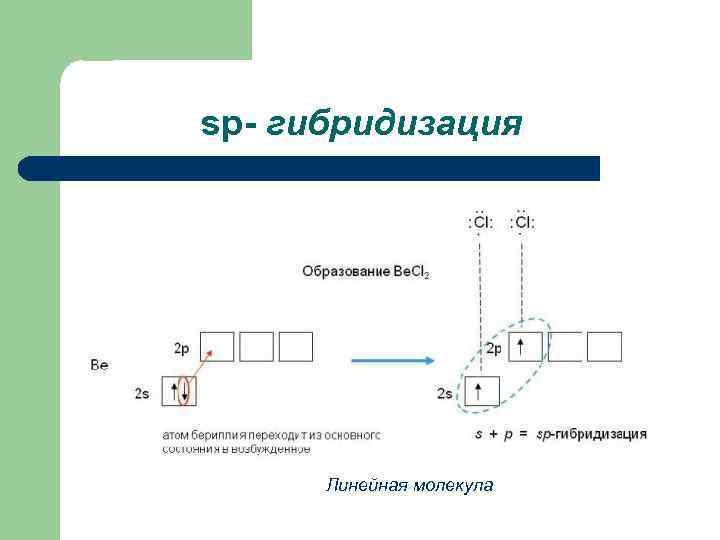 sp- гибридизация Линейная молекула
sp- гибридизация Линейная молекула
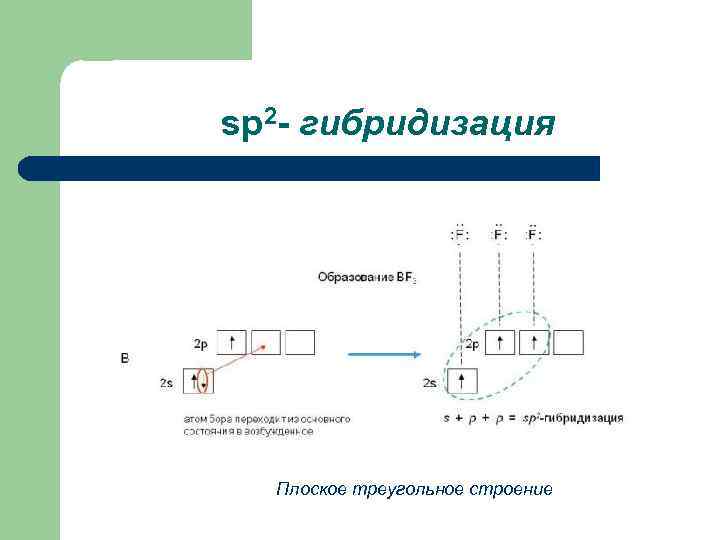 sp 2 - гибридизация Плоское треугольное строение
sp 2 - гибридизация Плоское треугольное строение
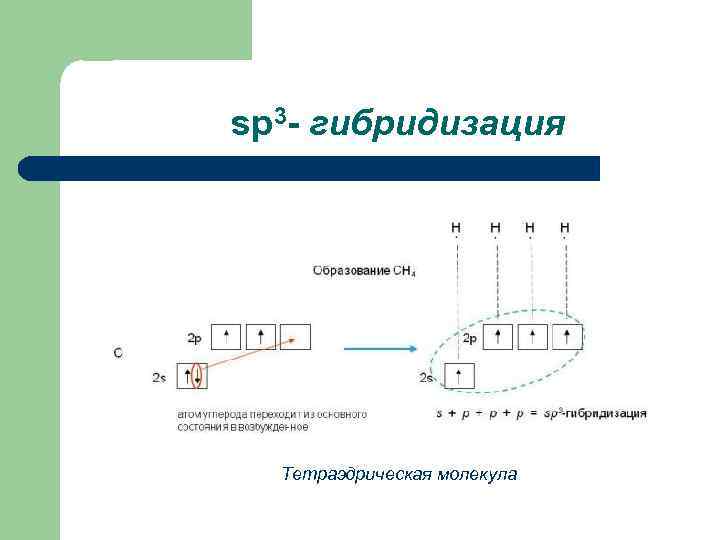 sp 3 - гибридизация Тетраэдрическая молекула
sp 3 - гибридизация Тетраэдрическая молекула
 Виды связей l l l Ковалентная неполярная Ковалентная полярная Ионная Водородная Металлическая
Виды связей l l l Ковалентная неполярная Ковалентная полярная Ионная Водородная Металлическая
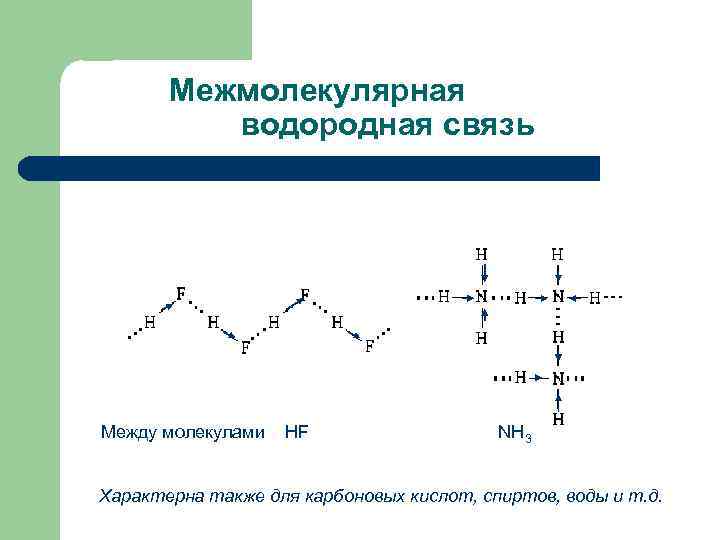 Межмолекулярная водородная связь Между молекулами HF NH 3 Характерна также для карбоновых кислот, спиртов, воды и т. д.
Межмолекулярная водородная связь Между молекулами HF NH 3 Характерна также для карбоновых кислот, спиртов, воды и т. д.
 Классификация веществ
Классификация веществ
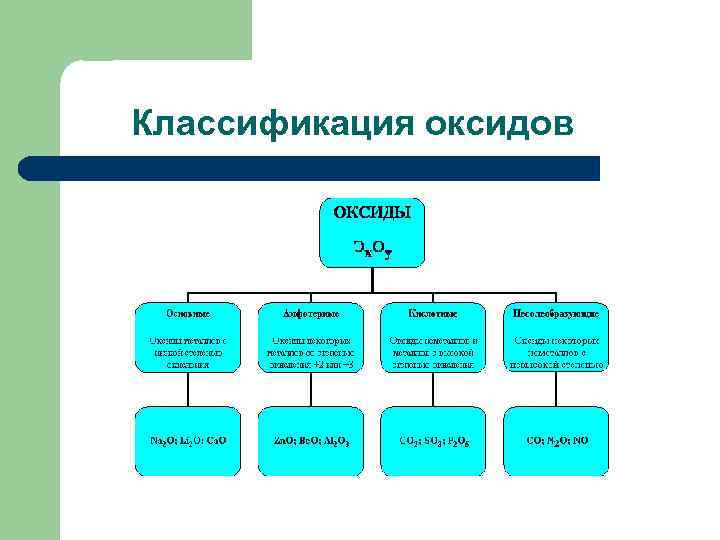 Классификация оксидов
Классификация оксидов
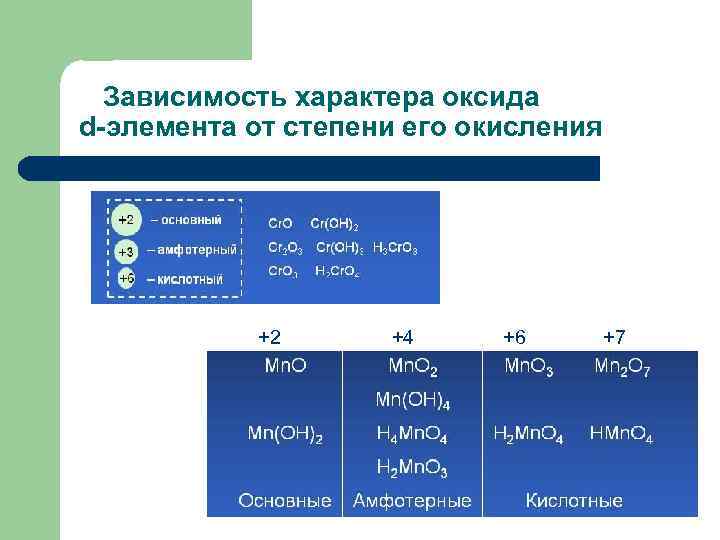 Зависимость характера оксида d-элемента от степени его окисления +2 +4 +6 +7
Зависимость характера оксида d-элемента от степени его окисления +2 +4 +6 +7
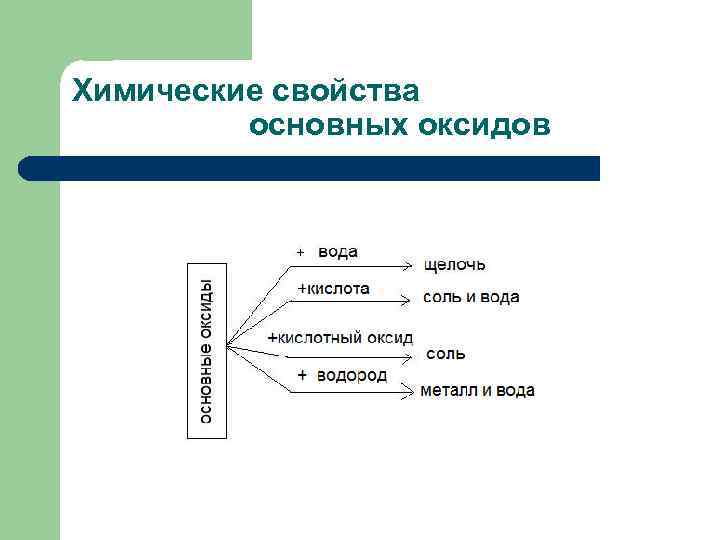 Химические свойства основных оксидов
Химические свойства основных оксидов
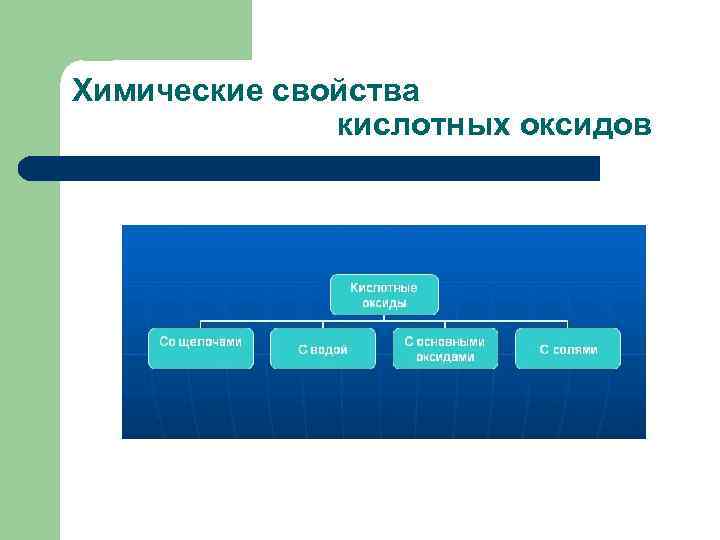 Химические свойства кислотных оксидов
Химические свойства кислотных оксидов
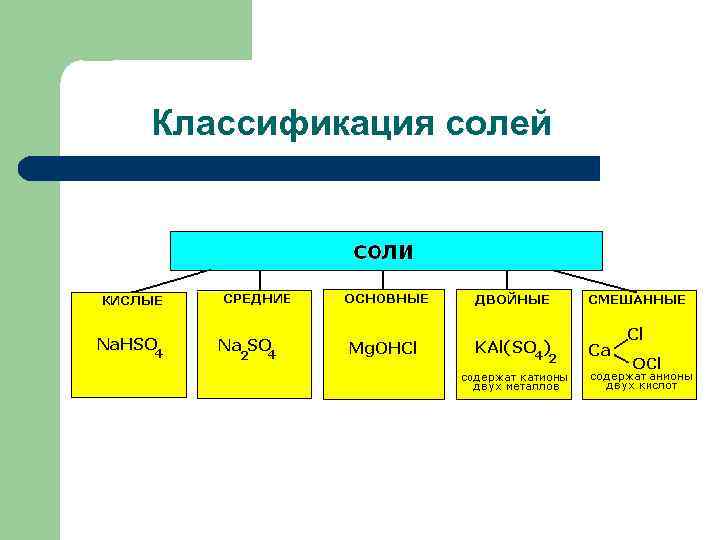 Классификация солей
Классификация солей
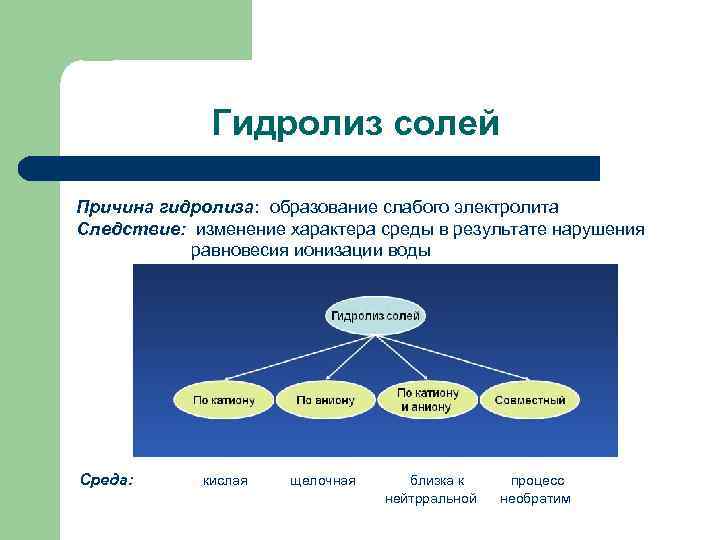 Гидролиз солей Причина гидролиза: образование слабого электролита Следствие: изменение характера среды в результате нарушения равновесия ионизации воды Среда: кислая щелочная близка к нейтрральной процесс необратим
Гидролиз солей Причина гидролиза: образование слабого электролита Следствие: изменение характера среды в результате нарушения равновесия ионизации воды Среда: кислая щелочная близка к нейтрральной процесс необратим
 Взаимодействие солей с водой ( гидролиз ) Гидролиз по катиону: Среда кислая Гидролиз по аниону: Среда щелочная Гидролиз по катиону и аниону: Среда близкая к нейтральной
Взаимодействие солей с водой ( гидролиз ) Гидролиз по катиону: Среда кислая Гидролиз по аниону: Среда щелочная Гидролиз по катиону и аниону: Среда близкая к нейтральной
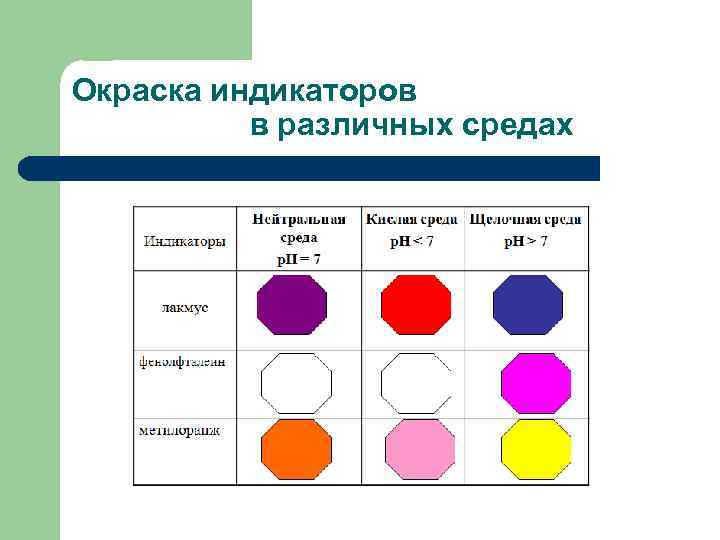 Окраска индикаторов в различных средах
Окраска индикаторов в различных средах
 Гидролиз соли по аниону 1. Диссоциация соли: Na. NO 2 Na+ + NO 2 - 2. Ионное уравнение: 3. Молекулярное уравнение: Среда раствора щелочная, лакмус – синий, фенолфталеин -малиновый
Гидролиз соли по аниону 1. Диссоциация соли: Na. NO 2 Na+ + NO 2 - 2. Ионное уравнение: 3. Молекулярное уравнение: Среда раствора щелочная, лакмус – синий, фенолфталеин -малиновый
 Гидролиз соли по катиону Fe. Cl 3 Fe 3+ + 3 Cl- 1 стадия: 2 стадия: З стадия: Среда раствора – кислая, лакмус – красный, метилоранж - красный
Гидролиз соли по катиону Fe. Cl 3 Fe 3+ + 3 Cl- 1 стадия: 2 стадия: З стадия: Среда раствора – кислая, лакмус – красный, метилоранж - красный
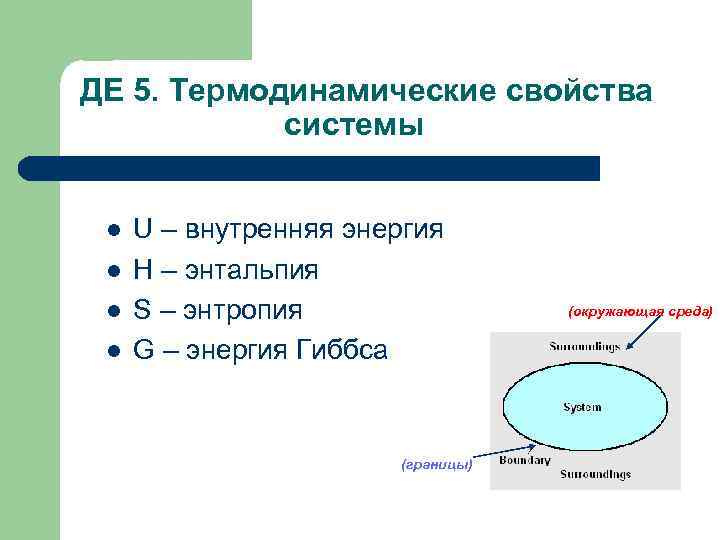 ДЕ 5. Термодинамические свойства системы l l U – внутренняя энергия Н – энтальпия S – энтропия G – энергия Гиббса (границы) (окружающая среда)
ДЕ 5. Термодинамические свойства системы l l U – внутренняя энергия Н – энтальпия S – энтропия G – энергия Гиббса (границы) (окружающая среда)
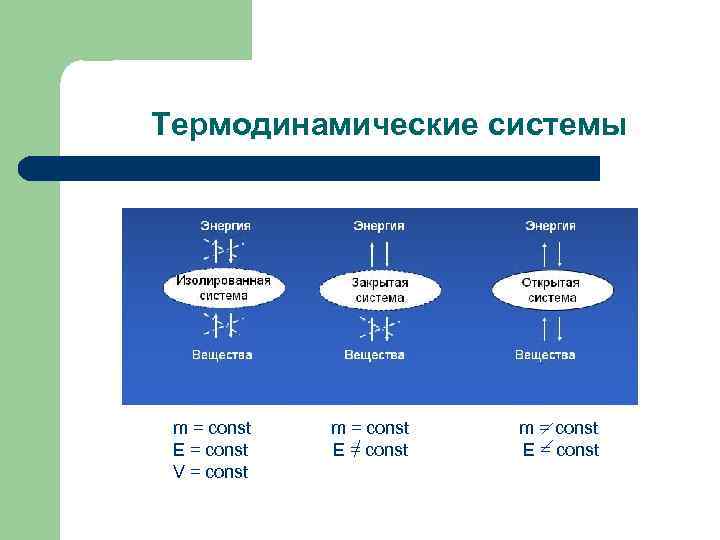 Термодинамические системы m = const E = const V = const m = const E = const
Термодинамические системы m = const E = const V = const m = const E = const
 Первый закон термодинамики Тепло, подводимое к системе, расходуется ею на увеличение внутренней энергии и на совершение работы
Первый закон термодинамики Тепло, подводимое к системе, расходуется ею на увеличение внутренней энергии и на совершение работы
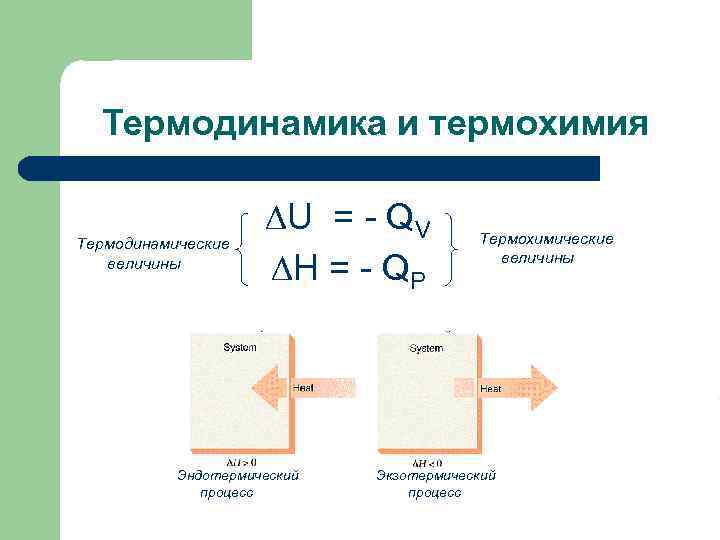 Термодинамика и термохимия Термодинамические величины ∆U = - QV ∆H = - QP Эндотермический процесс Термохимические величины Экзотермический процесс
Термодинамика и термохимия Термодинамические величины ∆U = - QV ∆H = - QP Эндотермический процесс Термохимические величины Экзотермический процесс
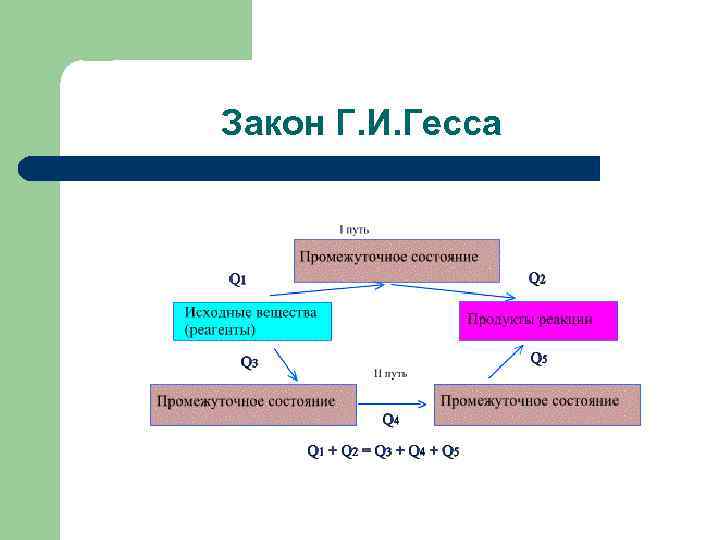 Закон Г. И. Гесса
Закон Г. И. Гесса
 Первое следствие l Закон Лавуазье- Лапласа: Энтальпия разложения химического соединения равна по величине и противоположна по знаку энтальпии его образования из продуктов разложения ∆Нобр. = - ∆Нразл.
Первое следствие l Закон Лавуазье- Лапласа: Энтальпия разложения химического соединения равна по величине и противоположна по знаку энтальпии его образования из продуктов разложения ∆Нобр. = - ∆Нразл.
 Второе следствие l Изменение энтальпии химической реакции равно разности между суммой энтальпий образования продуктов реакции и суммой энтальпий образования исходных веществ (с учетом стехиометрических коэффициентов)
Второе следствие l Изменение энтальпии химической реакции равно разности между суммой энтальпий образования продуктов реакции и суммой энтальпий образования исходных веществ (с учетом стехиометрических коэффициентов)
 Третье следствие l Изменение энтальпии химической реакции равно разности между суммой энтальпий сгорания исходных веществ и суммой энтальпий сгорания продуктов реакции (с учетом стехиометрических коэффициентов) ( combustion – сгорание)
Третье следствие l Изменение энтальпии химической реакции равно разности между суммой энтальпий сгорания исходных веществ и суммой энтальпий сгорания продуктов реакции (с учетом стехиометрических коэффициентов) ( combustion – сгорание)
 Второй закон термодинамики Теплота не может самопроизвольно (без компенсации) передаваться от тела менее нагретого к телу более нагретому Т 1 > Т 2
Второй закон термодинамики Теплота не может самопроизвольно (без компенсации) передаваться от тела менее нагретого к телу более нагретому Т 1 > Т 2
 Энергия Гиббса ∆G < 0 - реакция экзэргоническая ∆G > 0 - реакция эндэргоническая
Энергия Гиббса ∆G < 0 - реакция экзэргоническая ∆G > 0 - реакция эндэргоническая
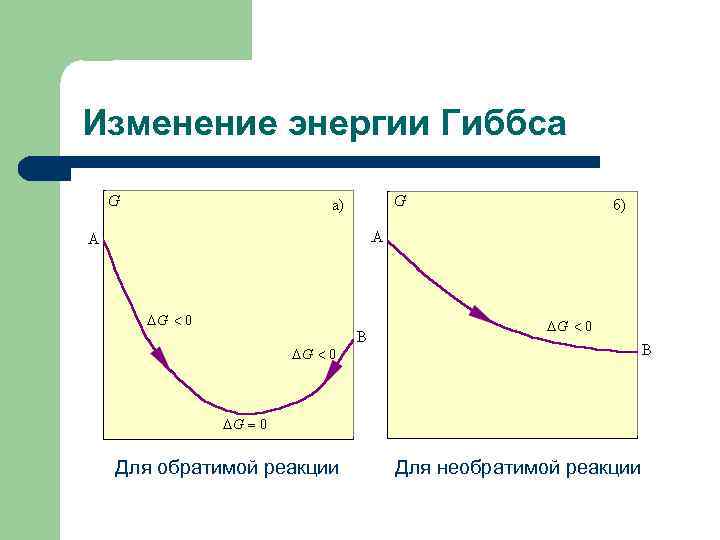 Изменение энергии Гиббса Для обратимой реакции Для необратимой реакции
Изменение энергии Гиббса Для обратимой реакции Для необратимой реакции
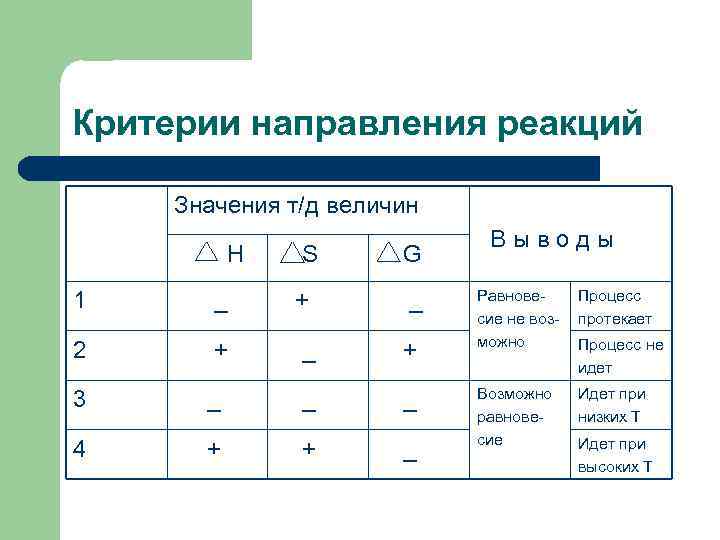 Критерии направления реакций Значения т/д величин Н S G 1 _ + _ 2 + _ + 3 _ _ _ 4 + + _ Выводы Равновесие не возможно Процесс протекает Возможно равновесие Идет при низких Т Процесс не идет Идет при высоких Т
Критерии направления реакций Значения т/д величин Н S G 1 _ + _ 2 + _ + 3 _ _ _ 4 + + _ Выводы Равновесие не возможно Процесс протекает Возможно равновесие Идет при низких Т Процесс не идет Идет при высоких Т
 Химическая кинетика Скорость химической реакции: Факторы, от которых зависит скорость химической реакции: - Природа реагирующих веществ - Концентрация реагирующих веществ - Температура - Характер среды - Катализатор
Химическая кинетика Скорость химической реакции: Факторы, от которых зависит скорость химической реакции: - Природа реагирующих веществ - Концентрация реагирующих веществ - Температура - Характер среды - Катализатор
 Закон действующих масс
Закон действующих масс
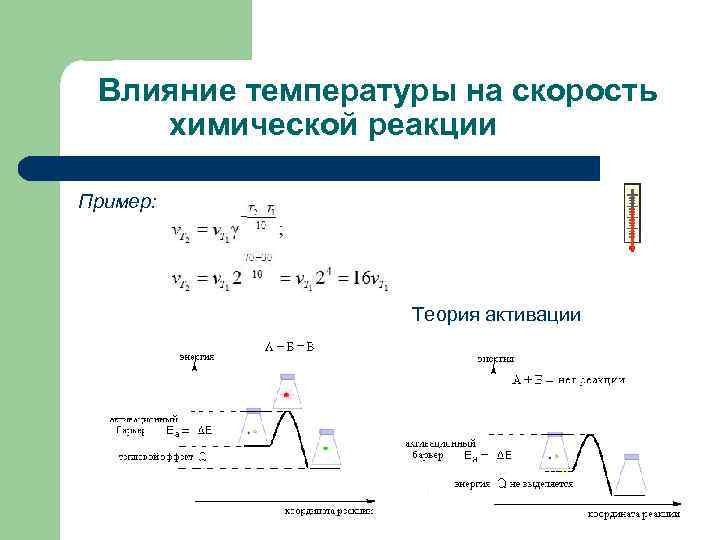 Влияние температуры на скорость химической реакции Пример: Теория активации
Влияние температуры на скорость химической реакции Пример: Теория активации
 Константа химического равновесия
Константа химического равновесия
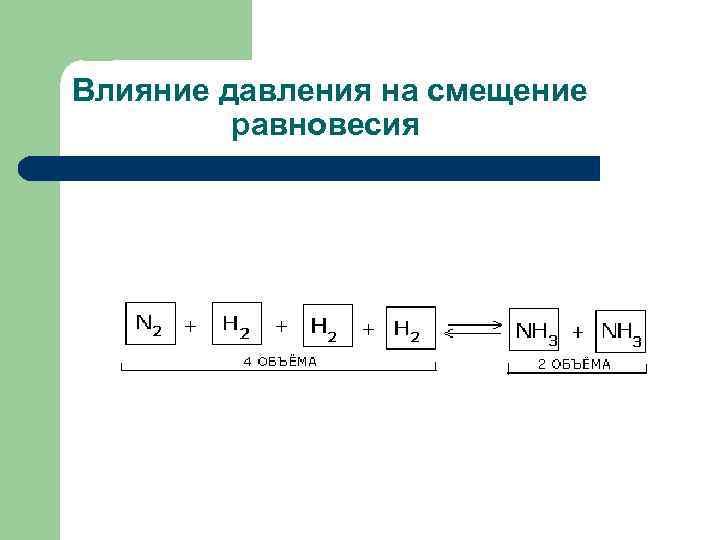 Влияние давления на смещение равновесия
Влияние давления на смещение равновесия
 Смещение химического равновесия
Смещение химического равновесия
 Химическое равновесие в системе СО 2(г) + С(тв) 2 СО(г) – Q сместится вправо при 1) повышении давления 2) понижении температуры 3) повышении концентрации СО 4) повышении температуры
Химическое равновесие в системе СО 2(г) + С(тв) 2 СО(г) – Q сместится вправо при 1) повышении давления 2) понижении температуры 3) повышении концентрации СО 4) повышении температуры
 Равновесие в системе N 2+ O 2 ↔ 2 NO – Q будет смещаться в сторону продуктов при l l 1. увеличении концентрации кислорода 2. увеличении давления 3. уменьшении давления 4. понижении температуры
Равновесие в системе N 2+ O 2 ↔ 2 NO – Q будет смещаться в сторону продуктов при l l 1. увеличении концентрации кислорода 2. увеличении давления 3. уменьшении давления 4. понижении температуры
 На смещение равновесия в системе N 2 + 3 H 2 ↔ 2 NH 3 + Q не влияет l l 1. понижение температуры 2. повышение давления 3. удаление аммиака из зоны реакции 4. применение катализатора
На смещение равновесия в системе N 2 + 3 H 2 ↔ 2 NH 3 + Q не влияет l l 1. понижение температуры 2. повышение давления 3. удаление аммиака из зоны реакции 4. применение катализатора
 ДЕ 6. Концентрация растворов l Массовая доля l Молярная концентрация эквивалента Титр Моляльная концентрация l l l С = m/M • V, моль/л Сэ = m/Mэ • V, моль экв. / л , г/мл , моль/кг l Мольная доля
ДЕ 6. Концентрация растворов l Массовая доля l Молярная концентрация эквивалента Титр Моляльная концентрация l l l С = m/M • V, моль/л Сэ = m/Mэ • V, моль экв. / л , г/мл , моль/кг l Мольная доля
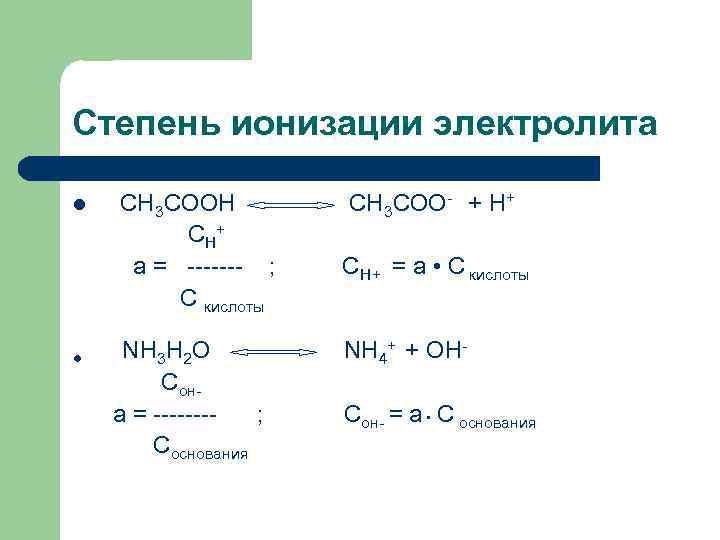 Степень ионизации электролита l l СН 3 СООН С Н+ а = ------- ; С кислоты NH 3 H 2 O Сона = -------; Соснования СН 3 СОО- + Н+ СН+ = а • С кислоты NH 4+ + OHСон- = а • С основания
Степень ионизации электролита l l СН 3 СООН С Н+ а = ------- ; С кислоты NH 3 H 2 O Сона = -------; Соснования СН 3 СОО- + Н+ СН+ = а • С кислоты NH 4+ + OHСон- = а • С основания
 Факторы, от которых зависит степень ионизации l l l Природа электролита Природа растворителя Концентрация электролита Температура Наличие одноименных ионов + уксусная к-та + метилоранж ← + ацетат натрия СН 3 СООН ↔ СН 3 СОО- + Н+ СН 3 СООNa → CH 3 COO- + Na+
Факторы, от которых зависит степень ионизации l l l Природа электролита Природа растворителя Концентрация электролита Температура Наличие одноименных ионов + уксусная к-та + метилоранж ← + ацетат натрия СН 3 СООН ↔ СН 3 СОО- + Н+ СН 3 СООNa → CH 3 COO- + Na+
 Закон разведения Оствальда КА ↔ К+ + АКонстанта ионизации электролита зависит от природы электролита и растворителя, а также от температуры. Немецкий химик Фридрих Вильгельм Оствальд 1853 -1932
Закон разведения Оствальда КА ↔ К+ + АКонстанта ионизации электролита зависит от природы электролита и растворителя, а также от температуры. Немецкий химик Фридрих Вильгельм Оствальд 1853 -1932
 Теория растворов сильных электролитов Ионная сила раствора – величина, характеризую- щая интенсивность электростатического поля всех ионов: Понятие ионной силы введено американским физико-химиком Гилбертом Льюисом в 1907 году Ионная сила плазмы крови I = 0, 15
Теория растворов сильных электролитов Ионная сила раствора – величина, характеризую- щая интенсивность электростатического поля всех ионов: Понятие ионной силы введено американским физико-химиком Гилбертом Льюисом в 1907 году Ионная сила плазмы крови I = 0, 15
 Расчет водородного показателя р. Н = -lg CН+ Электролиты Сильные p. H = p. Cк-ты Слабые p. H = p. Cк-ты +рα р. Н = ½ (p. Cк-ты + рka)
Расчет водородного показателя р. Н = -lg CН+ Электролиты Сильные p. H = p. Cк-ты Слабые p. H = p. Cк-ты +рα р. Н = ½ (p. Cк-ты + рka)
 250 С Шкала показателей водных сред С Н+ 100 10 -3 10 -7 10 -11 10 -14 СОН- 10 -14 10 -11 10 -7 10 -4 100 р. Н 0 3 7 11 14 р. ОН 14 11 7 3 0 Среда Кислая Нейтральная Щелочная
250 С Шкала показателей водных сред С Н+ 100 10 -3 10 -7 10 -11 10 -14 СОН- 10 -14 10 -11 10 -7 10 -4 100 р. Н 0 3 7 11 14 р. ОН 14 11 7 3 0 Среда Кислая Нейтральная Щелочная
![Расчет осмотического давления R= 8. 31 Дж/моль • К [П] к. Па R = Расчет осмотического давления R= 8. 31 Дж/моль • К [П] к. Па R =](https://present5.com/presentation/180690043_148020338/image-124.jpg) Расчет осмотического давления R= 8. 31 Дж/моль • К [П] к. Па R = 0. 082 л • атм/ моль • К [П] атм Для растворов электролитов: i = 1 + a(n-1)
Расчет осмотического давления R= 8. 31 Дж/моль • К [П] к. Па R = 0. 082 л • атм/ моль • К [П] атм Для растворов электролитов: i = 1 + a(n-1)
 Осмотическое давление биологических жидкостей l l Плазма крови Цельная кровь Спинно-мозговая жидкость Слезная жидкость 7, 40 атм 7, 63 атм 6, 86 атм 10, 80 атм
Осмотическое давление биологических жидкостей l l Плазма крови Цельная кровь Спинно-мозговая жидкость Слезная жидкость 7, 40 атм 7, 63 атм 6, 86 атм 10, 80 атм
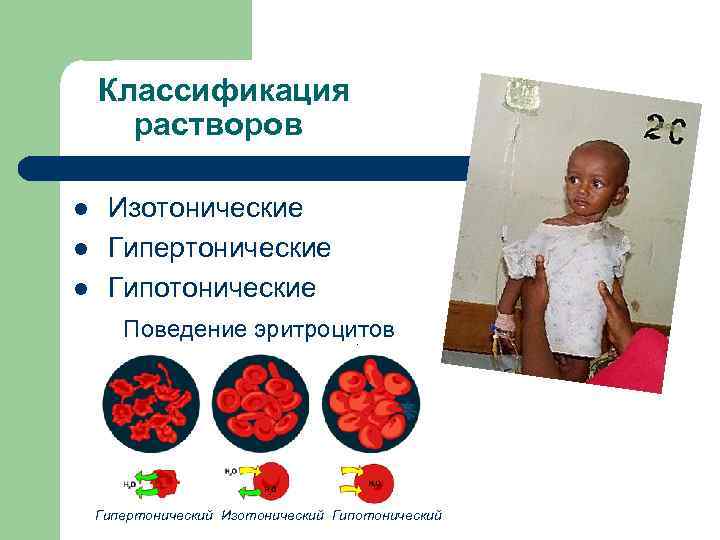 Классификация растворов l l l Изотонические Гипертонические Гипотонические Поведение эритроцитов Гипертонический Изотонический Гипотонический
Классификация растворов l l l Изотонические Гипертонические Гипотонические Поведение эритроцитов Гипертонический Изотонический Гипотонический
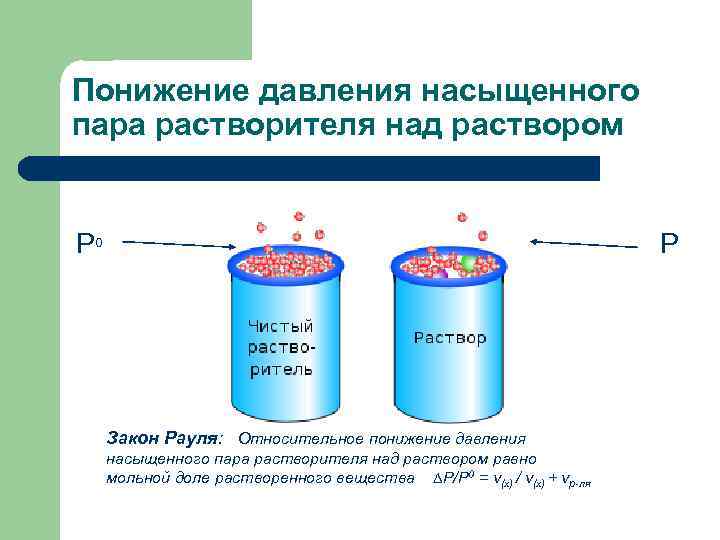 Понижение давления насыщенного пара растворителя над раствором Р 0 P Закон Рауля: Относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества ∆Р/Р 0 = ν(х) / ν(х) + νр-ля
Понижение давления насыщенного пара растворителя над раствором Р 0 P Закон Рауля: Относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества ∆Р/Р 0 = ν(х) / ν(х) + νр-ля
 ДЕ 7. Окислительно-восстановительные реакции Окислитель + Восстановитель Восстановленная форма ок-ля + Окисленная форма восс-ля
ДЕ 7. Окислительно-восстановительные реакции Окислитель + Восстановитель Восстановленная форма ок-ля + Окисленная форма восс-ля
 Расчет степени окисления
Расчет степени окисления
 Примеры окислителей l Атомы или молекулы сильно электроотрицательных элементов : F 2 O 2 Cl 2 N 2 S l Сложные анионы, содержащие элемент в высшей положительной степени окисления: Mn. O 4 - NO 3 - SO 42 Cl. O 4 - Cr. O 42 - Cr 2 O 72 - • Простые катионы с высокими зарядами: Fe 3+ Cu 2+ Sn 4+ Pb 4+ Hg 2+
Примеры окислителей l Атомы или молекулы сильно электроотрицательных элементов : F 2 O 2 Cl 2 N 2 S l Сложные анионы, содержащие элемент в высшей положительной степени окисления: Mn. O 4 - NO 3 - SO 42 Cl. O 4 - Cr. O 42 - Cr 2 O 72 - • Простые катионы с высокими зарядами: Fe 3+ Cu 2+ Sn 4+ Pb 4+ Hg 2+
 Примеры восстановителей l l Атомы электроположительных элементов (атомы щелочных и щелочно-земельных металлов) Na Li K Ba Ca Sr Простые отрицательно заряженные ионы: Cl- S 2 - Br- JПростые катионы с низкими зарядами: Fe 2+ Cu+ Sn 2+ Pb 2+ Hg+ Водород, гидриды ( Н-), углерод, оксид углерода (+2)
Примеры восстановителей l l Атомы электроположительных элементов (атомы щелочных и щелочно-земельных металлов) Na Li K Ba Ca Sr Простые отрицательно заряженные ионы: Cl- S 2 - Br- JПростые катионы с низкими зарядами: Fe 2+ Cu+ Sn 2+ Pb 2+ Hg+ Водород, гидриды ( Н-), углерод, оксид углерода (+2)
 Примеры веществ с двойственными свойствами S 2 - +6 е -2 NH 4 -3 SO 32 - - 2 е SO 42 - +4 +6 e NO 2+3 +6 -2 e NO 3+5
Примеры веществ с двойственными свойствами S 2 - +6 е -2 NH 4 -3 SO 32 - - 2 е SO 42 - +4 +6 e NO 2+3 +6 -2 e NO 3+5
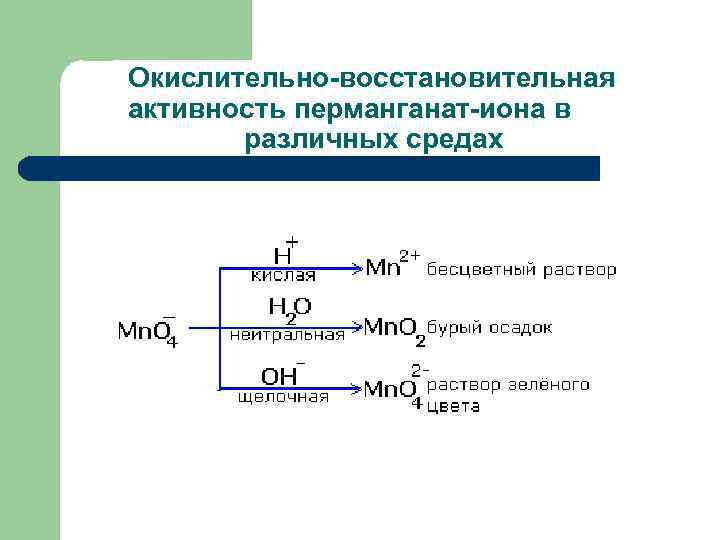 Окислительно-восстановительная активность перманганат-иона в различных средах
Окислительно-восстановительная активность перманганат-иона в различных средах
 Виды коррозии по механизму l l l Химическая коррозия Электрохимическая коррозия Биологическая коррозия
Виды коррозии по механизму l l l Химическая коррозия Электрохимическая коррозия Биологическая коррозия
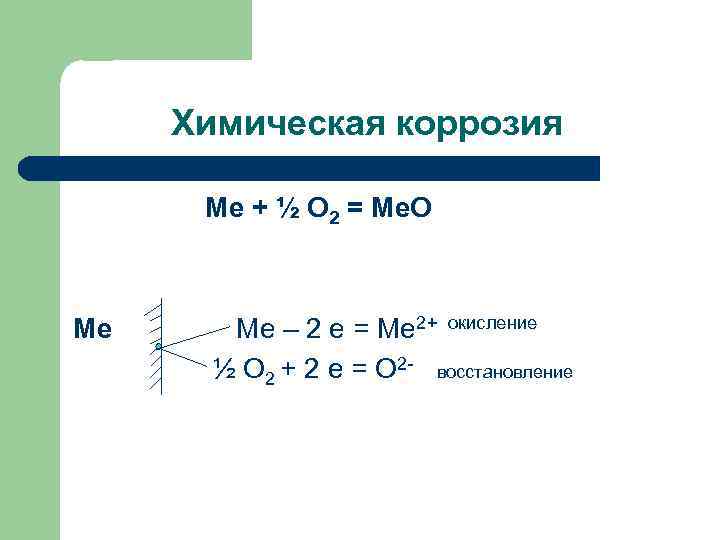 Химическая коррозия Ме + ½ О 2 = Ме. О Ме Ме – 2 е = Ме 2+ окисление ½ О 2 + 2 е = О 2 - восстановление
Химическая коррозия Ме + ½ О 2 = Ме. О Ме Ме – 2 е = Ме 2+ окисление ½ О 2 + 2 е = О 2 - восстановление
 Электрохимическая коррозия Электролит ( Н+, О 2, Н 2 О ) М е Ме – 2 е = Ме 2+ окисление 2 Н+ + 2 е = Н 2 восстановление Металл
Электрохимическая коррозия Электролит ( Н+, О 2, Н 2 О ) М е Ме – 2 е = Ме 2+ окисление 2 Н+ + 2 е = Н 2 восстановление Металл
 Уравнения возможных катодных процессов в полости рта l l 2 Н 2 О + 2 е = Н 2 + 2 ОН- (1) 2 Н+ + 2 е = Н 2 (2) водородная О 2 + 2 Н 2 О + 4 е = 4 ОН- (3) О 2 + 4 Н+ + 4 е = 2 Н 2 О (4) кислородная деполяризация
Уравнения возможных катодных процессов в полости рта l l 2 Н 2 О + 2 е = Н 2 + 2 ОН- (1) 2 Н+ + 2 е = Н 2 (2) водородная О 2 + 2 Н 2 О + 4 е = 4 ОН- (3) О 2 + 4 Н+ + 4 е = 2 Н 2 О (4) кислородная деполяризация
 Схема возникающего гальванического элемента (-) Fe Fe 2+ H+, O 2, H 2 O Cu (+) Анод Катод Условие работы гальванического элемента: Е+(катода) > Е-(анода)
Схема возникающего гальванического элемента (-) Fe Fe 2+ H+, O 2, H 2 O Cu (+) Анод Катод Условие работы гальванического элемента: Е+(катода) > Е-(анода)
 Потенциалы процессов ( 298 К ) l Потенциал водородной деполяризации: Е 2 Н+/Н = - 0, 059 р. Н – 0, 0295 lg PH 2 2 l Потенциал кислородной деполяризации: ЕО 2/2 ОН- = 1, 23 - 0, 059 р. Н + 0, 0147 lg. PO 2
Потенциалы процессов ( 298 К ) l Потенциал водородной деполяризации: Е 2 Н+/Н = - 0, 059 р. Н – 0, 0295 lg PH 2 2 l Потенциал кислородной деполяризации: ЕО 2/2 ОН- = 1, 23 - 0, 059 р. Н + 0, 0147 lg. PO 2
 Стадии процесса коррозии l l Анодное окисление металла Катодное восстановление окислителя Движение электронов в металле Движение ионов в среде электролита
Стадии процесса коррозии l l Анодное окисление металла Катодное восстановление окислителя Движение электронов в металле Движение ионов в среде электролита
 Скорость коррозии l Кислородная деполяризация Растворимость кислорода в воде при 250 С и РО 2 = 21 к. Па составляет 2, 6 • 10 -7 моль/мл l Водородная деполяризация Катализируют процесс металлы: Pt, Ni, Cо Не катализируют процесс: Hg, Pb, Cd, Zn, Sn
Скорость коррозии l Кислородная деполяризация Растворимость кислорода в воде при 250 С и РО 2 = 21 к. Па составляет 2, 6 • 10 -7 моль/мл l Водородная деполяризация Катализируют процесс металлы: Pt, Ni, Cо Не катализируют процесс: Hg, Pb, Cd, Zn, Sn
 Правило фаз Гиббса C+Ф=К+n или: С=К+n-Ф С – число степеней свободы; К – число компонентов; Ф – число фаз n – число внешних факторов, влияющих на систему Американский. физик-теоретик Дж. Уиллард Гиббс 1839 -1903
Правило фаз Гиббса C+Ф=К+n или: С=К+n-Ф С – число степеней свободы; К – число компонентов; Ф – число фаз n – число внешних факторов, влияющих на систему Американский. физик-теоретик Дж. Уиллард Гиббс 1839 -1903
 Виды диаграмм состояния l l l 1. Диаграммы состояния для сплавов, образующих механическую смесь индивидуальных компонентов при кристаллизации. 2. Диаграммы состояния для сплавов с неограниченной растворимостью в твердом состоянии 3. Диаграммы состояния для сплавов, образующих химические соединения при кристаллизации
Виды диаграмм состояния l l l 1. Диаграммы состояния для сплавов, образующих механическую смесь индивидуальных компонентов при кристаллизации. 2. Диаграммы состояния для сплавов с неограниченной растворимостью в твердом состоянии 3. Диаграммы состояния для сплавов, образующих химические соединения при кристаллизации
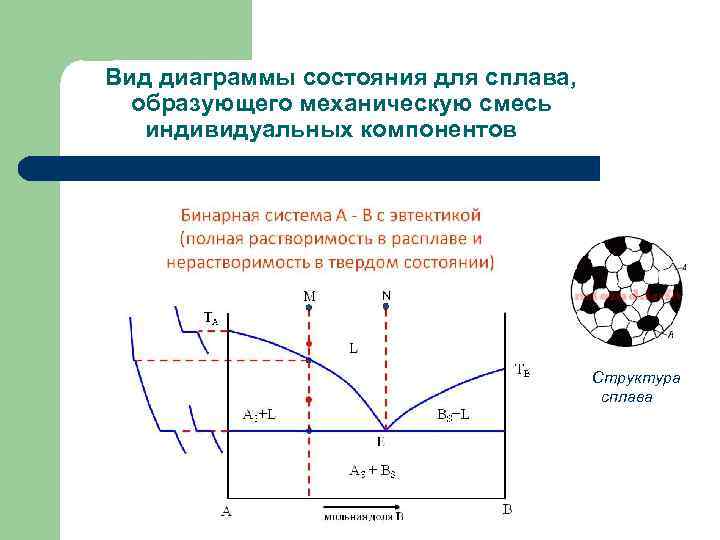 Вид диаграммы состояния для сплава, образующего механическую смесь индивидуальных компонентов I IIl II Е l. V V Состав сплава, % Структура сплава
Вид диаграммы состояния для сплава, образующего механическую смесь индивидуальных компонентов I IIl II Е l. V V Состав сплава, % Структура сплава
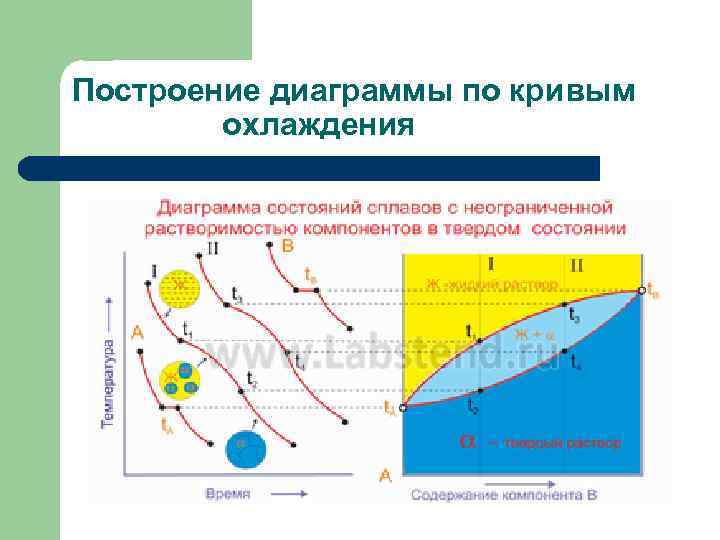 Построение диаграммы по кривым охлаждения
Построение диаграммы по кривым охлаждения
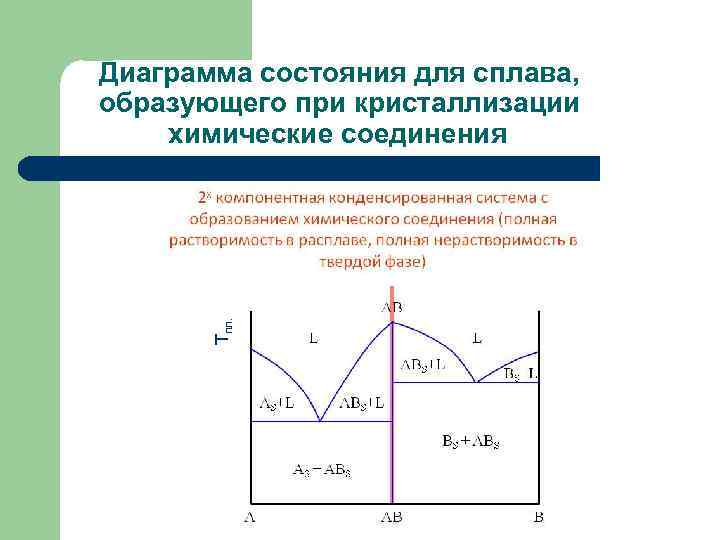 Тпл. Диаграмма состояния для сплава, образующего при кристаллизации химические соединения Состав сплава, %
Тпл. Диаграмма состояния для сплава, образующего при кристаллизации химические соединения Состав сплава, %


