Lektsia_8_Komplexnye_soedinenia.ppt
- Количество слайдов: 97
 Лекция КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
Лекция КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
 Основные вопросы темы: • Современные представления о строении и свойствах комплексных соединений. • Биологическая роль и применение в медицине комплексных соединений.
Основные вопросы темы: • Современные представления о строении и свойствах комплексных соединений. • Биологическая роль и применение в медицине комплексных соединений.
 Реагенты в химии Лекарственные препараты Витамины Катализаторы Хлорофилл Гемоглобин И др.
Реагенты в химии Лекарственные препараты Витамины Катализаторы Хлорофилл Гемоглобин И др.
 Чугаев Л. А. Комплексные соединения (КС) – это продукт сочетания простых соединений, способных к самостоятельному существованию КС– это такие соединения, в узлах кристаллической решётки которых находятся комплексы или комплексные ионы, способные к самостоятельному существованию
Чугаев Л. А. Комплексные соединения (КС) – это продукт сочетания простых соединений, способных к самостоятельному существованию КС– это такие соединения, в узлах кристаллической решётки которых находятся комплексы или комплексные ионы, способные к самостоятельному существованию
 Примеры реакций комплексообразования • Hg. I 2 + 2 KI = K 2[Hg. I 4] • KF + BF 3 = K[BF 4] • Al(OH)3+ Na. OH = Na[Al(OH)4] • Ag. Cl + 2 NH 3=[Ag(NH 3)2]Cl
Примеры реакций комплексообразования • Hg. I 2 + 2 KI = K 2[Hg. I 4] • KF + BF 3 = K[BF 4] • Al(OH)3+ Na. OH = Na[Al(OH)4] • Ag. Cl + 2 NH 3=[Ag(NH 3)2]Cl
![[Pt(NH 3)2 Cl 2 ]0 [Ni(CO)4] • Кристаллогидраты: Cu. SO 4 • 5 H [Pt(NH 3)2 Cl 2 ]0 [Ni(CO)4] • Кристаллогидраты: Cu. SO 4 • 5 H](https://present5.com/presentation/198569245_449820706/image-6.jpg) [Pt(NH 3)2 Cl 2 ]0 [Ni(CO)4] • Кристаллогидраты: Cu. SO 4 • 5 H 2 O [Cu(H 2 O)4]SO 4 Н 2 О Н - связь
[Pt(NH 3)2 Cl 2 ]0 [Ni(CO)4] • Кристаллогидраты: Cu. SO 4 • 5 H 2 O [Cu(H 2 O)4]SO 4 Н 2 О Н - связь
 Альфред Вернер Швейцарский химик, 1893 г
Альфред Вернер Швейцарский химик, 1893 г
![Составные части комплексных соединений Центральный атом Ион внешней сферы Лиганды [Co+3 (NH 3) 6]3+Cl Составные части комплексных соединений Центральный атом Ион внешней сферы Лиганды [Co+3 (NH 3) 6]3+Cl](https://present5.com/presentation/198569245_449820706/image-8.jpg) Составные части комплексных соединений Центральный атом Ион внешней сферы Лиганды [Co+3 (NH 3) 6]3+Cl 3 Внутреняя сфера Внешняя сфера Координационное число
Составные части комплексных соединений Центральный атом Ион внешней сферы Лиганды [Co+3 (NH 3) 6]3+Cl 3 Внутреняя сфера Внешняя сфера Координационное число
 Характеристика центрального атома Комплексообразующая способность элементов f >d>p>s Инертные газы также могут выступать в качестве комплексообразователя: Cs [Xe. F 7]
Характеристика центрального атома Комплексообразующая способность элементов f >d>p>s Инертные газы также могут выступать в качестве комплексообразователя: Cs [Xe. F 7]
 Важнейшие характеристики центрального атома : • Степень окисления • Координационное число • Ионный потенциал
Важнейшие характеристики центрального атома : • Степень окисления • Координационное число • Ионный потенциал
![Степень окисления Положительная K 3[Fe 3+(CN)6], K 4[Fe 2+(CN)6], Cs[Xe+6 F 7], К[BF 4] Степень окисления Положительная K 3[Fe 3+(CN)6], K 4[Fe 2+(CN)6], Cs[Xe+6 F 7], К[BF 4]](https://present5.com/presentation/198569245_449820706/image-11.jpg) Степень окисления Положительная K 3[Fe 3+(CN)6], K 4[Fe 2+(CN)6], Cs[Xe+6 F 7], К[BF 4] Отрицательная [N 3 H 4 ] Cl Нулевая [Cl 2(H 2 O)4]
Степень окисления Положительная K 3[Fe 3+(CN)6], K 4[Fe 2+(CN)6], Cs[Xe+6 F 7], К[BF 4] Отрицательная [N 3 H 4 ] Cl Нулевая [Cl 2(H 2 O)4]
 Координационное число (КЧ) Это число атомов или групп атомов, непосредственно связанных с центральным атомом
Координационное число (КЧ) Это число атомов или групп атомов, непосредственно связанных с центральным атомом
 КЧ зависит: - от размеров центрального атома и лигандов. Лат. liganda то, что должно быть связано
КЧ зависит: - от размеров центрального атома и лигандов. Лат. liganda то, что должно быть связано
![Na[BF 4] Na 3[Al. F 6] F F F F F B 3+ F Na[BF 4] Na 3[Al. F 6] F F F F F B 3+ F](https://present5.com/presentation/198569245_449820706/image-14.jpg) Na[BF 4] Na 3[Al. F 6] F F F F F B 3+ F F F r. B 3+ = 0, 02 нм F Al 3+ F F F F F r. Al 3+ = 0, 057 нм
Na[BF 4] Na 3[Al. F 6] F F F F F B 3+ F F F r. B 3+ = 0, 02 нм F Al 3+ F F F F F r. Al 3+ = 0, 057 нм
![Na 3[Al. F 6] Na [Al. Cl 4] Cl l F F l Cl Na 3[Al. F 6] Na [Al. Cl 4] Cl l F F l Cl](https://present5.com/presentation/198569245_449820706/image-15.jpg) Na 3[Al. F 6] Na [Al. Cl 4] Cl l F F l Cl F F l F Al 3+ F F l F F r. F_ = 0, 133 нм Cl r. Cl = 0, 181 нм
Na 3[Al. F 6] Na [Al. Cl 4] Cl l F F l Cl F F l F Al 3+ F F l F F r. F_ = 0, 133 нм Cl r. Cl = 0, 181 нм
 - от степени окисления центрального атома: Степень КЧ окисления ц. а. (подчеркнуто характерное) Примеры +1 2, 3 [Ag(NH 3)2]Cl +2 3, 4, 6 [Cu(NH 3)4]Cl 2 +3 4, 5, 6 Na 3[Co(NO 2)6] +4 6, 8 H 2[Sn. Cl 6]
- от степени окисления центрального атома: Степень КЧ окисления ц. а. (подчеркнуто характерное) Примеры +1 2, 3 [Ag(NH 3)2]Cl +2 3, 4, 6 [Cu(NH 3)4]Cl 2 +3 4, 5, 6 Na 3[Co(NO 2)6] +4 6, 8 H 2[Sn. Cl 6]
 Эмпирическое правило: чаще всего кч устойчивого комплекса в два раза больше степени окисления ц. а. КЧ = 2 Z
Эмпирическое правило: чаще всего кч устойчивого комплекса в два раза больше степени окисления ц. а. КЧ = 2 Z
![- концентрации исходных компонентов : Al(OH)3 + Na. OH= Na[Al(OH)4] Al(OH)3 +3 Na. OH= - концентрации исходных компонентов : Al(OH)3 + Na. OH= Na[Al(OH)4] Al(OH)3 +3 Na. OH=](https://present5.com/presentation/198569245_449820706/image-18.jpg) - концентрации исходных компонентов : Al(OH)3 + Na. OH= Na[Al(OH)4] Al(OH)3 +3 Na. OH= Na 3[Al(OH)6]
- концентрации исходных компонентов : Al(OH)3 + Na. OH= Na[Al(OH)4] Al(OH)3 +3 Na. OH= Na 3[Al(OH)6]
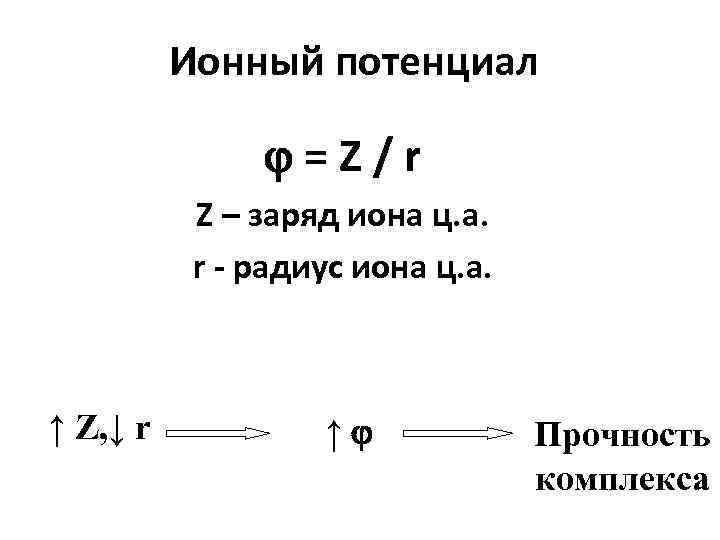 Ионный потенциал =Z/r Z – заряд иона ц. а. r - радиус иона ц. а. ↑ Z, ↓ r ↑ Прочность комплекса
Ионный потенциал =Z/r Z – заряд иона ц. а. r - радиус иона ц. а. ↑ Z, ↓ r ↑ Прочность комплекса
 Характеристика лигандов
Характеристика лигандов
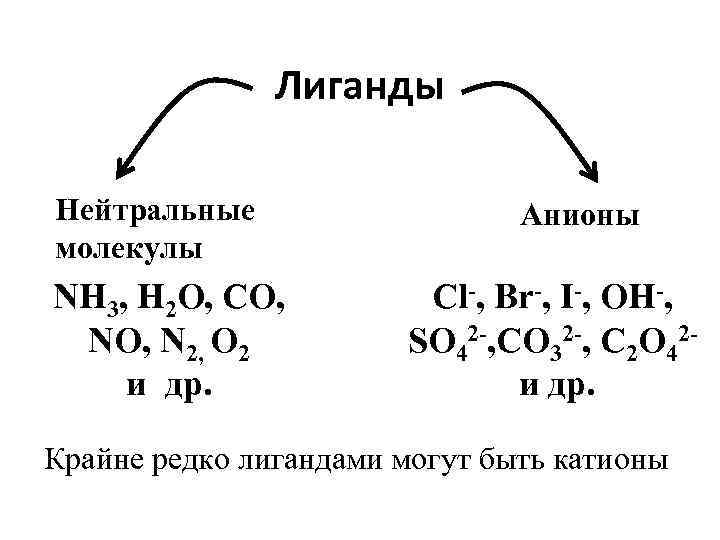 Лиганды Нейтральные молекулы NH 3, H 2 O, CO, N 2, O 2 и др. Анионы Cl , Br , I , OH , SO 42 , CO 32 , C 2 O 42 и др. Крайне редко лигандами могут быть катионы
Лиганды Нейтральные молекулы NH 3, H 2 O, CO, N 2, O 2 и др. Анионы Cl , Br , I , OH , SO 42 , CO 32 , C 2 O 42 и др. Крайне редко лигандами могут быть катионы
 Число донорных атомов в лиганде характеризует его координационную ёмкость – дентатность Лат. dentalus – имеющий зубы -монодентатные лиганды, содержат 1 донорный атом -, Cl-, Br-) (H 2 O, NH 3, OH
Число донорных атомов в лиганде характеризует его координационную ёмкость – дентатность Лат. dentalus – имеющий зубы -монодентатные лиганды, содержат 1 донорный атом -, Cl-, Br-) (H 2 O, NH 3, OH
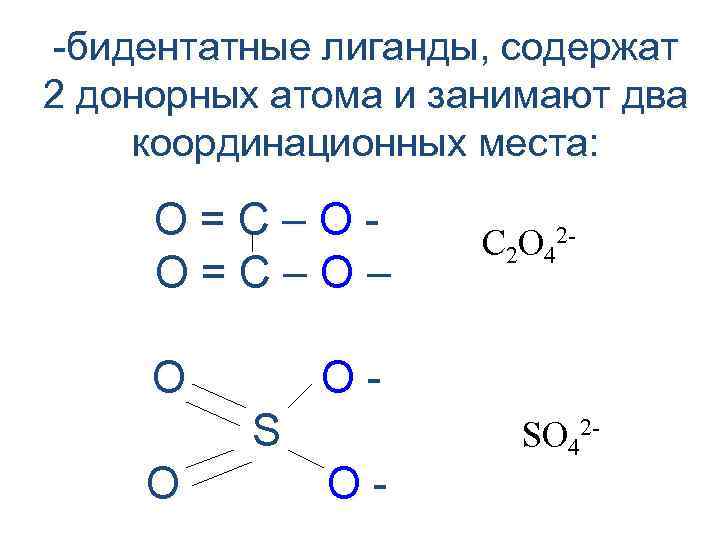 -бидентатные лиганды, содержат 2 донорных атома и занимают два координационных места: О=С–О– O OS O С 2 О 42 O- SО 42
-бидентатные лиганды, содержат 2 донорных атома и занимают два координационных места: О=С–О– O OS O С 2 О 42 O- SО 42
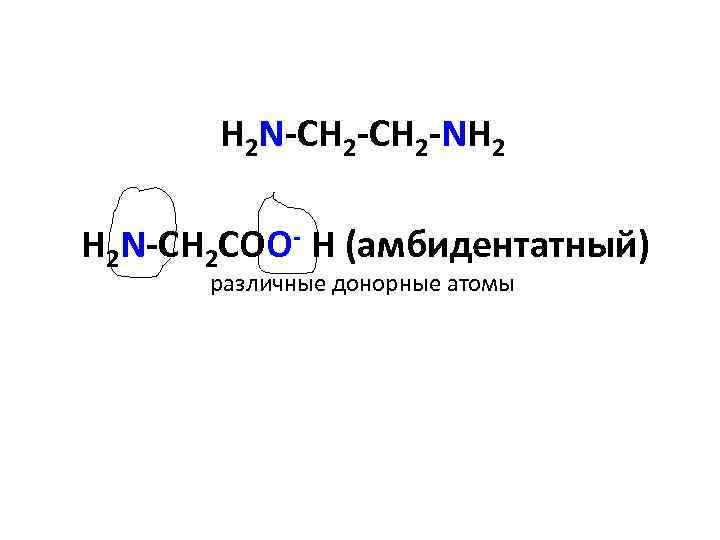 H 2 N-CH 2 -NH 2 H 2 N-CH 2 COO- H (амбидентатный) различные донорные атомы
H 2 N-CH 2 -NH 2 H 2 N-CH 2 COO- H (амбидентатный) различные донорные атомы
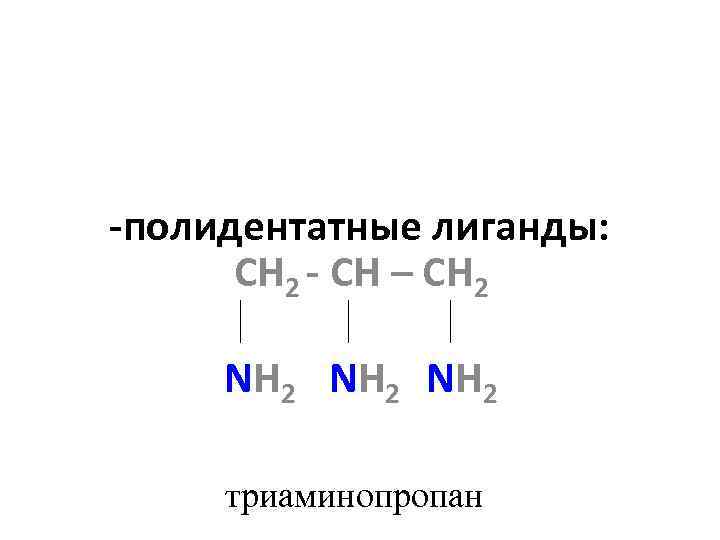 -полидентатные лиганды: СН 2 - СH – CH 2 NH 2 триаминопропан
-полидентатные лиганды: СН 2 - СH – CH 2 NH 2 триаминопропан
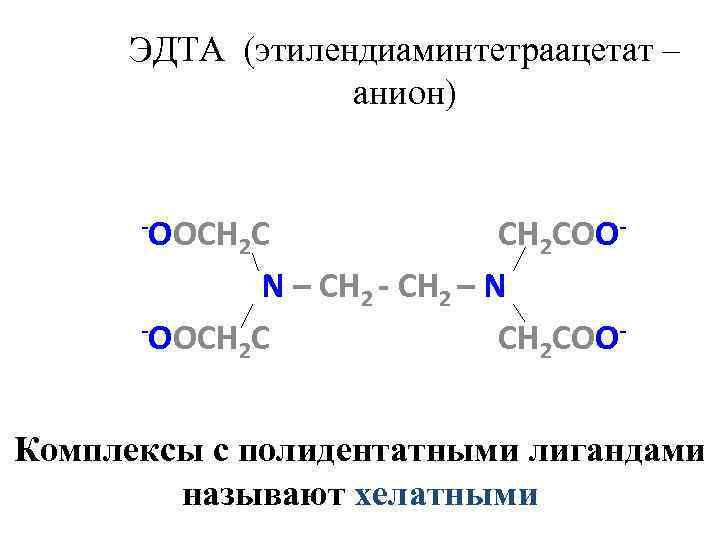 ЭДТА (этилендиаминтетраацетат – анион) -OOCH C CH 2 COO 2 N – CH 2 - CH 2 – N -OOCH C CH 2 COO 2 Комплексы с полидентатными лигандами называют хелатными
ЭДТА (этилендиаминтетраацетат – анион) -OOCH C CH 2 COO 2 N – CH 2 - CH 2 – N -OOCH C CH 2 COO 2 Комплексы с полидентатными лигандами называют хелатными
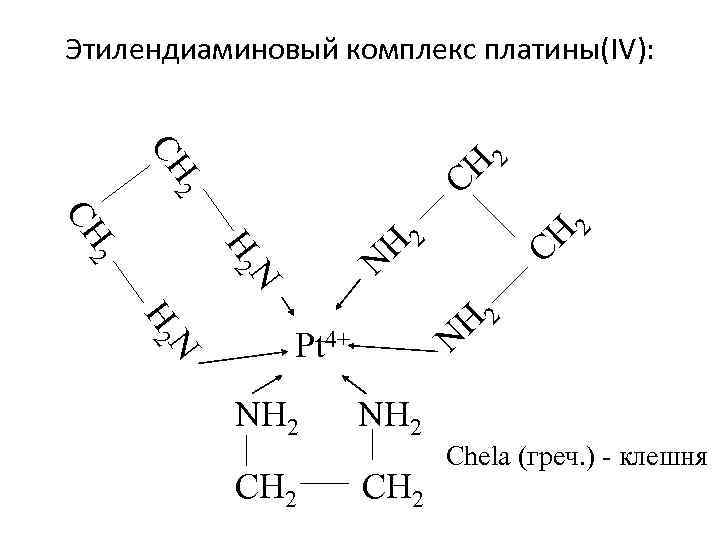 Этилендиаминовый комплекс платины(IV): 2 CH H 2 C N H 2 2 CH H 2 C H 2 N N H 2 N Pt 4+ NH 2 CH 2 Chela (греч. ) клешня
Этилендиаминовый комплекс платины(IV): 2 CH H 2 C N H 2 2 CH H 2 C H 2 N N H 2 N Pt 4+ NH 2 CH 2 Chela (греч. ) клешня
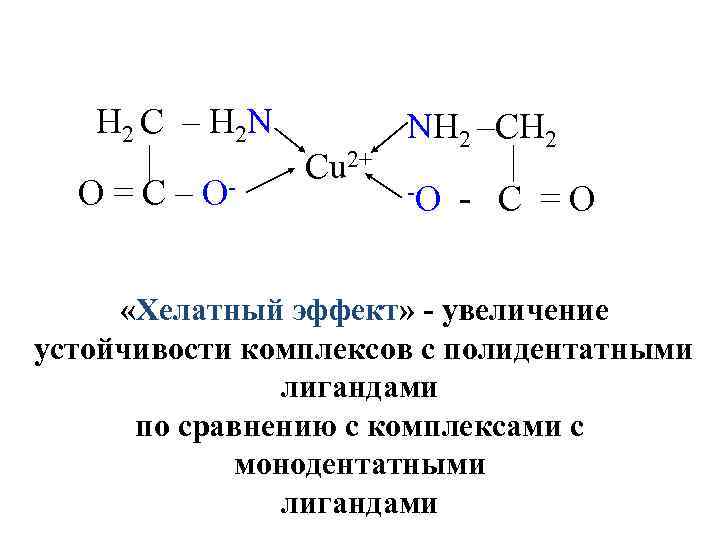 H 2 C – H 2 N O = C – O Cu 2+ NH 2 –CH 2 O C =O «Хелатный эффект» увеличение устойчивости комплексов с полидентатными лигандами по сравнению с комплексами с монодентатными лигандами
H 2 C – H 2 N O = C – O Cu 2+ NH 2 –CH 2 O C =O «Хелатный эффект» увеличение устойчивости комплексов с полидентатными лигандами по сравнению с комплексами с монодентатными лигандами
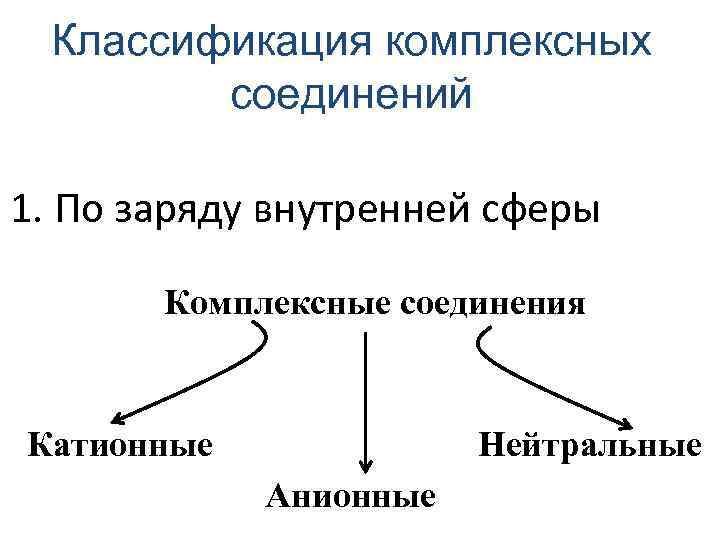 Классификация комплексных соединений 1. По заряду внутренней сферы Комплексные соединения Катионные Нейтральные Анионные
Классификация комплексных соединений 1. По заряду внутренней сферы Комплексные соединения Катионные Нейтральные Анионные
![2+ [Cu(NH 3)4]SO 4 + [Co(NH 3)4 Cl 2]Cl [Fe(CO)5] 0 Na 3[Co(NO 2)6] 2+ [Cu(NH 3)4]SO 4 + [Co(NH 3)4 Cl 2]Cl [Fe(CO)5] 0 Na 3[Co(NO 2)6]](https://present5.com/presentation/198569245_449820706/image-30.jpg) 2+ [Cu(NH 3)4]SO 4 + [Co(NH 3)4 Cl 2]Cl [Fe(CO)5] 0 Na 3[Co(NO 2)6] 3 [Pt(NH 3)2 Cl 2] K 3 [Fe(CN) 6] 3 0
2+ [Cu(NH 3)4]SO 4 + [Co(NH 3)4 Cl 2]Cl [Fe(CO)5] 0 Na 3[Co(NO 2)6] 3 [Pt(NH 3)2 Cl 2] K 3 [Fe(CN) 6] 3 0
 2. По природе лиганда: Гидроксокомплексы ( ОН-) Аквакомплексы (Н 2 О) Аммиакатные комплексы (NH 3) Ацидокомплексы ( CN- - циано, CNS— тиоциано, NO 2 - - нитро, Сl- - хлоро, SO 42– сульфато и т. д. ) • Карбонильные (СО) • И др. • •
2. По природе лиганда: Гидроксокомплексы ( ОН-) Аквакомплексы (Н 2 О) Аммиакатные комплексы (NH 3) Ацидокомплексы ( CN- - циано, CNS— тиоциано, NO 2 - - нитро, Сl- - хлоро, SO 42– сульфато и т. д. ) • Карбонильные (СО) • И др. • •
![Классификация КС по природе лигандов Лиганды Название Примеры OH Гидроксокомпле Na 3[Al(OH)6], ксы Na Классификация КС по природе лигандов Лиганды Название Примеры OH Гидроксокомпле Na 3[Al(OH)6], ксы Na](https://present5.com/presentation/198569245_449820706/image-32.jpg) Классификация КС по природе лигандов Лиганды Название Примеры OH Гидроксокомпле Na 3[Al(OH)6], ксы Na 2[Zn(OH)4] Анионы Ацидокомплек кислотных сы остатков: Cl , Br , SO 2 , CO 2 и 4 3 др. K 2[Hg. I 4], K 4[Fe(CN)6] Нейтральные молекулы: NH 3, H 2 O, и др. [Zn (NH 3)4]Cl 2 [Al(H 2 O)6]Cl 3 Аммиакаты, аквакомплексы
Классификация КС по природе лигандов Лиганды Название Примеры OH Гидроксокомпле Na 3[Al(OH)6], ксы Na 2[Zn(OH)4] Анионы Ацидокомплек кислотных сы остатков: Cl , Br , SO 2 , CO 2 и 4 3 др. K 2[Hg. I 4], K 4[Fe(CN)6] Нейтральные молекулы: NH 3, H 2 O, и др. [Zn (NH 3)4]Cl 2 [Al(H 2 O)6]Cl 3 Аммиакаты, аквакомплексы
![3. По способности ионизировать: • Электролиты [Cu(NH 3)4]SO 4 • Неэлектролиты [Pt(NH 3)2 Cl 3. По способности ионизировать: • Электролиты [Cu(NH 3)4]SO 4 • Неэлектролиты [Pt(NH 3)2 Cl](https://present5.com/presentation/198569245_449820706/image-33.jpg) 3. По способности ионизировать: • Электролиты [Cu(NH 3)4]SO 4 • Неэлектролиты [Pt(NH 3)2 Cl 2] 4. По свойствам электролита: • Кислоты Н[Au. Cl 4] • Основания [Cu(Н 2 О)4](ОН)2 • Соли [Ag(NH 3)2]Cl
3. По способности ионизировать: • Электролиты [Cu(NH 3)4]SO 4 • Неэлектролиты [Pt(NH 3)2 Cl 2] 4. По свойствам электролита: • Кислоты Н[Au. Cl 4] • Основания [Cu(Н 2 О)4](ОН)2 • Соли [Ag(NH 3)2]Cl
 Номенклатура комплексных соединений
Номенклатура комплексных соединений
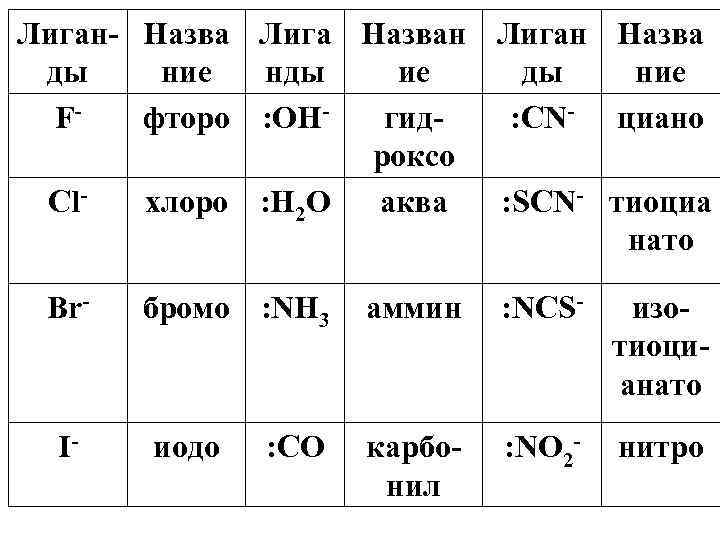 Лиган Назва Лига Назван Лиган Назва ды ние нды ие ды ние F фторо : OH гид : CN циано роксо Cl хлоро : H 2 O аква : SCN тиоциа нато Br I бромо : NH 3 иодо : CO аммин : NCS изо тиоци анато карбо нил : NO 2 нитро
Лиган Назва Лига Назван Лиган Назва ды ние нды ие ды ние F фторо : OH гид : CN циано роксо Cl хлоро : H 2 O аква : SCN тиоциа нато Br I бромо : NH 3 иодо : CO аммин : NCS изо тиоци анато карбо нил : NO 2 нитро
![[Cu(NH 3)4]SO 4 Сульфат тетраамминмеди (II) [Cr (NH 3)3(H 2 O)2 Cl]Br 2 Бромид [Cu(NH 3)4]SO 4 Сульфат тетраамминмеди (II) [Cr (NH 3)3(H 2 O)2 Cl]Br 2 Бромид](https://present5.com/presentation/198569245_449820706/image-36.jpg) [Cu(NH 3)4]SO 4 Сульфат тетраамминмеди (II) [Cr (NH 3)3(H 2 O)2 Cl]Br 2 Бромид хлородиакватриамминхрома (III) Na 3[Co(NO 2)6] ГГексанитрокобальтат (III) натрия Гексанитрокобальтат (Ш) натрия [Pt(NH 3)2 Cl 2] Дихлородиамминплатина
[Cu(NH 3)4]SO 4 Сульфат тетраамминмеди (II) [Cr (NH 3)3(H 2 O)2 Cl]Br 2 Бромид хлородиакватриамминхрома (III) Na 3[Co(NO 2)6] ГГексанитрокобальтат (III) натрия Гексанитрокобальтат (Ш) натрия [Pt(NH 3)2 Cl 2] Дихлородиамминплатина
 Природа химической связи в комплексных соединениях
Природа химической связи в комплексных соединениях
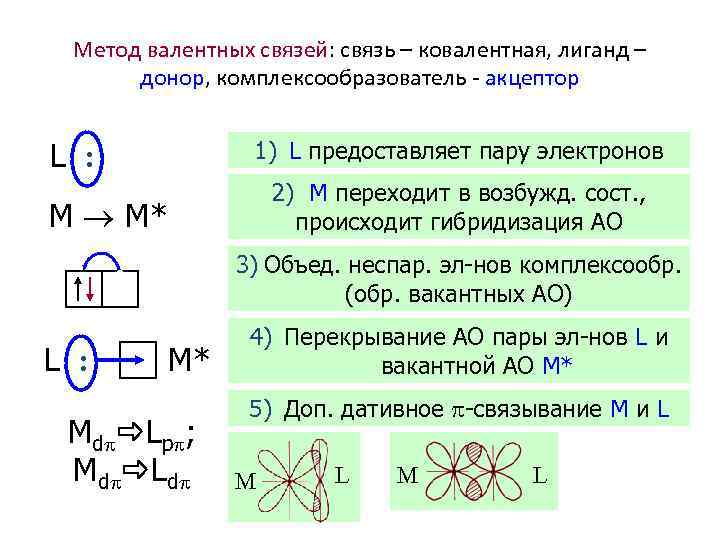 Метод валентных связей: связь – ковалентная, лиганд – донор, комплексообразователь - акцептор L : 1) L предоставляет пару электронов 2) M переходит в возбужд. сост. , происходит гибридизация АО M M* 3) Объед. неспар. эл-нов комплексообр. (обр. вакантных АО) L : M* Md Lp ; Md Ld 4) Перекрывание АО пары эл-нов L и вакантной АО M* 5) Доп. дативное -связывание M и L M L
Метод валентных связей: связь – ковалентная, лиганд – донор, комплексообразователь - акцептор L : 1) L предоставляет пару электронов 2) M переходит в возбужд. сост. , происходит гибридизация АО M M* 3) Объед. неспар. эл-нов комплексообр. (обр. вакантных АО) L : M* Md Lp ; Md Ld 4) Перекрывание АО пары эл-нов L и вакантной АО M* 5) Доп. дативное -связывание M и L M L
![Zn 2+ + 4 NH 3 [Zn(NH 3)4]2+ Zn 2+ + 4 NH 3 [Zn(NH 3)4]2+](https://present5.com/presentation/198569245_449820706/image-39.jpg) Zn 2+ + 4 NH 3 [Zn(NH 3)4]2+
Zn 2+ + 4 NH 3 [Zn(NH 3)4]2+
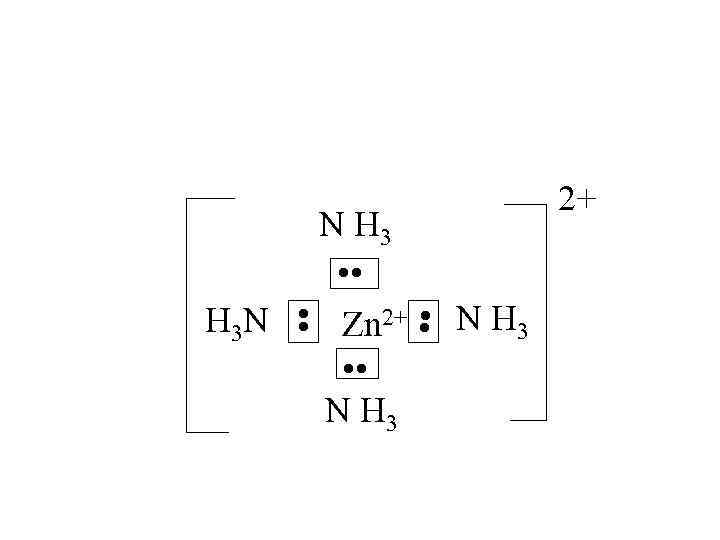 • • H 3 N N H 3 • • Zn 2+ • • N H 3 2+ N H 3
• • H 3 N N H 3 • • Zn 2+ • • N H 3 2+ N H 3
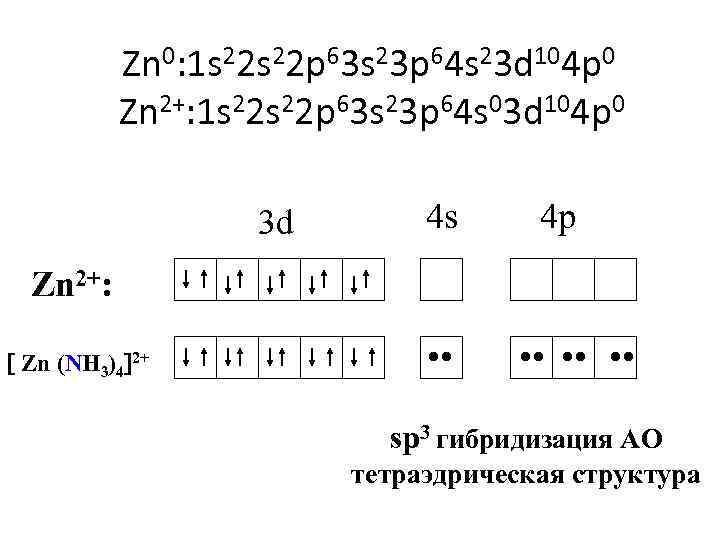 Zn 0: 1 s 22 p 63 s 23 p 64 s 23 d 104 p 0 Zn 2+: 1 s 22 p 63 s 23 p 64 s 03 d 104 p 0 3 d 4 s 4 p Zn 2+: Zn (NH 3)4 2+ • • sp 3 гибридизация АО тетраэдрическая структура
Zn 0: 1 s 22 p 63 s 23 p 64 s 23 d 104 p 0 Zn 2+: 1 s 22 p 63 s 23 p 64 s 03 d 104 p 0 3 d 4 s 4 p Zn 2+: Zn (NH 3)4 2+ • • sp 3 гибридизация АО тетраэдрическая структура
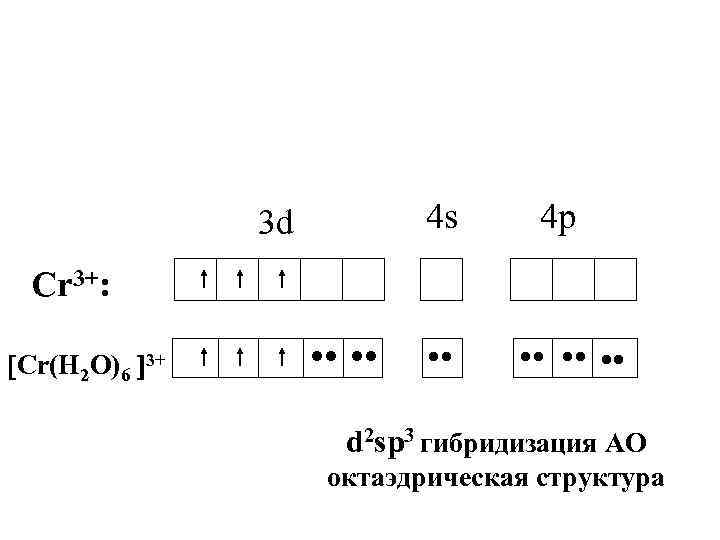 4 s 3 d 4 p Cr 3+: Cr(H 2 O)6 3+ • • • • d 2 sp 3 гибридизация АО октаэдрическая структура
4 s 3 d 4 p Cr 3+: Cr(H 2 O)6 3+ • • • • d 2 sp 3 гибридизация АО октаэдрическая структура
![Для атомов комплексообразователей: E(n-1)d Ens Enp End • Пример: комплексы никеля. Ni 0 [Ar] Для атомов комплексообразователей: E(n-1)d Ens Enp End • Пример: комплексы никеля. Ni 0 [Ar]](https://present5.com/presentation/198569245_449820706/image-43.jpg) Для атомов комплексообразователей: E(n-1)d Ens Enp End • Пример: комплексы никеля. Ni 0 [Ar] 3 d 84 s 24 p 0 Ni* 3 d 8 4 s 2 0 Атом Ni 0 парамагнитен 3 d 10 4 s o КЧ 4 Ni+II 4 p 3 d КЧ 4 4 p 0 sp 3 гибр. 8 4 s o 4 p [Ni(CO)4] уст. , диамагнитный, тетраэдрич. 0 sp 3 гибр. [Ni. Br 4]2– неуст. , парамагн. , тетраэдрич.
Для атомов комплексообразователей: E(n-1)d Ens Enp End • Пример: комплексы никеля. Ni 0 [Ar] 3 d 84 s 24 p 0 Ni* 3 d 8 4 s 2 0 Атом Ni 0 парамагнитен 3 d 10 4 s o КЧ 4 Ni+II 4 p 3 d КЧ 4 4 p 0 sp 3 гибр. 8 4 s o 4 p [Ni(CO)4] уст. , диамагнитный, тетраэдрич. 0 sp 3 гибр. [Ni. Br 4]2– неуст. , парамагн. , тетраэдрич.
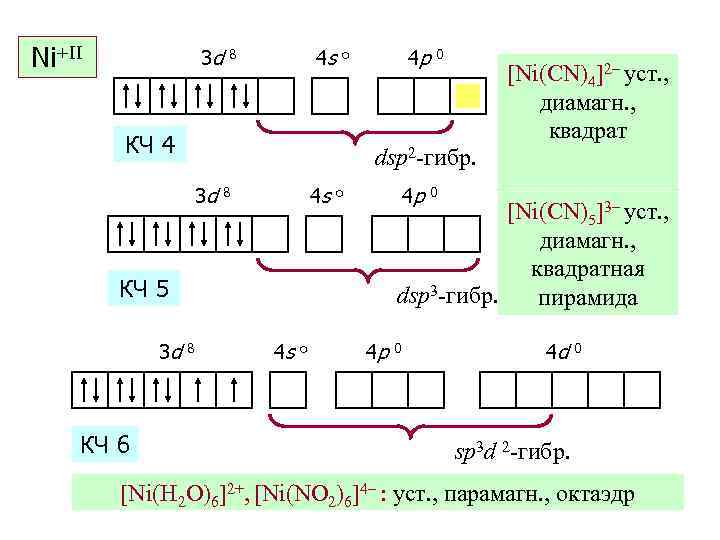 Ni+II 3 d 4 s 8 4 p o КЧ 4 dsp 2 гибр. 3 d 4 s 8 4 p o КЧ 6 8 4 s o [Ni(CN)4]2– уст. , диамагн. , квадрат 0 [Ni(CN)5]3– уст. , диамагн. , квадратная dsp 3 гибр. пирамида КЧ 5 3 d 0 4 p 0 4 d 0 sp 3 d 2 гибр. [Ni(H 2 O)6]2+, [Ni(NO 2)6]4– : уст. , парамагн. , октаэдр
Ni+II 3 d 4 s 8 4 p o КЧ 4 dsp 2 гибр. 3 d 4 s 8 4 p o КЧ 6 8 4 s o [Ni(CN)4]2– уст. , диамагн. , квадрат 0 [Ni(CN)5]3– уст. , диамагн. , квадратная dsp 3 гибр. пирамида КЧ 5 3 d 0 4 p 0 4 d 0 sp 3 d 2 гибр. [Ni(H 2 O)6]2+, [Ni(NO 2)6]4– : уст. , парамагн. , октаэдр
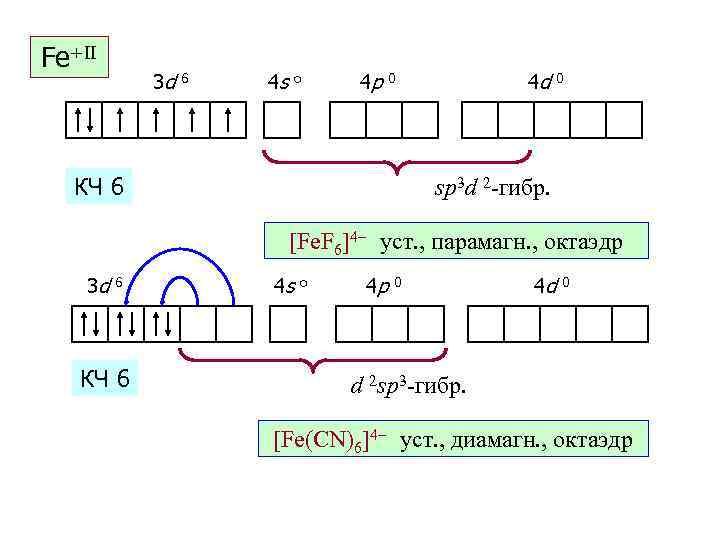 Fe+II 3 d 6 4 s o 4 p 4 d 0 КЧ 6 0 sp 3 d 2 гибр. [Fe. F 6]4– уст. , парамагн. , октаэдр 3 d 6 КЧ 6 4 s o 4 p 0 4 d 0 d 2 sp 3 гибр. [Fe(CN)6]4– уст. , диамагн. , октаэдр Fe+II
Fe+II 3 d 6 4 s o 4 p 4 d 0 КЧ 6 0 sp 3 d 2 гибр. [Fe. F 6]4– уст. , парамагн. , октаэдр 3 d 6 КЧ 6 4 s o 4 p 0 4 d 0 d 2 sp 3 гибр. [Fe(CN)6]4– уст. , диамагн. , октаэдр Fe+II
![Геометрическая конфигурация комплексов Тип гибр. КЧ Геом. форма Примеры sp 2 линейн. [Ag(CN)2]-, [Cu(NH Геометрическая конфигурация комплексов Тип гибр. КЧ Геом. форма Примеры sp 2 линейн. [Ag(CN)2]-, [Cu(NH](https://present5.com/presentation/198569245_449820706/image-46.jpg) Геометрическая конфигурация комплексов Тип гибр. КЧ Геом. форма Примеры sp 2 линейн. [Ag(CN)2]-, [Cu(NH 3)2]+ sp 2 3 треуг. [Hg. I 3]- sp 3, sd 3 4 тетраэдр [Be(OH)4]2 -, [Mn. Cl 4]2 - sp 2 d 4 квадрат [Ni(CN)4]2 -, [Pt. Cl 4]2 - sp 3 d(z 2), dsp 3 5 триг. бипир. [Fe(CO)5] sp 3 d(x 2 -y 2), d(x 2 -y 2)sp 3 d 2, d 2 sp 3 5 квадратная пирамида октаэдр [Mn. Cl 5]3 -, [Ni(CN)5]3 - sp 3 d 3 7 6 пентагон. бипирамида [Al(H 2 O)6]3+, [Fe(CN)6]3[V(CN)7]4 -, [Zr. F 7]3 -
Геометрическая конфигурация комплексов Тип гибр. КЧ Геом. форма Примеры sp 2 линейн. [Ag(CN)2]-, [Cu(NH 3)2]+ sp 2 3 треуг. [Hg. I 3]- sp 3, sd 3 4 тетраэдр [Be(OH)4]2 -, [Mn. Cl 4]2 - sp 2 d 4 квадрат [Ni(CN)4]2 -, [Pt. Cl 4]2 - sp 3 d(z 2), dsp 3 5 триг. бипир. [Fe(CO)5] sp 3 d(x 2 -y 2), d(x 2 -y 2)sp 3 d 2, d 2 sp 3 5 квадратная пирамида октаэдр [Mn. Cl 5]3 -, [Ni(CN)5]3 - sp 3 d 3 7 6 пентагон. бипирамида [Al(H 2 O)6]3+, [Fe(CN)6]3[V(CN)7]4 -, [Zr. F 7]3 -
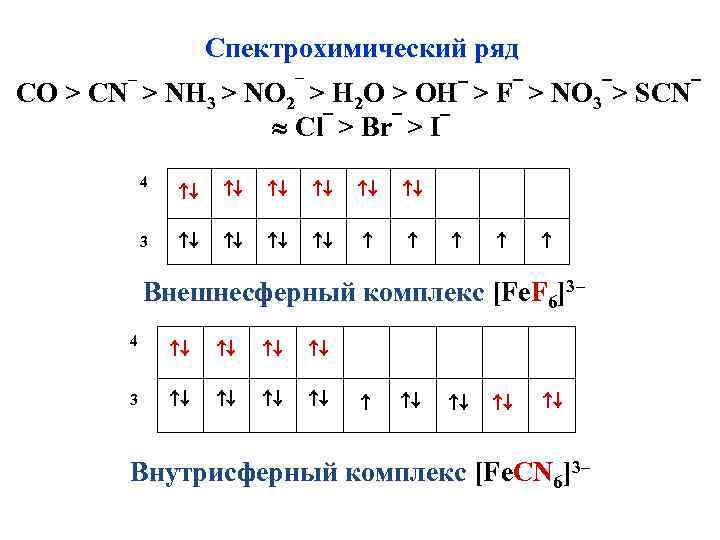 Спектрохимический ряд – СO > CN > NH 3 > 4 3 – NO 2 > H 2 O > OH > F > Cl > Br > I NО 3 > Внешнесферный комплекс [Fe. F 6]3– 4 3 Внутрисферный комплекс [Fe. CN 6]3– SCN
Спектрохимический ряд – СO > CN > NH 3 > 4 3 – NO 2 > H 2 O > OH > F > Cl > Br > I NО 3 > Внешнесферный комплекс [Fe. F 6]3– 4 3 Внутрисферный комплекс [Fe. CN 6]3– SCN
 ТЕОРИЯ КРИСТАЛЛИЧЕСКОГО ПОЛЯ • Лиганды – точечные заряды (кристаллическое поле). • Связь между лиогандами и ценртральным атомом чисто ионная. • Вырожденный d-подуровень центрального атома под действием поля лигандов расщепляется в соответствии с симметрией окружения.
ТЕОРИЯ КРИСТАЛЛИЧЕСКОГО ПОЛЯ • Лиганды – точечные заряды (кристаллическое поле). • Связь между лиогандами и ценртральным атомом чисто ионная. • Вырожденный d-подуровень центрального атома под действием поля лигандов расщепляется в соответствии с симметрией окружения.
![В случае [ML 6] ±, 0 : октаэдрическое поле лигандов • Поле слабо влияет В случае [ML 6] ±, 0 : октаэдрическое поле лигандов • Поле слабо влияет](https://present5.com/presentation/198569245_449820706/image-49.jpg) В случае [ML 6] ±, 0 : октаэдрическое поле лигандов • Поле слабо влияет (энергия падает) в случае АО d(xy), d(xz) и d(yz), располож. между осей координат (между лигандами) Eо d-АО • Поле сильно влияет (энергия растет) в случае АО d(z 2) и d(x 2– y 2), располож. вдоль осей координат (ближе всего к лигандам) d d – параметр расщепления |E –Eо| = 3/5 ; |E –Eо| = 2/5
В случае [ML 6] ±, 0 : октаэдрическое поле лигандов • Поле слабо влияет (энергия падает) в случае АО d(xy), d(xz) и d(yz), располож. между осей координат (между лигандами) Eо d-АО • Поле сильно влияет (энергия растет) в случае АО d(z 2) и d(x 2– y 2), располож. вдоль осей координат (ближе всего к лигандам) d d – параметр расщепления |E –Eо| = 3/5 ; |E –Eо| = 2/5
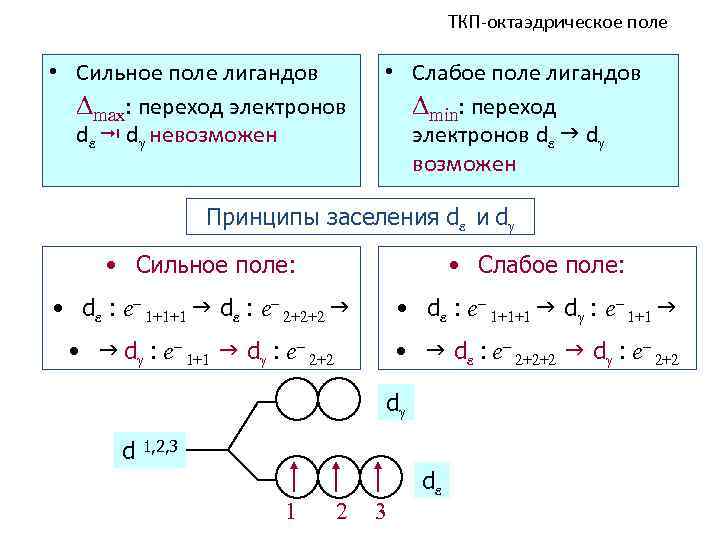 ТКП-октаэдрическое поле • Сильное поле лигандов max: переход электронов d d невозможен • Слабое поле лигандов min: переход электронов d d возможен Принципы заселения d и d • Сильное поле: • Слабое поле: • d : e– 1+1+1 d : e– 2+2+2 • d : e– 1+1+1 d : e– 1+1 • d : e– 1+1 d : e– 2+2 • d : e– 2+2+2 d : e– 2+2 d d 1, 2, 3 1 2 3 d
ТКП-октаэдрическое поле • Сильное поле лигандов max: переход электронов d d невозможен • Слабое поле лигандов min: переход электронов d d возможен Принципы заселения d и d • Сильное поле: • Слабое поле: • d : e– 1+1+1 d : e– 2+2+2 • d : e– 1+1+1 d : e– 1+1 • d : e– 1+1 d : e– 2+2 • d : e– 2+2+2 d : e– 2+2 d d 1, 2, 3 1 2 3 d
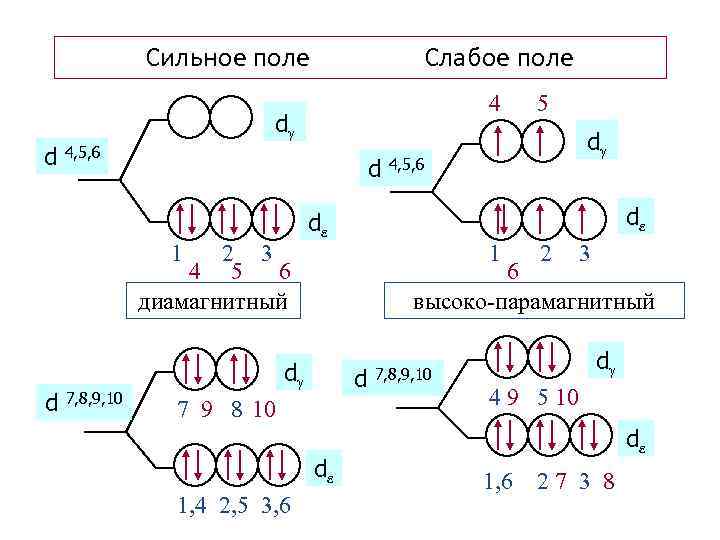 Сильное поле Слабое поле 4 d d 4, 5, 6 d 1 2 3 4 5 6 диамагнитный d 7, 8, 9, 10 d 4, 5, 6 d d 1 2 3 6 высоко парамагнитный d d 7 9 8 10 d 1, 4 2, 5 3, 6 5 7, 8, 9, 10 d 4 9 5 10 d 1, 6 2 7 3 8
Сильное поле Слабое поле 4 d d 4, 5, 6 d 1 2 3 4 5 6 диамагнитный d 7, 8, 9, 10 d 4, 5, 6 d d 1 2 3 6 высоко парамагнитный d d 7 9 8 10 d 1, 4 2, 5 3, 6 5 7, 8, 9, 10 d 4 9 5 10 d 1, 6 2 7 3 8
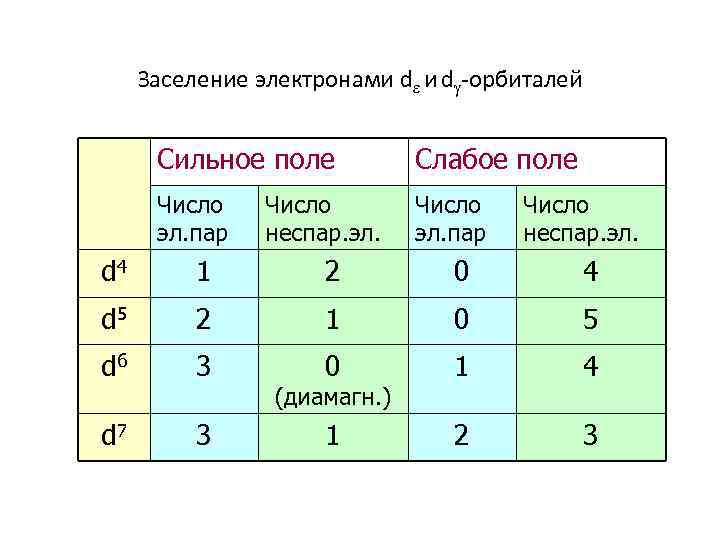 Заселение электронами d -орбиталей Сильное поле Слабое поле Число эл. пар Число неспар. эл. d 4 1 2 0 4 d 5 2 1 0 5 d 6 3 0 1 4 d 7 3 1 2 3 (диамагн. )
Заселение электронами d -орбиталей Сильное поле Слабое поле Число эл. пар Число неспар. эл. d 4 1 2 0 4 d 5 2 1 0 5 d 6 3 0 1 4 d 7 3 1 2 3 (диамагн. )
![Лиганды сильного и слабого поля Fe+II: [Ar] 3 d 64 s 04 p 0 Лиганды сильного и слабого поля Fe+II: [Ar] 3 d 64 s 04 p 0](https://present5.com/presentation/198569245_449820706/image-53.jpg) Лиганды сильного и слабого поля Fe+II: [Ar] 3 d 64 s 04 p 0 d d диамагн. [Fe(CN)6]4– парамагн. [Fe. F 6]4– Спектрохимический ряд лигандов: Br – < Cl– < F – < OH– < H 2 O < NH 3 < NO 2– < CN– CO Увеличение силы поля лигандов
Лиганды сильного и слабого поля Fe+II: [Ar] 3 d 64 s 04 p 0 d d диамагн. [Fe(CN)6]4– парамагн. [Fe. F 6]4– Спектрохимический ряд лигандов: Br – < Cl– < F – < OH– < H 2 O < NH 3 < NO 2– < CN– CO Увеличение силы поля лигандов
![[Co(H 2 O)6]2+ розовый [Co(CH 3 COO)2] ярко розовый [Co(NO 2)6]4 оранжевый [Co(NH 3)6]2+ [Co(H 2 O)6]2+ розовый [Co(CH 3 COO)2] ярко розовый [Co(NO 2)6]4 оранжевый [Co(NH 3)6]2+](https://present5.com/presentation/198569245_449820706/image-54.jpg) [Co(H 2 O)6]2+ розовый [Co(CH 3 COO)2] ярко розовый [Co(NO 2)6]4 оранжевый [Co(NH 3)6]2+ буро розовый Усиление поля лигандов Влияние поля лигандов на окраску комплексов
[Co(H 2 O)6]2+ розовый [Co(CH 3 COO)2] ярко розовый [Co(NO 2)6]4 оранжевый [Co(NH 3)6]2+ буро розовый Усиление поля лигандов Влияние поля лигандов на окраску комплексов
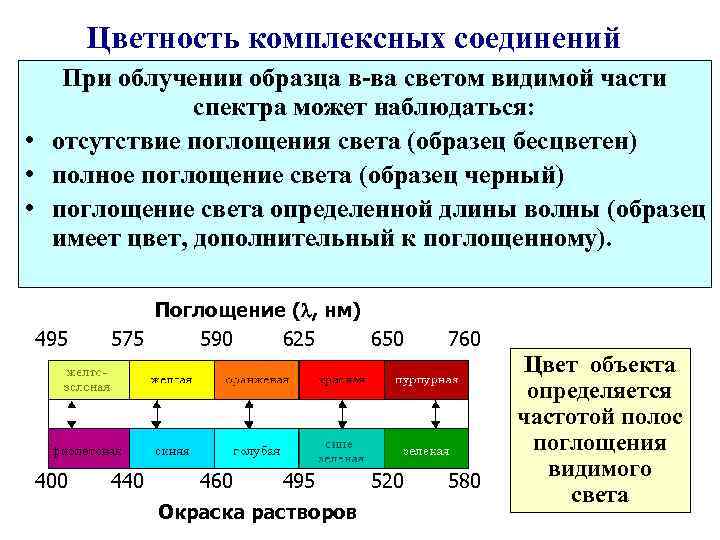 Цветность комплексных соединений При облучении образца в ва светом видимой части спектра может наблюдаться: • отсутствие поглощения света (образец бесцветен) • полное поглощение света (образец черный) • поглощение света определенной длины волны (образец имеет цвет, дополнительный к поглощенному). 495 400 Поглощение ( , нм) 575 590 625 650 440 460 495 Окраска растворов 520 760 580 Цвет объекта определяется частотой полос поглощения видимого света
Цветность комплексных соединений При облучении образца в ва светом видимой части спектра может наблюдаться: • отсутствие поглощения света (образец бесцветен) • полное поглощение света (образец черный) • поглощение света определенной длины волны (образец имеет цвет, дополнительный к поглощенному). 495 400 Поглощение ( , нм) 575 590 625 650 440 460 495 Окраска растворов 520 760 580 Цвет объекта определяется частотой полос поглощения видимого света
![Цветность комплексов фиолет. [Ti(H 2 O)6]3+ бесцв. [Cd(H 2 O)6]2+ d d d + Цветность комплексов фиолет. [Ti(H 2 O)6]3+ бесцв. [Cd(H 2 O)6]2+ d d d +](https://present5.com/presentation/198569245_449820706/image-56.jpg) Цветность комплексов фиолет. [Ti(H 2 O)6]3+ бесцв. [Cd(H 2 O)6]2+ d d d + h Комплекс иодида титана(III) с карбамидом + h d • Комплексы Sc(III), Cu(I), Zn(II), Cd(II) и др. не поглощают энергии в видимой части спектра и поэтому бесцветны.
Цветность комплексов фиолет. [Ti(H 2 O)6]3+ бесцв. [Cd(H 2 O)6]2+ d d d + h Комплекс иодида титана(III) с карбамидом + h d • Комплексы Sc(III), Cu(I), Zn(II), Cd(II) и др. не поглощают энергии в видимой части спектра и поэтому бесцветны.
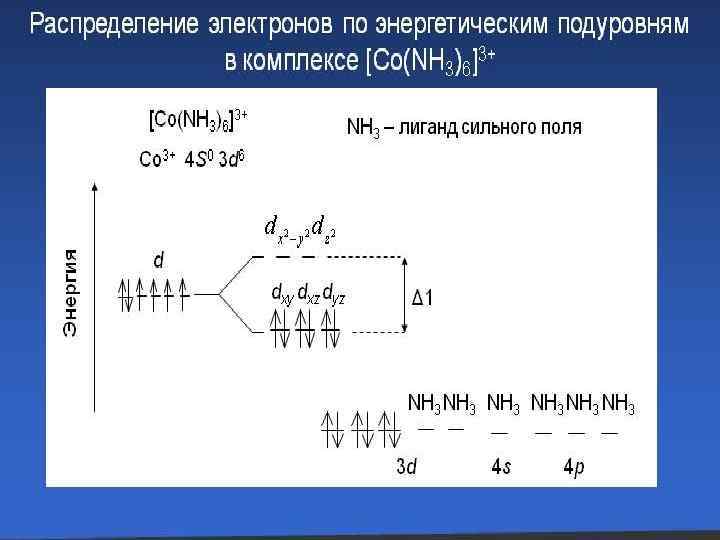

 Изомерия комплексных соединений • Изомерия – явление существования соединений, одинаковых по составу и мол. массе, но различающихся по строению и свойствам (изомеров). В случае комплексных соединений изомерия обусловлена: · различием в строении и координации лигандов · различием в строении внутренней координационной сферы · различным распределением частиц между внутренней и внешней сферой
Изомерия комплексных соединений • Изомерия – явление существования соединений, одинаковых по составу и мол. массе, но различающихся по строению и свойствам (изомеров). В случае комплексных соединений изомерия обусловлена: · различием в строении и координации лигандов · различием в строении внутренней координационной сферы · различным распределением частиц между внутренней и внешней сферой
![Изомерия лигандов • Связевая —NO 2– и —ONO– нитронитрито • [Co(NH 3)5 NO 2]2+ Изомерия лигандов • Связевая —NO 2– и —ONO– нитронитрито • [Co(NH 3)5 NO 2]2+](https://present5.com/presentation/198569245_449820706/image-60.jpg) Изомерия лигандов • Связевая —NO 2– и —ONO– нитронитрито • [Co(NH 3)5 NO 2]2+ (желтокоричн. р-р) • [Co(NH 3)5 ONO]2+ (розов. р-р) —NCS– и —SCN– тиоцианато-N тиоцианато-S • [Cr(H 2 O)5(NCS)]2+ • [Cr(H 2 O)5(SCN)]2+ • Изомерия лигандов Лиганды сложного строения (напр. , аминокислоты) образуют изомеры, координация которых ведет к получению комплексов с разными свойствами.
Изомерия лигандов • Связевая —NO 2– и —ONO– нитронитрито • [Co(NH 3)5 NO 2]2+ (желтокоричн. р-р) • [Co(NH 3)5 ONO]2+ (розов. р-р) —NCS– и —SCN– тиоцианато-N тиоцианато-S • [Cr(H 2 O)5(NCS)]2+ • [Cr(H 2 O)5(SCN)]2+ • Изомерия лигандов Лиганды сложного строения (напр. , аминокислоты) образуют изомеры, координация которых ведет к получению комплексов с разными свойствами.
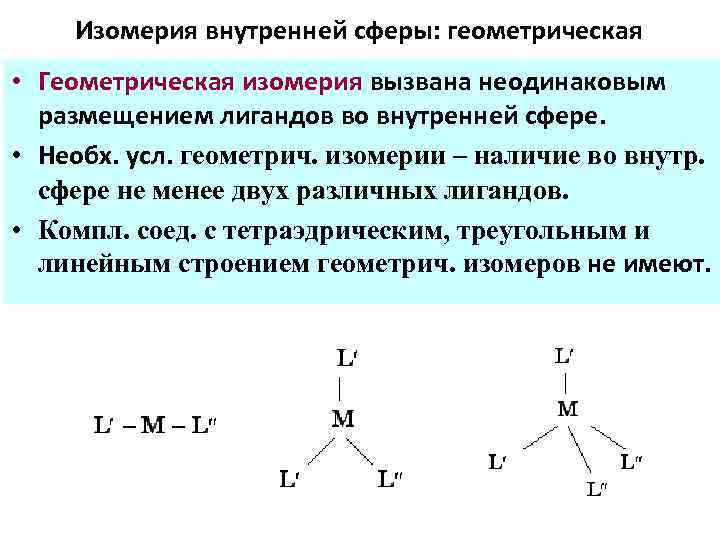 Изомерия внутренней сферы: геометрическая • Геометрическая изомерия вызвана неодинаковым размещением лигандов во внутренней сфере. • Необх. усл. геометрич. изомерии – наличие во внутр. сфере не менее двух различных лигандов. • Компл. соед. с тетраэдрическим, треугольным и линейным строением геометрич. изомеров не имеют.
Изомерия внутренней сферы: геометрическая • Геометрическая изомерия вызвана неодинаковым размещением лигандов во внутренней сфере. • Необх. усл. геометрич. изомерии – наличие во внутр. сфере не менее двух различных лигандов. • Компл. соед. с тетраэдрическим, треугольным и линейным строением геометрич. изомеров не имеют.
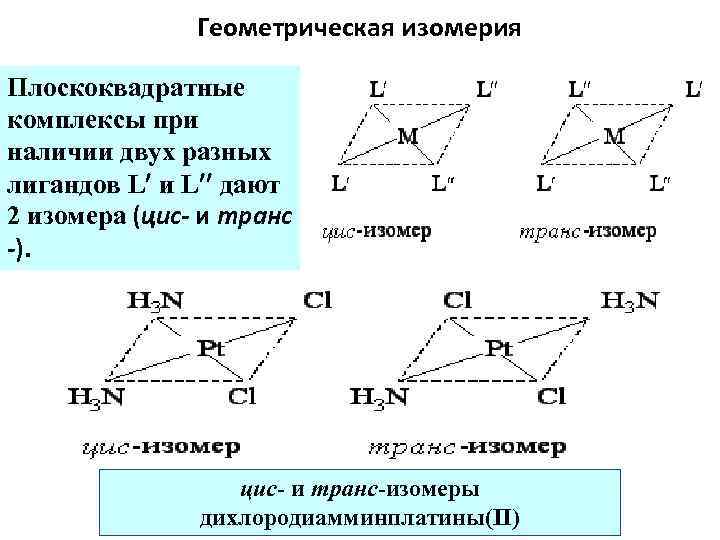 Геометрическая изомерия Плоскоквадратные комплексы при наличии двух разных лигандов L и L дают 2 изомера (цис- и транс -). цис и транс изомеры дихлородиамминплатины(II)
Геометрическая изомерия Плоскоквадратные комплексы при наличии двух разных лигандов L и L дают 2 изомера (цис- и транс -). цис и транс изомеры дихлородиамминплатины(II)
![Геометрическая изомерия [ML 5 L ]: изомеров нет цис и транс изомеры дигидроксотетраамминкобальта(II) Геометрическая изомерия [ML 5 L ]: изомеров нет цис и транс изомеры дигидроксотетраамминкобальта(II)](https://present5.com/presentation/198569245_449820706/image-63.jpg) Геометрическая изомерия [ML 5 L ]: изомеров нет цис и транс изомеры дигидроксотетраамминкобальта(II)
Геометрическая изомерия [ML 5 L ]: изомеров нет цис и транс изомеры дигидроксотетраамминкобальта(II)
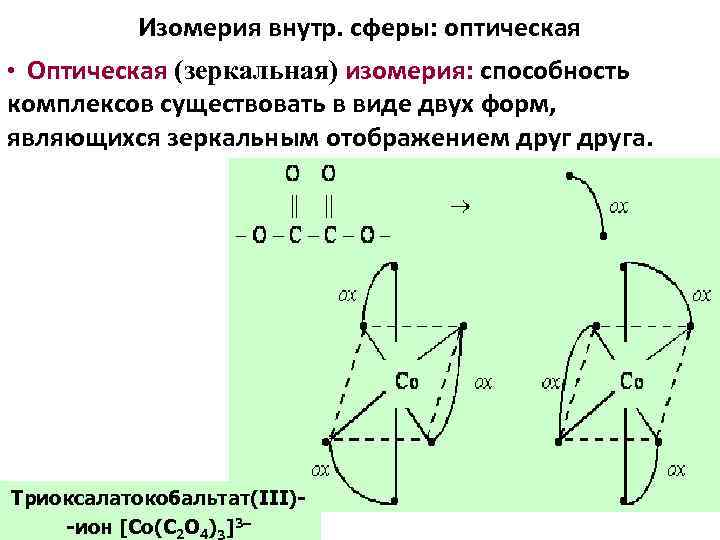 Изомерия внутр. сферы: оптическая • Оптическая (зеркальная) изомерия: способность комплексов существовать в виде двух форм, являющихся зеркальным отображением друга. Триоксалатокобальтат(III)-ион [Co(С 2 O 4)3]3–
Изомерия внутр. сферы: оптическая • Оптическая (зеркальная) изомерия: способность комплексов существовать в виде двух форм, являющихся зеркальным отображением друга. Триоксалатокобальтат(III)-ион [Co(С 2 O 4)3]3–
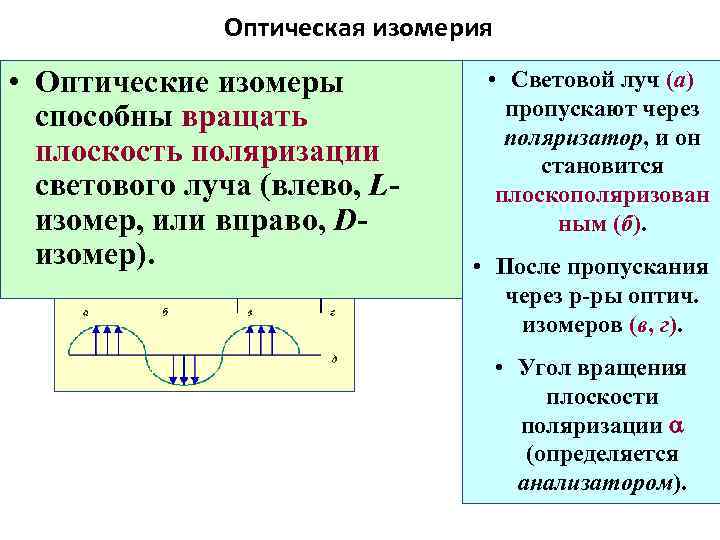 Оптическая изомерия • Оптические изомеры способны вращать плоскость поляризации светового луча (влево, L изомер, или вправо, D изомер). • Световой луч (а) пропускают через поляризатор, и он становится плоскополяризован ным (б). • После пропускания через р ры оптич. изомеров (в, г). • Угол вращения плоскости поляризации a (определяется анализатором).
Оптическая изомерия • Оптические изомеры способны вращать плоскость поляризации светового луча (влево, L изомер, или вправо, D изомер). • Световой луч (а) пропускают через поляризатор, и он становится плоскополяризован ным (б). • После пропускания через р ры оптич. изомеров (в, г). • Угол вращения плоскости поляризации a (определяется анализатором).
![гидратная • [Co(en)2 Cl 2]Cl · H 2 O • 1 Cl–; H 2 гидратная • [Co(en)2 Cl 2]Cl · H 2 O • 1 Cl–; H 2](https://present5.com/presentation/198569245_449820706/image-66.jpg) гидратная • [Co(en)2 Cl 2]Cl · H 2 O • 1 Cl–; H 2 O (Ag. Cl ) • [Co(H 2 O)(en)2 Cl]Cl 2 • 2 Cl– (2 Ag. Cl ) ионная Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия • [Co(NH 3)5 I]SO 4 • [Co(NH 3)5 SO 4]I • SO 42– (Ba. SO 4 ) • I– (Ag. I )
гидратная • [Co(en)2 Cl 2]Cl · H 2 O • 1 Cl–; H 2 O (Ag. Cl ) • [Co(H 2 O)(en)2 Cl]Cl 2 • 2 Cl– (2 Ag. Cl ) ионная Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия • [Co(NH 3)5 I]SO 4 • [Co(NH 3)5 SO 4]I • SO 42– (Ba. SO 4 ) • I– (Ag. I )
![Междусферная изомерия • Ионные (ионизационные) изомеры • [Pt(NH 3)4 Cl 2]Br 2 и [Pt(NH Междусферная изомерия • Ионные (ионизационные) изомеры • [Pt(NH 3)4 Cl 2]Br 2 и [Pt(NH](https://present5.com/presentation/198569245_449820706/image-67.jpg) Междусферная изомерия • Ионные (ионизационные) изомеры • [Pt(NH 3)4 Cl 2]Br 2 и [Pt(NH 3)4 Br 2]Cl 2 • [Pt(NH 3)4 SO 4](OH)2 и [Pt(NH 3)4(OH)2]SO 4 p. H 7 • Координационные изомеры • [Cr(NH 3)4(NCS)2] [Cr(NH 3)2(NCS)4] • [Cr(NH 3)6] [Cr(NCS)6]
Междусферная изомерия • Ионные (ионизационные) изомеры • [Pt(NH 3)4 Cl 2]Br 2 и [Pt(NH 3)4 Br 2]Cl 2 • [Pt(NH 3)4 SO 4](OH)2 и [Pt(NH 3)4(OH)2]SO 4 p. H 7 • Координационные изомеры • [Cr(NH 3)4(NCS)2] [Cr(NH 3)2(NCS)4] • [Cr(NH 3)6] [Cr(NCS)6]
![Диссоциация комплексных соединений Hg. I 2 KI K 2[Hg. I 4] Диссоциация комплексных соединений Hg. I 2 KI K 2[Hg. I 4]](https://present5.com/presentation/198569245_449820706/image-68.jpg) Диссоциация комплексных соединений Hg. I 2 KI K 2[Hg. I 4]
Диссоциация комплексных соединений Hg. I 2 KI K 2[Hg. I 4]
![Ковалентная (диссоциация по типу слабого электролита) K 4 [Fe(CN)6] Ионная связь (диссоциация по типу Ковалентная (диссоциация по типу слабого электролита) K 4 [Fe(CN)6] Ионная связь (диссоциация по типу](https://present5.com/presentation/198569245_449820706/image-69.jpg) Ковалентная (диссоциация по типу слабого электролита) K 4 [Fe(CN)6] Ионная связь (диссоциация по типу сильного электролита)
Ковалентная (диссоциация по типу слабого электролита) K 4 [Fe(CN)6] Ионная связь (диссоциация по типу сильного электролита)
![K 4 [Fe(CN)6] 4 K+ + [Fe(CN)6 ] 4 первичная диссоциация K 4 [Fe(CN)6] 4 K+ + [Fe(CN)6 ] 4 первичная диссоциация](https://present5.com/presentation/198569245_449820706/image-70.jpg) K 4 [Fe(CN)6] 4 K+ + [Fe(CN)6 ] 4 первичная диссоциация
K 4 [Fe(CN)6] 4 K+ + [Fe(CN)6 ] 4 первичная диссоциация
![[Fe(CN)6 ] вторичная диссоциация 4 2+ Fe +6(CN) Константа нестойкости (Кн): Кн = [Fe [Fe(CN)6 ] вторичная диссоциация 4 2+ Fe +6(CN) Константа нестойкости (Кн): Кн = [Fe](https://present5.com/presentation/198569245_449820706/image-71.jpg) [Fe(CN)6 ] вторичная диссоциация 4 2+ Fe +6(CN) Константа нестойкости (Кн): Кн = [Fe 2+] · [CN ]6 [[Fe (CN)6] 4 ] Kн = 110 31 (очень прочный комплекс)
[Fe(CN)6 ] вторичная диссоциация 4 2+ Fe +6(CN) Константа нестойкости (Кн): Кн = [Fe 2+] · [CN ]6 [[Fe (CN)6] 4 ] Kн = 110 31 (очень прочный комплекс)
![[Ni(NH 3)6]2+ Кн = 2· 10 -9 (непрочный комплекс) Куст. =1/ Кн [Ni(NH 3)6]2+ Кн = 2· 10 -9 (непрочный комплекс) Куст. =1/ Кн](https://present5.com/presentation/198569245_449820706/image-72.jpg) [Ni(NH 3)6]2+ Кн = 2· 10 -9 (непрочный комплекс) Куст. =1/ Кн
[Ni(NH 3)6]2+ Кн = 2· 10 -9 (непрочный комплекс) Куст. =1/ Кн
 Кн и Ку (β)относятся только к комплексному иону! Не забывайте !
Кн и Ку (β)относятся только к комплексному иону! Не забывайте !
 Правило циклов Чугаева Наибольшей устойчивостью обладают пяти- и шестичленные металлоциклы. Соединения с трех-, четырехчленными циклами и с числом звеньев больше семи образуются редко из-за их малой устойчивости. Стабильность хелатных комплексов возрастает с увеличением числа металлоциклов в комплексе.
Правило циклов Чугаева Наибольшей устойчивостью обладают пяти- и шестичленные металлоциклы. Соединения с трех-, четырехчленными циклами и с числом звеньев больше семи образуются редко из-за их малой устойчивости. Стабильность хелатных комплексов возрастает с увеличением числа металлоциклов в комплексе.
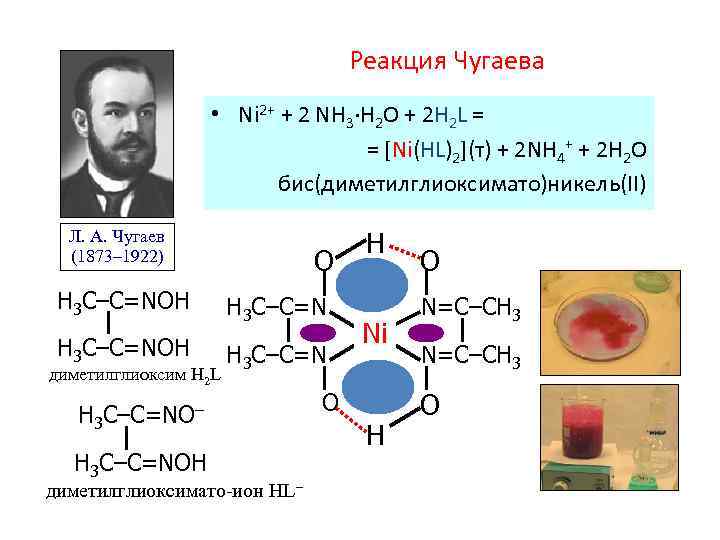 Реакция Чугаева • Ni 2+ + 2 NH 3·H 2 O + 2 H 2 L = = [Ni(HL)2](т) + 2 NH 4+ + 2 H 2 O бис(диметилглиоксимато)никель(II) Л. А. Чугаев (1873– 1922) O H 3 C–C=NOH H 3 C–C=N диметилглиоксим H 2 L H 3 C–C=NO– H 3 C–C=NOH диметилглиоксимато ион HL– H Ni O H O N=C–CH 3 O
Реакция Чугаева • Ni 2+ + 2 NH 3·H 2 O + 2 H 2 L = = [Ni(HL)2](т) + 2 NH 4+ + 2 H 2 O бис(диметилглиоксимато)никель(II) Л. А. Чугаев (1873– 1922) O H 3 C–C=NOH H 3 C–C=N диметилглиоксим H 2 L H 3 C–C=NO– H 3 C–C=NOH диметилглиоксимато ион HL– H Ni O H O N=C–CH 3 O
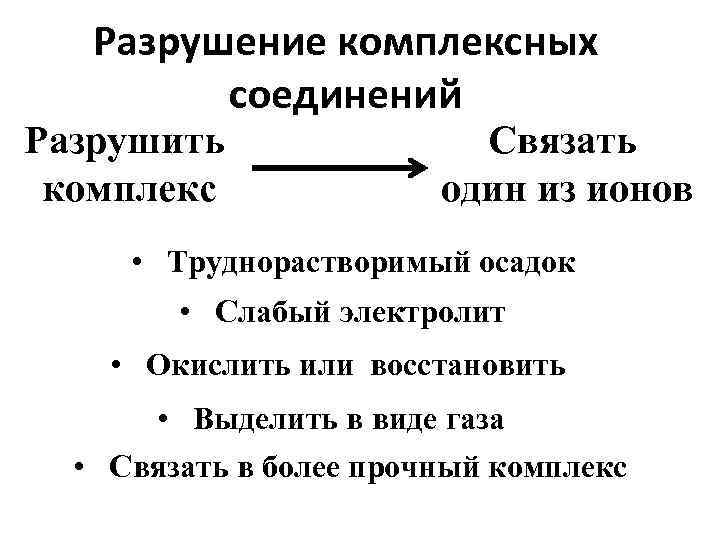 Разрушение комплексных соединений Разрушить комплекс Связать один из ионов • Труднорастворимый осадок • Слабый электролит • Окислить или восстановить • Выделить в виде газа • Связать в более прочный комплекс
Разрушение комплексных соединений Разрушить комплекс Связать один из ионов • Труднорастворимый осадок • Слабый электролит • Окислить или восстановить • Выделить в виде газа • Связать в более прочный комплекс
![[Ag (NH 3)2]+ Ag+ + 2 NH 3 Кн = 9, 3 -8 ·10 [Ag (NH 3)2]+ Ag+ + 2 NH 3 Кн = 9, 3 -8 ·10](https://present5.com/presentation/198569245_449820706/image-77.jpg) [Ag (NH 3)2]+ Ag+ + 2 NH 3 Кн = 9, 3 -8 ·10
[Ag (NH 3)2]+ Ag+ + 2 NH 3 Кн = 9, 3 -8 ·10
![++ KI =Ag. I + NH [Ag (NH 3)2] 3 + +K -16 Кs(Ag. ++ KI =Ag. I + NH [Ag (NH 3)2] 3 + +K -16 Кs(Ag.](https://present5.com/presentation/198569245_449820706/image-78.jpg) ++ KI =Ag. I + NH [Ag (NH 3)2] 3 + +K -16 Кs(Ag. I) = 1, 5·10 [Ag (NH 3)2]++2 CN = [Ag(CN)2] +2 NH 3 Кн = 8·10 22
++ KI =Ag. I + NH [Ag (NH 3)2] 3 + +K -16 Кs(Ag. I) = 1, 5·10 [Ag (NH 3)2]++2 CN = [Ag(CN)2] +2 NH 3 Кн = 8·10 22
![[Ag (NH 3)2 + ] + Ag + KI + 2 NH 3 + [Ag (NH 3)2 + ] + Ag + KI + 2 NH 3 +](https://present5.com/presentation/198569245_449820706/image-79.jpg) [Ag (NH 3)2 + ] + Ag + KI + 2 NH 3 + HNO 3 Образование труднорастворимого осадка + KCN NH 4 NO 3 Образование более прочного комплекса
[Ag (NH 3)2 + ] + Ag + KI + 2 NH 3 + HNO 3 Образование труднорастворимого осадка + KCN NH 4 NO 3 Образование более прочного комплекса
 Использование реакций комплексообразования в фармацевтическом анализе: Для обнаружения ионов. Например, ионы кобальта (II) можно от рыть реакцией с рубеановодородной кислотой в результате которой образуется коричнево желтый осадок H 2 N – C–NH 2 || || S S HN = C – C = NH + Co 2+ HN = C – C = NH + H+ | | HS SH S S Co Для разделения ионов. Так, если надо ионы Cu 2+ и Мg 2+ отделить друг от друга, то в раствор, содержащий их, добавляют избыток NН 4 ОН. При этом ионы меди (II) переходят в раствор в виде тетраамминмеди (II), а катионы Мg 2+ осаждаются в гидроксид магния Мg(ОН)2.
Использование реакций комплексообразования в фармацевтическом анализе: Для обнаружения ионов. Например, ионы кобальта (II) можно от рыть реакцией с рубеановодородной кислотой в результате которой образуется коричнево желтый осадок H 2 N – C–NH 2 || || S S HN = C – C = NH + Co 2+ HN = C – C = NH + H+ | | HS SH S S Co Для разделения ионов. Так, если надо ионы Cu 2+ и Мg 2+ отделить друг от друга, то в раствор, содержащий их, добавляют избыток NН 4 ОН. При этом ионы меди (II) переходят в раствор в виде тетраамминмеди (II), а катионы Мg 2+ осаждаются в гидроксид магния Мg(ОН)2.
 Для маскировки мешающих ионов. Например, при обнаружении ионов Ni 2+ в присутствии Fе 3+, последний связывают в устойчивый комплексный ион гексафтороферрат (III): Fe 3+ + 6 F [Fe. F 6]3 После маскировки Fе 3+ проводят аналитические реакции на ионы ни келя (II). Для растворения осадков. Так, при добавлении к хлориду се ребра концентрированной хлороводородной кислоты осадок Аg. Сl раст воряется : Ag. Cl + 2 HCl H 2[ Ag. Cl 3 ]
Для маскировки мешающих ионов. Например, при обнаружении ионов Ni 2+ в присутствии Fе 3+, последний связывают в устойчивый комплексный ион гексафтороферрат (III): Fe 3+ + 6 F [Fe. F 6]3 После маскировки Fе 3+ проводят аналитические реакции на ионы ни келя (II). Для растворения осадков. Так, при добавлении к хлориду се ребра концентрированной хлороводородной кислоты осадок Аg. Сl раст воряется : Ag. Cl + 2 HCl H 2[ Ag. Cl 3 ]
 Для изменения окислительно восстановительных свойств ионов. Например, молибден (VI) в виде Мо. О 3 Н 2 О не окисляет бензидин, а комплексный ион [P( Mo 2 O 7)6]7 по отношению к нему является окислителем. В экстракционном концентрировании и разделении веществ полу чают нейтральные комплексы, способные переходить из воды в органи ческий растворитель, не смешивающийся с ней. Для количественного определения различных химических соеди нений в том числе и лекарственных веществ, в состав которых вхо дят анионы, способные образовывать с титрантом комплексные соеди нения. Для этой цели применяют такие методы, как комплексонометрия, куприметрия и другие.
Для изменения окислительно восстановительных свойств ионов. Например, молибден (VI) в виде Мо. О 3 Н 2 О не окисляет бензидин, а комплексный ион [P( Mo 2 O 7)6]7 по отношению к нему является окислителем. В экстракционном концентрировании и разделении веществ полу чают нейтральные комплексы, способные переходить из воды в органи ческий растворитель, не смешивающийся с ней. Для количественного определения различных химических соеди нений в том числе и лекарственных веществ, в состав которых вхо дят анионы, способные образовывать с титрантом комплексные соеди нения. Для этой цели применяют такие методы, как комплексонометрия, куприметрия и другие.
 Биологическая роль комплексных соединений
Биологическая роль комплексных соединений
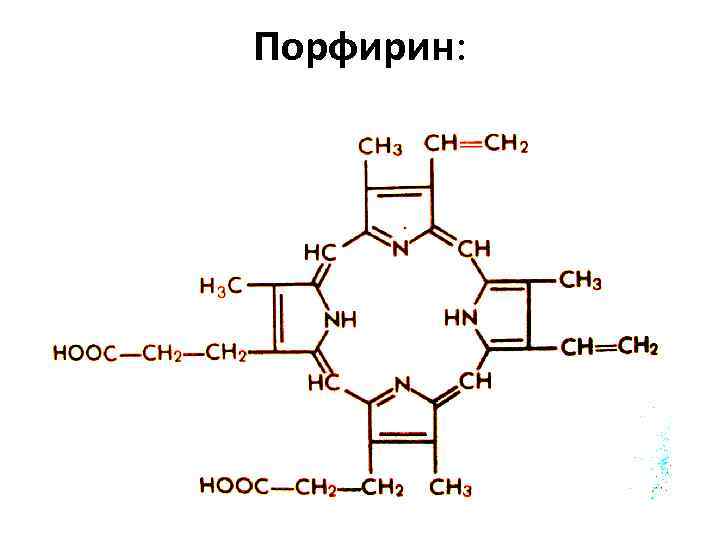 Порфирин:
Порфирин:
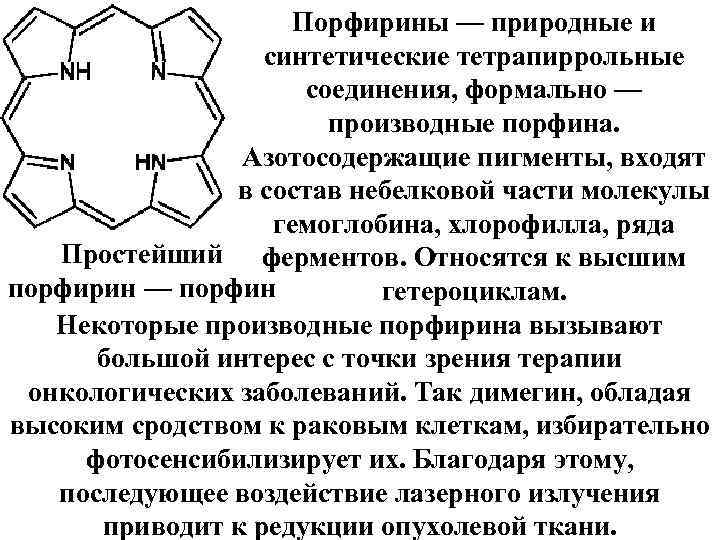 Порфирины — природные и синтетические тетрапиррольные соединения, формально — производные порфина. Азотосодержащие пигменты, входят в состав небелковой части молекулы гемоглобина, хлорофилла, ряда Простейший ферментов. Относятся к высшим порфирин — порфин гетероциклам. Некоторые производные порфирина вызывают большой интерес с точки зрения терапии онкологических заболеваний. Так димегин, обладая высоким сродством к раковым клеткам, избирательно фотосенсибилизирует их. Благодаря этому, последующее воздействие лазерного излучения приводит к редукции опухолевой ткани.
Порфирины — природные и синтетические тетрапиррольные соединения, формально — производные порфина. Азотосодержащие пигменты, входят в состав небелковой части молекулы гемоглобина, хлорофилла, ряда Простейший ферментов. Относятся к высшим порфирин — порфин гетероциклам. Некоторые производные порфирина вызывают большой интерес с точки зрения терапии онкологических заболеваний. Так димегин, обладая высоким сродством к раковым клеткам, избирательно фотосенсибилизирует их. Благодаря этому, последующее воздействие лазерного излучения приводит к редукции опухолевой ткани.
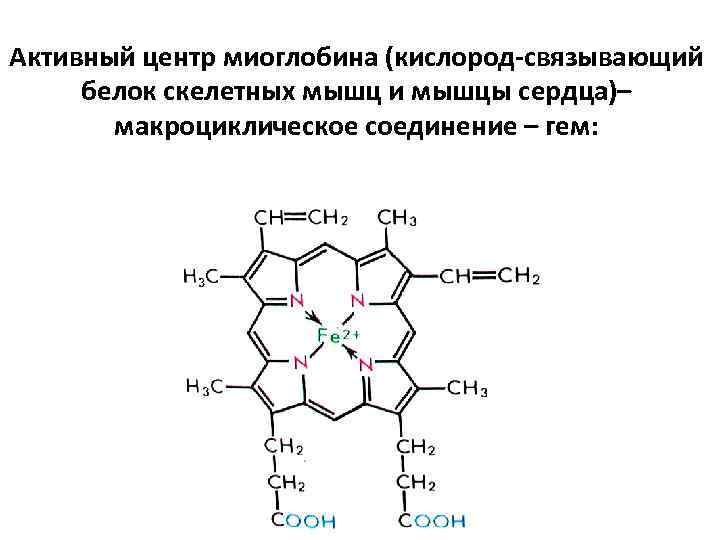 Активный центр миоглобина (кислород-связывающий белок скелетных мышц и мышцы сердца)– макроциклическое соединение – гем:
Активный центр миоглобина (кислород-связывающий белок скелетных мышц и мышцы сердца)– макроциклическое соединение – гем:
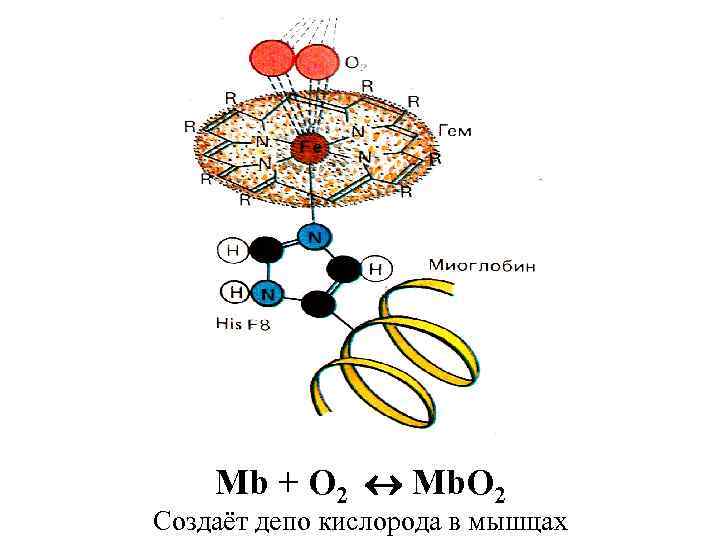 Mb + O 2 Mb. O 2 Создаёт депо кислорода в мышцах
Mb + O 2 Mb. O 2 Создаёт депо кислорода в мышцах
 Гемоглобин: Hb + 4 O 2 Hb (O 2)4
Гемоглобин: Hb + 4 O 2 Hb (O 2)4
 Молекула гемоглобина: 4 субъединицы глобина, окрашены в разные цвета
Молекула гемоглобина: 4 субъединицы глобина, окрашены в разные цвета
 Гемоглоби н (от др. греч. αἷμα — кровь и лат. globus — шар) — сложный железосодержащий белок. Главная функция гемоглобина заключается в трех этапах, определяющих три его свойства. 1 ый этап присоединение O 2 к гемоглобину. 2 ой образование сложных взаимоотношений между гемом и O 2, а именно превращение O 2 в синглетный кислород. Данный этап является этапом трансформации O 2 в его реакционно способную форму, необходимую для дальнейшего взаимодействия с клетками и является главной функцией гемоглобина. 3 ий этап отдача синглетного кислорода в ткани. У человека в капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином. Током крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где O 2 мало; здесь необходимый для протекания окислительных процессов кислород освобождается из связи с гемоглобином.
Гемоглоби н (от др. греч. αἷμα — кровь и лат. globus — шар) — сложный железосодержащий белок. Главная функция гемоглобина заключается в трех этапах, определяющих три его свойства. 1 ый этап присоединение O 2 к гемоглобину. 2 ой образование сложных взаимоотношений между гемом и O 2, а именно превращение O 2 в синглетный кислород. Данный этап является этапом трансформации O 2 в его реакционно способную форму, необходимую для дальнейшего взаимодействия с клетками и является главной функцией гемоглобина. 3 ий этап отдача синглетного кислорода в ткани. У человека в капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином. Током крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где O 2 мало; здесь необходимый для протекания окислительных процессов кислород освобождается из связи с гемоглобином.
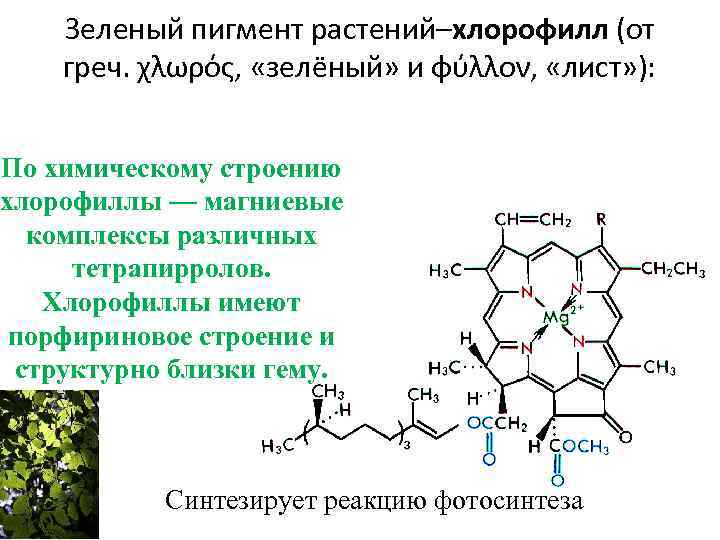 Зеленый пигмент растений–хлорофилл (от греч. χλωρός, «зелёный» и φύλλον, «лист» ): По химическому строению хлорофиллы — магниевые комплексы различных тетрапирролов. Хлорофиллы имеют порфириновое строение и структурно близки гему. Синтезирует реакцию фотосинтеза
Зеленый пигмент растений–хлорофилл (от греч. χλωρός, «зелёный» и φύλλον, «лист» ): По химическому строению хлорофиллы — магниевые комплексы различных тетрапирролов. Хлорофиллы имеют порфириновое строение и структурно близки гему. Синтезирует реакцию фотосинтеза
 Применение комплексных соединений в медицине
Применение комплексных соединений в медицине
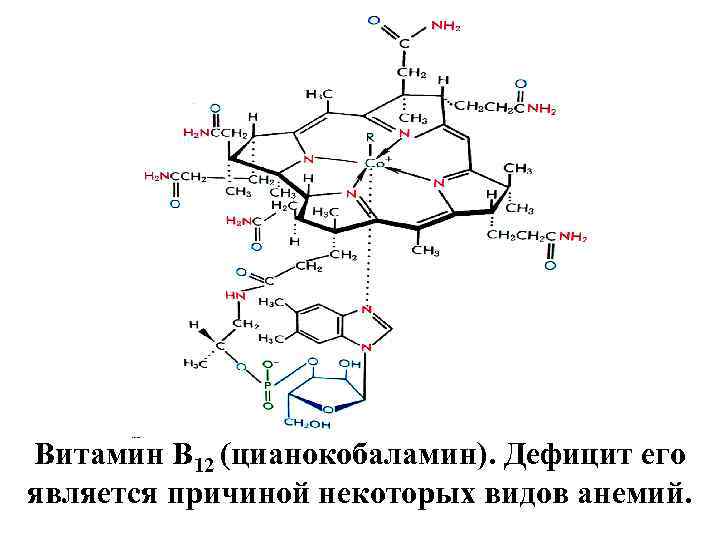 Витамин В 12 (цианокобаламин). Дефицит его является причиной некоторых видов анемий.
Витамин В 12 (цианокобаламин). Дефицит его является причиной некоторых видов анемий.
 Унитиол - антидот при отравлениях соединениями мышьяка, ртути и солями тяжелых металлов) Меркаптидная связь
Унитиол - антидот при отравлениях соединениями мышьяка, ртути и солями тяжелых металлов) Меркаптидная связь
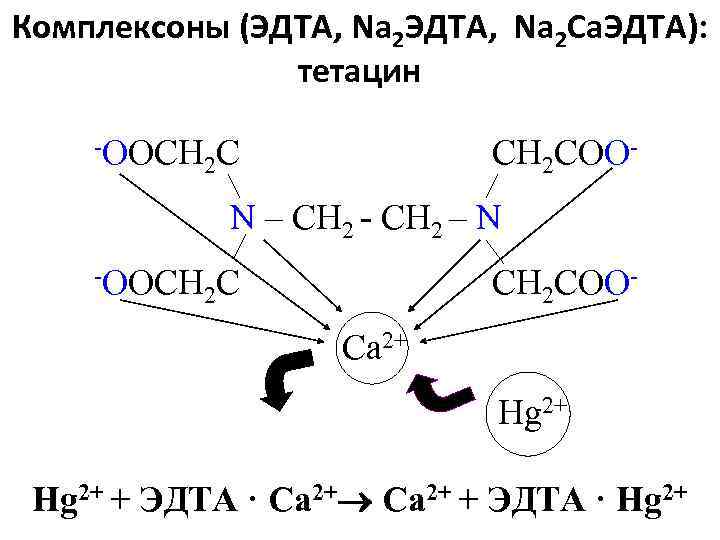 Комплексоны (ЭДТА, Na 2 Ca. ЭДТА): тетацин OOCH 2 COO N – CH 2 – N OOCH 2 COO Сa 2+ Hg 2+ + ЭДТА · Ca 2+ + ЭДТА · Hg 2+
Комплексоны (ЭДТА, Na 2 Ca. ЭДТА): тетацин OOCH 2 COO N – CH 2 – N OOCH 2 COO Сa 2+ Hg 2+ + ЭДТА · Ca 2+ + ЭДТА · Hg 2+
![Противоопухолевый препарат: цисизомер дихлородиамминплатины ЦИСПЛАТИН — цитотоксический препарат алкилирующего действия [Pt(NH 3)2 Cl 2] Противоопухолевый препарат: цисизомер дихлородиамминплатины ЦИСПЛАТИН — цитотоксический препарат алкилирующего действия [Pt(NH 3)2 Cl 2]](https://present5.com/presentation/198569245_449820706/image-96.jpg) Противоопухолевый препарат: цисизомер дихлородиамминплатины ЦИСПЛАТИН — цитотоксический препарат алкилирующего действия [Pt(NH 3)2 Cl 2]
Противоопухолевый препарат: цисизомер дихлородиамминплатины ЦИСПЛАТИН — цитотоксический препарат алкилирующего действия [Pt(NH 3)2 Cl 2]



