Классификация органических веществ и реакций.ppt
- Количество слайдов: 108
 Лекция Классификация органических веществ Классификация химических реакций
Лекция Классификация органических веществ Классификация химических реакций
 План 1. Классификация органических веществ 2. Номенклатура органических соединений 3. Классификация реакций в органической химии
План 1. Классификация органических веществ 2. Номенклатура органических соединений 3. Классификация реакций в органической химии
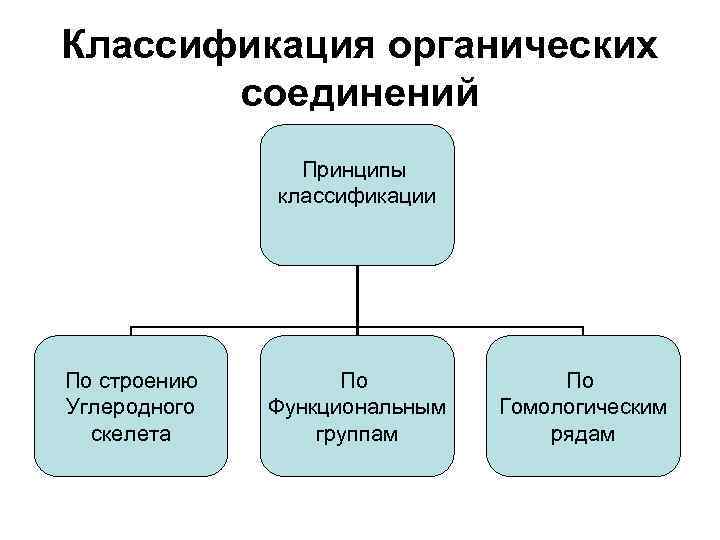 Классификация органических соединений Принципы классификации По строению Углеродного скелета По Функциональным группам По Гомологическим рядам
Классификация органических соединений Принципы классификации По строению Углеродного скелета По Функциональным группам По Гомологическим рядам
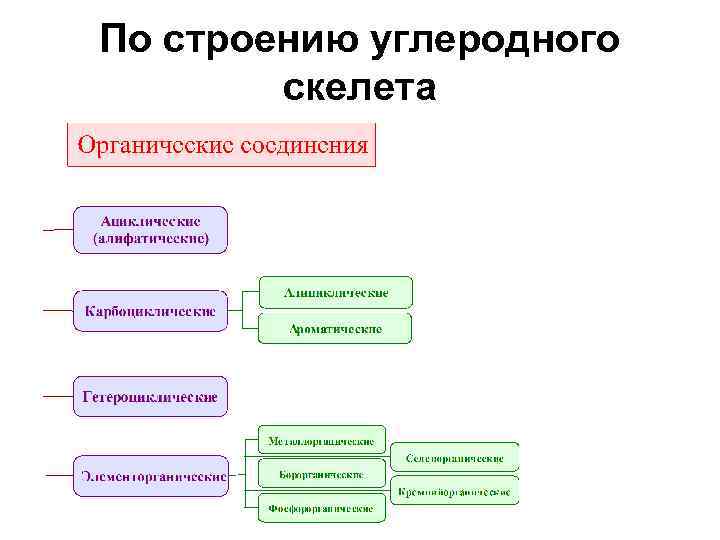 По строению углеродного скелета
По строению углеродного скелета
 По функциональным группам • • • углеводороды (R-Н) галогенуглеводороды (R-Hаl) спирты (R-ОН) альдегиды (R-CН=О) кетоны (RR’C=О) кислоты (R-СОOH)
По функциональным группам • • • углеводороды (R-Н) галогенуглеводороды (R-Hаl) спирты (R-ОН) альдегиды (R-CН=О) кетоны (RR’C=О) кислоты (R-СОOH)
 По функциональным группам • • простые эфиры (ROR’) сложные эфиры (RCОOR’) амины (R-NH 2) и др.
По функциональным группам • • простые эфиры (ROR’) сложные эфиры (RCОOR’) амины (R-NH 2) и др.
 По гомологическим рядам • Ряд соединений, сходных по химическим свойствам, имеющих общую эмпирическую формулу, в которой каждый последующий член отличается от предыдущего на группу СН 2 (гомологическая разность), называется гомологическим рядом
По гомологическим рядам • Ряд соединений, сходных по химическим свойствам, имеющих общую эмпирическую формулу, в которой каждый последующий член отличается от предыдущего на группу СН 2 (гомологическая разность), называется гомологическим рядом
 По гомологическим рядам • Алканы Сn. H 2 n+2 • Циклоалканы Сn. H 2 n • Алкены Сn. H 2 n • Алкадиены Сn. H 2 n-2 • Алкины Сn. H 2 n-2 • Арены (ароматические): ряд бензола Сn. H 2 n-6 полиядерные и конденсированные
По гомологическим рядам • Алканы Сn. H 2 n+2 • Циклоалканы Сn. H 2 n • Алкены Сn. H 2 n • Алкадиены Сn. H 2 n-2 • Алкины Сn. H 2 n-2 • Арены (ароматические): ряд бензола Сn. H 2 n-6 полиядерные и конденсированные
 Гомологические ряды • Предельные спирты Сn. H 2 n+1 OH • Предельные кислоты Сn. H 2 n+1 СООН • Ароматические кислоты ряда бензола Сn. H 2 n-7 СООН
Гомологические ряды • Предельные спирты Сn. H 2 n+1 OH • Предельные кислоты Сn. H 2 n+1 СООН • Ароматические кислоты ряда бензола Сn. H 2 n-7 СООН
 Номенклатура органических соединений • Тривиальная • Рациональная • Систематическая (заместительная и радикально – функциональная)
Номенклатура органических соединений • Тривиальная • Рациональная • Систематическая (заместительная и радикально – функциональная)
 Тривиальная номенклатура – чаще всего связана с источниками получения, запахом, цветом или другими особенностями, но ничего не связано с химическим строением органического вещества (муравьиная кислота, уксусная кислота, бензол, масляная кислота и другие)
Тривиальная номенклатура – чаще всего связана с источниками получения, запахом, цветом или другими особенностями, но ничего не связано с химическим строением органического вещества (муравьиная кислота, уксусная кислота, бензол, масляная кислота и другие)
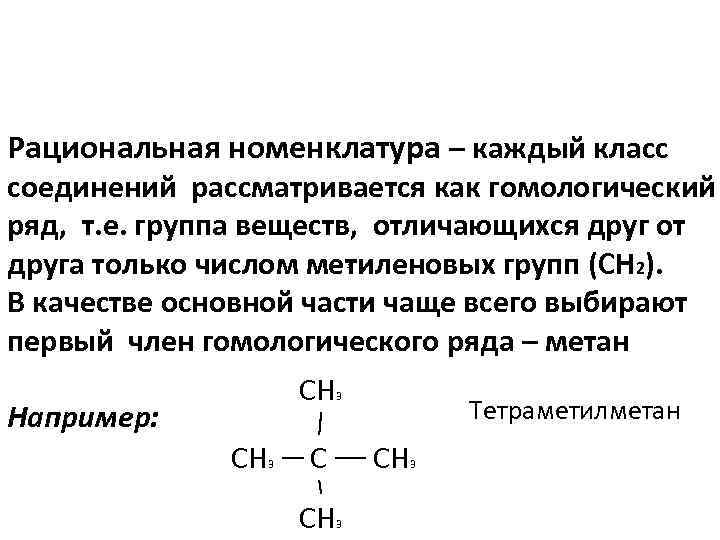 Рациональная номенклатура – каждый класс соединений рассматривается как гомологический ряд, т. е. группа веществ, отличающихся друг от друга только числом метиленовых групп (СН 2). В качестве основной части чаще всего выбирают первый член гомологического ряда – метан 3 СН Например: СН 3 3 С СН Тетраметилметан СН 3 3
Рациональная номенклатура – каждый класс соединений рассматривается как гомологический ряд, т. е. группа веществ, отличающихся друг от друга только числом метиленовых групп (СН 2). В качестве основной части чаще всего выбирают первый член гомологического ряда – метан 3 СН Например: СН 3 3 С СН Тетраметилметан СН 3 3
 Систематическая (заместительная) – номенклатура Международного химического союза (1930 г. ), дополненная на съездах теоретической и прикладной химии в 1957 и 1965 г. (ИЮПАК). Номенклатура ИЮПАК наиболее распространена в настоящее время.
Систематическая (заместительная) – номенклатура Международного химического союза (1930 г. ), дополненная на съездах теоретической и прикладной химии в 1957 и 1965 г. (ИЮПАК). Номенклатура ИЮПАК наиболее распространена в настоящее время.
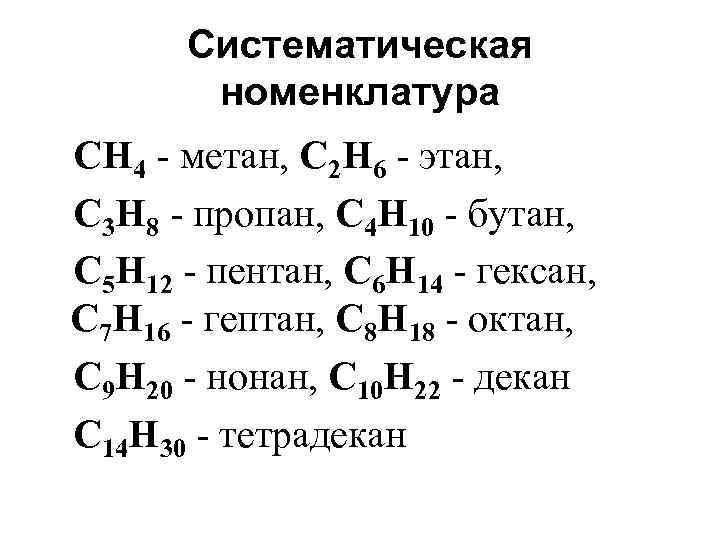 Систематическая номенклатура СН 4 - метан, С 2 Н 6 - этан, С 3 Н 8 - пропан, С 4 Н 10 - бутан, С 5 Н 12 - пентан, С 6 Н 14 - гексан, С 7 Н 16 - гептан, С 8 Н 18 - октан, С 9 Н 20 - нонан, С 10 Н 22 - декан C 14 H 30 - тетрадекан
Систематическая номенклатура СН 4 - метан, С 2 Н 6 - этан, С 3 Н 8 - пропан, С 4 Н 10 - бутан, С 5 Н 12 - пентан, С 6 Н 14 - гексан, С 7 Н 16 - гептан, С 8 Н 18 - октан, С 9 Н 20 - нонан, С 10 Н 22 - декан C 14 H 30 - тетрадекан
 Систематическая номенклатура • Выбирается самая длинная неразветвленная углеродная цепь • Нумеруются атомы углерода этой цепи с того конца, к которому ближе разветвление цепи (заместители, кратная связь)
Систематическая номенклатура • Выбирается самая длинная неразветвленная углеродная цепь • Нумеруются атомы углерода этой цепи с того конца, к которому ближе разветвление цепи (заместители, кратная связь)
 Систематическая номенклатура • Одинаковые заместители группируются (указываются в названии один раз) • В названии цифрой (цифрами) указывается место радикала (заместителя), называется заместитель и его количество, а затем называется углеводород, которому отвечает самая длинная углерод-углеродная цепь
Систематическая номенклатура • Одинаковые заместители группируются (указываются в названии один раз) • В названии цифрой (цифрами) указывается место радикала (заместителя), называется заместитель и его количество, а затем называется углеводород, которому отвечает самая длинная углерод-углеродная цепь
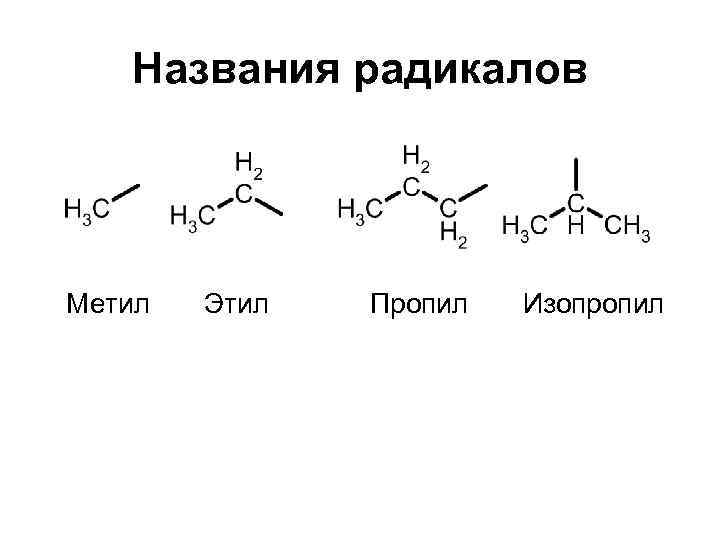 Названия радикалов Метил Этил Пропил Изопропил
Названия радикалов Метил Этил Пропил Изопропил
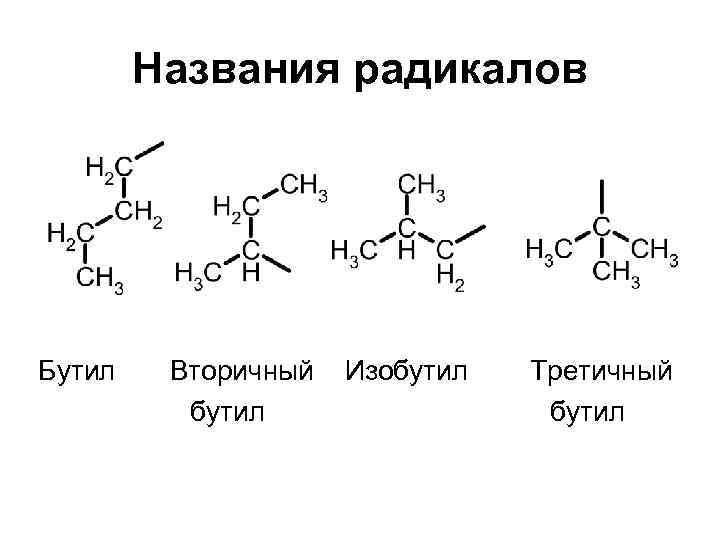 Названия радикалов Бутил Вторичный Изобутил Третичный бутил
Названия радикалов Бутил Вторичный Изобутил Третичный бутил
 Систематическая номенклатура • В названиях соединений с кратными углерод-углеродными связями заменяют суффикс “ан” на “ен” или “ин” • Для некоторых классов соединений к названию основной цепи добавляют суффиксы «ол» , «он» и др.
Систематическая номенклатура • В названиях соединений с кратными углерод-углеродными связями заменяют суффикс “ан” на “ен” или “ин” • Для некоторых классов соединений к названию основной цепи добавляют суффиксы «ол» , «он» и др.
 Изомерия • Изомеры - это соединения, имеющие одинаковый состав, но различное строение и вследствие этого разные физико-химические свойства
Изомерия • Изомеры - это соединения, имеющие одинаковый состав, но различное строение и вследствие этого разные физико-химические свойства
 Изомеры • Структурные (отличаются друг от друга способом связывания атомов) • Пространственные (соединения, имеющие одинаковый способ связывания атомов, но различное расположение атомов и групп в пространстве)
Изомеры • Структурные (отличаются друг от друга способом связывания атомов) • Пространственные (соединения, имеющие одинаковый способ связывания атомов, но различное расположение атомов и групп в пространстве)
 Структурная изомерия • Изомерия углеродного скелета • Изомерия положения кратной связи • Изомерия положения функциональной группы • Межклассовая изомерия
Структурная изомерия • Изомерия углеродного скелета • Изомерия положения кратной связи • Изомерия положения функциональной группы • Межклассовая изомерия
 Структурная изомерия Изомерия положения функциональной группы бутанол-1 бутен-1 бутанол-2 бутен-2
Структурная изомерия Изомерия положения функциональной группы бутанол-1 бутен-1 бутанол-2 бутен-2
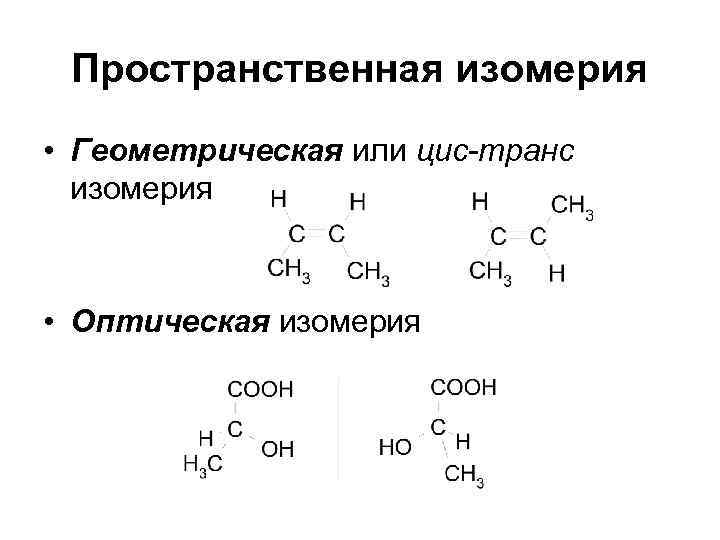 Пространственная изомерия • Геометрическая или цис-транс изомерия • Оптическая изомерия
Пространственная изомерия • Геометрическая или цис-транс изомерия • Оптическая изомерия
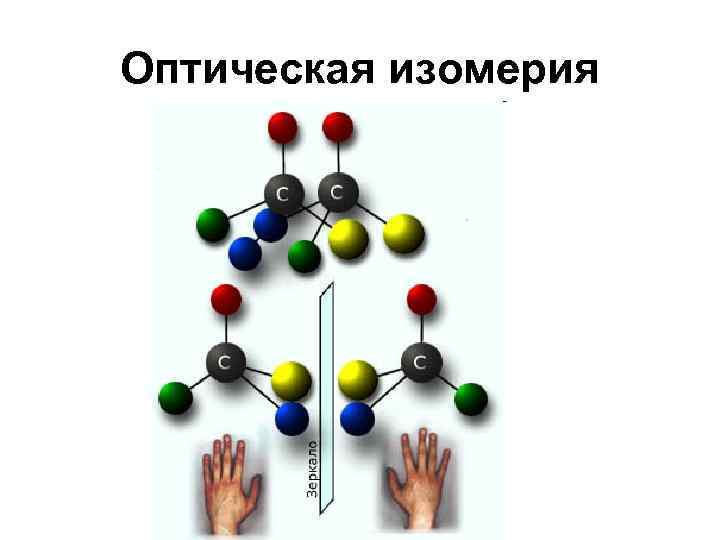 Оптическая изомерия
Оптическая изомерия
 Химическая связь в органических соединениях • Ковалентная связь – образуется обобщением пары валентных электронов с противоположными спинами: А + В А В Донорно-акцепторный механизм образования А: + В А: В
Химическая связь в органических соединениях • Ковалентная связь – образуется обобщением пары валентных электронов с противоположными спинами: А + В А В Донорно-акцепторный механизм образования А: + В А: В
 Химическая связь в органических соединениях Ковалентная связь: • -связь – перекрывание орбиталей вдоль линии, связывающей центры атомов
Химическая связь в органических соединениях Ковалентная связь: • -связь – перекрывание орбиталей вдоль линии, связывающей центры атомов
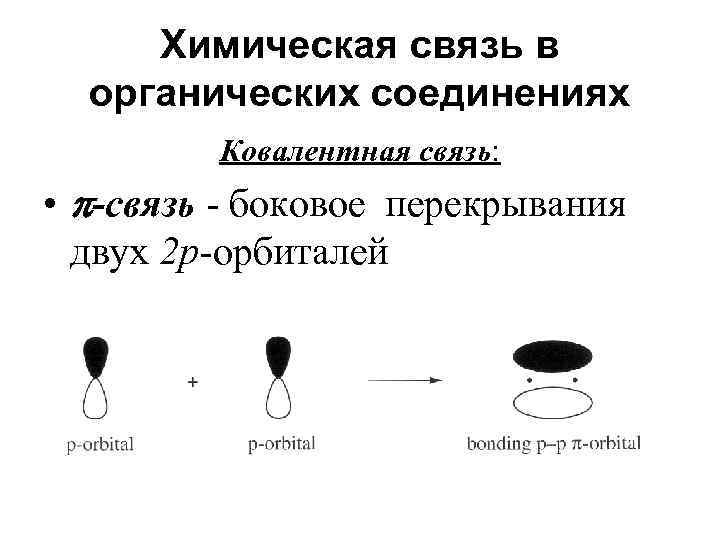 Химическая связь в органических соединениях Ковалентная связь: • -связь - боковое перекрывания двух 2 р-орбиталей
Химическая связь в органических соединениях Ковалентная связь: • -связь - боковое перекрывания двух 2 р-орбиталей
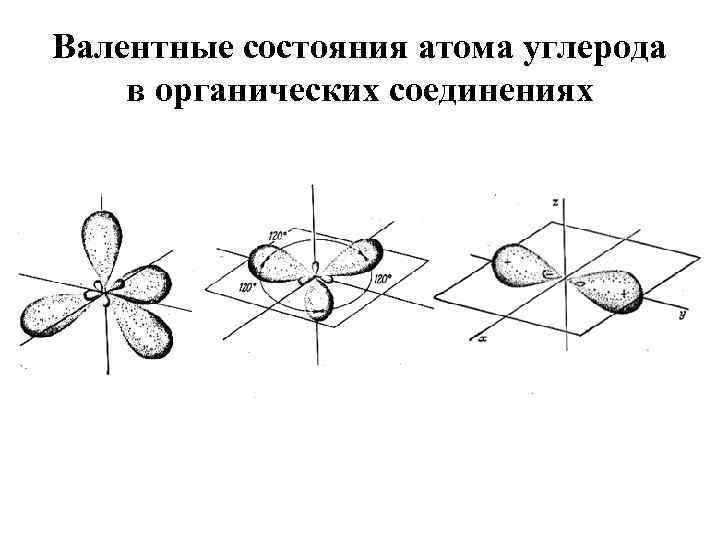 Валентные состояния атома углерода в органических соединениях
Валентные состояния атома углерода в органических соединениях
 Химическая связь в органических соединениях • Ионная связь – притяжение разноименных заряженных ионов, образующихся за счет передачи неспаренного электрона одного атома другому А + В [А]+[: В]-
Химическая связь в органических соединениях • Ионная связь – притяжение разноименных заряженных ионов, образующихся за счет передачи неспаренного электрона одного атома другому А + В [А]+[: В]-
 Химическая связь в органических соединениях • Водородная связь – химическая связь между атомами водорода, связанными с сильно электроотрицательными атомами (чаще всего атомами кислорода), и атомами, имеющими неподеленную электронную пару: X-H…: Y-Z
Химическая связь в органических соединениях • Водородная связь – химическая связь между атомами водорода, связанными с сильно электроотрицательными атомами (чаще всего атомами кислорода), и атомами, имеющими неподеленную электронную пару: X-H…: Y-Z
 Типы разрыва ковалентной связи • Гомолитический (радикальный) А В А + В • Гетеролитический (ионный) А В А+ + : В-
Типы разрыва ковалентной связи • Гомолитический (радикальный) А В А + В • Гетеролитический (ионный) А В А+ + : В-
 Гетеролитические реакции в зависимости от электронной природы атакующей частицы делят на нуклеофильные (символ N) и электрофильные (символ Е). При этом условно принято считать одну из взаимодействующих частиц реагентом, а другую субстратом, на которую действует реагент
Гетеролитические реакции в зависимости от электронной природы атакующей частицы делят на нуклеофильные (символ N) и электрофильные (символ Е). При этом условно принято считать одну из взаимодействующих частиц реагентом, а другую субстратом, на которую действует реагент
 Классификация органических реакций • Реакции замещения A-B + CD AD + B-C A-B + C- A- + B-C (SN) A-B + C+ A+ + B-C (SE) A-B + C A + B-C (SR)
Классификация органических реакций • Реакции замещения A-B + CD AD + B-C A-B + C- A- + B-C (SN) A-B + C+ A+ + B-C (SE) A-B + C A + B-C (SR)
 Классификация органических реакций • Реакции присоединения А=В + CD D-A-B-C А=В + C- A--B-C (АN) A=B + C+ A+-B-C (АE) A=B + C A-B-C (АR)
Классификация органических реакций • Реакции присоединения А=В + CD D-A-B-C А=В + C- A--B-C (АN) A=B + C+ A+-B-C (АE) A=B + C A-B-C (АR)
 Классификация органических реакций • Реакции элиминирования (отщепления) Е X-А-В-Y A=B + X-Y
Классификация органических реакций • Реакции элиминирования (отщепления) Е X-А-В-Y A=B + X-Y
 Классификация органических реакций • По молекулярности: - Мономолекулярные (SN 1, E 1) - Бимолекулярные (SN 2, E 2) Определяется числом частиц, участвующих в самой медленной стадии процесса
Классификация органических реакций • По молекулярности: - Мономолекулярные (SN 1, E 1) - Бимолекулярные (SN 2, E 2) Определяется числом частиц, участвующих в самой медленной стадии процесса
 Алканы (предельные углеводороды, парафины)
Алканы (предельные углеводороды, парафины)
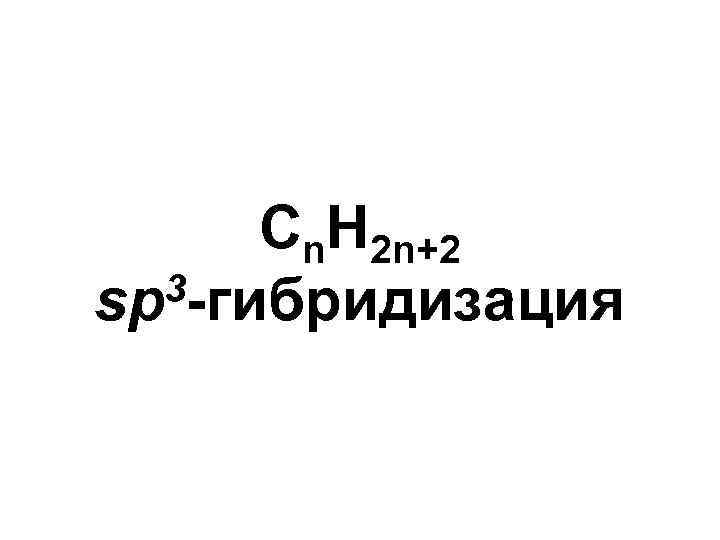 Cn. H 2 n+2 3 -гибридизация sp
Cn. H 2 n+2 3 -гибридизация sp
 Алканы • -связи между атомами углерода обладают цилиндрической симметрией (0, 154 нм) • группы вращаются вокруг углерод - углеродной связи почти свободно • возможны различные расположения атомов в пространстве, называемые конформациями
Алканы • -связи между атомами углерода обладают цилиндрической симметрией (0, 154 нм) • группы вращаются вокруг углерод - углеродной связи почти свободно • возможны различные расположения атомов в пространстве, называемые конформациями
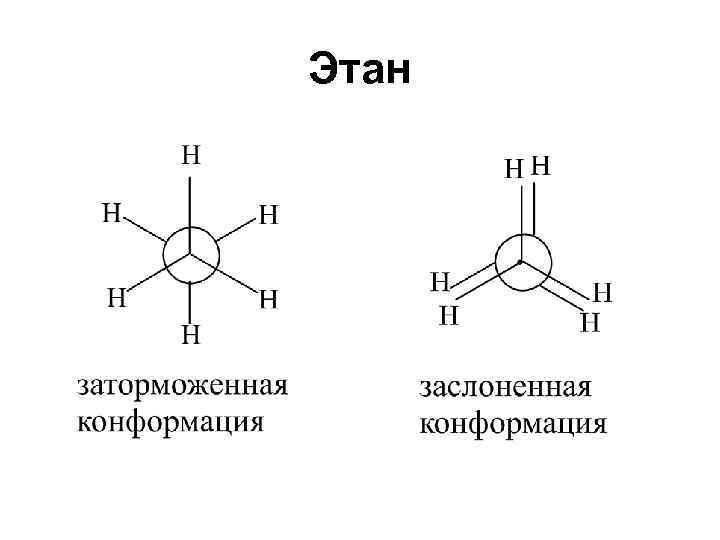 Этан
Этан
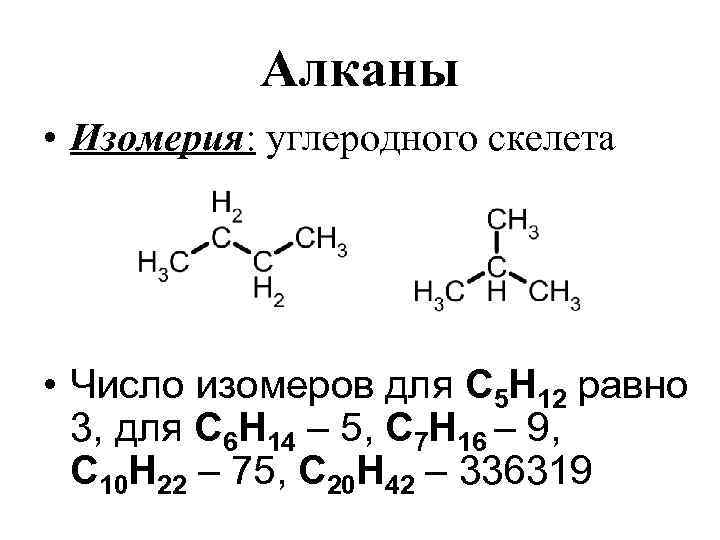 Алканы • Изомерия: углеродного скелета • Число изомеров для С 5 Н 12 равно 3, для С 6 Н 14 – 5, С 7 Н 16 – 9, С 10 Н 22 – 75, С 20 Н 42 – 336319
Алканы • Изомерия: углеродного скелета • Число изомеров для С 5 Н 12 равно 3, для С 6 Н 14 – 5, С 7 Н 16 – 9, С 10 Н 22 – 75, С 20 Н 42 – 336319
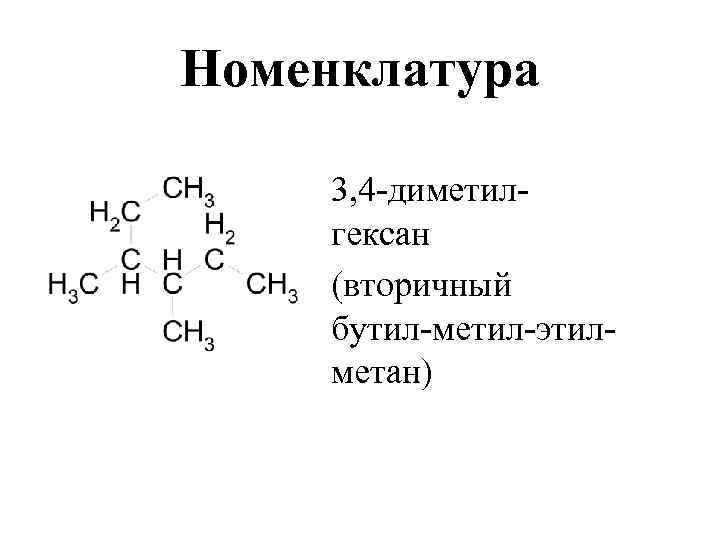 Номенклатура 3, 4 -диметилгексан (вторичный бутил-метил-этилметан)
Номенклатура 3, 4 -диметилгексан (вторичный бутил-метил-этилметан)
 Способы получения алканов Получение в промышленности метана и других алканов: • Фракционирование природного газа • Фракционирование перегонкой углеводородов нефти
Способы получения алканов Получение в промышленности метана и других алканов: • Фракционирование природного газа • Фракционирование перегонкой углеводородов нефти
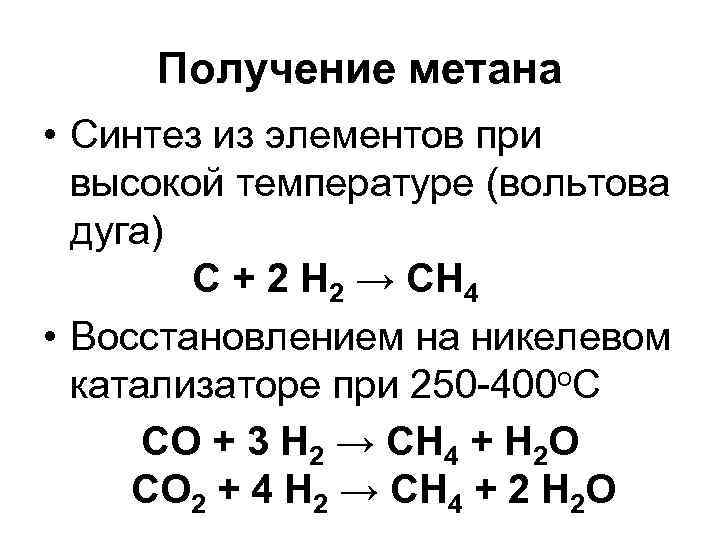 Получение метана • Синтез из элементов при высокой температуре (вольтова дуга) C + 2 H 2 → CH 4 • Восстановлением на никелевом катализаторе при 250 -400 о. С СО + 3 Н 2 → СН 4 + Н 2 О СО 2 + 4 Н 2 → СН 4 + 2 Н 2 О
Получение метана • Синтез из элементов при высокой температуре (вольтова дуга) C + 2 H 2 → CH 4 • Восстановлением на никелевом катализаторе при 250 -400 о. С СО + 3 Н 2 → СН 4 + Н 2 О СО 2 + 4 Н 2 → СН 4 + 2 Н 2 О
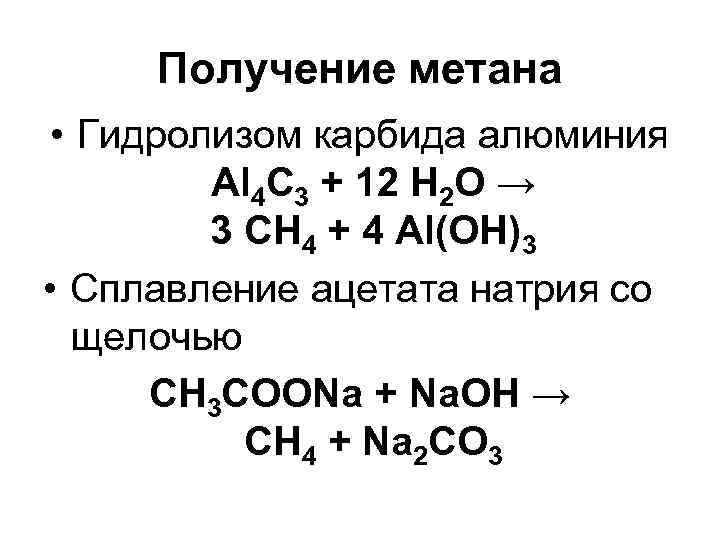 Получение метана • Гидролизом карбида алюминия Al 4 C 3 + 12 H 2 O → 3 CH 4 + 4 Al(OH)3 • Cплавление ацетата натрия со щелочью СН 3 СOONa + Na. OH → CH 4 + Na 2 CO 3
Получение метана • Гидролизом карбида алюминия Al 4 C 3 + 12 H 2 O → 3 CH 4 + 4 Al(OH)3 • Cплавление ацетата натрия со щелочью СН 3 СOONa + Na. OH → CH 4 + Na 2 CO 3
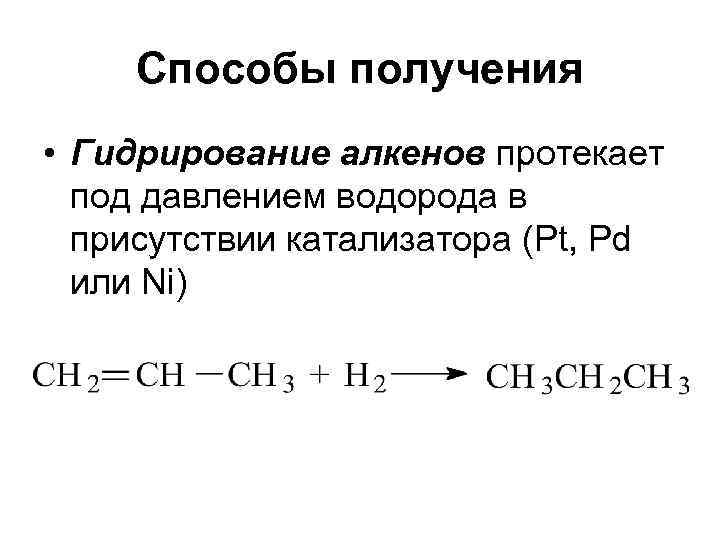 Способы получения • Гидрирование алкенов протекает под давлением водорода в присутствии катализатора (Pt, Pd или Ni)
Способы получения • Гидрирование алкенов протекает под давлением водорода в присутствии катализатора (Pt, Pd или Ni)
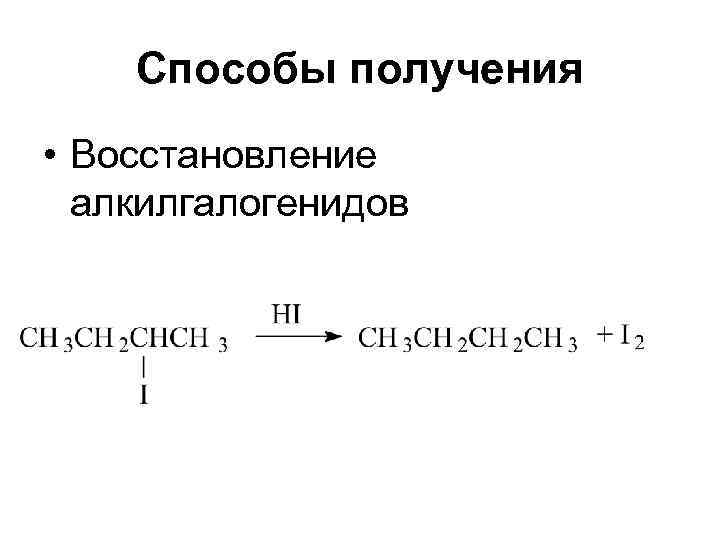 Способы получения • Восстановление алкилгалогенидов
Способы получения • Восстановление алкилгалогенидов
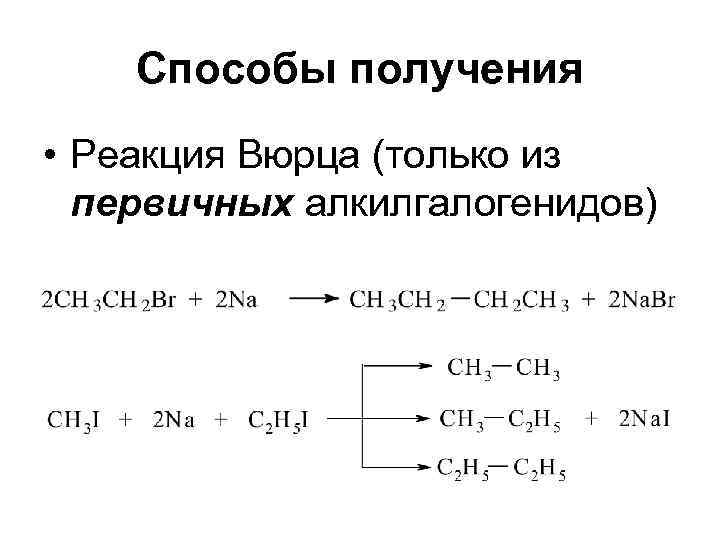 Способы получения • Реакция Вюрца (только из первичных алкилгалогенидов)
Способы получения • Реакция Вюрца (только из первичных алкилгалогенидов)
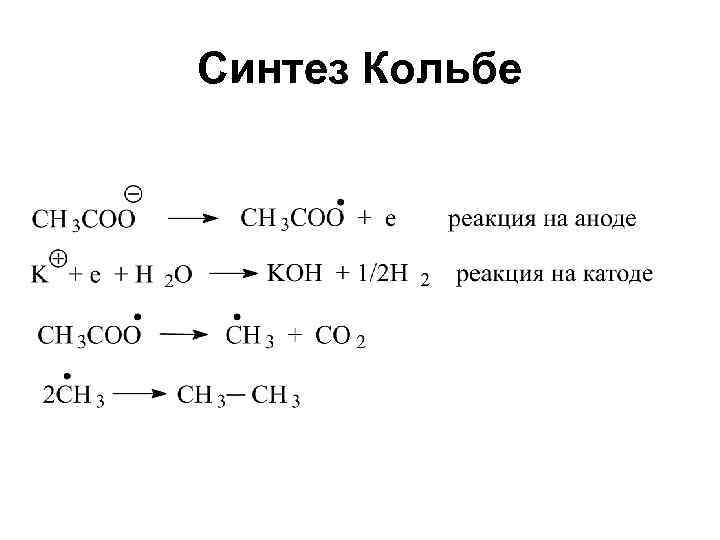 Синтез Кольбе
Синтез Кольбе
 Физические свойства • С 1 -С 4 при обычной температуре – газы • С 5 -С 15 – жидкости • с С 16 – твердые вещества • Плотность лежит в пределах 0. 4 -0. 7 г/мл • Растворимость в воде ничтожна
Физические свойства • С 1 -С 4 при обычной температуре – газы • С 5 -С 15 – жидкости • с С 16 – твердые вещества • Плотность лежит в пределах 0. 4 -0. 7 г/мл • Растворимость в воде ничтожна
 Химические свойства • Нечувствительны к ионным реагентам • Инертны по отношению к кислотам, основаниям, окислителям • Наиболее характерным свойством является радикальное замещение незаряженного атома водорода при действии незаряженных радикальных реагентов
Химические свойства • Нечувствительны к ионным реагентам • Инертны по отношению к кислотам, основаниям, окислителям • Наиболее характерным свойством является радикальное замещение незаряженного атома водорода при действии незаряженных радикальных реагентов
 Галогенирование Замещение атомов водорода на галоген - наиболее характерная реакция алканов
Галогенирование Замещение атомов водорода на галоген - наиболее характерная реакция алканов
 Механизм хлорирования • SR Cl 2 2 Cl (зарождение цепи) СН 4 + Cl CН 3 + НСl (рост цепи) CН 3 + Cl 2 Cl + CН 3 Сl (рост цепи) 2 Cl 2 (обрыв цепи) 2 CН 3 C 2 Н 6 (обрыв цепи) CН 3 + Cl CН 3 Сl (обрыв цепи)
Механизм хлорирования • SR Cl 2 2 Cl (зарождение цепи) СН 4 + Cl CН 3 + НСl (рост цепи) CН 3 + Cl 2 Cl + CН 3 Сl (рост цепи) 2 Cl 2 (обрыв цепи) 2 CН 3 C 2 Н 6 (обрыв цепи) CН 3 + Cl CН 3 Сl (обрыв цепи)
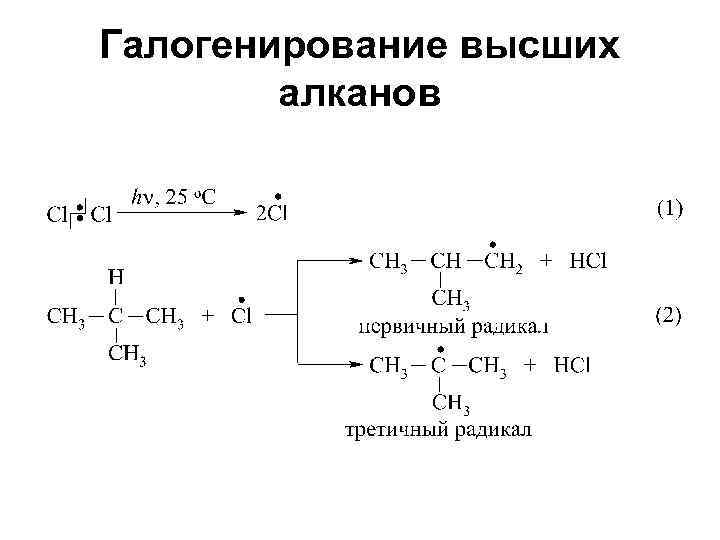 Галогенирование высших алканов
Галогенирование высших алканов
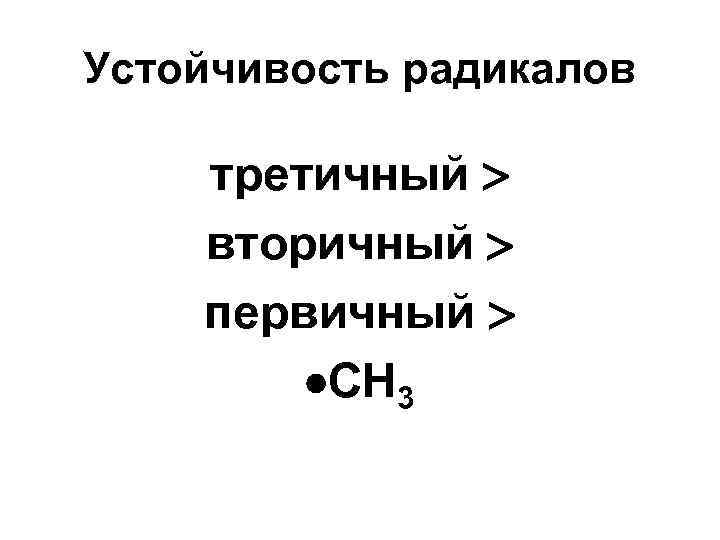 Устойчивость радикалов третичный вторичный первичный CH 3
Устойчивость радикалов третичный вторичный первичный CH 3
 Нитрование алканов
Нитрование алканов
 Сульфирование • Серная кислота при комнатной температуре не действует на алканы, а при нагревании она действует как окислитель. Дымящая серная кислота с высшими парафинами образует сульфокислоты: R-Н + Н 2 SО 4 R-SО 3 Н + Н 2 О
Сульфирование • Серная кислота при комнатной температуре не действует на алканы, а при нагревании она действует как окислитель. Дымящая серная кислота с высшими парафинами образует сульфокислоты: R-Н + Н 2 SО 4 R-SО 3 Н + Н 2 О
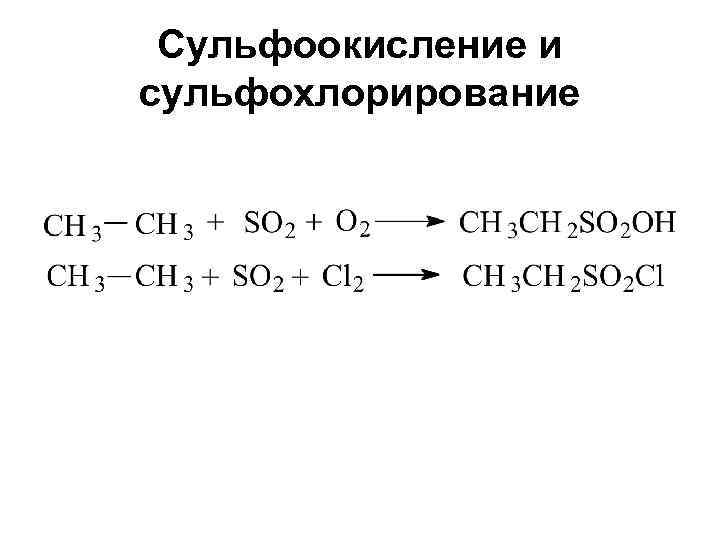 Сульфоокисление и сульфохлорирование
Сульфоокисление и сульфохлорирование
 Окисление • Кислород воздуха, КМn. О 4, К 2 Сr 2 О 7 и др. , окисляют парафины только при высоких температурах с разрывом углеродной цепи и образованием в основном кислот • Идет также процесс декарбоксилирования с выделением СО 2
Окисление • Кислород воздуха, КМn. О 4, К 2 Сr 2 О 7 и др. , окисляют парафины только при высоких температурах с разрывом углеродной цепи и образованием в основном кислот • Идет также процесс декарбоксилирования с выделением СО 2
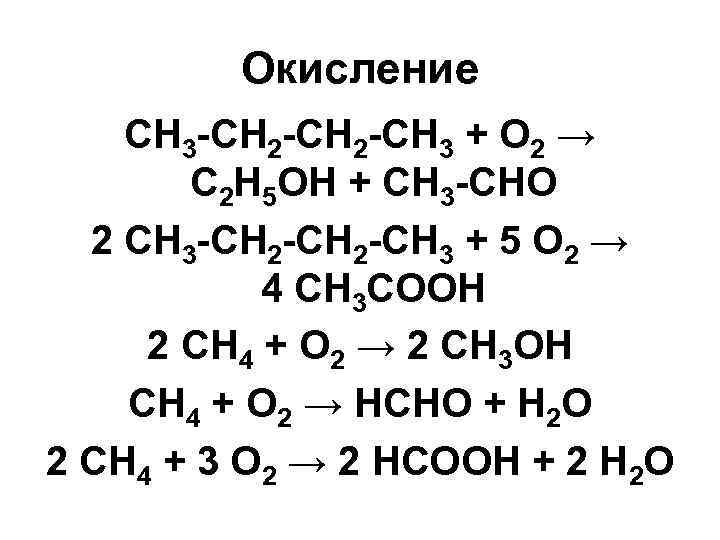 Окисление CH 3 -CH 2 -CH 3 + O 2 → C 2 H 5 OH + СН 3 -СНО 2 СН 3 -СН 2 -СН 3 + 5 О 2 → 4 СН 3 СООН 2 СН 4 + О 2 → 2 CH 3 OH СН 4 + О 2 → НСНО + Н 2 О 2 СН 4 + 3 О 2 → 2 НСООН + 2 Н 2 О
Окисление CH 3 -CH 2 -CH 3 + O 2 → C 2 H 5 OH + СН 3 -СНО 2 СН 3 -СН 2 -СН 3 + 5 О 2 → 4 СН 3 СООН 2 СН 4 + О 2 → 2 CH 3 OH СН 4 + О 2 → НСНО + Н 2 О 2 СН 4 + 3 О 2 → 2 НСООН + 2 Н 2 О
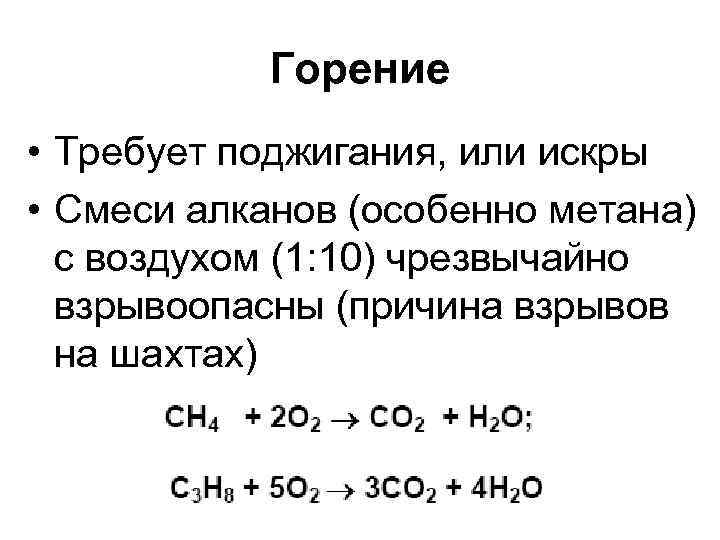 Горение • Требует поджигания, или искры • Смеси алканов (особенно метана) с воздухом (1: 10) чрезвычайно взрывоопасны (причина взрывов на шахтах)
Горение • Требует поджигания, или искры • Смеси алканов (особенно метана) с воздухом (1: 10) чрезвычайно взрывоопасны (причина взрывов на шахтах)
 Термический и каталитический крекинг • При температурах выше 1000 о. С все предельные углеводороды распадаются на углерод и водород (производство дешевой газовой сажи и водорода) СН 4 → C +2 H 2
Термический и каталитический крекинг • При температурах выше 1000 о. С все предельные углеводороды распадаются на углерод и водород (производство дешевой газовой сажи и водорода) СН 4 → C +2 H 2
 Термический и каталитический крекинг • В определенных условиях удается отделять промежуточные продукты (ацетилен получают из метана) 2 CH 4 → C 2 H 2 + 3 H 2
Термический и каталитический крекинг • В определенных условиях удается отделять промежуточные продукты (ацетилен получают из метана) 2 CH 4 → C 2 H 2 + 3 H 2
 Термический и каталитический крекинг С 5 Н 12 C 3 Н 8 + С 2 Н 4 С 16 Н 34 → С 8 Н 18 + С 8 Н 16 • Введение катализатора в процесс может сильно изменить направление реакции
Термический и каталитический крекинг С 5 Н 12 C 3 Н 8 + С 2 Н 4 С 16 Н 34 → С 8 Н 18 + С 8 Н 16 • Введение катализатора в процесс может сильно изменить направление реакции
 Каталитический крекинг • При каталитическом крекинге этана обычно образуется ацетилен С 2 Н 6 → С 2 Н 2 + 2 Н 2 • Из бутана получают бутадиен, а из 2 -метилбутана - изопрен CH 3 -CH 2 -CH 3 → CH 2=CH-CH=CH 2 + 2 H 2
Каталитический крекинг • При каталитическом крекинге этана обычно образуется ацетилен С 2 Н 6 → С 2 Н 2 + 2 Н 2 • Из бутана получают бутадиен, а из 2 -метилбутана - изопрен CH 3 -CH 2 -CH 3 → CH 2=CH-CH=CH 2 + 2 H 2
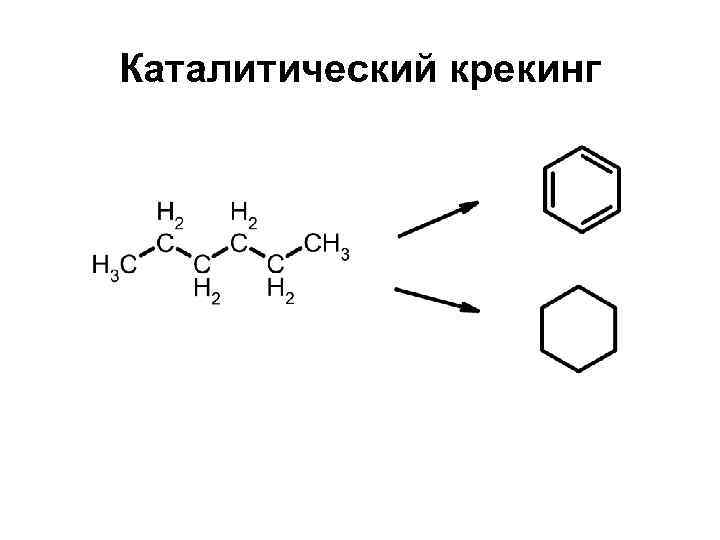 Каталитический крекинг
Каталитический крекинг
 Реакции изомеризации • В присутствии катализаторов (Al. Cl 3) нормальные алканы могут превращаться в алканы с разветвленной цепью:
Реакции изомеризации • В присутствии катализаторов (Al. Cl 3) нормальные алканы могут превращаться в алканы с разветвленной цепью:
 Применение алканов • Газообразное и жидкое топливо • Смазочные материалы • Сырье для получения сажи, ацетилена, высших синтетических кислот и др.
Применение алканов • Газообразное и жидкое топливо • Смазочные материалы • Сырье для получения сажи, ацетилена, высших синтетических кислот и др.
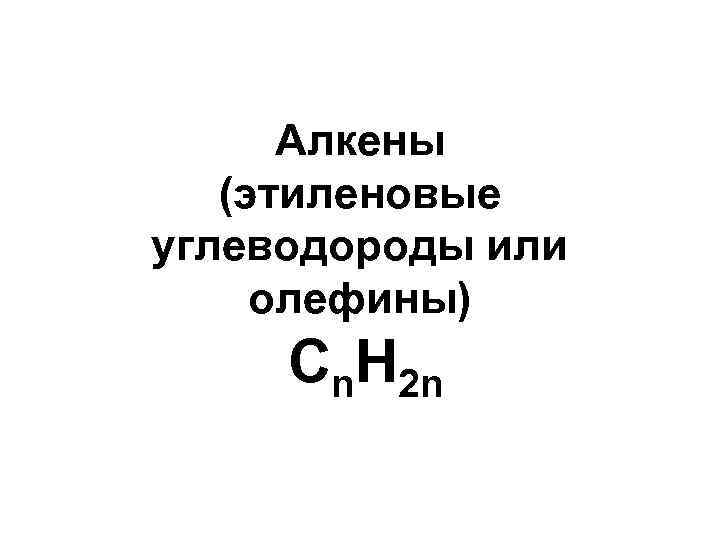 Алкены (этиленовые углеводороды или олефины) Cn. H 2 n
Алкены (этиленовые углеводороды или олефины) Cn. H 2 n
 Номенклатура • СН 2=СН 2 • СН 2=СН-СН 3 этен, этилен пропен, метилэтилен, пропилен • СН 2=СН-СН 2 -СН 3 1 -бутен, этилен, бутилен • СН 3 -СН=СН-СН 3 2 -бутен, симметричный диметилэтилен, псевдобутилен
Номенклатура • СН 2=СН 2 • СН 2=СН-СН 3 этен, этилен пропен, метилэтилен, пропилен • СН 2=СН-СН 2 -СН 3 1 -бутен, этилен, бутилен • СН 3 -СН=СН-СН 3 2 -бутен, симметричный диметилэтилен, псевдобутилен
 Изомерия Структурная изомерия • Углеродного скелета • Положения двойной связи СН 2=СН-СН 2 -СН 3 (бутен-1) СН 3 -СН=СН-СН 3 (бутен-2) • Межклассовая (с циклоалканами) Пространственная изомерия • Геометрическая
Изомерия Структурная изомерия • Углеродного скелета • Положения двойной связи СН 2=СН-СН 2 -СН 3 (бутен-1) СН 3 -СН=СН-СН 3 (бутен-2) • Межклассовая (с циклоалканами) Пространственная изомерия • Геометрическая
 Изомерия • Геометрическая изомерия (цистранс)
Изомерия • Геометрическая изомерия (цистранс)
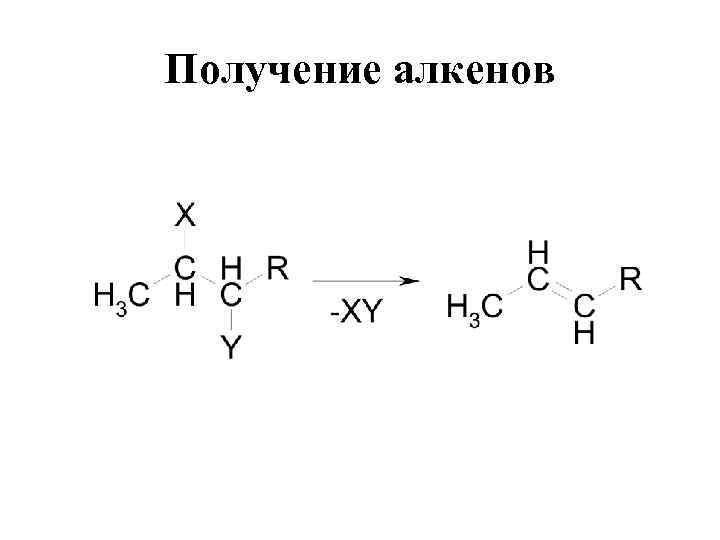 Получение алкенов
Получение алкенов
 Способы получения • Дегидрогенизацией предельных углеводородов на окиси хрома (катализатор): С 4 Н 10 СН 2=СН-СН 2 -СН 3
Способы получения • Дегидрогенизацией предельных углеводородов на окиси хрома (катализатор): С 4 Н 10 СН 2=СН-СН 2 -СН 3
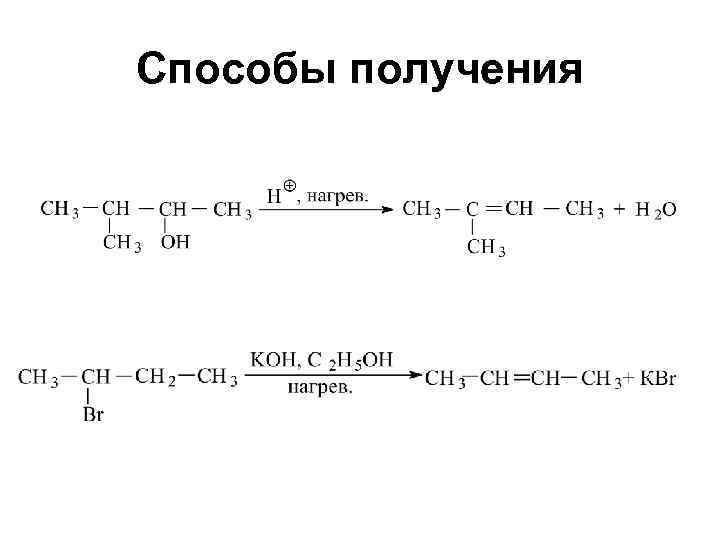 Способы получения
Способы получения
 • Отщепление воды и галогенводородов определяется правилом Зайцева: водород отщепляется от ближайшего углерода наименее гидрогенизированного
• Отщепление воды и галогенводородов определяется правилом Зайцева: водород отщепляется от ближайшего углерода наименее гидрогенизированного
 Способы получения
Способы получения
 Физические свойства • С 2 -С 4 – газы, С 5 -С 17 – жидкости, далее - твердые вещества • Перемещение двойной связи в центр молекулы вызывает повышение температуры кипения олефина
Физические свойства • С 2 -С 4 – газы, С 5 -С 17 – жидкости, далее - твердые вещества • Перемещение двойной связи в центр молекулы вызывает повышение температуры кипения олефина
 Физические свойства • Цис-изомеры кипят при более высокой температуре, чем трансизомеры • Плотность олефинов меньше единицы, но больше, чем соответствующих парафинов • Растворимость в воде мала, но выше, чем у парафинов
Физические свойства • Цис-изомеры кипят при более высокой температуре, чем трансизомеры • Плотность олефинов меньше единицы, но больше, чем соответствующих парафинов • Растворимость в воде мала, но выше, чем у парафинов
 Химические свойства • Реакции присоединения • Реакции окисления • Реакции полимеризации
Химические свойства • Реакции присоединения • Реакции окисления • Реакции полимеризации
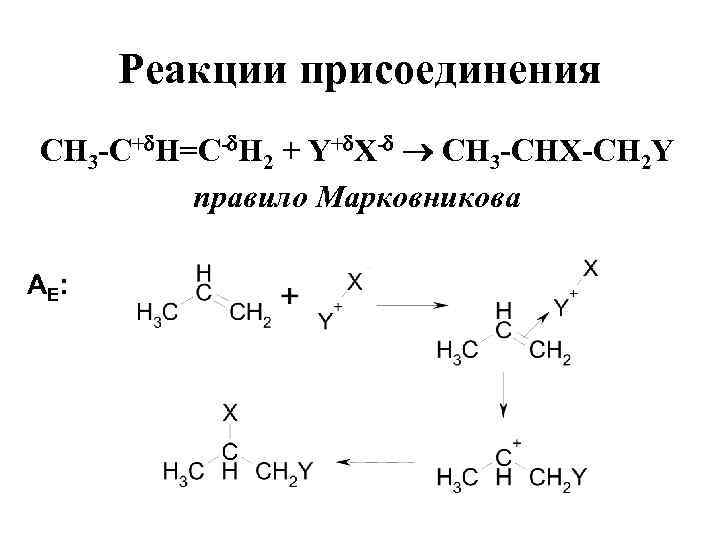 Реакции присоединения СН 3 -С+ Н=С- Н 2 + Y+ X- СН 3 -СНX-СН 2 Y правило Марковникова АE :
Реакции присоединения СН 3 -С+ Н=С- Н 2 + Y+ X- СН 3 -СНX-СН 2 Y правило Марковникова АE :
 Электрофильное присоединение • Правило Марковникова: водород присоединяется по месту разрыва двойной связи преимущественно к наиболее гидрогенизированному атому углерода
Электрофильное присоединение • Правило Марковникова: водород присоединяется по месту разрыва двойной связи преимущественно к наиболее гидрогенизированному атому углерода
 Устойчивость карбкатионов • Чем больше распределен (делокализован) заряд в карбкатионе, тем устойчивее карбкатион
Устойчивость карбкатионов • Чем больше распределен (делокализован) заряд в карбкатионе, тем устойчивее карбкатион
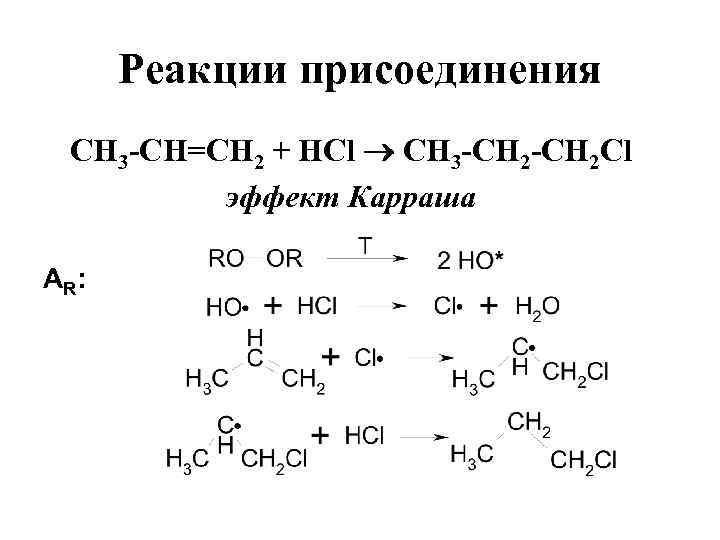 Реакции присоединения СН 3 -СН=СН 2 + HCl СН 3 -СН 2 Cl эффект Карраша А R:
Реакции присоединения СН 3 -СН=СН 2 + HCl СН 3 -СН 2 Cl эффект Карраша А R:
 Газообразное хлорирование пропилена
Газообразное хлорирование пропилена
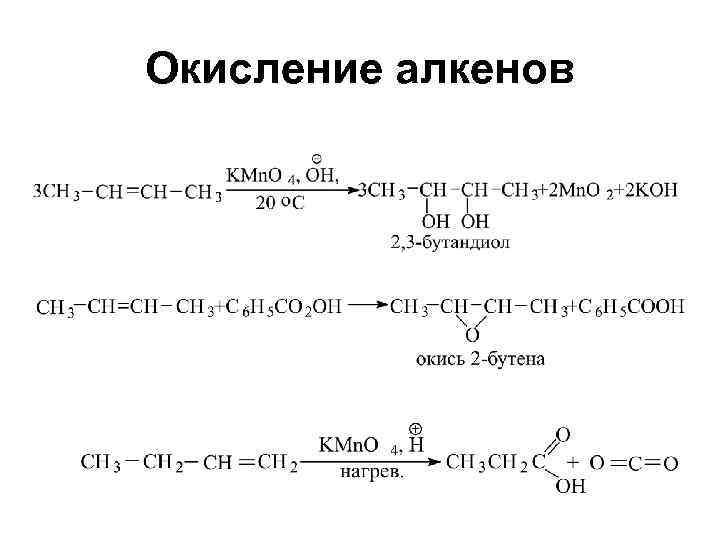 Окисление алкенов
Окисление алкенов
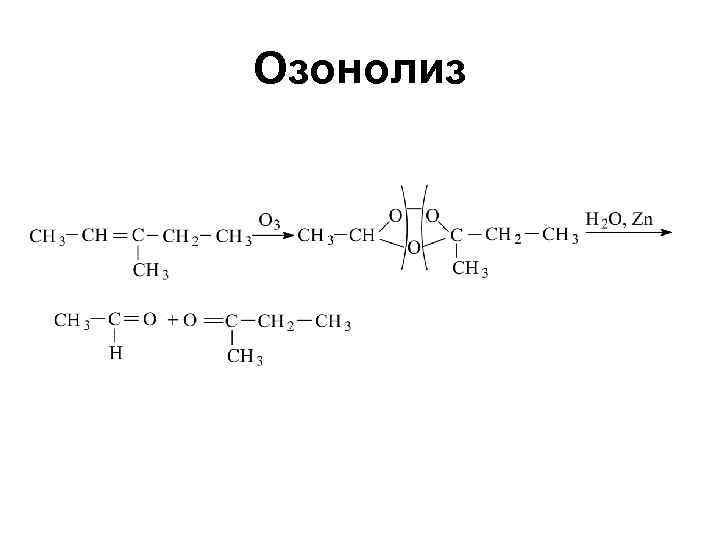 Озонолиз
Озонолиз
 Реакции полимеризации Получение полиэтилена: n СН 2=СН 2 (-СН 2 -)n Получение полипропилена: n СН 3 -СН=СН 2 (-СН-СН 2 -)n СН 3
Реакции полимеризации Получение полиэтилена: n СН 2=СН 2 (-СН 2 -)n Получение полипропилена: n СН 3 -СН=СН 2 (-СН-СН 2 -)n СН 3
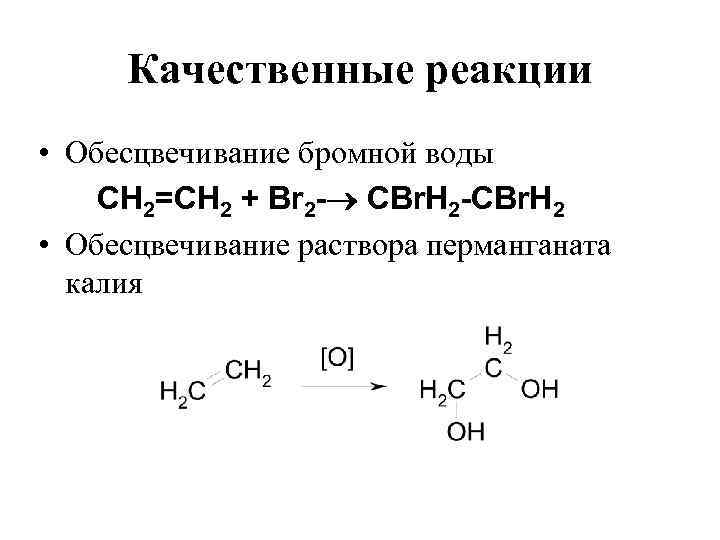 Качественные реакции • Обесцвечивание бромной воды СН 2=СН 2 + Вr 2 - CBr. Н 2 -СBr. Н 2 • Обесцвечивание раствора перманганата калия
Качественные реакции • Обесцвечивание бромной воды СН 2=СН 2 + Вr 2 - CBr. Н 2 -СBr. Н 2 • Обесцвечивание раствора перманганата калия
 Применение алкенов • В производстве полимерных материалов (пластмасс, каучуков, пленок) • Для получения спиртов, альдегидов, галогенопроизводных и многих других органических соединений
Применение алкенов • В производстве полимерных материалов (пластмасс, каучуков, пленок) • Для получения спиртов, альдегидов, галогенопроизводных и многих других органических соединений
 Алкадиены (диеновые углеводороды) Сn. Н 2 n-2
Алкадиены (диеновые углеводороды) Сn. Н 2 n-2
 Диеновые углеводороды • С кумуллированными связями СН 2=С=СН 2 пропадиен, аллен • С сопряженными связями СН 2=СН-СН=СН 2 1, 3 -бутадиен, дивинил • С изолированными связями СН 2=СН-СН 2 -СН=СН 2 1, 5 -гексадиен, диаллил
Диеновые углеводороды • С кумуллированными связями СН 2=С=СН 2 пропадиен, аллен • С сопряженными связями СН 2=СН-СН=СН 2 1, 3 -бутадиен, дивинил • С изолированными связями СН 2=СН-СН 2 -СН=СН 2 1, 5 -гексадиен, диаллил
 Изомерия • • Структурная изомерия Углеродного скелета Положения двойных связей Межклассовая (с алкинами) Пространственная изомерия Геометрическая
Изомерия • • Структурная изомерия Углеродного скелета Положения двойных связей Межклассовая (с алкинами) Пространственная изомерия Геометрическая
 Способы получения дивинила • Метод С. В. Лебедева, 1932 г. Ярославль СК-1 2 С 2 Н 5 ОН С 4 Н 6 + 2 Н 2 О + Н 2 (выход 70% от теоретического)
Способы получения дивинила • Метод С. В. Лебедева, 1932 г. Ярославль СК-1 2 С 2 Н 5 ОН С 4 Н 6 + 2 Н 2 О + Н 2 (выход 70% от теоретического)
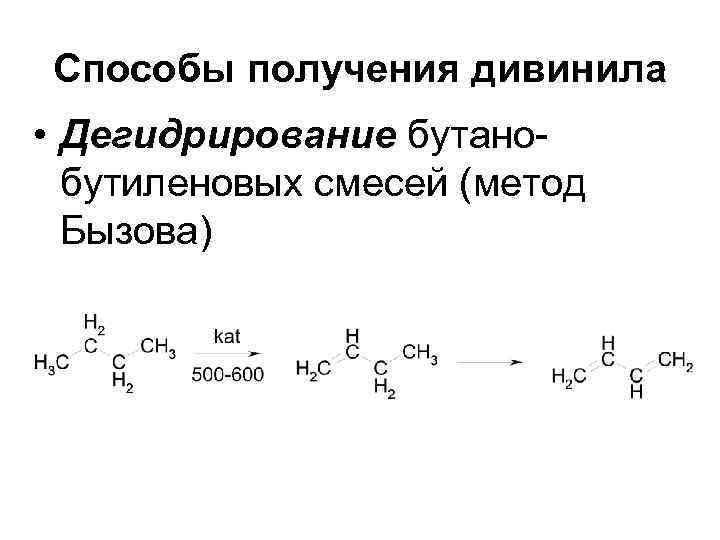 Способы получения дивинила • Дегидрирование бутанобутиленовых смесей (метод Бызова)
Способы получения дивинила • Дегидрирование бутанобутиленовых смесей (метод Бызова)
 Способы получения изопрена • Дегидрирование изопентан - изоамиленовых смесей С 5 Н 12 С 5 Н 10 С 5 Н 8
Способы получения изопрена • Дегидрирование изопентан - изоамиленовых смесей С 5 Н 12 С 5 Н 10 С 5 Н 8
 Сопряженные диены • Дивинил - газ с Ткип 4, 5 о. С, в воде нерастворим, легко взрывается с воздухом • Изопрен и другие простейшие диены - жидкости
Сопряженные диены • Дивинил - газ с Ткип 4, 5 о. С, в воде нерастворим, легко взрывается с воздухом • Изопрен и другие простейшие диены - жидкости
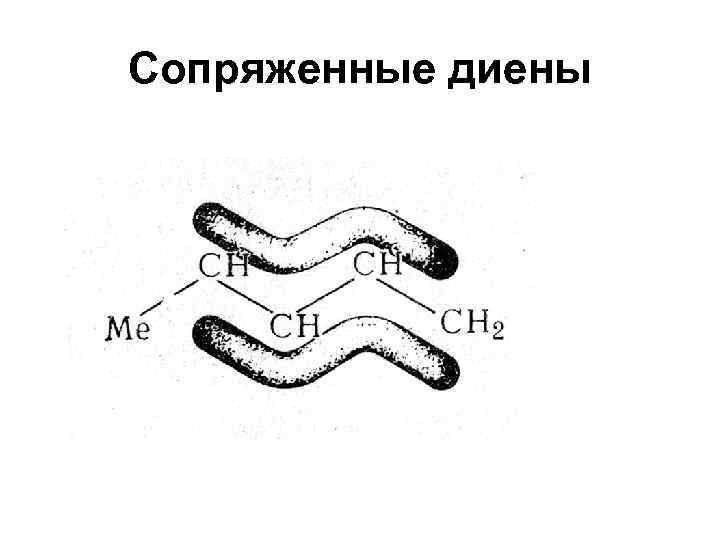 Сопряженные диены
Сопряженные диены
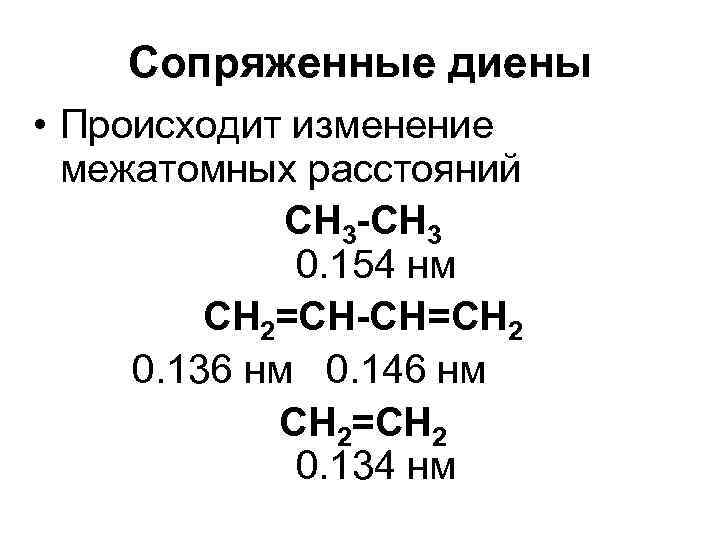 Сопряженные диены • Происходит изменение межатомных расстояний СН 3 -СН 3 0. 154 нм СН 2=СН-СН=СН 2 0. 136 нм 0. 146 нм СН 2=СН 2 0. 134 нм
Сопряженные диены • Происходит изменение межатомных расстояний СН 3 -СН 3 0. 154 нм СН 2=СН-СН=СН 2 0. 136 нм 0. 146 нм СН 2=СН 2 0. 134 нм
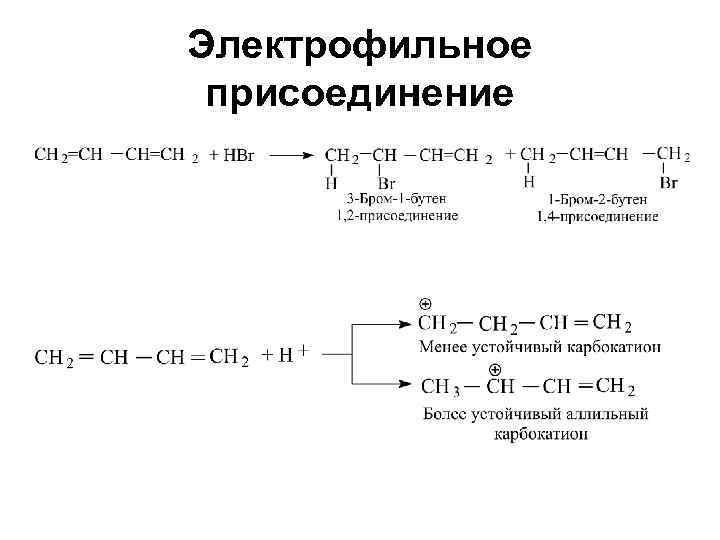 Электрофильное присоединение
Электрофильное присоединение
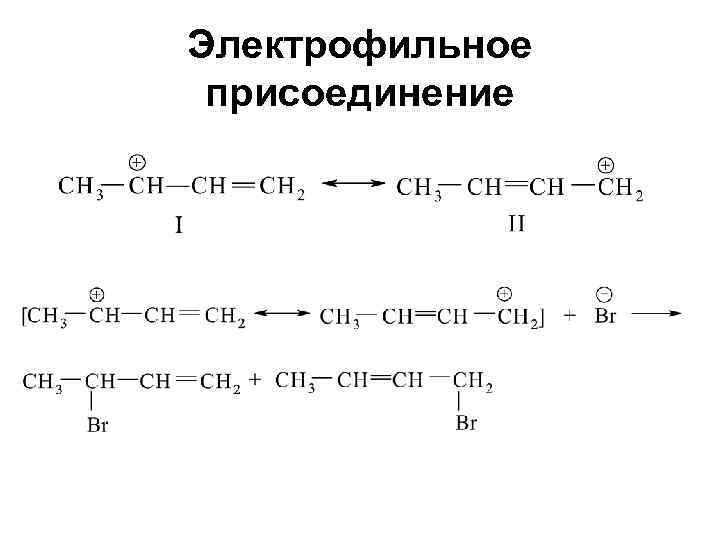 Электрофильное присоединение
Электрофильное присоединение
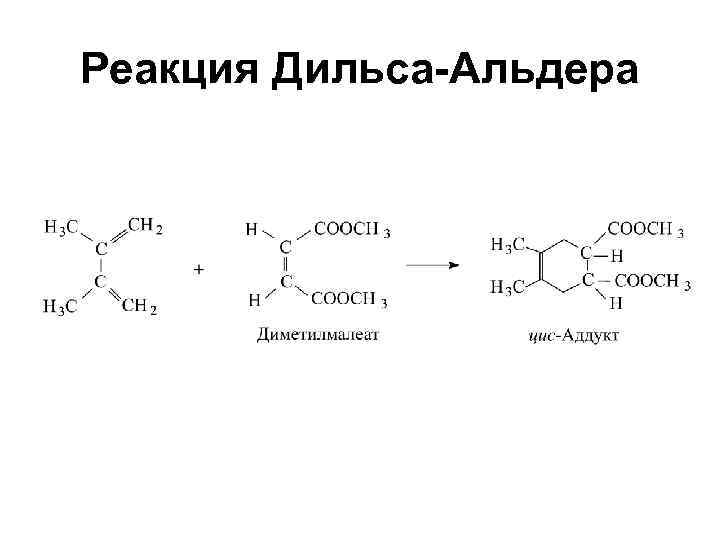 Реакция Дильса-Альдера
Реакция Дильса-Альдера
 Полимеризация
Полимеризация
 Натуральный каучук • Добывается из млечного сока некоторых растений (гевея, гваюлла, коксалыз, таусалыз и др. ) • Промышленное значение имеют только плантации гевеи
Натуральный каучук • Добывается из млечного сока некоторых растений (гевея, гваюлла, коксалыз, таусалыз и др. ) • Промышленное значение имеют только плантации гевеи
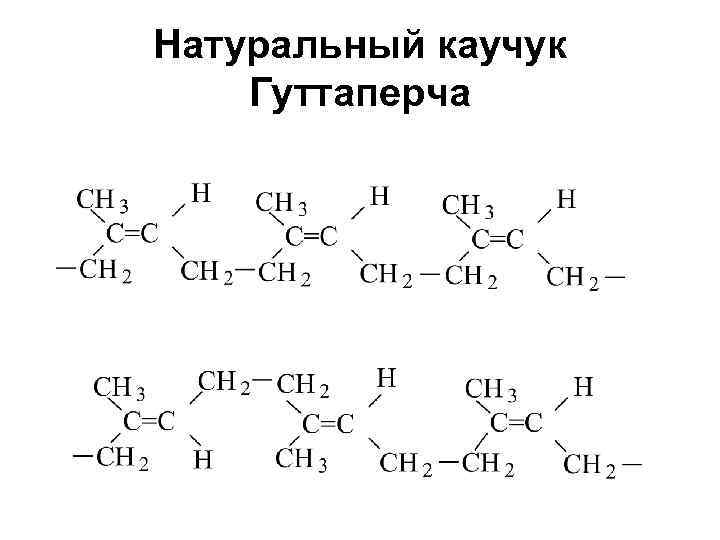 Натуральный каучук Гуттаперча
Натуральный каучук Гуттаперча

 Контрольное задание № 1 Напишите реакции окисления метана, бутана, этилена, бутена-2 и бутадиена-1, 3
Контрольное задание № 1 Напишите реакции окисления метана, бутана, этилена, бутена-2 и бутадиена-1, 3


