лекция 7 связи ионная.ppt
- Количество слайдов: 14
 ЛЕКЦИЯ Ионная связь Водородная связь. Металлическая связь.
ЛЕКЦИЯ Ионная связь Водородная связь. Металлическая связь.
 Ионная связь осуществляется в результате взаимного электростатического притяжения противоположно заряженных ионов. Например: Ионы м. б. простыми (Na, K, Mg и т. д. )катионы (J–, Cl–, Br –) , а также сложными, т. е. состоящими из 2 х и более анионы простых веществ. (NH 4+ и SO 42 -, NO 3–)
Ионная связь осуществляется в результате взаимного электростатического притяжения противоположно заряженных ионов. Например: Ионы м. б. простыми (Na, K, Mg и т. д. )катионы (J–, Cl–, Br –) , а также сложными, т. е. состоящими из 2 х и более анионы простых веществ. (NH 4+ и SO 42 -, NO 3–)
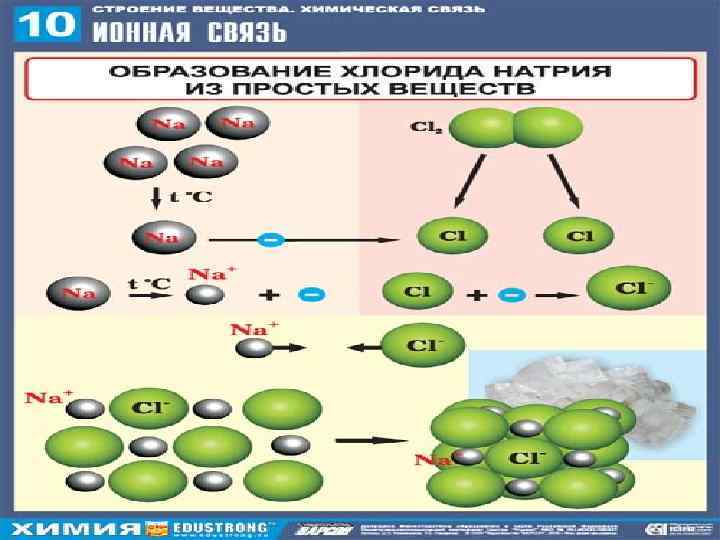
 Ковалентная связь обладает направленностью, ионная же связь в отличие от ковалентной направленностью не обладает, т. к. электрическое поле вокруг иона обладает сферической симметрией, поэтому взаимодействие между ионами осуществляется одинаково.
Ковалентная связь обладает направленностью, ионная же связь в отличие от ковалентной направленностью не обладает, т. к. электрическое поле вокруг иона обладает сферической симметрией, поэтому взаимодействие между ионами осуществляется одинаково.
 Происходит как бы обратный перенос части электронного заряда от аниона к катиону и электрические облака оказываются не полностью разделенными, а частично перекрытыми. Из этого следует, что ионную связь можно рассматривать как предельный случай полярной ковалентной связи. Особенно высоким поляризующим действием обладает ион Н+ (т. к. малый размер и отсутствие е–).
Происходит как бы обратный перенос части электронного заряда от аниона к катиону и электрические облака оказываются не полностью разделенными, а частично перекрытыми. Из этого следует, что ионную связь можно рассматривать как предельный случай полярной ковалентной связи. Особенно высоким поляризующим действием обладает ион Н+ (т. к. малый размер и отсутствие е–).
 Водородная связь Ещё в XIX замечено, что соединения галогенов с водородом сильно отличают (меняют) их свойства (tпл, tкип. ). Эти особенности указанных соединений объясняются способностью атома водорода, соединенного с атомом сильно электроотрицательного элемента, к образованию ещё одной химической связи – водородной. В первом приближении водородную связь можно объяснить действием электростатических сил. При образовании полярной ковалентной связи между атомом водорода и F, обладающего высокой электроотрицательностью, электрическое облако, которое принадлежало водороду, сильно смещается к атому фтора. Атом F приобретает (–) заряд, а ядро атома водорода с «внешней» стороны почти лишается электрического облака. Возникает электростатическое притяжение между протоном атома водорода и ( –) заряженным атомом фтора с другой стороны.
Водородная связь Ещё в XIX замечено, что соединения галогенов с водородом сильно отличают (меняют) их свойства (tпл, tкип. ). Эти особенности указанных соединений объясняются способностью атома водорода, соединенного с атомом сильно электроотрицательного элемента, к образованию ещё одной химической связи – водородной. В первом приближении водородную связь можно объяснить действием электростатических сил. При образовании полярной ковалентной связи между атомом водорода и F, обладающего высокой электроотрицательностью, электрическое облако, которое принадлежало водороду, сильно смещается к атому фтора. Атом F приобретает (–) заряд, а ядро атома водорода с «внешней» стороны почти лишается электрического облака. Возникает электростатическое притяжение между протоном атома водорода и ( –) заряженным атомом фтора с другой стороны.
 Ион водорода (протон) способен проникать в электронные оболочки других атомов. Н+ –F + H+ –F→ Н+ 134˚ F– Н+ Н+ F– F– Образуется полимерная цепочка _ _ _ Пунктиром обозначена водородная связь. Таким образом, условием образования водородной связи является высокая электроотрицательность атома, связанная в молекуле с водородом.
Ион водорода (протон) способен проникать в электронные оболочки других атомов. Н+ –F + H+ –F→ Н+ 134˚ F– Н+ Н+ F– F– Образуется полимерная цепочка _ _ _ Пунктиром обозначена водородная связь. Таким образом, условием образования водородной связи является высокая электроотрицательность атома, связанная в молекуле с водородом.
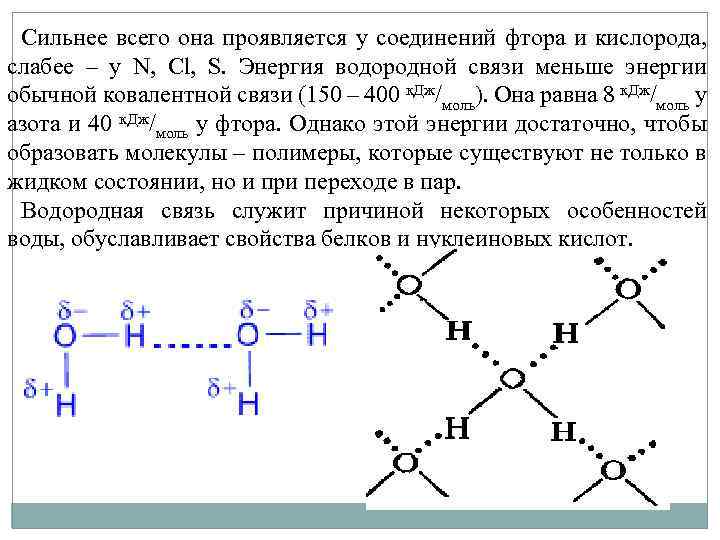 Сильнее всего она проявляется у соединений фтора и кислорода, слабее – у N, Cl, S. Энергия водородной связи меньше энергии обычной ковалентной связи (150 – 400 к. Дж/моль). Она равна 8 к. Дж/моль у азота и 40 к. Дж/моль у фтора. Однако этой энергии достаточно, чтобы образовать молекулы – полимеры, которые существуют не только в жидком состоянии, но и при переходе в пар. Водородная связь служит причиной некоторых особенностей воды, обуславливает свойства белков и нуклеиновых кислот.
Сильнее всего она проявляется у соединений фтора и кислорода, слабее – у N, Cl, S. Энергия водородной связи меньше энергии обычной ковалентной связи (150 – 400 к. Дж/моль). Она равна 8 к. Дж/моль у азота и 40 к. Дж/моль у фтора. Однако этой энергии достаточно, чтобы образовать молекулы – полимеры, которые существуют не только в жидком состоянии, но и при переходе в пар. Водородная связь служит причиной некоторых особенностей воды, обуславливает свойства белков и нуклеиновых кислот.
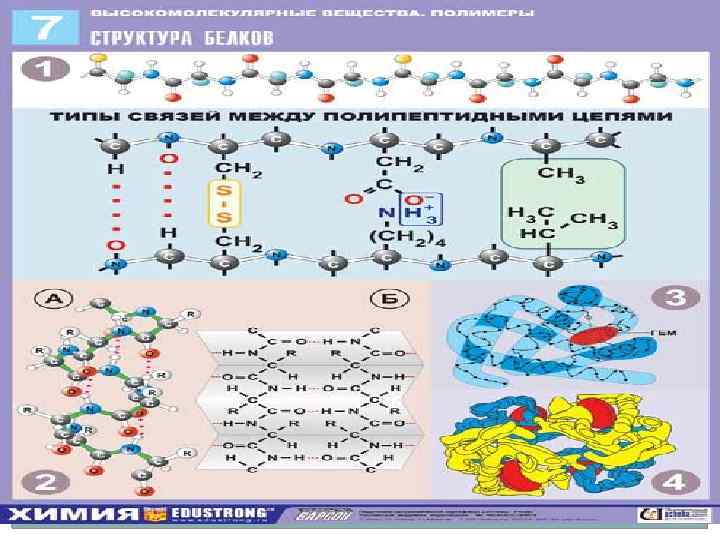
 Металлическая связь Металлы отличаются от других веществ высокой электро и теплопроводностью, а их структуры характеризуются высокими координационными числами. Многие металлы при сублимации переходят в состояние двухатомных молекул (Li 2, Cu 2, Ga 2 и т. д. ). В целом энергия межатомной связи в переходных металлах соизмерима с энергией ковалентных связей. Между ковалентной и металлической связью имеется сходство. Металлическая связь однако не проявляет свойств насыщаемости. Металлическая связь – многоцентровая химическая связь с дефицитом электронов в твердом или жидком веществе, основанная на обобществлении внешних электронов атомов.
Металлическая связь Металлы отличаются от других веществ высокой электро и теплопроводностью, а их структуры характеризуются высокими координационными числами. Многие металлы при сублимации переходят в состояние двухатомных молекул (Li 2, Cu 2, Ga 2 и т. д. ). В целом энергия межатомной связи в переходных металлах соизмерима с энергией ковалентных связей. Между ковалентной и металлической связью имеется сходство. Металлическая связь однако не проявляет свойств насыщаемости. Металлическая связь – многоцентровая химическая связь с дефицитом электронов в твердом или жидком веществе, основанная на обобществлении внешних электронов атомов.
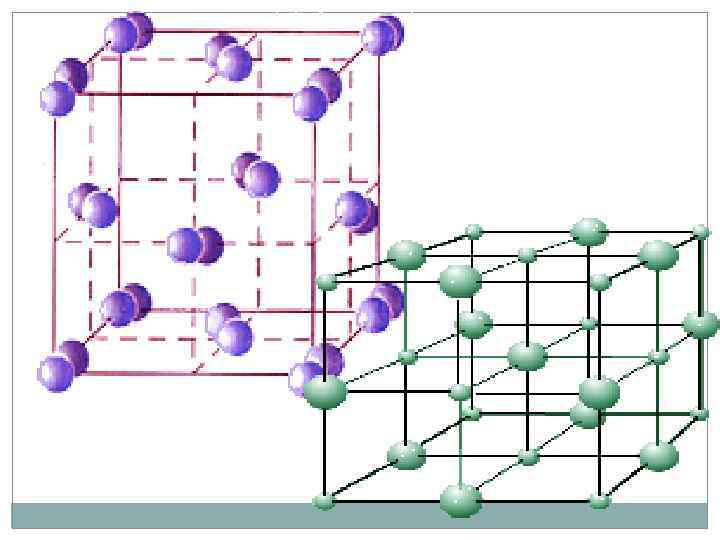
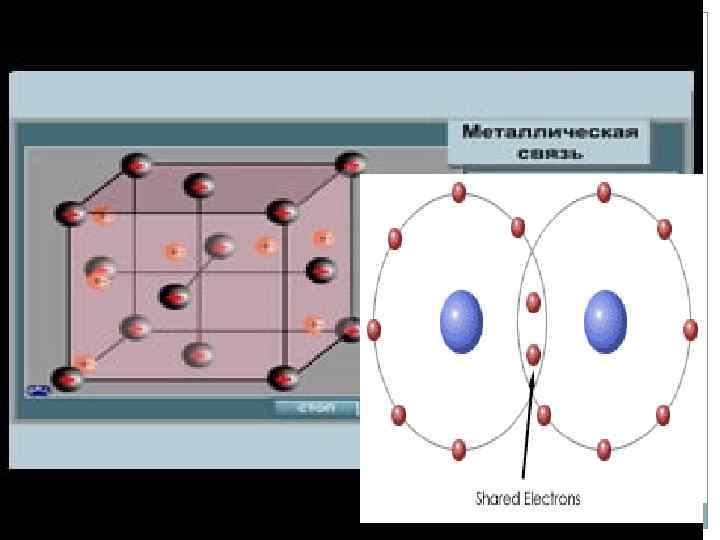
 Из свойств металлов следует, что часть электронов может передвигаться по всему объему металла. С другой стороны из кристаллической структуры металла следует, что их атомы не связаны друг с другом. В кристалле лития орбитали соседних облаков перекрываются. Каждый атом предоставляет на связь 4 валентных орбитали и всего 1 валентный электрон. Значит в кристалле металла число электронов значительно меньше числа орбиталей, поэтому электроны могут переходить из одной орбитали в другую. Тем самым они принимают участие в образовании связи между всеми атомами кристалла металла. Валентные электроны слабо удерживаются в атоме, т. е. легко перемещаются по всему кристаллу, это определяет электрическая проводимость металла. Металл можно рассматривать, как плотно упакованную структуру из (+) заряженных ионов, связанных друг с другом электронным газом.
Из свойств металлов следует, что часть электронов может передвигаться по всему объему металла. С другой стороны из кристаллической структуры металла следует, что их атомы не связаны друг с другом. В кристалле лития орбитали соседних облаков перекрываются. Каждый атом предоставляет на связь 4 валентных орбитали и всего 1 валентный электрон. Значит в кристалле металла число электронов значительно меньше числа орбиталей, поэтому электроны могут переходить из одной орбитали в другую. Тем самым они принимают участие в образовании связи между всеми атомами кристалла металла. Валентные электроны слабо удерживаются в атоме, т. е. легко перемещаются по всему кристаллу, это определяет электрическая проводимость металла. Металл можно рассматривать, как плотно упакованную структуру из (+) заряженных ионов, связанных друг с другом электронным газом.


