азот -Коля.ppt
- Количество слайдов: 34

Лекция II-6 Элементы группы VA

●Общая характеристика ● Азот. Круговорот азота в природе ● Молекулярный азот. Вероятные соединения азота (аммиак, гидразин, амины) ● Оксиды азота. Окислы и загрязнения атмосферы ● Азотистые кислоты. Нитраты. Азотная кислота. Нитриты
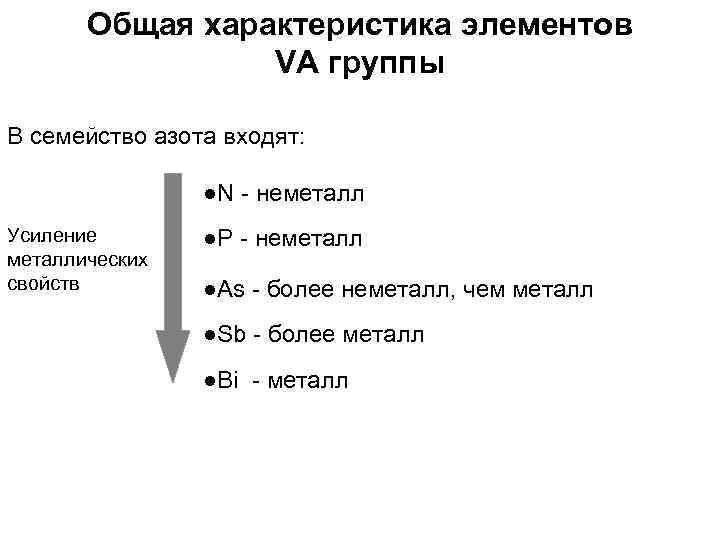
Общая характеристика элементов VA группы В семейство азота входят: ●N - неметалл Усиление металлических свойств ●P - неметалл ●As - более неметалл, чем металл ●Sb - более металл ●Bi - металл

Степень окисления для элементов данного семейства изменяется от -3 до +5 Для As, Sb и Bi наиболее характерные степени окисления от +3 до +5 Все элементы данного семейства проявляют степень окисления +3 в ряде оксидов ●N 2 O 3 – кислотный (ангидрид HNO 2) ●P 4 O 6 – кислотный (ангидрид H 3 PO 4) ●As 4 O 6 – амфотерный, более кислотный характер ●Sb 4 O 6 – амфотерный, более основной характер ●Bi 2 O 3 – основной Конфигурация внешней электронной оболочки ns 2 np 3
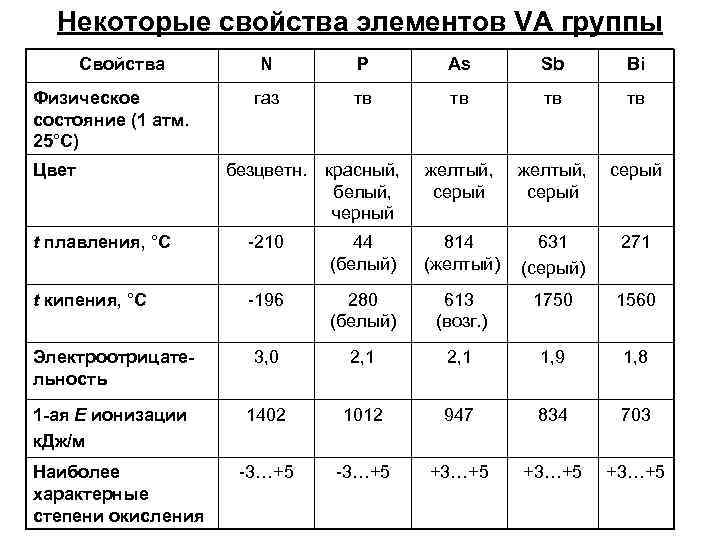
Некоторые свойства элементов VA группы Свойства N P As Sb Bi газ тв тв безцветн. красный, белый, черный желтый, серый t плавления, °С -210 44 (белый) 814 (желтый) 631 (серый) 271 t кипения, °С -196 280 (белый) 613 (возг. ) 1750 1560 Электроотрицательность 3, 0 2, 1 1, 9 1, 8 1 -ая Е ионизации к. Дж/м 1402 1012 947 834 703 -3…+5 +3…+5 Физическое состояние (1 атм. 25°С) Цвет Наиболее характерные степени окисления

Азот возглавляет группу VA В природе находится в виде газа N 2 и различных соединениях – органических и неорганических Молекулярный азот составляет основную часть воздуха: 78% по объему и 76% по весу
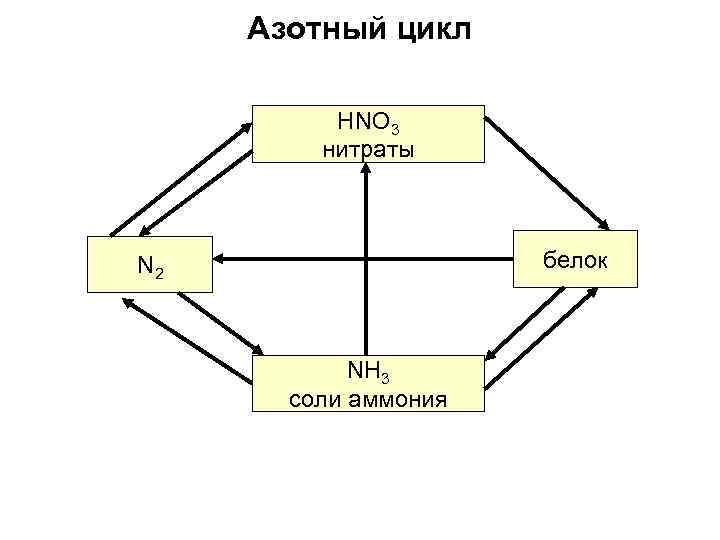
Азотный цикл HNO 3 нитраты белок N 2 NH 3 соли аммония

Азот может напрямую превращаться в аммиак в растениях или живых организмах при помощи фермента "нитросеназа" N 2 фермент NH 3 Процесс носит название "фиксация азота" и имеет большое значение для живой природы Азот также может перерабатываться бактериями в нитраты
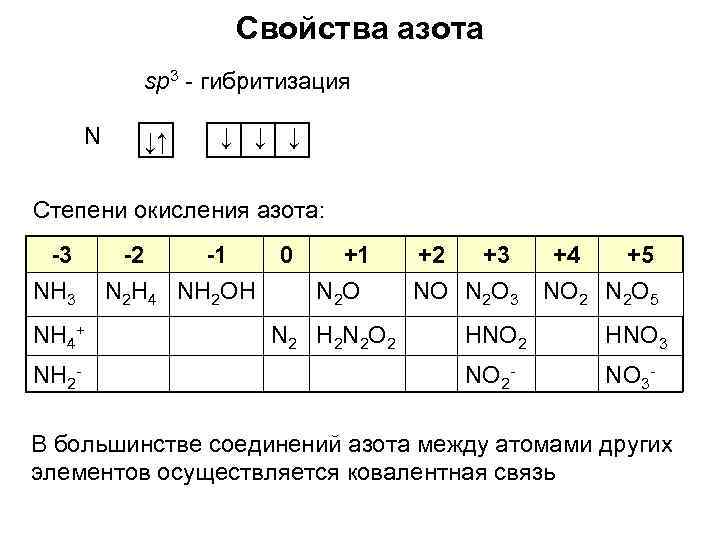
Свойства азота sp 3 - гибритизация N ↓↑ ↓ ↓ ↓ Степени окисления азота: -3 NH 4+ NH 2 - -2 -1 0 +1 N 2 H 4 NH 2 OH N 2 O N 2 H 2 N 2 O 2 +2 +3 NO N 2 O 3 +4 +5 NO 2 N 2 O 5 HNO 2 HNO 3 NO 2 - NO 3 - В большинстве соединений азота между атомами других элементов осуществляется ковалентная связь

Молекулярный азот В промышленности азот получают фракционной перегонкой жидкого воздуха и используют в основном для производства аммиака или создания инертной атмосферы В лаборатории азот можно получить несколькими способами: 1. 2 Na. N 3 300°C 2 N 2 + 2 Na t 2. NH 4 NO 2 N 2 + H 2 O t 3. (NH 4)2 Cr 2 O 7 N 2 + 4 H 2 O + Cr 2 O 3

Свойства молекулярного азота Образование молекулярного азота N 2 из атомов сопровождается выделением большого количества энергии: 2 N N 2 -ΔH = 944 к. Дж/моль k 25° = 10120 Атомы азота в молекуле соединены тройной связью:

Связь в молекуле азота ковалентная, следовательно он неполярен и плохо растворяется в воде и других полярных растворителях В одном объеме воды растворяется 0, 0235 объема азота Прочная внутримолекулярная ковалентная связь в азоте является естественной причиной очень слабого межмолекулярного взаимодействия, что приводит к тому, что он имеет низкие температуры плавления и кипения

Химические свойства азота При обычных условиях азот реагирует с литием, кислородными комплексами переходных металлов и азотофиксирующими бактериями 6 Li + N 2 2 Li 3 N При повышенной температуре азот более активен: N 2 + 3 H 2 kt 2 NH 3 N 2 + O 2 N 2 + 3 Mg 2 NO Mg 3 N 2 + Ca. C 2 C + Ca. HCN

Водородные соединения азота Аммиак – это ковалентное соединение, представляющее собой треугольную пирамиду с атомом азота в вершине Азот в молекуле аммиака имеет sp 3 гибритизацию. Молекула аммиака имеет неподеленную пару электронов, что существенным образом сказывается на его свойствах При нормальных условиях аммиак это газ с резким удушливым запахом и плотностью меньше чем у воздуха

Получение аммиака В промышленности: ●процесс Габера N 2 + 3 H 2 kt 2 NH 3 ΔH = -92, 2 к. Дж/моль t ~ 500°C, P ~ 1000 атм. Катализатор: железо, оксид железа
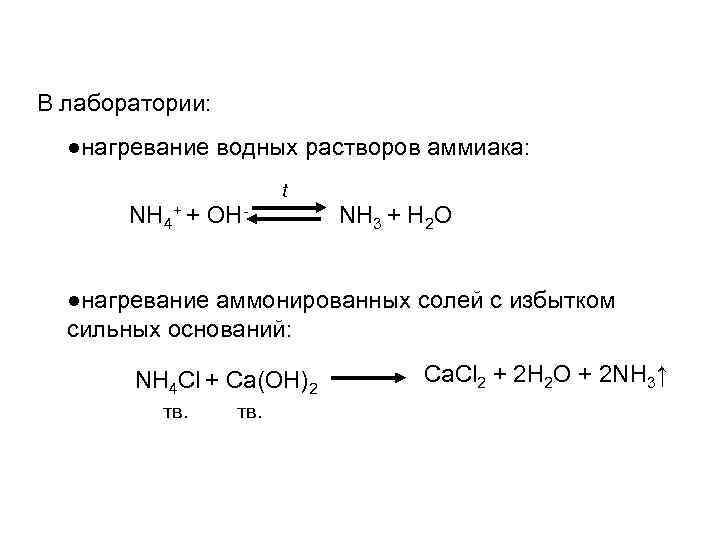
В лаборатории: ●нагревание водных растворов аммиака: t NH 4+ + OH- NH 3 + H 2 O ●нагревание аммонированных солей с избытком сильных оснований: NH 4 Cl + Ca(OH)2 тв. Ca. Cl 2 + 2 H 2 O + 2 NH 3↑

Свойства аммиака 1. Аммиак обладает восстанавливающими способностями 2 NH 3 + 3 Cl N 2 + 6 HCl 2 NH 3 + 3 Cu. O N 2↑ + 3 H 2 O + 3 Cu Аммиак горит в чистом O 2 4 NH 3 + 3 O 2 2 N 2 + 6 H 2 O В присутствии нагретого платинового катализатора 4 NH 3 + 5 O 2 t Pt 4 NO + 6 H 2 O эта реакция используется в промышленном процессе (процесс Оствальда) получения HNO 3

Аммиак очень хорошо растворяется в воде, он может давать 15 М раствор В водном растворе аммиака устанавливается равновесие: NH 3 + H 2 O г NH 4+(aq) + OH-(aq) Kв = 1, 8· 10 -5 ж Добавление раствора аммиака к растворам солей некоторых металлов приводит к осаждению нерастворимых гидроксидов: Cu 2+(aq) + 2 OH-(aq) Cu(OH)2

3. Аммиак – Льисово основание (имеется свободная пара электронов) и может взаимодействовать с акцептором электронов – Льисовой кислотой с образованием донорноакцепторной связи: : NH 3 + H+ NH 4+ NH 3 + HCl NH 4 Cl За счет этого может происходить растворение некоторых гидроксидов в избытке аммиачного раствора Cu(OH)2 + 4 NH 3(aq) [Cu(NH 3)4]2+ + 2 OH-

4. Аммиак легко сжимается и в жидком состоянии подобен воде Молекулы жидкого аммиака связаны водородными связями Аммиак плохо проводит электрический ток, но является прекрасным ионизирующем растворителем NH 3 + NH 3 ж ж осн-2 кисл-1 NH 4+ + NH 2 кисл-2 K = 10 -30 осн-1 Щелочные металлы могут растворятся в аммиаке, но при длительном хранение образуются амиды 2 Na + 2 NH 3 ж 2 Na. NH 2 + H 2
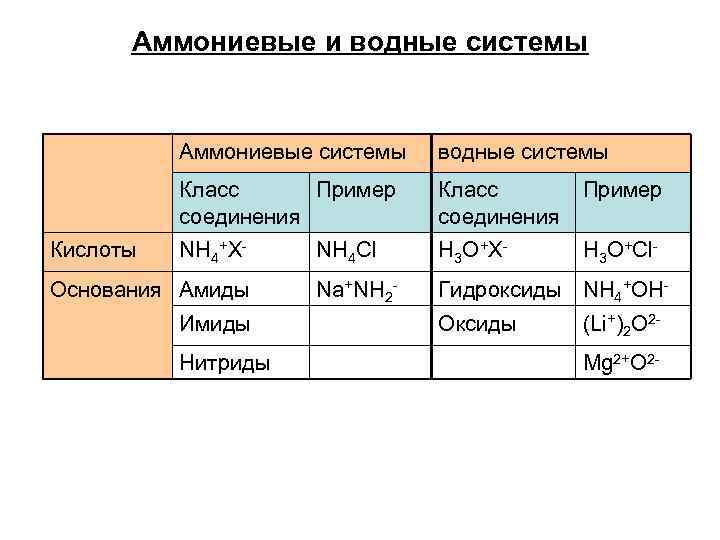
Аммониевые и водные системы Аммониевые системы Класс Пример соединения Кислоты водные системы Класс соединения Пример NH 4+X- NH 4 Cl H 3 O + X - H 3 O+Cl- Na+NH 2 - Гидроксиды NH 4+OH- Основания Амиды Имиды Нитриды Оксиды (Li+)2 O 2 Mg 2+O 2 -

Соли аммония Эти соли содержат ион аммония и имеют ионную природу Как правило они растворимы в воде и подвергаются гидролизу с образованием слабокислых растворов NH 4+ + H 2 O NH 3 + H 3 O+

Все аммониевые соли термически неустойчивы: ●галогениды возгоняются: NH 4 Cl тв NH 3 + HCl г г ●соли кислородных кислот разлагаются, образуя азот или оксид азота: NH 4 NO 2 N 2 + 2 H 2 O NH 4 NO 3 N 2 O + 2 H 2 O 3(NH 4)NO 3 N 2 + 3 SO 2 + 6 H 2 O + 3 NH 3 ●некоторые соли разлагаются с выделением аммиака: (NH 4)2 СO 3 2 NH 3 + H 2 O + СO 2
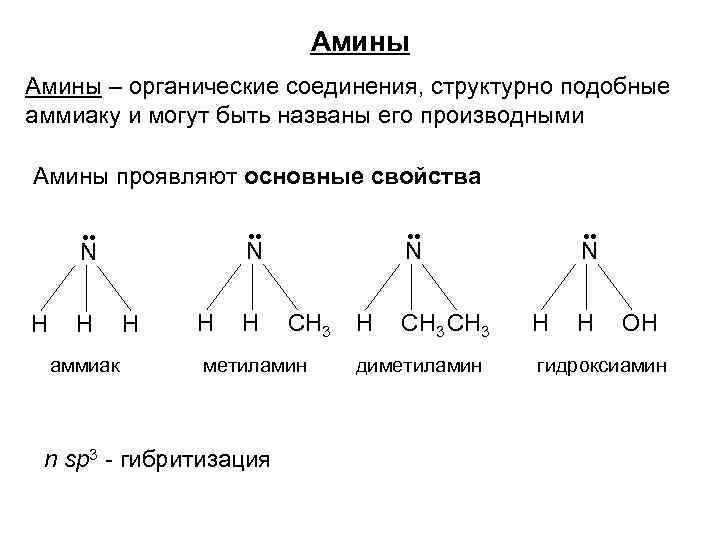
Амины – органические соединения, структурно подобные аммиаку и могут быть названы его производными Амины проявляют основные свойства ●● ●● N N H H аммиак ●● H H H N CH 3 метиламин n sp 3 - гибритизация ●● H CH 3 диметиламин N H H OH гидроксиамин

Гидразин – N 2 H 4 может быть рассмотрен как производная аммиака, в котором водород замещен на NH 2, NH 2 -NH 2. Его можно считать аналогом H 2 O 2 N 2 H 4 – мощный восстановительный агент, обычно он окисляется до N 2 Гидразин используют в ракетных топливах и используют в паре с H 2 O 2

Кислородные соединения азота Оксиды азота Азот образует несколько оксидов со степенями окисления от +1 до +5 ●N 2 O – оксид азота (I) ●NO – оксид азота (II) ●N 2 O 3 – оксид азота (III) ●NO 2 – оксид азота (IV) ●N 2 O 5 – оксид азота (V) Все оксиды устойчивы за исключением N 2 O 3, который разлагается на NO и NO 2 Оксиды азота считаются первичными загрязнителями атмосферы
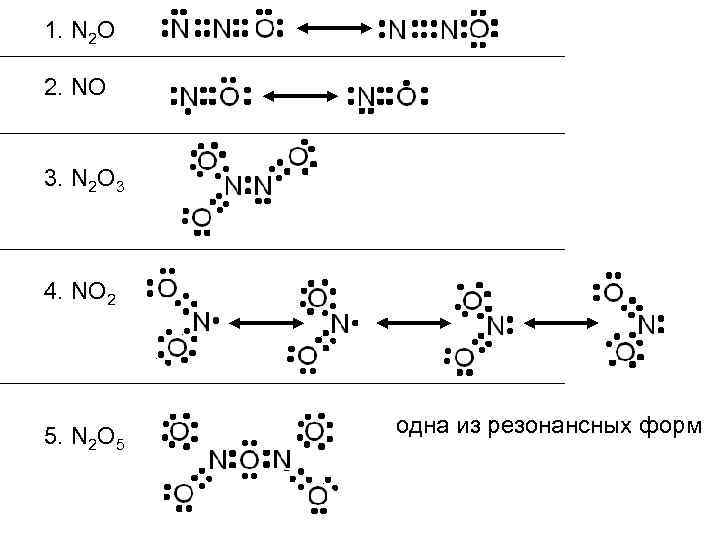
1. N 2 O 2. NO 3. N 2 O 3 4. NO 2 5. N 2 O 5 одна из резонансных форм
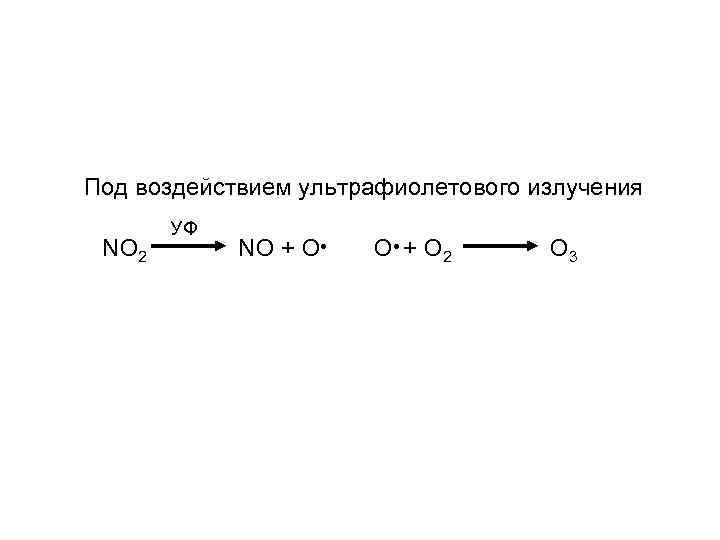
Под воздействием ультрафиолетового излучения NO 2 УФ NO + O● O● + O 2 O 3
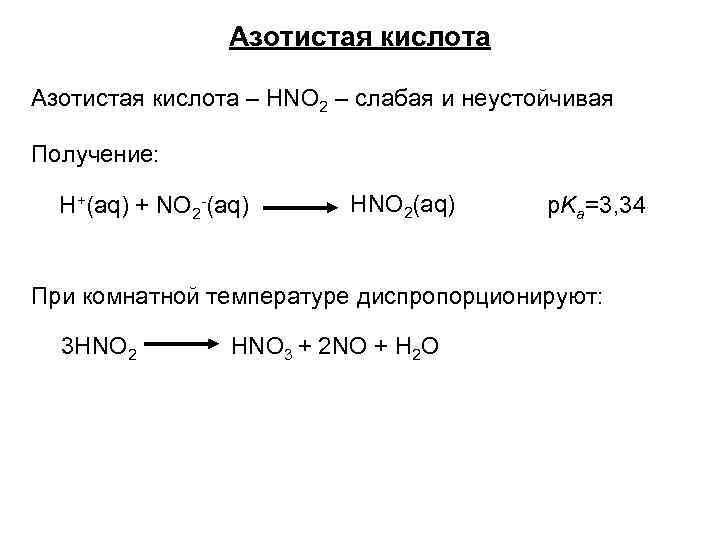
Азотистая кислота – HNO 2 – слабая и неустойчивая Получение: H+(aq) + NO 2 -(aq) HNO 2(aq) p. Ka=3, 34 При комнатной температуре диспропорционируют: 3 HNO 2 HNO 3 + 2 NO + H 2 O
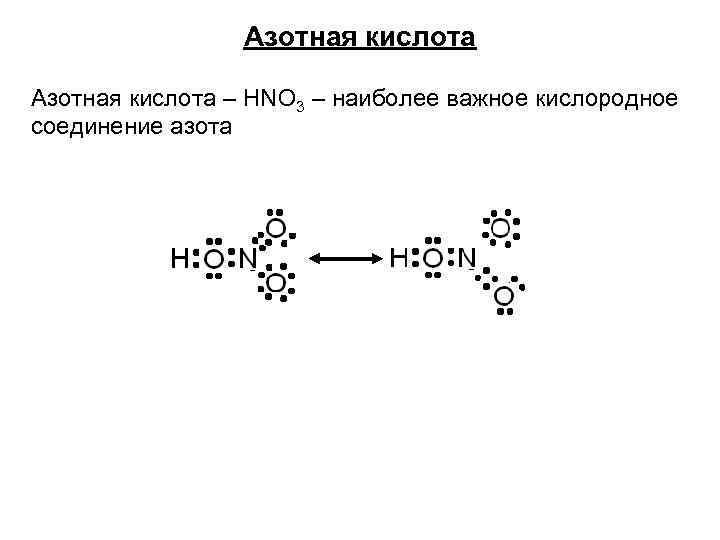
Азотная кислота – HNO 3 – наиболее важное кислородное соединение азота
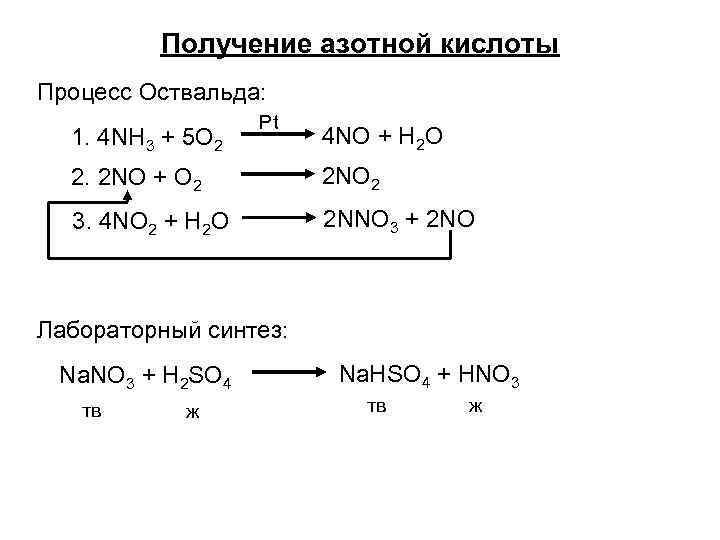
Получение азотной кислоты Процесс Оствальда: 1. 4 NH 3 + 5 O 2 Pt 4 NO + H 2 O 2. 2 NO + O 2 2 NO 2 3. 4 NO 2 + H 2 O 2 NNO 3 + 2 NO Лабораторный синтез: Na. NO 3 + H 2 SO 4 тв ж Na. HSO 4 + HNO 3 тв ж
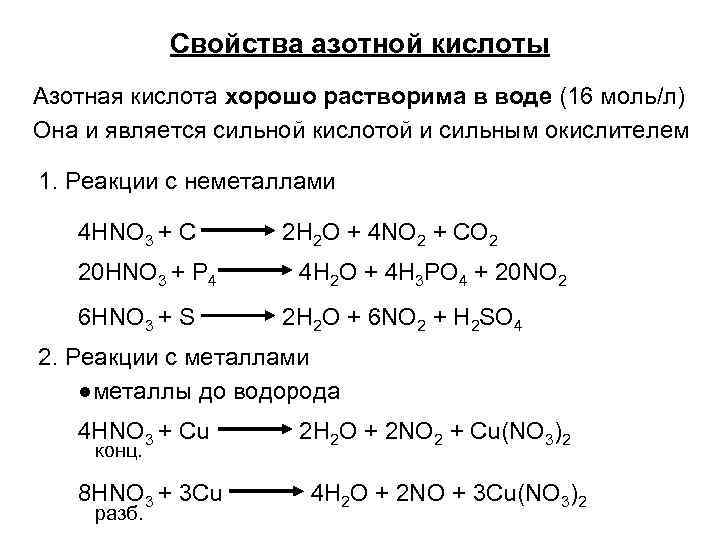
Свойства азотной кислоты Азотная кислота хорошо растворима в воде (16 моль/л) Она и является сильной кислотой и сильным окислителем 1. Реакции с неметаллами 4 HNO 3 + С 20 HNO 3 + P 4 6 HNO 3 + S 2 H 2 O + 4 NO 2 + CO 2 4 H 2 O + 4 H 3 PO 4 + 20 NO 2 2 H 2 O + 6 NO 2 + H 2 SO 4 2. Реакции с металлами ●металлы до водорода 4 HNO 3 + Сu конц. 8 HNO 3 + 3 Сu разб. 2 H 2 O + 2 NO 2 + Cu(NO 3)2 4 H 2 O + 2 NO + 3 Cu(NO 3)2
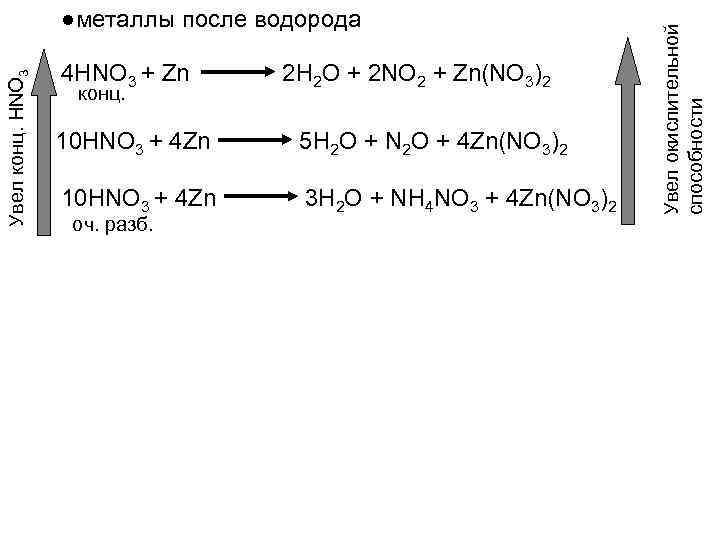
4 HNO 3 + Zn конц. 2 H 2 O + 2 NO 2 + Zn(NO 3)2 10 HNO 3 + 4 Zn 5 H 2 O + N 2 O + 4 Zn(NO 3)2 10 HNO 3 + 4 Zn 3 H 2 O + NH 4 NO 3 + 4 Zn(NO 3)2 оч. разб. Увел окислительной способности Увел конц. HNO 3 ●металлы после водорода

Соли азотной кислоты (нитраты) Соли азотной кислоты хорошо растворимы в воде При нагревании разлагаются Нитраты наиболее активных металлов образуют нитриты 2 KNO 3 t 2 KNO 2 + O 2 Нитраты большинства металлов дают оксид t 2 Cu(NO 3)2 2 Cu. O + NO 2 + O 2 Нитраты малоактивных металлов дают металл 2 Ag. NO 3 t 2 Ag + 2 NO 2 + O 2
азот -Коля.ppt