VA_gruppa__N_P_As (1).ppt
- Количество слайдов: 53
 ЛЕКЦИЯ № 9923634239 VA группа N, P, As, Sb, Bi
ЛЕКЦИЯ № 9923634239 VA группа N, P, As, Sb, Bi
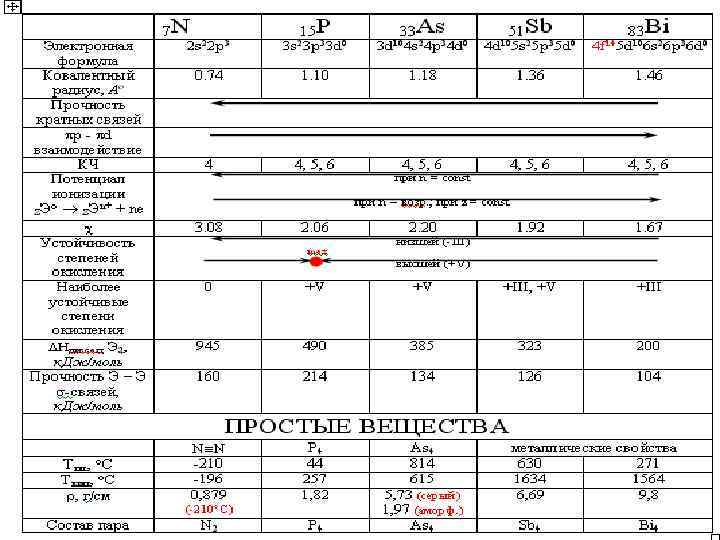
![ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМОВ (nd) np 3 […] ns 2 (n 1)d 10 np 3 ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМОВ (nd) np 3 […] ns 2 (n 1)d 10 np 3](https://present5.com/presentation/18320036_57097823/image-2.jpg) ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМОВ (nd) np 3 […] ns 2 (n 1)d 10 np 3 ns 2 Валентные возможности: N (3, 4); P–Bi (3– 6) С. О. : –III; 0; +III; +V
ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМОВ (nd) np 3 […] ns 2 (n 1)d 10 np 3 ns 2 Валентные возможности: N (3, 4); P–Bi (3– 6) С. О. : –III; 0; +III; +V
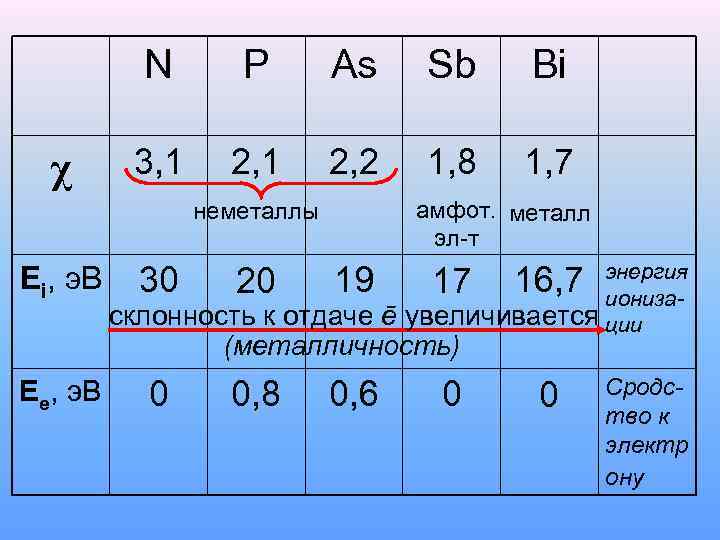 N χ P As Sb Bi 3, 1 2, 2 1, 8 1, 7 амфот. металл эл-т неметаллы Ei, э. В энергия ионизасклонность к отдаче ē увеличивается ции 30 20 19 17 16, 7 (металличность) Ee, э. В 0 0, 8 0, 6 0 0 Сродство к электр ону
N χ P As Sb Bi 3, 1 2, 2 1, 8 1, 7 амфот. металл эл-т неметаллы Ei, э. В энергия ионизасклонность к отдаче ē увеличивается ции 30 20 19 17 16, 7 (металличность) Ee, э. В 0 0, 8 0, 6 0 0 Сродство к электр ону
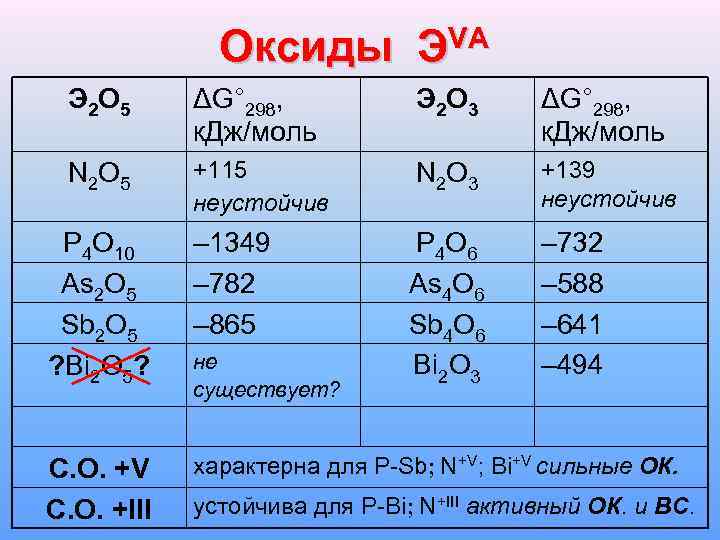 Оксиды ЭVA Э 2 О 5 ΔG° 298, к. Дж/моль Э 2 О 3 ΔG° 298, к. Дж/моль N 2 O 5 +115 неустойчив N 2 O 3 +139 неустойчив P 4 O 10 As 2 O 5 Sb 2 O 5 ? Bi 2 O 5? – 1349 – 782 – 865 P 4 O 6 As 4 O 6 Sb 4 O 6 Bi 2 O 3 – 732 – 588 – 641 – 494 С. О. +V С. О. +III характерна для P-Sb; N+V; Bi+V сильные ОК. не существует? устойчива для P-Bi; N+III активный ОК. и ВС.
Оксиды ЭVA Э 2 О 5 ΔG° 298, к. Дж/моль Э 2 О 3 ΔG° 298, к. Дж/моль N 2 O 5 +115 неустойчив N 2 O 3 +139 неустойчив P 4 O 10 As 2 O 5 Sb 2 O 5 ? Bi 2 O 5? – 1349 – 782 – 865 P 4 O 6 As 4 O 6 Sb 4 O 6 Bi 2 O 3 – 732 – 588 – 641 – 494 С. О. +V С. О. +III характерна для P-Sb; N+V; Bi+V сильные ОК. не существует? устойчива для P-Bi; N+III активный ОК. и ВС.
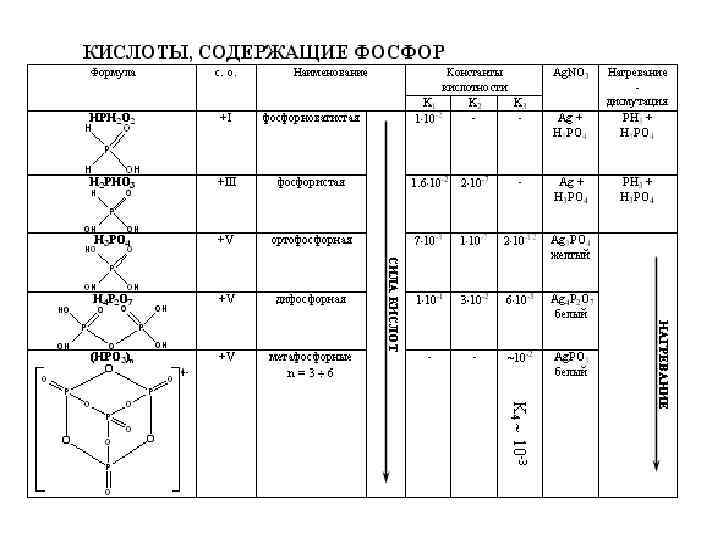
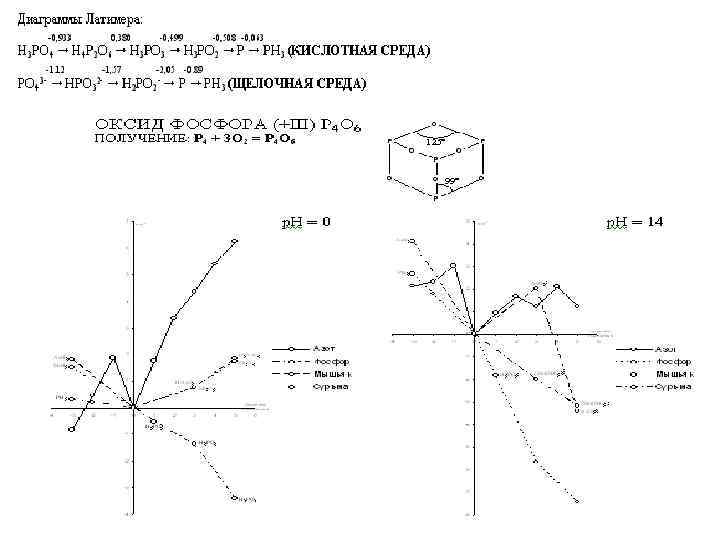
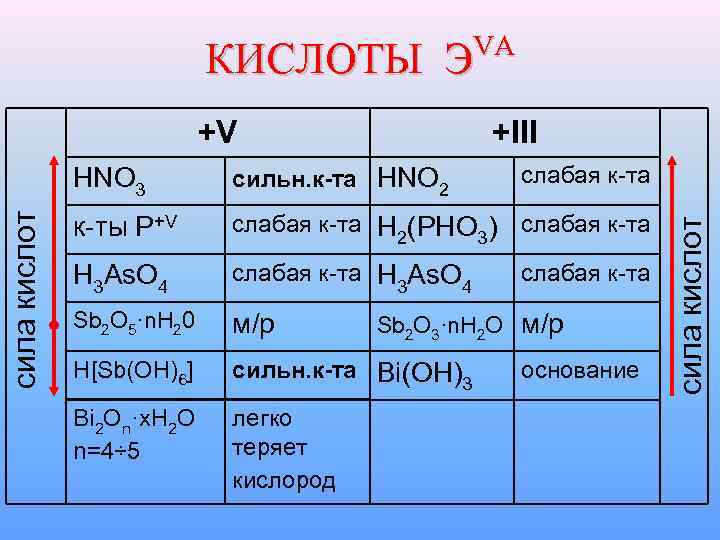 VA КИСЛОТЫ Э +V +III сильн. к та HNO 2 слабая к-та к-ты P+V слабая к-та H (PHO ) 2 3 слабая к-та H 3 As. O 4 слабая к-та H As. O 3 4 слабая к-та Sb 2 O 5·n. H 20 м/р H[Sb(OH)6] сильн. к та Bi(OH) 3 Bi 2 On·x. H 2 O легко теряет n=4÷ 5 кислород Sb 2 O 3·n. H 2 O основание сила кислот HNO 3
VA КИСЛОТЫ Э +V +III сильн. к та HNO 2 слабая к-та к-ты P+V слабая к-та H (PHO ) 2 3 слабая к-та H 3 As. O 4 слабая к-та H As. O 3 4 слабая к-та Sb 2 O 5·n. H 20 м/р H[Sb(OH)6] сильн. к та Bi(OH) 3 Bi 2 On·x. H 2 O легко теряет n=4÷ 5 кислород Sb 2 O 3·n. H 2 O основание сила кислот HNO 3
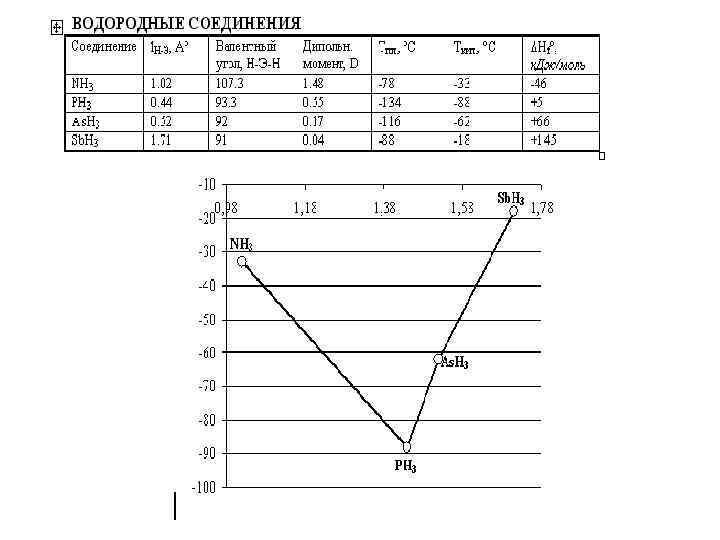
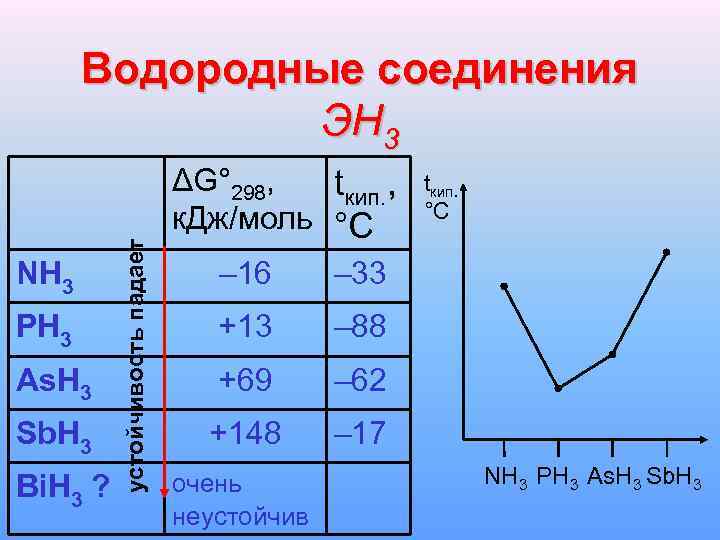 NH 3 PH 3 As. H 3 Sb. H 3 Bi. H 3 ? устойчивость падает Водородные соединения ЭН 3 ΔG° 298, tкип. , к. Дж/моль °С – 16 – 33 +13 – 88 +69 – 62 +148 tкип. °С – 17 очень неустойчив NH 3 PH 3 As. H 3 Sb. H 3
NH 3 PH 3 As. H 3 Sb. H 3 Bi. H 3 ? устойчивость падает Водородные соединения ЭН 3 ΔG° 298, tкип. , к. Дж/моль °С – 16 – 33 +13 – 88 +69 – 62 +148 tкип. °С – 17 очень неустойчив NH 3 PH 3 As. H 3 Sb. H 3
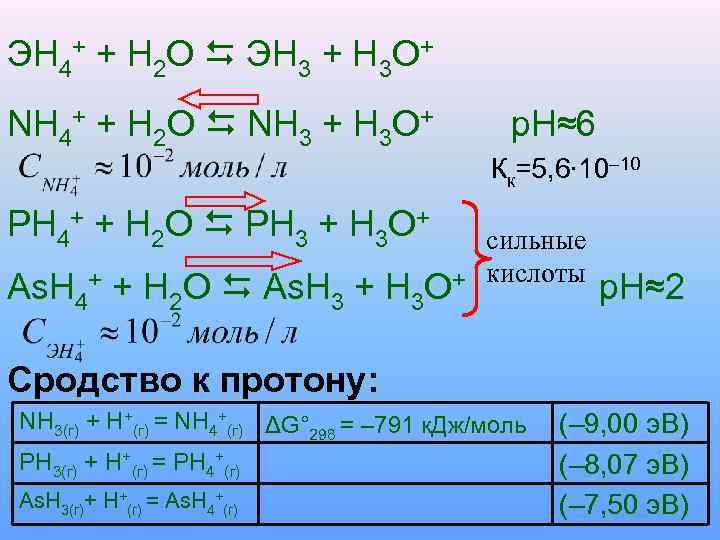 ЭН 4+ + Н 2 О ЭН 3 + Н 3 О+ NH 4+ + H 2 O NH 3 + H 3 O+ p. H≈6 Кк=5, 6∙ 10– 10 PH 4+ + H 2 O PH 3 + H 3 O+ As. H 4+ + H 2 O As. H 3 + H 3 O сильные кислоты + p. H≈2 Сродство к протону: NH 3(г) + H+(г) = NH 4+(г) ΔG° 298 = – 791 к. Дж/моль PH 3(г) + H+(г) = PH 4+(г) As. H 3(г)+ H+(г) = As. H 4+(г) (– 9, 00 э. В) (– 8, 07 э. В) (– 7, 50 э. В)
ЭН 4+ + Н 2 О ЭН 3 + Н 3 О+ NH 4+ + H 2 O NH 3 + H 3 O+ p. H≈6 Кк=5, 6∙ 10– 10 PH 4+ + H 2 O PH 3 + H 3 O+ As. H 4+ + H 2 O As. H 3 + H 3 O сильные кислоты + p. H≈2 Сродство к протону: NH 3(г) + H+(г) = NH 4+(г) ΔG° 298 = – 791 к. Дж/моль PH 3(г) + H+(г) = PH 4+(г) As. H 3(г)+ H+(г) = As. H 4+(г) (– 9, 00 э. В) (– 8, 07 э. В) (– 7, 50 э. В)
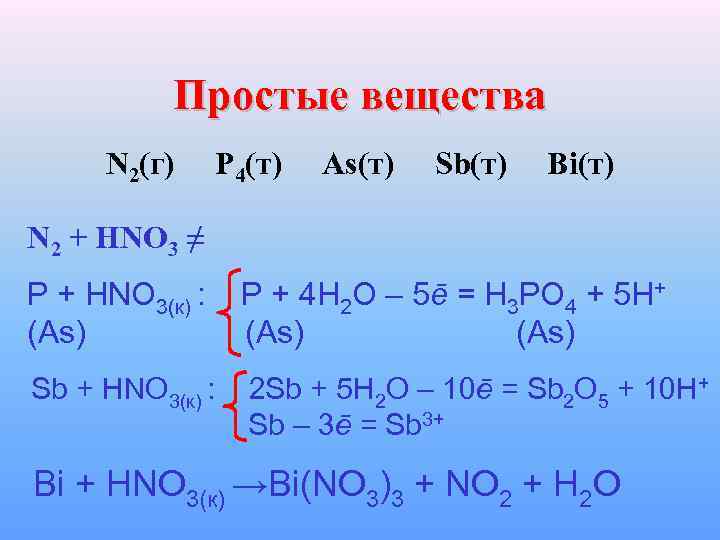 Простые вещества N 2(г) P 4(т) As(т) Sb(т) Bi(т) N 2 + HNO 3 ≠ P + HNO 3(к) : P + 4 H 2 O – 5ē = H 3 PO 4 + 5 H+ (As) (As) Sb + HNO 3(к) : 2 Sb + 5 H 2 O – 10ē = Sb 2 O 5 + 10 H+ Sb – 3ē = Sb 3+ Bi + HNO 3(к) →Bi(NO 3)3 + NO 2 + H 2 O
Простые вещества N 2(г) P 4(т) As(т) Sb(т) Bi(т) N 2 + HNO 3 ≠ P + HNO 3(к) : P + 4 H 2 O – 5ē = H 3 PO 4 + 5 H+ (As) (As) Sb + HNO 3(к) : 2 Sb + 5 H 2 O – 10ē = Sb 2 O 5 + 10 H+ Sb – 3ē = Sb 3+ Bi + HNO 3(к) →Bi(NO 3)3 + NO 2 + H 2 O
 Распространенность в природе N P As Sb Bi 0, 04 0, 12 5∙ 10– 4 5∙ 10– 5 1∙ 10– 5 N 2: атмосфера P: Апатиты 3 Ca 3(PO 4)2∙Ca(F, Cl) Фосфориты 3 Ca 3(PO 4)2∙Ca(OH)2 As – Bi – сульфидные руды: As 4 S 4 – реальгар As 2 S 3 – аурипигмент Sb 2 S 3 – антимонит Bi 2 S 3 – висмутин
Распространенность в природе N P As Sb Bi 0, 04 0, 12 5∙ 10– 4 5∙ 10– 5 1∙ 10– 5 N 2: атмосфера P: Апатиты 3 Ca 3(PO 4)2∙Ca(F, Cl) Фосфориты 3 Ca 3(PO 4)2∙Ca(OH)2 As – Bi – сульфидные руды: As 4 S 4 – реальгар As 2 S 3 – аурипигмент Sb 2 S 3 – антимонит Bi 2 S 3 – висмутин
 Водородные соединения азота ΔG° 298, к. Дж/моль NH 3 аммиак N 2 H 4 гидразин +149 NH 2 OH гидроксиламин – 18 HN 3 азид водорода – 17 +327 взр. неуст. : t 3 N 2 H 4 = 4 NH 3 + N 2 взр. неуст. : 2 HN 3 = 3 N 2 + H 2
Водородные соединения азота ΔG° 298, к. Дж/моль NH 3 аммиак N 2 H 4 гидразин +149 NH 2 OH гидроксиламин – 18 HN 3 азид водорода – 17 +327 взр. неуст. : t 3 N 2 H 4 = 4 NH 3 + N 2 взр. неуст. : 2 HN 3 = 3 N 2 + H 2
 АММИАК NH 3 N tпл. = – 78 °C tкип. = – 33, 4 °C H H H sp 3 – гибридизация µ = 1, 46 D 107° (полярная молекула) NH 3(ж): (NH 3)n водородные связи автопротолиз NH 3 + NH 3 ↔ NH 2–(S) + NH 4+(S); KS = 10– 33 (Хьюи, с. 223 – 227)
АММИАК NH 3 N tпл. = – 78 °C tкип. = – 33, 4 °C H H H sp 3 – гибридизация µ = 1, 46 D 107° (полярная молекула) NH 3(ж): (NH 3)n водородные связи автопротолиз NH 3 + NH 3 ↔ NH 2–(S) + NH 4+(S); KS = 10– 33 (Хьюи, с. 223 – 227)
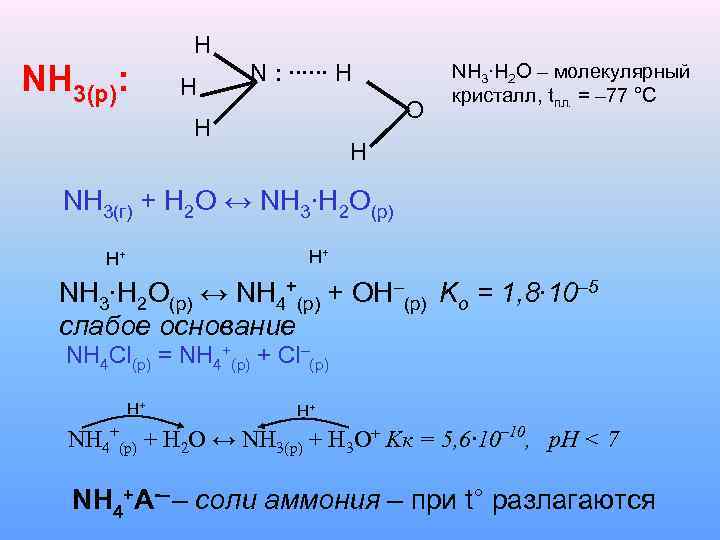 H NH 3(р): H N : ∙∙∙∙∙∙ H O H NH 3∙H 2 O – молекулярный кристалл, tпл. = – 77 °C H NH 3(г) + H 2 O ↔ NH 3∙H 2 O(р) H+ H+ NH 3∙H 2 O(р) ↔ NH 4+(р) + OH–(р) Ko = 1, 8∙ 10– 5 слабое основание NH 4 Cl(р) = NH 4+(р) + Cl–(р) H+ H+ NH 4+(р) + H 2 O ↔ NH 3(р) + H 3 O+ Kк = 5, 6∙ 10– 10, p. H < 7 NH 4+A – – соли аммония – при t° разлагаются
H NH 3(р): H N : ∙∙∙∙∙∙ H O H NH 3∙H 2 O – молекулярный кристалл, tпл. = – 77 °C H NH 3(г) + H 2 O ↔ NH 3∙H 2 O(р) H+ H+ NH 3∙H 2 O(р) ↔ NH 4+(р) + OH–(р) Ko = 1, 8∙ 10– 5 слабое основание NH 4 Cl(р) = NH 4+(р) + Cl–(р) H+ H+ NH 4+(р) + H 2 O ↔ NH 3(р) + H 3 O+ Kк = 5, 6∙ 10– 10, p. H < 7 NH 4+A – – соли аммония – при t° разлагаются
 Получение NH 3 промышленность: 3 H 2 + N 2 ↔ 2 NH 3 (t, p, катализ. , циркуляция N 2 и H 2) лаборатория: NH 4 Cl(т) + Na. OH(т) = NH 3↑ + Na. Cl + H 2 O
Получение NH 3 промышленность: 3 H 2 + N 2 ↔ 2 NH 3 (t, p, катализ. , циркуляция N 2 и H 2) лаборатория: NH 4 Cl(т) + Na. OH(т) = NH 3↑ + Na. Cl + H 2 O
 Окислительно восстановительные свойства NH 3(г): 4 NH 3 + O 2 = 2 N 2 + 6 H 2 O кат. 4 NH 3 + O 2 = 2 NO + 6 H 2 O (Pt, Rh) NH 3(р): 8 NH 3∙H 2 O – 6ē = N 2 + 8 H 2 O + 6 NH 4+ p. H ≤ 7 φ° = +0, 23 B 2 NH 3∙H 2 O + 6 OH– – 6ē = N 2 + 8 H 2 O p. H >7 φ° = – 0, 74 B 8 NH 3∙H 2 O + 3 Br 2(р) = N 2 + 8 H 2 O + 6 NH 4 Br 6 NH 3∙H 2 O + 2 KMn. O 4 = 3 N 2 + 2 Mn. O 2 + 4 H 2 O + 2 KOH
Окислительно восстановительные свойства NH 3(г): 4 NH 3 + O 2 = 2 N 2 + 6 H 2 O кат. 4 NH 3 + O 2 = 2 NO + 6 H 2 O (Pt, Rh) NH 3(р): 8 NH 3∙H 2 O – 6ē = N 2 + 8 H 2 O + 6 NH 4+ p. H ≤ 7 φ° = +0, 23 B 2 NH 3∙H 2 O + 6 OH– – 6ē = N 2 + 8 H 2 O p. H >7 φ° = – 0, 74 B 8 NH 3∙H 2 O + 3 Br 2(р) = N 2 + 8 H 2 O + 6 NH 4 Br 6 NH 3∙H 2 O + 2 KMn. O 4 = 3 N 2 + 2 Mn. O 2 + 4 H 2 O + 2 KOH
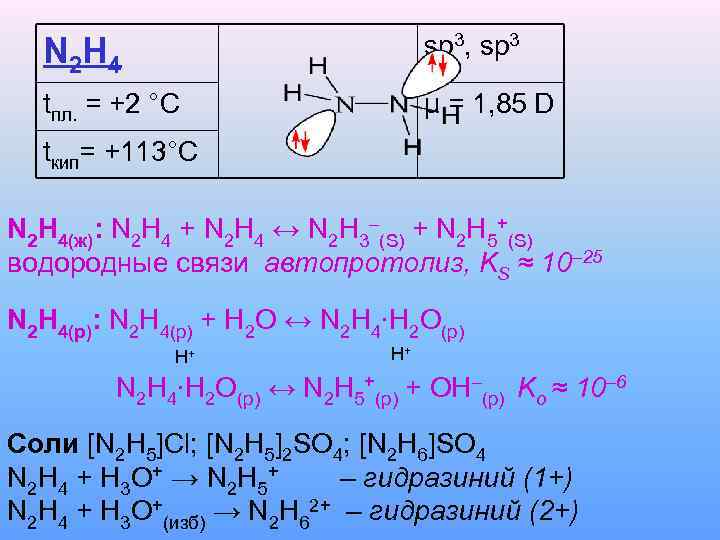 N 2 H 4 sp 3, sp 3 tпл. = +2 °C µ = 1, 85 D tкип= +113°C N 2 H 4(ж): N 2 H 4 + N 2 H 4 ↔ N 2 H 3–(S) + N 2 H 5+(S) водородные связи автопротолиз, KS ≈ 10– 25 N 2 H 4(p): N 2 H 4(p) + H 2 O ↔ N 2 H 4∙H 2 O(p) H+ H+ N 2 H 4∙H 2 O(p) ↔ N 2 H 5+(p) + OH–(p) Ko ≈ 10– 6 Соли [N 2 H 5]Cl; [N 2 H 5]2 SO 4; [N 2 H 6]SO 4 N 2 H 4 + H 3 O+ → N 2 H 5+ – гидразиний (1+) N 2 H 4 + H 3 O+(изб) → N 2 H 62+ – гидразиний (2+)
N 2 H 4 sp 3, sp 3 tпл. = +2 °C µ = 1, 85 D tкип= +113°C N 2 H 4(ж): N 2 H 4 + N 2 H 4 ↔ N 2 H 3–(S) + N 2 H 5+(S) водородные связи автопротолиз, KS ≈ 10– 25 N 2 H 4(p): N 2 H 4(p) + H 2 O ↔ N 2 H 4∙H 2 O(p) H+ H+ N 2 H 4∙H 2 O(p) ↔ N 2 H 5+(p) + OH–(p) Ko ≈ 10– 6 Соли [N 2 H 5]Cl; [N 2 H 5]2 SO 4; [N 2 H 6]SO 4 N 2 H 4 + H 3 O+ → N 2 H 5+ – гидразиний (1+) N 2 H 4 + H 3 O+(изб) → N 2 H 62+ – гидразиний (2+)
 Окислительно восстановительные свойства (Восст. св-ва p. H<7 N 2 H 5+ – 4ē = N 2 + 5 H+ сильнее при p. H>7 N 2 H 4∙H 2 O + 4 OH– – 4ē = p. H>7) N 2 + 5 H 2 O φ° = – 0, 24 B Окисл. св-ва p. H<7 N 2 H 5+ + 3 H+ + 2ē = 2 NH 4+ (сильнее при p. H<7) p. H>7 N 2 H 4∙H 2 O + 2ē φ° = +1, 27 B φ° = – 1, 16 B φ° = +0, 03 B = 2 NH 3∙H 2 O + 2 OH– Примеры: N 2 H 4 + 2 I 2 = N 2(г) + 4 HI t 3 N 2 H 4 = N 2(г) + 4 NH 3(г) Получение: 2 NH 3 + Na. Cl. O = N 2 H 4 + Na. Cl + H 2 O
Окислительно восстановительные свойства (Восст. св-ва p. H<7 N 2 H 5+ – 4ē = N 2 + 5 H+ сильнее при p. H>7 N 2 H 4∙H 2 O + 4 OH– – 4ē = p. H>7) N 2 + 5 H 2 O φ° = – 0, 24 B Окисл. св-ва p. H<7 N 2 H 5+ + 3 H+ + 2ē = 2 NH 4+ (сильнее при p. H<7) p. H>7 N 2 H 4∙H 2 O + 2ē φ° = +1, 27 B φ° = – 1, 16 B φ° = +0, 03 B = 2 NH 3∙H 2 O + 2 OH– Примеры: N 2 H 4 + 2 I 2 = N 2(г) + 4 HI t 3 N 2 H 4 = N 2(г) + 4 NH 3(г) Получение: 2 NH 3 + Na. Cl. O = N 2 H 4 + Na. Cl + H 2 O
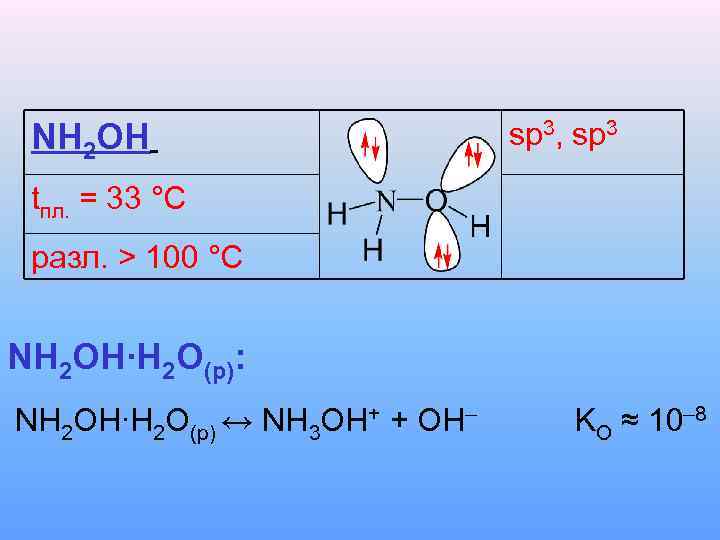 NH 2 OH sp 3, sp 3 tпл. = 33 °C разл. > 100 °C NH 2 OH∙H 2 O(p): NH 2 OH∙H 2 O(p) ↔ NH 3 OH+ + OH– KO ≈ 10– 8
NH 2 OH sp 3, sp 3 tпл. = 33 °C разл. > 100 °C NH 2 OH∙H 2 O(p): NH 2 OH∙H 2 O(p) ↔ NH 3 OH+ + OH– KO ≈ 10– 8
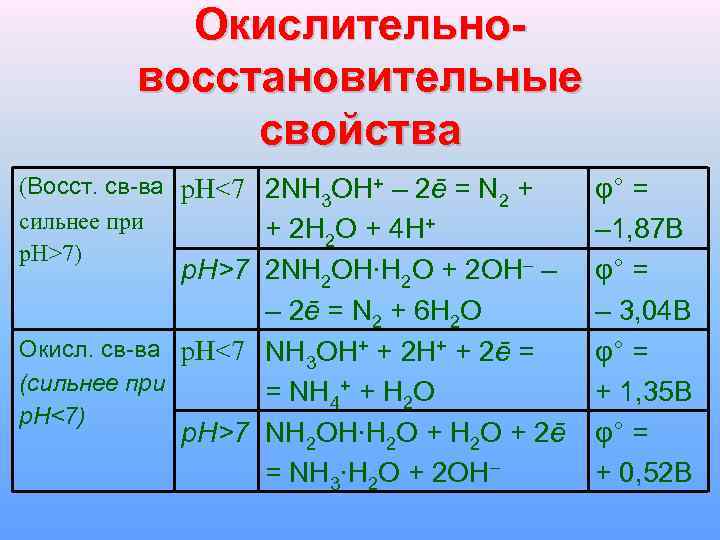 Окислительно восстановительные свойства (Восст. св-ва p. H<7 2 NH OH+ – 2ē = N + 3 2 сильнее при + 2 H 2 O + 4 H+ p. H>7) – φ° = – 1, 87 B p. H>7 2 NH 2 OH∙H 2 O + 2 OH – φ° = – 2ē = N 2 + 6 H 2 O – 3, 04 B Окисл. св-ва p. H<7 NH OH+ + 2ē = φ° = 3 (сильнее при = NH 4+ + H 2 O + 1, 35 B p. H<7) p. H>7 NH 2 OH∙H 2 O + 2ē φ° = = NH 3∙H 2 O + 2 OH– + 0, 52 B
Окислительно восстановительные свойства (Восст. св-ва p. H<7 2 NH OH+ – 2ē = N + 3 2 сильнее при + 2 H 2 O + 4 H+ p. H>7) – φ° = – 1, 87 B p. H>7 2 NH 2 OH∙H 2 O + 2 OH – φ° = – 2ē = N 2 + 6 H 2 O – 3, 04 B Окисл. св-ва p. H<7 NH OH+ + 2ē = φ° = 3 (сильнее при = NH 4+ + H 2 O + 1, 35 B p. H<7) p. H>7 NH 2 OH∙H 2 O + 2ē φ° = = NH 3∙H 2 O + 2 OH– + 0, 52 B
 ПРИМЕРЫ ОКИСЛ. ВОССТАН. СВОЙСТВ ГИДРОКСИЛАМИНА 2 NH 2 OH + I 2 + 2 KOH = N 2(г) + 2 KI + 4 H 2 O t 3 NH 2 OH = NH 3 + N 2 + 3 H 2 O Pt NH 2 OH → N 2 + NH 3 +N 2 O (OH–)
ПРИМЕРЫ ОКИСЛ. ВОССТАН. СВОЙСТВ ГИДРОКСИЛАМИНА 2 NH 2 OH + I 2 + 2 KOH = N 2(г) + 2 KI + 4 H 2 O t 3 NH 2 OH = NH 3 + N 2 + 3 H 2 O Pt NH 2 OH → N 2 + NH 3 +N 2 O (OH–)
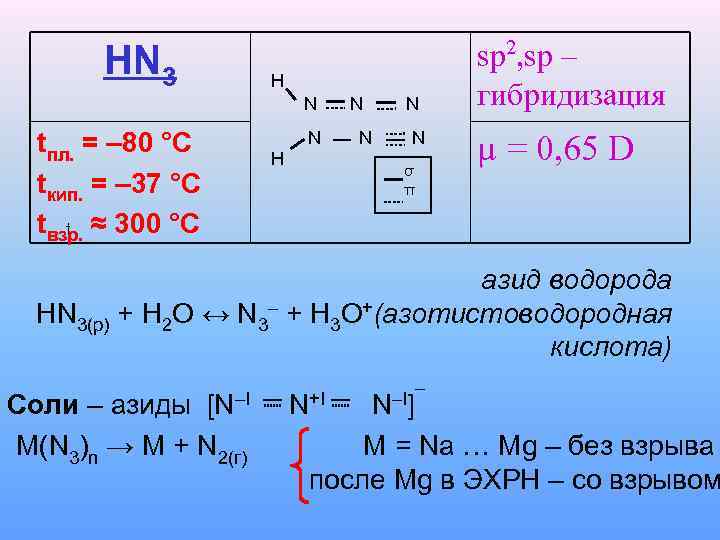 HN 3 H N tпл. = – 80 °C tкип. = – 37 °C tвзр. ≈ 300 °C t N H N N σ π sp 2, sp – гибридизация µ = 0, 65 D азид водорода HN 3(p) + H 2 O ↔ N 3– + H 3 O+(азотистоводородная кислота) Соли – азиды [N–I N+I N–I] – M(N 3)n → M + N 2(г) M = Na … Mg – без взрыва после Mg в ЭХРН – со взрывом
HN 3 H N tпл. = – 80 °C tкип. = – 37 °C tвзр. ≈ 300 °C t N H N N σ π sp 2, sp – гибридизация µ = 0, 65 D азид водорода HN 3(p) + H 2 O ↔ N 3– + H 3 O+(азотистоводородная кислота) Соли – азиды [N–I N+I N–I] – M(N 3)n → M + N 2(г) M = Na … Mg – без взрыва после Mg в ЭХРН – со взрывом
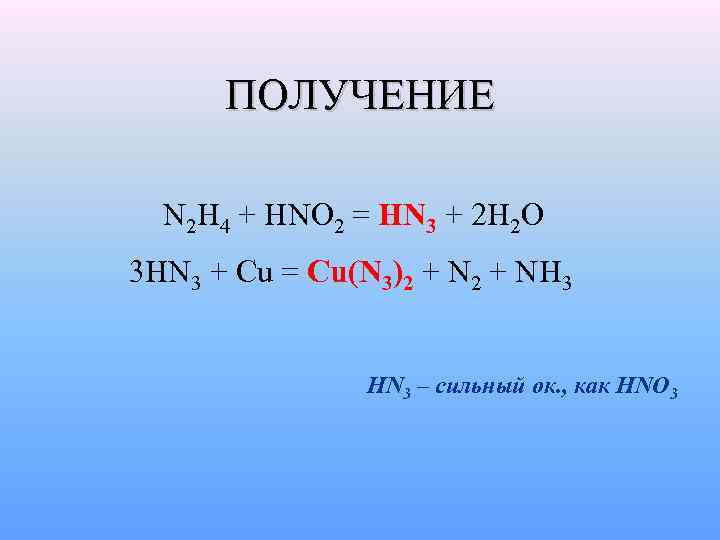 ПОЛУЧЕНИЕ N 2 H 4 + HNO 2 = HN 3 + 2 H 2 O 3 HN 3 + Cu = Cu(N 3)2 + NH 3 HN 3 – сильный ок. , как HNO 3
ПОЛУЧЕНИЕ N 2 H 4 + HNO 2 = HN 3 + 2 H 2 O 3 HN 3 + Cu = Cu(N 3)2 + NH 3 HN 3 – сильный ок. , как HNO 3
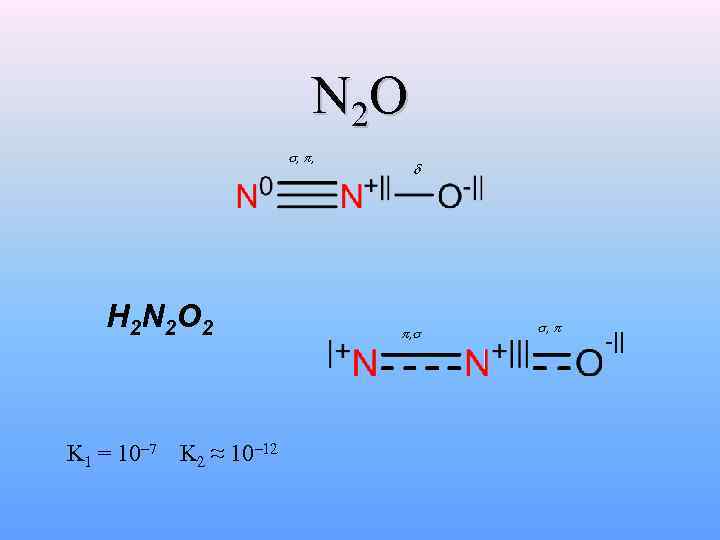 N 2 O , , H 2 N 2 O 2 K 1 = 10– 7 K 2 ≈ 10– 12 , , -||
N 2 O , , H 2 N 2 O 2 K 1 = 10– 7 K 2 ≈ 10– 12 , , -||
 Получение: NH 4 NO 3 = N 2 O + 2 H 2 O t < 400 °C
Получение: NH 4 NO 3 = N 2 O + 2 H 2 O t < 400 °C
 N 2 O - окислитель 2 N 2 O = 2 N 2 + O 2 t > 400 °C
N 2 O - окислитель 2 N 2 O = 2 N 2 + O 2 t > 400 °C
![NO [N+II O-II : ]+ нитрозил-катион 2 NO(г) ↔ N 2 O 2(ж, т) NO [N+II O-II : ]+ нитрозил-катион 2 NO(г) ↔ N 2 O 2(ж, т)](https://present5.com/presentation/18320036_57097823/image-25.jpg) NO [N+II O-II : ]+ нитрозил-катион 2 NO(г) ↔ N 2 O 2(ж, т) 2 NO(г) + O 2(г) =2 NO 2(г) N+II – 2ē = N+IV NO – восстановитель
NO [N+II O-II : ]+ нитрозил-катион 2 NO(г) ↔ N 2 O 2(ж, т) 2 NO(г) + O 2(г) =2 NO 2(г) N+II – 2ē = N+IV NO – восстановитель
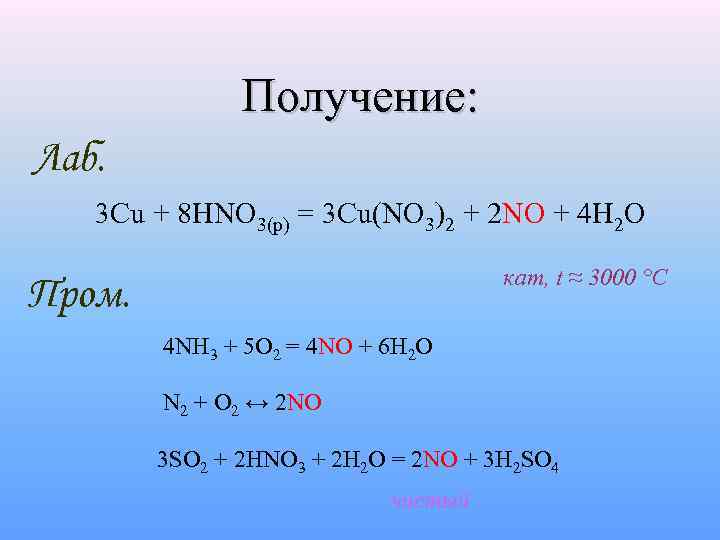 Получение: Лаб. 3 Cu + 8 HNO 3(p) = 3 Cu(NO 3)2 + 2 NO + 4 H 2 O кат, t ≈ 3000 °C Пром. 4 NH 3 + 5 O 2 = 4 NO + 6 H 2 O N 2 + O 2 ↔ 2 NO 3 SO 2 + 2 HNO 3 + 2 H 2 O = 2 NO + 3 H 2 SO 4 чистый
Получение: Лаб. 3 Cu + 8 HNO 3(p) = 3 Cu(NO 3)2 + 2 NO + 4 H 2 O кат, t ≈ 3000 °C Пром. 4 NH 3 + 5 O 2 = 4 NO + 6 H 2 O N 2 + O 2 ↔ 2 NO 3 SO 2 + 2 HNO 3 + 2 H 2 O = 2 NO + 3 H 2 SO 4 чистый
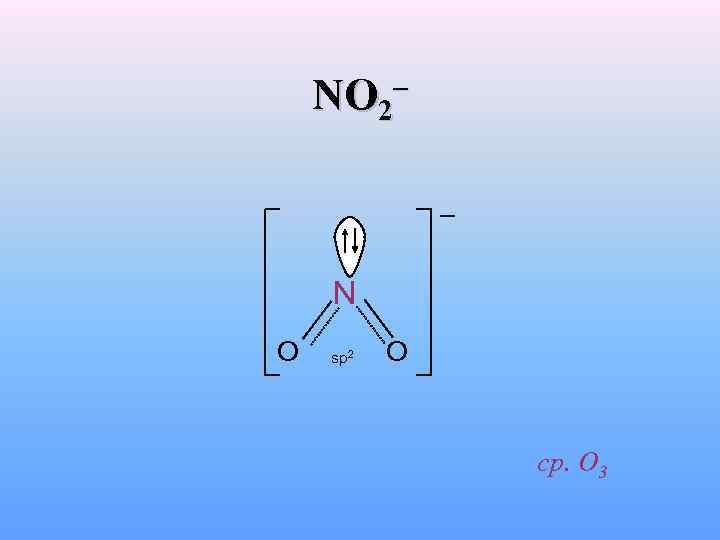 – NO 2 N O sp 2 O ср. O 3
– NO 2 N O sp 2 O ср. O 3
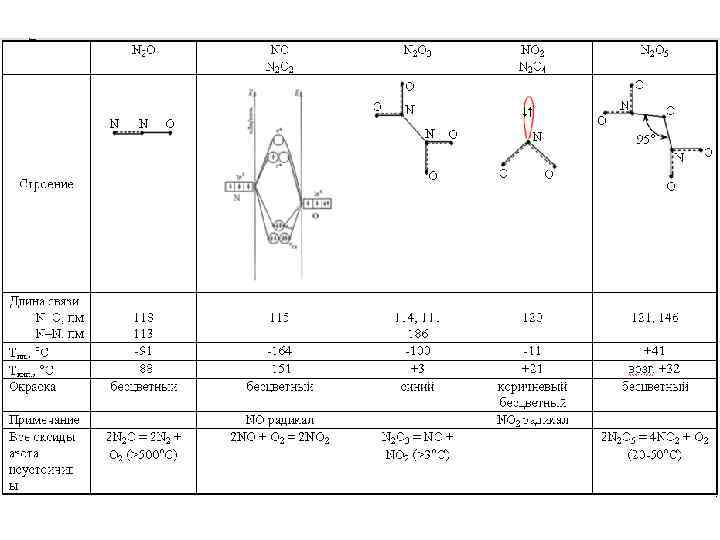
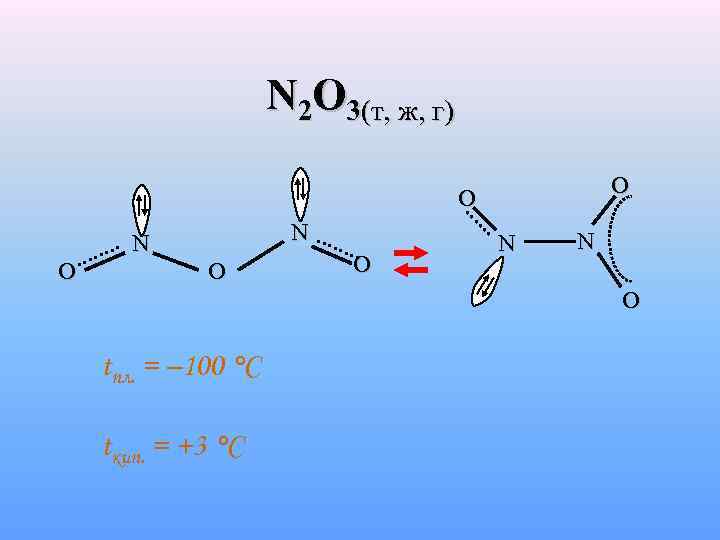 N 2 O 3(т, ж, г) O O О N N О О N N O tпл. = – 100 °C tкип. = +3 °C
N 2 O 3(т, ж, г) O O О N N О О N N O tпл. = – 100 °C tкип. = +3 °C
 N 2 O 3(т, ж, г) (NO+)(NO 2–) N 2 O 3(г) ↔ NO(г) + NO 2(г) - нитрит нитрозила 25 °C α = 90% 120 °C α ≈ 100% 3 N 2 O 3 + H 2 O(изб) = 2 HNO 3 + 4 NO (+следы HNO 2)
N 2 O 3(т, ж, г) (NO+)(NO 2–) N 2 O 3(г) ↔ NO(г) + NO 2(г) - нитрит нитрозила 25 °C α = 90% 120 °C α ≈ 100% 3 N 2 O 3 + H 2 O(изб) = 2 HNO 3 + 4 NO (+следы HNO 2)
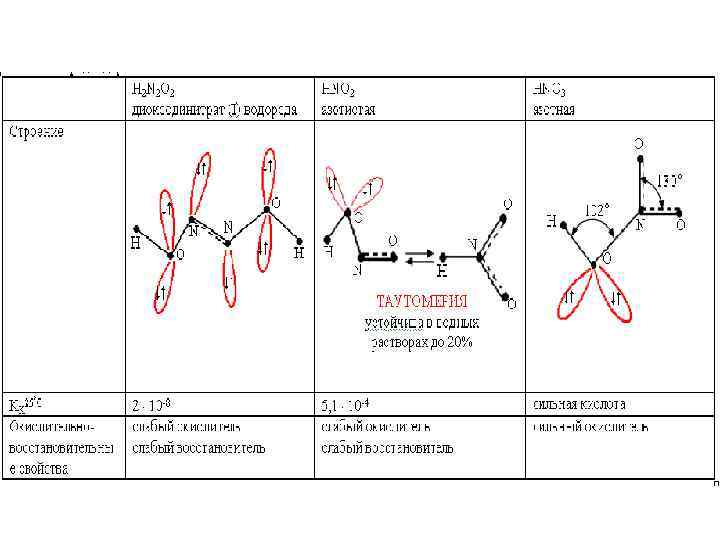
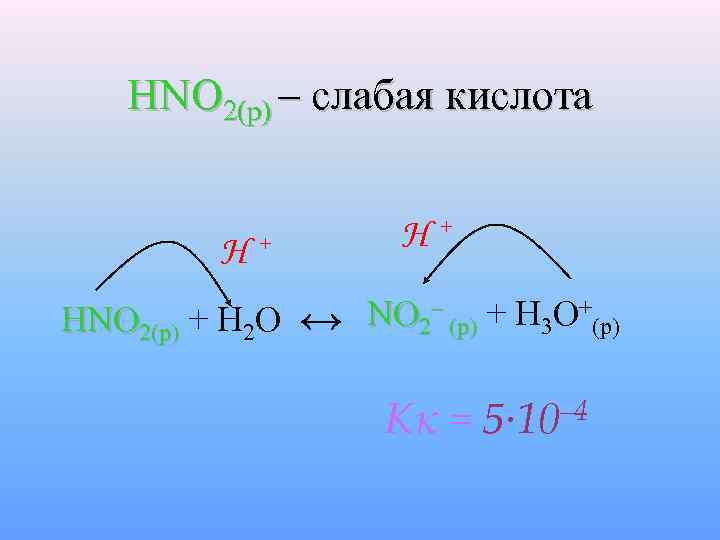 HNO 2(p) – слабая кислота H+ H+ HNO 2(p) + H 2 O ↔ NO 2– (p) + H 3 O+(p) Kк = – 4 5∙ 10
HNO 2(p) – слабая кислота H+ H+ HNO 2(p) + H 2 O ↔ NO 2– (p) + H 3 O+(p) Kк = – 4 5∙ 10
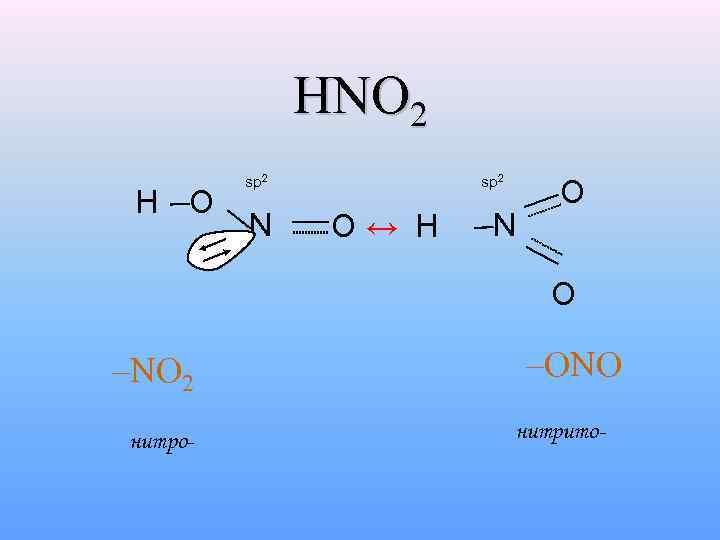 HNO 2 H O sp 2 N sp 2 O ↔ H N O –NO 2 нитро- –ONO нитрито-
HNO 2 H O sp 2 N sp 2 O ↔ H N O –NO 2 нитро- –ONO нитрито-
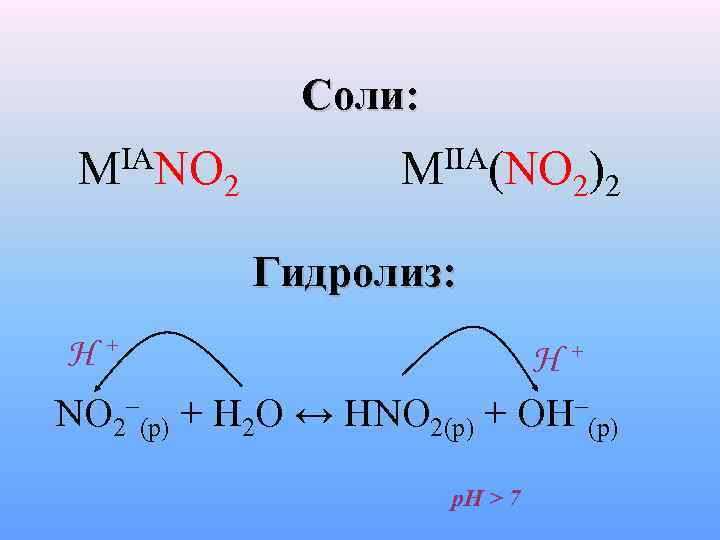 Соли: MIANO 2 MIIA(NO 2)2 Гидролиз: H+ H+ NO 2–(p) + H 2 O ↔ HNO 2(p) + OH–(p) p. H > 7
Соли: MIANO 2 MIIA(NO 2)2 Гидролиз: H+ H+ NO 2–(p) + H 2 O ↔ HNO 2(p) + OH–(p) p. H > 7
 Окислительно-восстановительные свойства NO 2– и HNO 2 PH<7 OK: - сильные окислители и восстановители NO 2– + 2 H+ + 1ē = NO + H 2 O φ° = +1, 2 B BC: NO 2– + H 2 O – 2ē = NO 3– + 2 H+ φ° = +0, 84 B PH>7 - слабые окислители и восстановители
Окислительно-восстановительные свойства NO 2– и HNO 2 PH<7 OK: - сильные окислители и восстановители NO 2– + 2 H+ + 1ē = NO + H 2 O φ° = +1, 2 B BC: NO 2– + H 2 O – 2ē = NO 3– + 2 H+ φ° = +0, 84 B PH>7 - слабые окислители и восстановители
![∙NO 2 sp sp 2 O [O N N O]+ нитроил O +)Cl. O ∙NO 2 sp sp 2 O [O N N O]+ нитроил O +)Cl. O](https://present5.com/presentation/18320036_57097823/image-34.jpg) ∙NO 2 sp sp 2 O [O N N O]+ нитроил O +)Cl. O (NO 2 4
∙NO 2 sp sp 2 O [O N N O]+ нитроил O +)Cl. O (NO 2 4
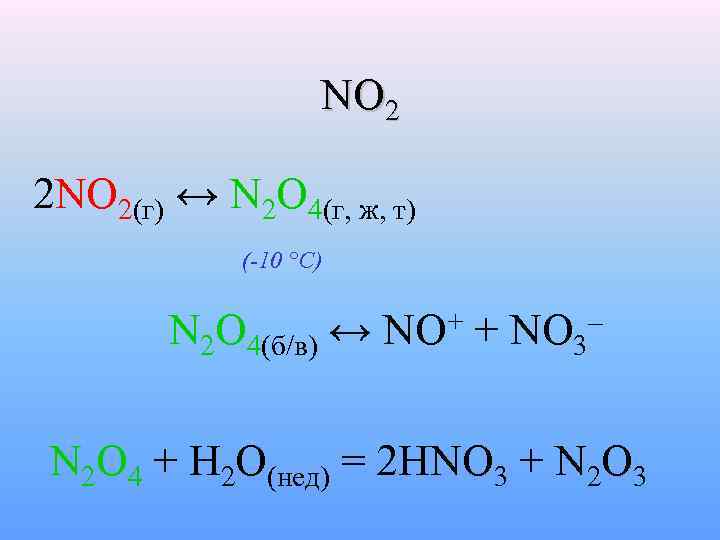 NO 2 2 NO 2(г) ↔ N 2 O 4(г, ж, т) (-10 °C) N 2 O 4(б/в) ↔ + NO + – NO 3 N 2 O 4 + H 2 O(нед) = 2 HNO 3 + N 2 O 3
NO 2 2 NO 2(г) ↔ N 2 O 4(г, ж, т) (-10 °C) N 2 O 4(б/в) ↔ + NO + – NO 3 N 2 O 4 + H 2 O(нед) = 2 HNO 3 + N 2 O 3
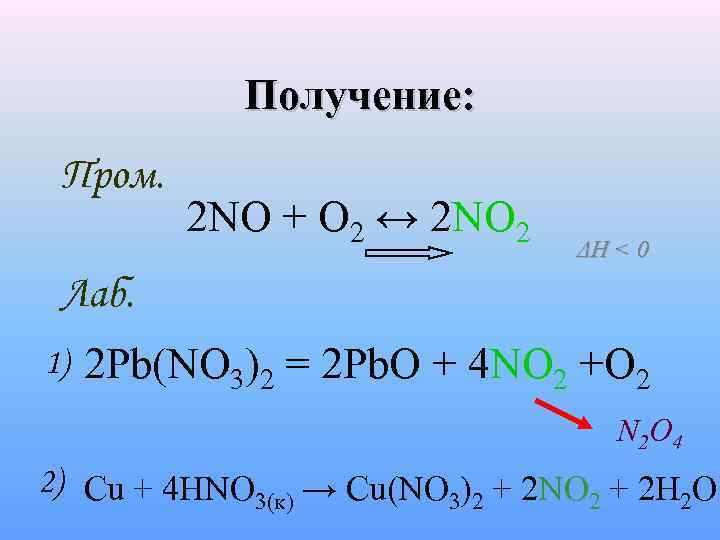 Получение: Пром. 2 NO + O 2 ↔ 2 NO 2 ΔH < 0 Лаб. 1) 2 Pb(NO 3)2 = 2 Pb. O + 4 NO 2 +O 2 N 2 O 4 2) Cu + 4 HNO 3(к) → Cu(NO 3)2 + 2 NO 2 + 2 H 2 O
Получение: Пром. 2 NO + O 2 ↔ 2 NO 2 ΔH < 0 Лаб. 1) 2 Pb(NO 3)2 = 2 Pb. O + 4 NO 2 +O 2 N 2 O 4 2) Cu + 4 HNO 3(к) → Cu(NO 3)2 + 2 NO 2 + 2 H 2 O
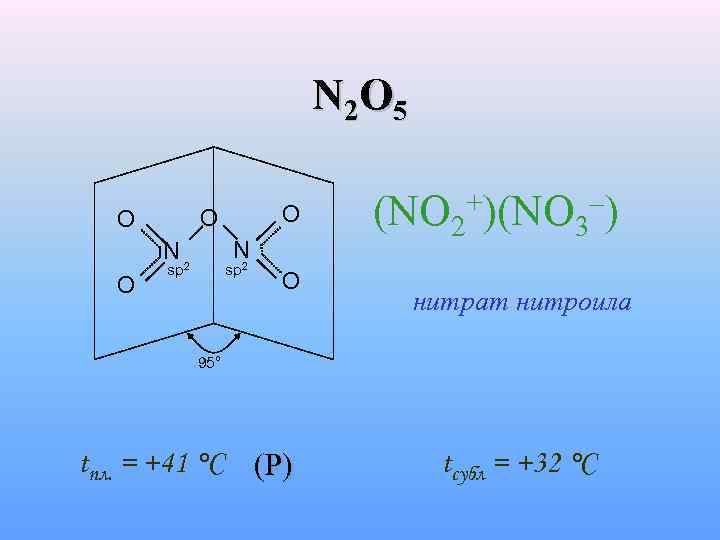 N 2 O 5 O O O O N N 2 sp 2 O (NO 2+)(NO 3–) нитрат нитроила 95° tпл. = +41 °C (P) tсубл = +32 °C
N 2 O 5 O O O O N N 2 sp 2 O (NO 2+)(NO 3–) нитрат нитроила 95° tпл. = +41 °C (P) tсубл = +32 °C
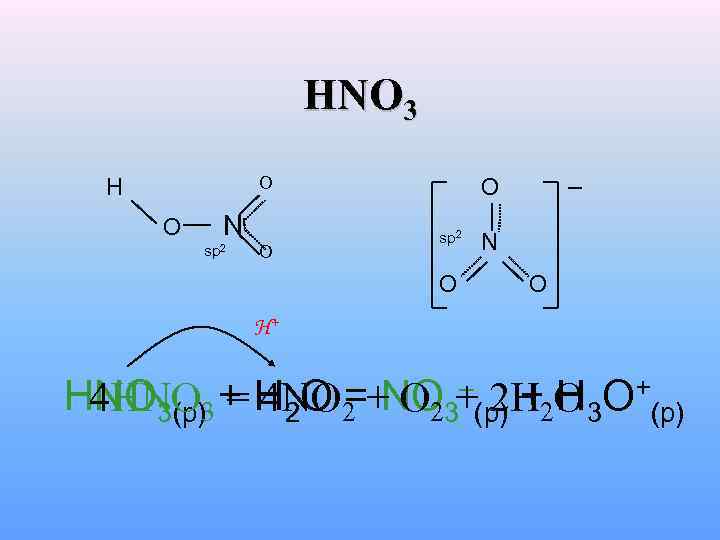 HNO 3 O H O N sp 2 O O sp 2 O N O H+ HNO 3(p)3 = 4 NO 2 + O 23+(p) + H 3 O+(p) 4 HNO + H 2 O = NO – 2 H 2 O
HNO 3 O H O N sp 2 O O sp 2 O N O H+ HNO 3(p)3 = 4 NO 2 + O 23+(p) + H 3 O+(p) 4 HNO + H 2 O = NO – 2 H 2 O
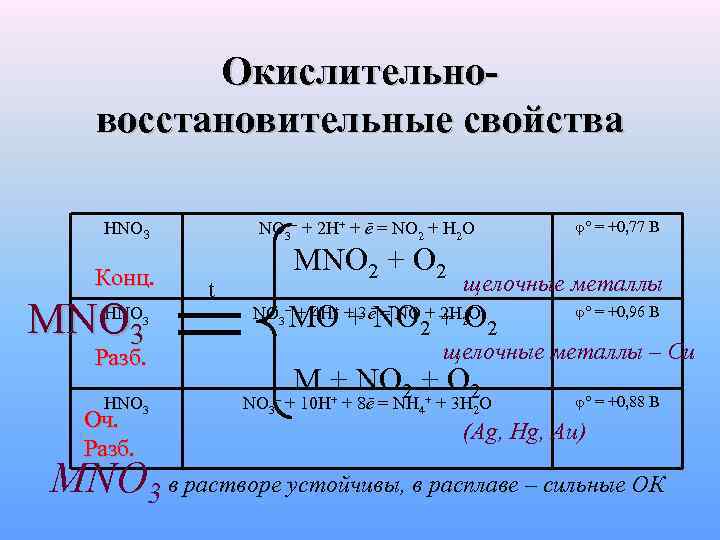 Окислительновосстановительные свойства HNO 3 Конц. MNO 3 HNO 3– + 2 H+ + ē = NO 2 + H 2 O MNO 2 + O 2 t Оч. Разб. щелочные металлы MO + NO 2 + O 2 NO 3– + 4 H+ + 3ē = NO + 2 H 2 O φ° = +0, 96 B щелочные металлы – Cu Разб. HNO 3 φ° = +0, 77 B M + NO 2 + O 2 NO 3 + 10 H+ + 8ē = NH 4+ + 3 H 2 O – φ° = +0, 88 B (Ag, Hg, Au) MNO 3 в растворе устойчивы, в расплаве – сильные ОК
Окислительновосстановительные свойства HNO 3 Конц. MNO 3 HNO 3– + 2 H+ + ē = NO 2 + H 2 O MNO 2 + O 2 t Оч. Разб. щелочные металлы MO + NO 2 + O 2 NO 3– + 4 H+ + 3ē = NO + 2 H 2 O φ° = +0, 96 B щелочные металлы – Cu Разб. HNO 3 φ° = +0, 77 B M + NO 2 + O 2 NO 3 + 10 H+ + 8ē = NH 4+ + 3 H 2 O – φ° = +0, 88 B (Ag, Hg, Au) MNO 3 в растворе устойчивы, в расплаве – сильные ОК
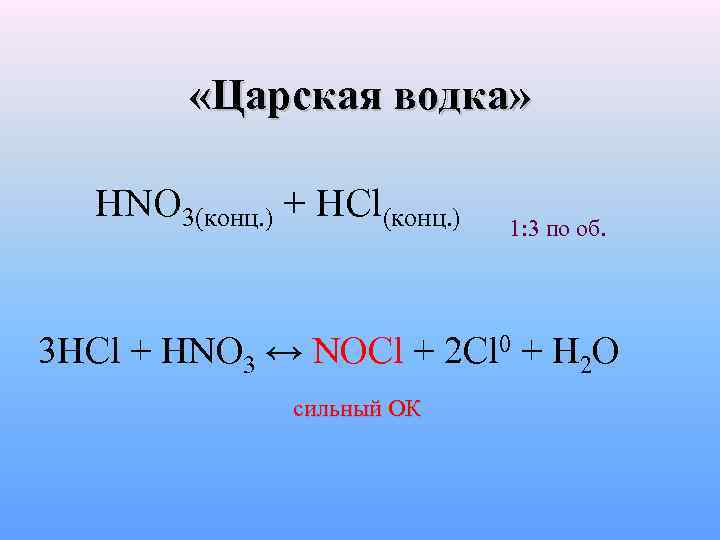 «Царская водка» HNO 3(конц. ) + HCl(конц. ) 1: 3 по об. 3 HCl + HNO 3 ↔ NOCl + 2 Cl 0 + H 2 O сильный ОК
«Царская водка» HNO 3(конц. ) + HCl(конц. ) 1: 3 по об. 3 HCl + HNO 3 ↔ NOCl + 2 Cl 0 + H 2 O сильный ОК
 «Царская водка» Примеры: 3 Pt + 4 HNO 3 + 18 HCl = 3 H 2[Pt. Cl 6] + 4 NO + 8 H 2 O Au + HNO 3 + HCl → H[Au. Cl 4] + NO + H 2 O
«Царская водка» Примеры: 3 Pt + 4 HNO 3 + 18 HCl = 3 H 2[Pt. Cl 6] + 4 NO + 8 H 2 O Au + HNO 3 + HCl → H[Au. Cl 4] + NO + H 2 O
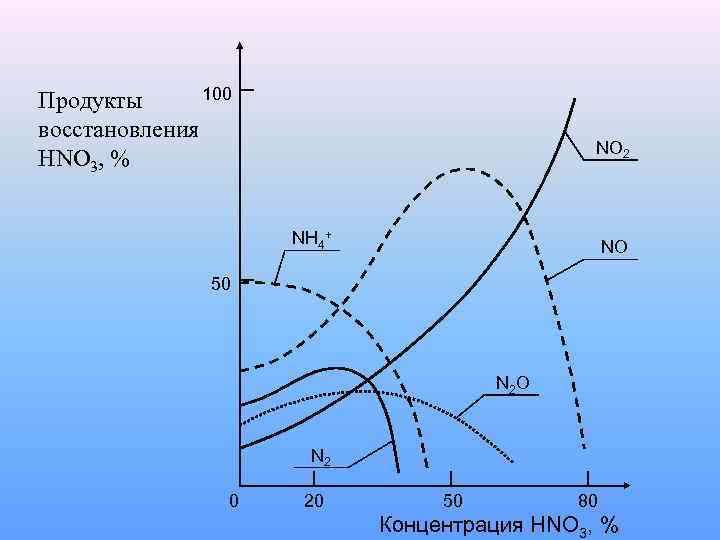 100 Продукты восстановления HNO 3, % NO 2 NH 4+ NO 50 N 2 O N 2 0 20 50 80 Концентрация HNO 3, %
100 Продукты восстановления HNO 3, % NO 2 NH 4+ NO 50 N 2 O N 2 0 20 50 80 Концентрация HNO 3, %

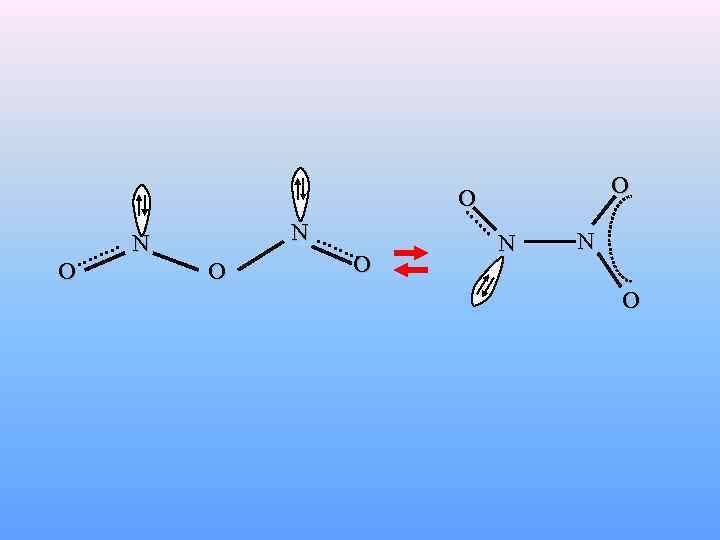 O O О N N О О N N O
O O О N N О О N N O


