9.окисление-восстан.ppt
- Количество слайдов: 30

ЛЕКЦИЯ № 9 РЕАКЦИИ ОКИСЛЕНИЯ И ВОССТАНОВЛЕНИЯ БИООРГАНИЧЕСКИХ СОЕДИНЕНИЙ ВАЖНЕЙШИЕ РЕДОКССИСТЕМЫ ОРГАНИЗМА

Кислород в атмосфере Земли появился около 600 млн. лет назад, что потребовало перестройки механизмов функционирования живых существ. Наряду с анаэробными организмами появились аэробные, метаболизм которых протекает с участием кислорода. Потребление О 2 человеком в покое составляет 250 мл/мин (360 литров в сутки), при физической работе может возрастать в десятки раз Н-субстрат-Н + ½ О 2 Н 2 О + дегидрированный (окисленный) субстрат Окисление органических субстратов – процесс аналогичный горению 2 Н О - 2 е 2 Н+ + 2 е О 2 - Н 2 О ∆G 0 = - 100 к. Дж/моль протонов - экзергонический процесс
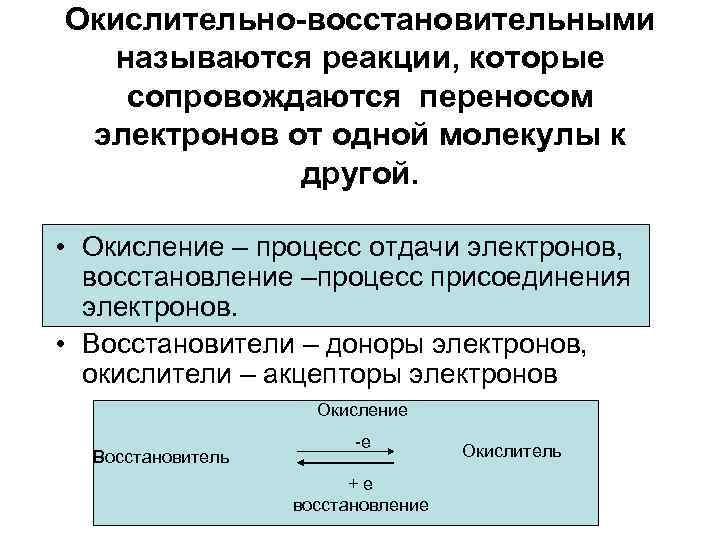
Окислительно-восстановительными называются реакции, которые сопровождаются переносом электронов от одной молекулы к другой. • Окисление – процесс отдачи электронов, восстановление –процесс присоединения электронов. • Восстановители – доноры электронов, окислители – акцепторы электронов Окисление Восстановитель -е +е восстановление Окислитель

Значение реакций окислениявосстановления в организме • 1. Окисление питательных веществ • (процессы катаболизма), при которых выделяется энергия, запасаемая в виде АТФ и используемая в процессах анаболизма (биосинтеза). • 2. Основа клеточного дыхания (окислительное фосфорилирование) • 3. Процессы свободнорадикального окисления липидов биологических мембран, белков, нуклеиновых кислот • 4. Процессы детоксикации ксенобиотиков
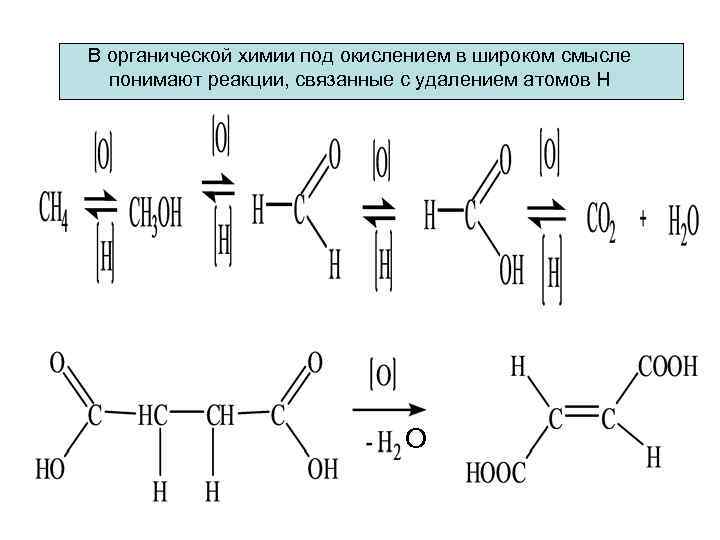
В органической химии под окислением в широком смысле понимают реакции, связанные с удалением атомов Н О
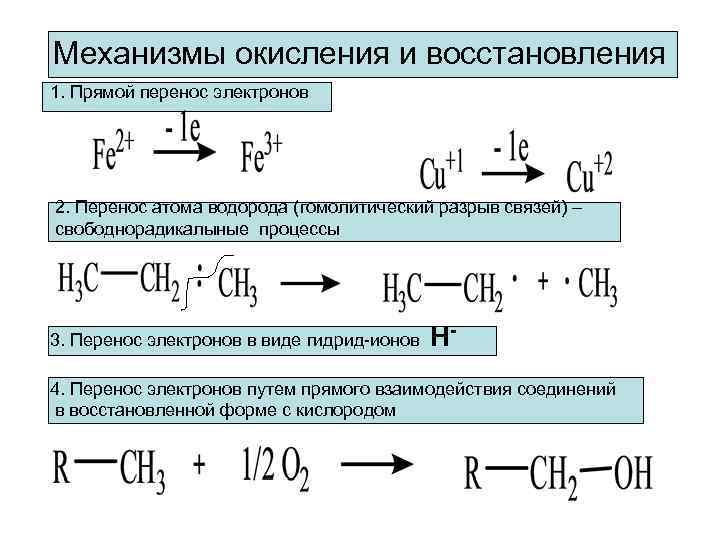
Механизмы окисления и восстановления 1. Прямой перенос электронов 2. Перенос атома водорода (гомолитический разрыв связей) – свободнорадикалыные процессы 3. Перенос электронов в виде гидрид-ионов Н- 4. Перенос электронов путем прямого взаимодействия соединений в восстановленной форме с кислородом
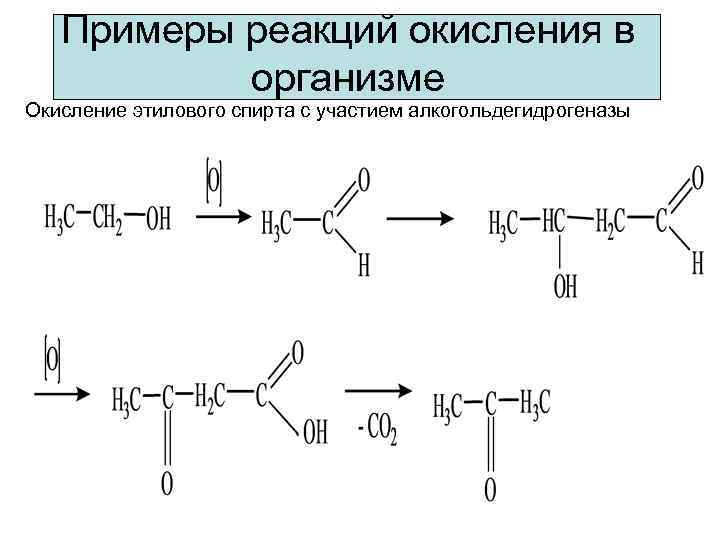
Примеры реакций окисления в организме Окисление этилового спирта с участием алкогольдегидрогеназы
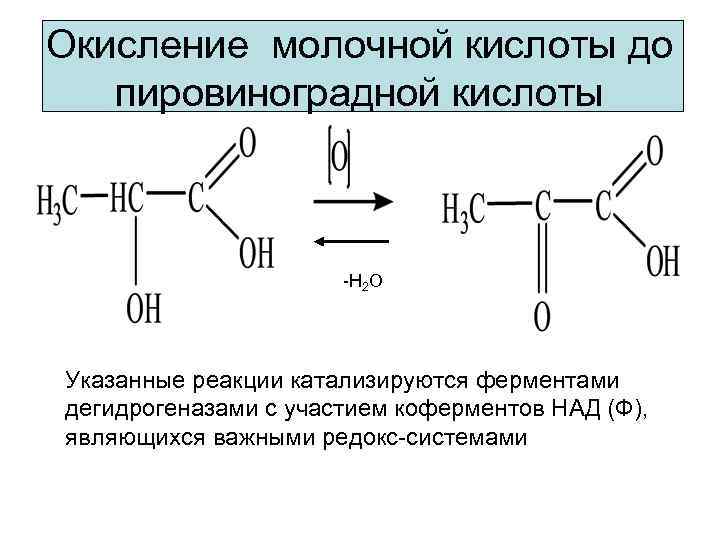
Окисление молочной кислоты до пировиноградной кислоты -H 2 O Указанные реакции катализируются ферментами дегидрогеназами с участием коферментов НАД (Ф), являющихся важными редокс-системами
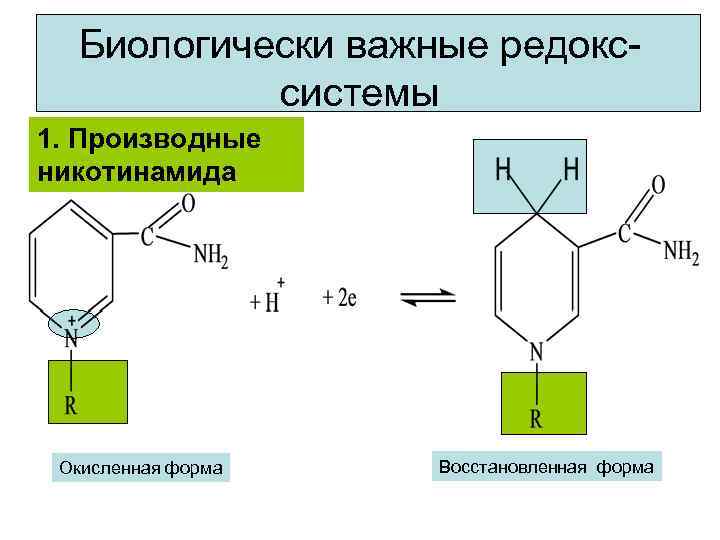
Биологически важные редокссистемы 1. Производные никотинамида Окисленная форма Восстановленная форма
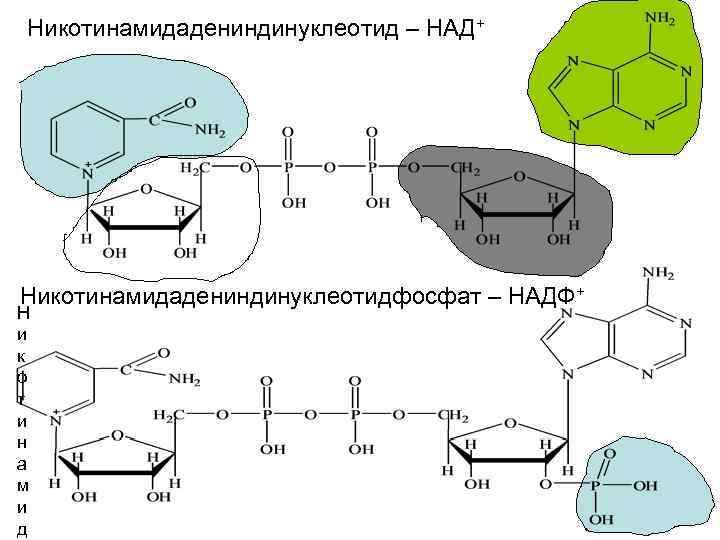
Никотинамидадениндинуклеотид – НАД+ Никотинамидадениндинуклеотидфосфат – НАДФ+ Н и к о т и н а м и д
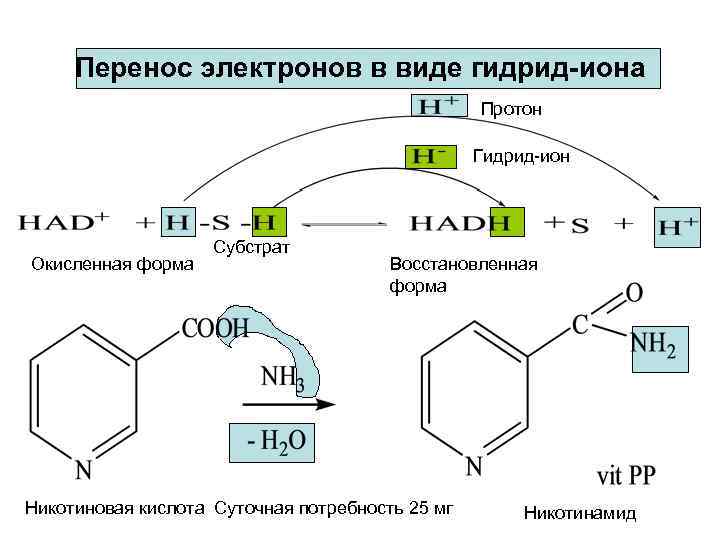
Перенос электронов в виде гидрид-иона Протон Гидрид-ион Окисленная форма Субстрат Восстановленная форма Никотиновая кислота Суточная потребность 25 мг Никотинамид
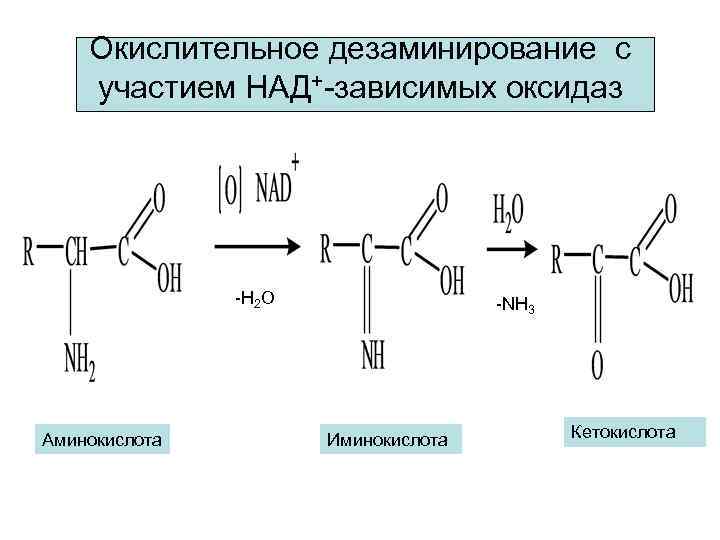
Окислительное дезаминирование с участием НАД+-зависимых оксидаз -Н 2 О Аминокислота -NH 3 Иминокислота Кетокислота
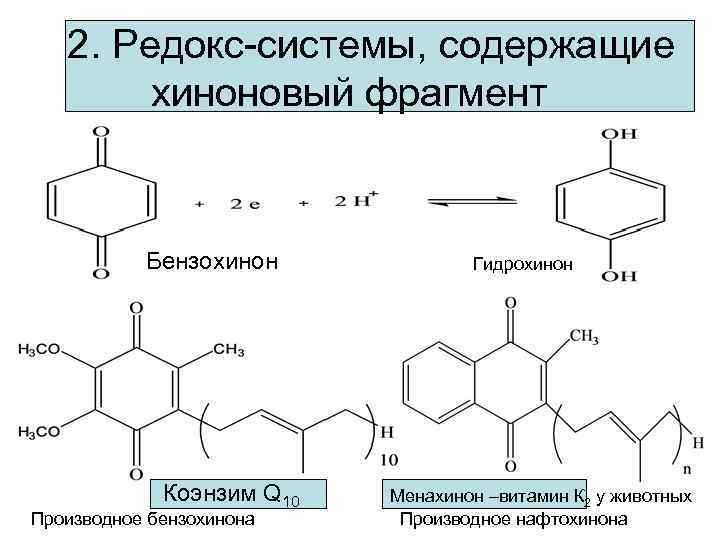
2. Редокс-системы, содержащие хиноновый фрагмент Бензохинон Коэнзим Q 10 Производное бензохинона Гидрохинон Менахинон –витамин К 2 у животных Производное нафтохинона
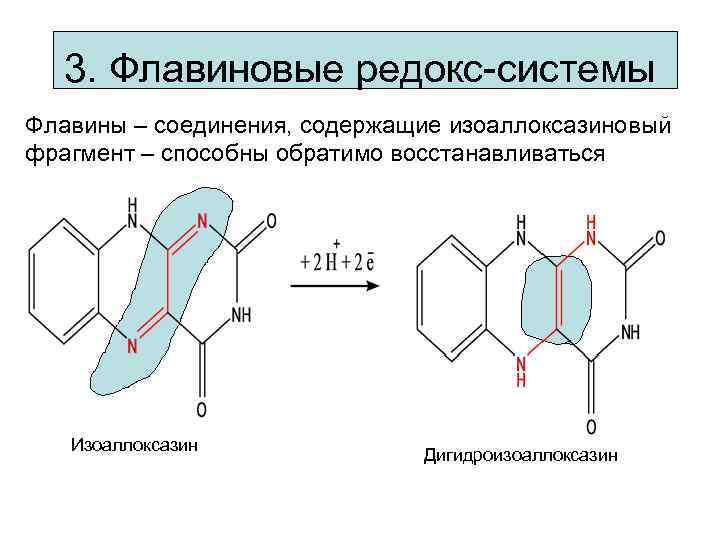
3. Флавиновые редокс-системы Флавины – соединения, содержащие изоаллоксазиновый фрагмент – способны обратимо восстанавливаться Изоаллоксазин Дигидроизоаллоксазин

Рибофлавин –витамин В 2 Остаток рибозы -радикал рибитил Рибофлавин выделен из молока в 1935 году, суточная потребность – 1 -3 мг/сутки
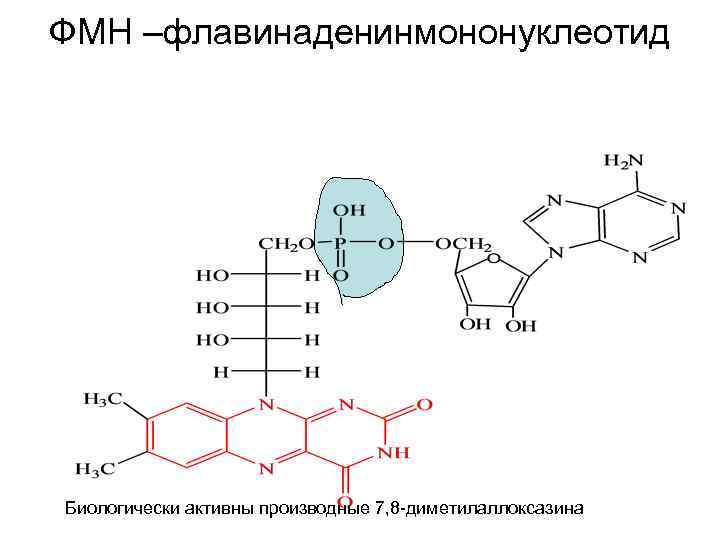
ФМН –флавинаденинмононуклеотид Биологически активны производные 7, 8 -диметилаллоксазина
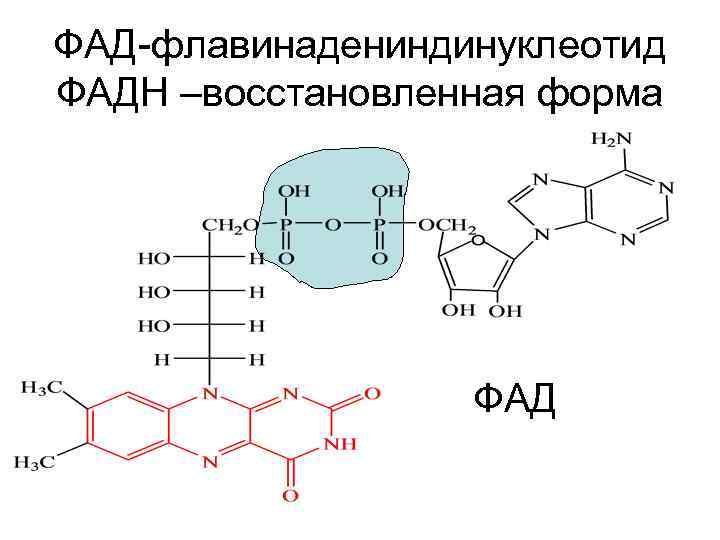
ФАД-флавинадениндинуклеотид ФАДН –восстановленная форма ФАД
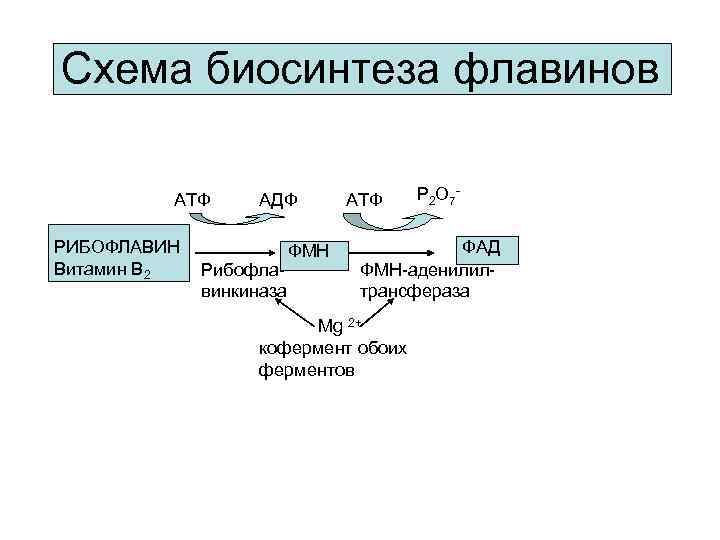
Схема биосинтеза флавинов АТФ РИБОФЛАВИН Витамин В 2 АДФ Рибофлавинкиназа ФМН АТФ Р 2 О 7 - ФАД ФМН-аденилилтрансфераза Mg 2+ кофермент обоих ферментов
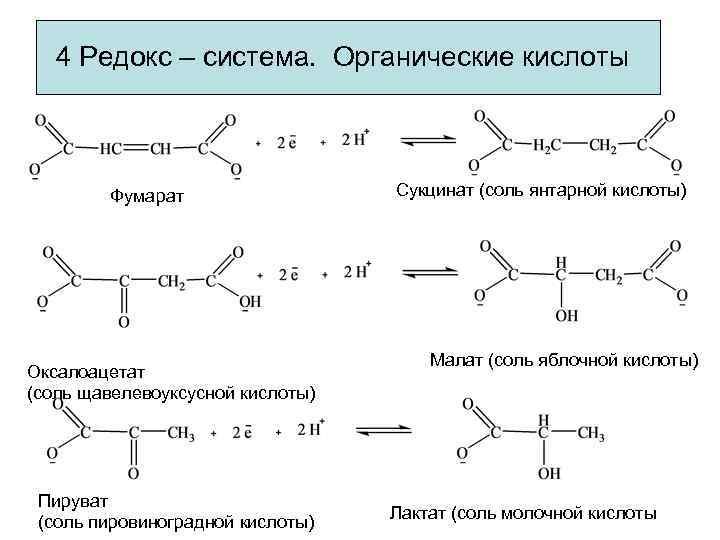
4 Редокс – система. Органические кислоты Фумарат Оксалоацетат (соль щавелевоуксусной кислоты) Пируват (соль пировиноградной кислоты) Сукцинат (соль янтарной кислоты) Малат (соль яблочной кислоты) Лактат (соль молочной кислоты
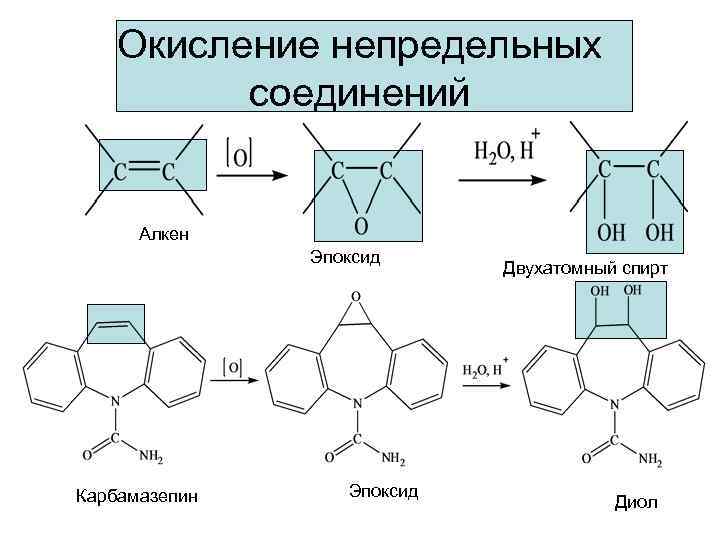
Окисление непредельных соединений Алкен Эпоксид Карбамазепин Эпоксид Двухатомный спирт Диол
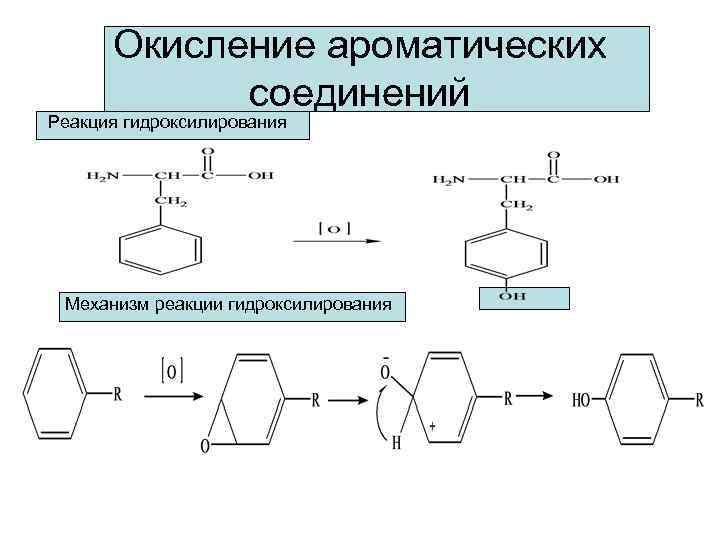
Окисление ароматических соединений Реакция гидроксилирования Механизм реакции гидроксилирования
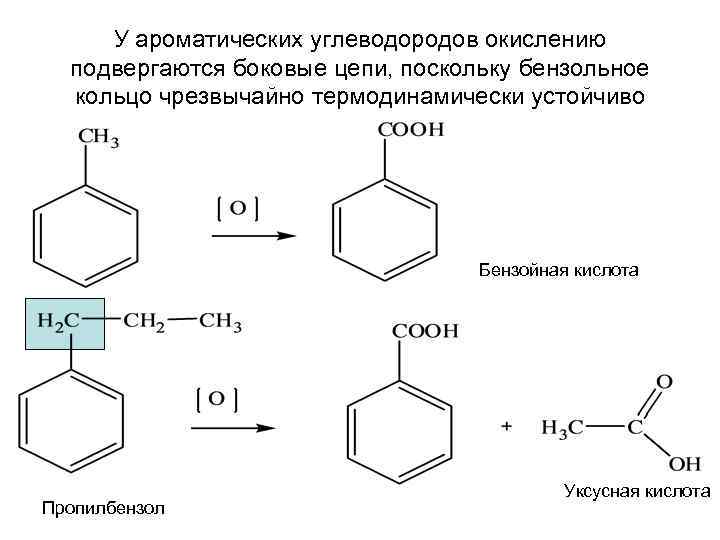
У ароматических углеводородов окислению подвергаются боковые цепи, поскольку бензольное кольцо чрезвычайно термодинамически устойчиво Бензойная кислота Пропилбензол Уксусная кислота
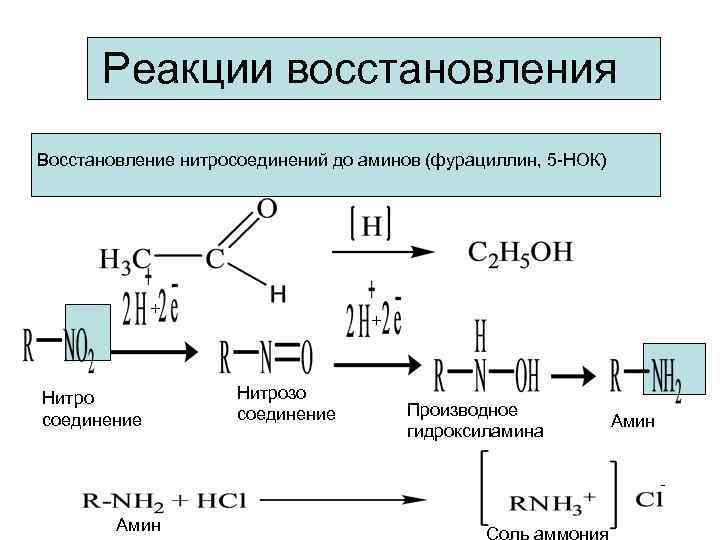
Реакции восстановления Восстановление нитросоединений до аминов (фурациллин, 5 -НОК) + Нитро соединение + Нитрозо соединение Производное гидроксиламина Амин - Амин Соль аммония
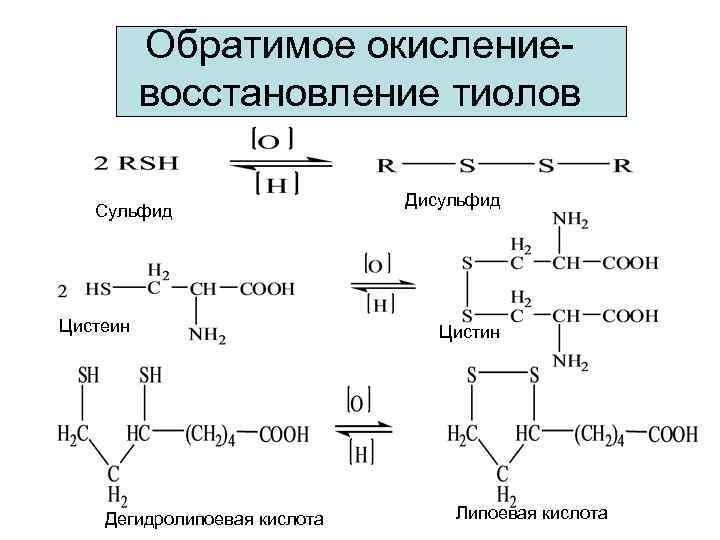
Обратимое окислениевосстановление тиолов Сульфид Цистеин Дегидролипоевая кислота Дисульфид Цистин Липоевая кислота
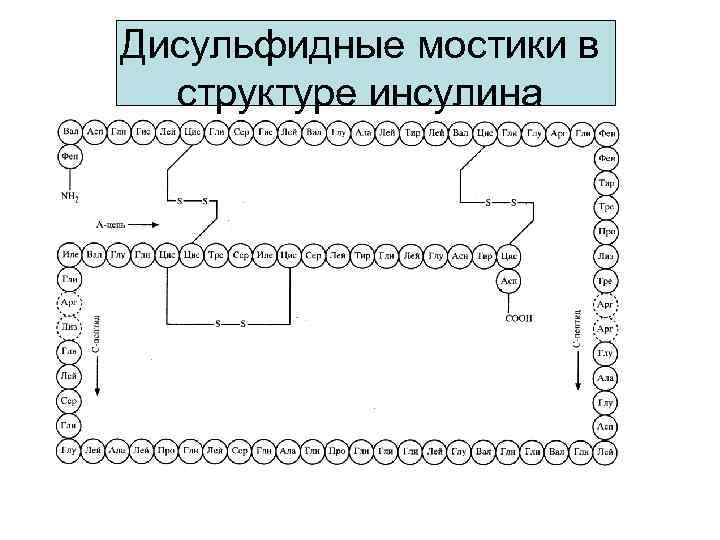
Дисульфидные мостики в структуре инсулина
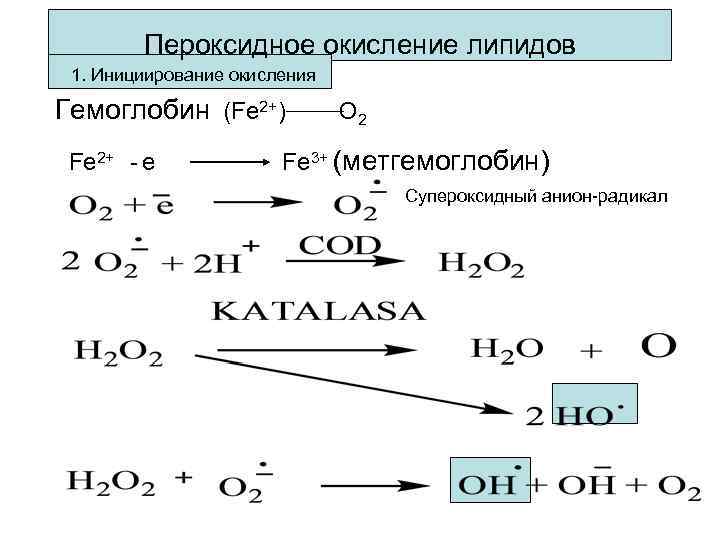
Пероксидное окисление липидов 1. Инициирование окисления Гемоглобин (Fe 2+) Fe 2+ - e О 2 Fe 3+ (метгемоглобин) Супероксидный анион-радикал
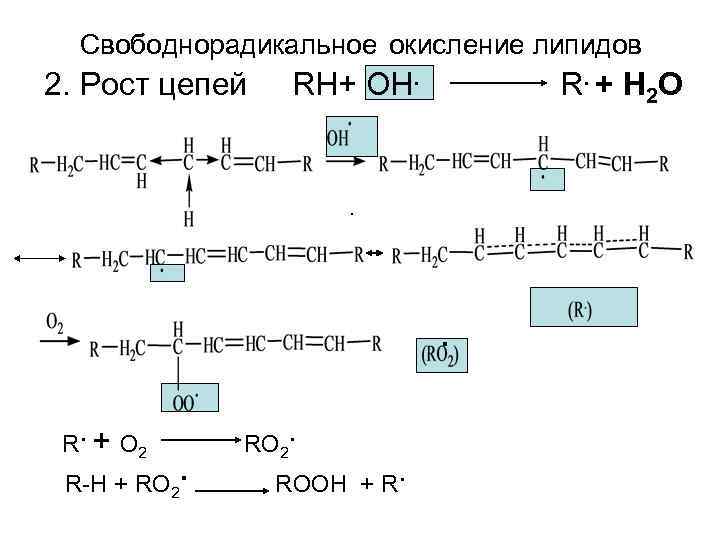
Свободнорадикальное окисление липидов 2. Рост цепей RH+ OH. R. + H 2 O · . R. + O 2 R-H + RO 2. ROOH + R.
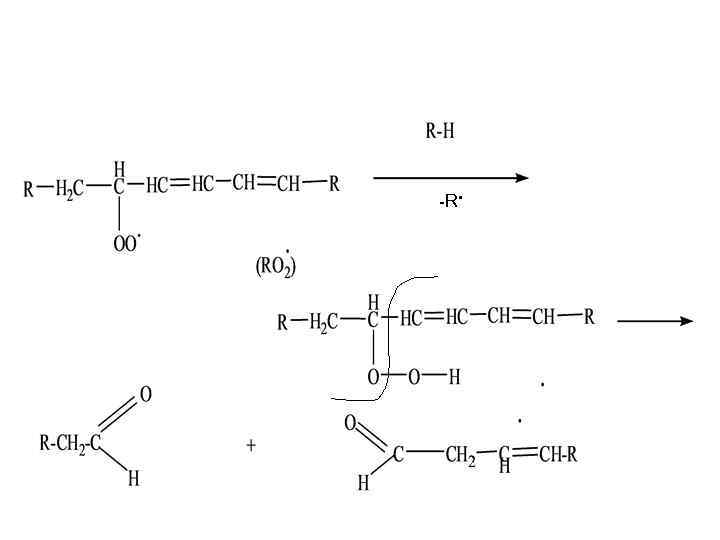
-R.
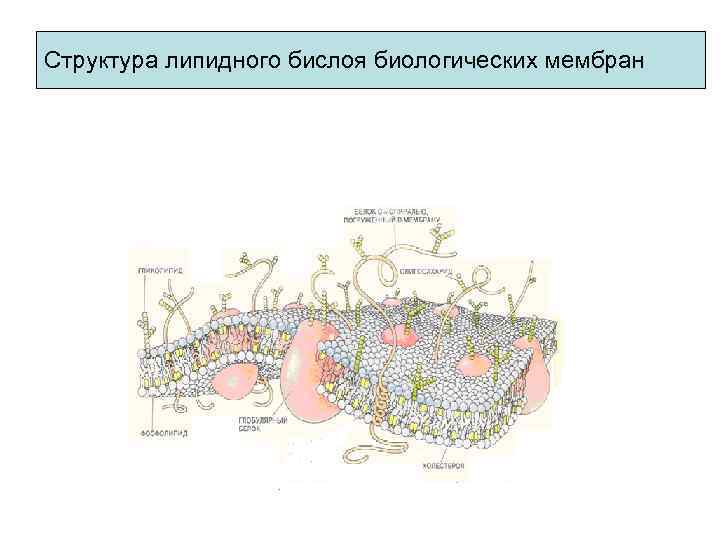
Структура липидного бислоя биологических мембран
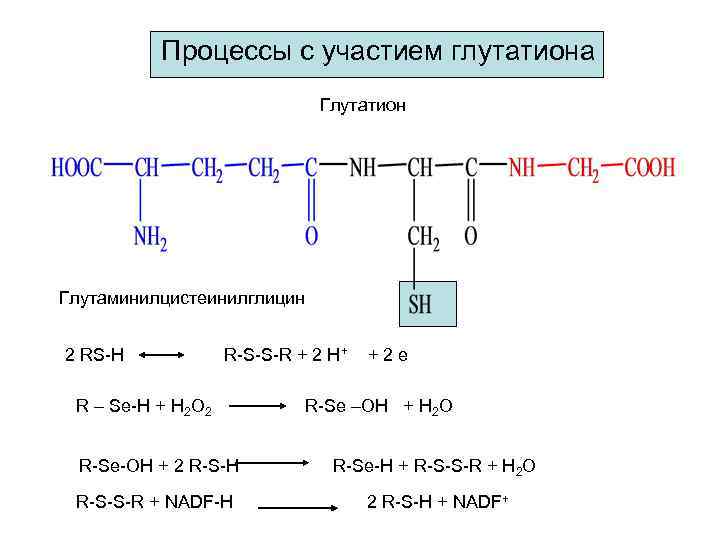
Процессы с участием глутатиона Глутатион Глутаминилцистеинилглицин 2 RS-H R-S-S-R + 2 H+ R – Se-H + H 2 O 2 +2 e R-Se –OH + H 2 O R-Se-OH + 2 R-S-H R-Se-H + R-S-S-R + H 2 O R-S-S-R + NADF-H 2 R-S-H + NADF +
9.окисление-восстан.ppt