Lektsia__9-2011.ppt
- Количество слайдов: 27
 Лекция № 9 Равновесия в растворах электролитов Константа диссоциации слабых электролитов. Произведение растворимости, его взаимосвязь с растворимостью. Условия образования и растворения осадка. Ионное произведение воды. p. H и p. OH растворов. Способы измерения p. H. Индикаторы. Ионные реакции в растворе. Правило Бертолле. Гидролиз солей. Константа и степень гидролиза. Условия смещения ионных равновесий.
Лекция № 9 Равновесия в растворах электролитов Константа диссоциации слабых электролитов. Произведение растворимости, его взаимосвязь с растворимостью. Условия образования и растворения осадка. Ионное произведение воды. p. H и p. OH растворов. Способы измерения p. H. Индикаторы. Ионные реакции в растворе. Правило Бертолле. Гидролиз солей. Константа и степень гидролиза. Условия смещения ионных равновесий.
 Константа диссоциации слабых электролитов КА ↔ К+ + А- Константу диссоциации кислоты обозначают Ка, константу диссоциации основания Кb. Константы диссоциации зависят от температуры, в меньшей мере от концентрации. Термодинамические константы диссоциации, в которые входят активности ионов, от концентрации не зависят
Константа диссоциации слабых электролитов КА ↔ К+ + А- Константу диссоциации кислоты обозначают Ка, константу диссоциации основания Кb. Константы диссоциации зависят от температуры, в меньшей мере от концентрации. Термодинамические константы диссоциации, в которые входят активности ионов, от концентрации не зависят
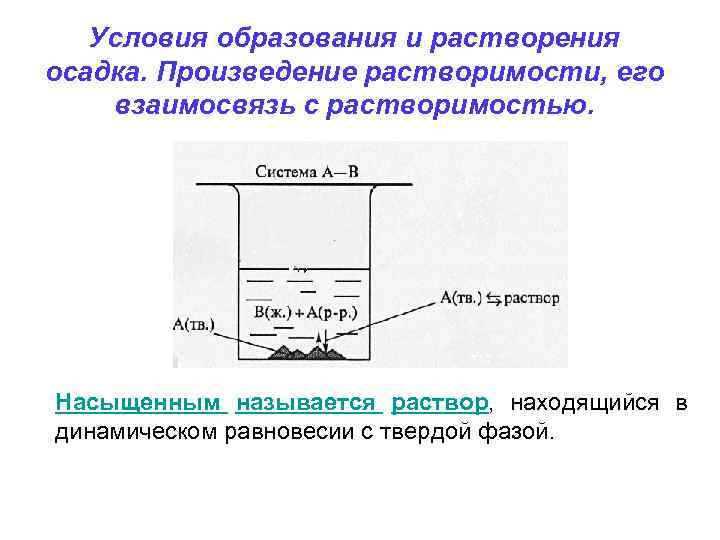 Условия образования и растворения осадка. Произведение растворимости, его взаимосвязь с растворимостью. Насыщенным называется раствор, находящийся в динамическом равновесии с твердой фазой.
Условия образования и растворения осадка. Произведение растворимости, его взаимосвязь с растворимостью. Насыщенным называется раствор, находящийся в динамическом равновесии с твердой фазой.
 • Ca. SO 4 (т) Ca 2+(р-р) + SO 42–(р-р) Ks=a. Ca 2+a. SO 42+ ≈ [Ca 2+][SO 42–] • [Ca. SO 4] = const Произведение растворимости или константа растворимости - произведение концентраций ионов в степенях их стехиометрических коэффициентов в насыщенном растворе твердого электролита есть величина постоянная при данной температуре ПР(Ca. SO 4) = [Ca 2+][SO 42–]
• Ca. SO 4 (т) Ca 2+(р-р) + SO 42–(р-р) Ks=a. Ca 2+a. SO 42+ ≈ [Ca 2+][SO 42–] • [Ca. SO 4] = const Произведение растворимости или константа растворимости - произведение концентраций ионов в степенях их стехиометрических коэффициентов в насыщенном растворе твердого электролита есть величина постоянная при данной температуре ПР(Ca. SO 4) = [Ca 2+][SO 42–]
![АВ А+ + В– Обозначив растворимость через s (моль/л), получим: [A+]=[B–]=s, ПР=[A+][B –]=s 2 АВ А+ + В– Обозначив растворимость через s (моль/л), получим: [A+]=[B–]=s, ПР=[A+][B –]=s 2](https://present5.com/presentation/141344298_132726598/image-5.jpg) АВ А+ + В– Обозначив растворимость через s (моль/л), получим: [A+]=[B–]=s, ПР=[A+][B –]=s 2 Pb. I 2 Pb 2+ + 2 I– Если соль имеет общую формулу AB 2, то она диссоциирует по уравнению: AB 2 A 2+ + 2 B– В этом случае : [A 2+]=s, [B–]=2 s, ПР=[A 2+][B–]2=s×(2 s)2=4 s 3
АВ А+ + В– Обозначив растворимость через s (моль/л), получим: [A+]=[B–]=s, ПР=[A+][B –]=s 2 Pb. I 2 Pb 2+ + 2 I– Если соль имеет общую формулу AB 2, то она диссоциирует по уравнению: AB 2 A 2+ + 2 B– В этом случае : [A 2+]=s, [B–]=2 s, ПР=[A 2+][B–]2=s×(2 s)2=4 s 3
 G = -RTln. Ks С учетом коэффициентов активности ионов: Если ионная сила раствора I 0, то ПР Ks ПК = [K+]m[А-]n - произведение неравновесных концентраций ПК>ПР, то раствор является пересыщенным, и из него выпадает осадок G>0 Условие растворения осадка (ненасыщенности раствора): ПК<ПР G<0 . Если оба процесса идут с одинаковой скоростью, и система приходит в состояние равновесия при ПК=ПР (насыщенный раствор) и G = 0.
G = -RTln. Ks С учетом коэффициентов активности ионов: Если ионная сила раствора I 0, то ПР Ks ПК = [K+]m[А-]n - произведение неравновесных концентраций ПК>ПР, то раствор является пересыщенным, и из него выпадает осадок G>0 Условие растворения осадка (ненасыщенности раствора): ПК<ПР G<0 . Если оба процесса идут с одинаковой скоростью, и система приходит в состояние равновесия при ПК=ПР (насыщенный раствор) и G = 0.
 • при добавлении небольшого количества любого сильного электролита увеличивается ионная сила раствора, уменьшаются коэффициенты активности ионов, увеличивается ПР, т. е. увеличивается растворимость малорастворимого электролита. Такое влияние другого электролита называется солевым эффектом
• при добавлении небольшого количества любого сильного электролита увеличивается ионная сила раствора, уменьшаются коэффициенты активности ионов, увеличивается ПР, т. е. увеличивается растворимость малорастворимого электролита. Такое влияние другого электролита называется солевым эффектом
 Ионное произведение воды, p. H и p. OH растворов. Способы измерения p. H. Индикаторы Такой процесс называется автопротолизом H 2 O H+ + OH– Концентрации ионов H+ и OH– при 25°С равны 10– 7 моль/л. Выражение для константы диссоциации воды имеет вид: [H+][OH–] = K [H 2 O] = Kw [H 2 O]=55, 5 моль/л. При 25°С Kw=10– 14 - ионное произведение воды
Ионное произведение воды, p. H и p. OH растворов. Способы измерения p. H. Индикаторы Такой процесс называется автопротолизом H 2 O H+ + OH– Концентрации ионов H+ и OH– при 25°С равны 10– 7 моль/л. Выражение для константы диссоциации воды имеет вид: [H+][OH–] = K [H 2 O] = Kw [H 2 O]=55, 5 моль/л. При 25°С Kw=10– 14 - ионное произведение воды
![• Нейтральный раствор [H+]=10– 7 моль/л; • кислый раствор [H+]>10– 7 моль/л; • • Нейтральный раствор [H+]=10– 7 моль/л; • кислый раствор [H+]>10– 7 моль/л; •](https://present5.com/presentation/141344298_132726598/image-9.jpg) • Нейтральный раствор [H+]=10– 7 моль/л; • кислый раствор [H+]>10– 7 моль/л; • щелочной раствор [H+]<10– 7 моль/л. p. H= –lg [H+] - эта величина называется водородным показателем В нейтральном растворе p. H=7, в кислом растворе p. H<7, в щелочном растворе p. H>7. Гидроксидный показатель p. OH = –lg[OH–] При 25°С выполняется равенство: p. H+p. OH=14.
• Нейтральный раствор [H+]=10– 7 моль/л; • кислый раствор [H+]>10– 7 моль/л; • щелочной раствор [H+]<10– 7 моль/л. p. H= –lg [H+] - эта величина называется водородным показателем В нейтральном растворе p. H=7, в кислом растворе p. H<7, в щелочном растворе p. H>7. Гидроксидный показатель p. OH = –lg[OH–] При 25°С выполняется равенство: p. H+p. OH=14.
 • Лакмус: нейтральная форма (фиолет. ) кислая (красный) щелочная (синий) • Фенолфталеин: нейтральная форма, кислая (бесцветный) щелочная (малиновый) • Метиловый оранжевый: нейтральная форма (оранжевый) кислая (красный) щелочная (желтый)
• Лакмус: нейтральная форма (фиолет. ) кислая (красный) щелочная (синий) • Фенолфталеин: нейтральная форма, кислая (бесцветный) щелочная (малиновый) • Метиловый оранжевый: нейтральная форма (оранжевый) кислая (красный) щелочная (желтый)
 Ионные реакции в растворе. • Zn + 4 HNO 3 Zn(NO 3)2 + 2 NO 2 + 2 H 2 O полное молекулярное уравнение Zn + 4 H++ 4 NO 3 - Zn 2+ +2 NO 3 -+2 NO 2 + 2 H 2 O полная ионная форма • 4 H+ + 4 NO 3 - 2 NO 2 + 2 H 2 O сокращенная ионная форма
Ионные реакции в растворе. • Zn + 4 HNO 3 Zn(NO 3)2 + 2 NO 2 + 2 H 2 O полное молекулярное уравнение Zn + 4 H++ 4 NO 3 - Zn 2+ +2 NO 3 -+2 NO 2 + 2 H 2 O полная ионная форма • 4 H+ + 4 NO 3 - 2 NO 2 + 2 H 2 O сокращенная ионная форма
 Правило Бертолле. Условия смещение ионных равновесий 1) образуется осадок (↓), например: молекулярное уравнение Ba. Cl 2 + Na 2 SO 4 = Ba. SO 4 ↓ + 2 Na. Cl; ионно-молекулярное уравнение Ba 2++2 Cl- +2 Na+ + SO 42 −= Ba. SO 4 ↓ + 2 Cl- + 2 Na+ Ba 2+ + SO 42 −= Ba. SO 4 ↓; сокращенная ионная форма Ионное равновесие, как и любое другое, смещается при изменении концентрации одного из ионов.
Правило Бертолле. Условия смещение ионных равновесий 1) образуется осадок (↓), например: молекулярное уравнение Ba. Cl 2 + Na 2 SO 4 = Ba. SO 4 ↓ + 2 Na. Cl; ионно-молекулярное уравнение Ba 2++2 Cl- +2 Na+ + SO 42 −= Ba. SO 4 ↓ + 2 Cl- + 2 Na+ Ba 2+ + SO 42 −= Ba. SO 4 ↓; сокращенная ионная форма Ионное равновесие, как и любое другое, смещается при изменении концентрации одного из ионов.
 2) выделяются газообразные вещества: молекулярное уравнение Na 2 S+ 2 HCl = H 2 S↑ + 2 Na. Cl; ионно-молекулярное уравнение: S 2 - + 2 H+ + 2 Cl-+2 Na+= H 2 S↑ + 2 Cl- +2 Na+; S 2 - + 2 H+ = H 2 S↑; сокращенная форма
2) выделяются газообразные вещества: молекулярное уравнение Na 2 S+ 2 HCl = H 2 S↑ + 2 Na. Cl; ионно-молекулярное уравнение: S 2 - + 2 H+ + 2 Cl-+2 Na+= H 2 S↑ + 2 Cl- +2 Na+; S 2 - + 2 H+ = H 2 S↑; сокращенная форма
 3) образуется слабый электролит: молекулярное уравнение HCl + KOH = KCl + H 2 O; ионно-молекулярное уравнение H+ + Cl- + K+ + OH− = H 2 O + Cl- + K+; H+ + OH− = H 2 O сокращенная форма
3) образуется слабый электролит: молекулярное уравнение HCl + KOH = KCl + H 2 O; ионно-молекулярное уравнение H+ + Cl- + K+ + OH− = H 2 O + Cl- + K+; H+ + OH− = H 2 O сокращенная форма
 4) образуются комплексные соединения, например: молекулярное уравнение Hg(NO 3)2 + 4 KI = K 2[Hg. I 4] + 2 KNO 3 ; ионно-молекулярное уравнение Hg 2++ NO 3 -+ 4 K++ 4 I- = [Hg. J 4]2 -+NO 3 -+ 4 K+. Hg 2++ 4 I- = [Hg. I 4]2 -
4) образуются комплексные соединения, например: молекулярное уравнение Hg(NO 3)2 + 4 KI = K 2[Hg. I 4] + 2 KNO 3 ; ионно-молекулярное уравнение Hg 2++ NO 3 -+ 4 K++ 4 I- = [Hg. J 4]2 -+NO 3 -+ 4 K+. Hg 2++ 4 I- = [Hg. I 4]2 -
 CH 3 COOH H+ + CH 3 COO– введение в раствор слабого электро-лита одноименных ионов уменьшает степень диссоциации этого электролита. • Правило Бертолле: Реакции в растворах электролитов всегда идут в сторону образования наименее диссоциированных или наименее растворимых веществ, т. е. в сторону большего связывания ионов. CH 3 COONa + HCl = CH 3 COOH + Na. Cl CH 3 COO– + H+ = CH 3 COOH
CH 3 COOH H+ + CH 3 COO– введение в раствор слабого электро-лита одноименных ионов уменьшает степень диссоциации этого электролита. • Правило Бертолле: Реакции в растворах электролитов всегда идут в сторону образования наименее диссоциированных или наименее растворимых веществ, т. е. в сторону большего связывания ионов. CH 3 COONa + HCl = CH 3 COOH + Na. Cl CH 3 COO– + H+ = CH 3 COOH
 Гидролиз солей. Константа и степень гидролиза Химическая реакция обменного характера растворяемого вещества с растворителем называется сольволизом. Если растворителем является вода, то процесс – гидролиз. Суть гидролиза солей заключается в том, что происходит смещение равновесия диссоциации воды вследствие связывания одного из ее ионов с образованием мало диссоциированного или трудно растворимого продукта
Гидролиз солей. Константа и степень гидролиза Химическая реакция обменного характера растворяемого вещества с растворителем называется сольволизом. Если растворителем является вода, то процесс – гидролиз. Суть гидролиза солей заключается в том, что происходит смещение равновесия диссоциации воды вследствие связывания одного из ее ионов с образованием мало диссоциированного или трудно растворимого продукта
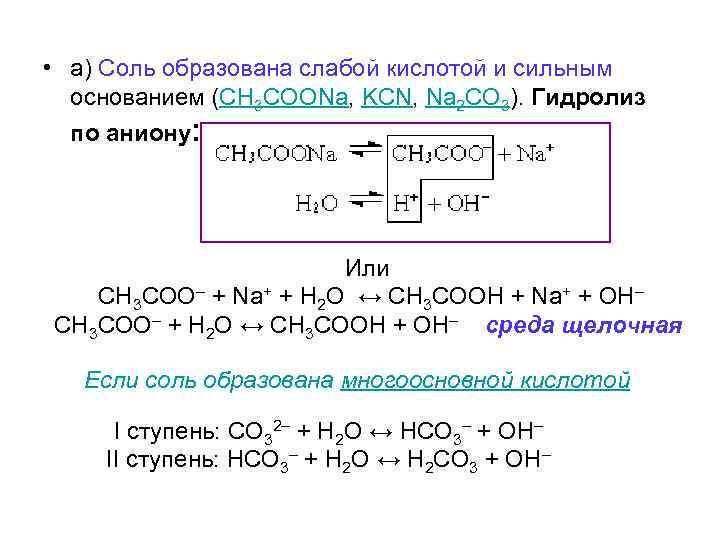 • а) Соль образована слабой кислотой и сильным основанием (CH 3 COONa, KCN, Na 2 CO 3). Гидролиз по аниону: Или CH 3 COO– + Na+ + H 2 O ↔ CH 3 COOH + Na+ + OH– CH 3 COO– + H 2 O ↔ CH 3 COOH + OH– среда щелочная Если соль образована многоосновной кислотой I ступень: CO 32– + H 2 O ↔ HCO 3– + OH– II ступень: HCO 3– + H 2 O ↔ H 2 CO 3 + OH–
• а) Соль образована слабой кислотой и сильным основанием (CH 3 COONa, KCN, Na 2 CO 3). Гидролиз по аниону: Или CH 3 COO– + Na+ + H 2 O ↔ CH 3 COOH + Na+ + OH– CH 3 COO– + H 2 O ↔ CH 3 COOH + OH– среда щелочная Если соль образована многоосновной кислотой I ступень: CO 32– + H 2 O ↔ HCO 3– + OH– II ступень: HCO 3– + H 2 O ↔ H 2 CO 3 + OH–
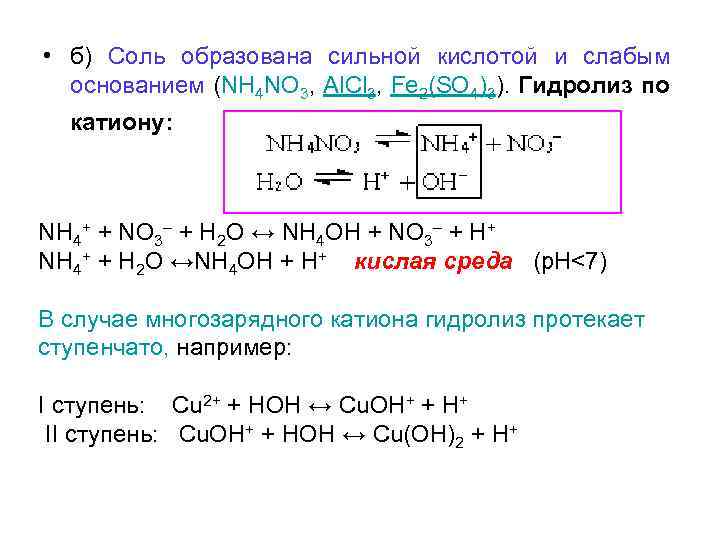 • б) Соль образована сильной кислотой и слабым основанием (NH 4 NO 3, Al. Cl 3, Fe 2(SO 4)3). Гидролиз по катиону: NH 4+ + NO 3– + H 2 O ↔ NH 4 OH + NO 3– + H+ NH 4+ + H 2 O ↔NH 4 OH + H+ кислая среда (p. H<7) В случае многозарядного катиона гидролиз протекает ступенчато, например: I ступень: Cu 2+ + HOH ↔ Cu. OH+ + H+ II ступень: Cu. OH+ + HOH ↔ Cu(OH)2 + H+
• б) Соль образована сильной кислотой и слабым основанием (NH 4 NO 3, Al. Cl 3, Fe 2(SO 4)3). Гидролиз по катиону: NH 4+ + NO 3– + H 2 O ↔ NH 4 OH + NO 3– + H+ NH 4+ + H 2 O ↔NH 4 OH + H+ кислая среда (p. H<7) В случае многозарядного катиона гидролиз протекает ступенчато, например: I ступень: Cu 2+ + HOH ↔ Cu. OH+ + H+ II ступень: Cu. OH+ + HOH ↔ Cu(OH)2 + H+
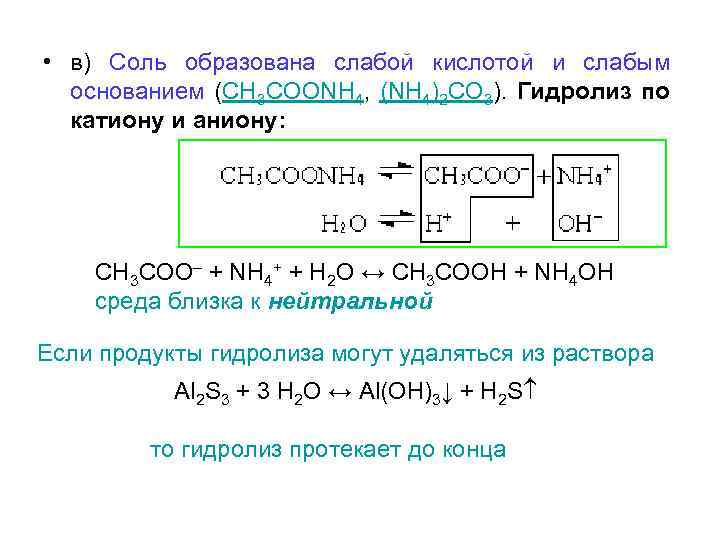 • в) Соль образована слабой кислотой и слабым основанием (CH 3 COONH 4, (NH 4)2 CO 3). Гидролиз по катиону и аниону: CH 3 COO– + NH 4+ + H 2 O ↔ CH 3 COOH + NH 4 OH среда близка к нейтральной Если продукты гидролиза могут удаляться из раствора Al 2 S 3 + 3 H 2 O ↔ Al(OH)3↓ + H 2 S то гидролиз протекает до конца
• в) Соль образована слабой кислотой и слабым основанием (CH 3 COONH 4, (NH 4)2 CO 3). Гидролиз по катиону и аниону: CH 3 COO– + NH 4+ + H 2 O ↔ CH 3 COOH + NH 4 OH среда близка к нейтральной Если продукты гидролиза могут удаляться из раствора Al 2 S 3 + 3 H 2 O ↔ Al(OH)3↓ + H 2 S то гидролиз протекает до конца
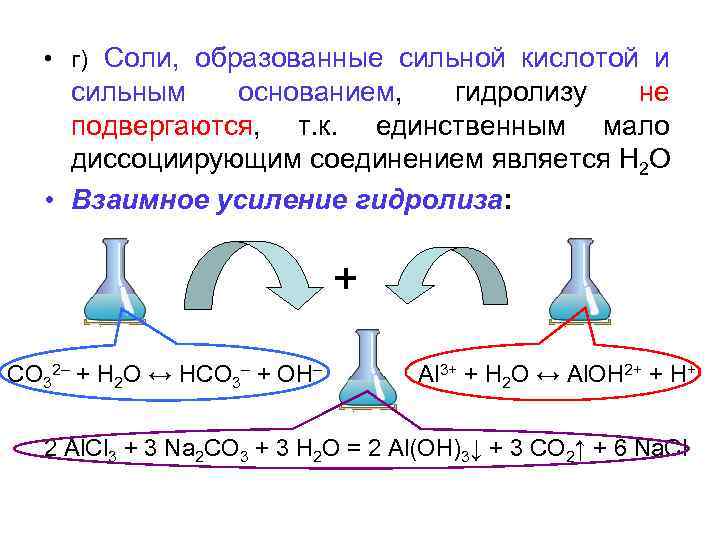 • г) Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются, т. к. единственным мало диссоциирующим соединением является H 2 O • Взаимное усиление гидролиза: + CO 32– + H 2 O ↔ HCO 3– + OH– Al 3+ + H 2 O ↔ Al. OH 2+ + H+ 2 Al. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O = 2 Al(OH)3↓ + 3 CO 2↑ + 6 Na. Cl
• г) Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются, т. к. единственным мало диссоциирующим соединением является H 2 O • Взаимное усиление гидролиза: + CO 32– + H 2 O ↔ HCO 3– + OH– Al 3+ + H 2 O ↔ Al. OH 2+ + H+ 2 Al. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O = 2 Al(OH)3↓ + 3 CO 2↑ + 6 Na. Cl
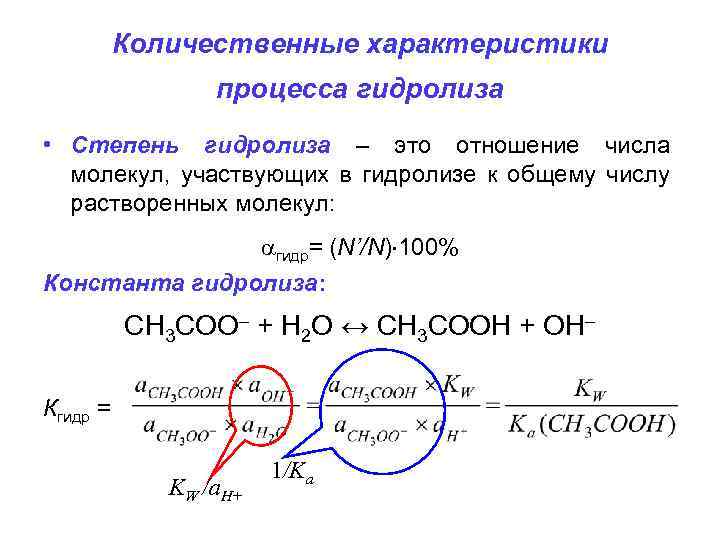 Количественные характеристики процесса гидролиза • Степень гидролиза – это отношение числа молекул, участвующих в гидролизе к общему числу растворенных молекул: гидр= (N’/N) 100% Константа гидролиза: CH 3 COO– + H 2 O ↔ CH 3 COOH + OH– Кгидр = KW /a. H+ 1/Ka
Количественные характеристики процесса гидролиза • Степень гидролиза – это отношение числа молекул, участвующих в гидролизе к общему числу растворенных молекул: гидр= (N’/N) 100% Константа гидролиза: CH 3 COO– + H 2 O ↔ CH 3 COOH + OH– Кгидр = KW /a. H+ 1/Ka
 • В случае гидролиза по аниону: Кгидр = • В случае гидролиза по катиону: Кгидр= • В случае гидролиза по аниону и катиону: Кгидр = если << 1, то Кгидр= 2 с
• В случае гидролиза по аниону: Кгидр = • В случае гидролиза по катиону: Кгидр= • В случае гидролиза по аниону и катиону: Кгидр = если << 1, то Кгидр= 2 с
 1. Гидролиз карбонатов 2 Cu. SO 4 + 2 Na 2 CO 3+ H 2 O (Cu. OH)2 CO 3↓+ CO 2 +2 Na 2 SO 4 2 Cu 2+ + 2 CO 32 - + HOH (Cu. OH)2 CO 3↓ + CO 2 При гидролизе карбонатов двухвалентных металлов образуются основные соли ПР Cu(OH) > ПР (Cu. OH) CO 2 2 3 Al 2(SO 4)3+3 Na 2 CO 3+3 H 2 O 2 Al(OH)3 ↓+3 CO 2 +3 Na 2 SO 4 Al 3+ + 3 CO 32 - + 3 HOH 2 Al(OH)3 ↓+3 CO 2 Al 3+ и Cr 3+- в водных растворах гидролизуются полностью
1. Гидролиз карбонатов 2 Cu. SO 4 + 2 Na 2 CO 3+ H 2 O (Cu. OH)2 CO 3↓+ CO 2 +2 Na 2 SO 4 2 Cu 2+ + 2 CO 32 - + HOH (Cu. OH)2 CO 3↓ + CO 2 При гидролизе карбонатов двухвалентных металлов образуются основные соли ПР Cu(OH) > ПР (Cu. OH) CO 2 2 3 Al 2(SO 4)3+3 Na 2 CO 3+3 H 2 O 2 Al(OH)3 ↓+3 CO 2 +3 Na 2 SO 4 Al 3+ + 3 CO 32 - + 3 HOH 2 Al(OH)3 ↓+3 CO 2 Al 3+ и Cr 3+- в водных растворах гидролизуются полностью
 2. Гидролиз сульфидов 2 Cr. Cl 3 + 3 K 2 S + 6 H 2 O 2 Cr(OH)3↓ + 3 H 2 S + 6 KCl 2 Cr 3++ 3 S 2 - + 6 HOH 2 Cr(OH)3↓ + 3 H 2 S 3. Гидролиз ацетатов Zn. Cl 2+2 CH 3 COOK+H 2 O (Zn. OH)CH 3 COO↓+CH 3 COOH+2 KCl Zn 2+ + 2 CH 3 COO- + HOH (Zn. OH)CH 3 COO↓ + CH 3 COOH При гидролизе ацетатов 2 и 3 -х валентных металлов образуются основные соли, число стадий гидролиза по катиону будет на одну меньше, чем его заряд.
2. Гидролиз сульфидов 2 Cr. Cl 3 + 3 K 2 S + 6 H 2 O 2 Cr(OH)3↓ + 3 H 2 S + 6 KCl 2 Cr 3++ 3 S 2 - + 6 HOH 2 Cr(OH)3↓ + 3 H 2 S 3. Гидролиз ацетатов Zn. Cl 2+2 CH 3 COOK+H 2 O (Zn. OH)CH 3 COO↓+CH 3 COOH+2 KCl Zn 2+ + 2 CH 3 COO- + HOH (Zn. OH)CH 3 COO↓ + CH 3 COOH При гидролизе ацетатов 2 и 3 -х валентных металлов образуются основные соли, число стадий гидролиза по катиону будет на одну меньше, чем его заряд.
 4. Гидролиз солей висмута(III) и сурьмы(III) Bi(NO 3)3 + H 2 O Bi. ONO 3↓ + 2 HNO 3 Bi 3+ + 2 HOH ↔ Bi(OH)2+ + 2 H+ Bi(OH)2+ ↔ H 2 O + Bi. O+ + NO 3 - Bi. ONO 3↓ Bi 3+ + 2 HOH + 3 NO 3 - Bi. ONO 3↓ + 2 H+ + 2 NO 3 - Sb. Cl 3 + H 2 O Sb. OCl ↓ + 2 HCl + HCl осадок растворяется + H 2 O осадок снова выпадает
4. Гидролиз солей висмута(III) и сурьмы(III) Bi(NO 3)3 + H 2 O Bi. ONO 3↓ + 2 HNO 3 Bi 3+ + 2 HOH ↔ Bi(OH)2+ + 2 H+ Bi(OH)2+ ↔ H 2 O + Bi. O+ + NO 3 - Bi. ONO 3↓ Bi 3+ + 2 HOH + 3 NO 3 - Bi. ONO 3↓ + 2 H+ + 2 NO 3 - Sb. Cl 3 + H 2 O Sb. OCl ↓ + 2 HCl + HCl осадок растворяется + H 2 O осадок снова выпадает
 5. Гидролиз силикатов Na 2 Si. O 3 + H 2 O ↔ 2 Na. OH + Na 2 Si 2 O 5 Si. O 32 - + HOH ↔ HSi. O 3 - + OHHSi. O 3 - ↔ H 2 O + Si 2 O 526. Гидролиз тетраборатов Me(I) Na 2 B 4 O 7 + 7 H 2 O ↔ 2 Na. OH + 4 H 3 BO 3 B 4 O 72 - + 7 H 2 O ↔ 4 H 3 BO 3 + 2 OH-
5. Гидролиз силикатов Na 2 Si. O 3 + H 2 O ↔ 2 Na. OH + Na 2 Si 2 O 5 Si. O 32 - + HOH ↔ HSi. O 3 - + OHHSi. O 3 - ↔ H 2 O + Si 2 O 526. Гидролиз тетраборатов Me(I) Na 2 B 4 O 7 + 7 H 2 O ↔ 2 Na. OH + 4 H 3 BO 3 B 4 O 72 - + 7 H 2 O ↔ 4 H 3 BO 3 + 2 OH-


