Лекция 9 Поглотительная способность почв.ppt
- Количество слайдов: 12

ЛЕКЦИЯ 9: ПОГЛОТИТЕЛЬНАЯ СПОСОБНОСТЬ ПОЧВ

Твердая фаза почвы представляет собой полидисперсную систему, состоящую из частиц разных размеров от крупных до мельчайших. Благодаря наличию тонкодисперсных частиц и пористости почва обладает способностью задерживать те или иные вещества, приходящие с ней в соприкосновение. Почвой задерживаются вещества в молекулярном и ионном состоянии, тонкие и коллоидальные суспензии. Явление поглощения и удерживания из почвенного раствора получило название поглотительной способности почв.

С поглотительной способностью связаны важнейшие особенности почвообразовательных процессов и многие свойства, определяющие плодородие почв. Поглотительная способность почв оказывает огромное влияние на условия произрастания растений. Под влиянием, которых в процессе сельскохозяйственного использования наблюдается существенное изменение поглотительных свойств почв. Явление поглощения получило объяснение благодаря трудам П. А. Костычева, К. К. Гедройца, В. Р. Вильямса и других исследователей.

Коллоидами называют частицы размером от 0, 2 до 0, 001 микрометра. Вследствие небольшой величины коллоидные частицы проходят через обычные фильтры, не оседают в воде, обнаруживают броуновское движение и характеризуются рядом других свойств. В воде такие частицы дают коллоидные растворы. В природных условиях коллоидные частицы образуются двумя путями – конденсационным и дисперсионным. В первом случае коллоидные частицы образуются вследствие физического или химического соединения молекул или ионов. Дисперсионное образование коллоидных частиц происходит при механическом или химическом раздробление более крупных частиц.
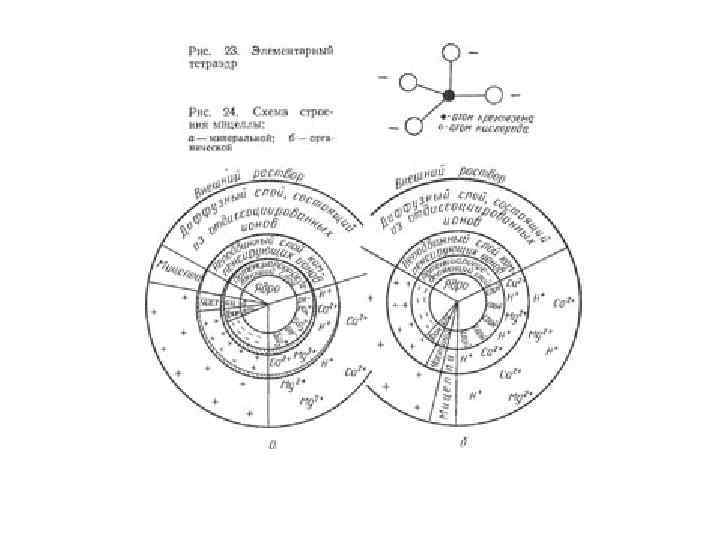

Почвенные коллоиды по своей природе делятся на минеральные, органические и смешанные (органоминеральные). Минеральная часть почвенных коллоидов состоит из небольшого количества тонкодисперсных первичных минералов, главным образом кварца и слюд, и в преобладающем большинстве – из вторичных минералов. Последние разделяются на кристаллические и аморфные. Вторичные минералы кристаллического строения чаще всего представлены группой гидрослюд, группой монтмориллонита, группой каолинита и группой полуторных окислов. К вторичным минералам аморфного строения относятся гидраты окиси железа, алюминия и кремния. Органические коллоиды почв, отличающиеся высокой степенью дисперсности, представлены основными группами гумусовых веществ: гуминовыми кислотами, фульвокислотами и их солями. Органоминеральные коллоидные комплексы представлены преимущественно соединениями гумусовых веществ с глинистыми и другими вторичными минералами.

Коагуляция – агрегирование коллоидных частиц. Условием агрегации частиц является либо дегидратация, то есть потеря водной оболочки (высушивание или замораживание почвы), либо изменение электрокинетического потенциала частиц вследствие прибавления в коллоидный раствор электролитов. Коагуляция может протекать под действием растворённых в дисперсной среде электролитов или в результате взаимного притяжения коллоидных частиц. В результате коагуляции коллоидов образуется осадок – коагулят. Для некоторых коллоидов характерна способность к обратному переходу коагулята в коллоидный раствор или золь. Явление перехода коагулята в золь называется пептизация коллоидов.

Виды поглотительной способности почв. К. К. Гедройц (1922) выделил пять видов поглотительной способности почв: механическую, биологическую, физическую, химическую и физикохимическую. Механическая поглотительная способность обусловлена свойством почвы не пропускать через себя частицы, взмученные в фильтрующейся воде. Механическая поглотительная способность зависит от гранулометрического и агрегатного состояния почвы, а также плотности сложения. Механическая поглотительная способность широко используется на практике. Например, водоочистка производится фильтрованием воды через песчанистые отстойники; с помощью заиливания достигают уменьшения фильтрации воды через стенки и дно оросительных каналов.

Биологическая поглотительная способность заключается в закрепление веществ в телах организмов. Оно осуществляется растениями, микроорганизмами и животными обитающими в почве. Важнейшей особенностью биологического поглощения является избирательное усвоение из растворов с минимальным содержанием наиболее важных для организмов веществ в присутствии больших количеств остальных соединений. Физическая поглотительная способность означает изменение концентрации молекул растворённого вещества в пограничном слое раствора, окружающем коллоиды. Она зависит от количества коллоидов почвы (то есть от механического состава и гумусированности почвы), а также от их качества. Особенностью физической адсорбции является поглощение почвой целых молекул. Химическая поглотительная способность – это способность почвы закреплять в форме труднорастворимых соединений ионы, поступающие в раствор. Закрепление ионов в результате химического поглощения происходит в том случае, когда в почвенном растворе содержится соль, образующая с веществами, находящимися в почве, труднорастворимое соединение. Физико-химическая поглотительная способность. Этот вид связан с поглощением ионов в двойном электрическом слое коллоидов. К. К. Гедройц называл этот тип поглотительной способности обменной.

Поглощение почвами катионов. Катионы в почвах поглощаются в результате реакций химического осаждения, обменного замещения в слое коплексирующих ионов, а также вследствие необменного закрепления в слое птенциалопределяющих ионов. При обменном поглощение способность катионов внедряться в комплексирующий слой ионов неодинакова. Из наиболее распространённых в почве обменных катионов – Ca 2+, Mg 2+, Na+, K+, NH 4+, Al 3+, Fe 3+ и H+ - способность поглощения возрастает с увеличением атомного веса и валентности катионов. Среди поглощенных катионов важная роль принадлежит кальцию, который характеризуется высокой способностью к внедрению в ППК и трудностью вытеснения из поглощенного состояния. Поглощение почвами анионов. Поглощение анионов обусловливается рядом факторов и прежде всего особенностями самих анионов, составом почвенных коллоидов, их электрическим потенциалом и реакцией среды. По способности к поглощению анионы располагаются в следующем ряде: Cl- = NO 3 - < SO 42 - < PO 43 - < OH-. Чем выше валентность аниона, тем больше его способность поглощаться почвой, исключение составляет гидроксил-ион. В природных условиях нитрат-ион и хлор-ион поглощаются почвами в заметных количествах лишь в крайне редких случаях. Сульфат-ион поглощается почвами в небольшом количестве. Поглощение фосфатов – явление, широко распространенное в природных условиях. Поглощение анионов в природных условиях проявляется в нескольких формах. Различают химическое, физико-химическое и биологическое поглощение анионов. Нитраты и хлориды не образуют труднорастворимых солей и поэтому они в почвах не закрепляются в результате химического поглощения. Сульфат-ион дает с кальцием труднорастворимое соединение, то есть поглощается химически. Прочность закрепления анионов и прежде всего фосфат-иона играет важную роль в агрономической практике.

Почвенная кислотность и щёлочность. Физико-химическая поглотительная способность почв в значительной мере объясняет природу почвенной кислотности и щелочности. Кислотность почв. Почвенная кислотность вызывается ионами водорода. В зависимости от того, в каком состоянии они находятся в почве различают актуальную и потенциальную форму кислотности. Реакция почвенного раствора в различных почвах колеблется от p. H 3, 5 до 8 -9 и выше. Наиболее кислую реакцию имеют болотные почвы верховых торфяников. Кислой реакцией почвенного раствора характеризуются подзолистые и дерново-подзолистые почвы (p. H 4 -6). Чернозёмы имеют близкую к нейтральной реакцию. Наиболее щелочную реакцию имеют солончаки, особенно содовые (p. H 8 -9 и выше). Сельскохозяйственные растения предъявляют разные требования к реакции почв. Наиболее благоприятной является слабокислая или слабощелочная реакция. С реакций почвенного раствора тесно связана и жизнедеятельность почвенной микрофлоры. В кислой среде преобладает деятельность грибной микрофлоры, в нейтральной и слабощелочной – деятельность бактериальной микрофлоры. Щёлочность почв. Различают актуальную и потенциальную щёлочность. Актуальная щёлочность обусловливается наличием в почвенном растворе гидролитически щелочных солей (NA 2 CO 3, Ca. CO 3). Потенциальная щелочность обнаруживается у почв, содержащих поглощенный натрий. При взаимодействие такой почвы с угольной кислотой, находящейся в почвенном растворе, происходит реакция замещения, результатом которой является накопление соды и подщелачивание раствора.

Поглощение почвой газов и паров. Кроме молекул, катионов и анионов, поглощаемых почвой из жидкой фазы, происходит поглощение молекул веществ из газообразной фазы. В газообразной фазе почвы находятся водород, азот, кислород и углекислый газ. Все эти газы могут при определенных условиях адсорбироваться почвой. Адсорбция газов наблюдается только в сухих участках почвы. Так как пары аммиака и воды могут не только сгущаться на поверхности, но и сжиматься в ё порах, они сорбируются с большей силой, нежели газы.
Лекция 9 Поглотительная способность почв.ppt